Область техники, к которой относится изобретение
[0001]
Настоящее изобретение относится к способу получения алканового соединения.
Уровень техники
[0002]
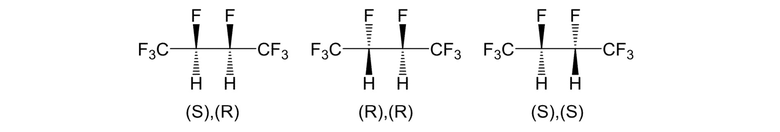
В качестве способа получения CF3CHFCHFCF3, который представляет собой галогенированное алкановое соединение, например, известно проведение реакции гидрирования перфтор-2-бутена, как описано в НПЛ 1. CF3CHFCHFCF3 имеет 3 изомера, т. е. (S), (R) изомер, (R), (R) изомер и (S), (S) изомер, показанные ниже; однако большая часть CF3CHFCHFCF3, полученная вышеуказанным способом получения, представляет собой (S), (R) изомер.
[0003]
Список цитирования
Непатентная литература
[0004]
NPL 1: Journal of Fluorine Chemistry, 1992, т. 59, стр. 9-14
Сущность настоящего изобретения
Техническая проблема
[0005]
Цель настоящего изобретения заключается в обеспечении способа получения алканового соединения, представленного R1CHX1CHX2R2 таким способом, что совместно получают (S),(R) изомер, (R),(R) изомер и (S),(S) изомер.
Решение проблемы
[0006]
Настоящее изобретение включает следующие конфигурации.
[0007]
Пункт 1. Способ получения алканового соединения, представленного формулой (1):
R1CHX1CHX2R2 (1)
Где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом галогена, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу; причем способ включает:
(IIA) реакцию, в присутствии катализатора и циклоалканового соединения, представленного формулой (3):
[0008]
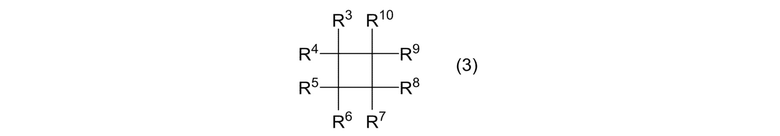
[0009]
где R3, R4, R5, R6, R7, R8, R9, и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена, алкильную группу или фторалкильную группу; алкенового соединения, представленного формулой (2):
[0010]
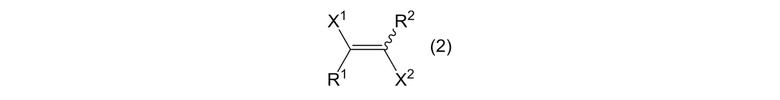
[0011]
где X1, X2, R1, и R2 представляют собой, как определено выше; и галогенсодержащего газа для гидрирования алкенового соединения, представленного формулой (2).
[0012]
Пункт 2. Способ получения по пункту 1, в котором количество циклоалканового соединения, представленного формулой (3), применяемое на стадии гидрирования, составляет 0,5-20 моль на моль алкенового соединения, представленного формулой (2).
[0013]
Пункт 3. Способ получения по пункту 1 или 2, где способ включает, перед стадией гидрирования:
(IA) реакцию циклоалканового соединения, представленного формулой (3):
[0014]
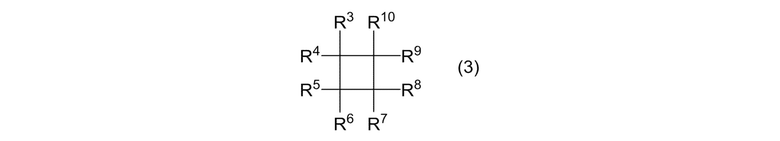
[0015]
где R3, R4, R5, R6, R7, R8, R9 и R10 представляют собой, как определено выше, при условии, что когда оба R1 и R2 в формуле (1) представляют собой алкильные группы, R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена или фторалкильную группу; и алкенового соединения, представленного формулой (4):
[0016]
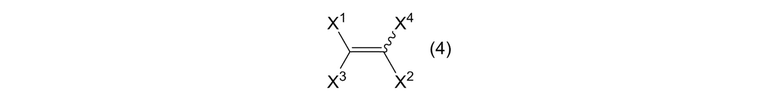
[0017]
где X1 и X2 представляют собой, как определено выше, и X3 и X4 являются одинаковыми или отличными, и каждый представляет собой атом галогена; получая алкеновое соединение, представленное формулой (2):
[0018]
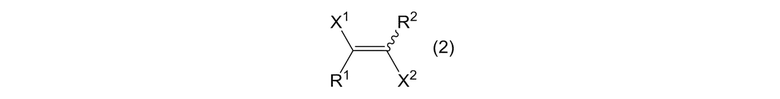
[0019]
ГДЕ X1, X2, R1, и R2 представляют собой, как определено выше.
[0020]
Пункт 4. Способ получения алканового соединения, представленного формулой (1):
R1CHX1CHX2R2 (1)
где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом галогена, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу; причем способ включает:
(IB) реакцию циклоалканового соединения, представленного формулой (3):
[0021]
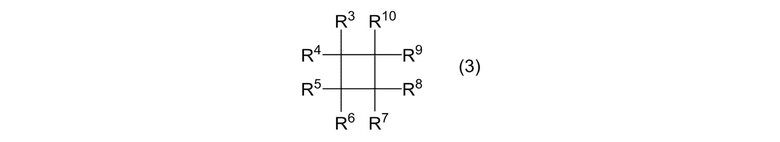
[0022]
где R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена, алкильную группу или фторалкильную группу, при условии, что когда оба R1 и R2 в формуле (1) представляют собой алкильные группы, R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена или фторалкильную группу; и алкенового соединения, представленного формулой (4):
[0023]
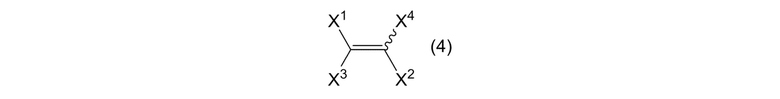
[0024]
где X1 и X2 представляют собой, как определено выше, и X3 и X4 являются одинаковыми или отличными, и каждый представляет собой атом галогена; получая смесь, содержащую циклоалкеновое соединение, представленное формулой (2):
[0025]
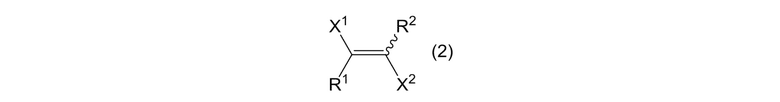
[0026]
где X1, X2, R1 и R2 представляют собой, как определено выше; и циклоалкановое соединение, представленное формулой (3); и
(IIB) реакцию смеси, полученной на стадии (IB), и галогенсодержащего газа в присутствии катализатора для гидрирования циклоалкенового соединения, представленного формулой (2).
[0027]
Пункт 5. Способ получения по пункту 4, где на стадии гидрирования, циклоалкановое соединение, представленное формулой (3), применяемое в качестве исходного соединения в смеси, содержится в количестве 0,5-20 моль на моль алкенового соединения, представленного формулой (2).
[0028]
Пункт 6. Способ получения по любому из пунктов 1-5, где стадию гидрирования проводят в газовой фазе.
[0029]
Пункт 7. Способ получения по любому из пунктов 1-6, где алкановое соединение, представленное формулой (1), которое получают, содержит 3 алкановых соединения, представленных формулами (1A), (1B) и (1C):
[0030]
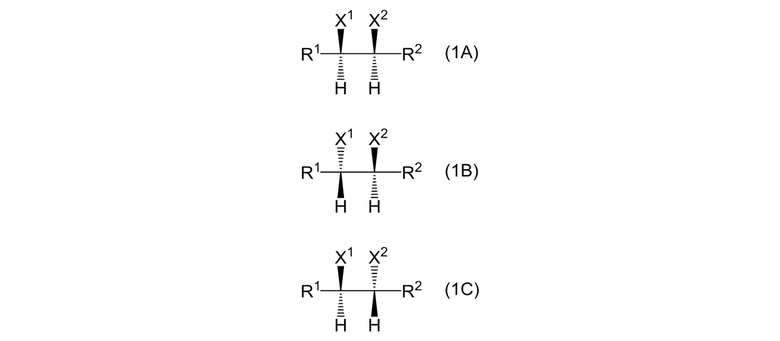
[0031]
где X1, X2, R1, и R2 представляют собой, как определено выше.
[0032]
Пункт 8. Способ получения по пункту 7, где 20-80 моль% алканового соединения, представленного формулой (1A), 10-40 моль% алканового соединения, представленного формулой (1B), и 10-40 моль% алканового соединения, представленного формулой (1C), получают, исходя из суммарного количества продукта, полученного стадией гидрирования, которое принимают за 100 моль%.
[0033]
Пункт 9. Композиция, содержащая 3 алкановых соединения, представленных формулами (1A), (1B) и (1C):
[0034]
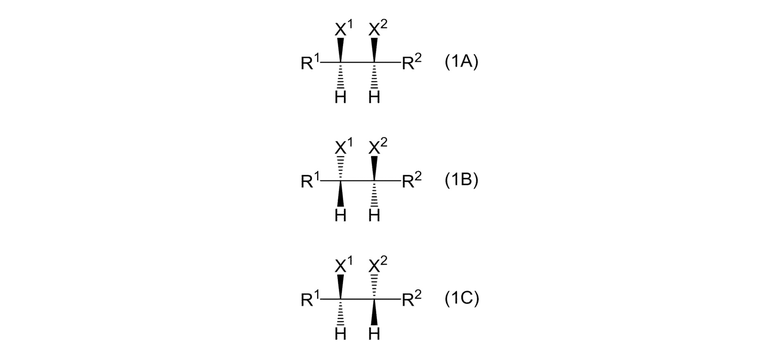
[0035]
где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом галогена, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу; и
причем алкановое соединение, представленное формулой (1A), содержится в количестве 20-80 моль%, алкановое соединение, представленного формулой (1B), содержится в количестве 10-40 моль%, и алкановое соединение, представленное формулой (1C), содержится в количестве 10-40 моль%, исходя из суммарной массы композиции, которую принимают за 100 моль%.
[0036]
Пункт 10, Композиция по пункту 9, которую применяют в качестве промежуточной композиции для органического синтеза, травильного газа или попутного газа.
Полезные эффекты настоящего изобретения
[0037]
Согласно настоящему изобретению, алкановое соединение, представленное R1CHX1CHX2R2, можно получить таким способом, что получают (S),(R) изомер, (R),(R) изомер и (S),(S) изомер.
Описание вариантов осуществления
[0038]
В настоящем изобретении, термин “включает” представляет собой понятие, включающее «содержащий», «состоящий по существу из» и «состоящий из». В настоящем описании числовой диапазон, обозначенный буквами «А-В», обозначает А или больше и В или меньше.
[0039]
В настоящем изобретении, “селективность” обозначает отношение (моль%) общего молярного количества целевого соединения, содержащегося в отходящем газе на выходе из реактора, относительно общего молярного количества соединений, отличных от исходного соединения, в отходящем газе.
[0040]
В настоящем изобретении, “степень конверсии” обозначает отношение (моль%) общего молярного количества соединений, отличных от исходного соединения, содержащихся в отходящем газе на выходе из реактора, относительно молярного количества исходного соединения, подаваемого в реактор.
[0041]
Общепринято, в НПЛ 1, CF3CHFCHFCF3 получали проведением реакции гидрирования 1,1,1,4,4,4-гексафтор-2-бутена; однако, большая часть изомеров, которые можно синтезировать, представляли собой только (S),(R) изомер. Это связано с тем, что известно, что реакция присоединения водорода с применением катализатора является син-присоединением, а реакция анти-присоединения, в которой два атома водорода присоединяются с противоположных направлений, является маловероятной. То есть согласно обычному способу трудно синтезировать другие изомеры, кроме (S)(R)-изомера. С другой стороны, согласно способу получения настоящего изобретения, алкановое соединение, представленное R1CHX1CHX2R2, можно получить таким образом, что (S),(R) изомер, (R),(R) изомер, и (S),(S) изомеры синтезируется совместно. Не только (S),(R)-изомер, но также (R),(R)-изомер и (S),(S)-изомер можно получить совместно, в результате чего можно получить структурные единицы с требуемой оптической активностью.
[0042]
1. Способ получения алканового соединения
1-1: Способ получения алканового соединения из алкенового соединения
Способ получения алкановое соединение настоящего изобретения представляет собой способ получения алканового соединения, представленного формулой (1):
R1CHX1CHX2R2 (1)
где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом галогена, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу; причем способ включает:
(IIA) реакцию в присутствии катализатора и циклоалканового соединения, представленного формулой (3):
[0043]
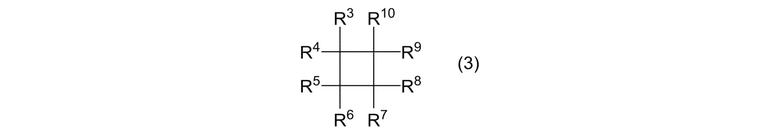
[0044]
где R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена, алкильную группу или фторалкильную группу, при условии, что когда оба R1 и R2 в формуле (1) представляют собой алкильные группы, R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена или фторалкильную группу; алкенового соединения, представленного формулой (2):
[0045]
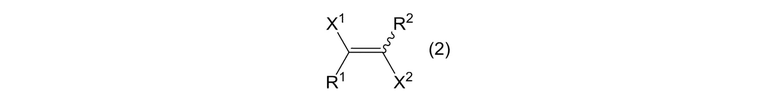
[0046]
где X1, X2, R1, и R2 представляют собой, как определено выше; и галогенсодержащего газа для гидрирования алкенового соединения, представленного формулой (2).
[0047]
Согласно настоящему изобретению, циклоалкановое соединение, представленного формулой (3), описанное выше, ингибирует часть реакции син-присоединения, в которой два атома водорода присоединяются к алкеновому соединению, представленному формулой (2) с одного и того же направления, и с большей вероятностью происходит реакция анти-присоединения, в которой два атома водорода присоединяются с противоположных направлений. В результате алкановое соединение, представленное формулой (1), можно получить таким образом, что совместно получают (S),(R) изомер, (R),(R) изомер и (S),(S) изомер.
[0048]
(1-1-1) Исходное соединение (алкеновое соединение)
Алкеновое соединение в качестве исходного соединения, которое можно применять в способе получения настоящего изобретения, представляет собой, как описано выше, алкеновое соединение, представленное формулой (2):
[0049]
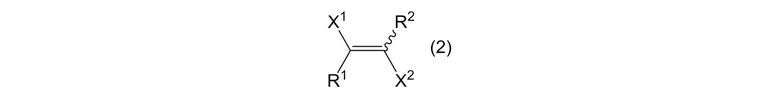
[0050]
где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом галогена, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу.
[0051]
Алкеновое соединение, представленное формулой (2), включает оба алкеновых соединения, представленных формулами (2A) и (2B):
[0052]
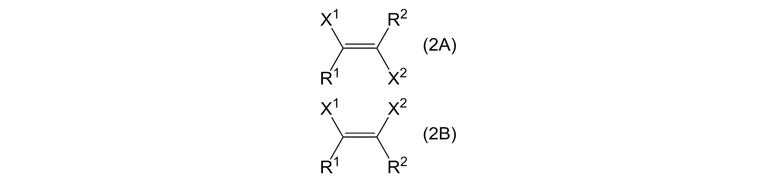
[0053]
где X1, X2, R1, и R2 представляют собой, как определено выше.
[0054]
В формуле (2), примеры атома галогена, представленного X1 и X2, включают атом фтора, атом хлора, атом брома и атом йода.
[0055]
В формуле (2), примеры алкильной группы, представленной R1 и R2, включают алкильные группы, содержащие 1-20 атомов углерода, предпочтительно 1-12 атомов углерода, более предпочтительно 1-6 атомов углерода, и даже более предпочтительно 1-3 атомов углерода, такие как метильная, этильная, н-пропильная и изопропильная группы.
[0056]
В формуле (2), фторалкильная группа, представленная R1 и R2, представляет собой, например, фторалкильную группу (в частности, перфторалкильную группу), содержащую 1-20 атомов углерода, предпочтительно 1-12 атомов углерода, более предпочтительно 1-6 атомов углерода, и даже более предпочтительно 1-3 атомов углерода, такие как трифторметильная и пентафторэтильная группы.
[0057]
Из них, X1 и X2 предпочтительно представляют собой атомы фтора, с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер).
[0058]
Кроме того, R1 и R2 предпочтительно представляют собой фторалкильные группы и более предпочтительно перфторалкильные группы, с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер).
[0059]
X1, X2, R1 и R2 могут быть одинаковыми или отличными.
[0060]
Конкретные примеры алкенового соединения, представленного формулой (2), в качестве исходного соединения, которое удодвлетворяет условиям выше, включают следующие:
[0061]
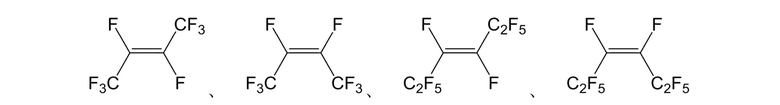
[0062]
Данные алкеновые соединения, представленные формулой (2), можно применять отдельно или в комбинации двух или более. Данные алкеновые соединения, представленные формулой (2), могут представлять собой известные или коммерческие продукты, или их можно получить для применения. Способ получения в случае получения алкенового соединения, представленного формулой (2), описан ниже.
[0063]
(1-1-2) Реакция присоединения водорода
В способе получения алкановое соединение из алкенового соединения в настоящем изобретении, например, в алкеновом соединении, представленном формулой (2), в качестве исходного соединения, X1 и X2 предпочтительно представляют собой атомы фтора, и R1 и R2 предпочтительно представляют собой фторалкильные группы, более предпочтительно перфторалкильные группы, и особенно предпочтительно трифторметильные группы, с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер).
[0064]
То есть, предпочтительной является реакция присоединения водорода (реакции син присоединения и анти присоединения) согласно следущей схеме реакции:
[0065]
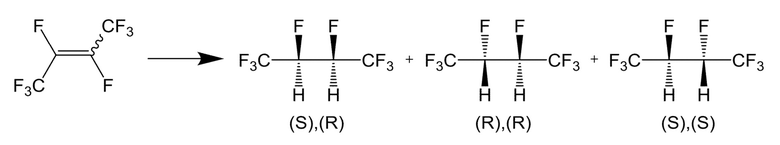
[0066]
[0067]
Стадию применения алкенового соединения, представленного формулой (2), в реакции присоединения водорода, получая алкановое соединение, представленное формулой (1), в настоящем изобретении предпочтительно проводят в газовой фазе, в случае проведения реакции присоединения водорода непрерывно после способа получения алкенового соединения, представленного формулой (2), описанного ниже, и с точки зрения производительности. Когда стадию применения алкенового соединения, представленного формулой (2), в реакции присоединения водорода для получения алканового соединения, представленного формулой (1), в настоящем изобретении проводят в газовой фазе, есть преимущества в том, что реакцию присоединения водорода можно осуществлять непрерывно после способа получения алкенового соединения, представленного формулой (2), описанного ниже, нет необходимости применять растворитель, не возникает промышленных отходов, и достигается отличная производительность
[0068]
Стадию применения алкенового соединения, представленного формулой (2), в реакции присоединения водорода для получения алканового соединения, представленного формулой (1), в настоящем изобретении предпочтительно проводят в газовой фазе, в частности газофазным способом с непрерывным потоком с применением реактора с неподвижным слоем. При применении газофазного способа с непрерывным потоком, устройство, функционирование т.д., могут быть упрощены, и это экономически выгодно.
[0069]
(1-1-3) Циклоалкановое соединение, представленное формулой (3)
Стадию применения алкенового соединения, представленного формулой (2), в реакции присоединения водорода для получения алканового соединения, представленного формулой (1), в настоящем изобретении проводят в присутствии циклоалканового соединения, представленного формулой (3):
[0070]
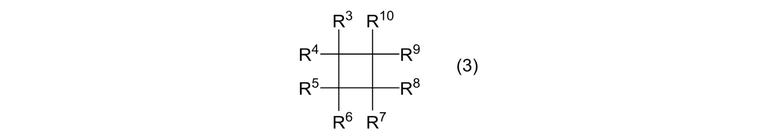
[0071]
где R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена, алкильную группу или фторалкильную группу.
[0072]
Циклоалкановое соединение, представленное формулой (3), ингибирует часть реакции син присоединения, в которой два атома водорода присоединяются к алкеновому соединению, представленному формулой (2), с одного и того же направления, и реакция анти присоединения, в которой два атома водорода присоединяются с противоположных направлений, является более вероятной. В результате алкановое соединение, представленное формулой (1), можно получить таким образом, что получают совместно (S),(R) изомер, (R),(R) изомер и (S),(S) изомер.
[0073]
В формуле (3), атом галогена, алкильная группа и фторалкильная группа, представленные R3, R4, R5, R6, R7, R8, R9 и R10, могут быть такими же как те, что описаны выше. То же применимо к предпочтительным конкретным примерам.
[0074]
Однако, согласно способу получения алкенового соединения, представленного формулой (2), описанного ниже, его можно получить в виде смеси, содержащей алкеновое соединение, представленное формулой (2), и циклоалкановое соединение, представленное формулой (3); однако, когда оба R1 и R2 представляют собой алкильные группы, если R3, R4, R5, R6, R7, R8, R9 и R10 также представляют собой алкильные группы, нельзя получить алкеновое соединение, представленное формулой (2). Следовательно, когда применяют способ получения, описанный ниже, в качестве способа получения алкенового соединения, представленного формулой (2), которое представляет собой исходное соединение, и когда оба R1 и R2 представляют собой алкильные группы, R3, R4, R5, R6, R7, R8, R9 и R10 предпочтительно представляют собой атомы галогена или фторалкильные группы.
[0075]
R3, R4, R5, R6, R7, R8, R9 и R10 предпочтительно представляют собой атомы галогена или фторалкильные группы, более предпочтительно атомы галогена, и даже более предпочтительно атомы фтора, с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер).
[0076]
Конкретные примеры циклоалканового соединения, представленного формулой (3), которое удовлетворяет условиям выше, включают следующие:
[0077]
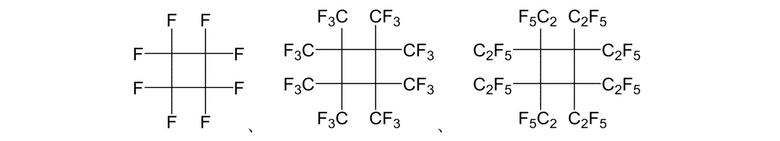
[0078]
[0079]
В способе получения настоящего изобретения, когда алкеновое соединение, представленное формулой (2), подвергают реакции присоединения водорода в присутствии циклоалканового соединения, представленного формулой (3), и катализатора, предпочтительно, например, приводить в контакт циклоалкановое соединение, представленное формулой (3), в виде газа (газовая фаза) с алкеновым соединением, представленным формулой (2).
[0080]
В способе получения настоящего изобретения, когда алкеновое соединение, представленное формулой (2), подвергают реакции присоединения водорода в присутствии циклоалканового соединения, представленного формулой (3), и катализатора, применяемое количество циклоалканового соединения представленного формулой (3) не ограничено. С точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер, и (S),(S) изомер), оно предпочтительно составляет 0,5-20 моль, более предпочтительно 0,7-15 моль, и даже более предпочтительно 0,8-10 моль, на моль алкенового соединения, представленного формулой (2), которое представляет собой исходное соединение.
[0081]
(1-1-4) Катализатор
Стадию применения алкенового соединения, представленного формулой (2), в реакции присоединения водорода для получения алканового соединения, представленного формулой (1), в настоящем изобретении проводят в присутствии катализатора.
[0082]
Металлы, входящие в состав катализатора, представляют собой элементы-переходные металлы, принадлежащие к группам 8-11 периодической таблицы, и более предпочтительно элементы-переходные металлы, принадлежащие к группам 9-10 периодической таблицы. Конкретные примеры данных металлов включают платину, палладий, родий, никель и подобные. Катализатор настоящего изобретения может содержать данный металл отдельно, может быть пористым металлическим катализатором или может содержать данный металл в виде соединения с другими элементами. Применяемые примеры включают сплавы каталитических металлов, таких как платина, палладий, родий и никель, и некаталитических металлов, таких как алюминий, кремний, магний и цинк, катализаторы, в которых некаталитические металлы элюируют из данных сплавов с применением кислотного или щелочного раствора (катализаторы Ренея), Pt(PtO2), катализатор Адамса (PtO2-H2O), коллоидный палладий, коллоидная платина, платиновая чернь и подобные. Их можно применять по отдельности или в комбинации из двух или более.
[0083]
Кроме того, в настоящем изобретении упомянутые выше металлы можно непосредственно применять в качестве катализаторов или можно наносить на носитель для применения. Носитель, который можно применять в данном случае, не ограничен, и его примеры включают углерод, оксид алюминия (Al2O3), диоксид циркония (ZrO2), диоксид кремния (SiO2), диоксид титана (TiO2) и подобные. Из них предпочтительными являются углерод, оксид алюминия и т.д., причем более предпочтительным является углерод, с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер). В качестве угля можно применять активированный уголь, аморфный углерод, графит, алмаз и подобные.
[0084]
В способе получения настоящего изобретения, когда алкеновое соединение, представленное формулой (2), подвергают реакции присоединения водорода в присутствии циклоалканового соединения, представленного формулой (3), и катализатора, предпочтительно, например, приводить в контакт катализатор в твердом состоянии (твердая фаза) с алкеновым соединением, представленным формулой (2). В данном случае, форма катализатора может быть порошковой; однако гранулы являются предпочтительными, когда их применяют для газофазной непрерывной проточной реакции.
[0085]
Удельная площадь поверхности катализатора, измеренная BET способом (в настоящем изобретении далее называют “BET удельная площадь поверхности”) обычно предпочтительно составляет 10-3000 м2/н, более предпочтительно 10-2500 м2/г, даже более предпочтительно 20-2000 м2/г, и особенно предпочтительно 30-1500 м2/г, с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер).
[0086]
(1-1-5) Галогенсодержащий газ
Примеры галогенсодержащего газа включают газообразный водород, а также смеси газообразного водорода и других газов (например, смесь водорода и инертного газа, такого как азот или аргон, смешанные в любом соотношении, и оксиводород, который представляет собой смешанный газ кислорода и водорода). Однако, поскольку в способе получения настоящего изобретения применяют реакцию присоединения водорода, предпочтительно, чтобы галогеноводород (фтороводород) и т.п. не содержались или присутствовали в очень малом количестве (например, 5% по объему или менее, исходя из суммарной массы галогенсодержащего газа) в качестве галогенсодержащего газа. С точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер), предпочтительно применять газообразный водород. Данные галогенсодержащие газы можно применять по отдельности или в комбинации двух или более.
[0087]
Обычно предпочтительно подавать галогенсодержащий газ в паровом состоянии вместе с алкеновым соединением, представленным формулой (2) (исходное соединение), в реактор. Подаваемое количество галогенсодержащего газа предпочтительно составляет 0,7-10 моль, более предпочтительно 0,8-5 моль, и даже более предпочтительно 0,9-3 моль, на моль алкенового соединения, представленного формулой (2) (исходное соединение), с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер).
[0088]
(1-1-6) Температура реакции
На стадии применения алкенового соединения, представленного формулой (2) (исходное соединение), в реакции присоединения водорода в настоящем изобретении, температура реакции обычно составляет 20-400°C, более предпочтительно 30-300°C, и даже более предпочтительно 40-200°C, с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер).
[0089]
(1-1-7) Продолжительность реакции
На стадии применения алкенового соединения, представленного формулой (2) (исходное соединение), в реакции присоединения водорода в настоящем изобретении, например, при применении газофазного проточного способа, продолжительность контакта исходного соединения с катализатором (W/F) [W: вес (г) катализатора, F: скорость потока (см3/сек) исходного соединения] предпочтительно составляет 0,5-50 г⋅сек/см3, более предпочтительно 1-40 г⋅сек/см3, и даже более предпочтительно 1,5-30 г⋅сек/см3, с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер). Продолжительность контакта относится к продолжительности контакта между исходным соединением и катализатором, а именно продолжительности реакции.
[0090]
(1-1-8) Реакционное давление
На стадии применения алкенового соединения, представленного формулой (2) (исходное соединение), в реакции присоединения водорода в настоящем изобретении, реакционное давление предпочтительно составляет 0 кПа или более, более предпочтительно 10 кПа или более, даже более предпочтительно 20 кПа или более, и особенно предпочтительно 30 кПа или более, с точки зрения степени конверсии реакции и селективности и выхода целевого алканового соединения ((S),(R) изомер, (R),(R) изомер и (S),(S) изомер). Верхний предел реакционного давления не ограничен и обычно составляет около 2 МПа. В настоящем изобретении давление является манометрическим давлением, если не указано иное.
[0091]
На стадии применения алкенового соединения, представленного формулой (2) (исходное соединение), в реакции присоединения водорода В настоящем изобретении, реактор для реакции алкенового соединения, представленного формулой (2) (исходное соединение), циклоалканового соединения, представленного формулой (3), и катализатора не ограничен по его форме и структуре, при условии, пока он может выдерживать температуру и давление, описанные выше. Примеры реактора включают вертикальный реактор, горизонтальный реактор, многотрубный реактор и подобные. Примеры материала реактора включают стекло, нержавеющую сталь, железо, никель, железо-никелевые сплавы и подобные.
[0092]
(1-1-9) Пример реакции присоединения водорода
Стадию применения алкенового соединения, представленного формулой (2) (исходное соединение), в реакции присоединения водорода в настоящем изобретении можно осуществлять в периодическом режиме или непрерывном режиме, в котором алкеновое соединение, представленное формулой (2), в качестве исходного соединения, непрерывно подают в реактор и алкановое соединение, представленное формулой (1), в качестве целевого соединения, непрерывно выводят из реактора. Стадию применения алкенового соединения, представленного формулой (2) (исходное соединение), в реакции присоединения водорода в настоящем изобретении предпочтительно проводят в газовой фазе, в частности газофазным способом с непрерывным потоком с применением реактора с неподвижным слоем. При применении газофазного способа с непрерывным потоком устройство, функционирование и т.д., могут быть упрощены, и это экономически выгодно.
[0093]
Атмосфера, в которой алкеновое соединение, представленное формулой (2) (исходное соединение), подвергают реакции присоединения водорода в настоящем изобретении предпочтительно представляет собой атмосферу инертного газа, атмосферу газообразного водорода или подобную, с точки зрения подавления разрушения катализатора. Примеры инертного газа включают азот, гелий, аргон и подобные. Среди данных инертных газов азот является предпочтительным с точки зрения снижения стоимости. Концентрация инертного газа составляет предпочтительно 0-50 моль% от газового компонента, вводимого в реактор.
[0094]
После завершения реакции присоединения водорода, при необходимости, очистительную обработку можно проводить согласно общему способу, посредством этого получая алкановое соединение, представленное формулой (1).
[0095]
(1-1-10) Целевое соединение (алкановое соединение)
Таким образом полученное целевое соединение настоящего изобретения представляет собой алкановое соединение, представленное формулой (1):
R1CHX1CHX2R2 (1)
где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом галогена, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу.
[0096]
X1, X2, R1 и R2 в формуле (2A) соответствуют, соответственно, X1, X2, R1 и R2 в формуле (2), описанной выше. Следовательно, примеры алканового соединения, представленного формулой (1), которое получают, включают CHF2CHF2, CF3CHFCHFCF3, C2F5CHFCHFC2F5 и подобные. Как описано выше, согласно общепринятому способу, большая часть полученных целевых продуктов представляет собой только (S),(R) изомер; однако, согласно способу получения настоящего изобретения, алкановое соединение, представленного формулой (1), можно получить таким способом, что совместно получают (S),(R) изомер, (R),(R) изомер и (S),(S) изомер. То есть, целевое соединение включает все из (S),(R) изомера, (R),(R) изомера и (S),(S) изомера. Соответственно, примеры полученного целевого соединения включают следующие:
[0097]
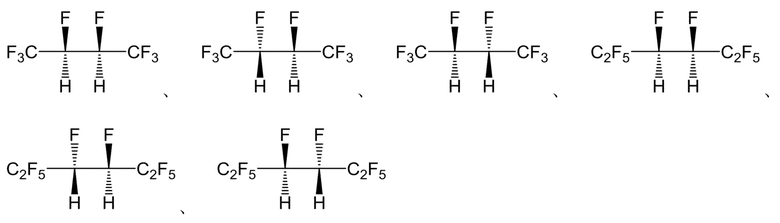
[0098]
Содержание (S),(R) изомера, (R),(R) изомера и (S),(S) изомера описано ниже. Каждый изомер анализируют газовой хроматографией (содержание), применяя хиральную колонку и ЯМР (определение структуры).
[0099]
Таким образом полученное алкановое соединение, представленное формулой (1), можно эффективно применять для различных применений, таких как промежуточные соединения для органического синтеза, травильного газа или попутного газа. В частности, когда ранее сообщенную реакцию применяют для алканового соединения, представленного формулой (1), можно также получить алкиновые соединения (CF3C≡CCF3 и т.д.), которые можно эффективно применять для различных применений, таких как травильные газы, очищающие газы, осадочные газы, хладагенты, теплоносители и строительные блоки для органического синтеза.
[0100]
1-2: Способ получения алкенового соединения
В способе получения настоящего изобретения, алкеновое соединение, представленное формулой (2), применяемое в качестве исходного соединения, может представлять собой известный или коммерческий продукт, или его можно получить, как описано выше. Например, алкеновое соединение, представленное формулой (2), модно получить согласно способам, описанным в Journal of the Chemical Society, 1953, стр. 2082-2084, US2404374B и т.д.
[0101]
Когда получают алкеновое соединение, представленное формулой (2), его способ получения включает, например:
(IA) реакцию циклоалканового соединения, представленного формулой (3):
[0102]
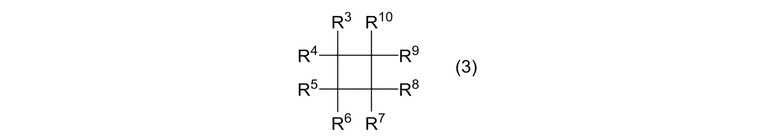
[0103]
где R3, R4, R5, R6, R7, R8, R9 и R10 представляют собой, как определено выше, при условии, что когда оба R1 и R2 в формуле (1) представляют собой алкильные группы, R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена или фторалкильную группу; и алкенового соединения, представленного формулой (4):
[0104]
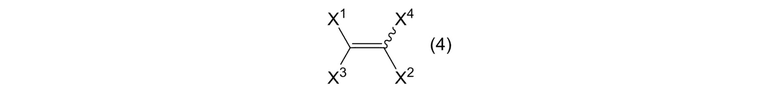
[0105]
где X1 и X2 представляют собой, как определено выше, и X3 и X4 являются одинаковыми или отличными, и каждый представляет собой атом галогена; получая алкеновое соединение, представленное формулой (2):
[0106]
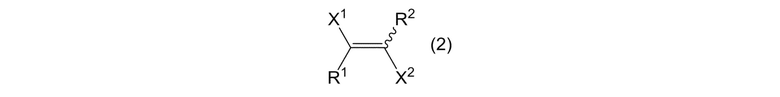
[0107]
где X1, X2, R1 и R2 представляют собой, как определено выше.
[0108]
(1-2-1) Исходное соединение (алкеновое соединение)
Алкеновое соединение, представленное формулой (4), в качестве пригодного исходного соединения, представляет собой, как описано выше, алкеновое соединение, представленное формулой (4):
[0109]
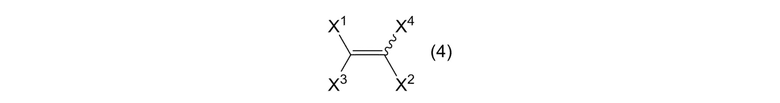
[0110]
где X1, X2, X3 и X4 являются одинаковыми или отличными, и каждый представляет собой атом галогена.
[0111]
Когда есть цис и транс изомеры, алкеновое соединение, представленное формулой (2), включает оба алкеновых соединения, представленные формулами (4A) и (4B):
[0112]
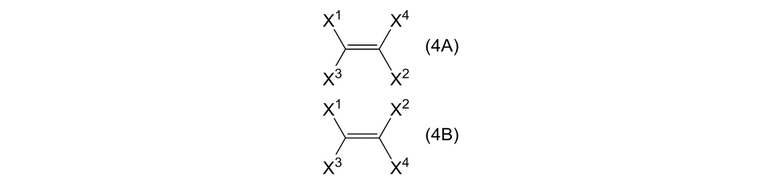
[0113]
где X1, X2, X3 и X4 представляют собой, как определено выше.
[0114]
В формуле (4), атомы галогена, представленные X1, X2, X3 и X4, могут представлять собой атомы галогена, представленные выше. То же применимо к предпочтительным конкретным примерам. Из них, атомы фтора являются предпочтительными с точки зрения степени конверсии реакции и селективности и выхода целевого алкенового соединения, представленного формулой (2).
[0115]
X1, X2, X3 и X4 могут быть одинаковыми или отличными.
[0116]
Конкретные примеры алкенового соединения, представленного формулой (4), в качестве исходного соединения, которое удовлетворяет условиям выше, включают следующие:
[0117]
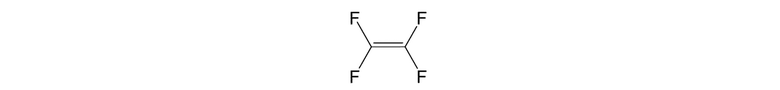
[0118]
Данные алкеновые соединения, представленные формулой (4), модно применять отдельно или в комбинации двух или более. Данные алкеновые соединения, представленные формулой (4), могут представлять собой известные или коммерческие продукты.
[0119]
(1-2-2) Циклоалкановое соединение, представленное формулой (3)
Для циклоалканового соединения, представленного формулой (3), можно непосредственно применять приведенное выше объяснение.
[0120]
(1-2-3) Реакция термического разложения
В способе получения алканового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), например, в алкеновом соединении, представленном формулой (4) в качестве исходного соединения, X1, X2, X3 и X4 предпочтительно представляют собой атомы фтора, и R3, R4, R5, R6, R7, R8, R9 и R10 также предпочтительно представляют собой атомы галогена, и более предпочтительно атомы фтора, с точки зрения степени конверсии реакции и селективности и выхода целевого алкенового соединения, представленного формулой (2).
[0121]
То есть, предпочтительно проводить реакцию термического разложения согласно следующей реакционной схеме:
[0122]
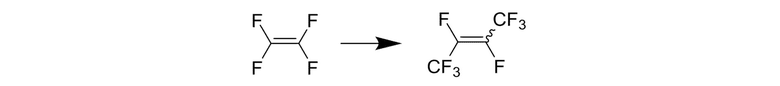
[0123]
[0124]
Стадию получения алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), предпочтительно проводят в газовой фазе, в случае непрерывного получения алканового соединения, представленного формулой (1), реакцией присоединения водорода, описанной выше, после данной стадии, и с точки зрения производительности. Когда стадию получения алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), проводят в газовой фазе, преимущества заключаются в том, что алкановое соединение, представленное формулой (1), можно непрерывно получать реакцией присоединения водорода после данной стадии, нет необходимости применять растворитель, не образуются промышленные отходы и достигается превосходная производительность.
[0125]
Стадию получения алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), предпочтительно проводят в газовой фазе, в частности газофазным способом с непрерывным потоком с применением реактора с неподвижным слоем. При применении газофазного способа с непрерывным потоком устройство, функционирование и т.д., можно упростить, и это экономически выгодно.
[0126]
(1-2-4) Температура реакции
На стадии получения алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), температура реакции обычно предпочтительно составляет 400-1000°C, более предпочтительно 500-900°C, и даже более предпочтительно 600-800°C, с точки зрения степени конверсии реакции и селективности и выхода целевого алкенового соединения, представленного формулой (2).
[0127]
(1-2-5) Продолжительность реакции (скорость потока)
На стадии получения алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), например, при применении газофазного проточного способа, скорость потока исходного соединения предпочтительно составляет 0,01-10 г/сек, более предпочтительно 0,05-5 г/сек, и даже более предпочтительно 0,1-1 г/сек, с точки зрения степени конверсии реакции и селективности и выхода целевого алкенового соединения, представленного формулой (2).
[0128]
(1-2-6) Реакционное давление
На стадии получения алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), реакционное давление предпочтительно составляет 0 кПа или более, более предпочтительно 10 кПа или более, даже более предпочтительно 20 кПа или более, и особенно предпочтительно 30 кПа или более, с точки зрения степени конверсии реакции и селективности и выхода целевого алкенового соединения, представленного формулой (2). Верхний предел реакционного давления не ограничен и обычно составляет приблизительно 2 МПа. В настоящем изобретение давление является манометрическим давлением, если не указано иное.
[0129]
На стадии получения алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), реактор для реакции алкенового соединения, представленного формулой (4) (исходное соединение) и циклоалканового соединения, представленного формулой (3), не ограничен по его форме и структуре при условии, что он может выдерживать температуру и давление, описанные выше. Примеры реактора включают вертикальный реактор, горизонтальный реактор, многотрубный реактор и подобные. Примеры материала реактора включают стекло, нержавеющую сталь, железо, никель, железоникелевые сплавы и подобные.
[0130]
(1-2-7) Пример реакции термического разложения
Стадию получения алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), можно проводить в периодическом режиме или непрерывном режиме, в котором алкеновое соединение, представленное формулой (4), в качестве исходного соединения, непрерывно подается в реактор, и алкеновое соединение, представленное формулой (2), в качестве целевого соединения, непрерывно выводится из реактора. Если алкеновое соединение, представленное формулой (2), в качестве целевого соединения, остается в реакторе, может протекать последующая побочная реакция; таким образом, предпочтительно проводить реакцию в непрерывном режиме. Стадию получения алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), предпочтительно проводить в газовой фазе, в частности газофазным способом с непрерывным потоком с применением реактора с неподвижным слоем. При применении газофазного способа с непрерывным потоком устройство, функционирование и т.д. могут быть упрощены, и это экономически выгодно.
[0131]
Атмосфера при получении алкенового соединения, представленного формулой (2), из алкенового соединения, представленного формулой (4), предпочтительно представляет собой атмосферу инертного газа с точки зрения подавления примесей. Примеры инертного газа включают азот, гелий, аргон и подобные. Среди данных инертных газов азот является предпочтительным с точки зрения снижения стоимости. Концентрация инертного газа составляет предпочтительно 0-50 моль% от газового компонента, вводимого в реактор.
[0132]
После завершения реакции присоединения водорода, при необходимости, очистительную обработку можно проводить согласно общему способу, посредством этого получая алкеновое соединение, представленное формулой (2).
[0133]
(1-2-8) Целевое соединение (алкеновое соединение)
Таким образом полученное алкеновое соединение, представленного формулой (2), представляет собой, как объяснено выше. То есть, объяснение выше можно применять для объяснения полученного алкенового соединения, представленного формулой (2).
[0134]
1-3: Способ получения алканового соединения, представленного формулой (1), из алкенового соединения, представленного формулой (4), через алкеновое соединение, представленное формулой (2)
Способ получения алкановое соединение настоящего изобретения представляет собой способ получения алканового соединения, представленного формулой (1):
R1CHX1CHX2R2 (1)
где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом галогена, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу; причем способ включает:
(IB) реакцию циклоалканового соединения, представленного формулой (3):
[0135]
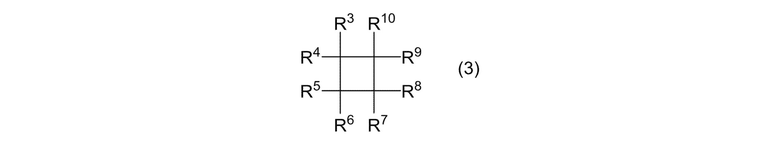
[0136]
где R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена, алкильную группу или фторалкильную группу, при условии, что когда оба R1 и R2 в формуле (1) представляют собой алкильные группы, R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом галогена или фторалкильную группу; и алкенового соединения, представленного формулой (4):
[0137]
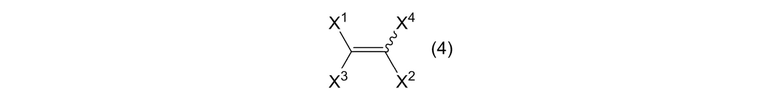
[0138]
где X1 и X2 представляют собой, как определено выше, и X3 и X4 являются одинаковыми или отличными, и каждый представляет собой атом галогена; получая смесь, содержащую циклоалкеновое соединение, представленное формулой (2):
[0139]
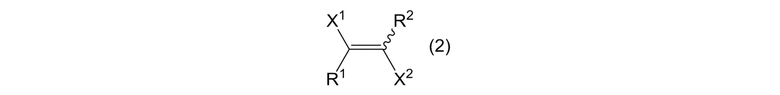
[0140]
где X1, X2, R1 и R2 представляют собой, как определено выше; и циклоалканового соединения, представленного формулой (3); и
(IIB) реакцию смеси, полученной на стадии (IB), и галогенсодержащего газа в присутствии катализатора для гидрирования циклоалкенового соединения, представленного формулой (2).
[0141]
(1-3-1) Стадия (IB)
Для стадии (IB) способа получения алканового соединения настоящего изобретения, можно непосредственно применять объяснение в “1-2: способ получения алкенового соединения”, описанном выше.
[0142]
(1-3-2) Стадия (IIB)
Алкеновое соединение, представленное формулой (2), получают стадией (IB), описанной выше. В то же время, также остается циклоалкановое соединение, представленное формулой (3), применяемое в реакции. Соответственно, в общем, смесь, содержащую алкеновое соединение, представленное формулой (2), и циклоалкановое соединение, представленное формулой (3), получают после стадии (IB).
[0143]
После стадии (IB), алкеновое соединение, представленное формулой (2), и циклоалкановое соединение, представленное формулой (3), можно разделять и применять на стадии (IIB); однако, поскольку, например, их композиционные формулы являются одинаковыми, и их молекулярные веса являются близкими, часто трудно разделить алкеновое соединение, представленное формулой (2), и циклоалкановое соединение, представленное формулой (3).
[0144]
Например, октафтор-2-бутен формулы (2), где X1 и X2 представляют собой атомы фтора, и R1 и R2 представляют собой трифторметильные группы:
[0145]
or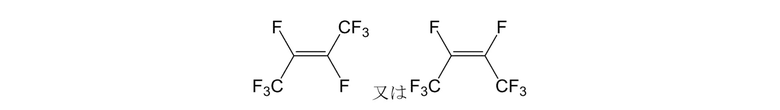
[0146]
и октафторциклобутан (C318) формулы (3), где R3, R4, R5, R6, R7, R8, R9 и R10 представляют собой атомы фтора:
[0147]
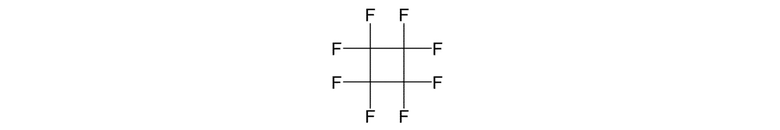
[0148]
оба имеют композиционную формулу C4F8 и имеют близкие температуры кипения; таким образом, их трудно разделить.
[0149]
В данном случае, смесь, содержащую алкеновое соединение, представленное формулой (2), и циклоалкановое соединение, представленное формулой (3), полученную после стадии (IB), можно непосредственно применять в качестве исходного материала на стадии (IIB) без очистки.
[0150]
То есть, реакция может протекать тем же способом, как в “1-1: Способ получения алканового соединения из алкенового соединения”, описанном выше, за исключением того, что смесь (предпочтительно смешаннй газ), содержащую алкеновое соединение, представленное формулой (2), и циклоалкановое соединение, представленное формулой (3), применяют вместо раздельного применения алкенового соединения, представленного формулой (2), и циклоалканового соединения, представленного формулой (3). Следовательно, объяснение в “1-1: Способ получения алканового соединения из алкенового соединения” можно применять непосредственно, за исключением того, что смесь (предпочтительно смешанный газ), содержащую алкеновое соединение, представленное формулой (2), и циклоалкановое соединение, представленное формулой (3), применяют вместо отдельного применения алкенового соединения, представленного формулой (2), и циклоалканового соединения, представленного формулой (3).
[0151]
2. Композиция
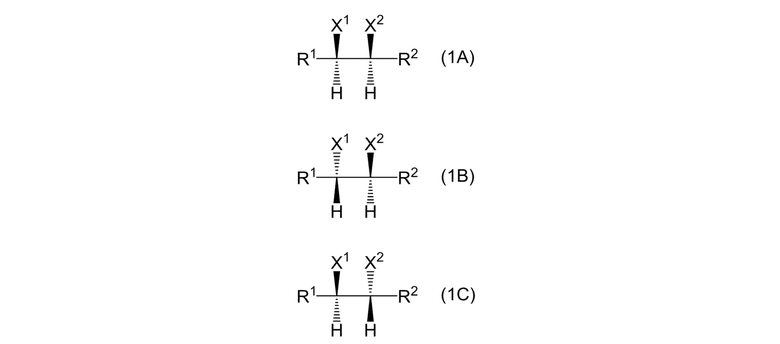
Алкановое соединение, представленное формулой (1), можно получить способом выше. Как описано выше, согласно способу получения настоящего изобретения, алкановое соединение, представленное формулой (1), можно получить таким способом, что совместно получают (S),(R) изомер, (R),(R) изомер и (S),(S) изомер. Следовательно, согласно способу получения настоящего изобретения, алкановое соединение, представленное формулой (1), можно получить в виде композиции, содержащей 3 алкановых соединения, представленных формулами (1A), (1B) и (1C):
[0152]
[0153]
где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом галогена, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу. Алкановое соединение, представленное формулой (1A), относится к (S),(R) изомеру, алкановое соединение, представленное формулой (1B), относится к (R),(R) изомеру, и алкановое соединение, представленное формулой (1C), относится к (S),(S) изомеру.
[0154]
В формулах (1A), (1B) и (1C), X1, X2, R1 и R2 могут быть такими, как описано выше.
[0155]
Согласно способу получения настоящего изобретения, объясненному выше, в реакции присоединения водорода, реакции син присоединения и анти присоединения протекают в одинаковой степени; таким образом, содержание алканового соединения, представленного формулой (1A), в композиции настоящего изобретения вероятно является почти таким же, как суммарное количество алканового соединения, представленного формулой (1B), и алканового соединения, представленного формулой (1C). Кроме того, поскольку образуются почти равные количества (R),(R) изомера и (S),(S) изомера, когда протекает реакция анти присоединения, содержание алканового соединения, представленного формулой (1B), вероятно является таким же, как количество алканового соединения, представленного формулой (1C). Следовательно, содержание алканового соединения, представленного формулой (1A), предпочтительно составляет 20-80 моль%, более предпочтительно 30-75 моль%, и даже более предпочтительно 40-70 моль%, исходя из суммарной массы композиции настоящего изобретения, которую принимают за 100 моль%. Кроме того, содержание алканового соединения, представленного формулой (1B), предпочтительно составляет 10-40 моль%, более предпочтительно 12,5-35 моль%, и даже более предпочтительно 15-30 моль%. Более того, содержание алканового соединения, представленного формулой (1C), предпочтительно составляет 10-40 моль%, более предпочтительно 12,5-35 моль%, и даже более предпочтительно 15-30 моль%. Каждый изомер анализируют газовой хроматографией (содержание), применяя хиральную колонку, и ЯМР (определение структуры).
[0156]
Согласно способу получения настоящего изобретения, алкановое соединение, представленное формулой (1), можно получить при высокой степени конверсии реакции, а также с высоким выходом и высокой селективностью. Следовательно, можно снизить компоненты, отличные от алканового соединения, представленного формулой (1), в композиции, что может облегчить очистку для получения алканового соединения, представленного формулой (1). Кроме того, на стадии (IB), если трудно разделить алкеновое соединение, представленное формулой (2), и циклоалкановое соединение, представленное формулой (3), даже когда циклоалкановое соединение, представленное формулой (3), остается в продукте, алкановое соединение, представленное формулой (1), и циклоалкановое соединение, представленное формулой (3), можно легко разделить обычным способом, поскольку они имеют различные композиционные формулы.
[0157]
Композицию настоящего изобретения, описанную выше, можно эффективно применять для различных применений, таких как промежуточные композиции для органического синтеза, травильные газы и попутные газы. В частности, когда описанную ранее реакцию применяют для композиции настоящего изобретения, содержащей алкановое соединение, представленное формулой (1), также можно получить алкиновые соединения (CF3C≡CCF3 и т.д.), которые можно эффективно применять для различных применений, таких как травильные газы, очищающие газы, попутные газы, хладагенты, теплоносители и строительные блоки для органического синтеза.
[0158]
Хотя варианты осуществления описаны выше, могут быть внесены различные изменения в форму и детали без отклонения от сущности и объема формулы изобретения.
Примеры
[0159]
Признаки настоящего изобретения поясняются ниже при рассмотрении примеров. Настоящее изобретение не ограничивается данными примерами.
[0160]
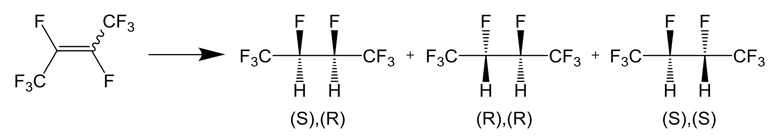
В способах получения алканового соединения примеров 1-5 и сравнительных примеров 1-3, исходное соединение представляет собой галогенированное бутановое соединение, представленное формулой (2A), где X1 и X2 представляют собой атомы фтора, и R1 и R2 представляют собой трифторметильные группы, и алкановое соединение получали реакцией я присоединения водорода согласно следующей реакционной схеме:
[0161]
[0162]
[0163]
Примеры 1-5 и сравнительные примеры 1-3: газофазная реакция
SUS трубку (внешний диаметр: 1/2 дюйма) в качестве реакционной трубы заполняли, в качестве катализатора, 5,0 г Pd/C катализатора, в котором палладий был на подложке из углерода (полученный N.E. Chemcat Corporation, содержащий 3 масс% паллдаия относительно массы катализатора). После сушки при 200°C в течение 2 часов в атмосфере азота, октафтор-2-бутен (исходное соединение; смесь цис- и транс-изомеров) протекал через реакционную трубу при нормальном давлении так, что продолжительность контакта (W/F) октафтор-2-бутена (исходное соединение) и Pd/C катализатора составляла 1,7-9,3 г⋅сек/см3. Октафторциклобутан (C318) те так, что молярное соотношение октафторциклобутана (C318) и октафтор-2-бутена (исходное соединение) составляло 0, 1 или 4 (молярное соотношение 0 обозначает, что C318 не тек). Затем, тек газообраный водород, который будет реагировать.
[0164]
Реакция протекала газофазным непрерывным проточным способом.
[0165]
Реакционную трубу нагревали до 70-100°C, начиная реакцию присоединения водорода.
[0166]
Молярное соотношение (соотношение H2/октафтор-2-бутен) газообразного водорода, который приводится в контакт с октафтор-2-бутеном (исходное соединение), регулировали равным 1,1, и дистиллят, прошедший через градирню, собирали через час после начала реакции. Однако в сравнительном примере 3 вместо газообразного водорода применяли газовую смесь, разбавленную газообразным азотом, так что молярное соотношение (N2/H2) азота и водорода составляло 4.
[0167]
После этого, масс-спектрометрию проводили газовая хроматография/масс-спектрометрия (GC/MS), применяя газовый хроматограф (изготовленный Shimadzu Corporation, торговое название: “GC-2014”). Структурный анализ, применяя ЯМР спектры, проводили, применяя ЯМР (изготовленный JEOL Ltd., торговое название: “400YH”). По результатам масс-спектрометрии и структурного анализа было подтверждено, что CF3CHFCHFCF3 получали в качестве целевого соединения. Результаты представлены в таблице 1.
[0168]
Таблица 1
C318/CF3CF=CFCF3
H2/CF3CF=CFCF3
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА ГАЛОГЕНИРОВАННОГО АЛКЕНОВОГО СОЕДИНЕНИЯ И ФТОРИРОВАННОГО АЛКИНОВОГО СОЕДИНЕНИЯ | 2020 |
|
RU2793785C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРАЛКИНОВОГО СОЕДИНЕНИЯ | 2022 |
|
RU2835968C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО БЕНЗИЛАМИНА И ПРОИЗВОДНОЕ АЦИЛБЕНЗИЛАМИНА | 2003 |
|
RU2362766C2 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДНОГО ПРОИЗВОДНОГО | 2009 |
|
RU2469025C2 |
| ПУТИ ПРИМЕНЕНИЯ ИНГИБИТОРОВ ФОСФОДИЭСТЕРАЗЫ | 2020 |
|
RU2795503C2 |
| Новый ингибитор на основе производного хинолина | 2019 |
|
RU2802283C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА И СОДЕРЖАЩИЕ ИХ ГЕРБИЦИДЫ | 1994 |
|
RU2154063C2 |
| НОВЫЕ КОМПЛЕКСЫ РУТЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2608731C2 |
| ПРОИЗВОДНЫЕ АМИДИНА, СМЕСЬ ИХ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫЕ ИЗОМЕРЫ И ИХ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТАГОНИСТИЧЕСКИМ ДЕЙСТВИЕМ В ОТНОШЕНИИ ЛЕЙКОТРИЕНА B | 1993 |
|
RU2124002C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО БЕНЗОКСАЗИНА, СПОСОБЫ ПОЛУЧЕНИЯ ЕГО ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 2000 |
|
RU2258069C2 |
Изобретение относится в двум вариантам способа получения алканового соединения, представленного формулой (1), где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом фтора, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу. При этом по одному из вариантов способ включает: (IIA) реакцию, в присутствии катализатора и циклоалканового соединения, представленного формулой (3), где R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми, и каждый представляет собой атом фтора или фторалкильную группу; алкенового соединения, представленного формулой (2), где X1, X2, R1 и R2 представляют собой как определено выше; и галогенсодержащего газа для гидрирования алкенового соединения, представленного формулой (2). Изобретение позволяет получать целевое соединение таким способом, что совместно получают (S),(R) изомер, (R),(R) изомер и (S),(S) изомер. 2 н. и 6 з.п. ф-лы, 5 пр., 1 табл.
R1CHX1CHX2R2 (1)
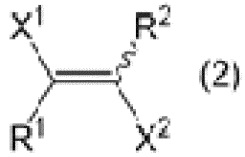
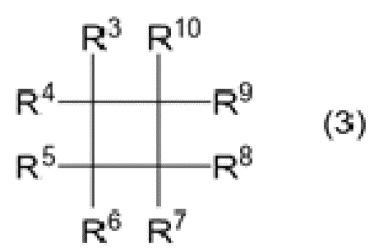
1. Способ получения алканового соединения, представленного формулой (1)
R1CHX1CHX2R2, (1)
где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом фтора, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу; причем способ включает:
(IIA) реакцию в присутствии катализатора и циклоалканового соединения, представленного формулой (3)
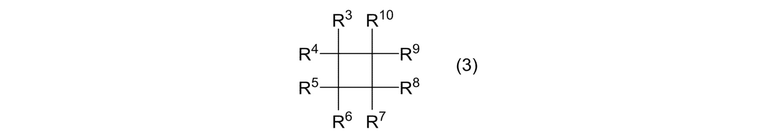
где R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми, и каждый представляет собой атом фтора или фторалкильную группу; алкенового соединения, представленного формулой (2)
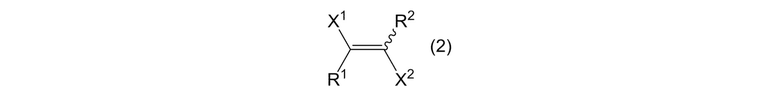
где X1, X2, R1 и R2 представляют собой, как определено выше; и галогенсодержащего газа для гидрирования алкенового соединения, представленного формулой (2).
2. Способ получения по п. 1, где количество циклоалканового соединения, представленного формулой (3), применяемое на стадии гидрирования, составляет 0,5-20 моль на моль алкенового соединения, представленного формулой (2).
3. Способ получения по п. 1 или 2, где способ включает, перед стадией гидрирования:
(IA) реакцию циклоалканового соединения, представленного формулой (3)
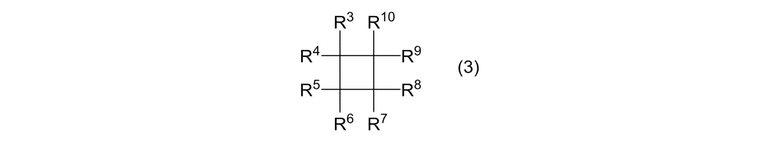
где R3, R4, R5, R6, R7, R8, R9 и R10 представляют собой, как определено выше; и алкенового соединения, представленного формулой (4)
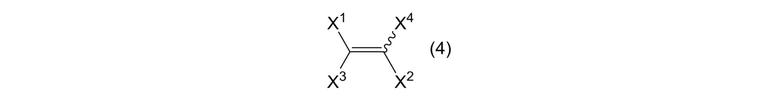
где X1 и X2 представляют собой, как определено выше, и X3 и X4 являются одинаковыми или отличными, и каждый представляет собой атом фтора; получая алкеновое соединение, представленное формулой (2)
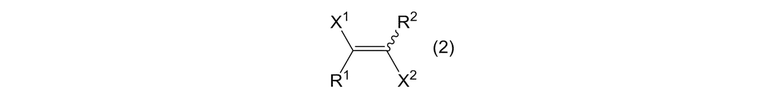
где X1, X2, R1 и R2 представляют собой, как определено выше.
4. Способ получения алканового соединения, представленного формулой (1)
R1CHX1CHX2R2, (1)
где X1 и X2 являются одинаковыми или отличными, и каждый представляет собой атом фтора, и R1 и R2 являются одинаковыми или отличными, и каждый представляет собой алкильную группу или фторалкильную группу; причем способ включает:
(IB) реакцию циклоалканового соединения, представленного формулой (3)
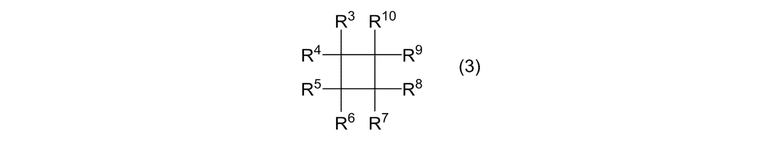
где R3, R4, R5, R6, R7, R8, R9 и R10 являются одинаковыми или отличными, и каждый представляет собой атом фтора или фторалкильную группу; и алкенового соединения, представленного формулой (4)
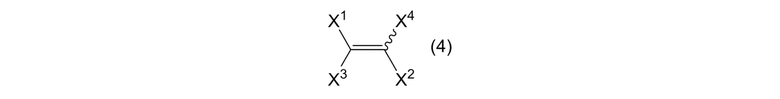
где X1 и X2 представляют собой, как определено выше, и X3 и X4 являются одинаковыми или отличными, и каждый представляет собой атом фтора; получая смесь, содержащую циклоалкеновое соединение, представленное формулой (2)
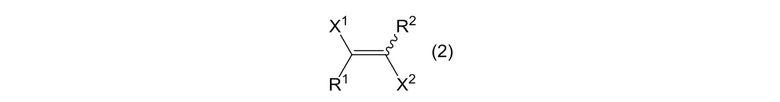
где X1, X2, R1 и R2 представляют собой, как определено выше; и циклоалкановое соединение, представленное формулой (3); и
(IIB) реакцию смеси, полученной на стадии (IB), и галогенсодержащего газа в присутствии катализатора для гидрирования циклоалкенового соединения, представленного формулой (2).
5. Способ получения по п. 4, где на стадии гидрирования, циклоалкановое соединение, представленное формулой (3), применяемое в качестве исходного соединения в смеси, содержится в количестве 0,5-20 моль на моль алкенового соединения, представленного формулой (2).
6. Способ получения по любому из пп. 1-5, где стадию гидрирования проводят в газовой фазе.
7. Способ получения по любому из пп. 1-6, где алкановое соединение, представленное формулой (1), которое получают, включает 3 алкановых соединения, представленных формулами (1A), (1B) и (1C)
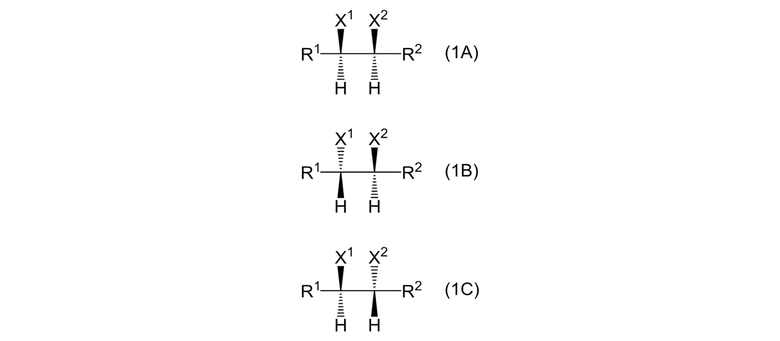
где X1, X2, R1 и R2 представляют собой, как определено выше.
8. Способ получения по п. 7, где получают 20-80 моль% алканового соединения, представленного формулой (1A), 10-40 моль% алканового соединения, представленного формулой (1B), и 10-40 моль% алканового соединения, представленного формулой (1C), исходя из суммарного количества продукта, полученного на стадии гидрирования, которое принимают за 100 моль%.
| KATING P.M | |||
| ET AL, HYDROGENATION OF FLUOROOLEFINS STUDIED BY GAS PHASE NMR: A NEW TECHNIQUE FOR HETEROGENEOUS CATALYSIS, J | |||
| AM | |||
| CHEM | |||
| SOC, 1996, VOL | |||
| Прибор для массовой выработки лекал | 1921 |
|
SU118A1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ ВЫЧЕРЧИВАНИЯ ДУГ ОКРУЖНОСТИ ПРИ КРОЙКЕ | 1927 |
|
SU10000A1 |
| HUDLICKY, T | |||
| ET AL, PRACTICAL PREPARATION OF SOME POTENTIALLY ANESTHETIC FLUOROALKANES: REGIOCONTROLLED INTRODUCTION OF HYDROGEN ATOMS, JOURNAL OF FLUORINE CHEMISTRY, 1992, | |||
Авторы
Даты
2023-08-08—Публикация
2020-11-24—Подача