Область техники
Настоящее изобретение относится к адъюванту для вакцины, в частности, к адъюванту на основе микро/наночастиц золедроната цинка с эффектом замедленного высвобождения, который может значительно усиливать гуморальный иммунный ответ и клеточный иммунный ответ, и может использоваться в качестве вакцинного адъюванта в получении вакцин. Настоящее изобретение относится к области иммунологии.
Уровень техники
Цинк представляет собой важный химический элемент с особыми биологическими функциями. Например, следовые количества цинка присутствуют примерно в 300 ферментах, участвующих в клеточном метаболизме, и они играют важную роль в клеточном дыхании, делении клеток, синтезе белка, синтезе ДНК, репарации повреждений и активации иммунной функции. Таким образом, дефицит или нарушение обмена цинка связаны со многими заболеваниями, в частности, с заболеваниями иммунной системы (Autoimmunity Reviews, 2015, 14(04) 277-285). В иммуноцитах двухвалентные катионы, включая цинк, играют важную роль в регуляции внутриклеточных сигнальных путей. Дефицит цинка оказывает влияние на выживаемость, пролиферацию и созревание лимфоцитов в системах врожденного иммунитета и адаптивного иммунитета; исследования показали, что дефицит цинка отрицательно влияет на продукцию и функцию цитокинов, синтезированных иммуноцитами, и на количество, пролиферацию и дифференцировку периферических и тимусных Т-клеток. Результаты исследований показали, что недостаток следовых количеств цинка приводит к «старению» иммунной системы у пожилых людей (Immunity & Aging, 2009, 6(9): 1-17). В общем, цинк играет важную роль в продукции, развитии и функционировании Т-клеток.
Бисфосфонаты (BP), как наиболее важные лекарственные средства для лечения остеопороза, представляют собой аналоги неорганического пирофосфата. Они образуются посредством замещения атома кислорода в пирофосфатной связи P-O-P на атом углерода и имеют специфический остов связи P-C-P. Они не могут легко ферментативно гидролизоваться в организме, устойчивы к высокой температуре и стабильны к воздействию многих химических веществ. Между тем, за счет молекулярной конфигурации P-C-P их трехмерную структуру можно объединить с гидроксиапатитом или ионами металлов кальция, железа и цинка. Золедроновая кислота (ZOL) представляет собой азотсодержащее лекарственное средство на основе бисфосфоновой кислоты с гетероциклической структурой. Он обладает сильным действием, низкой дозой и удобством в применении. Клинические исследования показали, что бисфосфонаты, используемые в качестве адъювантного лечения таких заболеваний, как множественная миелома, рак молочной железы, рак почки, рак предстательной железы и т. д., могут снизить частоту заболеваний, связанных с костями, у пациентов, снизить частоту рецидивов рака и пролонгировать выживаемость пациентов, тем самым улучшая клинические результаты. Золедронат особенно преимущественен с точки зрения противоопухолевого действия, и он широко используется в клинических исследованиях с различными злокачественными опухолями. Кроме того, результаты других исследований показали, что лекарственные средства на основе бисфосфонатов также обладают иммуномодулирующим действием и могут повысить гуморальный иммунный ответ, воздействуя на В-клетки (Cell Rep., 2013, 5 (2)); и золедроновая кислота может увеличить антигенспецифический ответ CD8+ Т-клеток (Vaccine, 2016, 34 (10): 1275-81).
Dieter Berndardt et al. разработали гель гидроксида цинка или гель гидроксида железа, способ его получения и его применение в качестве адъюванта для вакцины (патент США № 5252327, дата выдачи: 12 октября 1993 г.). Гель гидроксида цинка или гель гидроксида железа обладает хорошим адсорбционным эффектом на вирусы или белки, и имеет хороший адъювантный эффект; гель гидроксида цинка может стимулировать как гуморальный, так и клеточный иммунный ответ, в то время как гель гидроксида железа в основном усиливает гуморальный иммунный ответ, и оба обладают хорошей местной и системной переносимостью; и оба обладают более высоким иммуностимулирующим эффектом при использовании в сочетании с лецитином.
Hu Yunzhang et al. разработали вакцинный адъювант (патент Китая, публикация (уведомление) № CN101444623A, дата публикации (уведомление): 3 июня 2009 г.). Изобретение относится к адъюванту для вакцины, т. е. к соединению гидроксиду цинка, имеющему химическую формулу Zn(OH)2 и молекулярную массу по химической формуле 99,4046 дальтон, для применения в производстве адъюванта для вакцин, и для использования в получении адъюванта для вакцины против гепатита А. Гидроксид цинка, используемый в комбинации с вакциной в качестве адъюванта, может эффективно усиливать гуморальный иммунный ответ вакцины, и его эффект усиления иммунитета выше, чем у алюминиевого адъюванта. И результаты испытаний на животных показывают, что гидроксид цинка, используемый в качестве нового адъюванта для вакцины, имеет лучший сенсибилизирующий эффект и лучшие характеристики в отношении безопасности, чем алюминиевый адъювант.
Wang Haixuan et al. (Chinese Journal of Biologicals, 2011, 24 (10): 1174-1176) изучали иммунопотенцирование гепарансульфата (HS) и гидроксида цинка в качестве адъюванта на гуморальный иммунный ответ у мышей, индуцированный рекомбинантной полипептидной вакциной с антигенным эпитопом вируса гепатита С, и результаты показали, что комбинированный адъювант из HS и гидроксида цинка может эффективно усиливать гуморальный иммунный ответ у мышей, иммунизированных рекомбинантной полипептидной вакциной с антигенным эпитопом HCV, и может до некоторой степени снижать дозу антигена.
Hu Yunzhang et al. разработали вакцинный адъювант на основе фосфата цинка (патент Китая, публикация (уведомление) № CN101972477B, дата публикации (уведомление): 26 сентября 2012 г.). Изобретение относится к адъюванту для вакцины на основе фосфата цинка, в частности, относится к применению фосфата цинка в качестве адъюванта для вакцины и применению адъюванта для вакцины на основе фосфата цинка в производстве вакцин. Фосфат цинка используется в качестве вакцинного адъюванта в комбинации с антигеном, который может эффективно усиливать гуморальный иммунный ответ на вакцину. Его эффект усиления иммунитета выше, чем у алюминиевого адъюванта и адъюванта на основе гидроксида цинка, и результаты испытаний на животных показали, что при использовании в качестве адъюванта для вакцины фосфат цинка показал более высокий сенсибилизирующий эффект и лучшие свойства в отношении безопасности, чем алюминиевый адъювант и адъювант на основе гидроксида цинка.
Hu Yunzhang et al. разработали комбинированный вакцинный адъювант (патент Китая, публикация (уведомление) № CN102085366B, дата публикации (уведомление): 26 декабря 2012 г.). Изобретение относится к комбинированному вакцинному адъюванту, отличающемуся тем, что он состоит из следующих компонентов: ферулата натрия и гидроксида цинка в массовом соотношении от 10:1 до 50:1. Совместное применение комбинированного вакцинного адъюванта и вакцины может эффективно усиливать гуморальный иммунный ответ на вакцину. Эффект усиления аналогичен эффекту алюминиевого адъюванта, но превосходит эффект одного адъюванта ферулата натрия и одного адъюванта гидроксида цинка. И он нетоксичен, не имеет побочных эффектов, безопасен и надежен в дозе, необходимой для иммунизации. Сырье для комбинированного вакцинного адъюванта по изобретению является широкодоступным, и представляет собой коммерчески доступные продукты. Комбинированный вакцинный адъювант имеет простой способ приготовления, низкую стоимость и стабильную эффективность. Комбинированный адъювант для вакцины можно использовать в качестве адъюванта для вакцины против гепатита В, генно-инженерной вакцины, вирусной вакцины и т.п.
Wang Haixuan et al. разработали адъювант на основе золедроновой кислоты и вакцину, содержащую адъювант на основе золедроновой кислоты (патент Китая, публикация (уведомление) № CN103768595 B, дата публикации (уведомление): 2 марта 2016 г.). Изобретение относится к адъюванту на основе золедроновой кислоты и вакцине, содержащей адъювант на основе золедроновой кислоты, т. е. каждая доза вакцины содержит от 10 до 20 мкг адъюванта золедроновую кислоту. Адъювант на основе золедроновой кислоты, обеспеченный изобретением, имеет низкую токсичность и побочные эффекты, безопасен и надежен при применении в дозе, необходимой для иммунизации, может эффективно индуцировать антигенспецифический гуморальный иммунный ответ, и обладает иммунным эффектом, сходным с таковым у алюминиевого адъюванта, и его сырье является широкодоступным, и он имеет стабильную эффективность, и его можно использовать в качестве адъюванта для вакцин. Takuya SHISHIDO et al. разработали вакцинную фармацевтическую композицию, содержащую бисфосфонат, которая может индуцировать выработку эффективного гуморального иммунного ответа в организме и которую можно вводить трансдермально или через слизистые оболочки (патент США, номер публикации: 2017/ 0281759A1, дата публикации: 5 октября 2017 г.).
Cai Hongzhi et al. (Chinese Journal of Biologicals, 2013, 26 (05): 608-610) исследовали влияние комбинированного адъюванта на основе гидроксида цинка и гепарансульфата (HS) на гуморальный иммунный ответ у мышей, индуцированный вакциной против бешенства, и результаты показали, что комбинированный адъювант на основе гидроксида цинка и HS может усиливать гуморальный иммунный ответ у мышей, индуцированный вакциной против бешенства.
Chen Zhenpu et al. разработали адъювант на основе глицината цинка и вакцину, содержащую адъювант на основе глицината цинка (патент Китая, публикация (уведомление) № CN104096229A, дата публикации (уведомление): 15 октября 2014 г.). Изобретение относится к адъюванту на основе глицината цинка и вакцине, содержащей адъювант на основе глицината цинка, т. е. каждая доза вакцины содержит от 0,1 до 1 мг адъюванта глицината цинка, растворенного в PBS с pH=6-8. Адъювант на основе глицината цинка, обеспеченный изобретением, представляет собой адъювант для медицинской практики, и также питательный усилитель цинка. Он имеет низкую токсичность и побочные эффекты, безопасен и надежен в применении в дозе, необходимой для иммунизации. Он может эффективно индуцировать антигенспецифические гуморальные иммунные ответы, и эффект индуцированного гуморального иммунного ответа выше, чем в группе без адъюванта. Сырье для адъюванта глицината цинка является широкодоступным, и представляет собой коммерчески доступные продукты. Он имеет простой способ получения, низкую стоимость, стабильную эффективность, высокую биологическую активность, отсутствие токсических или неблагоприятных эффектов, и его можно добавлять в различные обычные вакцины и генно-инженерные вакцины в качестве адъюванта вакцины.
Mahsa Afshari et al. (Cytokine, 2016, 81: 71-76) использовали модель инфекции Leishmania на мышах BALB/c. Было обнаружено, что пероральное скармливание мышам сульфата цинка может значительно снизить паразитарную нагрузку и повысить уровень экспрессии мРНК цитокина Th1-профиля. Это указывает на то, что сульфат цинка может индуцировать сильный иммунный ответ Th1 у мышей BALB/c, зараженных Leishmania.
Сущность изобретения
Для преодоления недостатков существующих вакцинных алюминиевых адъювантов, т. е. неспособности стимулировать Th1-опосредованный иммунный ответ и неспособности усиливать иммуногенность вакцин на основе полипептидов и нуклеиновых кислот, и также с учетом роли золедроновой кислоты в усилении иммунитета, получен адъювант на основе микро/наночастиц золедроната цинка соосаждением золедроновой кислоты и микроэлемента цинка, который также играет важную роль в регуляции иммунной системы. Благодаря креативной работе авторы настоящего изобретения обнаружили, что адъювант на основе микро/наночастиц золедроната цинка может значительно повысить гуморальный иммунный ответ и клеточный иммунный ответ. Таким образом, настоящее изобретение относится к адъюванту для вакцины на основе золедроната цинка со значительным иммуностимулирующим действием.
Следовательно, в одном аспекте настоящее изобретение относится к адъюванту на основе микро/наночастиц золедроната цинка, полученному соосаждением ионов цинка вместе с фосфонокислотными группами, фосфатными радикалами и гидроксидными радикалами, который для краткости называется адъювантом на основе золедроната цинка.
В конкретном варианте адъювант на основе золедроната цинка по настоящему изобретению можно получить равномерным смешиванием раствора растворимой соли, содержащей ионы цинка, с золедроновой кислотой и раствором гидроксида натрия, или равномерным смешиванием раствора растворимой соли, содержащей ионы цинка, с золедроновой кислотой, раствором гидроксида натрия и фосфата натрия c получением адъюванта на основе золедроната цинка.
В конкретном варианте осуществления способ смешивания включает, не ограничивается этим, последовательное осаждение, раздельное осаждение с последующим смешиванием или соосаждением.
В одном варианте осуществления соотношение молярных концентраций цинка:золедроновой кислоты в адъюванте на основе золедроната цинка в общем не ограничивается. В предпочтительном варианте осуществления соотношение молярных концентраций цинка: золедроновой кислоты в адъюванте на основе золедроната цинка может составлять (1-8):1. Предпочтительно соотношение молярных концентраций цинка:золедроновой кислоты выбрано из 1:1, 4:1 и 8:1.
В одном варианте осуществления адъювант на основе золедроната цинка может также содержать фосфат. Например, комбинированный адъювант на основе золедроната цинка получают замещением золедроновой кислоты фосфатом в различных молярных соотношениях (неполное замещение) с помощью различных методов смешивания (например, последовательного осаждения, раздельного осаждения с последующим смешиванием или соосаждением и др.). В таком комбинированном адъюванте на основе золедроната цинка соотношение молярных концентраций Zn:фосфатного радикала в общем не ограничивается. В предпочтительном варианте осуществления соотношение молярных концентраций Zn:фосфатного радикала может составлять (1-8):1. Предпочтительно соотношение молярных концентраций Zn:фосфатного радикала выбрано из 1,5:1 и 4:1, тем самым образуя органический-неорганический гибридный адъювант золедронат цинка.
В другом варианте осуществления адъюванта золедроната цинка, адъювант на основе золедроната цинка может дополнительно содержать алюминий (Al); например, адъювант на основе золедроната цинка-алюминия получают замещением Zn на Al в различных соотношениях (неполное замещение) и с помощью различных методов смешивания (например, последовательного осаждения, разделенного осаждения с последующим смешиванием или соосаждением и т. д.). В таком адъюванте золедронат цинка-алюминий соотношение молярных концентраций Zn:Al в общем не ограничивается. В предпочтительном варианте осуществления соотношение молярных концентраций Zn:Al может составлять (0,02-1):1, и предпочтительно соотношение молярных концентраций Zn:Al выбрано из 0,375:1, 0,5:1 и 0,8:1.
В одном варианте осуществления конкретный тип соединения цинка не ограничивается, например, приемлемыми являются гидроксид цинка, фосфат цинка, сульфат цинка, карбонат цинка или другие типы цинксодержащих адъювантов, известные в данной области, при условии, что адъювант золедронат цинка получают осаждением ионов цинка и фосфонокислотных групп, фосфатных радикалов и гидроксидных радикалов.
В одном варианте осуществления раствор фосфата может быть выбран, не ограничиваясь этим, из фосфата натрия, гидрофосфата натрия (безводного, дигидрата, гептагидрата, додекагидрата), дигидрофосфата натрия (безводного, дигидрата), фосфата калия, гидрофосфата калия, дигидрофосфата калия, пирофосфата, полифосфорной кислоты и любых их смесей.
В одном варианте осуществления конкретный тип соединения алюминия не ограничивается, например, приемлемыми являются гидроксид алюминия, фосфат алюминия, сульфат алюминия или другие типы адъювантов на основе алюминия, известные в данной области техники, при условии, что адъювант золедронат цинк-алюминий получают осаждением ионов цинка и алюминия с фосфонокислотными группами, фосфатными радикалами и гидроксидными радикалами.
В одном аспекте настоящее изобретение относится к способу получения адъюванта на основе золедроната цинка, который включает:
осаждение ионов цинка посредством взаимодействия ионов цинка с фосфонокислотными группами, фосфатными радикалами и гидроксидными радикалами по отдельности или одновременно в растворе растворимой соли, с получением тем самым адъюванта на основе золедроната цинка.
В конкретном варианте осуществления способ включает:
а) получение раствора растворимой соли, содержащего ионы цинка,
b) равномерное смешивание раствора растворимой соли со стадии а) с золедроновой кислотой, гидроксидом натрия или равномерное смешивание раствора растворимой соли со стадии а) с золедроновой кислотой, раствором гидроксида натрия и фосфата натрия методом последовательного осаждения, раздельного осаждения с последующим перемешиванием или соосаждением с получением адъюванта на основе золедроната цинка.
В вариантах осуществления настоящего изобретения раствор растворимой соли в общем не ограничивается, например, он может быть выбран из раствора соляной кислоты.
В предпочтительном варианте осуществления способ дополнительно включает стерилизацию суспензии адъюванта на основе золедроната цинка, образованной после смешивания на стадии b), автоклавированием в условиях высокой температуры 121°C и высокого давления в течение 60 мин, охлаждением до комнатной температуры и затем выдерживанием при температуре от 2°C до 8°C, предпочтительно хранением при 4°C для дальнейшего применения. В одном варианте осуществления соотношение молярных концентраций цинка:золедроновой кислоты в адъюванте на основе золедроната цинка, полученном способом по настоящему изобретению, может составлять 1-8:1. В предпочтительном варианте осуществления соотношение молярных концентраций цинка:золедроновой кислоты выбрано из 1:1, 4:1 или 8:1.
В еще одном варианте осуществления в способе по настоящему изобретению для получения адъюванта на основе золедроната цинка-алюминия, адъювант на основе золедроната цинка-алюминия получают осаждением ионов цинка и ионов алюминия с фосфонокислотными группами, фосфатными радикалами и гидроксидными радикалами с использованием различных методов смешивания (например, последовательного осаждения, раздельного осаждения с последующим смешиванием или соосаждением и т. д.), где соотношение молярных концентраций Zn/Al установлено на уровне 0,375:1, 0,5:1 и 0,8:1.
Раствор растворимой соли ионов цинка, используемый здесь, может представлять собой раствор любой растворимой соли ионов цинка и предпочтительно представляет собой раствор ионов цинка в соляной кислоте.
В рамках настоящего изобретения, раствор золедроната предпочтительно представляет собой щелочной раствор золедроновой кислоты и гидроксида натрия.
В рамках настоящего изобретения, методы осаждения цинка и фосфоновокислотных групп могут представлять собой любые методы, при которых реакция осаждения происходит тщательным смешиванием раствора растворимой соли ионов цинка и щелочного раствора золедроновой кислоты и гидроксида натрия. Предпочтительно адъювант на основе золедроната цинка может быть приготовлен таким способом, как последовательное осаждение, раздельное осаждение с последующим перемешиванием или соосаждением и т. д.
В рамках настоящего изобретения, стерилизация может представлять любой метод, подходящий для стерилизации адъюванта на основе золедроната цинка. Например, может использоваться стерилизация паровым методом при высокой температуре и высоком давлении. Например, стерилизацию проводят при 121°C в течение 30-60 мин, предпочтительно 60 мин.
В одном варианте осуществления настоящее изобретение также относится к способу определения физических и химических свойств полученного адъюванта на основе золедроната цинка. В одном варианте осуществления для адъюванта определяют значение pH, размер частиц, дзета-потенциал, точку нулевого заряда (PZC) частиц, степень адсорбции и диссоциации с белками, степень осаждения ионов металлов, степень осаждения органической фосфоновой кислоты, степень растворения in vivo и in vitro осадка и т.д. а. Физические и химические свойства адъюванта можно определить обычными методами, например, см. US 9573811; Ai Xulu et al., Analysis of physicochemical properties of three aluminum hydroxide adjuvant, «Chinese Journal of Biologicals», 2015, 28(1): 44-477; и как описано в примерах, приведенных здесь.
В одном варианте осуществления адъювант на основе золедроната цинка, как здесь описано, имеет одно или более из следующих свойств: pH 8,0-9,0 до стерилизации, pH 6,0-8,0 после стерилизации, размер частиц 1-10 мкм, точку нулевого заряда частиц 4,0-11,4, степень осаждения ионов металлов > 99% и степень адсорбции белка > 80%.
В одном аспекте настоящее изобретение относится к композиции, в частности, фармацевтическому составу или композиции, которые содержат адъювант золедронат цинка, как здесь описано.
Способ получения фармацевтического состава или композиции включает стадию объединения адъюванта на основе золедроната цинка с носителем и, необязательно, одним или более вспомогательными ингредиентами.
В сущности, составы готовят однородным и равномерным объединением адъюванта на основе золедроната цинка с жидкими носителями или измельченными твердыми носителями, или с обоими, и затем, если необходимо, приданием продукту формы.
Жидкие лекарственные формы для перорального введения активных ингредиентов включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к адъюванту на основе золедроната цинка жидкие лекарственные формы могут содержать инертные разбавители, обычно используемые в данной области, например, такие как вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, масла (в частности, хлопковое, арахисовое, кукурузное масло, масло зародышей, оливковое, касторовое и кунжутное масло), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот и сорбитана и их смеси.
Помимо инертных разбавителей, композиции для перорального введения могут также включать адъюванты, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, подсластители, ароматизаторы, красители, отдушки и консерванты.
Суспензионные составы, в дополнение к адъюванту на основе золедроната цинка, могут содержать суспендирующие агенты, например, этоксилированные изостеариловые спирты, полиоксиэтиленсорбитол и сложные эфиры сорбитана, микрокристаллическую целлюлозу, метагидроксид алюминия, бентонит, агар-агар, трагакантовую камедь и их смеси.
Фармацевтическая композиция по настоящему изобретению для ректального или вагинального введения может быть представлена в виде суппозитория, который можно приготовить смешиванием адъюванта на основе золедроната цинка с одним или более подходящими нераздражающими эксципиентами или носителями (включая, например, какао-масло, полиэтиленгликоль, воск для суппозиториев или салицилат), которые являются твердыми при комнатной температуре и жидкими при температуре тела, тем самым расплавляясь в прямой кишке или влагалище с высвобождением адъюванта золедронат цинка. Состав, подходящий для вагинального введения по настоящему изобретению, также включает вагинальный суппозиторий, тампон, крем, гель, пасту, пену или спрей, содержащие подходящие носители, известные в данной области.
Фармацевтическая композиция по настоящему изобретению, подходящая для парентерального введения, содержит адъювант на основе золедроната цинка и один или более фармацевтически приемлемых стерильных изотонических водных или неводных носителей в комбинации с ним, включая раствор, дисперсию, суспензию или эмульсию, или стерильный порошок, который может быть восстановлен в стерильный инъекционный раствор или дисперсию перед использованием, которые могут содержать антиоксиданты, буферы, растворенные вещества, которые придают композиции изотоничность по отношению к крови предполагаемого реципиента, или суспендирующие агенты или загустители.
Примеры подходящих водных и неводных носителей, которые можно использовать в фармацевтических композициях по изобретению, включают воду, этанол, полиолы (такие как глицерин, пропиленгликоль, полиэтиленгликоль и т.п.) и их подходящие смеси, растительные масла, такие как оливковое масло и инъекционные растворы сложных органических эфиров, таких как этилолеат. Надлежащую текучесть можно поддерживать, например, за счет использования покрытия, таких как лецитин, поддержанием необходимого размера частиц (в случае дисперсий) и за счет использования поверхностно-активных веществ.
Эти композиции могут также содержать вспомогательные вещества, такие как смачивающие агенты, эмульгирующие агенты и диспергирующие агенты. Также может быть желательным включить в композиции изотонические агенты, такие как сахара, хлорид натрия и т.п. Кроме того, пролонгированное всасывание инъекционной фармацевтической формы можно обеспечить включением агентов, замедляющих абсорбцию, таких как моностеарат алюминия и желатин.
Депо-формы для инъекций можно получить формированием матриц микрокапсул адъюванта золедроната цинка в биодеградируемых полимерах (таких как полилактид-полигликолид). В зависимости от соотношения адъюванта на основе золедроната цинка к полимеру и природы конкретного используемого полимера скорость высвобождения адъюванта золедроната цинка можно регулировать. Примеры других биодеградируемых полимеров включают поли(ортоэфиры) и поли(ангидриды). Инъекционные препараты депо также получают включением адъюванта на основе золедроната цинка в липосомы или микроэмульсии, которые совместимы с тканями тела. Инъекционные материалы можно стерилизовать, например, фильтрованием через фильтр, задерживающий бактерии.
Составы могут быть представлены в однодозовых или многодозовых герметичных контейнерах (например, в ампулах и флаконах) и могут храниться в лиофилизированном состоянии, требующем только добавления стерильного жидкого носителя, например, воды для инъекций, непосредственно перед использованием. Растворы и суспензии для приготовления экстемпоро можно приготовить из стерильных порошков, гранул и таблеток описанного выше типа.
В одном аспекте настоящее изобретение также относится к иммуногенной композиции, содержащей адъювант на основе золедроната цинка, как здесь описано, и один или более антигенов.
В рамках настоящего изобретения, иммуногенная композиция при введении субъекту или животному индуцирует защитный иммунный ответ против указанного одного или более содержащихся в ней антигенов.
В одном аспекте настоящее изобретение также относится к вакцинной композиции, содержащей адъювант на основе золедроната цинка, как здесь описано, и один или более антигенов.
В рамках настоящего изобретения, вакцинная композиция при введении субъекту или животному индуцирует защитный иммунный ответ, например, против микроорганизма, или для эффективной защиты субъекта или животного от инфекции.
Вакцинную композицию можно использовать для профилактики или облегчения патологического состояния, при котором будет иметь место благоприятная реакция на модуляцию иммунного ответа. Такая вакцинная композиция может представлять собой профилактическую вакцину или терапевтическую вакцину. Предпочтительно вакцинная композиция включает генно-инженерную вакцину, такую как белковая вакцина, такая как рекомбинантная белковая вакцина против вируса ветряной оспы и опоясывающего лишая.
В одном аспекте настоящее изобретение также относится к адъюванту для вакцины, включающему адъювант на основе золедроната цинка, как здесь описано. Например, такой вакцинный адъювант может также включать дополнительный адъювант, как описано ниже.
В рамках настоящего изобретения, термин «адъювант» или «адъювант для вакцины» относится к веществу, способному неспецифически ускорять, пролонгировать или усиливать иммунный ответ против антигена.
Преимущественно адъюванты могут также уменьшить число иммунизаций или количество антигена, необходимых для выработки защитного иммунитета.
Хорошо известно, что адъювант сам по себе не стимулирует или практически не стимулирует иммунный ответ, но адъювант усиливает иммунный ответ против антигена. Следовательно, адъювант на основе золедроната цинка по настоящему изобретению можно комбинировать с одним или более антигенами с получением иммуногенной композиции или вакцины, которые можно использовать для стимуляции иммунного ответа у субъекта. В качестве антигенов в комплексе или составе иммуногенного или вакцинного типа можно использовать различные вещества. Например, аттенуированные и инактивированные вирусные и бактериальные патогены, очищенные макромолекулы, белки, полисахариды, токсоиды, рекомбинантные антигены, микроорганизмы, содержащие чужеродный ген патогена, синтетические пептиды, полинуклеотиды, антитела и опухолевые клетки и т. д. Антигены можно использовать как в профилактических и терапевтических вакцинах. Антигены включают белковые антигены, такие как гликопротеиновый антиген gE вируса ветряной оспы и опоясывающего лишая (VZV gE).
Различные иммуномодулирующие молекулы также можно использовать в комбинации с адъювантом на основе золедроната цинка по настоящему изобретению для изменения иммунного ответа у субъекта. Иммуномодуляторы, описанные здесь, относятся к группе составов, которые могут регулировать, балансировать и восстанавливать иммунную функцию организма. Обычно используемые иммуномодуляторы включают три основные категории, представляющие собой иммунные усилители, иммуносупрессоры и двунаправленные иммунные модуляторы.
Количества антигена и адъюванта на основе золедроната цинка в вакцинной композиции по настоящему изобретению и их вводимая доза определяется методами, хорошо известными специалистам в области фармацевтики, где необходимо учитывать такие факторы, как следующие: специфический антиген, возраст, пол, массу тела, вид и состояние конкретного животного или пациента, а также способ введения.
В предпочтительном варианте осуществления вакцинная композиция по настоящему изобретению дополнительно содержит один или более компонентов, выбранных из группы, состоящей из: поверхностно-активных веществ, промоторов абсорбции, водопоглощающих полимеров, веществ, которые ингибируют ферментативную деградацию, спиртов, органических растворителей, масел, агентов, регулирующих pH, консервантов, агентов, регулирующих осмотическое давление, пропеллентов, воды и любых их смесей.
Вакцинная композиция по настоящему изобретению может дополнительно включать фармацевтически приемлемый носитель. Количество носителя будет зависеть от количеств, выбранных для других ингредиентов, требуемой концентрации антигена, выбора пути введения (перорального или парентерального) и т.д. Носитель может быть добавлен к вакцине в любое подходящее время. В случае лиофилизированной вакцины носитель можно, например, добавить до введения. В качестве альтернативы, конечный продукт может быть изготовлен с носителем.
Примеры подходящих носителей включают, не ограничиваясь этим, стерильную воду, физиологический раствор, буферы, забуференный фосфатом физиологический раствор, забуференный хлорид натрия, растительные масла, минимальную эссенциальную среду (MEM), MEM с буфером HEPES и т. д.
Необязательно, вакцинная композиция по изобретению может содержать обычные дополнительные адъюванты в различных количествах в зависимости от адъюванта и желаемого результата.
Примеры подходящих дополнительных адъювантов включают, не ограничиваясь этим, стабилизаторы; эмульгаторы; регуляторы pH, такие как гидроксид натрия, соляная кислота и т.д.; поверхностно-активные вещества, такие как Твин® 80 (полисорбат 80, коммерчески доступный от Sigma Chemical Co., St. Louis, Mo.); липосомы; адъювант iscom; синтетические гликопептиды, такие как мурамилдипептиды; наполнители, такие как декстран; карбоксиполиметилен; стенки бактериальных клеток, такие как экстракт стенок микобактериальных клеток; их производные, такие как Corynebacterium parvum; Propionibacterium acne; Mycobacterium bovis, например, коровья бацилла Кальметта-Герена (BCG); белки вируса коровьей оспы или поксвируса животных; адъюванты из субвирусных частиц, таких как орбивирус; холерный токсин; N, N-диоктадецил-N',N'-бис(2-гидроксиэтил)пропандиамин (пиридин); монофосфориллипид А; бромид диметилдиоктадециламмония (DDA, коммерчески доступный от Kodak, Rochester, N.Y.); синтетические агенты и их смеси.
Примеры подходящих стабилизаторов включают, не ограничиваясь этим, сахарозу, желатин, пептон, экстракты белковых гидролизатов, такие как NZ-амин или NZ-амин AS. Примеры эмульгаторов включают, не ограничиваясь этим, минеральное масло, растительное масло, арахисовое масло и другие стандартные, метаболизируемые, нетоксичные масла, пригодные для инъекционных или интраназальных вакцинных композиций.
Для целей настоящего изобретения эти адъюванты обозначаются здесь как «дополнительные» адъюванты, просто для противопоставления с вышеописанным адъювантом на основе золедроната цинка, поскольку комбинация адъюванта на основе золедроната цинка и антигенного вещества может значительно усилить гуморальный иммунный ответ на антигенное вещество. Дополнительные адъюванты в первую очередь включаются в состав вакцины в качестве вспомогательных средств, используемых в процессе производства, хотя некоторые адъюванты действительно обладают в некоторой степени иммунологически усиливающими свойствами и имеют двойное назначение.
К вакцинной композиции можно добавить обычные консерванты в эффективных количествах в диапазоне примерно от 0,0001 мас.% до примерно 0,1 мас.%. В зависимости от конкретного консерванта, используемого в составе, могут быть пригодными количества ниже или выше указанного диапазона. Типичные консерванты включают, например, сорбат калия, метабисульфит натрия, фенол, метилпарабен, пропилпарабен, тимеросал и т. д.
Выбор инактивированной, модифицированной или другого типа вакцинной композиции и получение улучшенного состава вакцинной композиции по настоящему изобретению известен или легко определяется специалистами в данной области.
Как правило, вакцинную композицию по настоящему изобретению можно удобно вводить перорально, парентерально (подкожно, внутримышечно, внутривенно, внутрикожно или внутрибрюшинно), интрабуккально, интраназально или трансдермально. Способ введения, предусмотренный настоящим изобретением, будет зависеть от антигенного вещества и сопутствующих формообразующих веществ. Например, если вакцинная композиция содержит сапонины, которые нетоксичны при пероральном или интраназальном введении, то необходимо соблюдать осторожность при введении гликозидов сапогенинов в кровоток, поскольку они действуют как сильные гемолитики. Кроме того, многие антигены не будут эффективны при пероральном введении. Предпочтительно вакцинную композицию вводят внутримышечно или внутрибрюшинно.
Дозировка вакцинной композиции будет зависеть, в частности, от выбранного антигена, пути введения, вида и других обычных факторов. Полагается, что специалист в данной области может легко и без труда оттитровать соответствующую дозу для индукции иммуногенного ответа на каждый антиген, чтобы определить эффективное иммунизирующее количество и путь введения.
В отношении вакцинного адъюванта, то адъювант на основе золедроната цинка по настоящему изобретению может повышать эффективность вакцины за счет усиления иммуногенности более слабых антигенов (например, высокоочищенных или рекомбинантных антигенов), за счет уменьшения количества антигенов, необходимых для индукции иммунного ответа, или за счет снижения частоты иммунизаций, необходимой для защитной иммунизации. Адъювант на основе золедроната цинка по настоящему изобретению может повышать эффективность вакцины у субъектов (например, новорожденных, пожилых людей и лиц с ослабленным иммунитетом) со сниженными или ослабленными иммунными ответами и может повышать эффективность вакцины в тканях-мишенях. Альтернативно, адъювант золедронат цинка по настоящему изобретению может способствовать усилению клеточного иммунитета и/или гуморального иммунитета посредством «запуска» специфического цитокинового профиля.
Комбинацию антигена и/или иммуномодулирующей молекулы и адъюванта на основе золедроната цинка по настоящему изобретению можно тестировать в различных доклинических токсикологических исследованиях и исследованиях безопасности, хорошо известных в данной области.
Например, такую комбинацию можно оценить на животной модели, на которой антиген оказался иммуногенным и может воспроизводимо иммунизировать при том же пути, который предлагается для клинических испытаний у людей.
Комбинацию антигена и/или иммуномодулирующей молекулы и адъюванта на основе золедроната цинка по настоящему изобретению можно тестировать, например, с использованием подхода, установленного Центром оценки и исследований биологических препаратов/Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов и Национальным институтом аллергии и инфекционных заболеваний (Goldenthal K.L. et al. AID Res Hum Retroviruses, 9: S45-9 (1993)).
Специалистам в данной области известно, как определить для конкретной комбинации антигена и/или иммуномодулирующей молекулы с комбинированным адъювантом по изобретению подходящую антигенную нагрузку, путь иммунизации, дозу, чистоту антигена и схему вакцинации, пригодную для лечения конкретного патологического состояния у определенного вида животных.
Иммуногенную композицию или вакцину по изобретению для индукции иммунного ответа можно вводить в виде раствора или суспензии вместе с фармацевтически приемлемой средой.
Такой фармацевтически приемлемой средой может быть, например, вода, забуференный фосфатом физиологический раствор, нормальный физиологический раствор или другой физиологически забуференный солевой раствор, или другой растворитель или носитель, такой как гликоль, глицерин, и масло, такое как оливковое масло или органический сложный эфир для инъекций. Фармацевтически приемлемая среда также может содержать липосомы или мицеллы и может содержать иммуностимулирующие комплексы, полученные смешиванием полипептидных или пептидных антигенов с детергентом и гликозидом (таким как Quil A).
Иммуногенную композицию или вакцину по изобретению можно вводить различными путями для стимуляции иммунного ответа. Например, иммуногенная композиция или вакцина может быть доставлена подкожно, внутрикожно, внутрилимфатически, внутримышечно, интратуморально, внутрипузырно, внутрибрюшинно и внутрицеребрально.
Специалисты в данной области знают, как выбрать подходящие пути доставки для конкретных составов адъюванта золедроновой кислоты по изобретению.
В предпочтительном варианте осуществления настоящего изобретения способ вакцинации для лечения или профилактики инфекции у млекопитающего включает применение вакцины по настоящему изобретению, где вакцина будет конкретно вводиться внутримышечно или внутрибрюшинно. Вакцину можно вводить в виде однократной дозы или, предпочтительно, вводить несколько раз, например, два, три или четыре раза в неделю или в месяц в соответствии с использованием стратегии прайм-иммунизации/буст-иммунизации. Подходящая доза зависит от множества различных параметров.
В одном аспекте настоящее изобретение также относится к применению адъюванта на основе золедроната цинка, как здесь описано, для производства вакцинного адъюванта, фармацевтической композиции, иммуногенной композиции или вакцинной композиции. Предпочтительно вакцина включает белковую вакцину, такую как рекомбинантная белковая вакцина против вируса ветряной оспы и опоясывающего лишая.
Краткое описание фигур
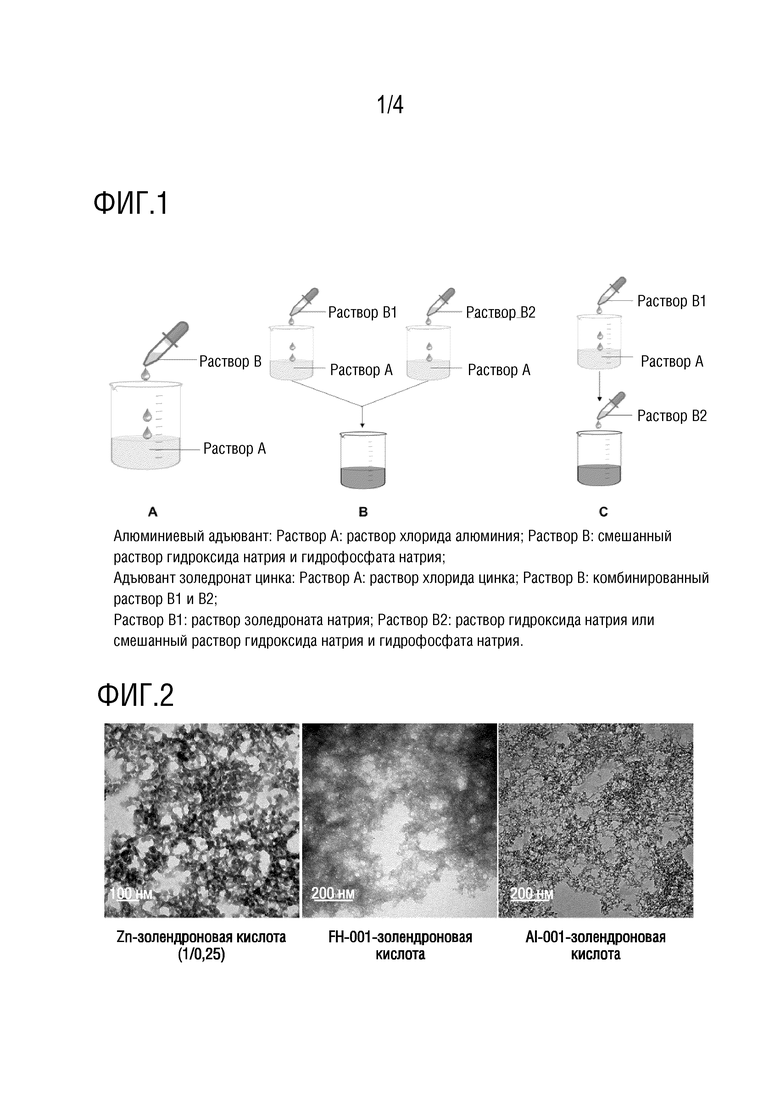
На фиг. 1: приведены схемы трех способов приготовления адъювантов.
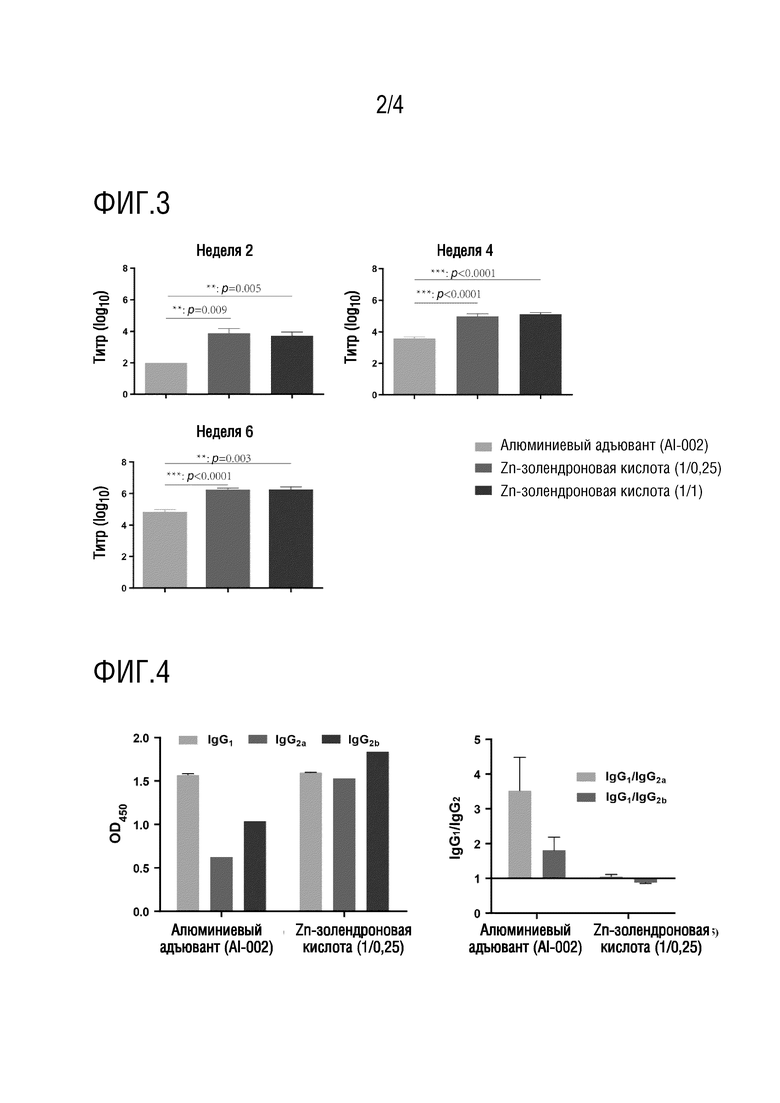
На фиг. 2: показана морфология частиц адъюванта на основе золедроната цинка, адъюванта на основе золедроната цинка и алюминия и адъюванта на основе золедроната алюминия.
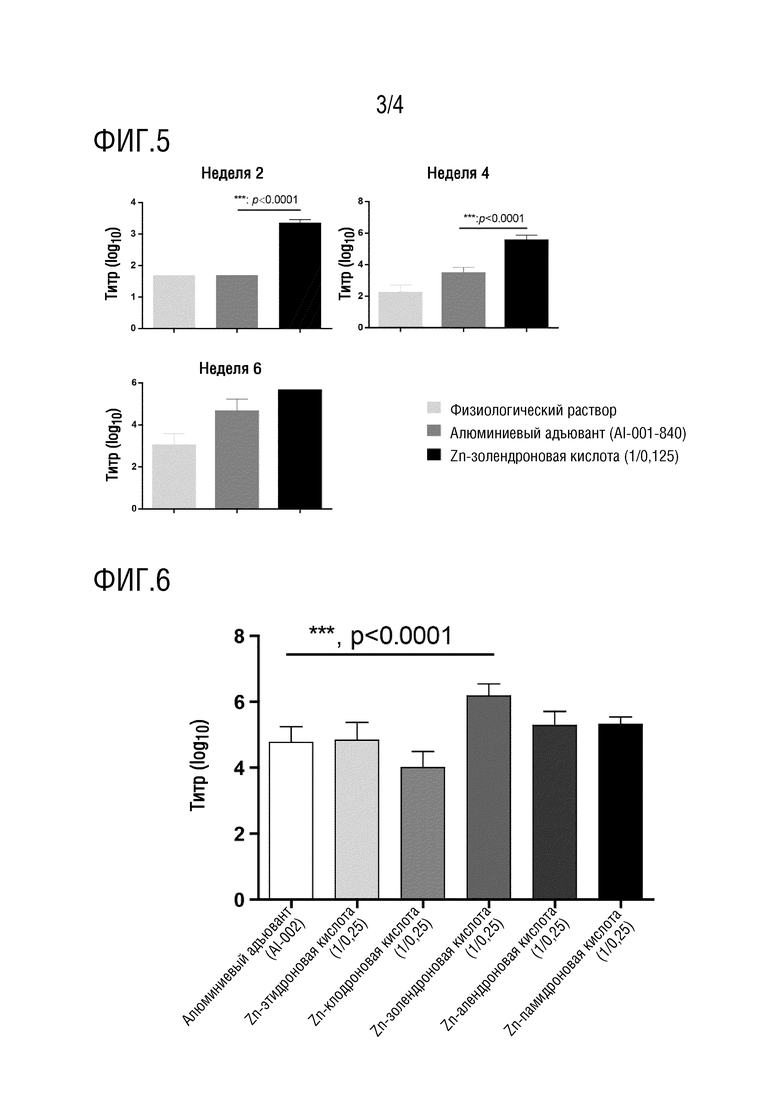
На фиг. 3: приведены результаты оценки адъювантной активности адъюванта на основе золедроната цинка в вакцине VZV gE, среднее значение ± стандартное отклонение: n=5, *p <0,05; **р <0,01; ***p <0,001, ****p <0,0001.
На фиг. 4: показано влияние адъюванта на основе золедроната цинка в комбинации с рекомбинантным белком gE VZV на изотипы мышиных антител, среднее значение ± стандартное отклонение: n=5, *p <0,05; **р <0,01; ***p <0,001, ****p <0,0001.
На фиг. 5: приведены результаты оценки адъювантной активности адъюванта на основе золедроната цинка с терапевтическим белком против вируса гепатита В, среднее значение ± стандартное отклонение: n=5, *p <0,05; **р <0,01; ***p <0,001, ****p <0,0001.
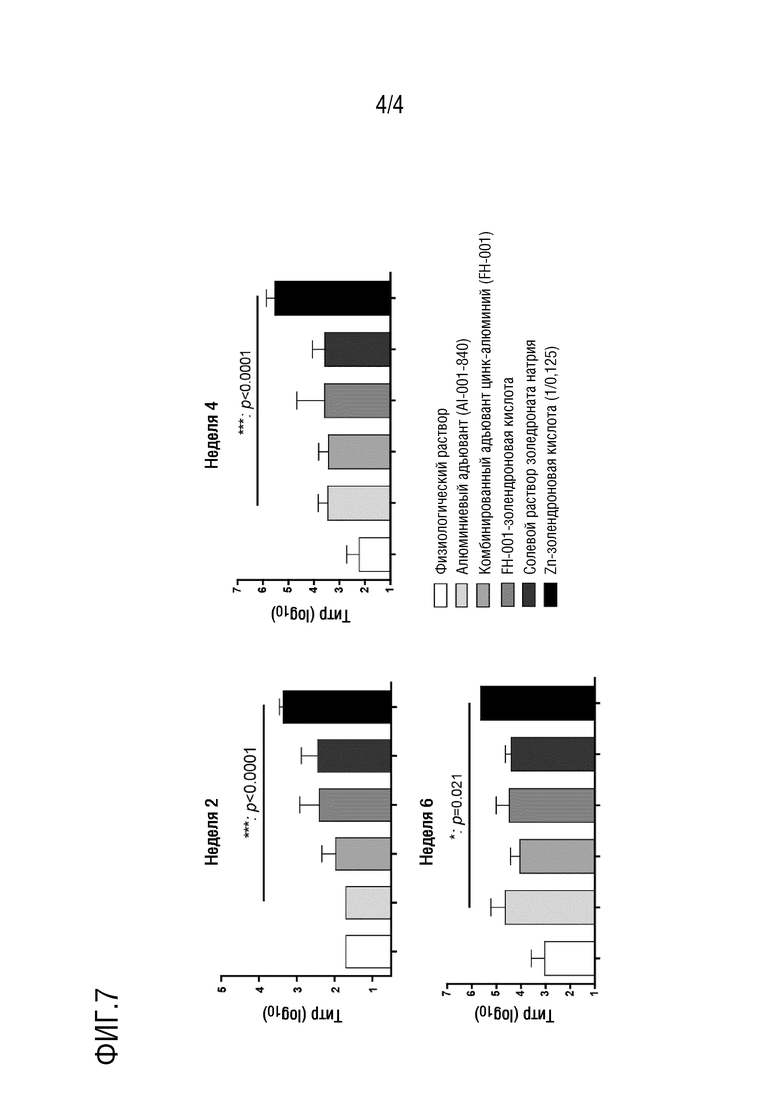
На фиг. 6: показано влияние других адъювантов на основе бисфосфоната цинка (Zn/Zol=1/0,25) в комбинации с VZV gE на титр антител в сыворотке мышей, среднее значение ± стандартное отклонение: n=5, *p <0,05; **р <0,01; ***p <0,001, ****p <0,0001.
На фиг. 7: показано влияние модифицированных адъювантов на основе золедроновой кислоты и золедроната цинка, в комбинации с терапевтическим белком против вируса гепатита В на титр сывороточных антител мышей, среднее значение ± стандартное отклонение: n=5, *p <0,05; **p <0,01; ***p <0,001, ****p <0,0001.
Конкретные модели для осуществления настоящего изобретения
Ниже подробно описаны варианты осуществления настоящего изобретения вместе с примерами. В примерах, в которых не указаны конкретные условия, подразумевается, что они должны выполняться в соответствии с обычными условиями или условиями, предложенными производителем. Реагенты или приборы, используемые без указания производителя, являются обычными продуктами, которые можно приобрести на коммерческой основе.
Материалы, используемые в следующих примерах получения, являются следующими:
Безводный хлорид цинка (ZnCl2): производства Xilong Chemical;
Гексагидрат хлорида алюминия (AlCl3·6H2O): производства Xilong Chemical;
Гидрофосфат натрия додекагидрат (Na2HPO4·12H2O): производства Xilong Chemical;
Гидроксид натрия (NaOH): производства Xilong Chemical;
Золедроновая кислота (C5H10N2O7P2): производства Hunan Huateng Pharmaceutical Co., Ltd.
Пример получения 1: получение адъюванта Zn-золедроновая кислота (1/0,25)
В соответствии с соотношением молярных концентраций Zn/ золедроновой кислоты 1:0,25 приготовили 50 мл 31,11 мМ раствора хлорида цинка, который был определен как раствор A; приготовили 50 мл раствора (7,78 мМ золедроновой кислоты+43 мМ гидроксида натрия+7,78 мМ гидрофосфата натрия), который был определен как раствор B. Раствор A и раствор B фильтровали через мембранный фильтр с размером пор 0,22 мкм для дальнейшего использования.
Приготовление суспензии адъюванта Zn-золедроновая кислота (1/0,25):
Растворы A и B использовали для получения суспензии адъюванта на основе золедроната цинка в соответствии со схемой, показанной на фиг. 1A, т. е. приготовленный раствор B добавляли по каплям в соответствии с объемным соотношением 1:1 к раствору A с образованием суспензии до его полного добавления.
Адъювант на основе золедроната цинка, полученный после смешивания, как показано на фиг. 1A, подвергали стерилизации в паровом автоклаве при 121°C в течение 60 мин, и затем охлаждали до комнатной температуры и затем хранили при 2-8°C.
Пример получения 2: получение адъюванта Zn-золедроновая кислота (1/1)
Приготовление растворов:
В соответствии с соотношением молярных концентраций Zn/ золедроновой кислоты 1:1 приготовили 50 мл 31,11 мМ раствора хлорида цинка, который был определен как раствор A; приготовили 50 мл раствора (31,11 мМ золедроновой кислоты+87 мМ гидроксида натрия), который был определен как раствор B. Раствор A и раствор B фильтровали через мембранный фильтр с размером пор 0,22 мкм для дальнейшего использования.
Как описано в примере получения 1, была приготовлена суспензия адъюванта Zn-золедроновая кислота (1/1).
Пример получения 3: получение адъюванта на основе золедроната цинка-алюминия (FH-001-золедроновая кислота)
Приготовление растворов:
В соответствии с молярной концентрацией Al/Zn 1:0,375, приготовили 50 мл смешанного раствора хлорида алюминия (122,44 мМ) и хлорида цинка (46,66 мМ), который был определен как раствор A; приготовили 50 мл раствора (18,66 мМ золедроновой кислоты+380 мМ гидроксида натрия), который был определен как раствор B. Раствор A и раствор B фильтровали через мембранный фильтр с размером пор 0,22 мкм для дальнейшего использования.
Как описано в примере получения 1, была приготовлена суспензия адъюванта FH-001-золедроновая кислота.
Пример получения 4: получение адъюванта золедронат алюминия (Al-001-золедроновая кислота)
Приготовление растворов:
В соответствии с молярной концентрацией Al/Zol 1:0,075 приготовили 50 мл 122,44 мМ раствора хлорида алюминия, который был определен как раствор A; приготовили 50 мл раствора (9,33 мМ золедроновой кислоты+9,33 мМ додекагидрата гидрофосфата натрия+370 мМ гидроксида натрия), который был определен как раствор B. Раствор A и раствор B фильтровали через мембранный фильтр с размером пор 0,22 мкм для дальнейшего использования.
Как описано в примере получения 1, была приготовлена суспензия адъюванта Al-001-золедроновая кислота.
Пример получения 5: получение Zn-золедроновой кислоты (1/ 0,125)
Приготовление растворов:
В соответствии с соотношением молярных концентраций Zn/ золедроновой кислоты 1:0,125 приготовили 50 мл 124,44 мМ раствора хлорида цинка, который был определен как раствор A; приготовили 50 мл раствора (15,56 мМ золедроновой кислоты+65,7 мМ гидроксида натрия), который был определен как раствор B. Раствор A и раствор B фильтровали через мембранный фильтр с размером пор 0,22 мкм для дальнейшего использования.
Как описано в примере получения 1, была приготовлена суспензия адъюванта Zn-золедроновая кислота (1/0,125).
Пример получения 6: приготовление алюминиевого адъюванта (Al-002)
Приготовление растворов:
Гексагидрат хлорида алюминия добавляли к воде с получением 0,5 л 62,22 мМ раствора хлорида алюминия, который был определен как раствор A; дигидрат гидрофосфата натрия и гидроксид натрия добавляли к воде с получением 0,5 л раствора, содержащего 18,68 мМ фосфата и 0,12 М гидроксида натрия, который был определен как раствор B. Растворы фильтровали через мембранный фильтр с размером пор 0,22 мкм для дальнейшего использования.
Как описано в примере получения 1, был приготовлен алюминиевый адъювант Al-002.
Пример получения 7: получение алюминиевого адъюванта (Al-001-840)
Приготовление растворов:
В соответствии с соотношением молярных концентраций фосфата/ Al 0,15 приготовили 0,5 л 124 мМ раствора хлорида алюминия, который был определен как раствор A; приготовили 0,5 л 18,6 мМ раствора гидрофосфата натрия, который был определен как раствор B. Раствор B дополнительно содержал 150 мМ гидроксида натрия. Растворы фильтровали через мембранный фильтр с размером пор 0,22 мкм для дальнейшего использования.
Как описано в примере получения 1, была приготовлена суспензия алюминиевого адъюванта Al-001-840.
Пример получения 8: приготовление адъюванта цинк-алюминий (FH-001)
Приготовление растворов:
Гексагидрат хлорида алюминия и безводный хлорид цинка добавляли к воде с получением 0,25 л раствора, содержащего 124,44 мМ хлорида алюминия и 46,68 мМ хлорида цинка, который был определен как раствор A; к воде добавляли дигидрат гидрофосфата натрия и гидроксид натрия с получением 0,25 л раствора, содержащего 18,68 мМ фосфата и 0,425 М гидроксида натрия, который был определен как раствор В. Растворы фильтровали через мембранный фильтр с размером пор 0,22 мкм для дальнейшего использования.
Приготовление комбинированного алюминиевого адъюванта:
Как показано на фиг. 1A, 0,25 л раствора B добавляли по каплям к 0,25 л раствора A до его полного добавления, с получением тем самым комбинированного адъюванта цинк-алюминий FH-001. Полученный комбинированный адъювант цинк-алюминий подвергали стерилизации в паровом автоклаве при 121°C в течение 60 мин, и затем охлаждали до комнатной температуры и затем хранили при 2-8°C.
Пример получения 9: получение адъюванта цинк-этидроновая кислота (1/0,25)
В соответствии с соотношением молярных концентраций Zn/ этидроновой кислоты 1:0,25 приготовили 50 мл 31,11 мМ раствора хлорида цинка, который был определен как раствор A; приготовили 50 мл раствора (7,78 мМ этидроновой кислоты+34 мМ гидроксида натрия+7,78 мМ гидрофосфата натрия), который был определен как раствор B. Раствор A и раствор B фильтровали через мембранный фильтр с размером пор 0,22 мкм для последующего использования.
Как описано в примере получения 1, была приготовлена суспензия адъюванта Zn-этидроновая кислота (1/0,25).
Пример получения 10: получение адъюванта Zn-клодроновая кислота (1/0,25)
В соответствии с соотношением молярных концентраций Zn/ клодроновой кислоты 1:0,25 приготовили 50 мл 31,11 мМ раствора хлорида цинка, который был определен как раствор A; приготовили 50 мл раствора (7,78 мМ клодроновой кислоты+36 мМ гидроксида натрия+7,78 мМ гидрофосфата натрия), который был определен как раствор B. Раствор A и раствор B фильтровали через мембранный фильтр с размером пор 0,22 мкм для последующего использования.
Как описано в примере получения 1, была приготовлена суспензия адъюванта Zn-клодроновая кислота (1/0,25).
Пример получения 11: получение адъюванта Zn-алендроновая кислота (1/0,25)
В соответствии с соотношением молярных концентраций Zn/ алендроновой кислоты 1:0,25 приготовили 50 мл 31,11 мМ раствора хлорида цинка, который был определен как раствор A; приготовили 50 мл раствора (7,78 мМ алендроновой кислоты+36 мМ гидроксида натрия+7,78 мМ гидрофосфата натрия), который был определен как раствор B. Раствор A и раствор B фильтровали через мембранный фильтр с размером пор 0,22 мкм для дальнейшего использования.
Как описано в примере получения 1, была приготовлена суспензия адъюванта Zn-алендроновая кислота (1/0,25).
Пример получения 12: получение адъюванта Zn-памидроновая кислота (1/0,25)
В соответствии с соотношением молярных концентраций Zn/ памидроновой кислоты 1:0,25 приготовили 50 мл 31,11 мМ раствора хлорида цинка, который был определен как раствор A; приготовили 50 мл раствора (7,78 мМ памидроновой кислоты+32 мМ гидроксида натрия+7,78 мМ гидрофосфата натрия), который был определен как раствор B. Раствор A и раствор B фильтровали через мембранный фильтр с размером пор 0,22 мкм для последующего использования.
Как описано в примере получения 1, была приготовлена суспензия адъюванта Zn-памидроновая кислота (1/0,25).
Далее настоящее изобретение будет описано ниже в сочетании с примерами.
Пример 1: определение физических и химических свойств адъюванта золедроната цинка
Следующие ниже методы определения были применимы к любому молярному соотношению Zn/золедроновой кислоты, т. е. к любому адъюванту на основе золедроната цинка, такому как адъювант золедронат цинка, с добавлением неорганической фосфорной кислоты или добавлением Al.
(1) Определение морфологии частиц адъюванта
После разбавления адъюванта золедроната цинка в 50 раз деионизированной водой, анализ проводили с использованием трансмиссионного электронного микроскопа (ТЕМ) JEM-2100 от Japan Electronics. Конкретные стадии заключались в следующем: нанесение образца адъюванта на медную сетку, покрытую углеродной пленкой, предоставление 10 мин для абсорбции, удаление остаточной жидкости фильтровальной бумагой, помещение образцов в камеру для образцов трансмиссионного электронного микроскопа для определения морфологии образца и получение фотографий для дальнейшего анализа.
Результаты эксперимента: можно было четко видеть, что адъювант Zn-золедроновая кислота (1/0,25) и адъювант Al-001-золедроновая кислота имели сферические частицы с наноядром, в то время как адъювант FH-001-золедроновая кислота имел форму пучка водорослей (фиг. 2).
(2) Определение pH
Отбирали образцы для тестирования, уравновешивали при комнатной температуре в течение не менее 30 мин и измеряли рН с использованием рН-метра со стеклянным электродом Sartorius.
Стандартный буфер (pH 7,00), стандартный буфер (pH 4,01) и стандартный буфер (pH 10,01) были выбраны для калибровки прибора в соответствии с требованиями инструкции по эксплуатации прибора.
Кнопку «Режим» нажимали для переключения режимов pH и мВ. Обычно режим pH выбирали при определении значения pH раствора.
Кнопку «Настройка» нажимали до тех пор, пока на дисплее не отображалось «чистый буфер», и затем нажимали кнопку «Ввод» для подтверждения и удаления данных предшествующей калибровки.
Нажимали кнопку «Настройка» до тех пор, пока на дисплее не отображалось «группа буферных растворов» «4.01, 7.00, 10.01», и затем нажимали кнопку «Ввод» для подтверждения.
Электрод осторожно извлекали из раствора для хранения электрода, электрод тщательно промывали деионизированной водой, и воду на поверхности удаляли промоканием фильтровальной бумагой после тщательного ополаскивания (следует соблюдать осторожность, чтобы не тереть электрод).
Электрод погружали в первый буферный раствор (pH 7,00) до тех пор, пока значение не стабилизировалось, и не появилась буква «S», затем нажимали кнопку «Стандартизовать», пока прибор не будет автоматически откалиброван. После успешной калибровки отображалась цифра «7.00» и наклон электрода.
Электрод извлекали из первого буферного раствора, тщательно промывали деионизированной водой и последовательно погружали электрод во второй буферный раствор (pH 4,01) до тех пор, пока значение не стабилизировалось, и не появилась буква «S», затем нажимали кнопку «Стандартизовать», пока прибор не будет автоматически откалиброван. После успешной калибровки отображается «4.01 7.00» и сообщение «Наклон». Наклон отображает измеренное значение наклона электрода, которое было приемлемым в диапазоне 90-105%.
Если было большое отклонение от теоретического значения, то отобразилось бы сообщение об ошибке (Err), в этом случае следует очистить электрод и повторить вышеописанные стадии для калибровки.
Вышеописанные операции повторяли для завершения калибровки третьей точки (pH 10,01).
После завершения калибровки электрод тщательно промывали деионизированной водой, и затем осторожно промокали фильтровальной бумагой. Раствор образца равномерно встряхивали, стеклянный электрод погружали в раствор образца до тех пор, пока значение pH изменялось не более чем на ± 0,05 в течение 1 мин, после чего показания подтверждали.
Раствор образца равномерно встряхивали и снова проводили измерение. Разница между двумя измеренными значениями pH не должна превышать 0,1. Среднее значение двух показаний было принято за значение pH тестируемого продукта.
Результаты эксперимента (таблица 1):
Диапазон значений pH для адъювантов Zn-золедроновая кислота составлял от 8,0 до 9,0 до стерилизации и от 6,5 до 7,0 после стерилизации.
(3) Определение размера частиц
Лазерный анализатор размера частиц Beckman LS 13320 включали и прогревали в течение 15 мин.
Запускали программное обеспечение управления анализатором, открывали закрытое отделение кюветы для образца, извлекали кювету для образца из резервуара для образца и добавляли 12 мл очищенной воды.
Кювету для образца помещали в резервуар для образца, и дверцу отсека закрывали.
Нажимали «запуск цикла», по очереди выбирали «измерение смещения», «выравнивание», «измерение фона», и, наконец, нажимали «запуск», нажимали «ОК» во всплывающем диалоговом окне для начала калибровки холостого фона.
Извлекали кювету для образца и в нее добавляли определенное количество стандартного образца (поставляется с анализатором); нажимали «запуск цикла», по очереди выбирали «измерение нагрузки», «ввод информации по образцу», «введение настройки анализа», «запуск анализа», и, наконец, нажимали «запуск», название стандартного образца вводили во всплывающее диалоговое окно, нажимали «ОК», когда параметр «затемнение» в программном обеспечении составлял от 8% до 12%, таким образом проводили измерение стандартного образца.
Для обеспечения точности и надежности экспериментальных данных, перед каждым измерением следует откалибровать холостой фон и измерить размер стандартного образца.
Закрытый отсек кюветы для образца открывали, и извлекали кювету для образца.
Водный раствор, содержащий стандартный образец в кювете для образца, удаляли, и в кювету для образца 3 раза добавляли деионизированную воду для очистки кюветы для образца.
После очистки добавляли 12 мл деионизированной воды, кювету для образца помещали в резервуар для образца, и дверцу отсека закрывали.
Нажимали «запуск цикла», по очереди выбирали «измерение смещения», «выравнивание», «измерение фона», и, наконец, нажимали «пуск», нажимали «ОК» во всплывающем диалоговом окне для начала калибровки холостого фона.
Кювету для образца извлекали, в нее добавляли определенный объем тестируемого образца, дверцу отсека для тестируемого образца открывали, кювету для образца помещали в резервуар для образца и дверцу отсека закрывали.
Нажимали «запуск цикла», по очереди выбирали «ввод информации по образцу», «введение настройки анализа», «запуск анализа», и, наконец, нажимали «запуск», название стандартного образца вводили во всплывающее диалоговое окно, нажимали «ОК», когда параметр «затемнение» в программном обеспечении составлял от 8% до 12%, таким образом проводили регистрацию показателей измерения размера частиц образцов.
Результаты эксперимента:
Размер частиц адъювантов на основе золедроната цинка составлял от 0,4 до 30 мкм, и размер большинства частиц составлял от 6 до 7 мкм.
pH/размер частиц нескольких партий адъюванта Zn-золедроновая кислота (1/0,25)
(1/0,25)
(4) Определение степени адсорбции
Построение стандартной кривой для стандарта BSA: 150 мМ NaCl использовали в качестве буфера для разведения, готовили серийные разведения стандарта BSA (2 мг/мл) и определяли оптическую плотность при 280 нм с использованием спектрофотометра UV2100 pro. Значение OD280 показало высокую точность 0,2-0,8 (пределы до 0,2-1,5).
Градиентное разведение BSA (EP): 150 мМ NaCl использовали в качестве буфера для разведения, определенное количество образца BSA взвешивали и разбавляли до градиента концентрации, указанного в EP: 0,5 мг/мл, 1 мг/мл, 2 мг/мл, 3 мг/мл, 5 мг/мл, 10 мг/мл, для дальнейшего использования.
BSA смешивали с адъювантом при соотношении BSA:адъювант=3:1 (объемное соотношение), что было установлено как условие проведения измерения степени адсорбции; после равномерного встряхивания адъюванта его смешивали с различными концентрациями BSA в соответствии с экспериментальными условиями, и проводили адсорбцию при комнатной температуре в течение 1 ч, и в течение данного периода проводили встряхивание 5 раз; центрифугирование выполняли при 13000 об/мин в течение 3 мин, затем отбирали супернатант для дальнейшего использования.
Определение концентрации белка: для определения концентрации белка в EP использовали метод Лоури. В данном эксперименте, в соответствии с практической ситуацией, UV2100pro использовали для непосредственного определения оптической плотности супернатанта при 280 нм, показания поддерживали в диапазоне 0,2-0,8, в противном случае супернатант необходимо было разбавить.
Расчет степени адсорбции: степень адсорбции=[1 - OD280 (коэффициент разбавления супернатанта X)/OD280 (когда степень адсорбции разведения X равна 0)] × 100
Результаты эксперимента были следующими:
Адсорбционная способность нескольких партий адъюванта Zn-золедроновая кислота (1/0,25) для белка
(5) Определение PZC:
Прибор для измерения: Nanobrook Omni (Brookhaven)
Процедура эксперимента: использовали 0,1 М NaOH/1% HNO3 для доведения pH адъюванта Zn-золедроновая кислота (1/0,125) до: 6,00/ 5,50/5,00/4,50/4,00/3,50/3,00/2,50/2,00.
Пассивирование электрода: в пробирку для образца добавляли 3-4 мл адъюванта. После того, как электрод был вставлен, цикл в SOP устанавливали на 50, и прибор запускали для пассивирования электрода.
Анализ образца: после извлечения электрода его нижний конец ополаскивали деионизированной водой, и затем добавляли соответствующий образец, цикл устанавливали на 15 в SOP, показатель устанавливали на 3, pH был установлен на соответствующий pH каждого образца, и прибор запускали.
Обработка данных: были получены соответствующие дзета-потенциалы при различных значениях pH, программное обеспечение, поставляемое с прибором, было запущено для получения значений PZC.
Результаты: PZC адъюванта Zn-золедроновая кислота (1/0,125) составляла 4,08.
Пример 2: определение степени осаждения цинка в адъюванте Zn-золедроновая кислота (1/0,125)
Пламенную атомно-абсорбционную спектрометрию (коррекция фона лампы D2) использовали для определения содержания цинка в адъювантах на основе золедроната цинка, и процедура определения была стандартизирована. Прибором для проведения анализа был атомно-абсорбционный спектрофотометр: Shimadzu AA6300C (P/N 206-52430).
Приготовление стандартного раствора и образца для определения: построение стандартной кривой: исходная концентрация стандарта цинка составляла 500 мкг/мл, и его разбавляли 0,1 М раствором соляной кислоты с получением стандартов 500 нг/мл, 1000 нг/мл, 1500 нг/мл, 2000 нг/мл и 2500 нг/мл.
Адъювант Zn-золедроновая кислота (1/0,125) центрифугировали при 13000 об/мин в течение 10 мин и супернатант удаляли. Образец разбавляли в 5 раз 0,1 М раствором азотной кислоты для определения, и для встряхивания и перемешивания использовали вихревой смеситель. Процесс определения был следующим:
Принцип работы AA-6300C и использование программного обеспечения WizAArd:
Включение питания: включали компьютер, переключатель питания AA-6300C, переключатель воздушного компрессора (давление 0,35 МПа), переключатель системы вентиляции;
Отверстие для ацетилена: клапан для ацетилена медленно открывали, чтобы убедиться, что первичное давление составляет 0,5 МПа, и вторичное давление равняется 0,1 МПа;
Основная процедура работы программного обеспечения WizAArd: вход в WizAArd → выбрать элемент → на странице «неподключенный прибор/отправка параметра» нажать <подключить/отправить параметр> → установить на странице «инициализация прибора» → проверить и отметить каждый пункт в «каталоге проверки анализа пламени прибора», нажать <OK> → установить длину волны [213,86], ширину щели [0,7], метод освещения [эмиссии], [настройка положения лампы] на странице «оптические параметры» для гарантии того, что фактическое положение и заданное положение лампы с полым катодом для определения ионов Zn идентичны, выбрать [включить лампу] → поиск по строке → регулировка исходного положения горелки → выбрать [параметр] в строке меню → [изменить параметр] → изменить метод освещения на <BGC-D2> → поиск по строке → зажигание: убедившись, что C2H2 включена и давление соответствует требованиям, одновременно нажать кнопки «продувка» и «зажигание» на главном устройстве до тех пор, пока не произойдет зажигание → автоматическое обнуление → установить холостой контроль (BLK), стандартный продукт (STD) и тестируемый образец (UNK) на листе MRT, ввести теоретическую концентрацию стандарта и название образца, и вручную загрузить образец через трубку для образца, выходящую из распылителя, установить объем образца не менее 1 мл каждый раз, выбрать [запуск] для тестирования → остановить пламя → сохранить данные и отключить прибор от компьютера → выключить;
Результаты теста:
Построение стандартной кривой концентрации цинка и Ab
стандарта цинка
(X, нг/мл)
Результаты определения степени осаждения цинка в адъюванте Zn-золедроновая кислота (1/0,125)
Пример 4: определение степени осаждения золедроновой кислоты в адъюванте Zn-золедроновая кислота (1/0,125)
Метод: УФ-спектрофотометрия, прибор: UV800 (Beckman coulter).
Золедроновая кислота содержит имидазольное кольцо и имеет максимум поглощения при 215 нм. Конкретная процедура измерения золедроновой кислоты в супернатанте адъюванта при 215 нм с помощью ультрафиолетового спектрофотометра была следующей:
Сначала готовили стандартные растворы золедроната натрия на физиологическом растворе 0,04 мг/мл, 0,03 мг/мл, 0,02 мг/мл, 0,015 мг/мл, 0,0075 мг/мл, 0,00375 мг/мл, и их значения OD215 измеряли при длине волны 215 нм, и строили стандартную кривую. В то же время центрифугировали адъювант Zn-золедроновая кислота (1/0,125) при 13000 об/мин в течение 10 мин, и затем отбирали супернатант. Поглощение золедроната натрия в супернатанте измеряли при длине волны 215 нм. Результаты были следующими:
Концентрация золедроната натрия и стандартная кривая OD215
стандарта
(x, мг/мл)
Результаты определения степени осаждения золедроновой кислоты в адъюванте Zn-золедроновая кислота (1/0,125)
золедроновой кислоты
в супернатанте (мкг/мл)
золедроновой кислоты
в адъюванте (мкг/мл)
(%)
(1/0,125)
Пример 5: определение адъювантной активности адъюванта Zn-золедронат в рекомбинантной белковой вакцине VZV gE
Приготовленные адъюванты на основе золедроната цинка (также названные как Zn-золедроновая кислота) использовали в качестве адъюванта, в котором соотношение молярных концентраций Zn/ золедроновой кислоты составляло 1:0,25 или 1:1. В качестве адъювантов их использовали в комбинации с антигеном VZV gE, и вместе вводили мышам внутримышечно и определяли титры специфических антител. Конкретный метод был следующим:
Экспериментальные животные: мыши Balb/C, 6-8 недель, 5 мышей/группу, самки.
Концентрация препарата: антиген: 50 мкг/мл.
Доза: 5 мкг/50 мкл/мышь; алюминиевый адъювант: 50 мкл/мышь; адъювант золедронат цинка: 50 мкл/мышь.
Экспериментальные группы: (1) основная группа с алюминиевым адъювантом (Al-002); (2) Zn-золедроновая кислота (1/0,25); (3) Zn-золедроновая кислота (1/1).
Протокол иммунизации: через 2 недели после первой иммунизации животных в соответствии с распределением на группы по вариантам иммунизации, отбирали образцы крови из глазницы для определения титра антител в сыворотке. Титр антител измеряли на второй неделе после первой иммунизации. Буст-иммунизацию проводили на второй неделе. Через 2 недели после буст- иммунизации образцы крови отбирали из глазницы для определения титра антител в сыворотке, и проводили третью иммунизацию. Через 2 недели определяли титр антител в сыворотке с помощью ELISA.
Определение титра связывающих антител с использованием иммуноферментного анализа (ELISA):
1. Раствор для покрытия антигеном: 1X PB буферный раствор 7,4 (4,343 г Na2HPO4 · 7H2O; 0,456 г NaH2PO4).
2. Раствор для промывания: PBST, набор для ELISA от компании Beijing Wantai.
3. Блокирующий раствор: 2X ED (разведение фермента): 1X PBS+0,5% казеина+2% желатина+0,1% консерванта (PROCLIN-300), разбавленный до 1X ультрачистой водой или дистиллированной водой для герметизации и разбавления образца.
4. Раствор для проявления окрашивания A: набор для ELISA от компании Beijing Wantai.
5. Раствор B для проявления окрашивания: набор для ELISA от компании Beijing Wantai.
6. Стоп-раствор: набор для ELISA от компании Beijing Wantai.
Порядок проведения эксперимента:
(1) Покрытие планшета: антиген VZV gE разбавляли буферным раствором для покрытия PB7.4 до определенной концентрации, обычно 100 нг/лунку, добавляли в 96-луночный полистироловый планшет из расчета 100 мкл/лунку, и планшет покрывали в течение ночи при 4°С.
(2) Блокирование: раствор для покрытия в лунке удаляли, планшет один раз промывали раствором для промывания PBST, сушили центрифугированием, добавляли блокирующий раствор по 200 мкл/ лунку и блокирование проводили в течение 4 ч при комнатной температуре.
(3) Добавление сыворотки с определенной степенью разбавления: блокирующий раствор в лунке удаляли, планшет промывали один раз PBST, центрифугировали, в первую лунку добавляли сыворотку, предназначенную для тестирования, в количестве 150 мкл/лунку, в каждую из следующих лунок добавляли разбавитель ED из расчета 100 мкл/лунку, разбавляли с градиентом в 3 раза, инкубировали и проводили реакцию при 25°C в течение 1 ч.
(4) Добавление меченного ферментом антитела (GAM-HRP): разбавитель сыворотки в лунке удаляли, планшет промывали 5 раз PBST, высушивали центрифугированием, добавляли меченное ферментом антитело (GAM-HRP, V:V=1:5000) из расчета 100 мкл/лунку, инкубировали и проводили реакцию при 25°C в течение 1 ч.
(5) Развитие окрашивания: вторичные антитела в лунке удаляли, планшет промывали 5 раз PBST, сушивали центрифугированием, добавляли 100 мкл/лунку раствора для проявления окрашивания, смешанный раствор A и B в равных объемах, и проводили реакцию при 25°C в течение 10 мин.
(6) Остановка реакции: добавляли 2 М стоп-раствор, содержащий серную кислоту, из расчета 50 мкл/лунку для остановки реакции.
(7) Считывание планшета: две длины волны 450 нм и 630 нм были установлены в качестве длин волн для измерения на микропланшетном ридере, и было определено значение OD каждой реакционной лунки.
Результаты эксперимента приведены на фиг. 3:
Адъювант смешивали с антигеном в равном объеме для иммунизации мышей. Иммунизация, забор крови и определение титра сывороточных антител проводили в соответствии с вышеописанной стратегией. В группе с адъювантом золедронатом цинка у мышей наблюдали быстрое и выраженное начало проявления эффекта уже после одной иммунизирующей инъекции; после двух иммунизирующих инъекций преимущество усиления гуморального иммунитета показало статистически значимое различие по сравнению с группой, получавшей алюминиевый адъювант, и разница все еще оставалась значимой после трех иммунизирующих инъекций.
Пример 6: влияние адъюванта золедроната цинка в комбинации с рекомбинантным белком VZV gE на изотипы мышиных антител
Стратегия иммунизации описана в примере 5.
Экспериментальные материалы:
1. Раствор для покрытия антигеном: 1X PB буферный раствор 7,4 (4,343 г Na2HPO4 • 7H2O; 0,456 г NaH2PO4).
2. Раствор для промывания: PBST, набор для ELISA от компании Beijing Wantai.
3. Блокирующий раствор: 2X ED (разведение фермента): 1X PBS+0,5% казеина+2% желатина+0,1% консерванта (PROCLIN-300), разбавленный до 1X ультрачистой водой или дистиллированной водой для герметизации и разбавления образца.
4. Раствор для проявления окрашивания A: набор для ELISA от компании Beijing Wantai.
5. Раствор B для проявления окрашивания: набор для ELISA от компании Beijing Wantai.
6. Стоп-раствор: набор для ELISA от компании Beijing Wantai.
Порядок проведения эксперимента:
(1) Покрытие планшета: антиген VZV gE разбавляли буферным раствором для покрытия PB7.4 до определенной концентрации, добавляли в 96-луночный полистироловый планшет из расчета 100 мкл/лунку, и планшет покрывали в течение ночи при 4°C.
(2) Блокирование: раствор для покрытия в лунке удаляли, планшет один раз промывали PBST, сушили центрифугированием, добавляли блокирующий раствор из расчета 200 мкл/лунку и блокирование проводили в течение 4 ч при комнатной температуре.
(3) Добавление сыворотки для тестирования: сыворотка, используемая для определения изотипа антител в сыворотке: через 2 недели после завершения 3 иммунизирующих инъекций, т. е. сыворотка, полученная на неделе 6; блокирующий раствор в лунке удаляли, планшет один раз промывали PBST, сушили центрифугированием, добавляли тестируемую сыворотку с определенной степенью разбавления из расчета 100 мкл/лунку, инкубировали и проводили реакцию в течение 1 ч при 25°C.
(4) Добавление меченного ферментом антитела: разбавитель сыворотки в лунке удаляли, планшет промывали 5 раз PBST, сушили центрифугированием, добавляли меченное ферментом антитело, которое специфически распознает каждый изотип антитела (IgG1, V:V=1:30000; IgG2a, V:V=1:1000; IgG2b, V:V=1:1000) по 100 мкл/лунку, инкубировали и реакцию проводили при 25°C в течение 1 ч.
(5) Развитие окрашивания: меченное ферментом антитело, удаляли из лунки, планшет промывали 5 раз PBST, сушили центрифугированием, добавляли раствор для проявления окрашивания, смешанный раствор A и B в равных объемах, разбавляли в 3 раза, вносили в лунку из расчета 100 мкл/лунку, реакцию проводили при 25°C в течение 10 мин.
(6) Остановка реакции: для остановки реакции добавляли 50 мкл/лунку 2 М стоп-раствора, содержащего серную кислоту.
(7) Считывание планшета: две длины волны 450 нм и 630 нм были установлены в качестве длин волн для измерения на микропланшетном ридере, и было измерено значение OD каждой реакционной лунки.
Результаты эксперимента приведены на фиг. 4:
Использовали экспериментальную процедуру, описанную в примере 5. Мышей иммунизировали адъювантом золедронатом цинка или алюминиевым адъювантом в комбинации с рекомбинантным белком gE VZV внутримышечной инъекцией. Процедура иммунизации была аналогичной описанной в примере 5. После 3 иммунизирующих инъекций образцы крови собирали через 2 недели, и результаты определения уровней каждого изотипа антител в сыворотке мышей показаны на фиг. 4. По сравнению с группой с алюминиевым адъювантом, в группе с введением адъюванта золедроната цинка наблюдали стимуляцию более высоких уровней изотипов антител IgG2a и IgG2b, и соотношение IgG1 к IgG2a и IgG2b было ниже, чем в группе с алюминиевым адъювантом, указывая на то, что он оказывает определенный стимулирующий эффект на иммунный путь, опосредованный Th1.
Пример 7: определение адъювантной активности адъюванта золедроната цинка в комбинации с терапевтическим белком против вируса гепатита В
Использовали экспериментальную процедуру, описанную в примере 5. Мышей иммунизировали адъювантом на основе золедроната цинка в комбинации с терапевтическим белком против вируса гепатита В внутримышечной инъекцией и определяли титры сывороточных антител. Результаты приведены на фиг. 5: по сравнению с группой, получавшей алюминиевый адъювант, группа с адъювантом золедронатом цинка показала быстрое начало и сильный иммунный ответ после уже одной иммунизирующей инъекции у мышей, и разница была статистически значимой; после 2 иммунизирующих инъекций преимущество в усилении гуморального иммунитета все еще было достоверным по сравнению с группой с алюминиевым адъювантом и было несколько лучше, чем в группе с алюминиевым адъювантом после 3 иммунизирующих инъекций.
Пример 8: влияние других адъювантов на основе бисфосфоната цинка в комбинации с VZV gE на титры антител в сыворотке мышей
Использовали экспериментальную процедуру, описанную в примере 5. Мышей иммунизировали адъювантом на основе бисфосфоната цинка в комбинации с рекомбинантным белком gE VZV внутримышечной инъекцией и определяли титры сывороточных антител. Результаты приведены на фиг. 6: после 3 иммунизирующих инъекций мышей в группе с адъювантом на основе золедроната цинка имела место достоверная разница в усилении гуморального иммунитета по сравнению с группой с алюминиевым адъювантом, в то время как эффекты других адъювантов на основе бисфосфоната цинка достроверно не различались по сравнению с алюминиевым адъювантом.
Пример 9: влияние адъюванта золедроната цинка в комбинации с VZV gE на титры антител в сыворотке мышей
Использовали экспериментальную процедуру, описанную в примере 5. Мышей иммунизировали адъювантом на основе золедроната цинка в комбинации с VZV gE внутримышечной инъекцией и определяли титры сывороточных антител. Как показано на фиг. 7, алюминиевый адъювант, комбинированный адъювант цинк-алюминий, комбинированный адъювант цинк-алюминий с добавлением золедроновой кислоты, и адъювант на основе золедроната цинка показали постепенно возрастающую тенденцию в повышении титра антител, и при сравнении наблюдали достоверную разницу между группой, получавшей адъювант на основе золедроната цинка, с группой с алюминиевым адъювантом.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛУЧЕНИЕ МИКРО/НАНОАДЪЮВАНТА НА ОСНОВЕ РИЗЕДРОНАТА ЦИНКА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ ВАКЦИННОГО АДЪЮВАНТА | 2020 |
|
RU2797509C1 |
| АДЪЮВАНТ | 2020 |
|
RU2736933C1 |
| АДЪЮВАНТ НА ОСНОВЕ ПОЛИИНОЗИНОВОЙ КИСЛОТЫ - ПОЛИЦИТИДИЛОВОЙ КИСЛОТЫ | 2005 |
|
RU2383552C2 |
| АДЪЮВАНТЫ НА МАСЛЯНОЙ ОСНОВЕ | 2014 |
|
RU2730011C2 |
| АДЪЮВАНТЫ НА МАСЛЯНОЙ ОСНОВЕ | 2014 |
|
RU2816849C2 |
| НОВЫЕ ВАКЦИННЫЕ СОСТАВЫ, ВКЛЮЧАЮЩИЕ САПОНИНСОДЕРЖАЩИЕ АДЪЮВАНТЫ | 2010 |
|
RU2555342C2 |
| КОМПОЗИЦИИ ВАКЦИН С ДВОЙНЫМ АДЪЮВАНТОМ, ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ | 2015 |
|
RU2729646C2 |
| АДЪЮВАНТЫ НА МАСЛЯНОЙ ОСНОВЕ | 2014 |
|
RU2816851C2 |
| КОМПОЗИЦИЯ АДЪЮВАНТА, СОДЕРЖАЩАЯ ПОЛИ-ГАММА-ГЛУТАМИНОВУЮ КИСЛОТУ | 2005 |
|
RU2390352C2 |
| Способ получения вакцинного адъюванта в виде эмульсии | 2022 |
|
RU2811696C1 |
Настоящее изобретение относится области биотехнологии и может быть применимо в медицинской практике. Изобретение раскрывает вакцинный адъювант на основе микрочастиц золедроната цинка, который содержит цинк и золедроновую кислоту соответсвенно, а также возможные добавки на основе фосфата и алюминия. Способ его получения включает проведение смешанного осаждения в растворе растворимой соли, содержащем ионы цинка, золедроновую кислоту и гидроксид натрия. Изобретение может быть использовано в качестве иммуностимулирующей добавки и адъюванта при получении фармацевтических композиций и составов. 5 н. и 14 з.п. ф-лы, 9 пр., 6 табл., 7 ил.
1. Вакцинный адъювант, содержащий эффективное количество микрочастиц золедроната цинка;
причем указанный вакцинный адъювант имеет соотношение молярных концентраций цинка : золедроновой кислоты 1-8:1.
2. Вакцинный адъювант по п.1, где указанный вакцинный адъювант имеет соотношение молярных концентраций цинка : золедроновой кислоты, выбранное из 1:1, 4:1 и 8:1.
3. Вакцинный адъювант по п.1, отличающийся любым из следующего:
(1) указанный вакцинный адъювант дополнительно содержит фосфат при соотношении молярных концентраций цинка : фосфата 1-8:1; и
(2) указанный вакцинный адъювант дополнительно содержит фосфат при соотношении молярных концентраций цинка : фосфата, выбранном из 1,5:1 и 4:1.
4. Вакцинный адъювант по п.1, отличающийся любым из следующего:
(1) указанный вакцинный адъювант дополнительно содержит алюминий при соотношении молярных концентраций цинка : алюминия 0,02-1:1; и
(2) указанный вакцинный адъювант дополнительно содержит алюминий при соотношении молярных концентраций цинка : алюминия, выбранном из 0,375:1, 0,5:1 и 0,8:1.
5. Вакцинный адъювант по п.1, где вакцинный адъювант получен способом, включающим следующие стадии:
а) получение раствора растворимой соли, содержащего ионы цинка;
b) равномерное смешивание раствора растворимой соли со стадии а) с золедроновой кислотой и гидроксидом натрия; или
равномерное смешивание раствора растворимой соли со стадии а) с золедроновой кислотой, гидроксидом натрия и раствором фосфата натрия,
методом последовательного осаждения, раздельного осаждения с последующим перемешиванием или соосаждением с получением вакцинного адъюванта.
6. Вакцинный адъювант по п.5, отличающийся одним или более из следующего:
(1) указанный раствор соли содержит раствор соляной кислоты; и
(2) указанный способ дополнительно включает стерилизацию смеси со стадии b) и хранение при 2-8°C для последующего использования.
7. Вакцинный адъювант по п.6, отличающийся любым из следующего:
(1) указанная стерилизация включает стерилизацию с использованием метода стерилизации при высокой температуре и высоком давлении; и
(2) указанная стерилизация включает стерилизацию, выполняемую при 121°C в течение 30-60 мин.
8. Вакцинный адъювант по п.1, отличающийся одним или более из следующего:
(1) указанный вакцинный адъювант имеет pH 8,0-9,0 до стерилизации;
(2) указанный вакцинный адъювант имеет pH 6,0-8,0 после стерилизации;
(3) указанный вакцинный адъювант имеет размер частиц 1-10 мкм;
(4) указанный вакцинный адъювант имеет точку нулевого заряда частицы 4,0-11,4; и
(5) указанный вакцинный адъювант имеет степень адсорбции белка >80%.
9. Вакцинный адъювант по п.8, где указанный белок представляет собой бычий сывороточный альбумин.
10. Способ получения вакцинного адъюванта, включающий:
а) получение раствора растворимой соли, содержащего ионы цинка;
b) равномерное смешивание раствора растворимой соли со стадии а) с золедроновой кислотой и гидроксидом натрия; или
равномерное смешивание раствора растворимой соли со стадии а) с золедроновой кислотой, гидроксидом натрия и раствором фосфата натрия,
методом последовательного осаждения, раздельного осаждения с последующим перемешиванием или соосаждением с получением вакцинного адъюванта,
где полученный вакцинный адъювант имеет соотношение молярных концентраций цинка : золедроновой кислоты 1-8:1.
11. Способ по п.10, где полученный вакцинный адъювант имеет соотношение молярных концентраций цинка: золедроновой кислоты, выбранное из 1:1, 4:1 и 8:1.
12. Способ по п.10, отличающийся одним или более из следующего:
(1) указанный раствор соли содержит раствор соляной кислоты; и
(2) указанный способ дополнительно включает стерилизацию смеси со стадии b) и хранение при 2-8°C для последующего использования.
13. Способ по п.12, отличающийся одним или более из следующего:
(1) указанная стерилизация включает стерилизацию с использованием метода стерилизации при высокой температуре и высоком давлении; и
(2) указанная стерилизация включает стерилизацию, выполняемую при 121°C в течение 30-60 мин.
14. Способ по п.10, отличающийся одним или более из следующего:
(1) полученный вакцинный адъювант имеет pH 8,0-9,0 до стерилизации;
(2) полученный вакцинный адъювант имеет pH 6,0-8,0 после стерилизации;
(3) полученный вакцинный адъювант размер частиц 1-10 мкм;
(4) полученный вакцинный адъювант имеет точку нулевого заряда частицы 4,0-11,4; и
(5) полученный вакцинный адъювант имеет степень адсорбции белка >80%.
15. Способ по п.14, где белок включает бычий сывороточный альбумин.
16. Вакцинная композиция, содержащая эффективное количество антигена и вакцинного адъюванта по любому из пп. 1-9, отличающаяся одним или более из следующего:
(1) указанный антиген включает белковый антиген; и
(2) указанный антиген включает гликопротеиновый антиген gE вируса ветряной оспы и опоясывающего лишая.
17. Применение вакцинного адъюванта по любому из пп. 1-9 в качестве иммуностимулирующей добавки в получении иммуногенной композиции.
18. Применение вакцинного адъюванта по любому из пп. 1-9 в качестве иммуностимулирующей добавки в получении вакцинной композиции.
19. Применение по п.18, отличающееся одним или более из следующего:
(1) указанная вакцина является белковой вакциной; и
(2) указанная вакцина представляет собой рекомбинантную белковую вакцину против вируса ветряной оспы и опоясывающего лишая.
| US 8722030 B2, 13.05.2014 | |||
| RU 2008111967 A1, 10.10.2009 | |||
| WO 2016035808 A1, 10.03.2016 | |||
| WO 2016156398 A1, 06.10.2016 | |||
| WO 2016035809 A1, 10.03.2016 | |||
| CN 103768595 A, 07.05.2014 | |||
| GOUIN F | |||
| et al.: "Adjuvant treatment with zoledronic acid after extensive curettage for giant cell tumours of bone", European Journal of Cancer, 2014, v | |||
| Устройство для выпрямления многофазного тока | 1923 |
|
SU50A1 |
Авторы
Даты
2023-08-11—Публикация
2020-04-10—Подача