Востребованность остеотропных материалов в современном мире растет с каждым годом. По данным НИИ Ревматологии РАМН в настоящее время около 2 млн пациентов нуждаются в операциях по замещению костной ткани. Травмы, хирургические вмешательства при опухолевых и воспалительных процессах требуют от врачей поиска новых подходов к замещению дефектов костной ткани или оптимизации процессов остеогенеза, в том числе с использованием специальных материалов. Актуальность разработки данного способа моделирования посттравматического дефекта обусловлена большой частотой встречаемости посттравматических компрессионных дефектов костной ткани, так же данный метод можно использования для изучения процессов остеоинтеграции и репаративного остеогенеза, так как воссоздаются условия, максимально приближенные к условиям формирования кости в зоне травматизации.
Существует способ моделирования переломов губчатой ткани для изучения остеоинтеграции и регенерации костной ткани (номер патента G09B 23\28 «Способ моделирования дефекта костной ткани для изучения остеоинтеграции костнопластического материала и регенерации губчатой костной ткани в эксперименте на кроликах» патентообладатель Федеральное государственное бюджетное образовательное учреждение высшего образования «Приволжский исследовательский медицинский университет» Министерства здравоохранения Российской Федерации. Заявка 20211109643, заявл. 07.04.2021, опубл. – 29.10.2021, Бюл. №31), при котором создавалась модель для изучения процессов остеоинтеграции костнопластических материалов и регенерации костной ткани путем формирования остеотомом краевого прямоугольного дефекта 7×5×4мм в ростральной половине гребня подвздошной кости, без резекции внутреннего кортикального слоя и с последующим имплантированием в сформированную зону костнопластического материала. Существенным недостатком данного метода является механическое удаление костных структур при его реализации, что не соответствует патогенетическим механизмам развития компрессионных и импрессионных переломов губчатой кости, а следовательно, искажает механизмы последующей репаративной регенерации и препятствует получению достоверной информации об органотипическом замещении полученного дефекта.
Известен «Способ моделирования костного дефекта бедренной кости» (номер патента G09B 23\28 патентообладатель Федеральное государственное учреждение Центральный научно-исследовательский институт травматологии и ортопедии имени Н.Н. Приорова Росмедтехнологий. Заявка 2007122659\14, заявл. 19.06.2007, опубл. 27.01.2009, Бюл. №3). Сущность данного метода заключается в формировании фрезой диафизарного костного дефекта бедренной кости лабораторного животного длиной 0,5-0,7 см путем резекции ¾ её диаметра. Авторы утверждают, что данный метод позволяет оценить формирование костной ткани при сращении диафизарных оскольчатых переломов длинных трубчатых костей, в том числе с использованием различных вариантов костной пластики. Недостатками данного метода являются отсутствие остеокластического компонента при моделировании дефекта и перелома, а также невозможности получения идентичного по размерам дефекта костной ткани у лабораторных животных.
Известен способ моделирования костного дефекта бедренной кости (патент RU2345423C1), заключающийся в формировании фрезерного дефекта диаметром 2 мм и глубиной 3 мм в бедренной кости крысы, в который впоследствии имплантировался остеопластический материал. Недостатками данного способа моделирования является небольшой объем экспериментального дефекта, затрудняющий установку в него достаточного количества остеопластического материала, высокую вероятность самопроизвольного органотипического замещения, что препятствует объективному изучению процессов репаративного остеогенеза. Так же необходимо отметить, что данный способ формирования дефекта патогенетически не схож с механизмом получения перелома, так как дефект формируется путем механического воздействия внешним устройством (Матвеев А.Г. Обеспечение радикальности с использованием новых вариантов костной пластики при лечении доброкачественных опухолей. Диссертация на соискание канд. мед. наук. Москва, 2000 г., с.125).
Наиболее близким к предлагаемому является способ моделирования внутрисуставного импрессионного перелома проксимального отдела большеберцовой кости, взятый за прототип (Патент А61В 17\00008 «Способ моделирования внутрисуставного импрессионного перелома проксимального отдела большеберцовой кости» Патентообладатель Федеральное государственное бюджетное образовательное учреждение высшего образования «Уральский государственный медицинский университет» Министерства здравоохранения Российской Федерации. Заявка 2017136912, заявл. 19.10.2017, опубл. 05.10.2018, бюл. №28). Способ позволяет моделировать внутрисуставной мыщелковый перелом с дисконгруэнтностью суставных поверхностей. При моделировании дефекта после осуществления доступа к проксимальному отделу большеберцовой кости и формирования четырехстороннего распила выполняется извлечение выпиленного фрагмента, после осуществляют надлом и смещение части мыщелка в дистальном направлении, что позволяется создать импресионный внутрисуставной перелом. Однако данный способ не позволяет создать стандартизированный полостной дефект костной ткани. Кроме того, этот метод является весьма травматичным, так как происходит разрушение не только костных, но и хрящевых структур коленного сустава, что приводит к продолжительному нарушению двигательной функции в данном сегменте опорно-двигательного аппарата.
Для создания модели посттравматического полостного метаэпифизарного костного дефекта максимально повторяющего патофизиологические механизмы его получения выполняется послойный доступ к дистальному метаэпифизарному отделу бедренной кости с латеральной стороны. После обнажения кости при помощи фрезы (диаметр – 20мм, толщина 1мм) производится распил кортикальной пластины прямоугольной формы с размерами сторон 10мм и 5мм, длина и ширина соответственно. Далее выполняется смещение кортикальной пластинки на глубину 8мм, в результате чего формируется компрессионный перелом подлежащей метаэпифизарной губчатой кости, затем при помощи элеватора «вдавленный» фрагмент поднимается и фиксируется к материнской кости в исходном положении. В результате образуется посттравматический отграниченный от окружающих мягких тканей костный дефект стандартного размера и формы, объем которого составляет 400мм3.
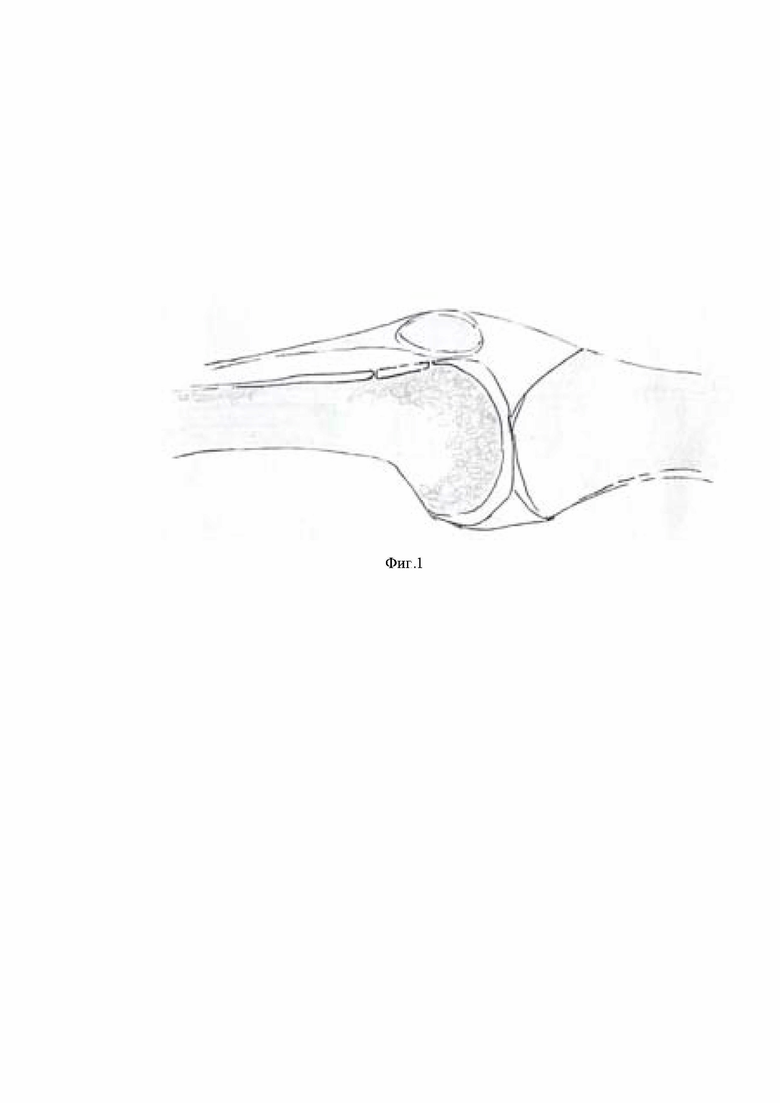
Изобретение поясняется рисунками, на которых поэтапно отражено формирование отграниченного метаэпифизарного дефекта костной ткани, полученного в результате компрессионного перелома.
На Фиг. 1 – выпиленный участок костной ткани (размер 10×5 мм).
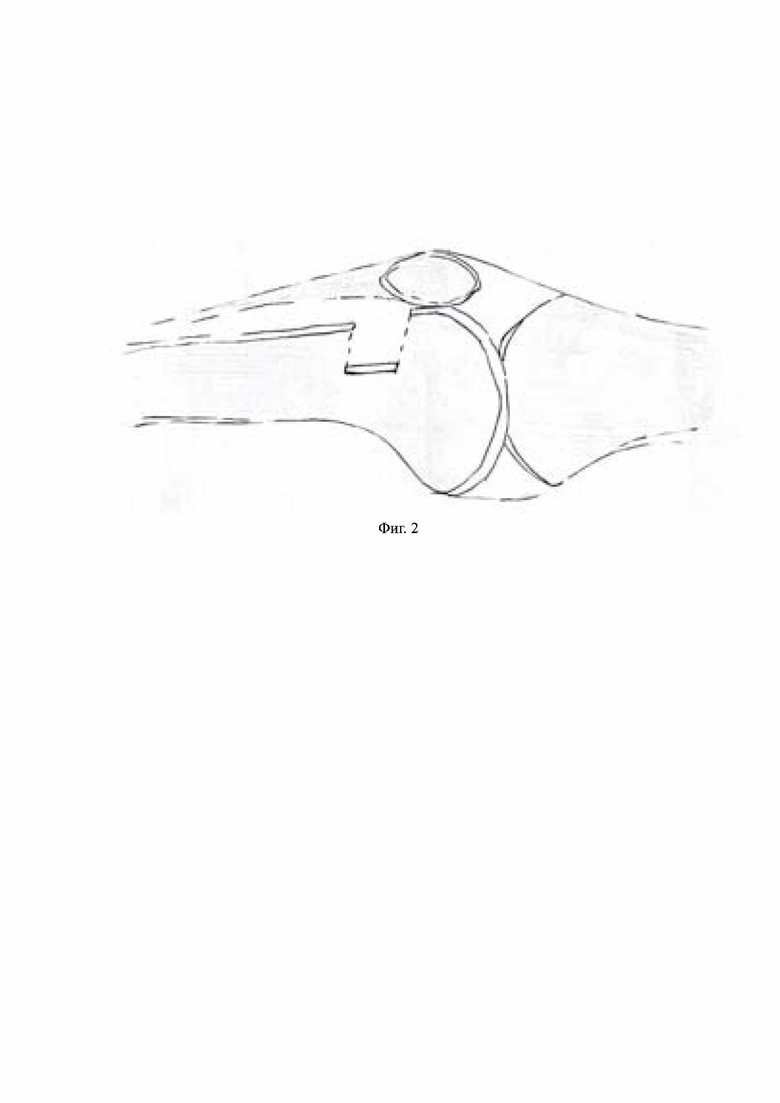
На Фиг. 2 – смещение кортикальной пластинки (на глубину 8 мм).
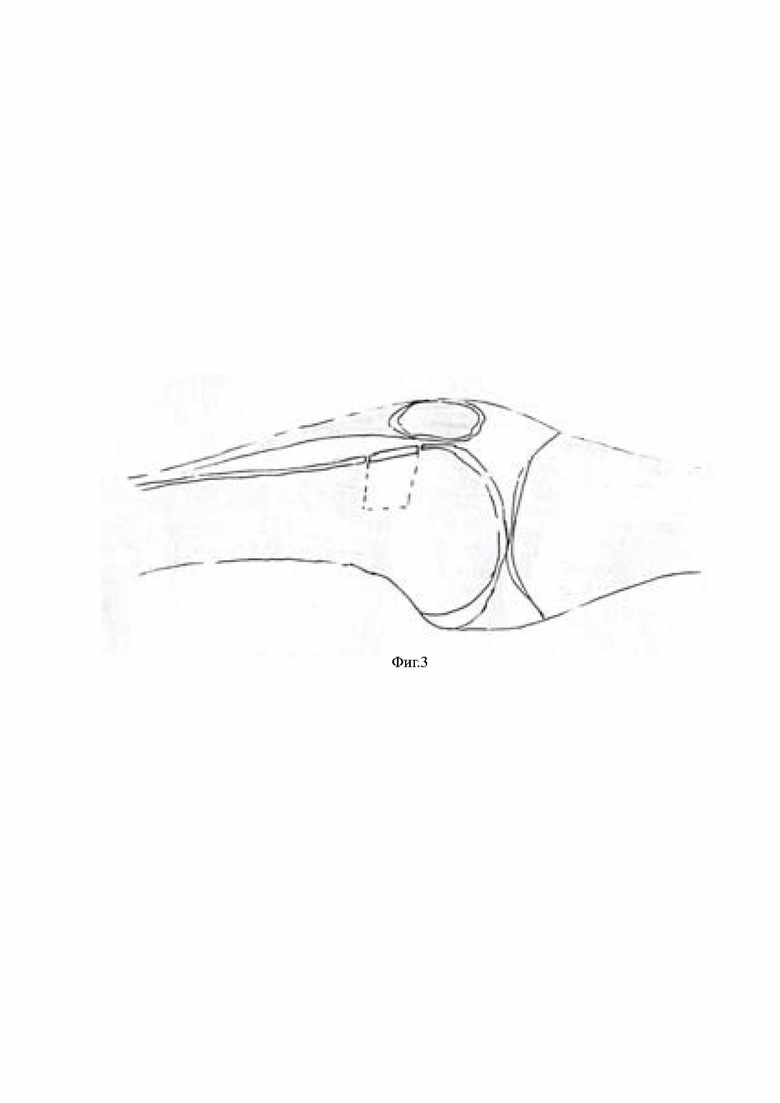
На Фиг. 3 – сформированная зона компрессии губчатой ткани.
Способ моделирования посттравматического компрессионного костного дефекта иллюстрируется следующим клиническим примером.
В качестве клинического примера выполнялось моделирование посттравматического костного дефекта у экспериментальных животных (кроликов) в количестве 36 штук. Эксперимент проводили с соблюдением принципов гуманности, которые изложены в директивах Европейского сообщества (86/609//ЕЕС) и Хельсинской декларации. Также авторами было получено разрешение на проведение экспериментального исследования этического комитета ОмГМУ № 128 от 03.02.2021 г. В условиях операционной в положении животного на спине с фиксированными конечностями под в\м седацией раствором золетила после 3-х кратной обработки операционного поле раствором антисептика, выполнялась гидропрепаровка мягких тканей Sol. Novocaini 0,25%-3,0. После рассечения кожных покровов и подлежащих тканей производился доступ к дистальному метаэпифизу правой бедренной кости. Сухожилие 4-х главой мышцы бедра и надколенник отводились в медиальную сторону. При помощи дисковой фрезы формировался прямоугольный выпил кортикальной пластины в зоне метафиэпифизаза бедренной кости размерами 10 мм на 5 мм. Далее кортикальная пластина «внедрялась» в метаэпифизарную кость на глубину 8 мм, после чего при помощи элеватора выполнялся её подъем и последующая фиксация к материнской кости. Зона вмешательства прикрывалась сухожилием 4-х главой мышцы бедра, рана послойно ушивалась. Накладывалась асептическая повязка, внешней иммобилизации не проводилась. Для выполнения стандартизированного дефекта было выбрано 36 кроликов породы «белый великан», массой 3700-4000 г. Продолжительность операции составила 10 минут, кровопотеря в пределах 2-3 мм. Стоит отметить, что в послеоперационном периоде у всех животных двигательная активность восстановилась через 2 суток. Переломов бедренной кости, контрактур и инфекционных осложнений не было зафиксировано ни у одного из животных.
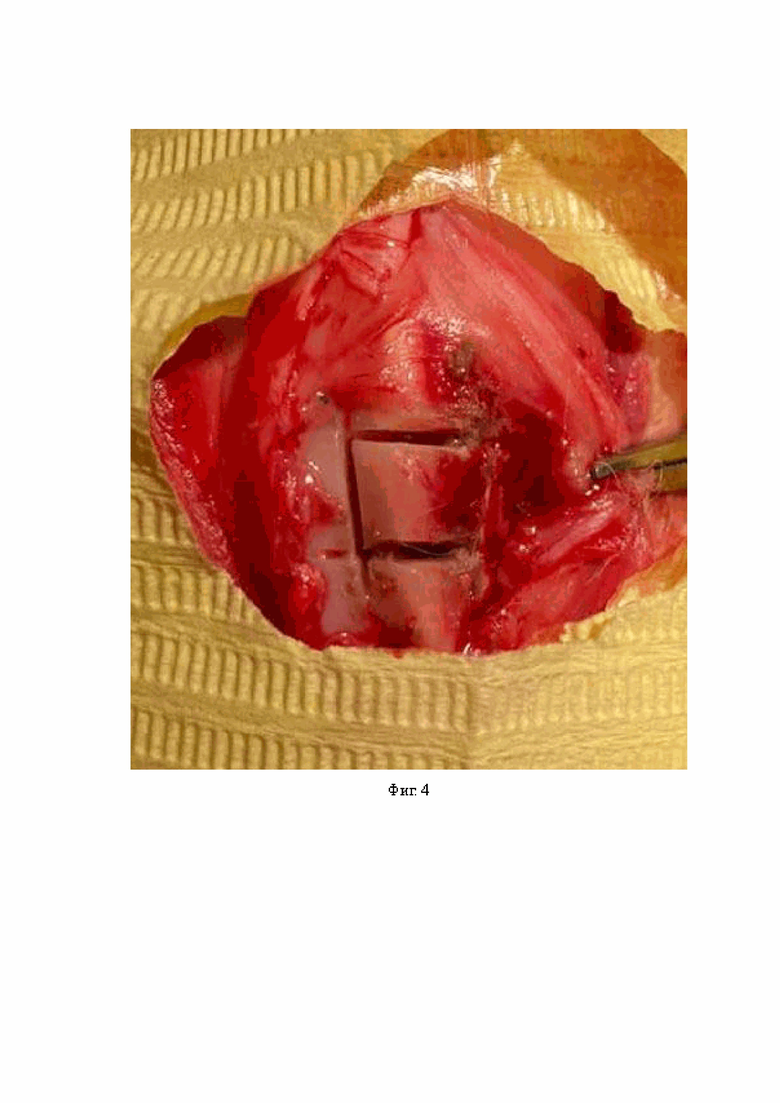
На Фиг. 4 – выпиленный участок костной ткани (размер 10×5 мм).
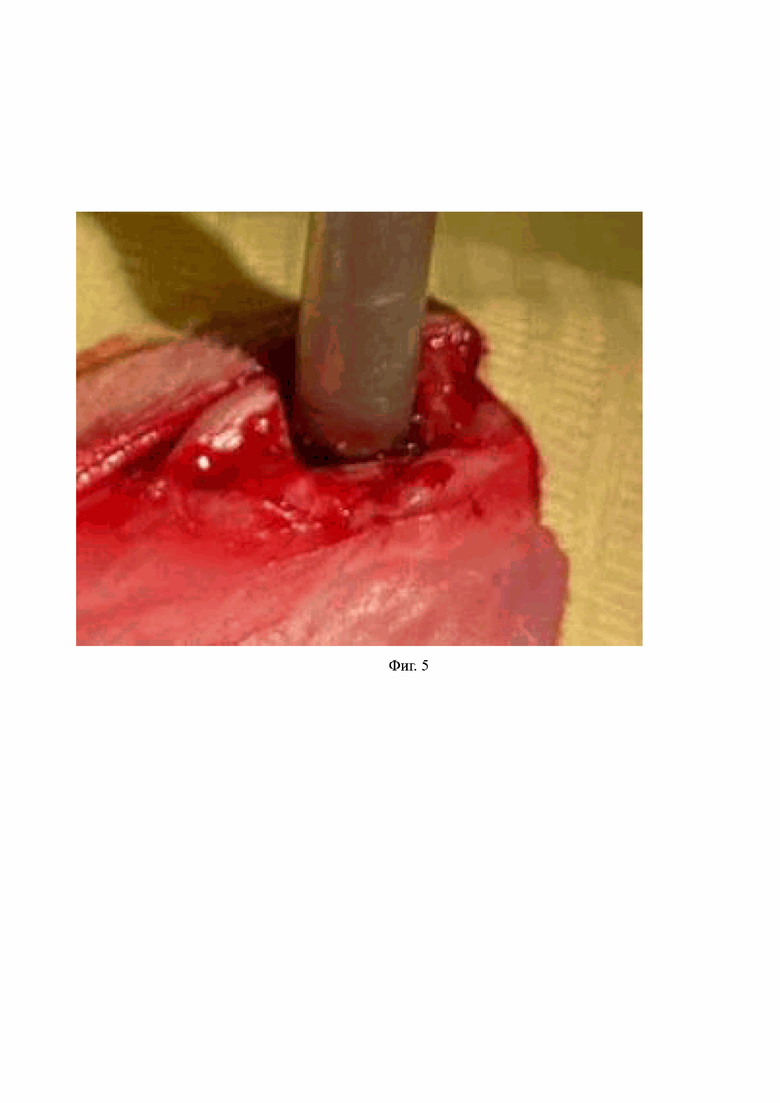
На Фиг. 5 – смещение кортикальной пластинки (глубина смещения 8 мм).
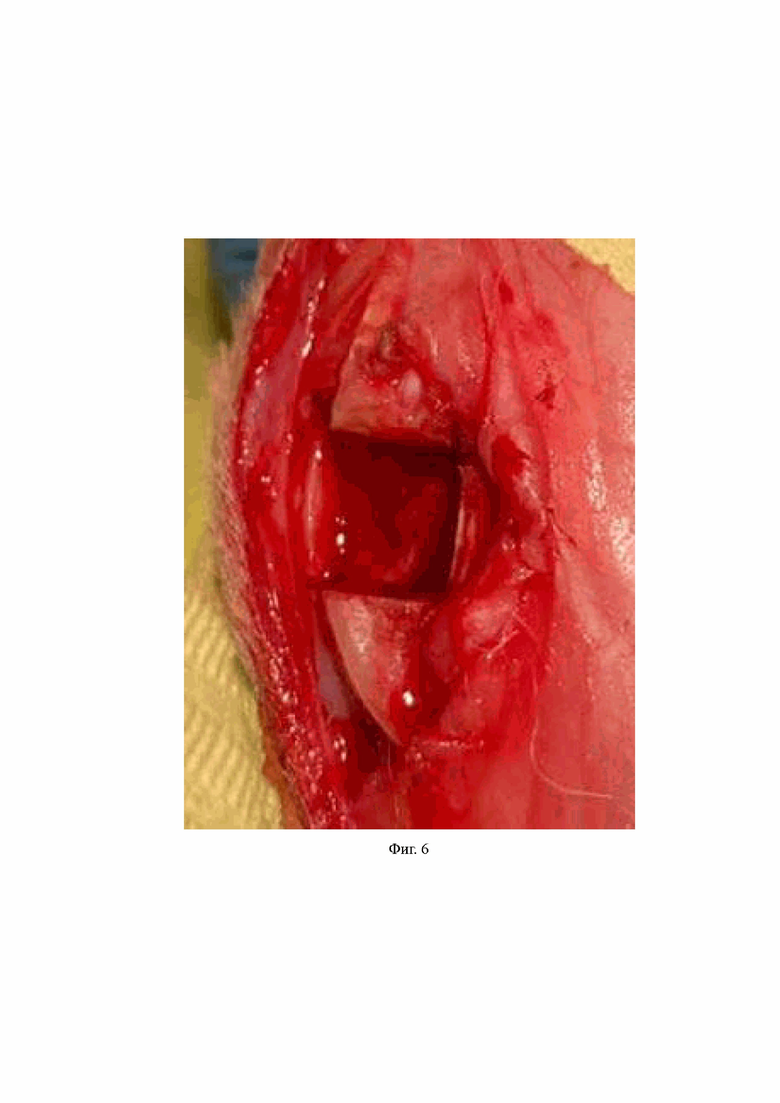
На Фиг. 6 – сформированная зона компрессии губчатой ткани.
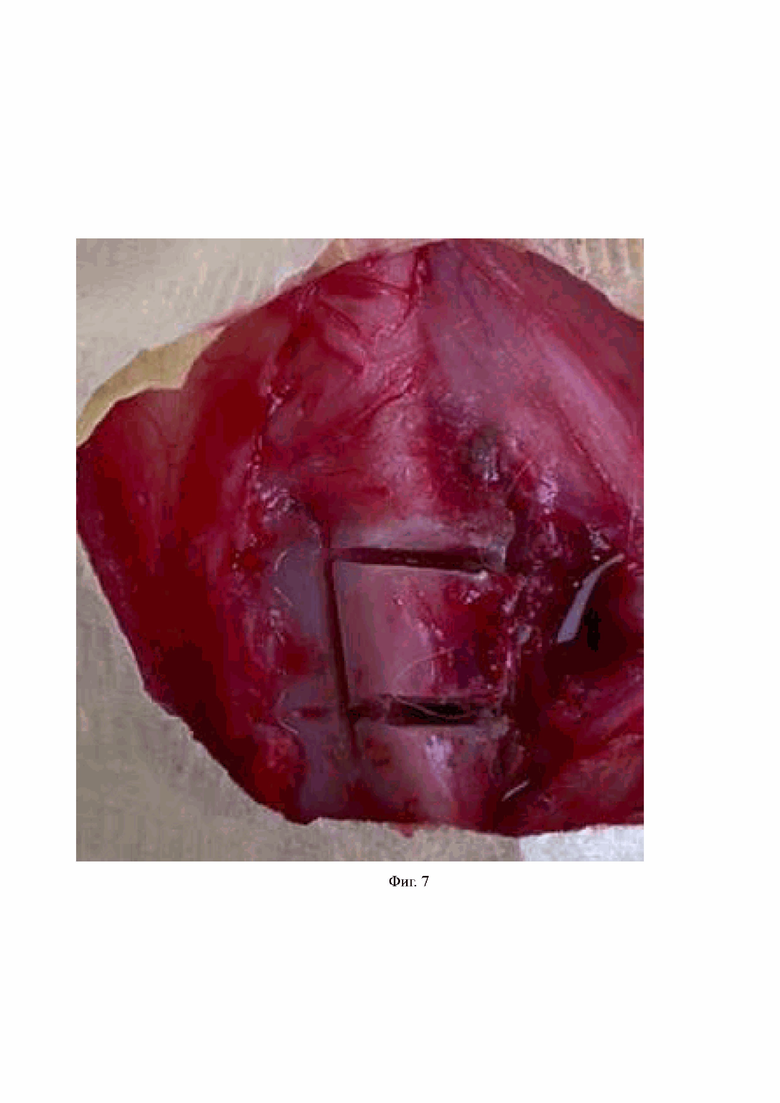
На Фиг. 7 – вид раны после элевации и фиксации кортикальной пластинки.
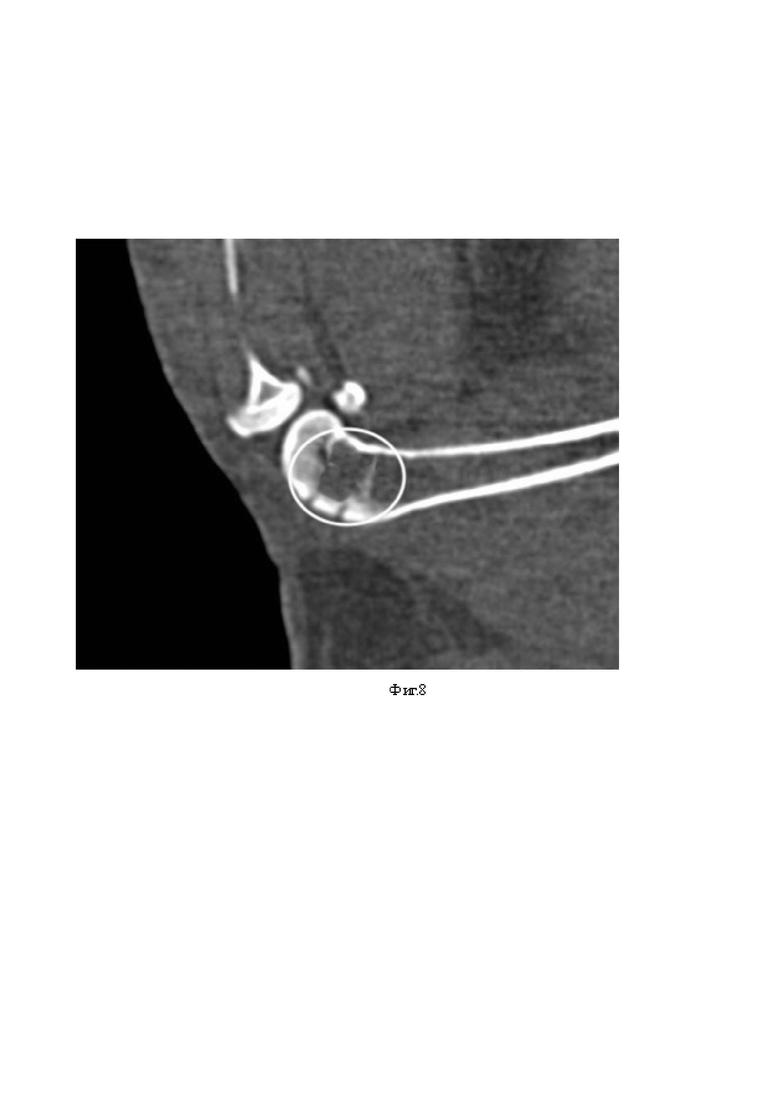
В ходе эксперимента для объективизации формирования метаэпифизарного костного дефекта выполнялось МСКТ исследование, подтверждающее локализацию, размеры посттравматического дефекта и восстановление остеотомированной кортикальной пластины (Фиг. 5).
Фиг. 8 - МСКТ снимок в сагиттальной проекции. На снимке выделена сформированная зона дефекта костной ткани.
Таким образом, данное изобретение позволяет полностью повторить патофизиологические механизмы получения отграниченных компрессионных метаэпифизарных костных дефектов у экспериментальных животных, стандартизировать их форму и размеры, исключить проникновение соединительнотканных элементов из окружающих мягких тканей, что в дальнейшем обеспечивает условия для детального исследования процессов репаративной регенерации костной ткани, а также остеоинтеграции при замещении дефекта остеоиндуктивными и остеокондуктивными материалами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ ВНУТРИСУСТАВНОГО ИМПРЕССИОННОГО ПЕРЕЛОМА ПРОКСИМАЛЬНОГО ОТДЕЛА БОЛЬШЕБЕРЦОВОЙ КОСТИ | 2017 |
|
RU2669047C1 |
| СПОСОБ ЛЕЧЕНИЯ ИМПРЕССИОННОГО ПЕРЕЛОМА МЕТАЭПИФИЗАРНОГО ОТДЕЛА ТРУБЧАТОЙ КОСТИ | 2010 |
|
RU2444319C1 |
| Способ моделирования костного дефекта на локтевом отростке овец для исследования регенераторного потенциала остеопластических материалов | 2024 |
|
RU2830364C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ВНУТРИСУСТАВНЫХ ПЕРЕЛОМОВ ДИСТАЛЬНОГО ОТДЕЛА ЛУЧЕВОЙ КОСТИ С ДЕФЕКТОМ МЕТАЭПИФИЗАРНОЙ ЗОНЫ | 2011 |
|
RU2453288C1 |
| Способ пластики посттравматических околосуставных дефектов длинных трубчатых костей (варианты) | 2022 |
|
RU2798904C1 |
| Способ моделирования дефекта костной ткани для изучения остеоинтеграции костнопластического материала и регенерации губчатой костной ткани в эксперименте на кроликах | 2021 |
|
RU2758556C1 |
| РЕГЕНЕРАТИВНЫЙ СПОСОБ ЛЕЧЕНИЯ ИМПРЕССИОННОГО ПЕРЕЛОМА ПРОКСИМАЛЬНОГО МЕТАЭПИФИЗА БОЛЬШЕБЕРЦОВОЙ КОСТИ | 2020 |
|
RU2743267C1 |
| Способ лечения импрессионных переломов мыщелоков большеберцовой кости | 2021 |
|
RU2777687C1 |
| Способ оперативного лечения импрессионной деформации и перелома заднего отдела наружного мыщелка большеберцовой кости | 2024 |
|
RU2830403C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ВНУТРИСУСТАВНОГО КОМПРЕССИОННОГО ПЕРЕЛОМА ПЯТОЧНОЙ КОСТИ И СКОБА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2012 |
|
RU2535451C2 |
Изобретение относится к медицине, а именно к экспериментальной травматологии и ортопедии и может быть использовано для моделирования посттравматического компрессионного костного дефекта. По передне-наружной поверхности дистального метаэпифиза бедренной кости кролика дисковой фрезой производят распил кортикальной пластины прямоугольной формы с размерами сторон 10 мм и 5 мм. Путем одномоментного смещения полученного костного фрагмента на глубину 8 мм создают зону компрессии подлежащей губчатой костной ткани. Кортикальный фрагмент поднимают, укладывают и фиксируют в исходном положении с формированием метаэпифизарного костного дефекта объемом 400 мм3. Способ обеспечивает полное повторение патофизиологических механизмов получения отграниченных компрессионных метаэпифизарных костных дефектов у экспериментальных животных, позволяет стандартизировать их форму и размеры и исключить проникновение соединительнотканных элементов из окружающих мягких тканей за счет формирования выпила кортикальной пластинки, компрессии подлежащей кости и ее элевации и фиксации к материнской кости. 8 ил., 1 пр.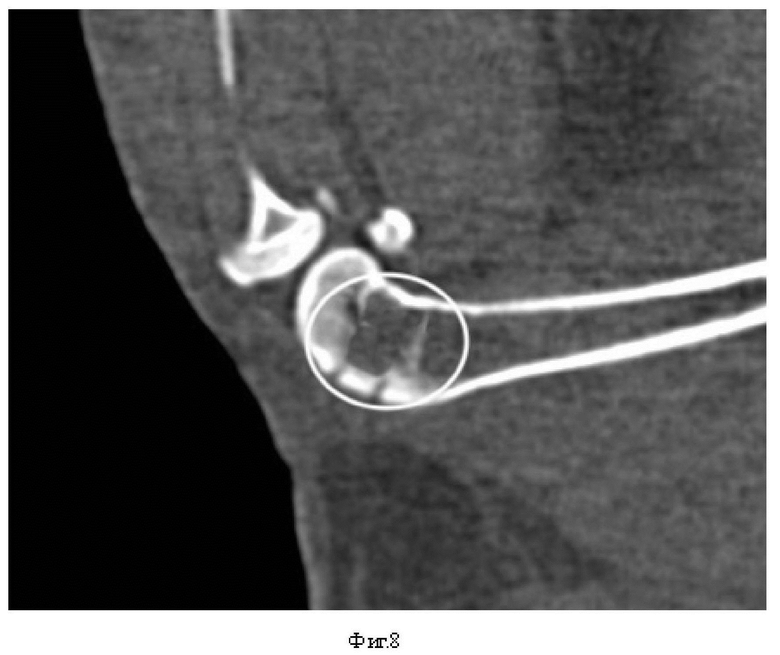
Способ моделирования посттравматического компрессионного костного дефекта, заключающийся в том, что по передне-наружной поверхности дистального метаэпифиза бедренной кости кролика дисковой фрезой производят распил кортикальной пластины прямоугольной формы с размерами сторон 10 мм и 5 мм, после чего путем одномоментного смещения полученного костного фрагмента на глубину 8 мм создают зону компрессии подлежащей губчатой костной ткани, далее кортикальный фрагмент поднимают, укладывают и фиксируют в исходном положении с формированием метаэпифизарного костного дефекта объемом 400 мм3.
| СПОСОБ МОДЕЛИРОВАНИЯ ВНУТРИСУСТАВНОГО ИМПРЕССИОННОГО ПЕРЕЛОМА ПРОКСИМАЛЬНОГО ОТДЕЛА БОЛЬШЕБЕРЦОВОЙ КОСТИ | 2017 |
|
RU2669047C1 |
| УСТРОЙСТВО ДЛЯ НАРУШЕНИЯ ЦЕЛОСТНОСТИ КОСТИ | 2006 |
|
RU2321896C1 |
| Способ моделирования посттравматического остеомиелита у мелких лабораторных животных | 1989 |
|
SU1691876A1 |
| СПОСОБ МОДЕЛИРОВАНИЯ КОСТНОГО ДЕФЕКТА БЕДРЕННОЙ КОСТИ | 2007 |
|
RU2345423C1 |
| Doblaré M., García J.M | |||
| On the modelling bone tissue fracture and healing of the bone tissue | |||
| Acta Cient Venez | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Haffner-Luntzer M., Ignatius A | |||
| Animal models for studying metaphyseal bone fracture healing | |||
| Eur Cell Mater | |||
Авторы
Даты
2023-08-28—Публикация
2022-12-07—Подача