Перекрестная ссылка на родственную заявку
Приоритет испрашивается согласно патентной заявки США № 15/434617, поданной 16 февраля 2017 года, полное содержание которой включено в настоящую заявку посредством ссылки.
Область техники, к которой относится изобретение
Настоящее раскрытие относится к 13-дезоксиантрациклинам, и более конкретно к 3'-дезамино-3'-(2"-пирролин-1"-ил)-5-имино-13-дезоксиантрациклинам, и к способам их получения и применения. Настоящее раскрытие также относится к синергетическим комбинациям 2-пирролинo-13-дезоксиантрациклинов и 13-дезоксиантрациклинов.
Предпосылки создания изобретения
Доксорубицин, антрациклиновый антибиотик, является одним из наиболее широко используемых и очень сильных противораковых средств. Он имеет широкий спектр противораковой активности, являясь полезным в лечении острого лимфобластного лейкоза, острого миелобластного лейкоза, опухоли Вильмса, нейробластомы, сарком мягких тканей и кости, карциномы молочной железы, карциномы яичника, переходноклеточной карциномы мочевого пузыря, карциномы щитовидной железы, карциномы желудка, болезни Ходжкина, злокачественной лимфомы и бронхогенной карциномы (инструкция по применению доксорубицина, Pfizer Inc., New York, NY). Для более широкого использования огромного туморицидного потециала, связанного со структурой антрациклиновых антибиотиков, были описаны тысячи синтетических производных, включая их аналоги, связанные с различными макромолекулами- носителями.
Nagy et al. (Proc. Natl. Acad. Sci. vol. 93, pp. 2464-2469, 1996) описывали, что модификация доксорубицина (соединение I) до 3'-дезамино-3'-(2"-пирролин-1"-ил)доксорубицина (соединение II; 2-пирролинoдоксорубицин) повышала противораковую активность в отношении человеческих и мышиных раковых клеток in vitro в 500 - 1000 раз по сравнению с доксорубицином.
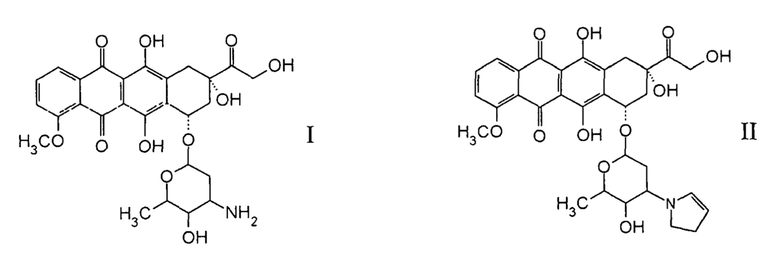
Доксорубицин быстро проникает в ядро клеток и связывается с высокой аффинностью с ДНК путем нековалентной интеркаляции между парами оснований, приводя к ингибированию синтеза биомакромолекул. Общепризнано, что биологические эффекты доксорубицина связаны с его способностью действовать в качестве ингибитора топоизомеразы II (topoII), нарушающего стадию повторного лигирования этого фермента и образующего тройной доксорубицин-DNA-topoII расщепляемый комплекс. Оказалось, что 2-пирролинo-доксорубицин действует таким же образом (Stepankova et al., Biochemical Pharmacology 82: 227-235, 2011). Существуют только некоторые различия в модификациях ДНК этими антрациклинами и получаемых в результате конформационных изменениях в ДНК. Подобным образом, способность 2-пирролинoдоксорубициновых модификаций ДНК ингибировать каталитическую активность топоизомеразы II не отличается существенным образом от способности доксорубицина. (Stepankova et al., supra).
Однако повышение активности доксорубицина путем преобразования его в 2-пирролинo-соединение делало его неспецифическим, что касается цитотоксичности. Следовательно, 2-пирролинoдоксорубицин является токсичным или летальным на уровне или ниже доз, которые требуются для противоракового эффекта (Jungwirth, A et al., International Journal of Oncology 10: 877-884, 1997; и Szepeshazi, K et al., Clinical Cancer Research, 7: 2854-2861, 2001). Как результат, 2-пирролинoдоксорубицин не был полезен в качестве лекарственного средства для лечения рака. Jungwirth et al., supra и Szepeshazi et al., supra предложили модифицировать 2-пирролинoдоксорубицин путем его конъюгирования в 14-положении OH с аналогами соматостатина или рилизинг-фактора лютеинизирующего гормона. Однако эти модификации в результате давали соединения, специфические в отношении некоторых опухолей, ограничивая, таким образом, широкий спектр активности исходного соединения.
Сущность изобретения
В соответствии с настоящим изобретением, обеспечиваются антрациклиновые соединения, содержащие 2-пирролинo группу, которые повышают противораковую активность широкого спектра, сохраняя при этом хороший профиль безопасности и такую характерную особенность антрациклина, как широкий спектр действия. В частности, соединения в соответствии с настоящим изобретением представлены формулой X:
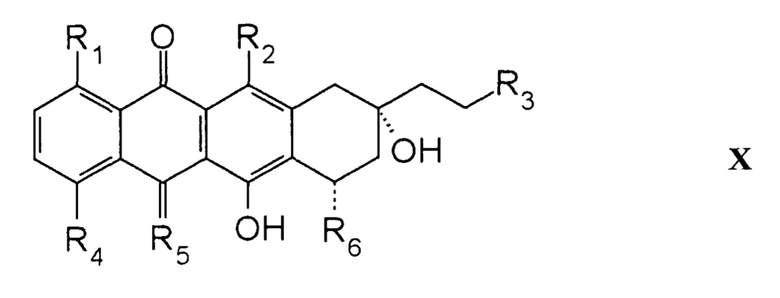
где:
каждый R1, R2 и R3 независимо представляет собой H или OH;
R4 выбран из группы, состоящей из H, OH, алкила и O-алкила;
R5 представляет собой O или NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин;
их фармацевтически приемлемые соли, их дейтерированные формы, их пролекарства, их изомеры, их сольваты и их смеси.
Предпочтительно, соединение представляет собой производное антрациклина, выбранное из группы, состоящей из 2-пирролинo-13-дезоксидоксорубицина, 2-пирролинo-13-дезоксидаунорубицина, 2-пирролинo-13-дезоксиэпирубицина, 2-пирролинo-13-дезоксикарминомицина и 2-пирролинo-13-дезоксиидарубицина и их 5-имино (R5 = NH) аналогов.
Настоящее изобретение также относится к фармацевтической композиции, которая включает соединение формулы X и фармацевтически приемлемый носитель или эксципиент.
Другой аспект настоящего изобретения относится к способу для подавления роста клеток, который включает введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества соединения формулы X или композиции, включающей соединение формулы X.
Настоящее изобретение также относится к терапевтически эффективному количеству синергетического комбинированного препарата, включающего первое соединение и второе соединение, где: первое соединение представляет собой 2-пирролинo-13-дезоксиантрациклин, имеющий формулу X:
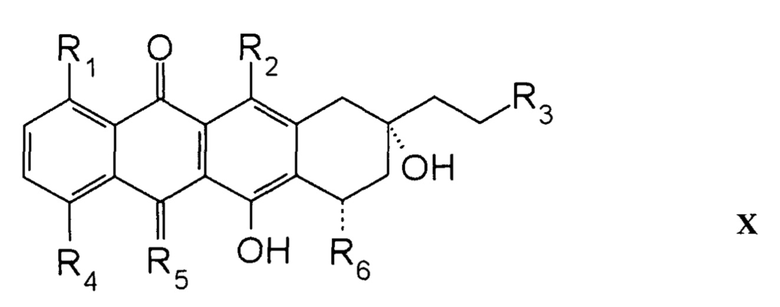
где:
каждый R1, R2 и R3 независимо представляет собой H или OH;
R4 выбран из группы, состоящей из H, OH, алкила и O-алкила;
R5 представляет собой O или NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин;
его фармацевтически приемлемые соли, его пролекарства, его дейтерированные формы, его изомеры, его сольваты и их смеси; и
второе соединение представляет собой 13-дезоксиантрациклин, при этом указанный 13-дезоксиантрациклин имеет формулу:
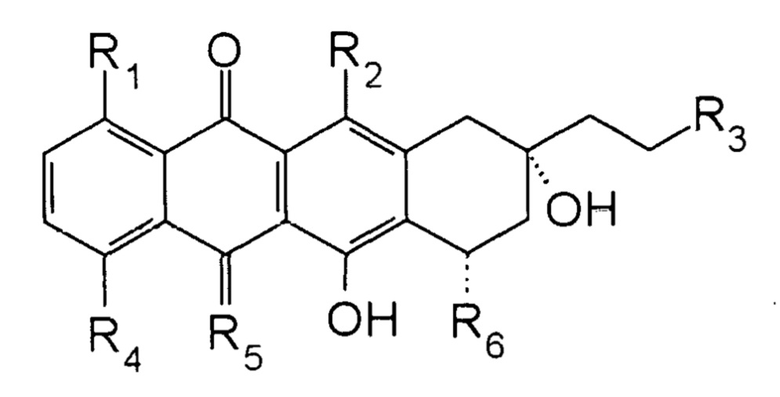
где
каждый из R1, R2 и R3 независимо выбран из группы, состоящей из H и OH;
R4 выбран из группы, состоящей из H, OH, алкила и O-алкила;
R5 выбран из группы, состоящей из O и NH; и
R6 представляет собой сахарный компонент;
его фармацевтически приемлемые соли, его пролекарство, его дейтерированные формы, его изомеры, его сольваты и их смеси;
и
где терапевтически эффективное количество синергетического комбинированного препарата подавляет рост клеток.
Предпочтительно первое соединение представляет собой производное антрациклина, выбранное из группы, состоящей из 2-пирролинo-13-дезоксидоксорубицина, 2-пирролинo-13-дезоксидаунорубицина, 2-пирролинo-13-дезоксиэпирубицина, 2-пирролинo-13-дезоксикарминомицина и 2-пирролинo-13-дезоксиидарубицина и их 5-имино аналогов, а второе соединение представляет собой производное антрациклина, выбранное из группы, состоящей из 13-дезоксидоксорубицина, 13-дезоксидаунорубицина, 13-дезоксиэпирубицина, 13-дезоксикарминомицина, 13-дезоксиидарубицина, 13-дезоксианнамицина и 13-дезоксиамрубицина и их 5-имино аналогов.
Еще в одном аспекте настоящего изобретения представлена фармацевтическая композиция, которая включает синергетический комбинированный препарат, раскрытый выше, и фармацевтически приемлемый носитель или эксципиент.
Настоящее изобретение также относится к способу подавления роста клеток синергетическим комбинированным препаратом, содержащим первое соединение, определенное выше, и второе соединение, определенное выше, включающему введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества синергетического комбинированного препарата, его фармацевтически приемлемых солей, его дейтерированных форм, его пролекарств, его изомеров или его сольватов.
Можно сформулировать и вводить синергетический комбинированный препарат, где второе соединение присутствует в количестве, которое меньше, чем его терапевтически эффективное количество. Также можно сформулировать и вводить синергетический комбинированный препарат, где первое соединение присутствует в количестве, которое меньше, чем его терапевтически эффективное количество. В качестве примера, когда второе соединение присутствует в количестве, которое меньше, чем его терапевтически эффективное количество, массовое отношение второго соединения к первому компоненту типично может быть от около 0,005 до около 0,10:1 и более типично от около 0,01 до около 0,10:1. Также, в качестве примера, когда первое соединение присутствует в количестве, которое меньше, чем его терапевтически эффективное количество, массовое отношение первого соединения к второму компоненту типично может быть от около 0,005 до около 0,10:1 и более типично от около 0,01 до около 0,10:1.
Другие цели и преимущества настоящего изобретения станут очевидными для специалистов в данной области техники из следующего подробного описания, где показаны и описаны только предпочтительные варианты осуществления просто путем иллюстрации наилучшего способа осуществления. Как должно быть понятно, изобретение допускает другие и разные варианты осуществления, и некоторые его детали могут быть модифицированы в некоторых очевидных отношениях без отступления от настоящего раскрытия. Соответственно, описание следует рассматривать как иллюстративное по своей природе, а не как ограничивающее.
Подробное описание изобретения
Хотя далее подробно описаны некоторые варианты осуществления настоящего изобретения, должно быть понятно, что изобретение не ограничивается в своем применении детализацией композиций и комбинаций соединений, описанных в прилагаемых примерах и экспериментах, поскольку настоящее изобретение может иметь другие варианты осуществления и может быть осуществлено различными способами.
2-Пирролинo-13-дезоксиантрациклиновые соединения, используемые в соответствии с настоящим изобретением, имеют следующую формулу X:
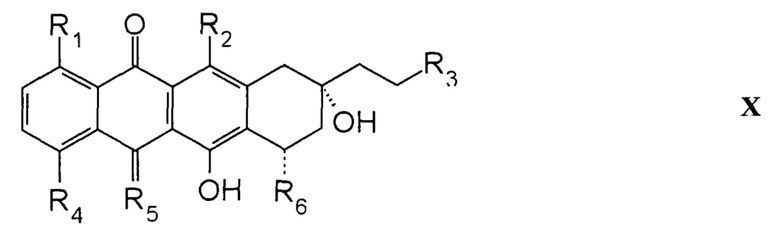
где каждый R1, R2 и R3 независимо представляет собой H или OH; R4 выбран из группы, состоящей из H, OH, алкила и O-алкила; R5 представляет собой O или NH; и R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин. Более типичные 2-пирролинo-13-дезоксиантрациклины представляют собой 2-пирролинo-13-дезоксидоксорубицин, 2-пирролинo-13-дезоксидаунорубицин, 2-пирролинo-13-дезоксиэпирубицин, 2-пирролинo-13-дезоксикарминомицин и 2-пирролинo-13-дезоксиидарубицин и их 5-имино аналоги (R5 = NH).
Алкильные группы типично содержат 1-6 атомов углерода и могут быть линейными или разветвленными. Примеры подходящих алкильных групп включают метил, этил, изопропил, н-пропил, бутил, н-бутил, пентил и гексил.
"Фармацевтически приемлемые соли" относятся к производным раскрываемых соединений, где исходное соединение модифицировано путем получения его кислотных солей. Соединения по настоящему изобретению образуют кислотно-аддитивные соли с широким спектром органических и неорганических кислот и включают физиологически приемлемые соли, которые часто используются в фармацевтической химии. Такие соли также являются частью настоящего изобретения. Типичные неорганические кислоты, используемые для образования таких солей, включают хлористоводородную, бромистоводородную, йодистоводородную, азотную, серную, фосфорную, гипофосфорную и т.п. Также могут использоваться соли, образованные из органических кислот, таких как алифатические моно- и дикарбоновые кислоты, фенил-замещенные алконовые кислоты, гидроксиалкановые и гидроксиалкандиовые кислоты, ароматические кислоты, алифатические и ароматические сульфоновые кислоты. Такие фармацевтически приемлемые соли, таким образом, включают ацетат, фенилацетат, трифторацетат, акрилат, аскорбат, бензоат, хлорбензоат, динитробензоат, гидроксибензоат, метоксибензоат, метилбензоат, о-ацетоксибензоат, нафталин-2-бензоат, бромид, изобутират, фенилбутират, β-гидроксибутират, бутин-1,4-диоат, гексин-1,4-диоат, капрат, каприлат, хлорид, циннамат, цитрат, формиат, фумарат, гликолят, гептаноат, гиппурат, лактат, малат, малеат, гидроксималеат, малонат, манделат, мезилат, никотинат, изоникотинат, нитрат, оксалат, фталат, терафталат, фосфат, моногидрофосфат, дигидрофосфат, метафосфат, пирофосфат, пропиолат, пропионат, фенилпропионат, салицилат, себацинат, сукцинат, суберат, сульфат, бисульфат, пиросульфат, сульфит, бисульфит, сульфонат, бензолсульфонат, п-бромбензолсульфонат, хлорбензолсульфонат, этансульфонат, 2-гидроксиэтансульфонат, метансульфонат, нафталин-1-сульфонат, нафталин-2-сульфонат, п-толуолсульфонат, ксилолсульфонат, тартрат и т.п.
Дейтерированные формы содержат тяжелвый водород, включая дейтерий и/или тритий.
Должно быть понятно, что соединения по настоящему изобретению относятся ко всем опитическим изомерам и стереоизомерам по различным возможным атомам в молекуле, если не указано иное.
Термин “сольваты” относится к соединению, образованному путем взаимодействия растворителя и растворенного вещества, и включает гидраты. Сольваты обычно представляют собой кристаллические твердые аддукты, содержащие молекулы растворителя в кристаллической структуре либо в стехиометрических, либо в нестехиометрических пропорциях.
Пролекарственные формы соединений, содержащих различные азот-содержащие функциональные группы (амино), могут включать следующие типы производных, где каждая R группа независимо может представлять собой водород, замещенную или незамещенную алкильную, арильную, алкенильную, алкинильную, гетероциклическую, алкиларильную, аралкильную, аралкенильную, аралкинильную, циклоалкильную или циклоалкенильную группу.
(a) Карбоксамиды, -NHC(O)R
(b) Карбаматы, -NHC(O)OR
(c) (Ацилокси)алкилкарбаматы, NHC(O)OROC(O)R
(d) Енамины,-NHCR(=CHCO2R) или -NHCR(=CHCONR2)
(e) Основание Шиффа,-N=CR2.
Синтез и очистка 13-дезоксиантрациклинов раскрыты в патентах США №№ 5942605; 5948896; и 7244829, которые включены в настоящую заявку посредством ссылки. Способ преобразования антрациклинов в 2-пирролинo-антрациклины раскрыт в Nagy et al., supra и в патенте США № 6184374, которые включены в настоящую заявку посредством ссылки.
Было обнаружено, что 13-дезокси формы доксорубицина, даунорубицина или других подобных антрациклинов не будут метаболически преобразовываться в кардиотоксичные 13-дигидро формы и, таким образом, не обладают кумулятивной необратимой кардиотоксичностью. В частности, см. WO99/08687, патенты США №№ 5948896 и 5942605 и PCT/US99/04704, раскрытие которых включено в настоящую заявку посредством ссылки.
5-имино-13-дезоксидоксорубицин испытан в Фазе I клинических испытаний у пациентов с прогрессирующими опухолями (Holstein, SA Investigative New Drugs. 2015, 33: 594-602). Это соединение обладает противораковой активностью при различных карциномах, саркомах и раке мочевого пузыря. Кроме того, соединение было хорошо переносимым с относительно слабой токсичностью антрациклина. До настоящего времени не было известно, будут ли такие 13-дезоксиантрациклиновые противораковые средства иметь повышенный противораковый эффект при преобразовании их в 2-пирролинo-аналоги, и будут ли они одновременно иметь приемлемый профиль безопасности. Как указано выше, 2-пирролинo-доксорубицин является очень сильным, но также токсичным и летальным на уровне или около доз, которые требуются для противораковой эффективности.
2-Пирролинo-13-дезоксиантрациклины формулы X демонстрируют противораковую, противоопухолевую и/или антинеопластическую эффективность, которая полезна для всех типов терапий для лечения рака, новообразований или опухолей, включая лейкоз, меланому, опухоли печени, молочной железы, яичника, предстательной железы, желудка, поджелудочной железы, легкого, почки, толстой кишки и центральной нервной системы. Лечения по настоящему изобретению обеспечивают способы подавления роста нормальных клеток (таких как псориатические клетки кожи), рака, опухолей и новообразований у млекопитающих, включая человека, с использованием соединений формулы X.
Фармацевтическая композиция по настоящему изобретению включает соединение или соединения формулы X, их фармацевтически приемлемые соли, их дейтерированные формы, их пролекарство, их изомеры и/или их сольваты в фармацевтически приемлемом носителе или эксципиенте. Эти фармацевтические композиции по настоящему изобретению являются полезными в противораковой терапии и лечении клеточно-пролиферативных расстройств. Фармацевтически приемлемые носители или эксципиенты хорошо известны специалистам обычной квалификации в области формулирования соединений в виде фармацевтических композиций, комбинаций, смесей и препаратов. Фармацевтически приемлемый носитель относится к одному или нескольким совместимым твердым или жидким наполнителям, разбавителям или инкапсулирующим веществам, которые являются подходящими для введения млекопитающим, включая человека. Фармацевтические композиции, комбинации, смеси и препараты, подходящие для парентерального введения, получают в стерильной форме, которая может представлять собой стерильный раствор или суспензию в приемлемом разбавителе или растворителе.
Количество активного ингредиента, содержащегося в фармацевтической композиции, может варьироваться в достаточно широких пределах в зависимости от многих факторов, таких как путь введения и носитель. В настоящем изобретении фармацевтическая композиция может содержать от около 0,1 до 1000 мг 2-пирролинo-13-дезоксиантрациклина формулы X на мл или грамм фармацевтической композиции.
В способе применения 2-пирролинo-13-дезоксиантрациклин формулы X, его фармацевтически приемлемые соли, его дейтерированные формы, его пролекарство, его изомеры и/или его сольваты вводят пациенту, нуждающемуся в этом, при дозе от около 0,1 мг/м2 площади поверхности тела до около 1000 мг/м2 площади поверхности тела, более типично от около 10 мг/м2 площади поверхности тела до около 500 мг/м2 площади поверхности тела. Дозы 2-пирролинo-13-дезоксиантрациклинов можно вводить так часто, как это необходимо. Фактический способ введения будет варьироваться в соответствии с конкретной лекарственной формой, композицией, комбинацией, смесью или препаратом, конкретным типом рака или клеточно-пролиферативного расстройства, подлежащим лечению, и конкретным пациентом, которого нужно лечить.
Композицию можно вводить пациенту любым способом, который приемлем с медицинской точки зрения, включая пероральное, парентеральное, местное введение или введение путем имплантации. Пероральное введение включает введение композиции в форме таблеток, капсул, таблеток для рассасывания, суспензий, растворов, эмульсий, порошков, сиропов и т.п. Предпочтительным путем введения является парентеральный.
Фактический способ и порядок введения могут варьироваться в соответствии с конкретной используемой фармацевтической композицией соединения формулы X, конкретным типом рака, подлежащим лечению, тяжестью болезненного состояния, подлежащего лечению, и конкретным пациентом, которого лечат. Пределы доз для введения компонентов могут варьироваться в зависимости от возраста, состояния, пола и тяжести заболевания у пациента, и их может определить специалист средней квалификации в данной области.
Примеры рака, который можно лечить в соответствии с настоящим изобретением, включают рак молочной железы, рак мочевого пузыря, саркому Karpi, лейкоз, такой как острый лимфобластный лейкоз и острый миелобластный лейкоз, опухоль Вильмса, нейробластому, лимфому, саркомы мягких тканей и кости, рак яичника, рак мочевого пузыря, включая переходноклеточный рак мочевого пузыря, рак щитовидной железы, карциному желудка, болезнь Ходжкина и бронхогенную карциному.
Для испытания, можно ли преобразовать 13-дезоксиантрациклин в 2-пирролинo-13-дезоксиантрациклин, использовали способ Nagy et al., supra, для преобразования амина в сахарном компоненте в 3’-дезамино-3’-(2’’-пирролин-1’’-ил) группу. В качестве примера, 5-имино-13-дезоксидоксорубицин III преобразовывали в 2-пирролинo-5-имино-13-дезоксидоксорубицин IV. Соединение IV испытывали in vitro и in vivo на противораковую активность и эффективность. Преобразование соединения III в соединение IV показано ниже:
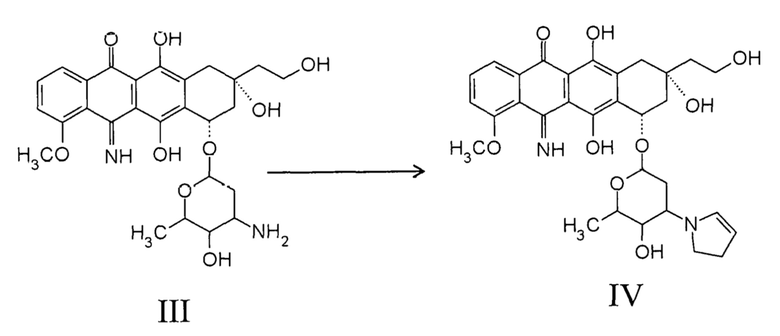
Преобразование 13-дезоксиантрациклина в 2-пирролинo-13-дезоксиантрациклин формулы X с улучшенной активностью и эффективностью показано, в качестве примера, в следующем синтезе и биологических испытаниях, которые предназначены для иллюстрации, а не для ограничения настоящего изобретения.
Пример 1
5-имино-13-дезоксидоксорубицин HCl соль (III, 62,4 мг, 0,1104 ммоль) растворяли в 10 мл диметилформамида (DMF) и 90 мл дихлорметана в колбе. Колбу продували азотом и затем добавляли по каплям 4-иодбутиральдегид (0,697 г, 3,535 ммоль, 33 эквивалента) в 10 мл дихлорметана. Затем добавляли N,N-диизопропилэтиламин (0,152 г, 205 мкл, 1,178 ммоль, 11 эквивалентов) через шприц и реакционную колбу оборачивали фольгой и оставляли для перемешивания на 1,25 часа при комнатной температуре. После завершения реакции, по данным высоко-эффективной жидкостной хроматографии (ВЭЖХ), добавляли 20 мл 1% раствора трифторуксусной кислоты (TFA) в метаноле. Раствор концентрировали на роторном испарителе до ¼ его исходного объема. Добавляли раствор простой эфир/гексан (1:5, 100 мл), при этом происходило образование темно-фиолетового осадка. Твердому веществу давали осадиться и светло-фиолетовый маточный раствор сливали через канюлю. Оставшееся твердое вещество промывали дополнительным объемом 1:5 эфира/гексана и затем сушили в течение ночи в условиях высокого вакуума в обернутой алюминиевой фольгой колбе. Выход 2-пирролинo-5-имино-13-дезоксидоксорубицина IV составил 61,0 мг (0,0878 ммоль, 79,5%) в виде фиолетового порошка, который имел чистоту 92% по данным ВЭЖХ.
Пример 2
Ингибирующую рост активность 2-пирролинo-5-имино-13-дезоксидоксорубицина IV, 5-имино-13-дезоксидоксорубицина III и доксорубицина I против нескольких раковых клеточных линий оценивали в флуоресцентном анализе с использованием резазурина. Ингибирующую рост активность измеряли как ингибирующую концентрацию соединения, необходимую для ингибирования клеточного роста на 50% (IC50). Раковые клетки высевали в 96-луночные планшеты (0,5-1×104 клеток/лунка) с подходящей средой, инкубировали с лекарственным средством в течение 48 часов и затем обрабатывали резазурином (конечная концентрация 0,01%), нефлуоресцентным синим красителем, в течение 24 часов. Флуоресценцию (возб.560нм/эм.590нм) регистрировали с использованием флуориметра для многолуночных планшетов BioTek SynergyHT. Здоровые клетки метаболизируют резазурин до резоруфина, флуоресцентного розового красителя. Таким образом, флуоресценция является показателем жизнеспособности клеток и используется для определения эффекта цитотоксических средств на клеточные культуры. Результаты анализов цитотоксической активности в пяти раковых клеточных линиях человека и одной нормальной клеточной линии человека представлены в Таблице 1. Против всех раковых клеток 2-пирролинo-5-имино-13-дезоксидоксорубицин IV был значительно более эффективным по сравнению с исходным соединением 5-имино-13-дезоксидоксорубицином III, с IC50 значениями, которые были в 13-27 раз ниже, чем значения 5-имино-13-дезоксидоксорубицина III. Активность 2-пирролинo-5-имино-13-дезоксидоксорубицина IV также была выше, чем у доксорубицина I, с IC50 значениями, которые в среднем были ниже, чем у доксорубицина I.
Соединения также испытывали против нормальной не-раковой клеточной линии, нормальных человеческих фибробластов (HADF). 2-пирролинo-5-имино-13-дезоксидоксорубицин IV имел цитотоксичность в два раза меньше (39,75/18,9), чем доксорубицин I, против HADF (нормальных) клеток. Результаты этих исследований показаны в Таблице 1.
Соединения также испытывали против клеточной линии фибросаркомы матки, MES-SA, чувствительной к доксорубицину (соединение I), и против клеточной линии фибросаркомы матки MES-SA/MX2, резистентной к доксорубицину. Эти результаты показаны в Таблице 2.
Антипролиферативная активность (IC50) Соединения IV, Соединения III и Соединения I против человеческих раковых клеточных линий и нормальной клеточной линии, определенная с использованием резазуринового анализа. IC50 значения представляют собой среднее значение (± SEM) от 3 отдельных анализов, каждый из которых осуществляли в трех повторах.
Соединение IV, как было показано, в среднем в 20 (10,09/0,49) раз более эффективно для ингибирования клеточного роста раковых клеток, чем соединение III, и в 18 (9,06/0,49) раз более эффективно, чем соединение I. Соединение IV в среднем в 81 (39,75/0,49) раз более активно против раковых клеток, чем против нормальной не-раковой клеточной линии. Соединение III в среднем только в 5,8 (58,9/10,09) раз более активно против раковых клеток, чем против нормальных клеток, а соединение I только в 2 (18,9/9,06) раза более активно. Таким образом, было показано, что селективность соединения IV в отношении раковых клеток по сравнению с нормальными клетками в 14 (81/5,8) раз больше по сравнению с соединением III и в 40 (81/2) раз больше по сравнению с соединением I. Этот результат был неожиданным и является очевидной протиположностью тому, что сообщалось для соединения II (2-пирролинoдоксорубицин), которое имело незначительную, или вообще не имело, селективность в отношении раковых клеток по сравнению с нормальными клетками. Еще более неожиданным и непредсказуемым было то, что селективность соединения IV в отношении раковых клеток по сравнению с нормальными клетками, как было показано, в 40 раз больше по сравнению с соединением I (доксорубицин). Таким образом, образование 2-пирролинo аналога 5-имино-13-дезоксидоксорубицина (III) дало более эффективный и более безопасный антрациклин по сравнению с образованием 2-пирролинo аналога доксорубицина (I), что дало высокоактивный токсин II без какой-либо терапевтической пользы.
Антипролиферативная активность (IC50) Соединения IV, Соединения III и Соединения I против человеческих раковых клеточных линий, чувствительных и резистентных к доксорубицину. IC50 значения представляют собой среднее значение (± SEM) от 3 отдельных анализов, каждый из которых осуществляли в трех повторах.
Соединение IV более эффективно, чем соединение III и является примерно равным по эффективности соединению I в доксорубицин-чувствительном штамме фибросаркомы. В резистентном штамме фибросаркомы соединение I в 14 (7,8/0,55) раз менее эффективно, чем в чувствительном штамме фибросаркомы, как и ожидалось. С другой стороны, соединение IV примерно также эффективно в резистентном штамме фибросаркомы, как и в чувствительном штамме фибросаркомы. Таким образом, соединение IV в 12 раз более эффективно, чем соединение I, в антрациклин- резистентной клеточной линии, показывая, что при лечени рака раковая ткань не будет становиться резистентной к соединению IV. Это отличительное свойство является существенным улучшением в соединении IV по сравнению с соединениями III и I.
Пример 3
Чтобы оценить активность лекарственного средства in vivo на рост первичной опухоли в модели саркомы, осуществляли эксперимент с использованием коммерчески доступных клеток фибросаркомы HT1080 человека, сконструированных для экспрессии люциферазы (HT1080-luc; PerkinElmer). Ингибирующую активность соединения III и соединения IV против HT1080-luc измеряли in vitro способами, описанными в Примере 2. Значение IC50 ± SEM (мкМ) для соединения IV составляло 3,51±1,79, а для соединения III составляло 10,0±6,1. HT1080-luc опухоли стимулировали у самок мышей SCID 6-недельного возраста (Harlan) путем ортотопической подкожной инъекции 1×106 клеток в каждый бок. После установления опухолей в течение 6 дней мышей рандомизировали в одну из трех групп лечения и обрабатывали три раза в неделю внутрибрюшинной инъекцией соединения IV или соединения III, 2,4 мг/кг в физиологическом забуференном физиологическом растворе (PBS), или инъекцией носителя (PBS). Результаты показаны в Таблице 3. На основании результатов биолюминесцентной визуализации in vivo прогрессирование опухоли снижалось статистически значимым образом на 20-й день у мышей, получавших соединение IV, по сравнению с мышами, получавшими только PBS. Прогрессирование опухоли не уменьшалось значимым образом при использовании соединения III. На 20-й день уменьшение массы опухоли составило 53% при использовании соединения IV, тогда как при использовании соединения III при той же заданной дозе оно составило только 36%. Эти результаты указывают на повышенную эффективность соединения IV по сравнению с соединением III при заданной дозе и согласуются с результатами in vitro, представленными выше. Соединение IV хорошо переносилось мышами без смертельных исходов и явных признаков токсичности, таких как птоз, лордоз, летаргия и потеря веса. Это противоположно 2-пирролинодоксорубицину, который может быть летальным при эффективном диапазоне доз.
Средняя масса опухоли в день 20. Звездочка (*) указывает на существенное уменьшение по сравнению с контролями, которых обрабатывали PBS (p < 0,05). Значения представляют собой средние значения + стандартная ошибка среднего.
Анти-клеточнопролиферативные терапевтические эффекты 2-пирролинo-13-дезоксиантрациклинов формулы X существенно повышались при комбинировании их с 13-дезоксиантрациклинами формулы Y. Этот повышенный терапевтический эффект является результатом неожиданного синергизма между 2-пирролинo-13-дезоксиантрациклинами и 13-дезоксиантрациклинами. 13-Дезоксиантрациклиновые соединения, используемые в соответствии с настоящим изобретением, имеют следующую формулу Y:
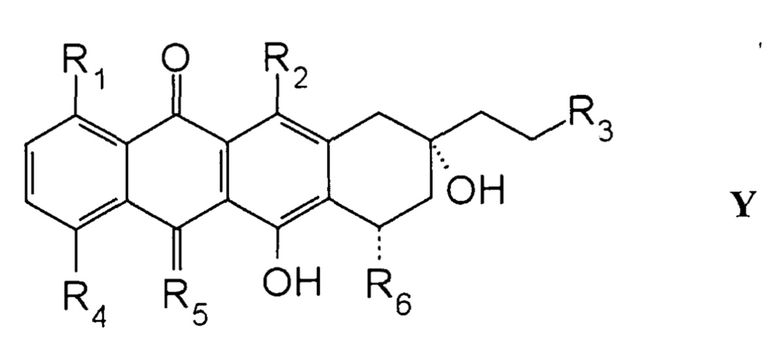
где каждый R1, R2 и R3 независимо представляет собой H или OH; R4 выбран из группы, состоящей из H, OH, алкила и O-алкила; R5 представляет собой O или NH; и R6 представляет собой сахар, содержащий первичную амино группу или не содержащий амино группу; их фармацевтически приемлемые соли, их дейтерированные формы, их пролекарства, их изомеры и/или их сольваты. Более типичные 13-дезоксиантрациклины представляют собой 13-дезоксидоксорубицин, 13-дезоксидаунорубицин, 13-дезоксиэпирубицин, 13-дезоксикарминомицин, 13-дезоксиидарубицин, 13-дезоксианнамицин и 13-дезоксиамрубицин и их 5-имино аналоги (R5 = NH).
Алкильная группа в представленной выше формуле Y является такой же, как раскрыто выше.
Кроме того, лечение по настоящему изобретению с использованием комбинации 2-пирролинo-13-дезоксиантрациклинов и 13-дезоксиантрациклинов демонстрирует противораковую, противоопухолевую и/или антинеопластическую эффективность, которая полезна для всех типов терапии для лечения клеточно-пролиферативных расстройств, таких как воспаление, псориаз, рак, новообразования или опухоли, включая лейкоз, меланому, опухоли печени, молочной железы, яичника, предстательной железы, желудка, поджелудочной железы, легкого, почки, толстой кишки и центральной нервной системы. Лечение по настоящему изобретению обеспечивает способ подавления роста рака, опухолей, новообразований и нормальных клеток у млекопитающих, включая человека.
Типичная композиция, комбинация, смесь или препарат, включающие компоненты в соответствии с настоящим раскрытием, представляют собой соединение формулы X, его фармацевтически приемлемую соль, его дейтерированную форму, его пролекарство, его изомер и/или его сольват в комбинации с соединением формулы Y; его фармацевтически приемлемой солью, его дейтерированной формой, его пролекарством, его изомером и/или его сольватом. Более типичная композиция, комбинация, смесь или препарат представляет собой 2-пирролинo-13-дезоксиантрациклин, выбранный из группы, состоящей из 2-пирролинo-13-дезоксидоксорубицина, 2-пирролинo-13-дезоксидаунорубицина, 2-пирролинo-13-дезоксиэпирубицина, 2-пирролинo-13-дезоксикарминомицина и 2-пирролинo-13-дезоксиидарубицина и их 5-имино аналогов; его фармацевтически приемлемую соль, его дейтерированную форму, его пролекарство, его изомер и/или его сольват, и 13-дезоксиантрациклин, выбранный из группы, состоящей из 13-дезоксидоксорубицина, 13-дезоксидаунорубицина, 13-дезоксиэпирубицина, 13-дезоксиидарубицина, 13-дезоксианнамицина, 13-дезоксикарминомицина, 13-дезоксиамрубицина и их 5-имино аналогов; его фармацевтически приемлемую соль, его дейтерированную форму, его пролекарство, его изомер и/или его сольват.
Компоненты композиции, комбинации, смеси или препарата можно вводить пациенту одновременно, раздельно, последовательно или один за другим. Компоненты можно вводить пациенту любым приемлемым способом, который приемлем с медицинской точки зрения, включая пероральное, парентеральное, местное введение или путем имплантации. Пероральное введение включает введение компонентов композиций, комбинаций, смесей или препаратов в форме таблеток, капсул, таблеток для рассасывания, суспензий, растворов, эмульсий, порошков, сиропов и т.п. Предпочтительным путем введения является парентеральный.
Фактический способ и порядок введения компонентов могут варьироваться в соответствии с конкретной фармацевтической композицией 2-пирролинo-13-дезоксиантрациклина формулы X и конкретной фармацевтической композицией 13-дезоксиантрациклина формулы Y, которые используют, конкретного рака или клеточно-пролиферативного расстройства, подлежащего лечению, тяжести болезненного состояния, подлежащего лечению, и конкретного пациента, которого лечат. Пределы доз для введения компонентов могут варьироваться в зависимости от возраста, состояния, пола и тяжести заболевания у пациента, и их может определить специалист средней квалификации в данной области.
Фармацевтическая композиция по настоящему изобретению включает 2-пирролинo-13-дезоксиантрациклин формулы X; его фармацевтически приемлемую соль, его дейтерированную форму, его пролекарство, его изомер и/или его сольват, смешанный вместе с 13-дезокси антрациклином формулы Y; его фармацевтически приемлемой солью, его дейтерированной формой, его пролекарством, его изомером и/или его сольватом в фармацевтически приемлемом носителе или эксципиенте. Эти фармацевтические композиции по настоящему изобретению являются полезными для противораковой терапии и лечения клеточно-пролиферативных расстройств.
Фармацевтически приемлемые носители или эксципиенты хорошо известны специалистам обычной квалификации в области формулирования соединений в виде фармацевтических композиций, комбинаций, смесей и препаратов. Фармацевтически приемлемый носитель относится к одному или нескольким совместимым твердым или жидким наполнителям, разбавителям или инкапсулирующим веществам, которые являются подходящими для введения млекопитающим, включая человека. Фармацевтические композиции, комбинации, смеси и препараты, подходящие для парентерального введения, получают в виде стерильной формы, которая может представлять собой стерильный раствор или суспензию в приемлемом разбавителе или растворителе.
Количество активного ингредиента, содержащегося в фармацевтической композиции, может варьироваться в достаточно широких пределах в зависимости от множества факторов, таких как путь введения и носитель. В настоящем изобретении фармацевтическая композиция может содержать от около 0,1 до 1000 мг 2-пирролинo-13-дезоксиантрациклина формулы X, его фармацевтически приемлемой соли, его дейтерированной формы, его пролекарства, его изомера и/или его сольвата и от около 0,1 до 1000 мг 13-дезоксиантрациклина формулы Y, его фармацевтически приемлемой соли, его дейтерированной формы, его пролекарства, его изомера и/или его сольвата.
В способе по настоящему изобретению 2-пирролинo-13-дезоксиантрациклин формулы X, его фармацевтически приемлемую соль, его дейтерированную форму, его пролекарство, его изомер и/или его сольват вводят пациенту, нуждающемуся в этом, при дозе от около 0,1 мг/м2 площади поверхности тела до около 1000 мг/м2 площади поверхности тела, более типично от около 10 мг/м2 площади поверхности тела до около 500 мг/м2 площади поверхности тела, и более типично парентеральным путем введения. 13-Дезокси антрациклин формулы Y, его фармацевтически приемлемую соль, его дейтерированную форму, его пролекарство, его изомер и/или его сольват по настоящему изобретению вводят пациенту, нуждающемуся в этом, при дозе от около 0,1 мг/м2 до около 1000 мг/м2, более типично от около 10 мг/м2 до около 500 мг/м2, и более типично парентеральным путем введения. 2-Пирролинo-13-дезоксиантрациклин и 13-дезоксиантрациклин можно вводить вместе в одной композиции, комбинации, смеси или препарате, или их можно вводить раздельно в любом порядке, последовательно в любом порядке или один за другим в любом порядке. Если их не вводят вместе, второе соединение типично вводят в течение 72 часов после введения первого соединения.
Противораковые/антипролиферативные терапевтические эффекты 2-пирролинo-13-дезоксиантрациклина существенно повышаются при помощи 13-дезоксиантрациклина без повышения токсичности. Подобным образом, противораковые/антипролиферативные терапевтические эффекты 13-дезоксиантрациклина существенно повышаются при помощи 2-пирролинo-13-дезоксиантрациклина без повышения токсичности. Это отсутствие повышения токсичности частично можно отнести за счет синергизма между двумя типами соединений. Дозы 2-пирролинo-13-дезоксиантрациклина и 13-дезоксиантрациклина можно вводить так часто, как это необходимо. Фактический способ и порядок введения будет варьироваться в соответствии с конкретной лекарственной формой, композицией, комбинацией, смесью или препаратом, конкретным типом рака, подлежащим лечению, и конкретным пациентом, которого лечат.
Усиленное анти-клеточнопролиферативное действие комбинации 2-пирролинo-13-дезоксиантрациклина формулы X с 13-дезоксиантрациклином формулы Y по настоящему изобретению показано, в качестве примера, в следующем биологическом испытании, которое предназначено для иллюстрации, а не для ограничения настоящего изобретения.
Пример 4
Клеточную линию фибросаркомы, HT1080, использовали для измерения IC50 значений и IC10 значений (ингибирующая концентрация соединения, необходимая для ингибирования клеточного роста на 10%) Соединения IV и Соединения III, как описано в Примере 2. IC50 концентрация представляет собой терапевтическое количество соединения. IC10 представляет собой не-терапевтическое субэффективное количество соединения. Клетки пассировали и высевали при плотности 5000 клеток/лунка в 96-луночные планшеты и планшеты инкубировали в течение 24 часов. После инкубации среду заменяли и IC50 и IC10 значения соединения IV и соединения III измеряли после 48 часов инкубации. Затем измеряли IC50 значения для соединения IV в присутствии соединения III при IC10 концентрации и для соединения III в присутствии соединения IV при IC10 концентрации после 48 часов инкубации. После инкубации в каждую лунку добавляли 20мкМ 0,1% AlamarBlue в 1xPBS. Планшеты затем инкубировали еще в течение 24 часов. Планшеты считывали на считывающем устройстве для микропланшетов при возб./эм. 485/528.
IC50 и IC10 значения (микромолярные) соединения IV и соединения III, IC50 соединения IV в присутствии IC10 соединения III, и IC50 соединения III в присутствии IC10 соединения IV, в HT1080 клетках.
Соединение IV в 12 раз (12,5/1,01) более эффективно в присутствии нетерапевтического количества соединения III, а соединение III в 35 раз (63,7/1,78) более эффективно в присутствии нетерапевтического количества соединения IV. Эти результаты наглядно свидетельствуют о том, что соединения IV и III являются синергичными друг с другом. Этот результат является неожиданным, поскольку оба соединения являются антрациклинами, и, как ожидают, должны действовать по одному и тому же механизму, и поэтому в комбинации должны быть только аддитивными. То есть, специалист в данной области со средней квалификацией мог бы ожидать, что IC10 концентрации одного соединения будут иметь незначительный эффект или вообще никакого эффекта на активность другого соединения. Таким образом, комбинация 2-пирролинo-13-дезоксиантрациклинов формулы X с 13-дезоксиантрациклинами формулы Y обеспечивает улучшенную композицию с повышенной активностью и эффективностью по сравнению с соединениями, используемыми отдельно.
Синергетическое взаимодействие происходит, когда фармакологический эффект введения комбинации двух лекарственных средств больше, чем аддитивные эффекты этих двух лекарственных средств, вводимых раздельно. Например, предположим, что доза первого лекарственного средства для обеспечения 30% ответа составляет 100 единиц, а доза второго лекарственного средства для обеспечения 30% ответа составляет 10 единиц. Если 100 единиц первого лекарственного средства плюс 10 единиц второго лекарственного средства обеспечивают 60% ответ, тогда имеет место аддитивный эффект между этими двумя лекарственными средствами. Однако, если 100 единиц первого лекарственного средства плюс 10 единиц второго лекарственного средства обеспечивают 90% ответ, тогда имеет место синергетический или сверхаддитивный эффект между этими двумя лекарственными средствами. Если соединения взаимодействовали аддитивным образом, можно ожидать, что IC50 соединения IV уменьшится от 12,53 мкМ до 10 мкМ в присутствии соединения III при IC10 концентрации. Однако IC50 соединения IV уменьшилась до 1 мкМ. Подобным образом, можно ожидать, что IC50 соединения III уменьшится от 63,37 мкМ до 50 мкМ в присутствии соединения IV при IC10 концентрации. Однако IC50 соединения III уменьшилась до 1,78 мкМ. Таким образом, 2-пирролинo-13-дезоксиантрациклины формулы X и 13-дезоксиантрациклины формулы Y по настоящему изобретению действуют усиленным образом или синергетически друг с другом с обеспечением высокоактивных и эффективных композиций, комбинаций, смесей или препаратов для подавления роста раковых клеток.
В соответствии с настоящим изобретением, соединения по настоящему изобретению можно использовать отдельно или в подходящей ассоциации, а также можно использовать в комбинации с фармацевтически приемлемыми носителями и другими фармацевтически активными соединениями. Активное средство может присутствовать в фармацевтической композиции в любом подходящем количестве.
Фармацевтически приемлемые носители, описанные в настоящей заявке, например, носители, адъюванты, эксципиенты или разбавители, хорошо известны специалистам в данной области. Как правило, фармацевтически приемлемый носитель является химически инертным по отношению к активным соединениям и не имеет вредных побочных эффектов или токсичности в условиях использования. Фармацевтически приемлемые носители могут включать полимеры и полимерные матрицы.
Выбор носителя будет частично определяться конкретным способом, используемым для введения композиции. Соответственно, существует большое разнообразие подходящих лекарственных форм для фармацевтической композиции по настоящему изобретению. Следующие лекарственные формы для перорального, аэрозольного, парентерального, подкожного, внутривенного, интраартериального, внутримышечного, интраперитонеального, интратекального, ректального и вагинального введения являются лишь иллюстративными и никоим образом не ограничивающими.
Лекарственные формы, подходящие для перорального введения, могут включать (а) жидкие растворы, такие как эффективное количество соединения, растворенное в разбавителях, таких как вода, физиологический раствор или апельсиновый сок; (b) капсулы, саше, таблетки, таблетки для рассасывания и пастилки, каждая из которых содержит заранее определенное количество активного ингредиента в виде твердых частиц или гранул; (c) порошки; (d) суспензии в подходящей жидкости; и (e) подходящие эмульсии. Жидкие композиции могут включать разбавители, такие как вода, циклодекстрин, диметилсульфоксид и спирты, например, этанол, бензиловый спирт, пропиленгликоль, глицерин и полиэтиленовые спирты, включая полиэтиленгликоль, с добавлением или без добавления фармацевтически приемлемого поверхностно-активного вещества, суспендирующего агента или эмульгатора. Капсулы могут быть обычными желатиновыми капсулами с твердой или мягкой оболочкой, содержащими, например, поверхностно-активные вещества, смазывающие вещества и инертные наполнители, такие как лактоза, сахароза, фосфат кальция и кукурузный крахмал. Таблетированные формы могут включать одно или несколько из следующих веществ: лактоза, сахароза, маннит, кукурузный крахмал, картофельный крахмал, альгиновая кислота, микрокристаллическая целлюлоза, аравийская камедь, желатин, гуаровая камедь, коллоидный диоксид кремния, кроскармеллоза натрия, тальк, стеарат магния, стеарат кальция, стеарат цинка, стеариновая кислота и другие эксципиенты, красители, разбавители, буферные агенты, разрыхлители, увлажнители, консерванты, отдушки и фармакологически совместимые носители. Формы для рассасывания могут включать активный ингредиент во вкусоароматическом веществе, обычно сахарозе и аравийской камеди или трагаканте, а также пастилки, включающие активный ингредиент в инертной основе, такой как желатин и глицерин, или сахароза и аравийская камедь, эмульсии и гели, содержащие в дополнение к активному ингредиенту такие носители, которые известны в данной области.
Соединения по отдельности или в комбинации с другими подходящими компонентами могут быть сформулированы в аэрозольные композиции для введения путем ингаляции. Эти аэрозольные композиции могут быть помещены в приемлемые пропелленты под давлением, такие как дихлордифторметан, пропан и азот. Они также могут быть сформулированы в виде фармацевтических композиций для препаратов под нормальным давлением, например в небулайзере или распылителе.
Композиции, подходящие для парентерального введения, включают водные и неводные изотонические стерильные инъекционные растворы, которые могут содержать антиоксиданты, буферы, бактериостаты и растворенные вещества, которые делают композицию изотонической с кровью предполагаемого реципиента, а также водные и неводные стерильные суспензии, которые могут включать суспендирующие агенты, солюбилизаторы, загустители, стабилизаторы и консерванты. Соединение можно вводить в физиологически приемлемом разбавителе в фармацевтическом носителе, таком как стерильная жидкость или смесь жидкостей, включая воду, физиологический раствор, водный раствор декстрозы и растворы соответствующих сахаров, спирт, такой как этанол, изопропанол или гексадециловый спирт, гликоли, такие как пропиленгликоль или полиэтиленгликоль, такой как поли(этиленгликоль) 400, глицеринкетали, такие как 2,2-диметил-1,3-диоксолан-4-метанол, простые эфиры, масло, жирную кислоту, сложный эфир или глицерид жирной кислоты или ацетилированный глицерид жирной кислоты, с добавлением или без добавления фармацевтически приемлемого поверхностно-активного вещества, такого как мыло или детергент, суспендирующего агента, такого как пектин, карбомеры, метилцеллюлоза, гидроксипропилметилцеллюлоза или карбоксиметилцеллюлоза, или эмульгаторов и других фармацевтических адъювантов.
Масла, которые можно использовать в парентеральных композициях, включают нефтяные, животные, растительные или синтетические масла. Конкретные примеры масел включают арахисовое, соевое, кунжутное, хлопковое, кукурузное, оливковое, вазелиновое и минеральное масло. Подходящие жирные кислоты для использования в парентеральных композициях включают олеиновую кислоту, стеариновую кислоту и изостеариновую кислоту. Этилолеат и изопропилмиристат являются примерами подходящих сложных эфиров жирных кислот. Подходящие мыла для использования в парентеральных композициях включают соли жирных кислот и щелочных металлов, аммония и триэтаноламина, а подходящие детергенты включают (а) катионные детергенты, такие как, например, галогениды диметилдиалкиламмония и галогениды алкилпиридиния, (b) анионные детергенты, такие как, например, алкил-, арил- и олефин-сульфонаты, алкил-, олефин-, эфир- и моноглицерид-сульфаты и сульфосукцинаты, (c) неионные детергенты, такие как, например, оксиды жирных аминов, алканоламиды жирных кислот и полиоксиэтилен-полипропиленовые сополимеры, (d) амфотерные детергенты, такие как, например, алкил-β-аминопропионаты и четвертичные аммониевые соли 2-алкилимидазолина, и (е) их смеси.
Парентеральные композиции типично содержат от около 0,5% масс. до около 25% масс. активного ингредиента в растворе. В таких композициях можно использовать подходящие консерванты и буферы. Чтобы минимизировать или устранить раздражение в месте инъекции, такие композиции могут содержать одно или несколько неионных поверхностно-активных веществ, имеющих гидрофильно-липофильный баланс (ГЛБ) от около 12 до около 17. Количество поверхностно-активного вещества в таких композициях варьируется от около 5% до около 15% по массе. Подходящие поверхностно-активные вещества включают сложные эфиры полиэтиленсорбитана и жирных кислот, такие как сорбитанмоноолеат, и высокомолекулярные аддукты этиленоксида с гидрофобным основанием, образованные конденсацией пропиленоксида с пропиленгликолем.
Фармацевтически приемлемые эксципиенты также хорошо известны специалистам в данной области. Выбор эксципиента будет частично определяться конкретным соединением, а также конкретным способом, используемым для введения композиции. Соответственно, существует большое разнообразие подходящих составов фармацевтической композиции по настоящему изобретению. Следующие способы и эксципиенты являются просто иллюстративными и никоим образом не ограничивающими. Фармацевтически приемлемые эксципиенты предпочтительно не мешают действию активных ингредиентов и не вызывают неблагоприятных побочных эффектов. Подходящие носители и эксципиенты включают растворители, такие как вода, спирт и пропиленгликоль, твердые абсорбенты и разбавители, поверхностно-активные вещества, суспендирующий агент, связующие для таблетирования, смазывающие вещества, отдушки и красители.
Композиции могут быть представлены в герметично закрытых однодозовых или многодозовых контейнерах, таких как ампулы и флаконы, и могут храниться в высушенном замораживанием (лиофилизированном) состоянии, требующем только добавления стерильного жидкого эксципиента, например воды для инъекций, непосредственно перед использованием. Экстемпоральные инъекционные растворы и суспензии можно получить из стерильных порошков, гранул и таблеток. Требования к эффективным фармацевтическим носителям для композиций для инъекций хорошо известны специалистам в данной области. См. Pharmaceutics and Pharmacy Practice, J.B. Lippincott Co., Philadelphia, PA, Banker and Chalmers, Eds., 238-250 (1982) и ASHP Handbook on Injectable Drugs, Toissel, 4th ed., 622-630 (1986).
Композиции, подходящие для местного применения, включают таблетки для рассасывания, включающие активный ингредиент во вкусоароматическом веществе, обычно сахарозе и аравийской камеди или трагаканте; пастилки, включающие активный ингредиент в инертной основе, такой как желатин и глицерин, или сахароза и аравийская камедь; и жидкости для полоскания рта, включающие активный ингредиент в подходящем жидком носителе; а также кремы, эмульсии и гели, содержащие, помимо активного ингредиента, такие носители, которые известны в данной области.
Кроме того, композиции, подходящие для ректального введения, могут быть представлены в виде суппозиториев путем смешивания с различными основами, такими как эмульгирующие основы или водорастворимые основы. Композиции, подходящие для вагинального введения, могут быть представлены в виде пессариев, тампонов, кремов, гелей, паст, пен или спреев, содержащих, в дополнение к активному ингредиенту, такие носители, которые известны в данной области техники как подходящие.
Специалистам в данной области должно быть понятно, что подходящие способы экзогенного введения соединения по настоящему изобретению животному являются доступными, и, хотя для введения конкретного соединения можно использовать несколько путей введения, конкретный путь может обеспечить более немедленный и более эффективный ответ, чем другой путь.
Иллюстративные варианты осуществления настоящего изобретения включают:
Вариант осуществления A. Соединение, представленное формулой:
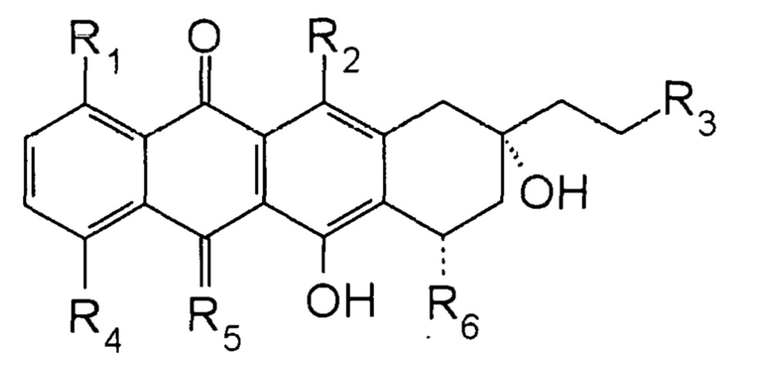
где:
каждый R1, R2 и R3 независимо представляет собой H или OH;
R4 выбран из группы, состоящей из H, OH, алкила и O-алкила;
R5 представляет собой O или NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин;
его фармацевтически приемлемые соли, его дейтерированная форма, его пролекарство, его изомер, его сольват и их смеси.
Вариант осуществления B. Соединение варианта осуществления A, где указанное соединение представляет собой производное антрациклина, выбранное из группы, состоящей из 2-пирролинo-13-дезоксидоксорубицина, 2-пирролинo-13-дезоксидаунорубицина, 2-пирролинo-13-дезоксиэпирубицина, 2-пирролинo-13-дезоксикарминомицина и 2-пирролинo-13-дезоксиидарубицина и их 5-имино аналогов.
Вариант осуществления C. Фармацевтическая композиция, включающая соединение варианта осуществления A или B и фармацевтически приемлемый носитель или эксципиент.
Вариант осуществления D. Способ подавления роста клеток, включающий введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества соединения, включающего:
2-пирролинo-13-дезоксиантрациклин, имеющий формулу:
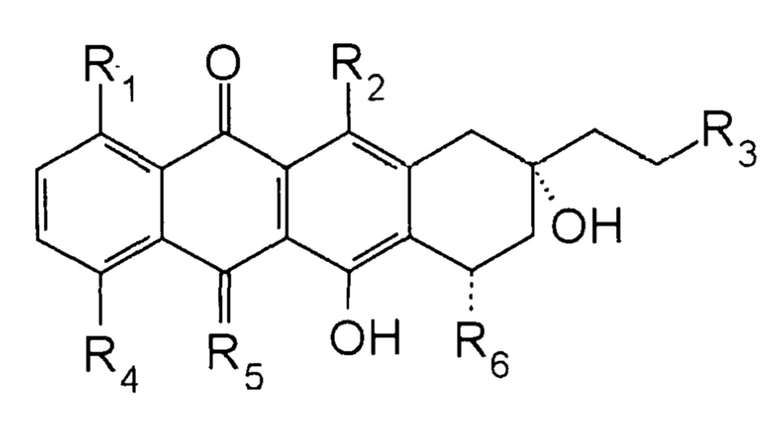
где:
каждый R1, R2 и R3 независимо представляет собой H или OH;
R4 выбран из группы, состоящей из H, OH, алкила и O-алкила;
R5 представляет собой O или NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин,
его фармацевтически приемлемой соли, его дейтерированной формы, его пролекарства, его изомера, его сольвата и их смесей.
Вариант осуществления E. Способ варианта осуществления D, где указанное соединение представляет собой производное антрациклина, выбранное из группы, состоящей из 2-пирролинo-13-дезоксидоксорубицина, 2-пирролинo-13-дезоксидаунорубицина, 2-пирролинo-13-дезоксиэпирубицина, 2-пирролинo-13-дезоксикарминомицина и 2-пирролинo-13-дезоксиидарубицина и их 5-имино аналогов.
Вариант осуществления F. Терапевтически эффективное количество синергетического комбинированного препарата, включающего первое соединение и второе соединение, где: первое соединение представляет собой 2-пирролинo-13-дезоксиантрациклин, имеющий формулу:
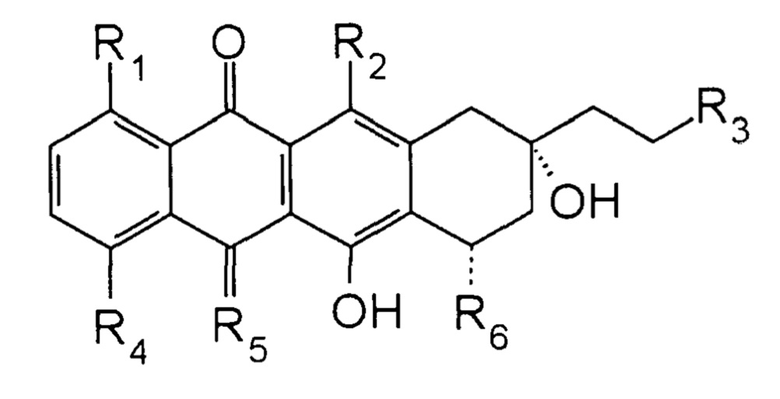
где:
каждый R1, R2 и R3 независимо представляет собой H или OH;
R4 выбран из группы, состоящей из H, OH, алкила и O-алкила;
R5 представляет собой O или NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин; его фармацевтически приемлемую соль, его дейтерированную форму, его пролекарство, его изомер, его сольват и их смеси; и
второе соединение представляет собой 13-дезоксиантрациклин, имеющий формулу:
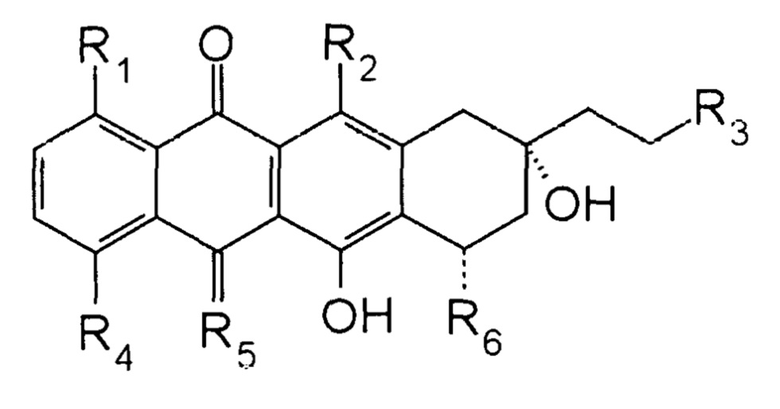
где
каждый из R1, R2 и R3 независимо выбран из группы, состоящей из H и OH;
R4 выбран из группы, состоящей из H, OH, алкила и O-алкила;
R5 выбран из группы, состоящей из O и NH; и
R6 представляет собой сахарный компонент; его фармацевтически приемлемую соль, его дейтерированную форму, его пролекарство, его изомер, его сольват и их смеси; и
где указанное терапевтически эффективное количество подавляет рост клеток.
Вариант осуществления G. Синергетический комбинированный препарат варианта осуществления F, где указанное первое соединение представляет собой производное антрациклина, выбранное из группы, состоящей из 2-пирролинo-13-дезоксидоксорубицина, 2-пирролинo-13-дезоксидаунорубицина, 2-пирролинo-13-дезоксиэпирубицина, 2-пирролинo-13-дезоксикарминомицина и 2-пирролинo-13-дезоксиидарубицина и их 5-имино аналогов, и указанное второе соединение представляет собой производное антрациклина, выбранное из группы, состоящей из 13-дезоксидоксорубицина, 13-дезоксидаунорубицина, 13-дезоксиэпирубицина, 13-дезоксикарминомицина, 13-дезоксиидарубицина, 13-дезоксианнамицина и 13-дезоксиамрубицина и их 5-имино аналогов.
Вариант осуществления H. Фармацевтическая композиция, включающая синергетический комбинированный препарат варианта осуществления F или G и фармацевтически приемлемый носитель или эксципиент.
Вариант осуществления I. Способ подавления роста клеток с использованием синергетического комбинированного препарата, содержащего первое соединение и второе соединение, включающий введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества указанного синергетического комбинированного препарата, где указанное первое соединение представляет собой 2-пирролинo-13-дезоксиантрациклин, имеющий формулу:
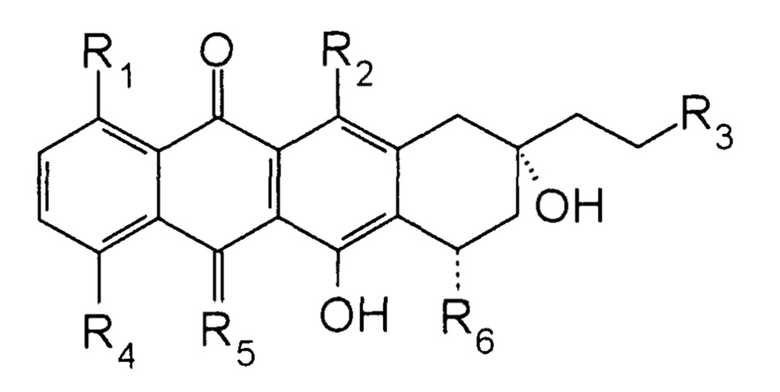
где:
каждый R1, R2 и R3 независимо представляет собой H или OH;
R4 выбран из группы, состоящей из H, OH, алкила и O-алкила;
R5 представляет собой O или NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин; его фармацевтически приемлемую соль, его дейтерированные формы, его пролекарство, его изомер, его сольват и их смеси; и
указанное второе соединение представляет собой 13-дезоксиантрациклин, имеющий формулу:
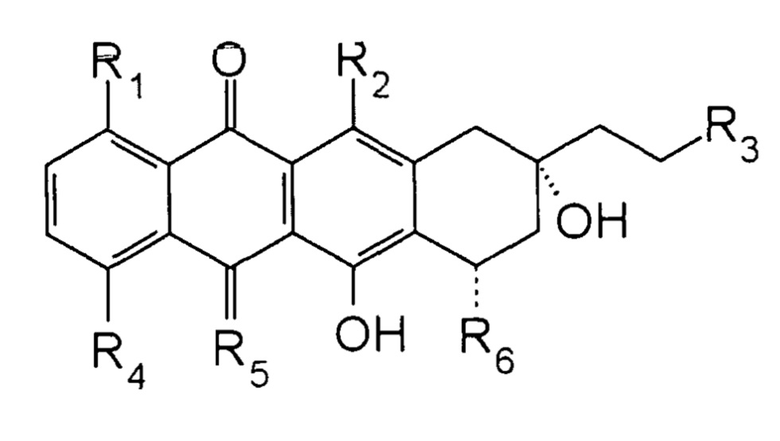
где
каждый из R1, R2 и R3 независимо выбран из группы, состоящей из H и OH;
R4 выбран из группы, состоящей из H, OH, алкила и O-алкила;
R5 выбран из группы, состоящей из O и NH; и
R6 представляет собой сахарный компонент; его фармацевтически приемлемую соль, его дейтерированную форму, его пролекарство, его изомер, его сольват и их смеси; и
где указанное терапевтически эффективное количество подавляет рост клеток.
Вариант осуществления J. Способ варианта осуществления I, где указанное первое соединение представляет собой производное антрациклина, выбранное из группы, состоящей из 2-пирролинo-13-дезоксидоксорубицина, 2-пирролинo-13-дезоксидаунорубицина, 2-пирролинo-13-дезоксиэпирубицина, 2-пирролинo-13-дезоксикарминомицина и 2-пирролинo-13-дезоксиидарубицина и их 5-имино аналогов, а второе соединение представляет собой производное антрациклина, выбранное из группы, состоящей из 13-дезоксидоксорубицина, 13-дезоксидаунорубицина, 13-дезоксиэпирубицина, 13-дезоксикарминомицина, 13-дезоксиидарубицина, 13-дезоксианнамицина и 13-дезоксиамрубицина и их 5-имино аналогов.
Вариант осуществления K. Синергетический комбинированный препарат варианта осуществления F или G, где указанное второе соединение присутствует в количестве, которое меньше, чем его терапевтически эффективное количество.
Вариант осуществления L. Синергетический комбинированный препарат варианта осуществления K, где массовое отношение второго соединения к первому компоненту составляет от около 0,005 до около 0,10:1.
Вариант осуществления M. Синергетический комбинированный препарат варианта осуществления K, где массовое отношение второго соединения к первому компоненту составляет от около 0,01 до около 0,10:1.
Вариант осуществления N. Синергетический комбинированный препарат варианта осуществления F или G, где указанное первое соединение присутствует в количестве, которое меньше, чем его терапевтически эффективное количество.
Вариант осуществления O. Синергетический комбинированный препарат варианта осуществления N, где массовое отношение первого соединения к второму компоненту составляет от около 0,005 до около 0,10:1.
Вариант осуществления P. Синергетический комбинированный препарат варианта осуществления N, где массовое отношение первого соединения к второму компоненту составляет от около 0,01 до около 0,10:1.
Вариант осуществления Q. Способ варианта осуществления I или J, где указанное второе соединение вводят в количестве, которое меньше, чем его терапевтически эффективное количество.
Вариант осуществления R. Способ варианта осуществления Q, где массовое отношение второго соединения к первому компоненту составляет от около 0,005 до около 0,10:1.
Вариант осуществления S. Способ варианта осуществления Q, где массовое отношение второго соединения к первому компоненту составляет от около 0,01 до около 0,10:1.
Вариант осуществления T. Способ варианта осуществления I или J, где указанное второе соединение вводят в количестве, которое меньше, чем его терапевтически эффективное количество.
Вариант осуществления U. Способ варианта осуществления T, где массовое отношение первого соединения к второму компоненту составляет от около 0,005 до около 0,10:1.
Вариант осуществления V. Способ варианта осуществления Q, где массовое отношение первого соединения к второму компоненту составляет от около 0,01 до около 0,10:1.
Термин “включающий” (и его грамматические варианты) в контексте настоящей заявки используется в инклюзивном смысле “содержащий” или “включающий в себя”, а не в исключающем смысле “состоящий только из”. Термины, определяемые артиклями “a”, “an” и “the”, в контексте настоящей заявки следует понимать как охватывающие как множественное, так и единственное число, если не указано иное.
Вышеприведенное описание иллюстрирует и описывает настоящее изобретение. Кроме того, раскрытие представляет и описывает только предпочтительные варианты осуществления, но, как указано выше, следует понимать, что предпочтительные варианты осуществления могут быть образованы в различных других комбинациях, модификациях и условиях, и возможны их изменения или модификации в пределах объема концепций изобретения, представленных в настоящей заявке, в соответствии с приведенными выше указаниями и/или навыками или знаниями в соответствующей области техники. Варианты осуществления, описанные выше, также предназначены для объяснения лучших способов, известных заявителю, и для того, чтобы дать возможность другим специалистам в данной области техники использовать изобретение в таких, либо других, вариантах осуществления и с различными модификациями, необходимыми для его конкретных применений или использований. Соответственно, описание не предназначено для ограничения изобретения формой, раскрытой в настоящей заявке. Также предполагается, что прилагаемая формула изобретения должна рассматриваться как включающая альтернативные варианты осуществления.
Все публикации и патентные заявки, процитированные в настоящем описании, включены в настоящую заявку посредством ссылки и для любых и всех целей, как если бы каждая отдельная публикация или патентная заявка была специально и индивидуально указана как включенная посредством ссылки. В случае несоответствия между настоящим раскрытием и любыми публикациями или патентной заявкой, включенными в настоящую заявку посредством ссылки, преимущество имеет настоящее раскрытие.
Настоящее изобретение относится к соединению формулы
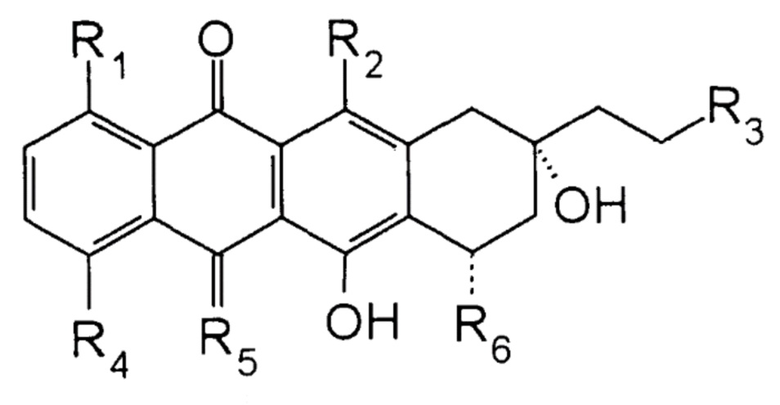 ,
,
где R1 представляет собой H; R2 и R3 представляют собой OH; R4 представляет собой O-С1-6алкил; R5 представляет собой NH и R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин, которое используется для подавления роста клеток фибросаркомы. Также изобретение относится к фармацевтической композиции и к синергетическому комбинированному препарату, содержащему данное соединение, а также к способу подавления роста клеток фибросаркомы. Технический результат - обеспечение антрациклинового соединения, содержащего 2-пирролинo-группу, которое повышает противораковую активность, сохраняя при этом хороший профиль безопасности. 8 н. и 12 з.п. ф-лы, 4 табл., 4 пр.
1. Соединение, представленное формулой
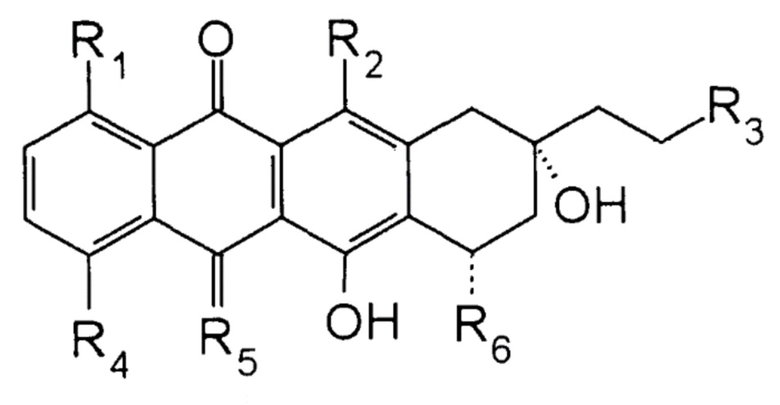
где R1 представляет собой H;
R2 и R3 представляют собой OH;
R4 представляет собой O-С1-6алкил;
R5 представляет собой NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин.
2. Соединение по п. 1, где указанное соединение представляет собой 5-иминоаналог производного 2-пирролинo-13-дезоксиэпирубицина.
3. Фармацевтическая композиция для подавления роста клеток фибросаркомы, содержащая эффективное количество соединения по п. 1 и фармацевтически приемлемый носитель или эксципиент.
4. Фармацевтическая композиция для подавления роста клеток фибросаркомы, содержащая эффективное количество соединения по п. 2 и фармацевтически приемлемый носитель или эксципиент.
5. Способ подавления роста клеток фибросаркомы, включающий введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества соединения, включающего:
2-пирролинo-13-дезоксиантрациклин, где указанный 2-пирролинo-13-дезоксиантрациклин представляет собой соединение формулы
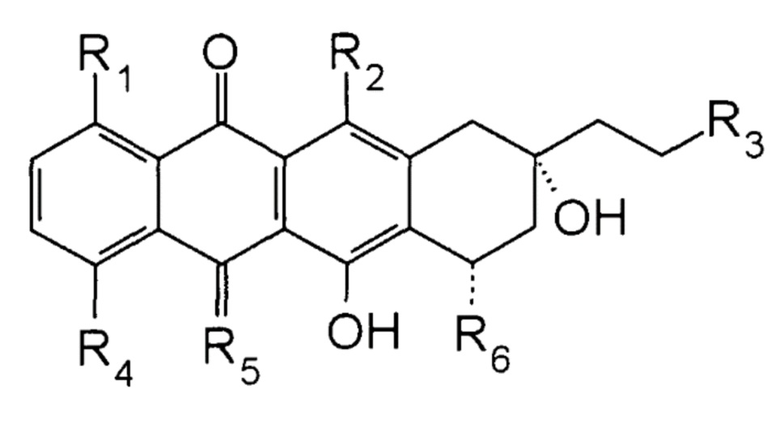
где R1 представляет собой H;
R2 и R3 представляют собой OH;
R4 представляет собой O-С1-6алкил;
R5 представляет собой NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин.
6. Способ по п. 5, где указанное соединение представляет собой 5-иминоаналог производного 2-пирролинo-13-дезоксиэпирубицина.
7. Синергетический комбинированный препарат в терапевтически эффективном количестве для подавления роста клеток фибросаркомы, включающий первое соединение и второе соединение, где первое соединение представляет собой 2-пирролинo-13-дезоксиантрациклин, имеющий формулу
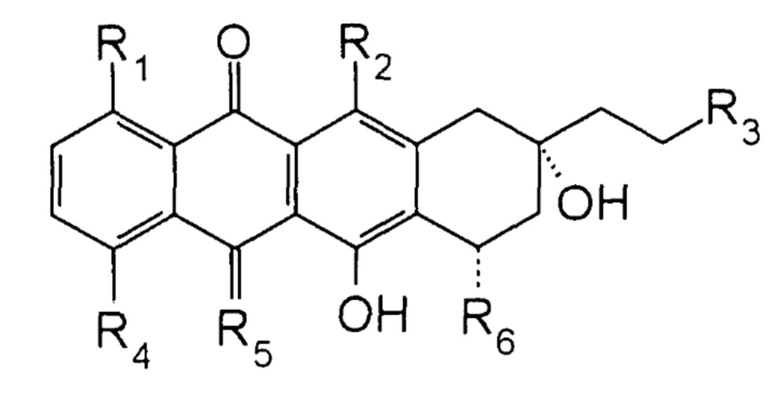 ,
,
где R1 представляет собой H;
R2 и R3 представляют собой OH;
R4 представляет собой O-С1-6алкил;
R5 представляет собой NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин; и
второе соединение представляет собой 13-дезоксиантрациклин, имеющий формулу
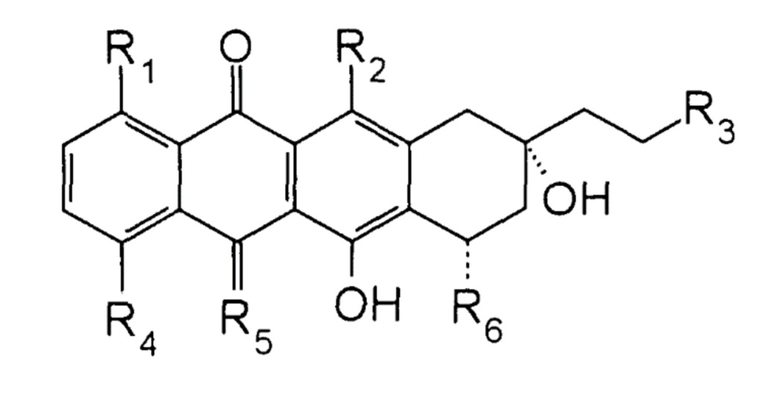 ,
,
где R1 представляет собой H;
R2 и R3 представляют собой OH;
R4 представляет собой O-С1-6алкил;
R5 представляет собой NH; и
R6 представляет собой 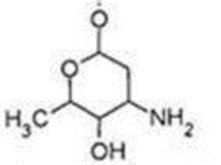 ; и
; и
где указанное терапевтически эффективное количество подавляет рост клеток.
8. Синергетический комбинированный препарат по п. 7, где указанное первое соединение представляет собой 5-иминоаналог производного 2-пирролинo-13-дезоксиэпирубицина, а указанное второе соединение представляет собой 5-иминоаналог производного 13-дезоксиэпирубицина.
9. Фармацевтическая композиция для подавления роста клеток фибросаркомы, содержащая эффективное количество синергетического комбинированного препарата по п. 7 и фармацевтически приемлемый носитель или эксципиент.
10. Фармацевтическая композиция для подавления роста клеток фибросаркомы, содержащая эффективное количество синергетического комбинированного препарата по п. 8 и фармацевтически приемлемый носитель или эксципиент.
11. Способ подавления роста клеток фибросаркомы с использованием синергетического комбинированного препарата, содержащего первое соединение и второе соединение, включающий введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества указанного синергетического комбинированного препарата, где указанное первое соединение представляет собой 2-пирролинo-13-дезоксиантрациклин, имеющий формулу
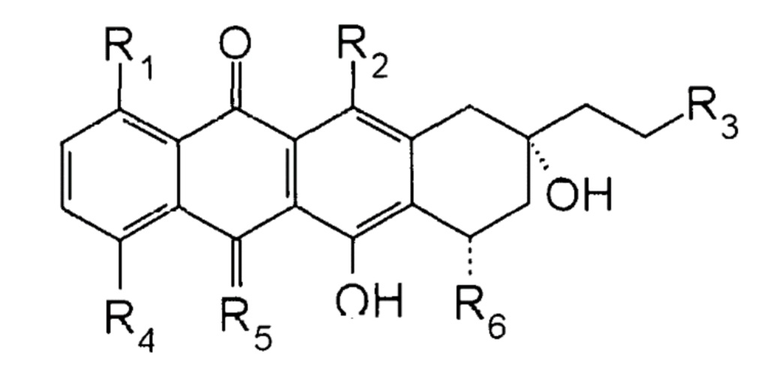 ,
,
где R1 представляет собой H;
R2 и R3 представляют собой OH;
R4 представляет собой O-С1-6алкил;
R5 представляет собой NH; и
R6 представляет собой 2-пирролинo-даунозамин или 2-пирролинo-эпидаунозамин; и
указанное второе соединение представляет собой 13-дезоксиантрациклин, имеющий формулу
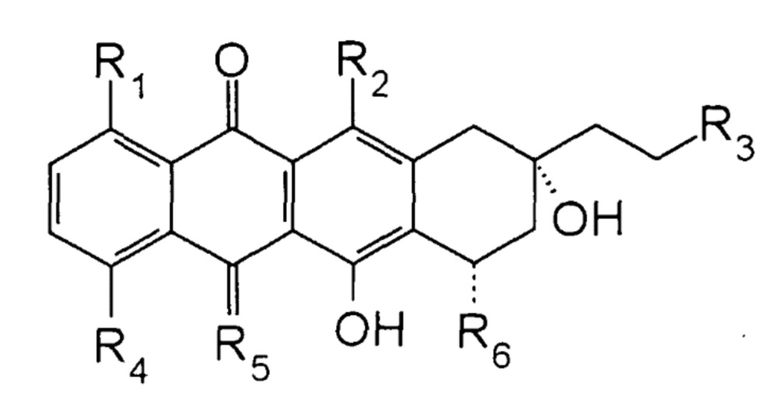
где
R1 представляет собой H;
R2 и R3 представляют собой OH;
R4 представляет собой O-С1-6алкил;
R5 представляет собой NH; и
R6 представляет собой  ; и
; и
где указанное терапевтически эффективное количество подавляет рост клеток.
12. Способ по п. 11, где указанное первое соединение представляет собой 5-иминоаналог производного 2-пирролинo-13-дезоксиэпирубицина, а второе соединение представляет собой 5-иминоаналог производного 13-дезоксиэпирубицина.
13. Синергетический комбинированный препарат по п. 7, где указанное второе соединение присутствует в количестве, которое меньше, чем его терапевтически эффективное количество.
14. Синергетический комбинированный препарат по п. 13, где массовое отношение второго соединения к первому соединению составляет от 0,005 до 0,10:1.
15. Синергетический комбинированный препарат по п. 7, где указанное первое соединение присутствует в количестве, которое меньше, чем его терапевтически эффективное количество.
16. Синергетический комбинированный препарат по п. 15, где массовое отношение первого соединения к второму соединению составляет от 0,005 до 0,10:1.
17. Способ по п. 11, где указанное второе соединение вводят в количестве, которое меньше, чем его терапевтически эффективное количество.
18. Способ по п. 17, где массовое отношение второго соединения к первому соединению составляет от 0,005 до 0,10:1.
19. Способ по п. 11, где указанное второе соединение вводят в количестве, которое меньше, чем его терапевтически эффективное количество.
20. Способ по п. 19, где массовое отношение первого соединения к второму соединению составляет от 0,005 до 0,10:1.
| US 7776832 B2, 17.08.2010 | |||
| Nagy, A | |||
| et | |||
| al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Proceedings of the National Academy of Sciences, 1996, 93(14), 7269-7273 | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| WO 1999045015 A1, 10.09.1999 | |||
| Твердый газогенерирующий материал для электрических выключателей, предохранителей и разрядников | 1945 |
|
SU66344A1 |
Авторы
Даты
2023-09-18—Публикация
2018-02-16—Подача