Настоящее изобретение относится к области клинической диагностики, а именно к способам определения типа диабетической фетопатии плода.
Сахарный диабет различного типа (1 тип, 2 тип, гестационный) во время беременности сопровождается различными акушерскими и перинатальными осложнениями, среди которых на первом месте стоит диабетическая фетопатия (ДФ). Так, в 36.5% гипергликемия матери приводит к рождению детей с ДФ [Urano-Tashiro Y, Sasaki Н, Sugawara-Kawasaki М, et al. Implication of Akt-dependent Prp19 alpha/14-3-3beta/Cdc5L complex formation in neuronal differentiation. J. Neurosci. Res. 2010; 88 (13): 2787-2797; doi:10.1002/jnr.22455]. Фетопатию в настоящее время диагностируют с помощью ультразвукового исследования во время беременности. Однако такая диагностика происходит на поздних сроках беременности (после 30-й недели беременности). Выявляются фенотипические признаки фетопатии, но более точная диагностика возможна только после родов. [www.amp.pharm.mssm.edu/Harmonizome/gene_set/CDC5L/Pathway+Commons+Protein-Protein+Interactions], [https://www.proteinatlas.org/ENSG00000096401-CDC5L].
Новорожденные от матерей с сахарным диабетом могут страдать нарушениями дыхания, метаболическим синдромом, имеют риск развития ожирения [https://amp.pharm.mssm.edu/archs4/gene/CDC5L]. Растущая популяция младенцев с метаболическим синдромом вызывает серьезную озабоченность по поводу риска развития у них сердечно-сосудистых заболеваний, которые могут дебютировать уже в подростковом возрасте [Tang L, Liu L, Li G, Jiang P, Wang Y, Li J. Expression Profiles of Long Noncoding RNAs in Intranasal LPS-Mediated Alzheimer's Disease Model in Mice. Biomed. Res. Int. 2019; 2019: 9642589; doi:10.1155/2019/9642589]. Наиболее распространенным признаком фетопатии является макросомия, которая является ответом на материнский диабет и может рассматриваться как очень ценный предиктор более поздней непереносимости глюкозы и возрастающего риска неправильного развития плода. До 45% младенцев, рожденных от матерей с диабетом, имеют макросомию, которая почти в 3 раза выше, чем у нормогликемических пациентов [Minocha R, Popova V, Kopytova D, et al. Mud2 functions in transcription by recruiting the Prp19 and TREX complexes to transcribed genes. Nucleic Acids Res. 2018; 46 (18): 9749-9763; doi:10.1093/nar/gky640].
Вырабатываемые в жировой ткани адипонектин, TNF-β, IL-6, IL-10 и лептин влияют на чувствительность беременных к инсулину [Mohammad I, Nousiainen K, Bhosale SD, et al. Quantitative proteomic characterization and comparison of T helper 17 and induced regulatory T cells. PLoS Biol. 2018; 16 (5): e2004194; doi:10.1371/journal.pbio.2004194], [[8] Ellison EM, Bradley-Whitman MA, Lovell MA. Single-Base Resolution Mapping of 5-Hydroxymethylcytosine Modifications in Hippocampus of Alzheimer's Disease Subjects. J. Mol. Neurosci. 2017; 63 (2): 185-197; doi:10.1007/s12031-017-0969-у]. При нарушении гликемического контроля у матери и повышенной инсулинорезистентности (ИР) уровень циркулирующей глюкозы повышается. Важным является тот факт, что чрезмерный уровень материнской глюкозы может проникать через плаценту, в отличие от материнского инсулина, который не проникает трансплацентарно. Начиная со второго триместра поджелудочная железа плода уже способна секретировать инсулин. Следовательно, комбинированное состояние материнской гипергликемии и избыточной секреции инсулина у плода связано с риском увеличения образования жировой ткани, что приводит к макросомии и нарушению морфогенеза [Minocha R, Popova V, Kopytova D, et al. Mud2 functions in transcription by recruiting the Prp19 and TREX complexes to transcribed genes. Nucleic Acids Res. 2018; 46(18): 9749-9763; doi:10.1093/nar/gky640].
Пороки сердца являются наиболее частым проявлением фетопатии с распространенностью до 12% [ D, Denegri М, Biggiogera М, Ajuh Р, Lamond AIA.I. Direct interaction between hnRNP-M and CDC5L/PLRG1 proteins affects alternative splice site choice. EMBO Rep. 2010; 11 (6): 445-451; doi: 10.103 8/embor.2010.64]. Имеются данные, свидетельствующие о том, что именно повышение ИР у матери и высокий уровень глюкозы в основном ответственны за неправильную дифференцировку кардиомиоцитов и порокиформированию пороков развития сердца [Kleinridders A, Pogoda НМ, Irlenbusch S, et al. PLRG1 is an essential regulator of cell proliferation and apoptosis during vertebrate development and tissue homeostasis. Mol Cell Biol. 2009; 29 (11): 3173-3185; doi: 10.1128/MCB.01807-08]. Симптомы гипертрофической кардиомиопатии, проявляющиеся в асимметричном увеличении перегородки с непропорционально гипертрофической перегородкой, обычно обнаруживались у 12,1% младенцев, страдающих новорожденных, матери которых страдают диабетом матери [Yang Н, Jin X, Kei LamKeiLam CW, Yan SK. Oxidative stress and diabetes mellitus. Clin Chem Lab Med. 2011; 49 (11): 1773-1782; doi: 10.1515/CCLM.2011.250].
D, Denegri М, Biggiogera М, Ajuh Р, Lamond AIA.I. Direct interaction between hnRNP-M and CDC5L/PLRG1 proteins affects alternative splice site choice. EMBO Rep. 2010; 11 (6): 445-451; doi: 10.103 8/embor.2010.64]. Имеются данные, свидетельствующие о том, что именно повышение ИР у матери и высокий уровень глюкозы в основном ответственны за неправильную дифференцировку кардиомиоцитов и порокиформированию пороков развития сердца [Kleinridders A, Pogoda НМ, Irlenbusch S, et al. PLRG1 is an essential regulator of cell proliferation and apoptosis during vertebrate development and tissue homeostasis. Mol Cell Biol. 2009; 29 (11): 3173-3185; doi: 10.1128/MCB.01807-08]. Симптомы гипертрофической кардиомиопатии, проявляющиеся в асимметричном увеличении перегородки с непропорционально гипертрофической перегородкой, обычно обнаруживались у 12,1% младенцев, страдающих новорожденных, матери которых страдают диабетом матери [Yang Н, Jin X, Kei LamKeiLam CW, Yan SK. Oxidative stress and diabetes mellitus. Clin Chem Lab Med. 2011; 49 (11): 1773-1782; doi: 10.1515/CCLM.2011.250].
На формирование нервной трубки также сильно влияет выраженность гипергликемии матери за счет прямого влияния на регуляцию с большой вариабельностью экспрессии эмбриональных генов, в частности, тех, которые участвуют в передаче сигналов Wnt- и TGF-β [Wright Е Jr, Seism-Bacon JL, Glass LC. Oxidative stress in type 2 diabetes: the role of fasting and postprandial glycaemia. Int J Clin Pract. 2006; 60 (3): 308-314; doi:10.1111/j.1368-5031.2006.00825.x]. Недавние исследования также показали, что этиология дефектов нервной трубки у новорожденных от матерей с диабетом включает повышенные уровни СОД (супероксиддисмутазы), ингибирование пентозофосфатного пути и расширенный окислительный стресс [Santilli F, Cipollone F, Mezzetti A, Chiarelli F. The role of nitric oxide in the development of diabetic angiopathy. Horm. Metab. Res. 2004; 36 (5): 319-335; doi: 10.1055/s-2004-814489], [https://amp.pharm.mssm.edu/archs4/gene/DPF3#tissueexpression].
Как проявление ДФ, также часто встречается гепатомегалия, которая тесно связана с макросомией. [Cui Н, Schlesinger J, Schoenhals S, et al. Phosphorylation of the chromatin remodeling factor DPF3a induces cardiac hypertrophy through releasing HEY repressors from DNA. Nucleic Acids Res. 2016; 44 (6): 2538-2553. doi:10.1093/nar/gkv1244]. Существует предположение, что HbA1c имеет большое прогностическое значение для мониторинга риска гепатомегалии, однако этот индикатор нельзя использовать изолированно [Liu Н, Luo Y, Li S, Wang S, Wang N, Jin X. Expression profiles of HA117 and its neighboring gene DPF3 in different colon segments of Hirschsprung's disease. Int J Clin. Exp. Pathol. 2014; 7 (7): 3966-3974. Published 2014 Jun 15]. Ультразвуковое исследование по-прежнему является самым надежным инструментальным методом определения гепатомегалии плода [Hoyal CR, Kammerer S, Roth RB, et al. Genetic polymorphisms in DPF3 associated with risk of breast cancer and lymph node metastases. J. Carcinog. 2005; 4: 13. Published 2005 Aug 19. doi: 10.1186/1477-3163-4-13].
Во втором и третьем триместрах беременности при динамическом ультразвуковом исследовании (УЗИ) можно зарегистрировать так называемый синдром опережающего развития плода, что является следствием развития гиперинсулинемии. В таком случае при УЗИ основным показателем является увеличение размеров плода с опережением реального срока на 2 недели, многоводие, отечность тканей и диспропорция размеров плода. Признаки ДФ при исследовании УЗИ, при котором особое внимание уделяется таким признаком, как кардиопатия, гепатоспленомегалия, двухконтурность головки, отек и утолщение подкожно-жирового слоя, могут быть показателями к инсулинотерапии. При диагностике фетопатии также учитываются показатели глюкозы в крови матери, результаты определения инсулина. В связи с этим постоянный динамический контроль уровня глюкозы в течение всего периода гестации является основным требованием для контроля риска развития фетопатии в соответствие с рекомендациями ВОЗ от 2016 года. Во многих случаях указанный способ не позволяет выявить тип формирующейся фетопатии, а значит, и провести эффективную терапию. Это приводит к осложнениям развития в постнатальном периоде.
Из уровня техники известен способ выявления диабетической фетопатии плода, включающий:
- забор образца крови матери;
- пробоподготовку образца крови матери с получением аналита;
- определение содержания по меньшей мере одного маркера диабетической фетопатии плода, выбранного из группы, состоящей из альфа-1-микроглобулина/предшественника бикунина (АМВР), аполипопротеина А-II, аполипопротеина В-100, аполипопротеина С-III, фактора комплемента Н, протромбина, кининогена-1, альфа-1-кислого гликопротеина, плазминогена, ингибитора интер-альфа-трипсина тяжелая цепь H1 и витронектина, в аналите;
- определение общего содержания белков в аналите;
- оценку доли по меньшей мере одного маркера диабетической фетопатии плода от общего содержания белков в аналите, где в случае, если: значение относительного содержания альфа-1-микроглобулина/предшественника бикунина (АМВР) составляет не более 0,3% от общего содержания белков в аналите и/или значение относительного содержания аполипопротеина А-II составляет не менее 4,6% от общего содержания белков в аналите и/или значение относительного содержания аполипопротеина В-100 составляет не менее 0,14% от общего содержания белков в аналите и/или значение относительного содержания аполипопротеина С-III составляет от 2,7 до 3,5% от общего содержания белков в аналите и/или значение относительного содержания фактора комплемента Н составляет не менее 0,25% от общего содержания белков в аналите и/или значение относительного содержания протромбина составляет не менее 0,48% от общего содержания белков в аналите и/или значение относительного содержания кининогена-1 составляет от 0,43 до 0,47% от общего содержания белков в аналите и/или значение относительного содержания альфа-1-кислого гликопротеина составляет от 1,30 до 1,83% от общего содержания белков в аналите и/или значение относительного содержания плазминогена составляет от 0,35 до 0,42% от общего содержания белков в аналите и/или значение относительного содержания ингибитора интер-альфа-трипсина тяжелая цепь H1 составляет не менее 0,63% от общего содержания белков в аналите и/или значение относительного содержания витронектина составляет не более 0,48% от общего содержания белков в аналите, определяют высокий риск развития фетопатии у плода [патент РФ RU 2742801]. Однако предложенный способ не позволяет выявлять тип фетопатии плода.
Также из уровня техники известен способ выявления диабетической фетопатии плода, включающий:
- определение типа сахарного диабета у матери;
- забор образца крови матери;
- пробоподготовку образца крови матери с получением аналита;
- определение значения концентрации по меньшей мере одного маркера диабетической фетопатии плода в аналите, при этом в качестве маркера диабетической фетопатии плода в аналите используют белок, выбранный из группы, состоящей из СЕАСАМ1, и/или CNDP1, и/или CRP;
- сравнение полученного значения концентрации маркера ДФ плода в аналите с контрольным значением, при этом фетопатия плода при диабете первого типа матери выявляется при значении концентрации маркера ДФ плода CEACAM1 в аналите не более контрольного значения 339 нг/дл, при этом фетопатия плода при диабете второго типа матери выявляется при значении концентрации маркера ДФ плода СЕАСАМ1 в аналите не более контрольного значения 94 нг/дл, при этом фетопатия плода при гестационном сахарном диабете матери выявляется при значении концентрации маркера диабетической фетопатии плода CEACAM1 в аналите не более контрольного значения 132 нг/дл, при этом фетопатия плода при диабете первого типа матери выявляется при значении концентрации маркера ДФ плода CNDP1 в аналите не менее контрольного значения 28 нг/мл, при этом фетопатия плода при диабете второго типа матери выявляется при значении концентрации маркера ДФ плода CNDP1 в аналите не менее контрольного значения 35 нг/мл, при этом фетопатия плода при гестационном сахарном диабете матери выявляется при значении концентрации маркера ДФ плода CNDP1 в аналите не менее контрольного значения 43 нг/мл, при этом фетопатия плода при гестационном сахарном диабете матери выявляется при значении концентрации маркера ДФ плода CRP в аналите не менее контрольного значения 4 мкг/мл [патент РФ RU 2770117]. Однако предложенный способ также не позволяет выявлять тип фетопатии плода.
Из уровня техники известен метод иммуноферментного анализа (ИФА). ИФА является одним из наиболее активно развивающихся направлений химической энзимологии как в нашей стране, так и за рубежом. Это обусловлено тем, что в ИФА уникальная специфичность иммунохимического анализа сочетается с высокой чувствительностью детекции ферментативной метки. В патентной и научной литературе появляется все больше сведений о рекордных пределах обнаружения веществ данным методом (вплоть до 10-21 моль в образце). Высокие результаты достигаются благодаря использованию неограниченных возможностей ферментов - биокатализаторов, которые позволяют создавать каскадные системы усиления различных химических сигналов. Высокая стабильность реагентов, простота методов регистрации и многие другие достоинства метода ИФА способствовали его широкому внедрению в различные области медицины, сельское хозяйство, биологическую промышленность, охрану окружающей среды, а также в научные исследования. Применение ИФА в различных областях научной и практической деятельности ставит перед исследователем задачу: освоить основные приемы, необходимые для самостоятельной разработки метода и его эффективного использования [A.M. Егоров, А.П. Осипов, Б.Б. Дзантиев, Е.М. Гаврилова. Теория и практика иммуноферментного анализа. - М.: Издательство "Высшая школа", 1991. - С. 3-42. - ISBN 5-06-000644-1.]. Однако данный метод сам по себе не позволяет определять тип ДФ, т.к. неясно, какие именно антигены являются маркерами фетопатии плода у беременных.
Таким образом, техническим результатом заявленного изобретения является повышение точности анализа при определении типа фетопатии плода, а также расширение арсенала существующих способов анализа в диагностике ДФ плода.
Технический результат изобретения обеспечивает способ определения типа диабетической фетопатии плода, включающий:
- забор образца крови матери;
- пробоподготовку образца крови матери с получением аналита;
- определение содержания по меньшей мере одного маркера типа фетопатии плода, выбранного из группы, включающей Pigment epithelium-derived factor, Thrombospondin-1, Phosphatidylinositol-glycan-specific phospholipase D, Insulinlike growth factor-binding protein complex acid labile subunit, Zinc finger protein DPF3, Apolipoprotein M, Nebulin, Complement C4-A, Complement C1q subcomponent subunit B, Rho guanine nucleotide exchange factor 3, Actin, cytoplasmic 1, C4b-binding protein alpha chain, Cell division cycle 5-like protein, Complement C5, Serum amyloid P-component, Disheveled-associated activator of morphogenesis 2, Laminin subunit beta-4, Leucine-rich alpha-2-glycoprotein, MKL/myocardin-like protein 2 в аналите, при этом если значение концентрации белка Pigment epithelium-derived factor составляет не менее 0,049 мкг/мл,
и/или значение концентрации белка Thrombospondin-1 составляет не менее 28,117 мкг/мл и/или значение концентрации белка Phosphatidylinositol-glycan-specific phospholipase D составляет не более 0,359 мкг/мл,
и/или значение концентрации белка Insulin-like growth factor-binding protein complex acid labile subunit составляет 2,579-3,26 мкг/мл,
и/или значение концентрации белка Zinc finger protein DPF3 составляет не более 0,007 мкг/мл,
и/или значение концентрации белка Apolipoprotein М составляет не более 7,387 мкг/мл,
и/или значение концентрации белка Nebulin составляет не более 0,002 мкг/мл,
и/или значение концентрации белка Complement С4-А составляет не менее 307,93 мкг/мл,
и/или значение концентрации белка Complement C1q subcomponent subunit В составляет не менее 36,694 мкг/мл,
и/или значение концентрации белка Rho guanine nucleotide exchange factor 3 составляет не менее 2,671 мкг/мл,
и/или значение концентрации белка Actin, cytoplasmic 1 составляет не менее 4,671 мкг/мл,
и/или значение концентрации белка C4b-binding protein alpha chain составляет не менее 20,986 мкг/мл,
и/или значение концентрации белка Cell division cycle 5-like protein составляет не менее 0,094 мкг/мл,
и/или значение концентрации белка Complement С5 составляет не менее 39,679 мкг/мл,
и/или значение концентрации белка Serum amyloid P-component составляет не менее 37,671 мкг/мл,
определяют синдром угнетения центральной нервной системы (CNS),
при этом если значение концентрации белка Phosphatidylinositol-glycan-specific phospholipase D составляет не менее 1,235 мкг/мл,
и/или значение концентрации белка Insulin-like growth factor-binding protein complex acid labile subunit составляет не менее 3,26 мкг/мл,
и/или значение концентрации белка Zinc finger protein DPF3 составляет не менее 0,2 мкг/мл,
и/или значение концентрации белка Disheveled-associated activator of morphogenesis 2 составляет не менее 1,501 мкг/мл,
и/или значение концентрации белка Laminin subunit beta-4 составляет не менее 4,474 мкг/мл,
и/или значение концентрации белка Leucine-rich alpha-2-glycoprotein составляет не менее 1,095 мкг/мл,
и/или значение концентрации белка MKL/myocardin-like protein 2 составляет не менее 0, 009 мкг/мл,
определяют кардиомиопатию (CRD),
при этом если значение концентрации белка Pigment epithelium-derived factor составляет 0,035-0,049 мкг/мл,
и/или значение концентрации белка Thrombospondin-1 составляет 15,751-28,117 мкг/мл,
и/или значение концентрации белка Disheveled-associated activator of morphogenesis 2 составляет 1,191-1,501 мкг/мл,
и/или значение концентрации белка Laminin subunit beta-4 составляет не более 0,665 мкг/мл,
определяют гепатомегалию (НРМ).
Авторами изобретения было проведено перекрестное исследование протеома пациентов с СД, родивших новорожденных с различными типами ДФ, а также контрольной группы недиабетических беременных женщин и пациентов с СД. В таблице 1 приведены результаты проведенного исследования. Данные о концентрации маркеров в крови пациентов при различных типах фетопатии указаны в процентах от значений концентрации этих маркеров в контрольной группе.
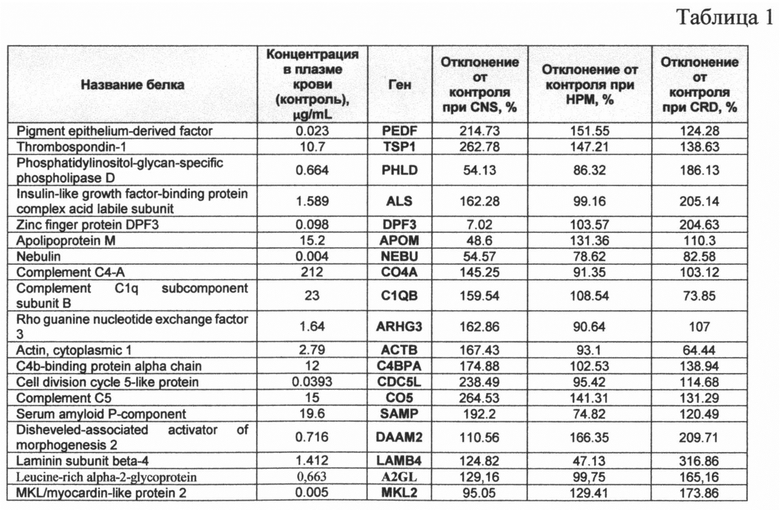
На основании полученных результатов были определены наиболее существенные серологические маркеры, детерминирующие морфогенез, дифференцировку кардиомиоцитов, проявление нейротрофических свойств и активности в отношении сплайсинга мРНК и репарации ДНК. Было установлено, что существует корреляция между значениями концентрации некоторых из указанных в таблице 1 маркеров и различными типами фетопатии новорожденных. В таблице 2 приведены значения концентрации маркеров, при которых, согласно заявленному изобретению, может быть определен тип фетопатии.

Значимость отклонения концентрации маркеров при различных типах фетопатии от контрольных значений определена статистическим тестом Крускала-Уоллиса при уровне значимости не более р<0.01.
Согласно заявленному изобретению, определение концентрации маркеров типов фетопатии плода в аналите может осуществляться методами иммуноферментного анализа или любыми другими методами, позволяющими определять концентрацию указанных маркеров в аналите (например, методом хромато-масс-спектрометрии). Как вариант, в этих целях могут быть использованы коммерческие ИФА - наборы, известные из уровня техники. Определение концентрации маркера в аналите производится в соответствии с инструкцией к соответствующему набору. Например, для определения концентрации в образце белка Pigment epithelium-derived factor может быть, например, использован коммерческий набор PEDF elisa kit: Human pigment epithelium-derived factor, PEDF ELISA Kit (mybiosource.com/human-elisa-kits/pigment-epithelium-derived-factor-pedf/702956). Для определения концентрации в образце белка Nebulin может быть, например, использован коммерческий набор Human Nebulin (NEB) ELISA Kit (https://www.abbexa.com/human-nebulin-elisa-kit). Для определения концентрации в образце белка Zinc finger protein DPF3 может быть, например, использован коммерческий набор Human Zinc Finger Protein DPF3 (DPF3) ELISA Kit (https://www.abbexa.corn/human-zinc-finger-protein-dpf3-elisa-kit) или любые другие наборы, позволяющие осуществлять определение концентрации указанных в таблице 1 маркеров ДФ плода.
Как вариант, в качестве образца крови может быть использована плазма или сыворотка венозной крови матери.
Указанный способ позволяет составлять полные и модульные диагностические панели для проведения мониторингового анализа и подтверждающего анализа в диагностике типа фетопатии плода.
В случае раннего определения типа патологии возникает возможность проведения своевременной корректирующей или компенсаторной терапии.
Проведение исследования в формате диагностической панели по предложенным в рамках изобретения маркерам или их сочетаниям также возможно, например, в формате иммуноферментного анализа (ИФА).
Заявленный способ иллюстрируется нижеследующими примерами.
Пример 1. Реализация заявленного изобретения
Пациентка Т, 25 лет, первая нормально протекающая беременность. Страдает сахарным диабетом первого типа в течение 4 лет. Находится на комбинированной терапии (короткие + пролонгированные инсулины). На момент постановки на учет по беременности в женской консультации заболевание находится в стадии субкомпенсации: уровень гликемии натощак - 4,7 ммоль/л, через 1 час после еды - 11,0 ммоль/л. В течение беременности пациентка находилась под наблюдением врача-эндокринолога с контролем гликемии и коррекцией проводимой терапии. Уровень гликированного гемоглобина (HbA1c) по триместрам: 5,3%-5,1%-5,4%, соответственно.
УЗИ плода в 1-м триместре - без особенностей.
УЗИ на сроке 26 недель - без особенностей.
На сроке 30 недель проведено протеомное исследование плазмы крови на наличие маркеров типа фетопатии в соответствии с заявленным способом. Результаты исследования приведены в таблице 3.
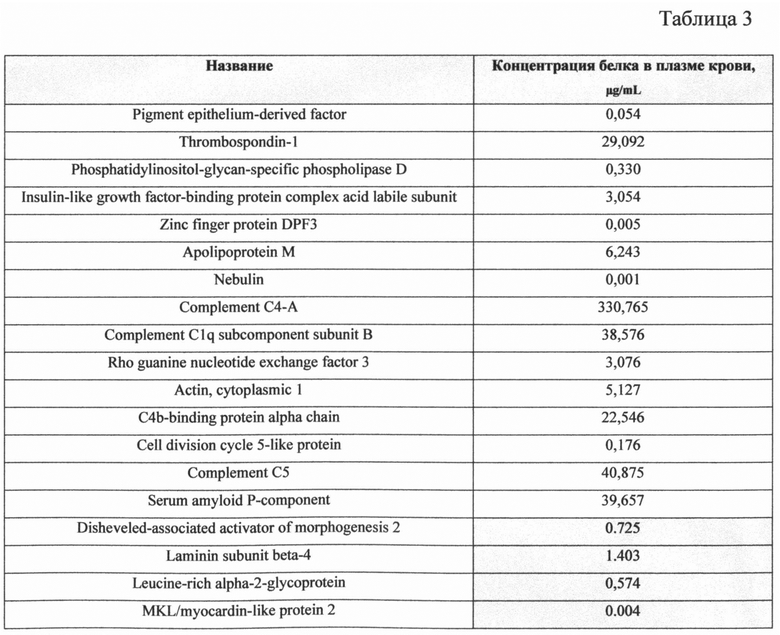
Полученные данные свидетельствуют о синдроме угнетения центральной нервной системы (CNS) у плода.
УЗИ на сроке 32 недели - тенденция к крупному плоду, многоводие, признаков фетопатии не выявлено.
УЗИ на сроке 37 недель - крупный плод, предполагаемая масса плода 4000±100 г, многоводие, признаков фетопатии не выявлено.
Родоразрешение на сроке 37 недель путем операции кесарева сечения. Родился живой доношенный мальчик, вес 4192 г, рост 57 см, баллы по шкале Апгар 8/9, с признаками фетопатии (синдром угнетения центральной нервной системы) и морфофункциональной незрелости.
Таким образом, использование заявленного способа позволяет повысить точность анализа при определении типа диабетической фетопатии плода.
Пример 2
Пациентка А, 23 года, первая нормально протекающая беременность. Страдает сахарным диабетом первого типа в течение 6 лет. Постоянно наблюдается эндокринологом, находится на комбинированной терапии (короткие + пролонгированные инсулины). При постановке на учет по беременности в женской консультации уровень гликемии натощак - 5,2 ммоль/л, через 1 час после еды - 18,2 ммоль/л. В течение беременности пациентка находилась под наблюдением врача-эндокринолога с контролем гликемии и коррекцией проводимой терапии. Уровень гликированного гемоглобина (HbA1c) в I, II и III триместрах беременности 8,2%-7,1%-7,4%, соответственно.
При УЗ исследованиях на сроке 12-13 недель и 19-20 недель - патологии не выявлено.
При УЗ исследовании на сроке 25 недель - тенденция к крупному плоду, умеренное многоводие, утолщение шейной складки.
На сроке 28 недель проведено протеомное исследование плазмы крови на наличие маркеров типа фетопатии в соответствии с заявленным способом. Результаты исследования приведены в таблице 4.
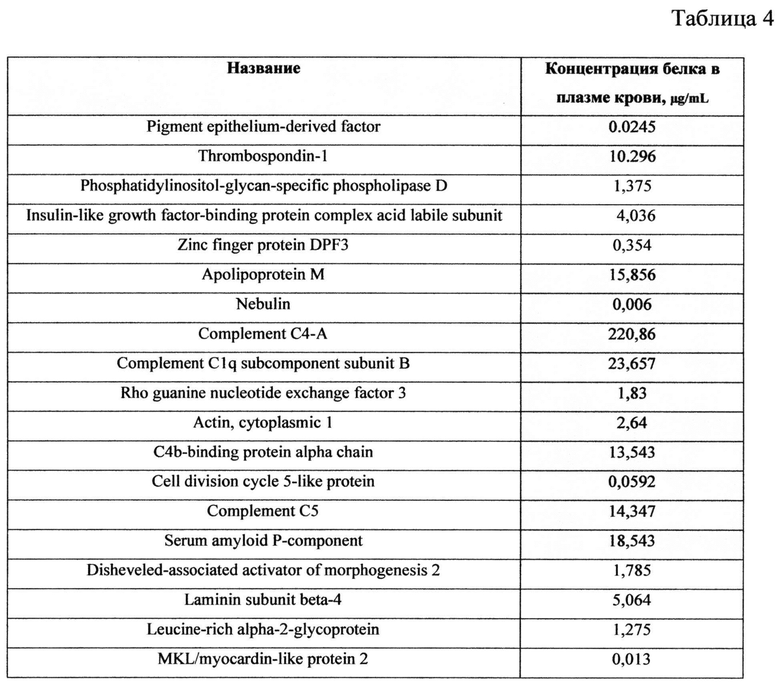
Полученные данные свидетельствуют о кардиомиопатии плода (CRD).
УЗИ в 36 недель - крупный плод.
Родоразрешение на сроке 37 недель путем операции кесарева сечения, родился живой мальчик, вес 4000 г, рост 52 см, баллы по шкале Апгар 8/9. У ребенка отмечается угнетение рефлексов, крипторхизм. Выявлена кардиомиопатия.
Таким образом, использование заявленного способа позволяет повысить точность анализа при определении типа фетопатии плода.
Пример 3
Пациентка К, 25 лет, первая нормально протекающая беременность. Страдает сахарным диабетом первого типа. Постоянно наблюдается эндокринологом, находится на комбинированной терапии (короткие + пролонгированные инсулины). При постановке на учет по беременности в женской консультации уровень гликемии натощак - 5,4 ммоль/л, через 1 час после еды - 19,0 ммоль/л. В течение беременности пациентка находилась под наблюдением врача-эндокринолога с контролем гликемии и коррекцией проводимой терапии. Уровень гликированного гемоглобина (HbA1c) в I, II и III триместрах беременности 8,5%-7,4%-7,2%, соответственно.
При УЗ исследованиях на сроке 12-13 недель и 19-20 недель - патологии не выявлено.
При УЗ исследовании на сроке 25 недель - тенденция к крупному плоду, умеренное многоводие.
На сроке 28 недель проведено протеомное исследование плазмы крови на наличие маркеров типа фетопатии в соответствии с заявленным способом. Результаты исследования приведены в таблице 5.
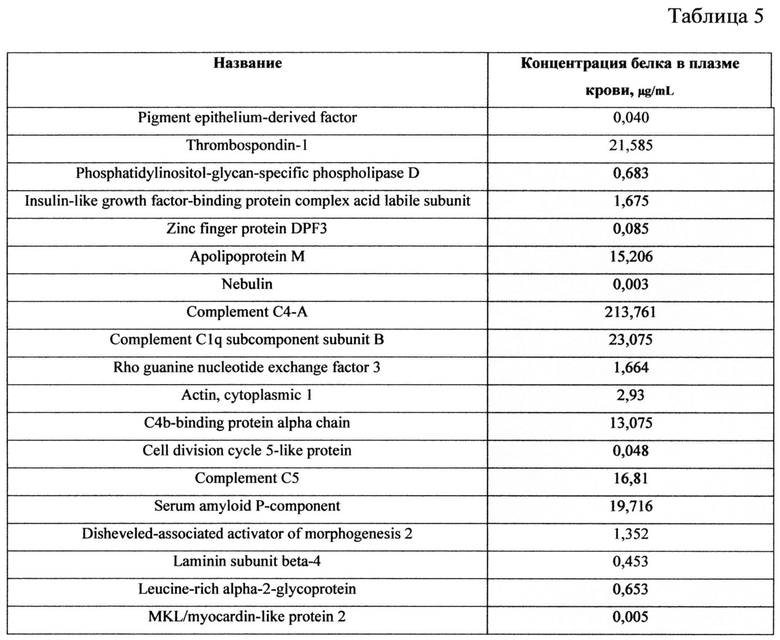
Полученные данные свидетельствуют о гепатомегалии плода (НРМ).
УЗИ в 35 недель - крупный плод.
Родоразрешение на сроке 36 недель самопроизвольные, через естественные родовые пути, родился живой мальчик, вес 3850 г, рост 53 см, баллы по шкале Апгар 8/9. У ребенка отмечается угнетение рефлексов. Выявлена гепатомегалия.
Таким образом, использование заявленного способа позволяет повысить точность анализа при определении типа фетопатии плода.
Пример 4
Пациентка С, 25 лет, вторая нормально протекающая беременность. Первая беременность закончилась срочными самопроизвольными родами на сроке 39 недель, ребенок здоров. При первичном обращении в женскую консультацию в сроке 10 недель уровень гликемии натощак 4,7 ммоль/л, в дальнейшем (ПГТТ) пероральный глюкозотолерантный тест не проводился. На сроке 28 недель отмечено повышение уровня гликемии натощак до 6,5 ммоль/л, поставлен диагноз ГСД, назначена диетотерапия. На фоне диетотерапии уровень гликемии натощак 5,4 ммоль/л, через 1 час после еды - 7,2 ммоль/л. На сроке 36 недель подключена инсулинотерапия (инсулины пролонгированного действия), уровень гликемии натощак 5,0 ммоль/л, через 1 час после еды - 6,0 ммоль/л.
В течение беременности проводились УЗ исследования на сроках 21 неделя, 29 недель, 36 недель - признаков фетопатии не выявлено.
На сроке 29 недель проведено протеомное исследование плазмы крови на наличие маркеров типа фетопатии в соответствии с заявленным способом. Результаты исследования приведены в таблице 6.

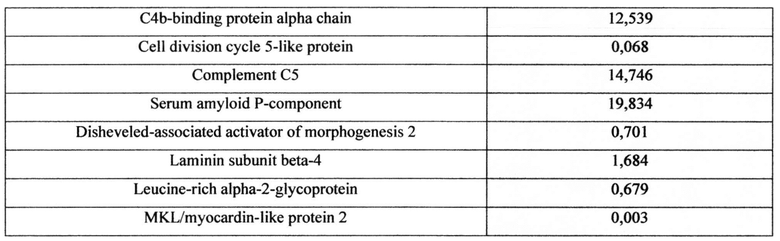
Уровни всех исследованных белков находятся в пределах нормы, что является показателем нормального развития плода.
Роды срочные (на 40 неделе), самопроизвольные. Родилась живая доношенная девочка, вес 3280 г, рост 50 см, баллы по шкале Апгар 9/9. Признаков фетопатии не выявлено.
Таким образом, использование заявленного способа позволяет повысить точность анализа при определении типа фетопатии плода с высокой точностью.
Пример 5
В рамках оценки точности определения типа диабетической фетопатии плода с использованием заявленного способа были проведены сравнительное исследование 15 женщин с различными типами фетопатии заявленным способом, а также методом УЗИ в качестве контроля. Результаты исследования приведены в таблице 7.

По результатам оценки точности анализа в диагностике диабетической фетопатии плода с использованием заявленного способа было установлено повышение точности по сравнению с контрольным методом на 26%. Таким образом, использование заявленного способа позволяет повысить точность анализа при определении типа фетопатии плода.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫЯВЛЕНИЯ ДИАБЕТИЧЕСКОЙ ФЕТОПАТИИ ПЛОДА | 2020 |
|
RU2770117C2 |
| СПОСОБ ВЫЯВЛЕНИЯ ДИАБЕТИЧЕСКОЙ ФЕТОПАТИИ ПЛОДА | 2020 |
|
RU2742801C1 |
| Способ ранней диагностики и прогнозирования диабетической фетопатии при гестационном сахарном диабете | 2024 |
|
RU2823332C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ТИПА САХАРНОГО ДИАБЕТА | 2021 |
|
RU2788106C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ФЕТОПАТИИ У БЕРЕМЕННЫХ С ГЕСТАЦИОННЫМ САХАРНЫМ ДИАБЕТОМ ВО II ПОЛОВИНЕ БЕРЕМЕННОСТИ | 2017 |
|
RU2667129C1 |
| Способ прогнозирования развития ранней анемии недоношенных тяжелой степени, требующей проведения гемотрансфузии | 2019 |
|
RU2719656C1 |
| Способ прогнозирования развития ранней анемии недоношенных | 2019 |
|
RU2699657C1 |
| СПОСОБ СКРИНИНГОВОГО ОБСЛЕДОВАНИЯ ЖЕНЩИН ДЛЯ ПРЕНАТАЛЬНОЙ ДИАГНОСТИКИ ВРОЖДЕННЫХ АНОМАЛИЙ И ВНУТРИУТРОБНОГО ИНФИЦИРОВАНИЯ ПЛОДА | 2011 |
|
RU2461006C1 |
| Способ прогнозирования развития ранней анемии недоношенных | 2019 |
|
RU2719657C1 |
| СПОСОБ ВЫЯВЛЕНИЯ САХАРНОГО ДИАБЕТА ПЕРВОГО ТИПА | 2020 |
|
RU2752372C1 |
Предложенная группа изобретений относится к медицине, а именно к клинической диагностике. Предложены способы определения признака диабетической фетопатии плода. Осуществляют забор образца крови матери, пробоподготовку образца крови матери с получением аналита и определение содержания маркера признака диабетической фетопатии плода в аналите. По отклонению концентрации исследуемого маркера от установленных значений определяют синдром угнетения центральной нервной системы, кардиомиопатию или гепатомегалию. Предложенная группа изобретений обеспечивает повышение точности анализа при определении признака диабетической фетопатии плода, а также расширение арсенала существующих способов анализа за счет определения отклонения в концентрации исследуемого маркера в крови матери. 3 н. и 6 з.п. ф-лы, 7 табл., 5 пр.
1. Способ определения признака диабетической фетопатии плода, включающий:
- забор образца крови матери;
- пробоподготовку образца крови матери с получением аналита;
- определение содержания маркера признака диабетической фетопатии плода, выбранного из группы, включающей Pigment epithelium-derived factor, Thrombospondin-1, Phosphatidylinositol-glycan-specific phospholipase D, Insulin-like growth factor-binding protein complex acid labile subunit, Zinc finger protein DPF3, Apolipoprotein M, Nebulin, Complement C4-A, Complement C1q subcomponent subunit B, Rho guanine nucleotide exchange factor 3, Actin, cytoplasmic 1, C4b-binding protein alpha chain, Cell division cycle 5-like protein, Complement C5, Serum amyloid P-component,
при этом, если значение концентрации белка Pigment epithelium-derived factor составляет не менее 0,049 мкг/мл,
или значение концентрации белка Thrombospondin-1 составляет не менее 28,117 мкг/мл,
или значение концентрации белка Phosphatidylinositol-glycan-specific phospholipase D составляет не более 0,359 мкг/мл,
или значение концентрации белка Insulin-like growth factor-binding protein complex acid labile subunit составляет 2,579-3,26 мкг/мл,
или значение концентрации белка Zinc finger protein DPF3 составляет не более 0,007 мкг/мл,
или значение концентрации белка Apolipoprotein М составляет не более 7,387 мкг/мл,
или значение концентрации белка Nebulin составляет не более 0,002 мкг/мл,
или значение концентрации белка Complement С4-А составляет не менее 307,93 мкг/мл,
или значение концентрации белка Complement C1q subcomponent subunit В составляет не менее 36,694 мкг/мл,
или значение концентрации белка Rho guanine nucleotide exchange factor 3 составляет не менее 2,671 мкг/мл,
или значение концентрации белка Actin, cytoplasmic 1 составляет не менее 4,671 мкг/мл,
или значение концентрации белка C4b-binding protein alpha chain составляет не менее 20,986 мкг/мл,
или значение концентрации белка Cell division cycle 5-like protein составляет не менее 0,094 мкг/мл,
или значение концентрации белка Complement С5 составляет не менее 39,679 мкг/мл,
или значение концентрации белка Serum amyloid P-component составляет не менее 37,671 мкг/мл,
определяют синдром угнетения центральной нервной системы.
2. Способ по п. 1, отличающийся тем, что определение концентрации маркера признака диабетической фетопатии плода в аналите осуществляется методом иммуноферментного анализа.
3. Способ по п. 1, отличающийся тем, что определение концентрации маркера признака диабетической фетопатии плода в аналите осуществляется методом хромато масс-спектрометрии.
4. Способ определения признака диабетической фетопатии плода, включающий:
- забор образца крови матери;
- пробоподготовку образца крови матери с получением аналита;
- определение содержания маркера признака диабетической фетопатии плода, выбранного из группы, включающей Phosphatidylinositol-glycan-specific phospholipase D, Insulin-like growth factor-binding protein complex acid labile subunit, Zinc finger protein DPF3, Disheveled-associated activator of morphogenesis 2, Laminin subunit beta-4, Leucine-rich alpha-2-glycoprotein, MKL/myocardin-like protein 2,
при этом, если значение концентрации белка Phosphatidylinositol-glycan-specific phospholipase D составляет не менее 1,235 мкг/мл,
или значение концентрации белка Insulin-like growth factor-binding protein complex acid labile subunit составляет не менее 3,26 мкг/мл,
или значение концентрации белка Zinc finger protein DPF3 составляет не менее 0,2 мкг/мл,
или значение концентрации белка Disheveled-associated activator of morphogenesis 2 составляет не менее 1,501 мкг/мл,
или значение концентрации белка Laminin subunit beta-4 составляет не менее 4,474 мкг/мл,
или значение концентрации белка Leucine-rich alpha-2-glycoprotein составляет не менее 1,095 мкг/мл,
или значение концентрации белка MKL/myocardin-like protein 2 составляет не менее 0, 009 мкг/мл,
определяют кардиомиопатию.
5. Способ по п. 4, отличающийся тем, что определение концентрации маркера признака диабетической фетопатии плода в аналите осуществляется методом иммуноферментного анализа.
6. Способ по п. 4, отличающийся тем, что определение концентрации маркера признака диабетической фетопатии плода в аналите осуществляется методом хромато масс-спектрометрии.
7. Способ определения признака диабетической фетопатии плода, включающий:
- забор образца крови матери;
- пробоподготовку образца крови матери с получением аналита;
- определение содержания маркера признака диабетической фетопатии плода, выбранного из группы, включающей Pigment epithelium-derived factor, Thrombospondin-1, Disheveled-associated activator of morphogenesis 2, Laminin subunit beta-4,
при этом, если значение концентрации белка Pigment epithelium-derived factor составляет 0,035-0,049 мкг/мл,
или значение концентрации белка Thrombospondin-1 составляет 15,751-28,117 мкг/мл,
или значение концентрации белка Disheveled-associated activator of morphogenesis 2 составляет 1,191-1,501 мкг/мл,
или значение концентрации белка Laminin subunit beta-4 составляет не более 0,665 мкг/мл,
определяют гепатомегалию.
8. Способ по п. 7, отличающийся тем, что определение концентрации маркера признака диабетической фетопатии плода в аналите осуществляется методом иммуноферментного анализа.
9. Способ по п. 7, отличающийся тем, что определение концентрации маркера признака диабетической фетопатии плода в аналите осуществляется методом хромато масс-спектрометрии.
| СПОСОБ ВЫЯВЛЕНИЯ ДИАБЕТИЧЕСКОЙ ФЕТОПАТИИ ПЛОДА | 2020 |
|
RU2742801C1 |
| СВИРИДОВА М.И | |||
| и др | |||
| Диабетическая фетопатия как исход манифестного сахарного диабета, впервые выявленного во время беременности | |||
| Эффективная фармакотерапия | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| KOPYLOV A.T | |||
| et al., Association of Proteins Modulating Immune Response and Insulin Clearance During Gestation with Antenatal Complications in | |||
Авторы
Даты
2023-09-19—Публикация
2022-05-06—Подача