Область техники, к которой относится изобретение
Настоящее изобретение относится к области способов изготовления меток поверхностно-усиленной рамановской спектроскопии (SERS). Способ изготовления согласно настоящему изобретению является воспроизводимым и универсальным и позволяет производить целесообразным образом большие количества SERS-меток, характеризующихся узким распределением по размерам и высокой долей агрегатов с малым числом. SERS-метки, изготовленные заявленным способом изготовления, описанным в данном документе, обеспечивают повышенные ответы SERS в группе.
Предпосылки создания изобретения
Метки поверхностно-усиленной рамановской спектроскопии (SERS) оказались полезными для множества применений, включая нанесение этикеток на продукты для целей идентификации и аутентификации, а также высокопроизводительный мультиплексный скрининг в технологии микрочипов, диагностике и биоимиджинге. SERS-метки представляют собой агрегаты наночастиц с плазмонной поверхностью и адсорбированными на их поверхности активными репортерными молекулами рамановского рассеяния. Наночастицы с плазмонной поверхностью ответственны за генерирование электрического поля, необходимого для рамановского усиления, в то время как активная репортерная молекула рамановского рассеяния обеспечивает уникальный вибрационный отпечаток SERS-метки. Обычно агрегаты представляют собой внешний слой покрытия, который a) изолирует SERS-метку от внешней среды, тем самым предотвращая вымывание активных репортерных молекул рамановского рассеяния из SERS-метки и защищая SERS-метку от загрязнения внешней среды, которое может вызвать к вибрационному шуму, b) увеличивает коллоидную стабильность SERS-метки и c) обеспечивает удобную поверхность для дальнейшей химической функционализации. На сегодняшний день в качестве внешних слоев покрытия используются полимеры и диоксид кремния.
Из-за сильной зависимости плазмонных свойств от агрегированных состояний наночастиц производство SERS-меток с большим количеством агрегатов с малым числом очень желательно для получения увеличенных SERS-ответов в группе. SERS-метки с большим количеством агрегатов с малым числом получали либо с помощью методов постсинтетической сортировки, либо с помощью процессов синтеза с контролируемой агрегацией.
Например, фракционирование в потоке при наличии поля, применяемое к смеси, содержащей отдельные наночастицы и агрегаты наночастиц размером от димеров до октамеров, привело к получению фракции, обогащенной димерными (10%), тримерными (21%) и тетрамными (13%) SERS-метками, но которая, тем не менее, содержала высокую процентную долю одиночных наночастиц (52%) (J. Am. Chem. Soc. 2010, 132, 10903-10910). Смесь, содержащая отдельные наночастицы и агрегаты размером от димеров до додекамеров, была обогащена димерными (52%) и тримерными (32%) SERS-метками с помощью центрифужного способа постсинтетической сортировки в высоковязкой среде с градиентом плотности, такой как водная среда с градиентом плотности йодиксанола (US9802818B2). Помимо того, что методы постсинтетической сортировки трудоемки и ресурсозатратны, для них необходимо применение жестких условий (в случае, например, высоковязких реагентов), которые приводят к дестабилизации SERS-меток без покрытия. Таким образом, методы постсинтетической сортировки совместимы только с SERS-метками, имеющими покрытие из диоксида кремния или полимера. Следовательно, процессы синтеза с контролируемой агрегацией имеют большое преимущество для производства SERS-меток с узким распределением по размерам и высоким соотношением агрегатов с малым числом.
Агрегация с использованием твердой подложки позволила получить SERS-метки с узким распределением по размерам. В публикации Ruan и соавт. (Adv. Optical Mater. 2014, 2, 65 - 73) описан синтез SERS-меток с ассиметричными центральной и периферической структурами, имеющих некоторое количество, т. е. 18 ± 2, периферических структур в виде наносфер Au со средним диаметром 24 нм на центральную структуру в виде наносферы Au со средним диаметром 180 нм. Синтез предусматривает адсорбцию стабилизированных цетилтриметиламмония бромидом центральных структур наночастиц Au на покрытом оксидом индия и олова предметном стекле или кремниевой пластинке с последующим погружением функционализированной твердой подложки в раствор 4-аминотиофенола в воде/ацетонитриле для адсорбции активной репортерной молекулы рамановского рассеяния на поверхности наночастиц Au и последующим погружением на 1 час в суспензию наночастиц Au со средним диаметром 24 нм. Агрегатное состояние SERS-меток можно отслеживать путем контроля времени погружения функционализированной твердой подложки в суспензию периферических наночастиц Au и/или уменьшения концентрации периферических наночастиц Au в указанной суспензии. В основе способа, описанного Ruan и соавт., лежит применение такого поверхностно-активного вещества как цетилтриметиламмония бромид, для стабилизации коллоида Au, что значительно уменьшает поверхность, доступную для адсорбции активной репортерной молекулы рамановского рассеяния, на центральной структуре наночастицы Au и тем самым интенсивность SERS-сигнала, подаваемого SERS-метками. Для связывания периферических наночастиц Au с центральной структурой наночастиц Au в способе агрегации задействуют активные репортерные молекулы рамановского рассеяния, обладающие двумя функциональными группами со сродством к поверхности из Au. Таким образом, данный способ применим только для получения SERS-меток, содержащих активные репортерные молекулы рамановского рассеяния, у которых имеется две функциональные группы со сродством к поверхности из Au, что представляет собой серьезное ограничение с точки зрения применения активных репортерных молекул рамановского рассеяния в качестве «отпечатка» SERS-метки. Более того, при указанном способе необходимо длительное время реакции, и он не подходит для рентабельного получения больших количеств SERS-меток.
Еще один способ сборки SERS-меток с узким распределением по размерам с использованием твердой подложки был описан Yoon и соавт. (ACS Nano 2012, 8, 7199 - 7208). В основе способа лежат зависящие от размера склонности наночастиц Au, адсорбированных на предметных стеклах с функциональными аминогруппами, и применение алкандитиолов для связывания периферических наночастиц Au с центральной структурой наночастицы Au. Были получены SERS-метки с 13±3 периферическими наночастицами Au со средним диаметром 13 нм на центральную структуру наночастицы Au со средним диаметром 51 нм. Способ, разработанный Yoon и соавт., судя по всему, делает возможным включение любой активной репортерной молекулы рамановского рассеяния в SERS-метку. Однако указанный способ имеет ограничения с точки зрения размеров наночастиц Au, которые можно использовать, и поверхности центральной структуры наночастицы Au, доступной для активных репортерных молекул рамановского рассеяния. Более того, при данном способе необходимо длительное время реакции, и он не подходит для рентабельного получения больших количеств SERS-меток.
Таким образом, остается потребность в воспроизводимых, рентабельных и универсальных способах изготовления SERS-меток, которые сделают возможным получение целесообразным образом больших количеств SERS-меток, характеризующихся узким распределением по размерам и высокой долей агрегатов с малым числом. Для получения увеличенных согласованных SERS-ответов очень необходимы SERS-метки с большим количеством агрегатов с малым числом.
Краткое описание изобретения
Соответственно, предмет настоящего изобретения заключается в создании универсального, рентабельного и воспроизводимого способа изготовления SERS-меток, который сделает возможным получение целесообразным образом больших количеств SERS-меток, характеризующихся узким распределением по размерам и высокой долей агрегатов с малым числом. Это достигается при помощи реализации способа изготовления меток для поверхностно-усиленной рамановской спектроскопии (SERS), предпочтительно SERS-меток для применения в качестве защитного элемента, предусматривающего следующие стадии:
a) получение первого коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
b) получение второго коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, активных репортерных молекул рамановского рассеяния, адсорбированных на поверхности указанных наночастиц, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
c) объединение первого коллоида со вторым коллоидом таким образом, чтобы соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло от приблизительно 25 : 1 до приблизительно 1 : 1, предпочтительно от приблизительно 5 : 1 до приблизительно 1 : 1, более предпочтительно от 4 : 1 до приблизительно 3 : 1 с получением третьего коллоида;
d) индукцию агрегации наночастиц с помощью любой из стадий d1) - d3) или их комбинации:
d1) смешивание третьего коллоида, полученного на стадии c), при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3;
d2) добавление раствора соли, предпочтительно раствора неорганической соли, к третьему коллоиду, полученному на стадии c);
d3) добавление водорастворимого растворителя к третьему коллоиду, полученному на стадии c); и
e) остановку агрегации.
Предпочтительно, стадия b) в заявляемом и описанном в настоящем документе способе предусматривает следующие стадии, осуществляемые в порядке b1)-b3):
b1) получение коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
b2) доведение pH коллоида до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния, которые должны адсорбироваться на поверхности наночастиц, не несут суммарный электрический заряд, при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ, предпочтительно ниже -40 мВ; и
b3) добавление раствора активных репортерных молекул рамановского рассеяния в растворителе к коллоиду, полученному на стадии b2), при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ.
В дополнительном предпочтительном варианте осуществления стадии c) и d) осуществляют одновременно в проточной системе непрерывного действия. В дополнительном предпочтительном варианте осуществления размер наночастиц в первом коллоиде отличается от размера наночастиц во втором коллоиде.
Как проиллюстрировано с помощью примеров E1-E14, заявляемый в настоящем документе способ делает возможным интеграцию ряда активных репортерных молекул рамановского рассеяния в SERS-метку и не ограничен сочетанием конкретных размеров наночастиц, что позволяет также синтезировать SERS-метки, содержащие наночастицы с одинаковым размером, что подтверждается, например, примерами E1-E8 и E12-E14. Дополнительно, заявляемый и описываемый в настоящем документе способ изготовления позволяет получить SERS-метки с узким распределением по размерам, как проиллюстрировано, например, на фиг. 3a и фиг. 3b, и высоким соотношение агрегатов с малым числом, как проиллюстрировано, например, на фиг. 3a и фиг. 3b, и характеризуется значимо более коротким временем реакции по сравнению со способами, известными из литературы.
Краткое описание чертежей
На фиг. 1a схематично изображен способ изготовления SERS-меток по настоящему изобретению. Способ изготовления предусматривает объединение второго коллоида (120a), фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером (121a), диспергированных в водном растворителе (не показан), при этом наночастицы имеют адсорбированные на их поверхности активные репортерные молекулы рамановского рассеяния (122a) и стабилизирующее средство (не показано), с первым коллоидом, фактически состоящим из наночастиц с плазмонной поверхностью и по существу одинаковым размером (130a), диспергированных в водном растворителе (не показан), при этом наночастицы имеют адсорбированное на их поверхности стабилизирующее средство (не показано), и индукцию агрегации наночастиц с получением SERS-меток (140a).
На фиг. 1b схематично представлен вариант осуществления способа изготовления SERS-меток по настоящему изобретению. В данном конкретном способе изготовления проточный реактор непрерывного действия содержит два резервуара (111b, 112b) под давлением, тройник (113b) и резервуар (114b) для сбора, при этом каждый из двух резервуаров (111b, 112b) под давлением соединен с помощью трубки с тройником (113b), который сам соединен с помощью трубки с резервуаром (114b) для сбора. Способ изготовления предусматривает объединение и одновременное смешивание при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3, в трубке, соединяющей тройник (113b) с резервуаром (114b) для сбора проточного реактора непрерывного действия, первого коллоида, подаваемого из резервуара (112b) под давлением и фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером (130b), диспергированных в водном растворителе (не показан), при этом указанные наночастицы имеют адсорбированное на их поверхности стабилизирующее средство (не показано), со вторым коллоидом (120b), подаваемым из резервуара (111b) под давлением и фактически состоящим из наночастиц с плазмонной поверхностью и по существу одинаковым размером (121b), диспергированных в водном растворителе (не показан), при этом указанные наночастицы имеют адсорбированные на их поверхности активные репортерные молекулы (122b) рамановского рассеяния и стабилизирующее средство (не показано). Смешивание при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3, индуцирует агрегацию наночастиц. Стадию агрегации останавливают в резервуаре (114b) для сбора, тем самым получая целевые SERS-метки (140b).
На фиг. 1c схематично представлен вариант осуществления способа изготовления SERS-меток по настоящему изобретению. В данном конкретном способе изготовления проточный реактор непрерывного действия содержит три резервуара (111c, 112c, 150c) под давлением, тройник (113c) и резервуар (114c) для сбора. Каждый из двух резервуаров (111c, 112c) под давлением соединен с помощью трубки с тройником (113c), который сам соединен с помощью трубки с резервуаром (114c) для сбора. Способ изготовления предусматривает объединение и одновременное смешивание при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3, в трубке, соединяющей тройник (113c) с резервуаром (114c) для сбора проточного реактора непрерывного действия, первого коллоида, подаваемого из резервуара (112c) под давлением и фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером (130c), диспергированных в водном растворителе (не показан), при этом наночастицы имеют адсорбированное на их поверхности стабилизирующее средство (не показано), со вторым коллоидом (120c), подаваемым из резервуара (111c) под давлением и фактически состоящим из наночастиц с плазмонной поверхностью и по существу одинаковым размером (121c), диспергированных в водном растворителе (не показан), при этом указанные наночастицы имеют адсорбированные на их поверхности активные репортерные молекулы (122c) рамановского рассеяния и стабилизирующее средство (не показано). Смешивание при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3, индуцирует агрегацию наночастиц. Стадию агрегации останавливают путем введения воды, хранящейся в резервуаре (150c) под давлением, в трубку, ведущую в резервуар (114c) для сбора, с тем, чтобы разбавить коллоид, путем введения основного раствора, хранящегося в резервуаре (150c) под давлением, в трубку, ведущую в резервуар (114c) для сбора, путем введения полимера, хранящегося в резервуаре (150c) под давлением, в трубку, ведущую в резервуар (114c) для сбора, или путем введения предшественника диэлектрического материала, хранящегося в резервуаре (150c) под давлением, в трубку, ведущую в резервуар (114c) для сбора, тем самым получая целевые SERS-метки (140c).
На фиг. 2a-c проиллюстрировано изменение интенсивности SERS-сигнала со временем реакции агрегации: на фиг. 2a показано изменение интенсивности SERS со временем реакции агрегации у SERS-меток, изготовленных так, как описано в примере E1; на фиг. 2b показано изменение интенсивности SERS со временем реакции агрегации у SERS-меток, изготовленных так, как описано в примере E14; на фиг. 2c показано изменение интенсивности SERS со временем реакции агрегации у SERS-меток, изготовленных так, как описано в примере E13. Горизонтальная ось соответствует времени реакции агрегации в секундах, а вертикальная ось соответствует SERS-ответу при возбуждении на 785 нм. Регистрируемую интенсивность SERS измеряли с временем для аккумулирования заряда светодиодом 100 мс каждые 1 секунду при заданной концентрации золота, и для данной интенсивности сигнала устанавливали корреляцию с образцами, разведенными до 12,5 мкг Au/мл и подвергаемыми сканированию с 1-секундным временем для аккумулирования заряда светодиодом.
На фиг. 3a-b представлены SEM-изображения, полученные от SERS-меток, содержащих наночастицы разных размеров и изготовленных согласно примеру E9 (фиг. 3a) и 10 (фиг. 3b). Как подтверждается SEM-изображениями, SERS-метки, изготовленные в соответствии с настоящим изобретением, обогащены агрегатами с малым числом, такими как димеры, тримеры и тетрамеры, и имеют узкое распределение по размерам.
Фиг. 4 представляет собой график, иллюстрирующий значение ζ-потенциала первого коллоида A2 (на графике изображен закрашенными кружками) и вторых коллоидов D2 (на графике изображен закрашенными треугольниками), D5 (на графике изображен закрашенными ромбами) и D6 (на графике изображен закрашенными квадратами), при титровании указанных коллоидов водным раствором 1 н. HCl или водным раствором 1 н. NaOH. Горизонтальная ось соответствует значению pH, а вертикальная ось соответствует значению ζ-потенциала (мВ). Условия, при которых была видна агрегация (т. е. коллоиды были нестабильными), обведены кружком. Как подтверждается фиг. 4, ряд коллоидов, характеризующихся значением ζ-потенциала ниже -25 мВ, были стабильными. Такие коллоиды можно применять в качестве первого и второго коллоидов соответственно в способе изготовления по настоящему изобретению.
На фиг. 5 проиллюстрировано развитие значений интенсивности SERS-сигнала у коллоидов, агрегирующихся в проточной системе. Каждое измерение проводили на 1-метровых отметках вдоль 7-м прозрачной трубки из FEP. Данные, представленные ромбами, соединенными сплошной линией, были получены на SERS-метках, полученных так, как описано в примере E8. Данные, представленные кружками, соединенными пунктирной линией, были получены на SERS-метках, полученных так, как описано в примере E11.
Подробное описание
Определения
Для трактовки значения терминов, рассмотренных в описании и изложенных в формуле изобретения, должны использоваться следующие определения.
В контексте настоящего документа форма единственного числа объекта указывает на один объект или более и необязательно ограничивает его единственным числом.
В контексте настоящего документа подразумевается, что термин «по меньшей мере» означает один или несколько, например, один, или два, или три.
Термин «содержащий» в контексте настоящего документа является неисключительным и допускающим изменения. Так, например, раствор, содержащий соединение A, может включать иные соединения, помимо А. Вместе с тем, термин «содержащий» также охватывает, как и его конкретный вариант осуществления, более ограничительные значения «состоящий по существу из» и «состоящий из», так что, например, «раствор, содержащий A, B и необязательно C» также может (в основном) состоять из A и B или (в основном) состоять из A, B и C.
Когда настоящее описание касается «предпочтительных» вариантов осуществления/признаков, комбинации этих «предпочтительных» вариантов осуществления/признаков также следует рассматривать как раскрытые до тех пор, пока данная комбинация «предпочтительных» вариантов осуществления/признаков имеет значение с технической точки зрения.
В контексте настоящего документа термин «приблизительно» означает, что указанное количество или значение может иметь конкретное определенное значение или некоторое иное значение, соседнее с ним. В целом, термин «приблизительно», обозначающий определенное значение, предназначен для обозначения диапазона в пределах ± 5% значения. В качестве одного примера, фраза «приблизительно 100» обозначает диапазон 100 ± 5, т. е. диапазон от 95 до 105. Предпочтительно, диапазон, обозначенный термином «приблизительно», означает диапазон в пределах ± 3 % значения, более предпочтительно, ± 1 %. В целом, при использовании термина «приблизительно» можно ожидать, что подобные результаты или эффекты согласно настоящему изобретению могут быть получены в диапазоне в пределах ± 5% указанного значения.
Неожиданно было обнаружено, что способ изготовления меток для поверхностно-усиленной рамановской спектроскопии (SERS), предпочтительно SERS-меток для применения в качестве защитного элемента, предусматривает следующие стадии:
a) получение первого коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
b) получение второго коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, активных репортерных молекул рамановского рассеяния, адсорбированных на поверхности указанных наночастиц, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
c) объединение первого коллоида со вторым коллоидом таким образом, чтобы соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло от приблизительно 25 : 1 до приблизительно 1 : 1, предпочтительно от приблизительно 5 : 1 до приблизительно 1 : 1, более предпочтительно от приблизительно 4 : 1 до приблизительно 3 : 1 с получением третьего коллоида;
d) индукцию агрегации наночастиц с помощью любой из стадий d1) - d3) или их комбинации:
d1) смешивание третьего коллоида, полученного на стадии c), при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3;
d2) добавление раствора соли, предпочтительно раствора неорганической соли, к третьему коллоиду, полученному на стадии c);
d3) добавление водорастворимого растворителя к третьему коллоиду, полученному на стадии c); и
e) остановку агрегации;
дает рентабельным и целесообразным способом большое количество SERS-меток с узким распределением по размерам и высоким соотношением агрегатов с малым числом. Способ не имеет каких-либо ограничений с точки зрения активной репортерной молекулы рамановского рассеяния, подлежащей применению в качестве «отпечатка» SERS-метки, или размера наночастиц с плазмонной поверхностью, содержащихся в первом и втором коллоиде, что позволяет изготавливать различные SERS-метки.
Как хорошо известно специалисту в данной области техники и используется в настоящем документе, SERS-метка содержит один агрегат наночастиц с плазмонной поверхностью и активными репортерными молекулами рамановского рассеяния, адсорбированными на поверхности наночастиц. Наночастицы с плазмонной поверхностью ответственны за генерирование электрического поля, необходимого для рамановского усиления, в то время как активные репортерные молекулы рамановского рассеяния обеспечивают уникальный вибрационный отпечаток SERS-метки. SERS-метка может дополнительно содержать внешний слой покрытия, изолирующий агрегат наночастиц с адсорбированными на поверхности активными молекулами рамановского рассеяния от внешней среды. Таким образом, внешний слой покрытия a) изолирует SERS-метку от внешней среды, тем самым предотвращая вымывание активных репортерных молекул рамановского рассеяния из SERS-метки и защищая SERS-метку от загрязнения внешней среды, которое может вызвать появление ложных пиков, b) увеличивает коллоидную стабильность SERS-метки и c) обеспечивает удобную поверхность для дальнейшей химической функционализации. Слои внешнего покрытия включают диоксид кремния и полимеры, такие как полиэтиленимин (PEI), натриевая соль сополимера стирола и малеиновой кислоты (PSMA), полидиаллилдиметиламмония хлорид (PDADMAC).
Благодаря проявляющемуся SERS-сигналу SERS-метки, полученные с помощью заявляемого и описываемого в настоящем документе способа изготовления, особенно пригодны в качестве защитного элемента для защиты документов и изделий от подделки и незаконного воспроизведения. В контексте настоящего документа термин «защитный элемент» обозначает элемент, который может быть включен в или нанесен на защищаемый документ или изделие с целью определения его подлинности и его защиты от подделок и незаконного воспроизведения. Защитный элемент может представлять собой знак, изображение, рисунок или графический элемент, напечатанные, нанесенные в виде покрытия или напыленные на защитный элемент или изделие с чернилами, лаком или композицией для нанесения покрытия, которые содержат SERS-метки, полученные с помощью способа изготовления по настоящему изобретению. Альтернативно, SERS-метки могут функционировать в качестве защитного элемента, если они встроены в основу защищаемого документа. Термины «защищаемый документ» и «защищаемое изделие» относятся к документу или изделию, имеющим ценность, которая делает их потенциально подверженными попыткам подделки или незаконного воспроизведения, и которые обычно защищены от подделки или фальсификации по меньшей мере одним защитным признаком. Термин «защищаемое изделие» в контексте настоящего документа охватывает все изделия, которые должны быть защищены от подделки и/или незаконного воспроизведения, чтобы гарантировать их содержимое. Примеры защищаемых документов включают без ограничения ценные документы и ценные коммерческие товары. Типичные примеры ценных документов включают без ограничения банкноты, юридические документы, билеты, чеки, ваучеры, гербовые марки, акцизные марки, соглашения и т. п., документы, удостоверяющие личность, такие как паспорта, удостоверения личности, визы, банковские карты, кредитные карты, транзакционные карты, документы для получения доступа, входные билеты и т. п. Ценные коммерческие товары охватывают упаковочный материал, в частности, для косметических изделий, нутрицевтических изделий, фармацевтических изделий, спиртных напитков, табачных изделий, напитков или пищевых продуктов, электротехнических/электронных изделий, тканей или ювелирных изделий, т. е. изделий, которые должны быть защищены от подделки и/или незаконного воспроизведения для гарантирования действительности содержимого упаковки, подобного, например, к истинным лекарственным средствам. Примеры упаковочных материалов включают без ограничения этикетки, такие как товарные этикетки для аутентификации, этикетки и печати с защитой от раскрытия.
В контексте настоящего изобретения по определению термин «наночастица» означает отдельную частицу, имеющую размер, соответствующий максимальному физическому размеру (например, длине, диаметру и т. д.) в диапазоне от 20 ± 5 нм до 160 ± 5 нм, предпочтительно от 40 ± 5 нм до 140 ± 5 нм. Наночастица в контексте настоящего изобретения имеет плазмонную поверхность, т. е. наночастица имеет внешнюю поверхность, способную усиливать рамановское рассеяние активной молекулы рамановского рассеяния. Внешняя поверхность наночастиц выполнена из любого известного SERS-усиливающего материала. Предпочтительно, SERS-усиливающий материал выбран из золота (Au), серебра (Ag), меди (Cu), алюминия (Al), палладия (Pd), платины (Pt) или их смеси или сплава, и более предпочтительно из золота (Au). Наночастица в контексте настоящего изобретения может быть твердой или полой и предпочтительно является твердой. Твердая наночастица может быть выполнена из одного материала, т. е. из SERS-усиливающего материала внешней поверхности наночастицы, или из нескольких материалов, т. е. материал(-ы) центральной структуры наночастицы может(могут) отличаться от SERS-усиливающего материала внешней поверхности наночастицы. Полая наночастица представляет собой наночастицу, центральная структура которой представляет собой пустое пространство. Наночастица может иметь любую форму, которую можно получить. Предпочтительно, наночастица представляет собой твердую наночастицу из Au. Предпочтительно, наночастица имеет форму, выбранную из группы, состоящей из сферы, сфероида, стержня, диска, призмы и куба, более предпочтительно выбранную из сферы и сфероида, и еще более предпочтительно наночастица имеет форму сфероида.
В контексте настоящего документа формулировка «наночастицы с по существу одинаковым размером» означает, что указанные наночастицы имеют размер, соответствующий максимальному физическому размеру (например, длине, диаметру и т. д.) в пределах ± 20 нм, предпочтительно в пределах ± 10 нм от среднего размера, определенного для указанных наночастиц с помощью способов электронной микроскопии, таких как трансмиссионная электронная микроскопия (TEM) или сканирующая электронная микроскопия (SEM), или, если применимо, с помощью способа из публикации Haiss и соавт. (Anal. Chem. 2007, 79, 4215-4221).
Наночастицы первого коллоида, второго коллоида и коллоида, полученного на стадии b1), диспергируют в водном растворителе. В контексте настоящего документа термин «водный растворитель» относится к воде и смеси воды с одним или несколькими водорастворимыми растворителями, причем водорастворимый растворитель предпочтительно выбран из перечня, включающего метанол, этанол, пропанол, изопропанол, тетрагидрофуран, N-метил-2-пирролидон (NMP), диметилсульфоксид (DMSO), N,N-диметилформамид (DMF), ацетон и ацетонитрил.
Первый коллоид, полученный на стадии а) способа изготовления, второй коллоид, полученный на стадии b) способа изготовления, а также коллоид, полученный на стадии b1) способа изготовления, не содержат полимеров или поверхностно-активных веществ для стабилизации. Стабилизация коллоидов полимерами (например, поливинилпирролидоном) или поверхностно-активными веществами (например, бромидом цетилтриметиламмония) хорошо известна из уровня техники. Тем не менее, поскольку полимеры и поверхностно-активные вещества добавляют к коллоидам до добавления активных репортерных молекул рамановского рассеяния, они значительно уменьшают поверхность, доступную на наночастицах для адсорбции активных репортерных молекул рамановского рассеяния, и увеличивают расстояние между коллоидными частицами в агрегате, что, как следствие, приводит к тому, что у SERS-меток наблюдается более низкая интенсивность SERS-сигнала. Для преодоления данного недостатка первый коллоид, второй коллоид, а также коллоид, полученный на стадии b1), не содержат поверхностно-активных веществ и полимеров.
Стабилизирующее средство, адсорбированное на поверхности наночастиц первого коллоида, второго коллоида и коллоида, полученного на стадии b1), предпочтительно выбрано из карбоновых кислот, солей карбоновых кислот, фосфорных кислот, солей фосфорных кислот, аскорбиновой кислоты, солей аскорбиновой кислоты и их смесей. Во избежание конкуренции между активными репортерными молекулами рамановского рассеяния и стабилизирующим средством во время адсорбции активных репортерных молекул рамановского рассеяния на поверхности наночастиц предпочтительно, чтобы стабилизирующее средство не содержало групп, обладающих сродством к SERS-усиливающим материалам, в частности к золоту. Примерами таких групп являются азотсодержащие группы, серосодержащие группы, этинильные группы, цианогруппы и изоцианидные группы.
В контексте настоящего документа термин «карбоновая кислота» относится к органическому соединению, содержащему карбоксильную группу (C(=O)OH), и охватывает монокарбоновые кислоты (т. е. органические соединения, содержащие одну карбоксильную группу), такие как молочная кислота, и поликарбоновые кислоты (т. е. органические соединения, содержащие две или более карбоксильных групп), такие как лимонная кислота.
В контексте настоящего документа термин «соль карбоновой кислоты» относится к натриевой или калиевой соли карбоновой кислоты.
Предпочтительно, стабилизирующее средство выбрано из карбоновых кислот, солей карбоновых кислот, аскорбиновой кислоты, солей аскорбиновой кислоты и их смесей. Еще более предпочтительно, стабилизирующее средство выбрано из лимонной кислоты, солей лимонной кислоты, молочной кислоты, солей молочной кислоты, аскорбиновой кислоты, солей аскорбиновой кислоты и их смесей. К солям лимонной кислоты относятся дигидроцитрат мононатрия, гидроцитрат динатрия, цитрат тринатрия, дигидроцитрат монокалия, гидроцитрат дикалия и цитрат трикалия. К солям молочной кислоты относятся лактат натрия и лактат калия. К солям аскорбиновой кислоты относятся аскорбат натрия и аскорбат калия. В наиболее предпочтительном варианте осуществления стабилизирующее средство выбрано из лимонной кислоты, дигидроцитрата мононатрия, гидроцитрата динатрия, цитрата тринатрия, дигидроцитрата монокалия, гидроцитрата дикалия и цитрата трикалия, а также их смесей.
Преимущественно, заявляемый и описываемый в настоящем документе способ изготовления позволяет интегрировать любую активную репортерную молекулу рамановского рассеяния в SERS-метку. К предпочтительным активным репортерным молекулам рамановского рассеяния относятся полностью сопряженные молекулы, содержащие арильную группу, замещенную одним или несколькими заместителями, выбранными из NR1R2, -SH, -≡, -≡N и -N═, предпочтительно из -NR1R2 и -SH, и/или N-содержащую гетероарильную группу, и/или S-содержащую гетероарильную группу, при этом остатки R1 и R2 независимо друг от друга выбраны из -H и алкила, предпочтительно из -H и C1-C4-алкила.
Как известно специалисту в области органической химии, полностью сопряженная молекула представляет собой молекулу, имеющую систему сопряженных электронов, охватывающую всю молекулу. Система сопряженных электронов представляет собой систему соединенных p-орбиталей с делокализованными электронами.
Как хорошо известно специалисту в настоящей области техники, «арильная группа» представляет собой группу, полученную из моноциклического или полициклического ароматического углеводородного соединения путем удаления одного атома водорода от кольцевого атома углерода. Примеры арильных групп включают без ограничения фенильную, нафтильную, антраценильную, фенантрильную и пиренильную.
S-содержащее гетероароматическое соединение представляет собой ароматическое соединение, содержащее гетероатом серы как часть циклической сопряженной π-системы. Как часть циклической сопряженной π-системы, S-содержащее гетероароматическое соединение может дополнительно содержать один или несколько атомов азота. Примеры S-содержащих гетероарильных групп включают без ограничения тиофенильную, тиазолильную, изотиазолильную, тиадиазолильную, бензотиофенильную, бензотиазолильную, бензоизотиазолильную, бензотиадиазолильную, имидазотиазолильную и имидазотиадиазолильную.
N-содержащее гетероароматическое соединение представляет собой ароматическое соединение, содержащее по меньшей мере один гетероатом азота как часть циклической сопряженной π-системы. Как часть циклической сопряженной π-системы, N-содержащее гетероароматическое соединение может дополнительно содержать один или несколько атомов кислорода. Примеры N-содержащих гетероарильных групп включают без ограничения имидазолильную, пиразолильную, триазолильную, тетразолильную, бензоимидазолильную, индазолильную, бензотриазолильную, пиридинильную, пиримидинильную, пиридазинильную, триазинильную, хинолинильную, изохинолинильную, диазанфатильную, хиналозинильную, циннолинильную, фталазинильную, хиноксалинильную, пуринильную, азафенантрильную, диазафенантрильную, азаантраценильную, диазаантраценильную, азапиренильную, диазапиренильную, оксазолильную, изоксазолильную, оксадиазолильную, бензоксазолильную, бензизоксазолильную и бензоксадиазолильную.
К предпочтительным активным репортерным молекулам рамановского рассеяния относятся без ограничения следующие:
- полностью сопряженное соединение, состоящее из арильной группы, замещенной одним или несколькими заместителями, выбранными из -NR1R2, -SH, -≡, -≡N и -N═, предпочтительно из -NR1R2 и -SH, которая соединена напрямую или посредством линкера -L1- с арильной группой, замещенной одним или несколькими заместителями, выбранными из перечня, включающего аминогруппу (-NH2), N-алкиламиногруппу, N,N-диалкиламиногруппу, тиоловую группу, этинильную группу, цианогруппу и изоцианидную группу, N-содержащую гетероарильную группу или S-содержащую гетероарильную группу, при этом
заместители R1 и R2 имеют значения, которые определены в настоящем документе;
линкер -L1- выбран из -CR8═CR9-, -N=N-, -≡-, -CR10═CR11-o-C6H4-, -CR10═CR11-m-C6H4-, -CR10═CR11-p-C6H4-, -CR10═CR11-o-C6H4-CR12═CR13-, -CR10═CR11-m-C6H4-CR12═CR13-, -CR10═CR11-p-C6H4-CR12═CR13-, -CR14═N-N═CR15-,
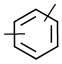 ,
,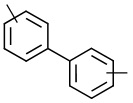 ,
,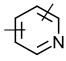 ,
,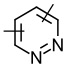 ,
,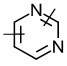 ,
,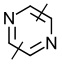 ,
,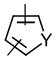 ,
,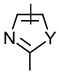 ,
,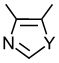 ,
, ,
,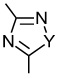 ,
,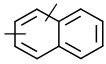 ,
, ,
,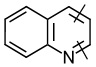 ,
,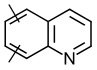 ,
,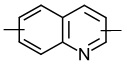 ,
,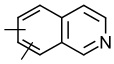 ,
,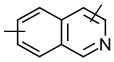 ,
,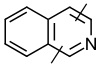 ,
,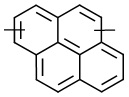 ,
,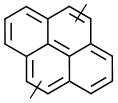 ,
,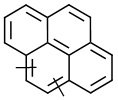 ,
, ;
;
и
заместители R8 - R15 выбраны из водорода, алкила, алкокси, алкилтио, формила, циано, нитро, галогенида, гидроксикарбонила и алкоксикарбонила;
- полностью сопряженное соединение, состоящее из N-содержащей гетероарильной группы, которая соединена напрямую или посредством линкера -L1- с N-содержащей гетероарильной группой или S-содержащей гетероарильной группой,
при этом
линкер -L1- выбран из -CR8═CR9-, -N=N-, -≡-, -CR10═CR11-o-C6H4-, -CR10═CR11-m-C6H4-, -CR10═CR11-p-C6H4-, -CR10═CR11-o-C6H4-CR12═CR13-, -CR10═CR11-m-C6H4-CR12═CR13-, -CR10═CR11-p-C6H4-CR12═CR13-, -CR14═N-N═CR15-,
 ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ;
;
и
заместители R8 - R15 выбраны из водорода, алкила, алкокси, алкилтио, формила, циано, нитро, галогенида, гидроксикарбонила и алкоксикарбонила;
- полностью сопряженное соединение, состоящее из S-содержащей гетероарильной группы, которая соединена напрямую или посредством линкера -L1- с S-содержащей гетероарильной группой,
при этом
линкер -L1- выбран из -CR8═CR9-, -N=N-, -≡-, -CR10═CR11-o-C6H4-, -CR10═CR11-m-C6H4-, -CR10═CR11-p-C6H4-, -CR10═CR11-o-C6H4-CR12═CR13-, -CR10═CR11-m-C6H4-CR12═CR13-, -CR10═CR11-p-C6H4-CR12═CR13-, -CR14═N-N═CR15-,
 ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ;
;
и заместители R8 - R15 выбраны из водорода, алкила, алкокси, алкилтио, формила, циано, нитро, галогенида, гидроксикарбонила и алкоксикарбонила;
и
- полностью сопряженное соединение, состоящее из арильной группы, замещенной одним или несколькими, предпочтительно по меньшей мере двумя, заместителями, выбранными из -NR1R2, -SH, -≡, -≡N та -N═, предпочтительно из -NR1R2 и -SH, N-содержащей гетероарильной группы, необязательно замещенной одним или несколькими заместителями, выбранными из -NR3R4, -SH, -≡, -≡N и -N═, или S-содержащей гетероарильной группы, необязательно замещенной одним или несколькими заместителями, выбранными из -NR5R6, -SH, -≡, -≡N и -N═, соединенной напрямую с атомом водорода, при этом заместители R1 и R2 имеют значения, определенные в настоящем документе, и заместители R3 - R6 независимо друг от друга выбраны из -H и алкила, предпочтительно из -H и C1-C4-алкила.
Арильная группа, замещенная одним или несколькими заместителями, выбранными из -NR1R2, -SH, -≡, -≡N и -N═, предпочтительно из -NR1R2 и -SH, может содержать один или несколько дополнительных заместителей, предпочтительно выбранных из гидрокси, алкила, алкокси, алкилтио, формила, нитро, галогенида, гидроксикарбонила, алкоксикарбонила и О-содержащей гетероарильной группы и более предпочтительно выбранных из алкила, алкокси, алкилтио, галогенидов и О-содержащей гетероарильной группы.
N-содержащая гетероарильная группа и S-содержащая гетероарильная группа могут содержать один или несколько дополнительных заместителей, предпочтительно выбранных из амино, N-алкиламино, N,N-диалкиламино, тиола, гидрокси, алкила, алкокси, алкилтио, формила, циано, изоцианида, этинила, нитро, галогенида, гидроксикарбонила, алкоксикарбонила и О-содержащей гетероарильной группы, предпочтительно из алкильной, алкокси, алкилтио, галогенидов и O-содержащей гетероарильной группы.
Примеры О-содержащих гетероарильных групп включают без ограничения фуранильную, бензофуранильную, изобензофуранильную, оксазолильную, изоксазолильную, бензоксазолильную и оксадиазолильную.
Предпочтительным активным репортерным соединением рамановского рассеяния является соединение общей формулы (I),
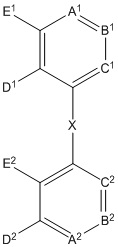
при этом
A1, B1 и C1 независимо друг от друга выбраны из N, CR16 и CR17, при условии, что только один из A1, B1 и C1 представляет собой N;
A2, B2 и C2 независимо друг от друга выбраны из N, CR18 и CR19, при условии, что только один из A2, B2 и C2 представляет собой N;
E1, D1, E2, D2, R16, R17, R18 и R19 независимо друг от друга выбраны из водорода, амино, N-алкиламино, N,N-диалкиламино, тиола, гидрокси, алкила, алкокси, алкилтио, формила, циано, изоцианида, алкинила, нитро, галогенида, гидроксикарбонила, алкоксикарбонила и О-содержащей гетероарильной группы, предпочтительно из водорода, алкила, алкокси, алкилтио, галогенидов и О-содержащей гетероарильной группы; и
X представляет собой одинарную связь или линкер -L2-, выбранный из -CR8═CR9-, -N=N-, -≡-, -CR10═CR11-o-C6H4-, -CR10═CR11-m-C6H4-, -CR10═CR11-p-C6H4-, -CR10═CR11-o-C6H4-CR12═CR13-, -CR10═CR11-m-C6H4-CR12═CR13-, -CR10═CR11-p-C6H4-CR12═CR13-, -CR14═N-N═CR15-,
 ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ;
;
при этом R8 - R15 выбраны из водорода, алкила, алкокси, алкилтио, формила, циано, нитро, галогенида, гидроксикарбонила и алкоксикарбонила.
Предпочтительно, остатки A1 и A2 представляют собой N в общей формуле (I). Более предпочтительно, остатки A1 и A2 представляют собой N, а заместители E1, D1, E2, D2, R16, R17, R18 и R19 представляют собой водород в общей формуле (I).
К активным репортерным молекулам рамановского рассеяния относятся без ограничения следующие: 2-меркаптопиридин; бензолтиол; меркаптобензойная кислота; 4-нитробензолтиол; 3,4-дихлорбензолтиол; 3-фтортиофенол; 4-фтортиофенол; 3-5-бис(трифторметил)бензолтиол; 4-меркаптофенол; бифенил-4-тиол, 7-меркапто-4-метилкумарин, 1-(4-гидроксифенил)-1H-тетразол-5-тиол, 2-фтортиофенол, 2-нафталинтиол, 4-(((3-меркапто-5-(2-метоксифенил)-4H-1,2,4-триазол-4-ил)имино)метил)фенол, (2-трифторметил)бензолтиол, 4-аминотиофенол, 1-нафталинтиол, 1,1',4,1''-терфенил-4-тиол, бифенил-4,4'-дитиол, тиосалициловая кислота, 4-(((3-меркапто-5-(2-пиридинил)-4H-1,2,4-триазол-4-ил)имино)метил)-1,2-бензолдиол, 4-(((3-меркапто-5-(2-пиридинил)-4H-1,2,4-триазол-4-ил)имино)метил)бензойная кислота, 2,3,4,6-тетрафторбензолтиол, (5-(4-метоксифенил)-1,3,4-оксидазол-2-тиол), (E)-1,2-ди(пиридин-4-ил)этен, 5-(пиридин-4-ил)-1,3,4-оксадиазол-2-тиол и 1,4-бис((E)-2-(пиридин-4-ил)винил)бензол.
Первый коллоид, полученный на стадии a), характеризуется значением ζ-потенциала ниже или равным -25 мВ. Второй коллоид, полученный на стадии b), характеризуется значением ζ-потенциала ниже или равным -25 мВ.
В контексте настоящего документа значение ζ-потенциала коллоида относится к значению ζ-потенциала, измеренному для указанного коллоида при концентрации 0,05 мг материала наночастиц/мл с помощью Malvern Zetasizer Nano-ZS с 1-мл изогнутыми капиллярными кюветами. Если необходимо, а именно в случае коллоидов с концентрацией выше 0,05 мг материала наночастиц/мл, перед измерением ζ-потенциала коллоид разводят деионизированной водой до достижения концентрации материала наночастиц 0,05 мг/мл.
Предпочтительно, концентрация материала наночастиц (мг/мл) в первом коллоиде и во втором коллоиде ниже 0,66 мг/мл и более предпочтительно составляет от приблизительно 0,05 мг/мл до приблизительно 0,30 мг/мл, для примера, 0,05 мг/мл, 0,10 мг/мл, 0,15 мг/мл, 0,20 мг/мл, 0,25 мг/мл и 0,30 мг/мл.
После объединения первого коллоида со вторым коллоидом, например путем простого добавления второго коллоида к первому коллоиду таким образом, чтобы соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло от приблизительно 25 : 1 до приблизительно 1 : 1, предпочтительно от приблизительно 5 : 1 до приблизительно 1 : 1, более предпочтительно от приблизительно 4 : 1 до приблизительно 3 : 1, индуцируется агрегация наночастиц. Описываемая в настоящем документе агрегация заключается в избирательной агрегации наночастиц второго коллоида с наночастицами первого коллоида, т. е. отсутствует агрегация наночастиц первого коллоида с наночастицами первого коллоида, а также отсутствует или имеет место незначительная агрегация наночастиц второго коллоида с наночастицами второго коллоида.
Агрегацию наночастиц индуцируют с помощью любой из стадий d1) - d3) или их комбинации:
d1) смешивание третьего коллоида, полученного на стадии c), при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3;
d2) добавление раствора соли, предпочтительно раствора неорганической соли, к третьему коллоиду, полученному на стадии c);
d3) добавление водорастворимого растворителя к третьему коллоиду, полученному на стадии c).
В предпочтительном варианте осуществления индукция агрегации наночастиц предусматривает стадию d1), а именно смешивание третьего коллоида, полученного на стадии c), при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3. Суммарный электрический заряд активной репортерной молекулы рамановского рассеяния и значение pH, соответствующее указанному суммарному электрическому заряду, можно спрогнозировать с помощью таких онлайн-инструментов, как Chemicalize.com (Chemicalize. ChemAxon. http://chemicalize.com/#/calculation). При pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3, происходит избирательная агрегация наночастиц первого коллоида с наночастицами второго коллоида.
Альтернативно, индукция агрегации наночастиц предусматривает стадию d2) добавления раствора соли, предпочтительно раствора неорганической соли, к третьему коллоиду, полученному на стадии c). Индуцируемая солями агрегация наночастиц является хорошо известным для специалистов в области коллоидной химии способом индукции агрегации наночастиц (ChemPhysChem 2018, 19, 24 - 28). Примеры неорганических солей, которые необходимо применять на стадии d2) способа изготовления, в форме раствора, такого как водный раствор, включают без ограничения фторид натрия, хлорид натрия, бромид натрия, йодид натрия, хлорид магния, хлорид калия и их смеси.
В дополнительном альтернативном варианте осуществления индукция агрегации наночастиц предусматривает стадию d3), а именно добавление водорастворимого растворителя к третьему коллоиду, полученному на стадии c). Водорастворимый растворитель предпочтительно выбран из перечня, включающего метанол, этанол, пропанол, изопропанол, тетрагидрофуран, N-метил-2-пирролидон (NMP), диметилсульфоксид (DMSO), N,N-диметилформамид (DMF), ацетон и ацетонитрил.
Предпочтительный способ изготовления по настоящему изобретению предусматривает следующие стадии:
a) получение первого коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
b) получение второго коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, активной репортерной молекулы рамановского рассеяния общей формулы (I), адсорбированной на поверхности указанных наночастиц, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
c) объединение первого коллоида со вторым коллоидом таким образом, чтобы соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло от приблизительно 25 : 1 до приблизительно 1 : 1, предпочтительно от приблизительно 5 : 1 до приблизительно 1 : 1, более предпочтительно от приблизительно 4 : 1 до приблизительно 3 : 1 с получением третьего коллоида;
d) индукцию агрегации наночастиц с помощью любой из стадий d1) - d3) или их комбинации:
d1) смешивание третьего коллоида, полученного на стадии c), при pH в диапазоне от приблизительно 2,2 до приблизительно 6,1, предпочтительно от приблизительно 2,6 до приблизительно 5,7;
d2) добавление раствора соли, предпочтительно раствора неорганической соли, к третьему коллоиду, полученному на стадии c);
d3) добавление водорастворимого растворителя к третьему коллоиду, полученному на стадии c); и
e) остановку агрегации.
Предпочтительно, в описанных в настоящем документе способах изготовления стадия b) предусматривает следующие стадии, осуществляемые в порядке b1)-b3):
b1) получение коллоида, содержащего наночастицы с плазмонной поверхностью и по существу одинаковым размером, диспергированные в водном растворителе, и стабилизирующее средство, адсорбированное на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
b2) доведение pH коллоида до значения, превышающего наиболее низкое значение pH, при котором активные репортерные молекулы рамановского рассеяния, которые должны адсорбироваться на поверхности наночастиц, не несут суммарный электрический заряд, при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ, предпочтительно ниже -40 мВ; и
b3) добавление раствора активных молекул рамановского рассеяния в растворителе к коллоиду, полученному на стадии b2), при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ.
Коллоид, полученный на стадии b1) заявляемого в настоящем документе способа изготовления, фактически состоит из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц. Первый коллоид, полученный на стадии а) заявляемого в настоящем документе способа изготовления, фактически состоит из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц. Второй коллоид, полученный на стадии b) заявляемого в настоящем документе способа изготовления, фактически состоит из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, активных репортерных молекул рамановского рассеяния, адсорбированных на поверхности указанных наночастиц, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц. Таким образом, наночастицы первого коллоида и наночастицы второго коллоида не несут на своей поверхности молекулы или организмы, обеспечивающие специфическое взаимодействие посредством механизма соответствия «ключ к замку» между наночастицами первого коллоида и наночастицами второго коллоида. Примеры таких молекул включают антитела, белки, антигены, комплементарные цепи ДНК и комплементарные цепи РНК. Примеры таких организмов включают бактерии, вирусы и споры. Таким образом, первый коллоид, второй коллоид, а также коллоид, полученный на стадии b1), помимо того, что они не содержат поверхностно-активных веществ и полимеров, они также не содержат таких молекул, как антитела, белки, антигены, комплементарные цепи ДНК и комплементарные цепи РНК, а также таких организмов, как бактерии, вирусы и споры.
На стадии b2) способа изготовления по настоящему изобретению pH коллоида доводят до значения, превышающего наиболее низкое значение pH, при котором активные репортерные молекулы рамановского рассеяния, которые должны адсорбироваться на поверхности наночастиц, не несут суммарный электрический заряд, при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ, предпочтительно ниже -40 мВ. Суммарный электрический заряд активной репортерной молекулы рамановского рассеяния и значение pH, соответствующее указанному суммарному электрическому заряду, можно спрогнозировать с помощью таких онлайн-инструментов, как Chemicalize.com (Chemicalize. ChemAxon. http://chemicalize.com/#/calculation).
Предпочтительно, на стадии b2) pH коллоида доводят до диапазона от приблизительно 8,2 до приблизительно 12,1, при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ, предпочтительно ниже -40 мВ. В более предпочтительном варианте осуществления pH коллоида доводят на стадии b2) до значения приблизительно 11,0.
На стадии b3) по настоящему изобретению раствор активной репортерной молекулы рамановского рассеяния в растворителе добавляют в коллоид, полученный на стадии b2), при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ. Растворитель, применяемый для получения раствора активной репортерной молекулы рамановского рассеяния, охватывает любой водный растворитель и любой органический растворитель, подходящий для растворения активной репортерной молекулы рамановского рассеяния. Примеры органических растворителей включают без ограничения спирты, предпочтительно выбранные из метанола, этанола, пропанола и изопропанола, тетрагидрофурана, N-метил-2-пирролидона (NMP), диметилсульфоксида (DMSO), N,N-диметилформамида (DMF), ацетона и ацетонитрила. К водным растворителям относятся без ограничения вода и смеси воды и водорастворимых растворителей, таких как метанол, этанол, пропанол, изопропанол, тетрагидрофуран, N-метил-2-пирролидон (NMP), диметилсульфоксид (DMSO),
N,N-диметилформамид (DMF), ацетон и ацетонитрил.
Предпочтительный способ изготовления по настоящему изобретению предусматривает следующие стадии:
a) получение первого коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
b) получение второго коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, активной репортерной молекулы рамановского рассеяния общей формулы (I), адсорбированной на поверхности указанных наночастиц, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
c) объединение первого коллоида со вторым коллоидом таким образом, чтобы соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло от приблизительно 25 : 1 до приблизительно 1 : 1, предпочтительно от приблизительно 5 : 1 до приблизительно 1 : 1, более предпочтительно от 4 : 1 до приблизительно 3 : 1 с получением третьего коллоида;
d) индукцию агрегации наночастиц с помощью любой из стадий d1) - d3) или их комбинации:
d1) смешивание третьего коллоида, полученного на стадии c), при pH в диапазоне от приблизительно 2,2 до приблизительно 6,1, предпочтительно от приблизительно 2,6 до приблизительно 5,7;
d2) добавление раствора соли, предпочтительно раствора неорганической соли, к третьему коллоиду, полученному на стадии c);
d3) добавление водорастворимого растворителя к третьему коллоиду, полученному на стадии c); и
e) остановку агрегации,
при этом стадия b) предусматривает следующие стадии, осуществляемые в порядке b1)-b3):
b1) получение коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
b2) доведение pH коллоида до значения у диапазоне от приблизительно 8,0 до приблизительно 12,1, предпочтительно от приблизительно 8,2 до 12,1, при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ, предпочтительно ниже -40 мВ; и
b3) добавление раствора активной репортерной молекулы рамановского рассеяния общей формулы (I) в растворителе к коллоиду, полученному на стадии b2), при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ.
Авторами настоящего изобретения было обнаружено, что интенсивность сигнала SERS-меток, изготовленных в соответствии с настоящим изобретением, можно дополнительно увеличить путем обеспечения адсорбции субмонослоя или монослоя активных репортерных молекул рамановского рассеяния на поверхности наночастиц, содержащихся во втором коллоиде. Таким образом, дополнительный предпочтительный вариант осуществления по настоящему изобретению относится к способу изготовления SERS-меток, как заявлено в настоящем документе, при этом наночастицы второго коллоида имеют абсорбированный на их поверхности субмонослой или монослой активных репортерных молекул рамановского рассеяния. В контексте настоящего документа монослой активных репортерных молекул рамановского рассеяния, адсорбированных на поверхности наночастиц второго коллоида, относится к слою толщиной в одну активную репортерную молекулу рамановского рассеяния, адсорбированному на поверхности указанных наночастиц. В контексте настоящего документа субмонослой активных репортерных молекул рамановского рассеяния относится к неполному монослою активных репортерных молекул рамановского рассеяния. Для обеспечения того, что субмонослой или монослой активных репортерных молекул рамановского рассеяния адсорбируется на поверхности наночастиц второго коллоида, количество активных репортерных молекул рамановского рассеяния, добавляемых на стадии b3) к коллоиду, полученному на стадии b2), необходимо рассчитывать с помощью хорошо известных специалисту в настоящей области техники способов, учитывающих зависимость от формы и размера наночастиц второго коллоида.
Заявляемый в настоящем документе способ изготовления позволяет также получать SERS-метки, содержащие смесь разных активных репортерных молекул рамановского рассеяния, т. е. смесь из двух или более разных активных репортерных молекул рамановского рассеяния. Это дает особое преимущество, поскольку обеспечивается доступ к ряду SERS-меток, при этом каждая из указанных SERS-меток характеризуется уникальным SERS-сигналом, путем комбинирования в различных соотношениях ограниченного числа различных активных репортерных молекул рамановского рассеяния. Для получения таких SERS-меток наночастицы второго коллоида, полученные на стадии b), подготавливают таким образом, чтобы на их поверхности была абсорбирована смесь различных активных репортерных молекул рамановского рассеяния (т. е. смесь из двух или более различных активных репортерных молекул рамановского рассеяния). Такой второй коллоид можно получить с помощью стадии b3) способа изготовления раствора активных молекул рамановского рассеяния в растворителе, содержащем две или более различных активных репортерных молекул рамановского рассеяния, или путем последовательного осуществления стадии b3) способа изготовления и с применением каждый раз другого раствора, содержащего другую активную репортерную молекулу рамановского рассеяния. Таким образом, дополнительный вариант осуществления по настоящему изобретению относится к способу изготовления, при котором на стадии b3) раствор активных репортерных молекул рамановского рассеяния в растворителе содержит смесь из двух или более различных активных репортерных молекул рамановского рассеяния. Другой дополнительный вариант осуществления по настоящему изобретению относится к способу изготовления, при котором стадию b3) последовательно осуществляют n раз, при этом n≥2, с применением каждый раз раствора, содержащего активную репортерную молекулу рамановского рассеяния, которая структурно отличается от активных репортерных молекул рамановского рассеяния, применяемых в остальных n-1 растворах, применяемых на оставшихся n-1 стадиях. В контексте настоящего документа различные активные репортерные молекулы рамановского рассеяния относятся к активным репортерным молекулам рамановского рассеяния, имеющим различную химическую структуру и обеспечивающим другой спектр SERS.
Для дополнительного увеличения количества агрегатов с малым числом и, как следствие, интенсивности SERS-сигнала, подаваемого SERS-метками, изготовленными с помощью заявляемого в настоящем документе способа изготовления, предпочтительно, чтобы на стадии c) соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло от приблизительно 5 : 1 до приблизительно 1 : 1, предпочтительно от приблизительно 4 : 1 до приблизительно 3 : 1. Как продемонстрировано, например, с помощью примера 10 и фиг. 3b, соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида, составляющее от приблизительно 5 : 1 до приблизительно 1 : 1, обеспечивает доступ к SERS-меткам с высоким количеством агрегатов с малым числом, таких как димеры, тримеры и тетрамеры.
Для индукции агрегации с помощью способа, описанного для стадии d1), необходимо примешать третий коллоид, полученный на стадии c), при pH диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3, что в случае активной репортерной молекулы рамановского рассеяния общей формулы (I) представляет собой pH в диапазоне от приблизительно 2,2 до приблизительно 6,1, предпочтительно от приблизительно 2,6 до приблизительно 5,7. Этого можно достичь либо путем добавления кислого раствора к третьему коллоиду, полученному на стадии c), или путем доведения pH первого коллоида до такого значения, чтобы коллоид, полученный на стадии d1), имел необходимое значение pH.
Таким образом, один вариант осуществления по настоящему изобретению относится к способу изготовления, при котором стадия d1) дополнительно предусматривает добавление кислого раствора к третьему коллоиду, полученному на стадии c), при перемешивании, так чтобы pH полученного коллоида составлял в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3, что в случае активной репортерной молекулы рамановского рассеяния общей формулы (I) представляет собой pH в диапазоне от приблизительно 2,2 до приблизительно 6,1, предпочтительно от приблизительно 2,6 до приблизительно 5,7. Подходящие кислые растворы включают без ограничения уксусную кислоту, соляную кислоту и азотную кислоту.
Во избежание дополнительной стадии изготовления удобно довести значение pH первого коллоида до такой величины, чтобы коллоид, полученный на стадии d1), имел pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3, что в случае активной репортерной молекулы рамановского рассеяния общей формулы (I) представляет собой pH в диапазоне от приблизительно 2,2 до приблизительно 6,1, предпочтительно от приблизительно 2,6 до приблизительно 5,7.
Заявляемый в настоящем документе способ изготовления также предусматривает стадию e) остановки агрегации. Предпочтительно, стадия e) предусматривает любую из следующих стадий e1) - e4):
e1) доведение pH коллоида, полученного на стадии d), до значения, превышающего наиболее низкое значение pH, при котором активные репортерные молекулы рамановского рассеяния, которые должны адсорбироваться на поверхности наночастиц, не несут суммарный электрический заряд;
e2) разведение коллоида, полученного на стадии d), водой, предпочтительно так, чтобы концентрация наночастиц в коллоиде стала ниже 6*109 наночастиц/мл;
e3) добавление полимера к коллоиду, полученному на стадии d);
e4) добавление предшественника диэлектрического материала к коллоиду, полученному на стадии d).
В заявляемом в настоящем документе способе изготовления по настоящему изобретению агрегацию можно остановить любым из способов e1) - e4).
Доведение pH коллоида, полученного на стадии d), до значения, превышающего наиболее низкое значение pH, при котором активные репортерные молекулы рамановского рассеяния, которые должны адсорбироваться на поверхности наночастиц, не несут суммарный электрический заряд, как описано на стадии e1), что приводит к увеличению количества электростатических отталкиваний между агрегатами наночастиц, приводя к остановке процесса агрегации. Суммарный электрический заряд активной репортерной молекулы рамановского рассеяния и значение pH, соответствующее указанному суммарному электрическому заряду, можно спрогнозировать с помощью таких онлайн-инструментов, как Chemicalize.com (Chemicalize. ChemAxon. http://chemicalize.com/#/calculation).
Добавление полимера к коллоиду, полученному на стадии d), как описано для стадии e3), приводит к увеличению количества стерических отталкиваний между агрегатами наночастиц и приводит к остановке процесса агрегации. Преимущественно, чтобы полимер, применяемый на стадии e3), не оказывал влияния на SERS-сигнал от SERS-метки. К подходящим полимерам относятся без ограничения поливинилпирролидон и полиэтиленгликоль.
Добавление предшественника диэлектрического материала к коллоиду, полученному на стадии d), как описано на стадии e4), приводит к инкапсуляции агрегатов наночастиц по меньшей мере с одним слоем диэлектрического материала, что стабилизирует SERS-метки и безоговорочно приводит к остановке процесса агрегации. Предпочтительно, предшественник диэлектрического материала представляет собой предшественник диоксида кремния. К предшественникам диоксида кремния относятся без ограничения растворы тетраэтилортосиликата и 3-аминопропилтриметоксисилана в этаноле, растворы тетраэтилортосиликата и (3-меркаптопропил)триметоксисилана в этаноле, растворы силиката натрия в воде и растворы (3-меркаптопропил)триметоксисилана в воде.
Альтернативно, процесс агрегации можно остановить путем разведения коллоида, полученного на стадии d), водой. Предпочтительно, агрегацию останавливают путем разведения коллоида, полученного на стадии d), водой так, чтобы достигалась концентрация материала наночастиц [мкг/мл], которая ниже или равна 12,5 мкг/мл (см., например: E1 - E8, E11 - E14). Альтернативно, агрегацию останавливают путем разведения коллоида, полученного на стадии d), водой так, чтобы концентрация наночастиц стала ниже 6*109 наночастиц/мл.
Дополнительный предпочтительный вариант осуществления настоящего изобретения относится к способу изготовления SERS-меток, при котором стадия e) фактически состоит из стадии e3), и способ изготовления дополнительно предусматривает разведение коллоида, полученного на стадии e3), водой и/или нанесение на SERS-метки покрытия диэлектрического материала.
В дополнительном предпочтительном варианте осуществления стадии c) и d) заявляемого в настоящем документе способа изготовления осуществляют одновременно в проточной системе непрерывного действия. В данном конкретном способе изготовления применяют проточный реактор непрерывного действия. Такой проточный реактор непрерывного действия схематически изображен на фиг. 1b и фиг. 1c и состоит из двух резервуаров (111b, 112b, 111c, 112c) под давлением, соединенных с помощью трубки с тройником (113b, 113c) и резервуаром (114b, 114c) для сбора. В резервуаре (111b, 111c) под давлением хранится второй коллоид, а в резервуаре (112b, 112c) под давлением хранится первый коллоид. Для сбора SERS-меток и, необязательно, для остановки агрегации (114c) применяют сообщающийся с атмосферой сосуд (114b, 114c). Трубку, соединяющую каждый из резервуаров (111b, 112b, 111c, 112c) под давлением с тройником (113b, 113c), применяют для транспортировки коллоидов. Дополнительную трубку, соединяющую тройник (113b, 113c) с резервуаром (114b, 114c) для сбора, применяют для осуществления агрегации. Агрегаты наночастиц, полученные в результате агрегации, собирают в сосуд (114b) для сбора, где останавливают агрегацию.
При одновременном осуществлении стадий c) и d) способа изготовления в проточной системе непрерывного действия дополнительно предпочтительно, чтобы стадию e) также осуществляли в проточной системе непрерывного действия.
Как упомянуто выше, наночастицы, применяемые в способе изготовления SERS-меток, могут иметь любую форму, которую можно получить, такую как сфера, сфероид, стержень, диск, призма и куб. Предпочтительно, форма наночастиц с плазмонной поверхностью, применяемых в заявляемом в настоящем документе способе изготовления по настоящему изобретению, выбрана из сферы и сфероида. Еще более предпочтительно, указанные наночастицы имеют форму сфероида.
В предпочтительном варианте осуществления наночастицы первого коллоида и наночастицы второго коллоида имеют одинаковый размер. Удобно, чтобы при таком способе изготовления SERS-меток коллоидом, применяемым для получения второго коллоида (т. е. коллоида, получаемого на стадии b1)), был первый коллоид.
В альтернативном варианте осуществления размер наночастиц первого коллоида отличается от размера наночастиц второго коллоида. Например, размер наночастиц в первом коллоиде может быть меньше размера наночастиц во втором коллоиде, в результате чего SERS-метки структуры, схожие с таковой у SERS-меток, изображенных на фиг. 3а, или размер наночастиц в первом коллоиде может превышать размер наночастиц во втором коллоиде, в результате чего SERS-метки имеют структуры, схожие с таковой SERS-меток, изображенных на фиг. 3b.
Заявляемый в настоящем документе способ изготовления предпочтительно осуществляют с коллоидами, при этом плазмонная поверхность наночастиц в первом коллоиде и/или плазмонная поверхность наночастиц во втором коллоиде состоит из золота, более предпочтительно с коллоидами, содержащими твердые наночастицы золота, и еще более предпочтительно с коллоидами золота, стабилизированными цитратом.
Примеры
Настоящее изобретение далее будет описано более подробно в соответствии со следующими неограничивающими примерами.
Общая часть
Описанные далее реагенты получали от следующих поставщиков:
Тригидрат хлораурата золота (>99,9%; CAS № 16961-25-4), боргидрид натрия (99,99%; CAS № 16940-66-2), трехосновный дигидрат цитрата натрия (≥99,5%; CAS № 6132-04-3), (E)-1,2-ди(пиридин-4-ил)этен (97%; CAS № 13362-78-2), 5-(пиридин-4-ил)-1,3,4-оксадиазол-2-тиол (97%; CAS № 15264-63-8), гидроксид натрия (реагент ACS, ≥97%; CAS № 1310-73-2), гидрохлорид гидроксиламина (99,999%; CAS № 5470-11-1), терефталевый альдегид (ReagentPlus, 99%, CAS № 623-27-8), 4-метилпиридин (99%; CAS № 108-89-4), уксусный ангидрид (ReagentPlus, ≥99%; CAS № 108-24-7), дихлорметан (безводный, 99,8%; CAS № 75-09-2) и метанол (HPLC, ≥99,9%; CAS № 67-56-1) были приобретены у Sigma Aldrich. Соляная кислота (со следовым содержанием металлов, 34-37%; CAS № 7647-01-0) была приобретена у Fisher Scientific.
Значения ζ-потенциала измеряли с применением Malvern Zetasizer Nano-ZS с 1-мл изогнутыми капиллярными кюветами (DTS1060). Спектры оптического поглощения регистрировали на спектрофотометре Agilent 8453 и Perkin Elmer Lambda 650.
Изображения, полученные с помощью сканирующего электронного микроскопа (SEM), фиксировали на Hitachi S-4500.
785-нм рамановские спектры получали на Ocean Optics QE 6500.
Размер номинальных 140-нм золотых коллоидных частиц определяли путем отправки образца в EAG Laboratories для получения изображений трансмиссионной электронной микроскопии (ТЕМ). Изображения анализировали с помощью программного обеспечения ImageJ (https://imagej.nih.gov/ij/). Партия считалась номинально соответствующей 140 нм, если среднечисловой размер частиц находился в пределах ± 9 нм от номинального диаметра, при этом среднечисленный размер частиц определяли путем измерения 230 отдельных частиц на микрофотографиях TEM. Связанной с размером характеристикой, выбранной для описания отдельных частиц, был диаметр «эквивалентного круга» (CE), который соответствует диаметру круга, площадь которого равна площади ортогональной проекции частицы.
Диаметр наночастиц золота d (нм) для партий наночастиц размером 40, 60, 90 нм рассчитывали способом, описанным у Haiss и соавт. (Anal. Chem. 2007, 79, 4215-4221), с применением следующего уравнения:
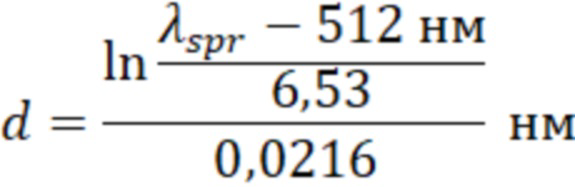
где λspr обозначает положение пика поверхностного плазмонного резонанса на графике экстинкции, полученном для образца коллоида на Perkin Elmer Lambda 650, работающем в УФ/видимом спектре. Партию считали номинально соответствующей 40 нм, 60 нм или 90 нм, если положение пика поверхностного плазмонного резонанса коррелировало с диаметром в пределах ± 9 нм от номинального диаметра.
Получение исходного раствора коллоидного Au (S1 - S4)
Исходные растворы коллоидного золота (S1 - S4), характеризующиеся размером наночастиц Au (нм), концентрациями Au (мг/мл) и значениями pH, указанными в таблице 1, изготавливали так, как описано ниже.
I.1 Получение исходного раствора 40-нм коллоидного золота (S1)
В снабженном рубашкой и тщательно очищенном 100-л стеклянном реакторе (ChemGlass) 79,5 л воды с сопротивлением 17 МОм охлаждали до 3,5 ± 0,5oC. Добавляли тригидрат хлораурата золота (100 г) в виде 20 мас. % раствора в воде при перемешивании лопастной мешалкой на скорости 400 об/мин. Объединяли трехосновный дигидрат цитрата натрия (174,3 г) в виде 30 мас. % раствора в воде и гидрохлорид гидроксиламина (155,6 г) в виде 23,5 мас. % раствора в воде и добавляли в реактор. Спустя 10 с в реактор вносили 800 мкл боргидрида натрия в виде 0,063 мас. % раствора в 0,01 н. гидроксида натрия. Реагентам давали прореагировать в течение 2 минут, а затем выливали в чистый барабан с получением исходного раствора 40-нм коллоидного Au (S1) с концентрацией золота 0,25 мг Au/мл и значением pH приблизительно 2,4.
I.2 Получение исходного раствора 60-нм коллоидного золота (S2)
В снабженном рубашкой и тщательно очищенном 100-л стеклянном реакторе (ChemGlass) 79,5 л воды с сопротивлением 17 МОм охлаждали до 3,5 ± 0,5oC. Добавляли тригидрат хлораурата золота (200 г) в виде 20 мас. % раствора в воде при перемешивании лопастной мешалкой на скорости 400 об/мин. Объединяли трехосновный дигидрат цитрата натрия (173,3 г) в виде 30 мас. % раствора в воде и гидрохлорид гидроксиламина (217,1 г) в виде 17,5 мас. % раствора в воде и добавляли в реактор. Спустя 10 с в реактор вносили 800 мкл боргидрида натрия в виде 0,052 мас. % раствора в 0,01 н. гидроксида натрия. Реагентам давали прореагировать в течение 2 минут, а затем выливали в чистый барабан. Партию разводили водой с сопротивлением 17 МОм до 160 л с получением исходного раствора 60-нм коллоидного Au (S2) с концентрацией золота 0,25 мг Au/мл и pH приблизительно 2,4.
I.3 Получение исходного раствора 90-нм коллоидного золота (S3)
В снабженном рубашкой и тщательно очищенном 100-л стеклянном реакторе (ChemGlass) 79,5 л воды с сопротивлением 17 МОм охлаждали до 3,5 ± 0,5oC. Добавляли тригидрат хлораурата золота (200 г) в виде 20 мас. % раствора в воде при перемешивании лопастной мешалкой на скорости 400 об/мин. Объединяли трехосновный дигидрат цитрата натрия (173,3 г) в виде 30 мас. % раствора в воде и гидрохлорид гидроксиламина (217,1 г) в виде 17,5 мас. % раствора в воде и добавляли в реактор. Спустя 10 с в реактор вносили 900 мкл боргидрида натрия в виде 0,01 мас. % раствора в 0,01 н. гидроксида натрия. Реагентам давали прореагировать в течение 2 минут, а затем выливали в чистый барабан. Партию разводили водой с сопротивлением 17 MОм до 160 л с получением исходного раствора 90-нм коллоидного Au (S3) с концентрацией золота 0,25 мг Au/мл и pH приблизительно 2,4.
I.4 Получение исходного раствора 140-нм коллоидного золота (S4)
В 2-л стеклянном бутыле перемешивали 1,5 л воды с сопротивлением 17 МОм при комнатной температуре. Добавляли тригидрат хлораурата золота (2,5 г) в виде 20 мас. % раствора в воде при перемешивании. Объединяли трехосновный дигидрат цитрата натрия (15,37 г) в виде 30,7 мас. % раствора в воде и гидрохлорид гидроксиламина (8,37 г) в виде 16,7 мас. % раствора в воде и добавляли в реактор. Спустя 5 с в реактор вносили 25 мкл боргидрида натрия в виде 0,01 мас. % раствора в 0,01 н. гидроксида натрия. Дополнительное перемешивание в течение 15 минут давало исходный раствор 140-нм коллоидного Au (S4) с концентрацией золота 0,25 мг Au/мл и pH приблизительно 2,4.
Таблица 1. Результаты изучения характеристик исходных растворов коллоидного Au (S1 - S4)

Получение первого коллоида (A1 - A9) (стадия a) способа изготовления)
Первые коллоиды (A1 - A9) получали из растворов коллоидного Au S1, S2 и S4. При необходимости (в случае, например, коллоидов Au A1 и A7) исходные растворы коллоидного Au разводили деионизированной водой так, чтобы получалась концентрация Au (мг/мл), указанная в таблице 2. Дополнительно, при необходимости (в случае, например, коллоидов Au A3, A4, A5, A6, A8, A9) исходные растворы коллоидного Au сами по себе или после разведения обрабатывали водным 0,1 мМ раствором NaOH или водным 0,1 мМ раствором HCl с тем, чтобы довести значение pH первых коллоидов до значения pH, указанного в таблице 2.
Таблица 2. Результаты изучения характеристик первых коллоидов (A1 - A9)

Для применения в способе изготовления по настоящему изобретению подходили только стабильные первые коллоиды, т. е. коллоиды, в которых не было агрегации. Первые коллоиды A1 - A9 были стабильными, т. е. в них нельзя было выявить агрегацию наночастиц Au путем визуального обнаружения изменения цвета с розового на пурпурный. Кроме того, как видно на фиг. 4, стабильным был ряд коллоидов Au, характеризовавшихся значением дзета-потенциала, который был ниже или равным -25 мВ, по результатам измерения, описанного ниже в разделе IV. Следовательно, такие коллоиды Au также были пригодны к применению в качестве первых коллоидов в способе изготовления по настоящему изобретению.
Получение второго коллоида, содержащего наночастицы Au и активные репортерные молекулы рамановского рассеяния, адсорбированные на поверхности наночастиц Au (D1 - D11) (стадия b) способа изготовления)
Коллоиды Au (B1 - B8), характеризующиеся концентрациями Au (мг/мл) и значениями pH, указанными в таблице 3, получали из исходных растворов коллоидного Au S1 - S3. Получение предусматривало, при необходимости (в случае, например, коллоидов Au B1 и B5), разведение исходных растворов коллоидного Au деионизированной водой так, чтобы получалась указанная концентрация Au (мг/мл), и доведение значения pH путем добавления водного 1 M раствора NaOH в исходные растворы коллоидного Au как есть или после разведения.
Таблица 3. Результаты изучения характеристик коллоидов Au B1 - B9

Активную репортерную молекулу рамановского рассеяния 1,4-бис((E)-2-(пиридин-4-ил)винил)бензол синтезировали так, как описано ниже.
В 50-мл круглодонную колбу с мешалкой загружали терефталевый альдегид (3,44 г, 25,7 ммоля), 4-метилпиридин (9,57 г, 103 ммоля) и уксусный ангидрид (25 мл). Смесь кипятили в колбе с обратным холодильником до полного удаления альдегида (4 ч, проверяли с помощью TLC). Реакционную смесь охлаждали до комнатной температуры и гасили путем выливания ее в 100 мл ледяной воды. Холодную смесь нейтрализовали до pH 7 с помощью водного 6 н. раствора NaOH, а образовавшийся бурый осадок фильтровали, промывали водой и сушили на воздухе. Экстракция дихлорметаном с последующим концентрированием растворителя досуха давала неочищенный продукт, который очищали с помощью колоночной флэш-хроматографии на силикагеле (метанол/дихлорметан: 5/95) с получением 0,875 г целевой активной репортерной молекулы рамановского рассеяния в виде желтого твердого вещества (12%).
Второй коллоид (D1 - D11), содержащий наночастицы Au с адсорбированными на их поверхности активными репортерными молекулами рамановского рассеяния, получали путем добавления некоторого объема 0,1 мМ раствора активных репортерных молекул рамановского рассеяния в этаноле к 20 мл коллоида Au (B1 - B5, B9) или 3 л коллоида Au (B8) с последующим перемешиванием полученной смеси в течение 30 мин (в случае второго коллоида D1 - D7, D9 - D11)/1 ч (в случае второго коллоида D8) при комнатной температуре. В таблице 4 приведено краткое описание активных репортерных молекул рамановского рассеяния и объемы раствора активных репортерных молекул рамановского рассеяния в этаноле, которые применяли для получения второго коллоида D1 - D11.
Таблица 4. Получение вторых коллоидов D1 - D11
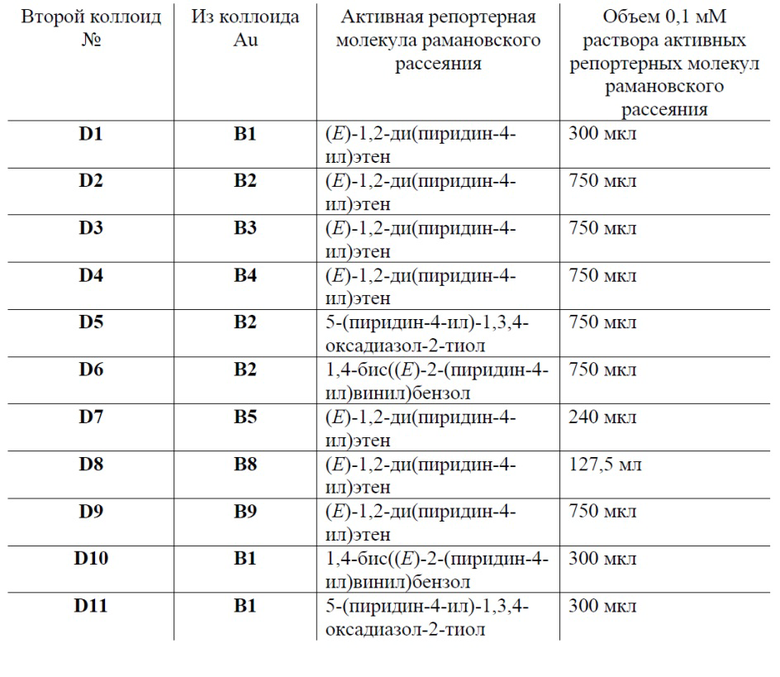
Обработка 20 мл коллоидов Au B6 и B7 со значением pH ниже наиболее низкого значения pH, при котором (E)-1,2-ди(пиридин-4-ил)этен не нес суммарного электрического заряда, по результатам прогнозирования Chemicalize.com, посредством 750 мкл 0,1 мМ раствора (E)-1,2-ди(пиридин-4-ил)этена в этаноле с последующим перемешиванием полученной смеси в течение 30 мин при комнатной температуре приводила к получению нестабильных коллоидов, о чем свидетельствовало визуальное обнаружение изменения цвета смеси с розового на пурпурный при перемешивании. Нестабильные коллоиды нельзя было применять в способе изготовления по настоящему изобретению. Для обеспечения стабильности второго коллоида, т. е. во избежание агрегации наночастиц Au, содержащихся в указанном коллоиде, было важно, чтобы в процессе получения и хранения указанного коллоида значение ζ-потенциала было ниже или равным -25 мВ, а значение pH было выше наиболее низкого значения pH, при котором активная репортерная молекула рамановского рассеяния, адсорбируемая на наночастицах Au, не несет суммарного электрического заряда, при этом указанное значение можно было спрогнозировать, например, с помощью Chemicalize.com. В этом смысле значение pH коллоида Au (B1 - B5, B8, B9), применяемого для получения второго коллоида, перед обработкой активной репортерной молекулой рамановского рассеяния доводили до значения, которое было выше наиболее низкого значения pH, при котором активная репортерная молекула рамановского рассеяния, адсорбируемая на наночастицах Au, содержащихся в коллоиде Au (B1 - B5, B8, B9), не несет суммарный электрический заряд, при этом указанное значение можно было спрогнозировать, например, с помощью Chemicalize.com.
Стабильность первого и второго коллоидов. Для того, чтобы их можно было применять в способе изготовления по настоящему изобретению, дающему SERS-метки с высоким количеством агрегатов малого размера, первый и второй коллоиды должны были быть стабильными, т. е. во время получения и хранения указанных коллоидов необходимо было избежать агрегации наночастиц. Это можно было обеспечить поддержанием значения ζ-потенциала указанных коллоидов на уровне ниже или равном -25 мВ. Как видно на фиг. 4 и в таблице 5, в качестве первого и второго коллоидов в способе изготовления SERS-меток по настоящему изобретению можно было применять ряд коллоидов Au.
ζ-потенциал первого коллоида A2 и вторых коллоидов D2, D5 и D6 измеряли в зависимости от pH при концентрации 0,05 мг Au/мл при комнатной температуре. Результаты представлены в таблице 5 и графически изображены на фиг. 4.
Измерения ζ-потенциала осуществляли на Malvern Zetasizer Nano-ZS с 1-мл изогнутыми капиллярными кюветами. Физические свойства воды при 25°C и золота были предварительно загруженными в устройство. Каждый из первого коллоида A2 и вторых коллоидов D2, D5 и D6 разводили деионизированной водой до концентрации 0,05 мг Au/мл.
Значения ζ-потенциала первого коллоида A2 и второго коллоида D2, D5 и D6 при приблизительно pH, применяемом для синтеза SERS-меток по настоящему изобретению, представлены во 2-м столбце таблицы 5. Значения ζ-потенциала первого коллоида A2 и второго коллоида D2, D5 и D6 при pH, при котором коллоиды становятся нестабильными, представлены в 3-м столбце таблицы 5. Нестабильность коллоида определяли путем визуального обнаружения изменения цвета коллоида с розового на пурпурный.
Таблица 5. Результаты измерения ζ-потенциала первого и второго коллоидов
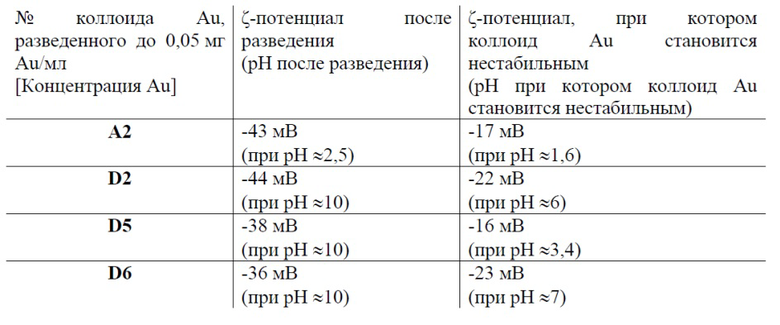
V. Объединение первого коллоида и вторых коллоидов, индукция агрегации и остановка агрегации (стадия c), d) и e) способа изготовления)
V.1 SERS-метки, содержащие наночастицы Au одинакового размера (примеры E1 - E8, E12 - E14)
V.1.a Порционная агрегация (примеры E1 - E7, E12 - E14)
Второй коллоид (D1 - D6, D9 - D11, 20 мл) быстро выливали в 80 мл первого коллоида (A1 - A5, A9) и смесь перемешивали в резервуаре для смешивания при помощи магнитной мешалки. Через 30 секунд после объединения коллоидов отбирали аликвоту объемом 125 мкл и разводили ее водой до 1 мл, тем самым останавливая агрегацию. При таком разведении (12,5 мкг Au/мл, что соответствовало приблизительно 5,72*109 наночастиц Au/мл) агрегация прекращалась, и с помощью лазерного возбуждения на уровне 785 нм и спектрометра QE65000, приобретенного у Ocean Optics Inc., установленного на время для аккумулирования заряда светодиодом в одну секунду, измеряли SERS-сигнал. Результаты измерений SERS-сигнала, осуществляемых на SERS-метках, изготовленных так, как описано выше, показаны в таблице 6.
Как представлено в примерах E1 - E7 и E12 - E14 согласно заявляемому в настоящем документе способу по настоящему изобретению и в сравнительных примерах C1 - C3, избирательная агрегация частиц первого коллоида и частиц второго коллоида не происходила при низких значениях pH, таких как 1,8, и при значениях pH, которые были выше наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имели суммарный электрический заряд от 0 до 0,3, по результатам прогнозирования Chemicalize.com.
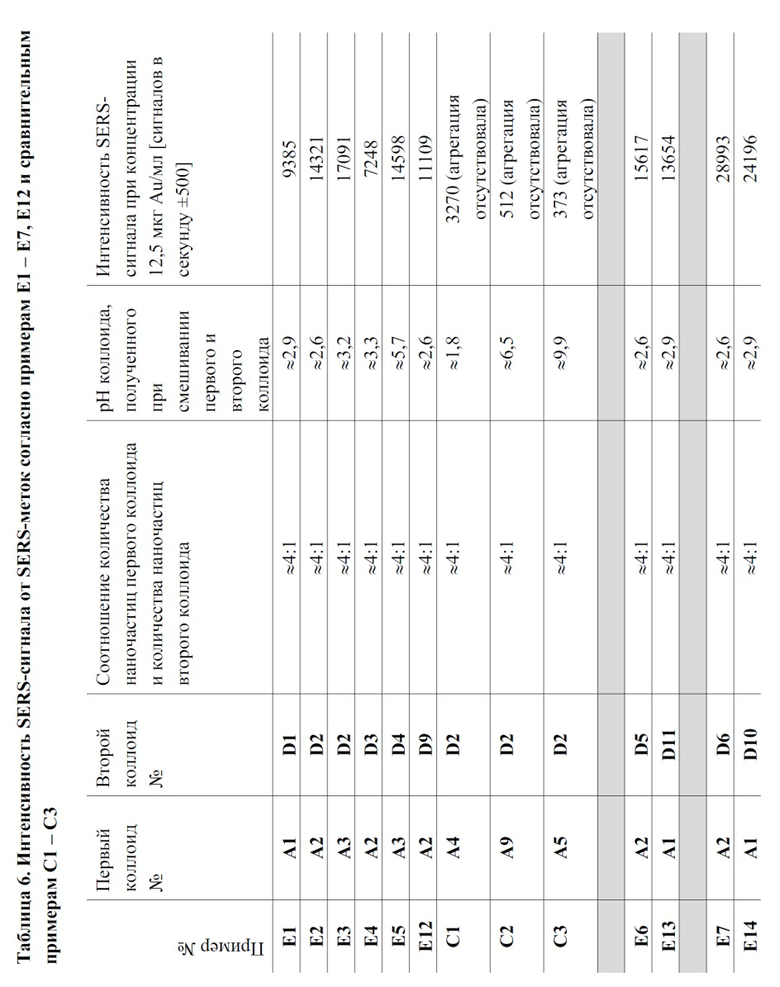
V.1.b Агрегация в проточной системе непрерывного действия (пример E8)
Схема проточного реактора непрерывного действия, применяемого в способе изготовления по настоящему изобретению, представлена на фиг. 1b. Резервуар (111b) под давлением содержал второй коллоид, а второй резервуар (112b) под давлением содержал первый коллоид. Для сбора SERS-меток использовали сообщающийся с атмосферой сосуд (114b), который содержал концентрированный раствор полимера для остановки реакции агрегации. Для транспорта коллоида применяли трубки из прозрачного фторированного этиленпропилена (FEP) от Cole Parmer® Scientific Experts с номинальным внутренним диаметром 8 мм. Для соединения резервуара (111b) под давлением с Т-образным коннектором (113b) использовали 30 см трубки из FEP. Для соединения резервуара (112b) под давлением с Т-образным коннектором (113b) использовали 30 см трубки из FEP. Для соединения Т-образного коннектора (113b) с сосудом (114b) для сбора использовали 7 м трубки из FEP. Данная секция трубки между Т-образным коннектором (113b) и сосудом (114b) для сбора была секцией, в которой происходила агрегация.
Описанные выше коллоиды A8 (12 л) и D8 (3 л) размещались в резервуарах 112b и 111b соответственно. В резервуар (111b), содержащий второй коллоид (D8), подавали давление так, чтобы скорость потока коллоида составляла 0,66 л/мин. В резервуар (112b), содержащий первый коллоид (A8), подавали давление так, чтобы скорость потока коллоида составляла 2,65 л/мин. После объединения в Т-образном коннекторе объединенный коллоид, характеризующийся соотношением количества наночастиц первого коллоида A8 и количества наночастиц второго коллоида D8, составлявшим ≈4:1, имел значение pH приблизительно 4,8 и скорость потока в трубке для агрегации, составлявшую 3,31 л/мин, что давало линейную скорость 1,1 м/с. Измерения SERS проводили через прозрачную трубку из FEP на отметке 1 м по длине трубки для агрегации с помощью зонда, соединенного оптоволоконным кабелем со спектрометром Ocean Optics QE65000 с возбуждением на уровне 785 нм. Время для аккумулирования заряда светодиодом сокращали так, чтобы результат измерения на отметке на конце трубки был равен значению, полученному у аликвоты объемом 50 мкл, отобранной из отверстия трубки и разведенной до 1 мл водой (12,5 мкг Au/мл), т. е. значению у образца, в котором агрегация была остановлена разведением водой, и измеряли с помощью лазерного возбуждения на уровне 785 нм и спектрометра Ocean Optics QE65000 с установленным временем для аккумулирования заряда светодиодом в одну секунду. Результаты измерений SERS представлены графически на фиг. 5 в виде ромбов, соединенных сплошной линией. Интенсивность сигнала SERS от образца, взятого на конце трубки и имевшего результат измерений 12,5 мкг Au/мл, составляла 11044 импульса в секунду [± 500].
V.2 Первый коллоид и второй коллоид содержали наночастицы Au различного размера (примеры E9 - E11)
V.2.a Порционная агрегация (примеры E9 и E10)
Пример E9
Второй коллоид (D7, 30 мл) быстро выливали в первый коллоид (A1, 55 мл) и смесь перемешивали в резервуаре для смешивания при помощи магнитной мешалки. Соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло ≈6,3:1. После 30 секунд перемешивания при pH, равном примерно 2,9, агрегацию останавливали добавлением раствора полимера, и полученные агрегаты дополнительно покрывали диоксидом кремния согласно способу, описанному в US8497131B2, с получением целевых SERS-меток. На пластинки диоксида кремния каплями наносили ~2-мкл аликвоты SERS-меток и высушивали их. Образец визуализировали на автоэмиссионном сканирующем электронном микроскопе Hitachi S-4500, полученное изображение представлено на фиг. 3a. SERS-сигнал измеряли с использованием лазерного возбуждения на уровне 785 нм и спектрометра QE65000, приобретенного у Ocean Optics Inc., с установленным временем для аккумулирования заряда светодиодом в одну секунду. Интенсивность SERS-сигнала, измеренная для 12,5 мкг Au/мл, составляла 18377 импульсов в секунду [± 500].
Пример E10
Второй коллоид (D7, 20 мл) быстро выливали в первый коллоид (A7, 200 мл) и смесь перемешивали в резервуаре для смешивания при помощи магнитной мешалки. Соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло ≈2,65:1.
После 30 секунд перемешивания при pH, равном примерно 2,9, агрегацию останавливали добавлением раствора полимера, и полученные агрегаты покрывали диоксидом кремния согласно способу, описанному в US8497131B2, с получением целевых SERS-меток. На пластинки диоксида кремния каплями наносили ~2-мкл аликвоты SERS-меток и высушивали их. Образец визуализировали на автоэмиссионном сканирующем электронном микроскопе Hitachi S-4500, полученное изображение представлено на фиг. 3b.
V.2.b Агрегация в проточной системе (пример E11)
Схема проточного реактора непрерывного действия, применяемого в способе изготовления по настоящему изобретению, представлена на фиг. 1b. Резервуар (111b) под давлением содержал второй коллоид, а второй резервуар (112b) под давлением содержал первый коллоид. Для сбора SERS-меток и для остановки агрегации применяли сообщающийся с атмосферой сосуд (резервуар для сбора, 114b). Для транспорта коллоида применяли трубки из фторированного этиленпропилена (FEP) от Cole Parmer® Scientific Experts с номинальным внутренним диаметром 8 мм. Для соединения резервуара (111b) под давлением с Т-образным коннектором (113b) использовали 30 см трубки из прозрачного FEP. Для соединения резервуара (112b) под давлением с Т-образным коннектором (113b) использовали 30 см трубки из FEP. Для соединения Т-образного коннектора (113b) с сосудом (114b) для сбора использовали 7 м трубки из FEP. Данная секция трубки между Т-образным коннектором (113b) и сосудом (114b) для сбора была секцией, в которой происходила агрегация.
Описанные выше коллоиды A6 (12 л) и D8 (3 л) размещались в резервуарах 112b и 111b соответственно. В резервуар (111b), содержащий второй коллоид (D8), подавали давление так, чтобы скорость потока коллоида составляла 0,66 л/мин. В резервуар (112b), содержащий первый коллоид (A6), подавали давление так, чтобы скорость потока активированного коллоида составляла 2,65 л/мин. После объединения в Т-образном коннекторе объединенный коллоид, характеризующийся соотношением количества наночастиц первого коллоида A6 и количества наночастиц второго коллоида D8, составлявшим ≈1,2 : 1, имел pH приблизительно 4,8 и скорость потока в трубке для агрегации, составлявшую 3,31 л/мин, что давало линейную скорость 1,1 м/с. Измерения SERS проводили через прозрачную трубку из FEP на отметке 1 м по длине трубки для агрегации с помощью зонда, соединенного оптоволоконным кабелем со спектрометром Ocean Optics QE65000 с возбуждением на уровне 785 нм. Время для аккумулирования заряда светодиодом сокращали так, чтобы результат измерения на отметке на конце трубки был равен значению, полученному у аликвоты объемом 50 мкл, отобранной из отверстия трубки и разведенной до 1 мл водой (12,5 мкг Au/мл), (стадия e2), и измеряли с помощью лазерного возбуждения на уровне 785 нм и спектрометра Ocean Optics QE65000 с установленным временем для аккумулирования заряда светодиодом в одну секунду. Результаты данных измерений графически представлены на фиг. 5 в виде кружков, соединенных пунктирной линией. Интенсивность сигнала SERS от образца, взятого на конце трубки и имевшего результат измерений 12,5 мкг Au/мл, составляла 28303 импульса в секунду [± 500].
| название | год | авторы | номер документа |
|---|---|---|---|
| ДИМЕРНАЯ ОККЛЮДАНТНАЯ НАНОСТРУКТУРА, МЕЧЕННАЯ МОЛЕКУЛОЙ, АКТИВНОЙ В ОТНОШЕНИИ РАМАНОВСКОГО РАССЕЯНИЯ, ЛОКАЛИЗОВАННОЙ В МЕЖЧАСТИЧНОМ СОЕДИНЕНИИ, ЕЕ ИСПОЛЬЗОВАНИЕ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2010 |
|
RU2542386C2 |
| НАНО- И МИКРОЧАСТИЦЫ ДЛЯ ИЗОЛЯЦИИ СПЕЦИФИЧЕСКИХ СУБПОПУЛЯЦИЙ ЭКЗОСОМ И ИХ АНАЛИЗА | 2020 |
|
RU2733884C1 |
| УСТРОЙСТВО УСИЛЕНИЯ КОМБИНАЦИОННОГО РАССЕЯНИЯ СВЕТА | 2018 |
|
RU2696899C1 |
| ВОЗОБНОВЛЯЕМАЯ ПОДЛОЖКА ДЛЯ ДЕТЕКТИРОВАНИЯ ПОВЕРХНОСТНО-УСИЛЕННОГО РАМАНОВСКОГО РАССЕЯНИЯ | 2012 |
|
RU2543691C2 |
| ОПТИЧЕСКИЙ ДАТЧИК С МНОГОСЛОЙНОЙ ПЛАЗМОННОЙ СТРУКТУРОЙ ДЛЯ УСОВЕРШЕНСТВОВАННОГО ОБНАРУЖЕНИЯ ХИМИЧЕСКИХ ГРУПП ПОСРЕДСТВОМ SERS | 2005 |
|
RU2361193C2 |
| Способ измерения рН на основе серебряных нанопроволок | 2022 |
|
RU2808717C1 |
| Способ твердофазного каталитического анализа содержания аналита в образце с использованием серебряных нанопроволок | 2022 |
|
RU2808559C1 |
| Способ каталитического разложения пероксида водорода с помощью серебряных нанопроволок | 2022 |
|
RU2815436C1 |
| Оптический сенсор с плазмонной структурой для определения химических веществ низких концентраций и способ его получения | 2019 |
|
RU2720075C1 |
| СПОСОБ ЗАЩИТЫ ОТ ПОДДЕЛКИ И КОНТРОЛЯ ПОДЛИННОСТИ ИЗДЕЛИЙ | 2011 |
|
RU2450358C1 |
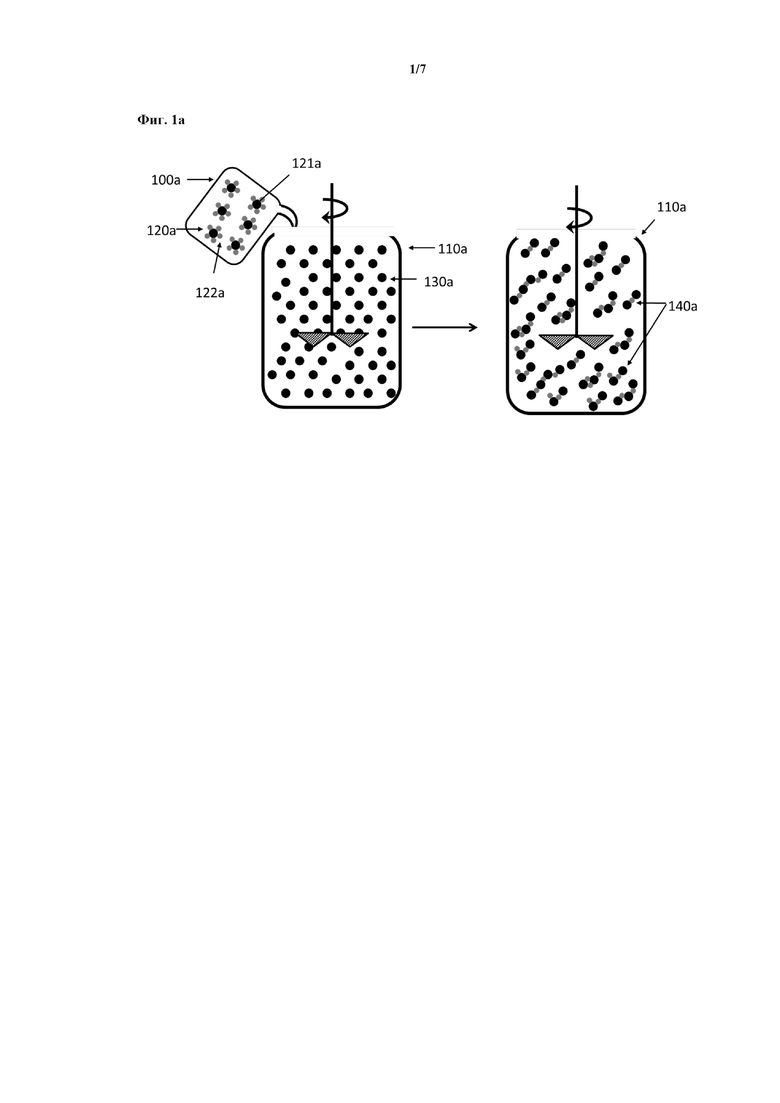
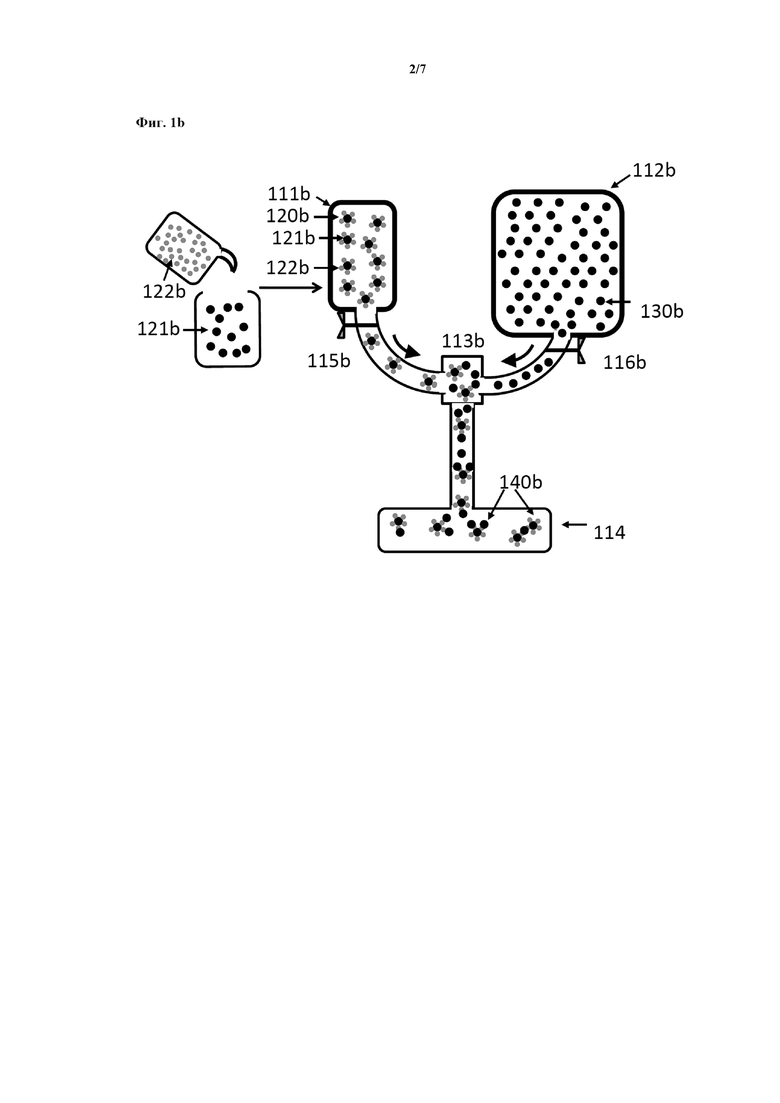
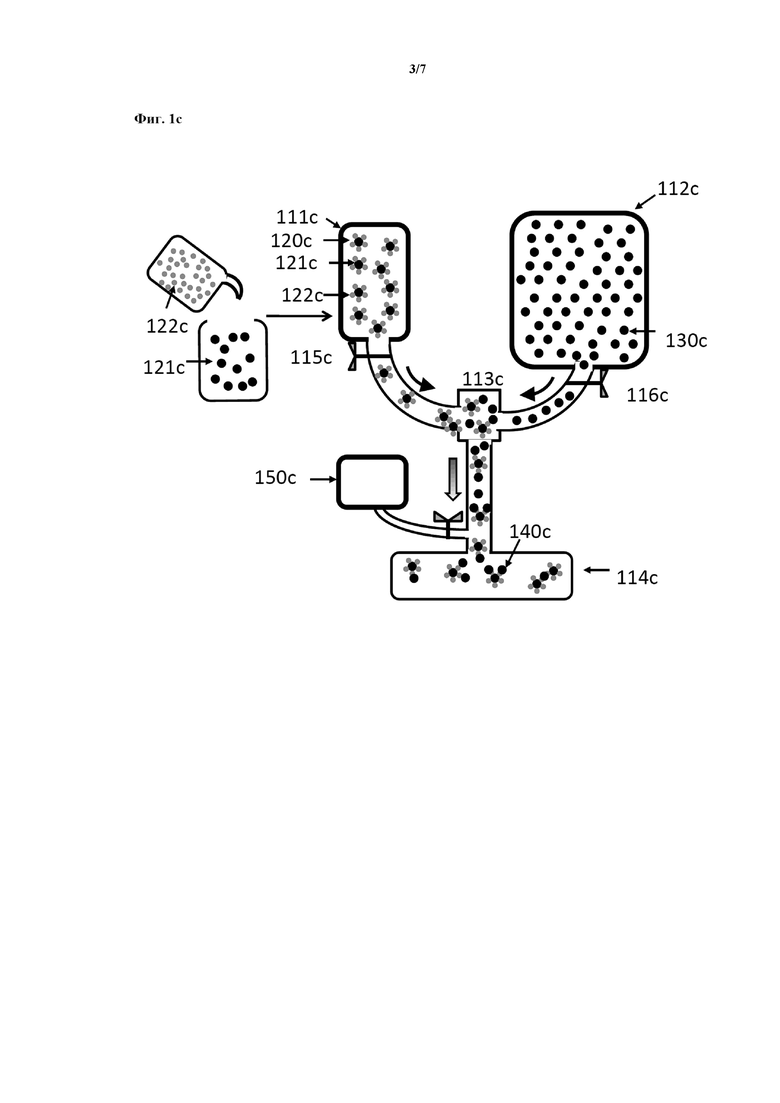
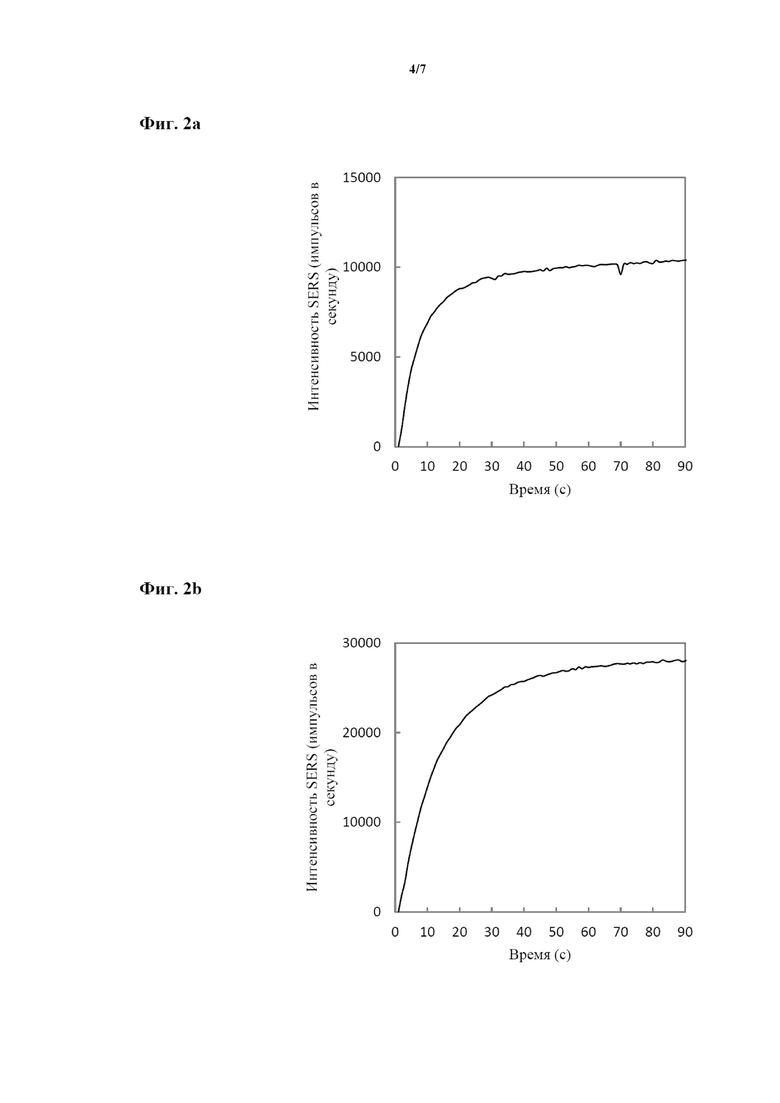
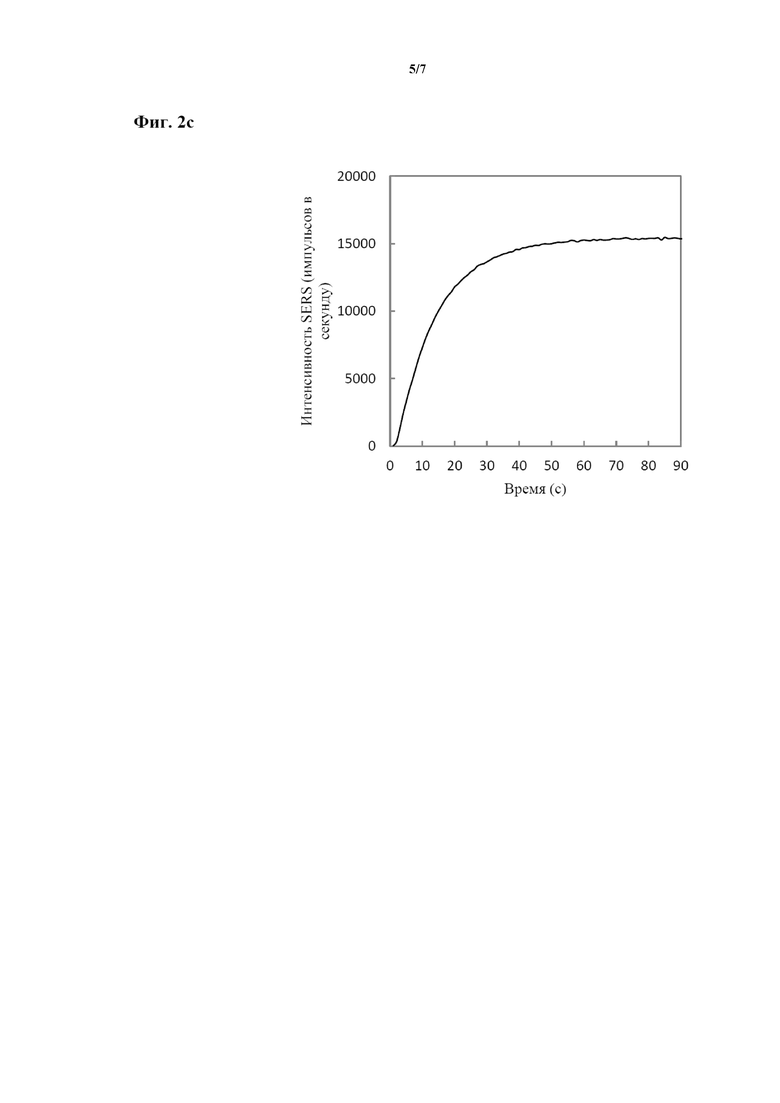
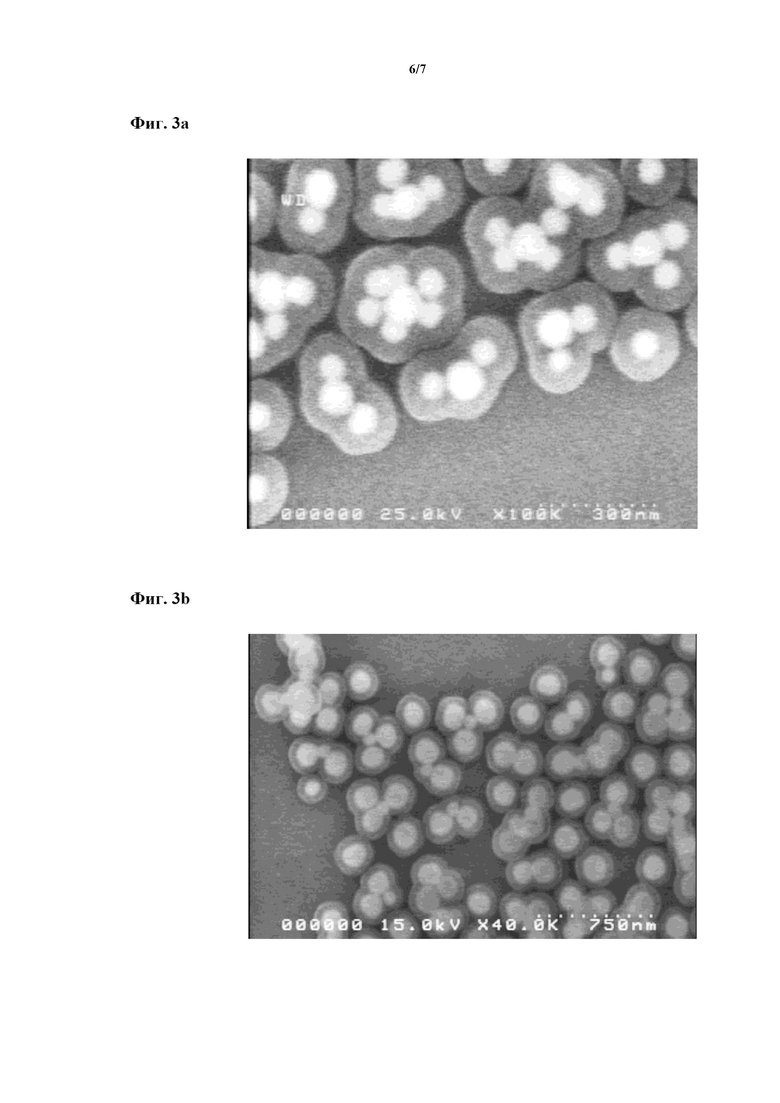
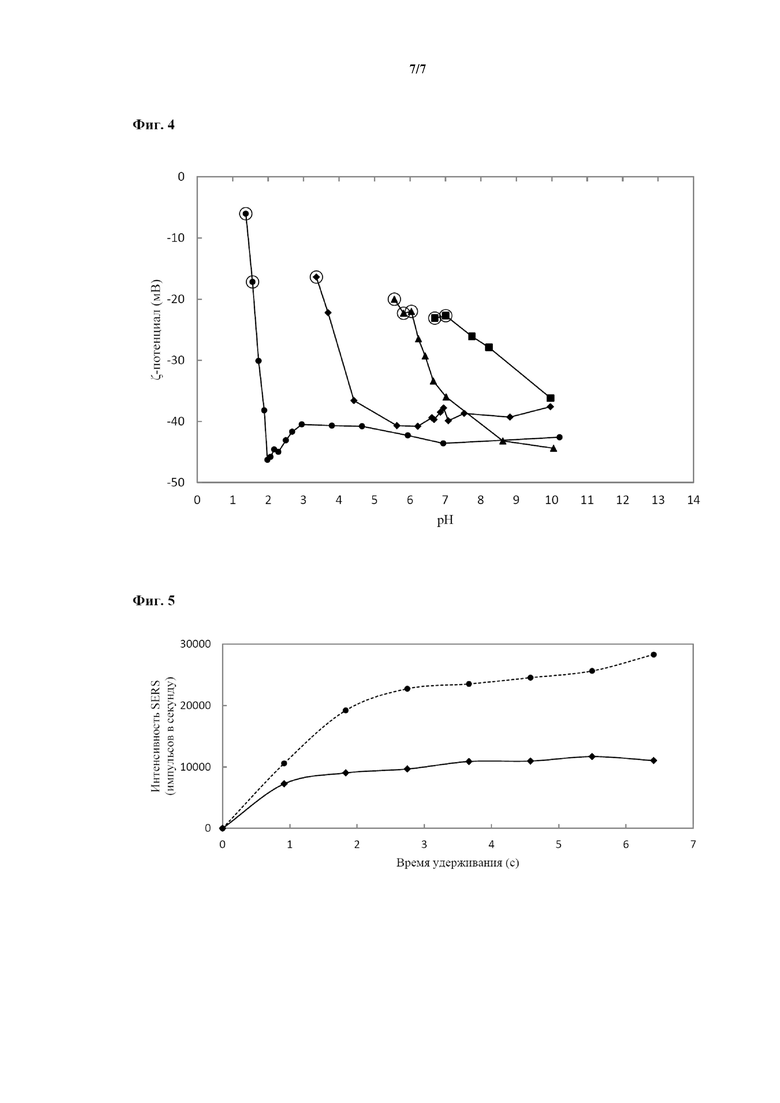
Изобретение относится к области способов изготовления меток поверхностно-усиленной рамановской спектроскопии (SERS). Заявленный способ изготовления меток для поверхностно-усиленной рамановской спектроскопии (SERS) предусматривает следующие стадии: a) получение первого коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ξ-потенциала ниже или равным -25 мВ; b) получение второго коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, активных репортерных молекул рамановского рассеяния, адсорбированных на поверхности указанных наночастиц, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ξ-потенциала ниже или равным -25 мВ; c) объединение первого коллоида со вторым коллоидом таким образом, чтобы соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло от приблизительно 25:1 до приблизительно 1:1, предпочтительно от приблизительно 5:1 до приблизительно 1:1 с получением третьего коллоида; и d) индукцию агрегации наночастиц. При этом индукция агрегации наночастиц происходит с помощью любой из стадий d1)–d3) или их комбинации: d1) смешивание третьего коллоида, полученного на стадии c), при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3; d2) добавление раствора соли, предпочтительно раствора неорганической соли, к третьему коллоиду, полученному на стадии c); d3) добавление водорастворимого растворителя к третьему коллоиду, полученному на стадии c); и e) остановку агрегации. Технический результат – возможность производить целесообразным образом большие количества SERS-меток, характеризующихся узким распределением по размерам и высокой долей агрегатов с малым числом, SERS-метки обеспечивают повышенные ответы SERS в группе. 14 з.п. ф-лы, 5 ил., 6 табл.
1. Способ изготовления меток для поверхностно-усиленной рамановской спектроскопии (SERS), предусматривающий следующие стадии:
a) получение первого коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
b) получение второго коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, активных репортерных молекул рамановского рассеяния, адсорбированных на поверхности указанных наночастиц, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
c) объединение первого коллоида со вторым коллоидом таким образом, чтобы соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляло от приблизительно 25:1 до приблизительно 1:1, предпочтительно от приблизительно 5:1 до приблизительно 1:1 с получением третьего коллоида;
d) индукцию агрегации наночастиц с помощью любой из стадий d1)–d3) или их комбинации:
d1) смешивание третьего коллоида, полученного на стадии c), при pH в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3;
d2) добавление раствора соли, предпочтительно раствора неорганической соли, к третьему коллоиду, полученному на стадии c);
d3) добавление водорастворимого растворителя к третьему коллоиду, полученному на стадии c); и
e) остановку агрегации.
2. Способ по п. 1, отличающийся тем, что стадия b) предусматривает следующие стадии, осуществляемые в порядке b1)-b3):
b1) получение коллоида, фактически состоящего из наночастиц с плазмонной поверхностью и по существу одинаковым размером, диспергированных в водном растворителе, и стабилизирующего средства, адсорбированного на поверхности указанных наночастиц, и характеризующегося значением ζ-потенциала ниже или равным -25 мВ;
b2) доведение pH коллоида до значения, превышающего наиболее низкое значение pH, при котором активные репортерные молекулы рамановского рассеяния, которые должны адсорбироваться на поверхности наночастиц, не несут суммарный электрический заряд, при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ, предпочтительно ниже -40 мВ; и
b3) добавление раствора активных репортерных молекул рамановского рассеяния в растворителе к коллоиду, полученному на стадии b2), при этом поддерживая значение ζ-потенциала ниже или равным -25 мВ.
3. Способ по п. 1 или 2, отличающийся тем, что стабилизирующее средство выбрано из карбоновых кислот, солей карбоновых кислот, фосфорных кислот, солей фосфорных кислот, аскорбиновой кислоты, солей аскорбиновой кислоты и их смесей.
4. Способ по любому из пп. 1-3, отличающийся тем, что наночастицы второго коллоида имеют абсорбированный на их поверхности субмонослой или монослой активных репортерных молекул рамановского рассеяния.
5. Способ по любому из пп. 2-4, отличающийся тем, что на стадии b3) раствор активных репортерных молекул рамановского рассеяния в растворителе содержит смесь из двух или более различных активных репортерных молекул рамановского рассеяния.
6. Способ по любому из пп. 1-5, отличающийся тем, что на стадии c) соотношение количества наночастиц первого коллоида и количества наночастиц второго коллоида составляет от приблизительно 4:1 до приблизительно 3:1.
7. Способ по любому из пп. 1-6, отличающийся тем, что стадия d1) дополнительно предусматривает добавление кислого раствора к третьему коллоиду, полученному на стадии c), при перемешивании, так чтобы значение pH у полученного коллоида составляло в диапазоне от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3.
8. Способ по любому из пп. 1-6, отличающийся тем, что pH первого коллоида доводят так, чтобы pH третьего коллоида, полученного на стадии d1), составлял от приблизительно 2,2 до наиболее низкого значения pH, при котором активные репортерные молекулы рамановского рассеяния имеют суммарный электрический заряд от 0 до 0,3.
9. Способ по любому из пп. 1-8, отличающийся тем, что стадия e) предусматривает любую из следующих стадий e1)–e4):
e1) доведение pH коллоида, полученного на стадии d), до значения, превышающего наиболее низкое значение pH, при котором активные репортерные молекулы рамановского рассеяния, которые должны адсорбироваться на поверхности наночастиц, не несут суммарный электрический заряд;
e2) разведение коллоида, полученного на стадии d), водой;
e3) добавление полимера к коллоиду, полученному на стадии d);
e4) добавление предшественника диэлектрического материала к коллоиду, полученному на стадии d).
10. Способ по любому из пп. 1-9, отличающийся тем, что стадия e) фактически состоит из стадии e3), и способ изготовления дополнительно предусматривает разведение коллоида, полученного на стадии e3), водой и/или нанесение на SERS-метки покрытия диэлектрического материала.
11. Способ по любому из пп. 1-10, отличающийся тем, что стадии c) и d) осуществляют одновременно в проточной системе непрерывного действия.
12. Способ по п. 11, отличающийся тем, что стадию e) осуществляют в проточной системе непрерывного действия.
13. Способ по любому из пп. 1-12, отличающийся тем, что наночастицы первого коллоида и наночастицы второго коллоида имеют одинаковый размер.
14. Способ по любому из пп. 1-12, отличающийся тем, что размер наночастиц первого коллоида отличается от размера наночастиц второго коллоида.
15. Способ по любому из пп. 1-14, отличающийся тем, что плазмонная поверхность наночастиц в первом коллоиде и/или плазмонная поверхность наночастиц во втором коллоиде выполнены из золота.
| US 20080118986 A1, 22.05.2008 | |||
| US 9546958 B2, 17.01.2017 | |||
| US 20080081340 A1, 03.04.2008 | |||
| US 20080003576 A1, 03.01.2008 | |||
| JP 2007502716 A, 15.02.2007 | |||
| WO 2016059429 A1, 21.04.2016. |
Авторы
Даты
2023-09-27—Публикация
2020-07-13—Подача