Изобретение относится к области клинической медицины, а именно к терапии, кардиологии, гастроэнтерологии и может быть использовано для оценки риска развития атрофического гастрита. Изобретение может быть использовано для выявления заболевания на ранней стадии развития.
Под хроническим гастритом понимается хроническое воспаление слизистой оболочки желудка, которое проявляется клеточной инфильтрацией слизистой, нарушением физиологической регенерации и, в результате, атрофией железистого эпителия, кишечной метаплазией, нарушением секреторной, моторной и инкреторной функций желудка [2].
Акцент на изучение сочетанного течения ишемической болезни сердца и гастродуоденопатий далеко не случаен. Прежде всего, больным хронической ишемической болезнью сердца (ИБС) в составе базисной терапии назначаются антиагреганты, воздействующие на звено патогенеза (синтез простагландинов) слизистую оболочку желудка. В ряде случаев больным показана двойная, тройная антиагрегантаная терапия, антикоагулянтная терапия для профилактики сердечно – сосудистых осложнений. В качестве гастропротекторов рассматриваемый контингент больных длительно принимает ингибиторы протонной помпы (ИПП), что также может способствовать атрофическим преобразованиям слизистой оболочки желудка. Логично и закономерно возникает необходимость создать благоприятный фон для проведения эффективного лечения кардиопатологии и при этом минимизировать осложнения со стороны гастродуоденальной зоны.
Диагноз ИБС устанавливается на основании общеклинического обследования, а также общих инструментальных методов (включают регистрацию ЭКГ в покое и при физической нагрузке на велоэргометре, суточное мониторирование ЭКГ, ДС БЦА и ЭХО КГ и коронароангиографию (при наличии показаний)). Верификация гастродуоденальной патологии выполнялась на основании Хьюстонской классификации гастритов (1996 г.), Киотского консенсуса (2015 г.), клинических рекомендаций Российской Гастроэнтерологической Ассоциации.
Для верификации сопутствующего поражения гастродуоденальной зоны больным с клинически установленным диагнозом ИБС после информирования об объеме и возможных осложнениях инвазивного исследования при их согласии выполняли ЭГДС на базе эндоскопического отделения КОГБУЗ «КОКБ» с помощью эндоскопической аппаратуры – видеогастроскоп OLYMPUS H 170 (Olympus Medical Systems Corp, Япония). Для оценки морфологической картины слизистой оболочки желудка применяли систему OLGA (2008 г.), с помощью которой использовали интегральный подход с оценкой гистологической выраженности атрофии в антральном отделе и теле желудка с определением баллов в каждом биоптате (изучали 5 биоптатов (из тела желудка (2) и антрума (3)).
Диагностика данных заболеваний трудоемка, требует сложной специальной аппаратуры, на которой пациенту приходится выполнять большое число исследований, в том числе и инвазивных. Для диагностики заболеваний гастродуоденальной зоны необходимо проводить ЭГДС, но оно в виду его технического выполнения считается для пациентов одним из неприятных исследований. Диагностика трудна, а в ряде случаев даже не выполнима.
Целью создания заявляемого способа является предварительная оценка риска атрофического гастрита у пациентов с серьезным кардиологическим заболеванием, а именно хронической ИБС, которые, в связи с профилактикой сердечно-сосудистых осложнений нуждаются в применении антиагрегантов, которые имеют воздействие на слизистую оболочку желудка. Данные пациенты уже прошли обследования сердечно-сосудистой системы и имеют результаты этих анализов.
Также проведение коронароангиографии выполняется пациентам с высоким риском сердечно – сосудистых осложнений, таким образом мы рассматриваем наиболее тяжелую когорту пациентов с сердечно – сосудистыми заболеваниями. На основании анализа выявленных источников информации следует, что данный вопрос в полной мере не решен.
Известен способ диагностики атрофического гастрита (патент РФ № 2474824), включающий изучение клинических показателей и иммунологического исследования факторов крови путем определения концентрации фактора роста эндотелия сосудов VEGF в сыворотке крови. При значении этого показателя выше 226 пг/мл устанавливают наличие атрофии слизистой оболочки гастродуоденальной зоны.
Недостатком данного способа является определение одного показателя – фактора роста эндотелия VEGF. Данный способ может быть использован только для скринингового исследования степени тяжести атрофического гастрита.
Известен способ диагностики хронического гастрита (патент РФ № 2282397), основанный на проведении видеофиброгастроскопии с использованием витального красителя метиленового синего и эндоскопической ультрасонографии складок желудка и определяют их ширину, соотношение минимальной к максимальной высоте желудочной складки от подслизистого слоя, а также оценивают размеры и форму желудочных полей.
Недостатком данного способа является наличие противопоказаний, инвазивность методики, а также присутствие дорогостоящего оборудования.
Известен способ диагностики гастрита у детей (патент РФ № 2331364), который заключается в определении в тощаковой порции желудочного сока содержания провоспалительного цитокина IL-1В и при значении показателя от 28,6 пг/мл и выше диагностируют наличие гастрита.
Недостатком данного способа является инвазивный забор желудочного сока, ограничение применения данного способа у детей.
Техническим результатом от использования заявляемого технического решения - логит – регрессионной модели, является прогнозирование наличия хронического атрофического гастрита у пациентов хронической ишемической болезнью сердца на основании анализов, уже полученных при исследовании сердечно-сосудистой системы и только одного анализа гастродуоденальной зоны – на инфицированность H. Pylori.
Результат достигается тем, что на основании 4 критериев рассчитывается вероятность развития хронического атрофического гастрита.
Диагностика пациентов с хронической ИБС согласно клиническим рекомендациям (Национальным рекомендациям по диагностике и лечению стабильной стенокардии (2008, 2020), РКО и рекомендациям ESC по лечению стабильной ишемической болезни сердца (2013, 2019)) требует выполнения диагностических исследований (регистрация ЭКГ в покое и при физической нагрузке на велоэргометре, суточное мониторирование ЭКГ, ДС БЦА и ЭХО КГ и коронароангиографию (при наличии показаний). Методы диагностики в большей своей мере безболезненны, за исключением коронароангографии, которая выполняется пациентам с высоким риском сердечно – сосудистых осложнений для решения вопроса об их дальнейшей лечебной тактике (консервативная терапия или хирургическая коррекция коронарного русла).
Способ обеспечивает создание благоприятного фона для проведения эффективного лечения кардиопатологии и, при этом, минимизирует проведение инвазивных анализов гастродуоденальной зоны.
Если рассчитанный с помощью логит-модели порог у больного составляет более 20 %, то к этому больному, в виду высокой прогнозируемой вероятности хронического атрофического гастрита, требуется особое внимание.
Описание заявляемого способа
Способ оценки риска развития атрофического гастрита у пациентов хронической ишемической болезнью сердца заключается в том, что:
- выявляют инфицированность H. pylori,
- проводят опрос пациентов и определяют наличие у пациента неконтролируемого приема ингибиторов протоновой помпы (ИПП), нестероидных противовоспалительных препаратов (НПВП);
- на основании уже проведенных исследований поражения коронарных и каротидных артерий определяют следующие показатели:
- тип сосудистого поражения коронарных артерий по данным коронароангиографии:
- или без поражения коронарных артерий,
- или однососудистое, или двухсосудистое,
- или трехсосудистое поражение;
- процент стенозирования брахиоцефальных артерий по данным дуплексного сканирования: или более 20%, или менее 20%.
Далее установленным факторам риска присваивают градации и определяют прогностические коэффициенты по формуле, где при помощи уравнения регрессии, имеющего вид: 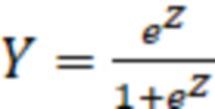 ,
,
где 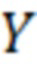 – вероятность наличия хронического атрофического гастрита (ХАГ) и
– вероятность наличия хронического атрофического гастрита (ХАГ) и 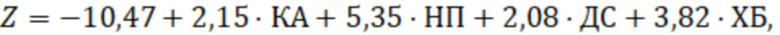 определяют вероятность развития хронического атрофического гастрита у пациентов хронической ишемической болезнью сердца, где:
определяют вероятность развития хронического атрофического гастрита у пациентов хронической ишемической болезнью сердца, где:
КА – тип сосудистого поражения коронарных артерий по данным коронароангиографии: либо двухсосудистое, либо трехсосудистое поражение коронарных артерий – 1, либо однососудистое поражение коронарных артерий и отсутствие – 0;
НП – неконтролируемый прием ИПП и НПВП (да – 1, нет – 0).
ДС – процент стенозирования брахиоцефальных артерий по данным дуплексного сканирования (стенозирование брахиоцефальных артерий более 20% – 1, стенозирование брахиоцефальных артерий менее 20% – 0).
ХБ – инфицированность H. pylori (да – 1, нет – 0).
Способ позволяет оценить вероятность развития хронического атрофического гастрита у пациентов хронической ишемической болезни сердца на основании 4 критериев и их математического преобразования.
Примеры реализации заявляемого способа
Дуплексное сканирование брахиоцефальных артерий проводилось на аппарате Vivid E9 (GE, США).
Изучение каротидного русла выполнялось измерением толщины комплекса интима – медиа и атеросклеротических бляшек общей сонной артерии методом дуплексного сканирования брахиоцефальных артерий (Ведение пациентов с заболеваниями брахиоцефальных артерий, Клинические рекомендации РФ 2013 – 2017, Российское общество ангиологов и сосудистых хирургов, Ассоциация сердечно-сосудистых хирургов России, Российское научное общество рентгенэндоваскулярных хирургов и интервенционных радиологов, Всероссийское научное общество кардиологов, Ассоциация флебологов России, Клинические рекомендации Артериальная гипертензия у взрослых, 2020, РКО).
Нормой толщины комплекса интима – медия ОСА был выбран показатель <0,9 мм.
Локальное утолщение ТИМ оценивали по степени нарушения обструкции: нестенозирующая (сужение просвета сосуда по диаметру менее 20%), стенозирующая (сужение просвета сосуда по диаметру более 20%).
Коронарография проводилась с помощью ангиографического комплекса GE Innova 3100 IQ (Производитель: GE Medical Systems (США)) с целью определения степени тяжести атеросклеротического процесса и решения вопроса об оперативном вмешательстве для повышения качества жизни пациентов (Клинические рекомендации, стабильная ишемическая болезнь сердца, 2020, РКО). При анализе сосудистого поражения коронарного русла определяется тип поражения (одно – сосудистое, двух – сосудистое, трех – сосудистое поражение, или без поражения коронарных артерий), процент стенозирования коронарных артерий (51 – 75%, 76 – 95%, 95 – 99%, 100%), архитектоника поражения коронарных артерий (ПМЖВ, ПКА, ЛКА, ОВ, ВТК, ДА, ЗМЖВ, ЗБВ).
Диагностику Н. pylori осуществляли методами: конкретно и согласно Клиническим рекомендациям РГА (Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению язвенной болезни, 2016, 2020; Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых, 2018) [3, 4].
Пациентам для верификации инфекции H. pylori был выполнен серологический метод определения антител в сыворотке крови («ИФА – Хеликобактер IgG», тест – система иммуноферментная для выявления иммуноглобулинов класса G к Helicobacter pylori) и определение антигена к Helicobacter pylori в стуле (ИФА, тест – система CITO TEST H. pylori АГ). В ходе обследования пациентов, сбора жалоб и анамнеза выявлялось наличие критерия – неконтролируемый прием ИПП и НПВП.
Прогнозирование вероятности развития хронического атрофического гастрита возможно осуществлять с помощью модели логистической регрессии (логит – модели), которая представляется в виде:
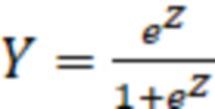 ,
,
где 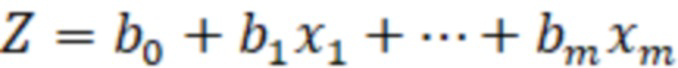 – линейная комбинация факторных переменных, а
– линейная комбинация факторных переменных, а 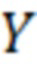 – вероятность наличия ХАГ. Построение и анализ логит – модели проводился с помощью процедуры Логит-регрессия модуля Нелинейное оценивание программы STATISTICA 10 на уровне значимости 5% (
– вероятность наличия ХАГ. Построение и анализ логит – модели проводился с помощью процедуры Логит-регрессия модуля Нелинейное оценивание программы STATISTICA 10 на уровне значимости 5% (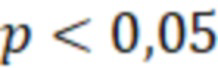 ).
).
Таким образом, можно выделить 4 группы значений факторов.
1 группа: отсутствие факторов риска, один фактор или два фактора без НП. В этом случае прогнозируемая вероятность развития ХАГ не превышает 1,1%.
2 группа: 2 фактора с НП три фактора без НП. В этом случае прогнозируемая вероятность развития ХАГ составляет от 4,5% до 8,2%.
3 группа: факторы НП и ХБ или 3 фактора или три фактора без НП. В этом случае прогнозируемая вероятность развития ХАГ составляет от 21,4% до 29,1%.
4 группа: 3 фактора с НП или 4 фактора. В этом случае прогнозируемая вероятность развития ХАГ выше 68,4%.
Данные формулы были получены на основании исследования 308 пациентов хронической ишемической болезнью сердца.
Установлено, что среди пациентов с хронической ИБС 77,3% (238) имели патологию верхних отделов ЖКТ, а именно хронический атрофический гастрит – 24,4% (58) пациентов, хронический неатрофический гастрит – 50,8% (121) пациентов.
Распространенность хеликобактериоза составила 85,3% (203) пациентов. Распространенность хеликобактериоза в когорте больных хронической ИБС составила 65,9% (203).
Инфицированность в группе пациентов с хроническим атрофическим гастритом составила – 98,3% (57) пациентов.
При использовании модели логит – регрессии выявлено, что среди пациентов с хроническим атрофическим гастритом порог высокого прогнозируемого риска по данной патологии более 20% был выявлен у 96,6% (n=56) пациентов: 2 пациента имели высокий риск 8,2%, 1 пациент – 21,4%, 2 пациента – 29,2%, 12 пациентов – 68,5%, 8 пациентов – 70,1%, 33 пациента – 94,9%.
Пример 1.
Пациент С., 62 года. При поступлении жалобы на боли давящего, сжимающего характера за грудиной, возникающие при физической нагрузке (быстрая ходьба, подъем на 2 этаж, подъем в гору), проходит в покое или приемом нитроглицерина. Одышку при физической нагрузке (быстрая ходьба, подъем на 2 этаж, подъем в гору). На чувство жжения в области желудка, нарушения консистенции и частоты стула реже 3 раз в неделю. Жалобам диспепсического характера значимого внимания не уделял, указав, что периодически беспокоили (изжога, отрыжка воздухом) с 30 лет. Пациент часто и бесконтрольно принимает НПВП и ИПП. Коронароангиография – стеноз п/3 ПМЖВ > 75%. Стенозы устья п/3 и с/3 ПКА > 75%. Левый тип КК. ДС БЦА – Атеросклероз внечерепных отделов брахиоцефальных артерий со стенозированием: области каротидной бифуркации слева на 30 – 35%, справа на 30 – 35%; устья и проксимального отдела левой внутренней сонной артерии на 25 – 30%. Непрямолинейность хода позвоночных артерий. ЭГДС с биопсией – атрофический гастрит, (OLGA антрум – I стадия, тело – II стадия). По данным биопсии – атрофический гастрит, инфицированный H. pylori. ПЦР исследование – Штамм H. pylori Cag A. Антибиотикочувствительность H. pylori – высокочувствительный к кларитромицину, амоксициклину, умеренно чувствительный к тетрациклину, резистентный к метронидазолу. Иммуноферментный анализ антигена к Helicobacter pylori в стуле – положительный.
Просчитываем риск хронического атрофического гастрита на основании построенной модели:
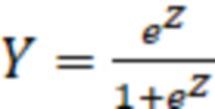 ,
,
где 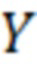 – вероятность наличия ХАГ и
– вероятность наличия ХАГ и 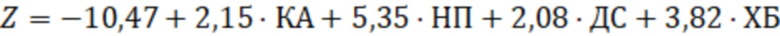
На основании построенной модели – риск хронического атрофического гастрита составил 94,9%.
Таким образом, предложенный способ позволяет оценить вероятность развития хронического атрофического гастрита у больных хронической ишемической болезнью сердца по ограниченному набору показателей, что способствует более рациональному определению тактики комплексной терапии рассматриваемого контингента больных, и в итоге благоприятно скажется на переносимости и приверженности терапии у пациентов, более тщательному контролю за коморбидной патологией. Положительный эффект предлагаемого способа подтвержден результатами его применения у 57 пациентов, исследованных по поводу риска развития атрофического гастрита. На основании данных критериев можно установить, что наличие двух-сосудистого или трех-сосудистого поражения коронарных артерий по данным коронароангиографии, стенозирование брахиоцефальных артерий более 20% по данным дуплексного сканирования, наличие неконтролируемого приема НПВП, ИПП и инфицированность H. pylori определяют вероятность развития хронического атрофического гастрита у больных хронической ишемической болезнью сердца.
Тест согласно настоящему изобретению является воспроизводимым, точным, высокопроизводительным, легким в использовании способом количественного определения степени риска развития атрофического гастрита у пациентов хронической ишемической болезнью сердца.
СПИСОК ЛИТЕРАТУРЫ
1. Андреев Д.Н. Возможности оптимизации эрадикационной терапии инфекции Helicobacter pylori в современной клинической практике / Д.Н. Андреев, Д.Т. Дичева, И.В. Маев // Терапевтический архив. – 2017 . – №2. – С. 84–90.
2. Аруин, Л.И. Хронический гастрит / Л.И. Аруин, П.Я. Григорьева, В.А. Исаков [и др.] – Амстердам, 1993. – 362 с.
3. Ивашкин, В.Т. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению язвенной болезни / В.Т. Ивашкин, А.А. Шептулин, И.В. Маев [и др.] // РЖГГК. – 2016. – Т. 6. – № 26. – С. 40–54.
4. Ивашкин, В.Т. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых / В.Т. Ивашкин, И.В. Маев, Т.Л. Лапина [и др.] // РЖГГК. – 2018. – Т. 1. – № 28. – С. 55–70.
5. Маев, И.В. Рак желудка: факторы риска и возможности канцеропревенции / И.В. Маев, Д.Н. Андреев // Consilium Medicum. – 2014. – Т. 16. № 12. – С. 45–50.
6. Маев, И.В. Болезни желудка / И.В. Маев, А.А. Самсонов, Д.Н. Андреев. – Москва : ГЭОТАР – Медиа, 2015. – 976 с.
7. Correa, P. Gastric cancer: overview/ P. Correa// Gastroenterol. Clin. North Am. – 2013. – Vol. 42, № 2. – P. 211–217.
8. Chen, H.N. Helicobacter pylori eradication cannot reduce the risk of gastric cancer in patients with intestinal metaplasia and dysplasia: evidence from a meta-analysis / H.N. Chen, Z. Wang, X. Li [et al.] // Gastric. Cancer. – 2016. – Vol. 19, № 1. – P. 166–175.
9. Dixon, M.F. Classification and grading of gastritis. The updated Sydney System. International Workshop on the Histopathology of Gastritis, Houston 1994 / M.F. Dixon, R.M. Genta, J.H. Yardley [et al.] // Am. J. Surg. Pathol. – 1996. – Vol. 20, № 10. – P. 1161–1181.
10. Morgan, D.R. Helicobacter pylori infection. Sleisenger and Fordtran's Gastrointestinal and Liver Disease: Pathophysiology, Diagnosis, Management / D.R. Morgan, S.E. Crowe. – Philadelphia. – 2015. – P. 856–884.
11. Rugge, M. OLGA staging for gastritis: a tutorial/ M. Rugge, P. Correa, F. Di Mario [et al.] // Dig. Liv. Dis. – 2008. – Vol. 40, № 8. – P. 650–658.
12. Rugge, M. Operative link for gastritis assessment vs operative link on intestinal metaplasia assessment/ M. Rugge, M. Fassan, M. Pizzi [et al.] // World J. Gastroenterol. – 2011. – Vol. 17, № 41. – P. 4596–4601.
13. Rugge, M. OLGA gastritis staging in young adults and country-specific gastric cancer risk / M. Rugge, J.G. Kim, V. Mahachai, [et al.] // Int. J. Surg. Pathol. – 2008. – Vol. 16, № 2. – P. 150–154.
14. Yoshida, T. Cancer development based on chronic active gastritis and resulting gastric atrophy as assessed by serum levels of pepsinogen and Helicobacter pylori antibody titer/ T. Yoshida // Int. J. Cancer. – 2014. – Vol. 134, № 6. – P. 1445–1457.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ АТРОФИЧЕСКОГО ГАСТРИТА | 2011 |
|
RU2474824C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ДЕСТРУКТИВНЫХ ИЗМЕНЕНИЙ СЛИЗИСТОЙ ОБОЛОЧКИ ГАСТРОДУОДЕНАЛЬНОЙ ЗОНЫ | 2008 |
|
RU2391915C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ HELICOBACTER PYLORI-АССОЦИИРОВАННОГО ХРОНИЧЕСКОГО ГАСТРИТА, ОСНОВАННЫЙ НА ОПРЕДЕЛЕНИИ ИММУНОЛОГИЧЕСКИХ ПОКАЗАТЕЛЕЙ У ЕВРОПЕОИДОВ ХАКАСИИ | 2015 |
|
RU2614851C1 |
| Способ индукции экстракардиальной реваскуляризации миокарда у больных ишемической болезнью сердца | 2021 |
|
RU2758024C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ СИНДРОМА ПОЛИОРГАННОЙ НЕДОСТАТОЧНОСТИ У ПАЦИЕНТОВ ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ | 2017 |
|
RU2641033C1 |
| СПОСОБ ДИАГНОСТИКИ СТЕПЕНИ АКТИВНОСТИ АНТРАЛЬНОГО ХЕЛИКОБАКТЕР-АССОЦИИРОВАННОГО ГАСТРИТА У БОЛЬНЫХ БРОНХИАЛЬНОЙ АСТМОЙ | 2009 |
|
RU2394499C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ЭКЗЕМЫ У БОЛЬНЫХ С СОПУТСТВУЮЩИМ ХРОНИЧЕСКИМ ГАСТРОДУОДЕНИТОМ | 2011 |
|
RU2461836C1 |
| СПОСОБЫ И ПРОДУКТЫ ДЛЯ ДИАГНОСТИКИ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ И РАКА ЖЕЛУДКА, СВЯЗАННОГО С АТРОФИЧЕСКИМ ГАСТРИТОМ | 2008 |
|
RU2519646C2 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ АТРОФИЧЕСКОГО ГАСТРИТА У ЕВРОПЕОИДОВ ХАКАСИИ | 2014 |
|
RU2561054C1 |
| Способ прогнозирования наличия кальциноза коронарных артерий и грудного отдела аорты по уровню артериальной жесткости у пациентов высокого риска сердечно-сосудистых осложнений со сниженной минеральной плотностью костной ткани | 2019 |
|
RU2723361C1 |
Изобретение относится к медицине, а именно к терапии, кардиологии и гастроэнтерологии и может быть использовано для оценки вероятности наличия атрофического гастрита у пациентов с хронической ишемической болезнью. Для этого по данным коронароангиографии определяют тип сосудистого поражения коронарных артерий, наличие у пациента неконтролируемого приёма ингибиторов протоновой помпы ИПП и нестероидных противовоспалительных препаратов НПВП. По данным дуплексного сканирования определяют процент стенозирования брахиоцефальных артерий. Выявляют инфицированность H. Pylori. Далее установленным факторам риска присваивают градации и определяют прогностические коэффициенты. Затем при помощи уравнения регрессии определяют вероятность наличия хронического атрофического гастрита Y по разработанной математической формуле, в %. Изобретение позволяет прогнозировать наличие хронического атрофического гастрита у пациентов с хронической ишемической болезнью сердца на основании анализов, уже полученных при исследовании сердечно-сосудистой системы и только одного анализа гастродуоденальной зоны – на инфицированность H. Pylori. 1 пр.
Способ оценки вероятности наличия хронического атрофического гастрита у пациентов с хронической ишемической болезнью сердца заключается в том, что на основании четырёх факторов:
- на основании уже проведённых исследований поражения коронарных и каротидных артерий по данным коронароангиографии определяют тип сосудистого поражения коронарных артерий: или без поражения коронарных артерий, или однососудистое, или двухсосудистое, или трехсосудистое поражение - фактор риска КА;
- проводят опрос пациентов и определяют наличие у пациента неконтролируемого приёма ингибиторов протоновой помпы ИПП и нестероидных противовоспалительных препаратов НПВП - фактор риска НП;
- по данным дуплексного сканирования определяют процент стенозирования брахиоцефальных артерий: или 20% и более или менее 20% - фактор риска ДС;
- выявляют инфицированность H. pylori - фактор риска ХБ;
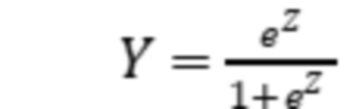 далее установленным факторам риска присваивают градации и определяют прогностические коэффициенты, затем при помощи уравнения регрессии определяют вероятность развития хронического атрофического гастрита Y: х100%,
далее установленным факторам риска присваивают градации и определяют прогностические коэффициенты, затем при помощи уравнения регрессии определяют вероятность развития хронического атрофического гастрита Y: х100%,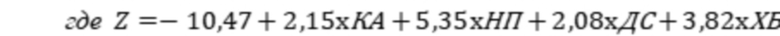 , где:
, где:
- фактору риска КА присваивают значение 1 при двухсосудистом либо трехсосудистом поражении коронарных артерий; а значение 0 присваивают либо при однососудистом поражении коронарных артерий, либо при отсутствии поражения;
фактору риска НП присваивают значение 1 при неконтролируемом приёме ИПП и НПВП, а значение 0, если нет неконтролируемого приёма ИПП и НПВП;
- фактору риска ДС присваивают значение 1, если стенозирование брахиоцефальных артерий не менее 20%, а значение 0, если стенозирование брахиоцефальных артерий менее 20%;
- фактору риска ХБ присваивают значение 1, если пациент инфицирован, а значение 0, если не инфицирован.
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ HELICOBACTER PYLORI-АССОЦИИРОВАННОГО ХРОНИЧЕСКОГО ГАСТРИТА, ОСНОВАННЫЙ НА ОПРЕДЕЛЕНИИ ИММУНОЛОГИЧЕСКИХ ПОКАЗАТЕЛЕЙ У ЕВРОПЕОИДОВ ХАКАСИИ | 2015 |
|
RU2614851C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ АТРОФИЧЕСКОГО ГАСТРИТА У ЕВРОПЕОИДОВ ХАКАСИИ | 2014 |
|
RU2561054C1 |
| Модуляционное устройство | 1930 |
|
SU22746A1 |
| МАГОМЕДОВА Б.М | |||
| и др | |||
| Изменения слизистой оболочки верхних отделов желудочно-кишечного тракта при ишемической болезни сердца | |||
| Кардиоваскулярная терапия и профилактика, 2017; 16(6): 65-69 | |||
| ПРИХОДЬКО М.Н | |||
| Особенности коронарного русла больных стабильной стенокардией с | |||
Авторы
Даты
2023-10-25—Публикация
2022-07-28—Подача