Изобретение относится к медицине, а именно к пластической и реконструктивной хирургии, и может быть использовано для выбора эффективного метода лечения у пациентов с келоидными рубцами.
Пластическая хирургия накопила большой опыт в диагностике и лечении келоидных рубцовых деформаций кожи с использованием современных методик. При этом в настоящий момент совершенно точно можно сказать, что не существует единого метода коррекции келоидного рубца или рубцовой деформации. Каждый случай уникален и каждый случай должен быть тщательно диагностирован для корректного подбора метода лечения или комбинации из нескольких методик. Поэтому актуальность выбора наиболее эффективного метода лечения келоидного рубца не вызывает никаких сомнений.
Известен способ выбора лечения келоидных рубцов (А.В. Таганов, М.А. Бизунова, Ю.М. Криницына, И.Г. Сергеева. Анализ методов лечения келоидных рубцов. https://doi.org/10.17116/klinderma201716397-102), который включает проведение планиметрии с помощью цифровой фотографии и учет индивидуальных особенностей пациента.
Недостатком данного способа является его недостаточная информативность для определения объективных критериев рубцовой ткани, стадии рубца, что не позволяет точно выбрать наиболее эффективное лечение.
Наиболее близким является способ выбора лечения келоидного рубца, включающий сбор анамнеза с выявлением наличия или отсутствия функциональных нарушений, сроков существования рубцовой ткани. В этом способе первым этапом проводится тщательный сбор анамнеза с выявлением предыдущего лечения и его эффективности, оценивается наличие или отсутствие функциональных нарушений, и при имеющихся значимых функциональных нарушениях, пациенту предлагается выполнение оперативного лечения вне зависимости от срока, прошедшего с момента травмы (операции). При отсутствии тяжелых функциональных нарушений, при незрелых рубцах (сроком менее 6 месяцев с момента травмы), назначается консервативное лечение до их полного созревания, в случае неудовлетворенности результатом консервативное лечение продолжается до 12 месяцев. При наличии зрелых рубцов определяется распространенность рубцовой деформации и ресурсов окружающих здоровых тканей, решается вопрос о хирургическом лечении с различными видами пластики (трапециевидными и треугольными лоскутами, аутодермопластика) или рубцы иссекаются. При отсутствии натяжения выполняется иссечение рубцов в 1 этап. При имеющемся натяжении -иссечение осуществляется в 2-3 этапа с интервалом не менее 6 месяцев. По показаниям выполняется лазеротерапия CO2-лазером UltraPulse. (Романец О.П. Методы оптимизации лечения и профилактики рубцов. Дисс.на соиск. уч. ст.к.м.н., 2016, с. 104, https://www.dissercat.com/content/metody-optimizatsii-lecheniya-i-profilaktiki-rubtsov)
Недостатком данного способа является большая вероятность неточного выбора инвазивного лечения, поскольку не учитывается индивидуальное состояние тканей келоидного рубца.
Задачей предлагаемого изобретения является устранение указанных недостатков, повышение точности выбора инвазивного способа лечения келоидного рубца за счет определения более информативных критериев рубцовой ткани и обеспечение индивидуального подхода при определении вида инвазивного лечения: криолазерного или хирургического.
Для решения поставленной задачи в способе выбора эффективного инвазивного лечения келоидного рубца, включающем сбор анамнеза с выявлением наличия или отсутствия функциональных нарушений, сроков существования рубцовой ткани, предложено дополнительно проводить гистологическое исследование с определением реакции остеокластоподобных элементов и иммуногистохимическое исследование рубцовой ткани, при котором выявляют значения ММР1, К III и IV типов, α-SMA. При имеющихся функциональных нарушениях, вне зависимости от срока, существования рубцовой ткани при получении показателя реакции остеокластоподобных элементов в пределах 5,0-6,0 у.е., значения величины коллагена III типа в пределах 1,0-1,6 у.е., коллагена IV типа в пределах 0,4-1,0 у.е., ММР1 в пределах 0,0-1,4 у.е., α-SMA в пределах 0,0-0,6, проводят хирургическое лечение. При отсутствии функциональных нарушений, сроков существования рубцовой ткани менее 6 месяцев, и при получении значения показателя реакции остеокластоподобных элементов равного 4,0 у.е., а значение величины коллагена III типа в пределах 2,5-3,7 у.е., коллагена IV типа, равного 2,0 у.е., ММР1 равной, 6,0 у.е., α-SMA в пределах 5,4-6,0 у.е. проводят криолазерное лечение келоидного рубца.
Выбор предлагаемых параметров, а именно остеокластоподобных элементов, ММР1, коллагенов III и IV типов, α-SMA при гистологическом и иммуногистохимическом обследовании перед операцией позволяет персонализировано планировать выбор способа лечения каждому пациенту. Это повышает эффективность проводимого лечения и позволяет получить хорошие результаты у пациентов с келоидными рубцами.
Кроме этого, обследование пациентов в предоперационном периоде позволяет планировать и выбирать лечение, сокращая число осложнений и рецидивов, уменьшая сроки реабилитации, а также добиться хороших функциональных и эстетических результатов у пациентов с келоидными рубцами.
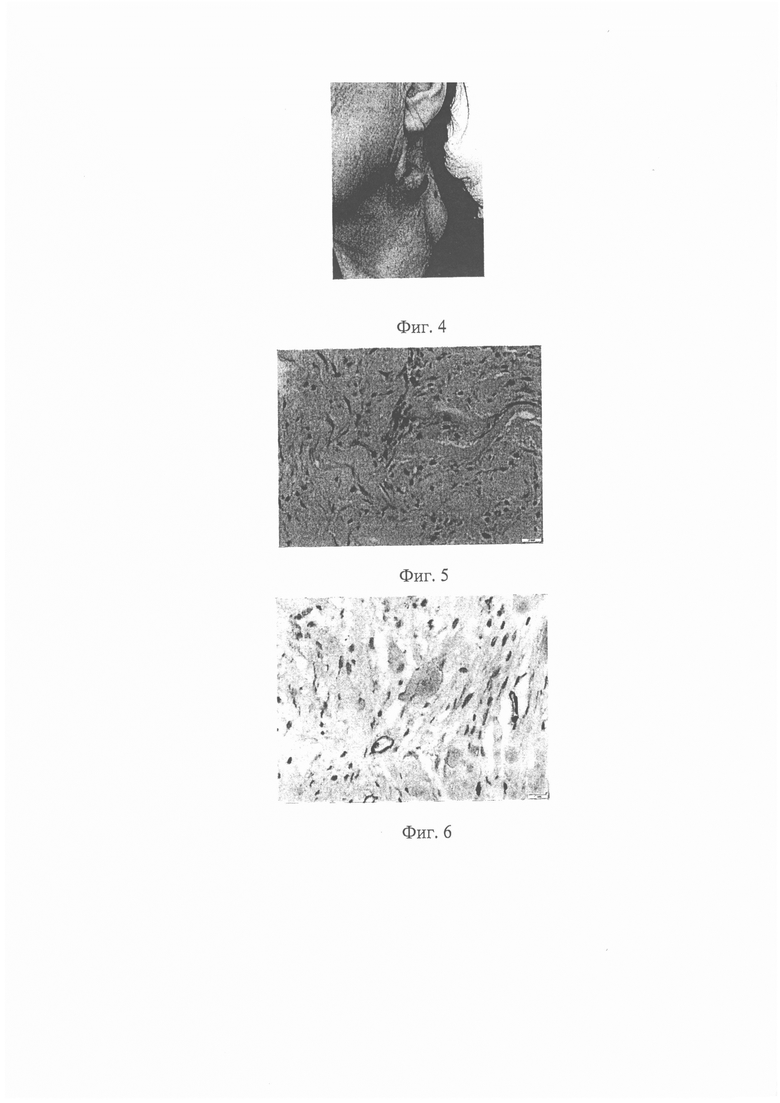
На фиг.1 представлено фото пациентки с келоидным рубцом ушной раковины справа с наличием функциональных нарушений и сроком существования рубца 4 месяца (пример 5, см. таблицу); на фиг.2 - микрофотограмма пациентки с гиалинизированными структурами с наличием остеокластических элементов (пример 5, см. таблицу); на фиг.3 иммуногистохимическое исследование пациентки с относительным увеличением коллагена III и IV типов, и с выраженной реакцией α-SMA положительных миофибробластов среди клеток инфильтрата, а также высокой продукцией ММР1 макрофагами (пример 5, см. таблицу); на фиг.4 представлена пациентка с келоидным рубцом боковой поверхности шеи слева с отсутствием функциональных нарушений со сроком существования рубца более 11 месяцев (пример 6, см. таблицу), а на фиг.5 представлена гистология данной пациентки, с наличием остеокластоподобных элементов; на фиг.6 представлена иммуногистохимия данной пациентки с активностью ММР1 в макрофагах и миофибробластических элементах, достоверно большим количеством α-SMA- положительных миофибробластических элементов и коллагенов коллагена III и IV типов (пример 5, см. таблицу).
Способ осуществляется следующим образом.
В предоперационном периоде оценивается анамнез келоидного рубца с выявлением наличия или отсутствия функциональных нарушений, сроков существования рубцовой ткани.
После анализа этих клинических характеристик рубцово-измененной ткани, проводят панч биопсию в области рубца с последующей гистологической и иммуногистохимической диагностикой, которая осуществляется согласно стандартным протоколам (Мавликеев М.О., Архипова С.С., Чернова О.Н., Титова А.А., Певнер Г.О., Шафтгуллина А.К., Киясов А.П. Краткий курс гистологической техники. Учебно-методическое пособие под научной редакцией Р.В. Деева, Казанский Университет, 2020, 5-70 с), (Иммуногистохимические методы: Руководство /Ed. By George L. Kumar, Lars Rudbeck:DAKO, пер. с англ. Под ред. Г.А.Франка и П.Г. Малькова, М., 2011, с. 69-101).
При проведении гистологического и иммуногистохимического исследования материал фиксируется в 10% забуференном формалине.
Далее выполняется фиксация, проводка, заливка в парафин и окрашивание серийных срезов толщиной 4 мкм по гематоксилину и эозину Ван-Гизону.
Серийные парафиновые срезы толщиной 4 мкм, расположенные на стеклах, покрытых полилизиновым слоем (Menzel Glaser Polylisine, Германия) при иммуногистохимическом исследовании изготавливаются в соответствии с международными рекомендациями
(Иммуногистохимические методы: Руководство /Ed. By George L. Kumar, Lars Rudbeck:DAKO, пер. с англ. Под ред. Г.А.Франка и П.Г. Малькова - М., 2011-е. 128-160).
Неокрашенные срезы обрабатывали с помощью стандартного метода иммуногистохимии с термической демаскировкой антигенов в ретривере (Thermo Scientific, США). В качестве первичных антител использовали мышиные моноклональные антитела к коллагену I типа (клон 3G3, Santa Cruz, разведение 1:100), коллагену III типа (клон В-4, Santa Cruz, разведение 1:50), коллагену IV типа (клон COL-94, Santa Cruz, разведение 1:50), ММР-1 (клон 3В6, Santa Cruz, разведение 1:100), SMA (клон 1А4, Dako Agilent, Для выявления первичных антител, связавшихся с соответствующими антигенами, использовали универсальную полимерную систему Histofme® Simple Stain MAX PO (MULTI) (Nichirei, Япония), содержащую декстрановый каркас с многократно присоединенными молекулами фермента пероксидазы хрена и вторичными антителами к антимышиным и антикроличьим иммуноглобулинам (Ig), меченными стрептовидин-биотином. Для визуализации места связывания антитела с антигеном использовали реакцию окисления субстрата 3,3-диаминобензидина (ДАБ) пероксидазой хрена в присутствии перекиси водорода с образованием нерастворимого в органических растворителях конечного продукта реакции, который был виден в виде коричневого окрашивания специфических структур клеток (N-Histofine® DAB-2V, Nichirei, Япония). Срезы инкубировали с ДАБ в течение 5-10 минут, а затем ядра докрашивались гематоксилином Майера. При постановке иммуногистохимических реакций ставили положительные и отрицательные контроли. В качестве отрицательных контролей брали образцы исследуемых срезов, которые подвергались стандартной процедуре ИГХ исследования, но без инкубации с первичными антителами. Положительный контроль для каждого антитела отбирали в соответствии с рекомендациями производителя антител.
Оценка гистологических и иммуногистохимических изменений для выраженности ММР1, коллагена III и IV типов, α-SMA и остеокластоподобных элементов осуществляется в условных единицах.
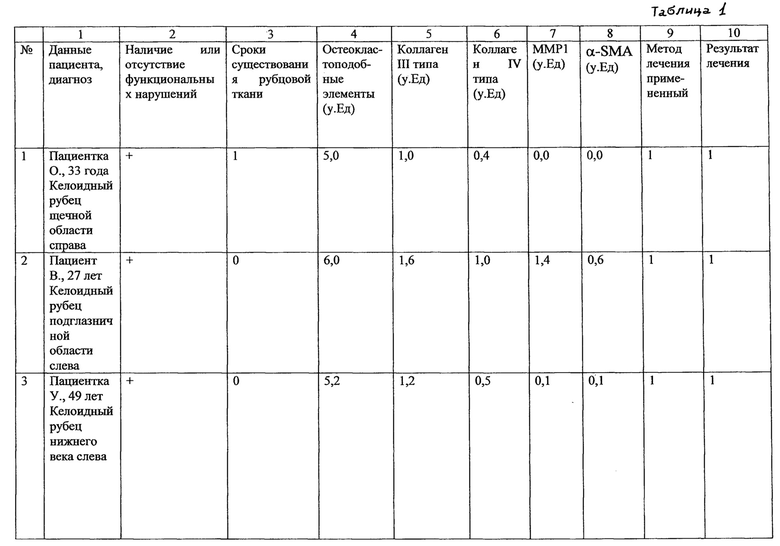
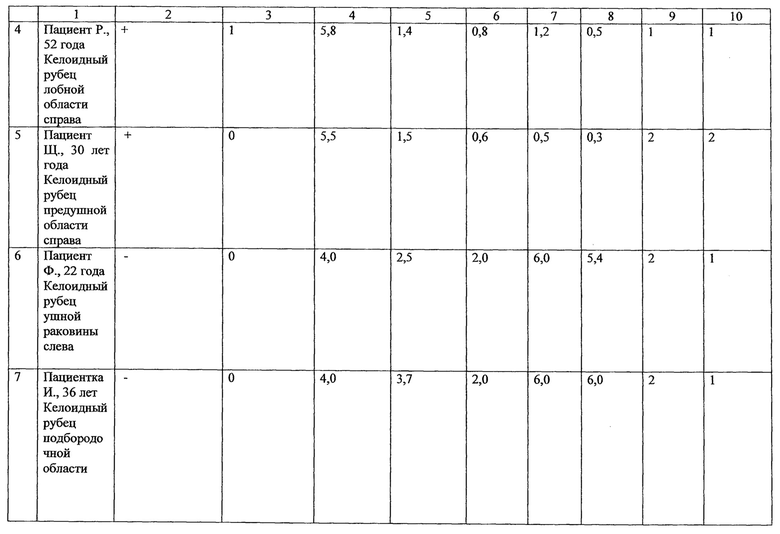
Осуществление способа показано на клинических примерах, данные по которым приведены в таблице 1. Клинические результаты представлены в столбце 10, (таблица) где хороший результат лечения обозначен (1), при котором была достигнута полная резорбция патологического рубца с сохранением косметического и функционального состояния анатомической области. Неудовлетворительный результат характеризовался продолженным ростом рубца после криолазерного лечения или рецидивом рубцовой ткани, подтвержденным как клинически, так и гистологически обозначен в таблице как (2).
Пример выбора эффективного вида лечения пациентки номер 10, описанный в таблице 1, которая отказалась от выбора метода лечения согласно клинико-морфологическому прогнозу и ей было проведено хирургическое лечение келоидного рубца ушной раковины слева. Через 2 месяца пациентка отмечает появление рецидива в послеоперационной области. После этого было проведено криолазерное лечение, и был получен хороший результат, который удовлетворил пациентку и функционально, и эстетически.
По вышеописанной методике было проведено исследование 110 пациентов с различной локализацией келоидных рубцов в области головы и шеи. Прогноз эффективности инвазивного лечения келоидных рубцов подтвердился на 95,5%. Все пациенты наблюдались в течение 1 года после операции и регулярно приходили на контрольные осмотры через 1, 3, 6 месяцев и через год после операции.
Предлагаемый способ выбора эффективного вида лечения келоидного рубца дает высокую результативность и позволяет подобрать индивидуально каждому пациенту определенную методику исходя из его клинико-морфологических параметров и сроков существования рубцовой ткани. Это позволяет оценить риски и возможности различных методов инвазивного лечения келоидного рубца и определить индивидуально исходя из клинической и морфологической характеристики необходимый и результативный вид лечения. С помощью данного способа выбора эффективного вида лечения возможно ускорить сроки реабилитации и добиться хороших функциональных и эстетических результатов у пациентов с келоидными рубцами.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования эффективности инвазивного лечения гипертрофического рубца | 2023 |
|
RU2803864C1 |
| Способ лечения гипертрофических и келоидных рубцов в области головы и шеи | 2020 |
|
RU2744669C1 |
| Способ прогнозирования формирования патологического рубца при заживлении операционной раны | 2018 |
|
RU2694009C1 |
| Способ прогнозирования формирования келоидного рубца | 2019 |
|
RU2709519C1 |
| Способ лечения пациентов с рубцовыми поражениями кожи | 2019 |
|
RU2712183C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПАТОЛОГИЧЕСКОГО РУБЦЕВАНИЯ ПРИ ХЕЙЛО- И ХЕЙЛОРИНОПЛАСТИКЕ У ДЕТЕЙ | 2010 |
|
RU2426125C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ СКВОЗНОГО ДЕФЕКТА КРЫЛА НОСА | 2009 |
|
RU2394511C1 |
| Способ дифференциальной диагностики красного плоского лишая и лейкоплакии слизистой оболочки полости рта | 2017 |
|
RU2651050C1 |
| СПОСОБ ПРОГНОЗА ТЕЧЕНИЯ САРКОИДОЗА | 2013 |
|
RU2549454C1 |
| Способ прогнозирования риска прогрессирования люминального рака молочной железы | 2024 |
|
RU2836845C1 |
Изобретение относится к медицине, а именно к пластической и реконструктивной хирургии. Способ выбора инвазивного лечения келоидного рубца включает сбор анамнеза с выявлением наличия или отсутствия функциональных нарушений, сроков существования рубцовой ткани. Дополнительно проводят гистологическое исследование с определением реакции остеокластоподобных элементов и иммуногистохимическое исследование рубцовой ткани, при котором выявляют значения ММР1, К III и IV типов, α-SMA. При имеющихся функциональных нарушениях вне зависимости от срока существования рубцовой ткани, при получении показателя реакции остеокластоподобных элементов в пределах 5,0-6,0 у.е., значения величины коллагена III типа в пределах 1,0-1,6 у.е., коллагена IV типа в пределах 0,4-1,0 у.е., ММР1 в пределах 0,0-1,4 у.е., α-SMA в пределах 0,0-0,6, проводят хирургическое лечение. При отсутствии функциональных нарушений, сроков существования рубцовой ткани менее 6 месяцев и при получении значения показателя реакции остеокластоподобных элементов равного 4,0 у.е., а значение величины коллагена III типа в пределах 2,5-3,7 у.е., коллагена IV типа, равного 2,0 у.е., ММР1, равной 6,0 у.е., α-SMA в пределах 5,4-6,0 у.е. проводят криолазерное лечение келоидного рубца. Изобретение позволяет подобрать индивидуально каждому пациенту определенную методику лечения, ускорить сроки реабилитации и добиться хороших функциональных и эстетических результатов у пациентов с келоидными рубцами. 6 ил., 1 табл.
Способ выбора инвазивного лечения келоидного рубца, включающий сбор анамнеза с выявлением наличия или отсутствия функциональных нарушений, сроков существования рубцовой ткани, отличающийся тем, что дополнительно проводят гистологическое исследование с определением реакции остеокластоподобных элементов и иммуногистохимическое исследование рубцовой ткани, при котором выявляют значения ММР1, К III и IV типов, α-SMA, и при имеющихся функциональных нарушениях вне зависимости от срока существования рубцовой ткани, при получении показателя реакции остеокластоподобных элементов в пределах 5,0-6,0 у.е., значения величины коллагена III типа в пределах 1,0-1,6 у.е., коллагена IV типа в пределах 0,4-1,0 у.е., ММР1 в пределах 0,0-1,4 у.е., α-SMA в пределах 0,0-0,6, проводят хирургическое лечение; при отсутствии функциональных нарушений, сроков существования рубцовой ткани менее 6 месяцев и при получении значения показателя реакции остеокластоподобных элементов равного 4,0 у.е., а значение величины коллагена III типа в пределах 2,5-3,7 у.е., коллагена IV типа, равного 2,0 у.е., ММР1, равной 6,0 у.е., α-SMA в пределах 5,4-6,0 у.е. проводят криолазерное лечение келоидного рубца.
| Способ лечения келоидов или гипертрофических рубцов с использованием антисмысловых соединений, направленно действующих на фактор роста соединительной ткани(CTGF) | 2012 |
|
RU2608655C2 |
| ЛЕЧЕНИЕ КЕЛОИДОВ | 2011 |
|
RU2578426C2 |
| СПОСОБ ЛЕЧЕНИЯ ГИПЕРТРОФИЧЕСКИХ И КЕЛОИДНЫХ РУБЦОВ | 2001 |
|
RU2200557C1 |
| ДЕРКАЧ Н.Н | |||
| и др | |||
| ОСОБЕННОСТИ КОЛЛАГЕНООБРАЗОВАНИЯ В СТРОМАЛЬНО-СОСУДИСТОМ КОМПОНЕНТЕ ТКАНЕЙ ГРЫЖЕВЫХ ВОРОТ И ГРЫЖЕВОГО МЕШКА У БОЛЬНЫХ С ПОСЛЕОПЕРАЦИОННЫМИ ВЕНТРАЛЬНЫМИ ГРЫЖАМИ / НАУЧНЫЙ ЭЛЕКТРОННЫЙ ЖУРНАЛ INNOVA, 2016, N 4(5), стр | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Dylan E | |||
| Lee et al | |||
Авторы
Даты
2023-10-26—Публикация
2023-04-06—Подача