Изобретение относится к медицине, а именно к интервенционной кардиологии, и предназначено для прогнозирования эффективности сердечной ресинхронизирующей терапии у больных с хронической сердечной недостаточностью (ХСН).
Хроническая сердечная недостаточность (ХСН) остается одной из наиболее важных проблем современной кардиологии. Одним из эффективных методов ее лечения является сердечная ресинхронизирующая терапия (СРТ). В основе этого метода лежит ресинхронизация, то есть восстановление синхронного сокращения желудочков сердца и коррекция нарушений электромеханических свойств миокарда, связанных с нарушением внутри- и межжелудочкового проведения. Для проведения СРТ выполняется имплантация специального бивентрикулярного электрокардиостимулятора с установкой трех электродов. Два из них - стимуляционные электроды, расположенные в правом предсердии и правом желудочке (ПЖ). Третий электрод предназначен для стимуляции левого желудочка (ЛЖ) со стороны эпикарда. В большинстве случаев используется трансвенозный доступ для проведения левожелудочкового электрода через основной ствол коронарного синуса (КС) в дистальные его венозные ветви на свободных стенках ЛЖ. Вопрос выбора области стимуляции ЛЖ при проведении СРТ остается нерешенным. Существуют исследования, показывающие четкую связь ответа на СРТ с областью имплантации левожелудочкового электрода. Одним из первых влияние взаимного расположения желудочковых электродов на эффективность СРТ продемонстрировал Е.К. Heist. По данным рентгенограмм 51 пациента с СРТ в прямой и боковой проекциях было установлено, что наибольшее расстояние между дистальными частями право- и левожелудочкового электродов коррелировало с более выраженным гемодинамическим ответом на СРТ. Принципиальный практический интерес имеет имплантация именно левожелудочкового электрода. Во многих случаях его положение ограничено анатомией венозного русла, возможностью фиксации электрода в нужном месте. Для оптимизации позиционирования левожелудочкового электрода были предложены различные алгоритмы, в том числе деление ЛЖ на сегменты, при этом установлено, что именно латеральная позиция имеет больший клинический эффект. В исследовании F.M. Merchant и соавт.было показано достоверное увеличение смертности, уменьшение степени обратного ремоделирования ЛЖ, а также усугубление ФК ХСН в группе с апикальной позицией левожелудочкового электрода по сравнению с группой базальной или срединной зоны имплантации за период наблюдения 15 месяцев. В большинстве исследований, касающихся топического расположения электродов, использовалась прямая визуализирующая методика- рентгенография, либо рентгеноскопия с применением стандартных рентгенологических проекций. При оценке достоверности рентгенологических заключений по позиции желудочковых электродов в сравнении с данными компьютерной томографии оказалось, что заключения, полученные первым способом, достаточно субъективны: точность позиции правожелудочкового электрода составила 37%, левожелудочкового электрода по длинной оси - 33%, по короткой - 41%; воспроизводимость данных - 64% для правожелудочкового электрода, 58% -для левожелудочкового электрода по длинной оси и 37% - по короткой оси. Были предприняты попытки оптимизации выбора зоны стимуляции на основе детерминации зон механической диссинхронии миокарда. Так, имплантация левожелудочкового электрода относительно зоны максимальной внутрижелудочковой диссинхронии миокарда рассматривалась в работах С.Ypenburg и соавт. По данным тканевой допплерографии, самыми частыми зонами поздней активации ЛЖ являлись его задняя (36%) и боковая (33%) стенки; стимуляция в зоне поздней активации ЛЖ ассоциировалась с большим ответом на СРТ и лучшим прогнозом через 6 месяцев наблюдения. В исследовании TARGET было выявлено более выраженное улучшение клинических и гемодинамических параметров, а также снижение смертности и уровня госпитализаций вследствие ХСН у пациентов с СРТ, которым имплантация левожелудочкового электрода проводилась с учетом зоны наибольшей внутрижелудочковой диссинхронии. Однако, итоговое расположение левожелудочкового электрода, прежде всего, зависит от анатомии вен коронарного синуса, наличия или отсутствия у пациента диафрагмальной стимуляции, а также свойств и стабильности положения самого электрода. Большой вклад в ответ на СРТ оказывает расстояние от стимулирующего полюса имплантированного левожелудочкового электрода до поздней зоны активации ЛЖ. Доказано, что при увеличении данного расстояния на величину более одного сегмента ЛЖ у пациентов не наблюдается отчетливого обратного ремоделирования через 6 месяцев и более после проведения СРТ. В настоящее время существует методика неинвазивного электрофизиологического картирования (НЭФК), с помощью которой при полной блокаде левой ножки пучка Гиса визуализируется зона поздней активации. При этом реконструкция трехмерной (3D) модели сердца при НЭФК выполняется как по данным компьютерной томографии, так и магнитно-резонансной томографии, что дает возможность дополнительно получить информацию о наличии фиброза или рубца ЛЖ. Методика НЭФК, помимо хорошей визуализации расположения желудочковых электродов, позволяет соотносить анатомические данные с функциональными изменениями электрического проведения. (Ревишвили А.Ш. и др. Клинические рекомендации по проведению электрофизиологических исследований, катетерной абляции и применению имплантируемых антиаритмических устройств. - 2017.).
Основная проблема существующих клинических рекомендаций, используемых для отбора кандидатов для проведения СРТ, заключается в объективно низкой точности прогноза эффективности терапии. В литературе имеются данные о том, что 30-40% прооперированных пациентов не улучшают своего состояния после имплантации устройств СРТ несмотря на полное соответствие критериям отбора и соблюдение всех рекомендаций послеоперационного лечения. Следовательно, улучшение качества дооперационного прогноза успешности СРТ является исключительно актуальной задачей фундаментальной и практической кардиологии, которая в настоящее время продолжает решаться с использованием разнообразных клинических признаков и усовершенствований существующих методик оценки.
Авторам не удалось найти в доступных источниках информации ближайший аналог заявляемого изобретения.
Техническим результатом заявляемого изобретения является осуществление прогнозирования для пациента-кандидата на СРТ эффективности, целесообразности и оправданности проведения данного вида лечения с использованием оптимизации расположения стимулирующих электродов. Также техническим результатом является снижение количества пациентов без эффекта от СРТ.
Для реализации заявленного технического результата в способе прогнозирования эффективности электрокардиостимуляционной ресинхронизирующей терапии, согласно изобретения претенденту на ресинхронизирующую терапию выполняют стандартное медицинское обследование, из которого берут данные ИМТ (индекс массы тела), ФВЛЖ (фракция левого желудочка), КДР_ЛЖ, также выполняют КТ (компьютерная томография торса), МРТ (магнитно-резонансная томография торса), по сегментированным изображениям которых строят цифровую геометрическую модель туловища, легких и сердца в форме конечно-элементной сетки желудочков сердца, в которой задают ход миокардиальных волокон, размечают непроводящие участки постинфарктных рубцов и участки фиброза со сниженной проводимостью, далее моделируют различные комбинации размещения электродов на поверхности ЛЖ, на основе геометрической модели проводят первый расчет персонифицированной электрофизиологической модели возбуждения желудочков сердца в режиме имитации естественного ритма при блокаде левой ножки пучка Гиса (БЛНПГ) с вычислением:
ATRVLV_LBBB (1) - индекс межжелудочковой диссинхронии при БЛНПГ;
TAT95_LBBB/MTV (1) - время 95% активации желудочков при БЛНПГ нормированное на объем миокардиальной ткани,
а также в режиме бивентрикулярной стимуляции для различных комбинаций размещения электродов с вычислением для каждой комбинации электродов:
ATRVLV_BiV (1) - индекса межжелудочковой диссинхронии при БиВ стимуляции и DLvInfarct (1) - расстояния от ЛЖ электрода до зоны инфаркта/фиброза,
далее полученные характеристики подставляют в ML-классификатор:
F=-0.19*ИМТ-15.33* ФВ_ЛЖ_до_СРТ+0.08* КДР_ЛЖ_до_СРТ-0.019* ATRVLV _BiV-0.04* ATRVLV _LBBB+3.96* TAT95_ LBBB /MTV+0.03* DLvInfarct+2.76
Рассчитывают первый набор значений ML-балла на поверхности ЛЖ ML-балл=1/(1+е-F),
далее строят регрессионную модель, предсказывающую второй набор значений ML-балла для скорректированного алгоритмом, второго набора комбинаций размещения электродов на поверхности ЛЖ, после чего с помощью байесовской оптимизации производят выбор точки стимуляции на поверхности ЛЖ, где ML-балл имеет максимальное значение, далее для этой точки производят расчет характеристик ML-классификатора: ATRVLV_LBBB (2); TAT95_LBBB/MTV (2); ATRVLV _BiV (2); DLvInfarct (2), после чего регрессионная модель переобучается по крайней мере два раза до достижения показателя алгоритма, при которых две последние итерации предсказали одну и ту же точку, для которой фиксируют значение ML-балла и при значении ML-балла больше или равном 0,5 прогнозируют, что претендент на ресинхронизирующую терапию будет респондером, а при значении ML-балла меньше 0,5 прогнозируют, что претендент на ресинхронизирующую терапию будет нереспондером.
Изобретение поясняется чертежами.
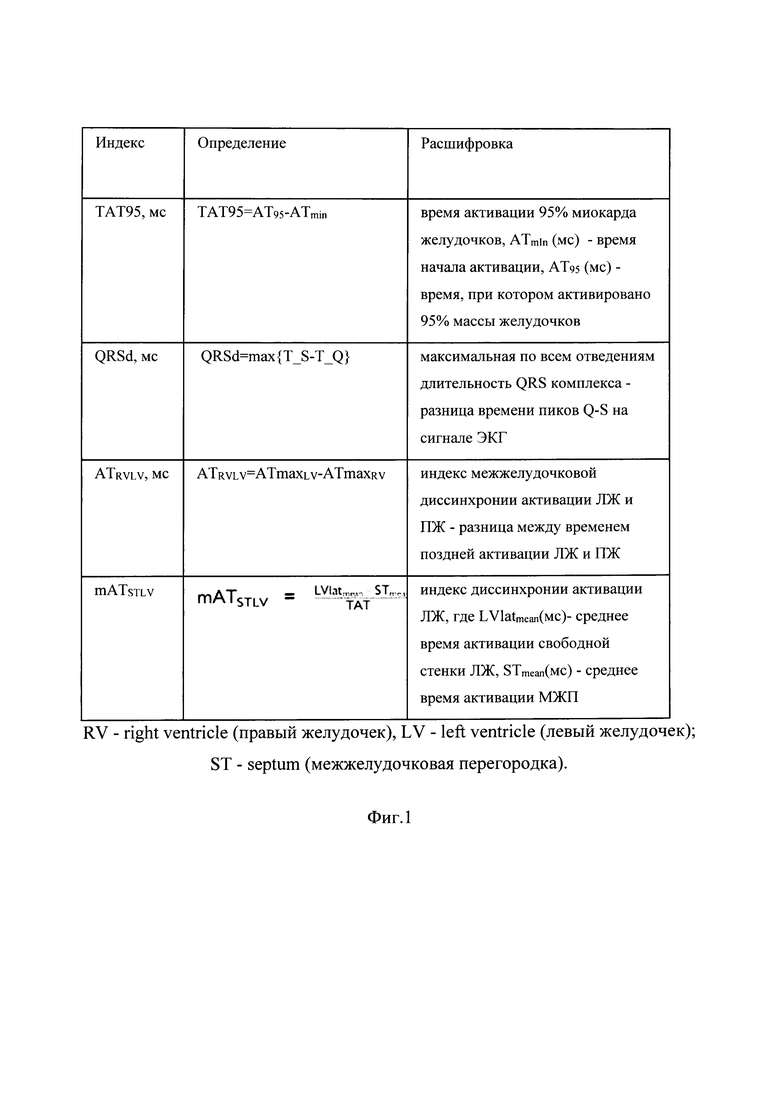
На фиг. 1 изображен способ прогнозирования эффективности сердечной ресинхронизирующей терапии с использованием оптимизации расположения стимулирующих электродов, индексы диссинхронии.
На фиг. 2 - то же, признаки, вошедшие в ML-классификатор.
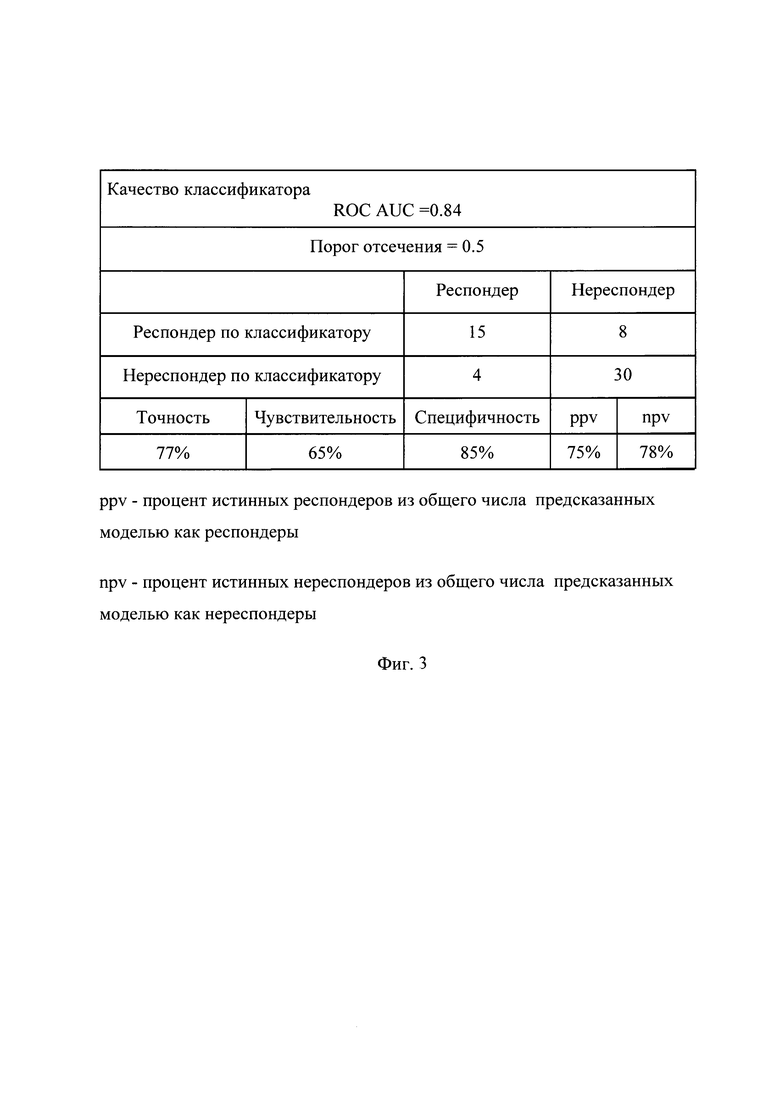
На фиг. 3 - то же, качественные характеристики ML-классификатора.
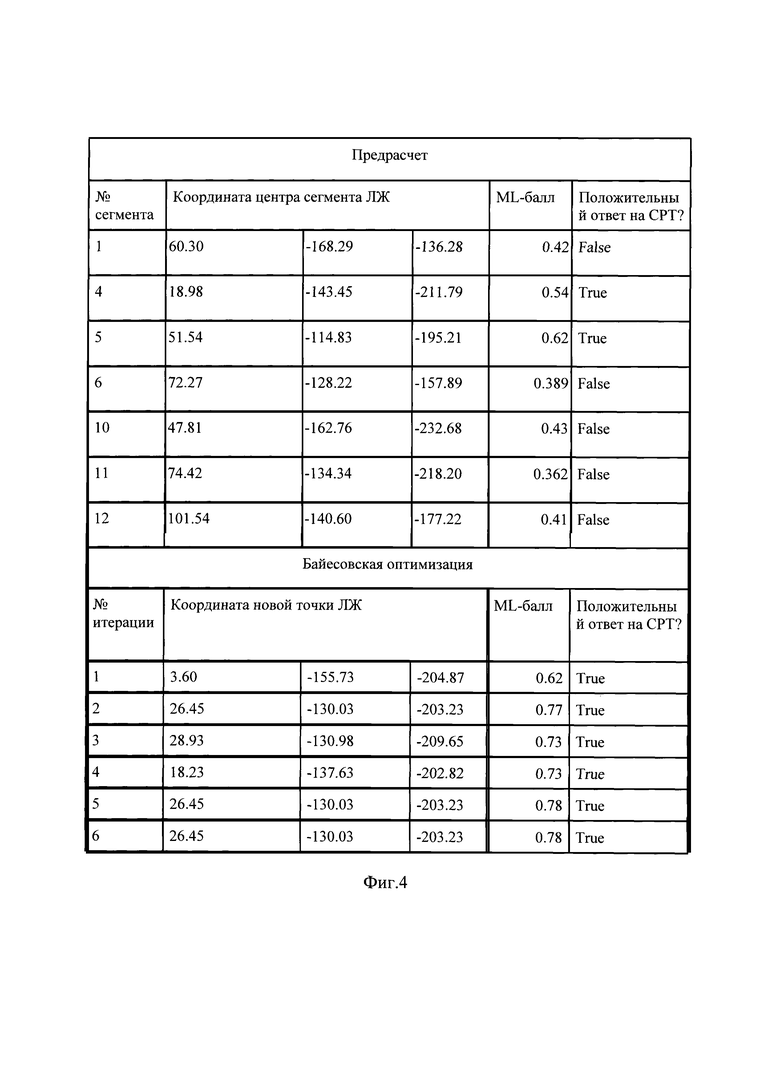
На фиг. 4 - то же, работа алгоритма оптимизации расположения стимулирующих электродов поэтапно в клиническом примере для пациента 1.
Способ осуществляют следующим образом.
Предварительно был разработан классификатор для оценки вероятности ответа на СРТ.
С помощью методов машинного обучения (анг.Machine Learning (ML)) был построен ML-классификатор, определяющий вероятность успеха СРТ [Khamzin, 2021].
Классификатор был обучен на гибридном наборе клинических и модельных данных для когорты из 57 пациентов, разделенных на 2 подгруппы - респондеры и нереспондеры согласно выбранному критерию успешности СРТ - увеличение фракции выброса (ФВ) ЛЖ более чем на 10% (ФВ10) через один год после имплантации СРТ устройств. Для построения ML-классификатора ответа на СРТ был использован гибридный набор клинических и модельных данных, содержащий:
1. Дооперационные клинические признаки из стандартных протоколов обследований претендентов на СРТ.
2. Дооперационные клинические признаки, вычисляемые при помощи геометрической модели желудочков, построенной на основе данных КТ/МРТ изображений:
• MTV - объем миокардиальной ткани, мл
• InfarctV - объем области постинфарктного рубца/фиброза, мл
• DLvRv - расстояние между ЛЖ и ПЖ электродами, мм
• DLvLATZ - расстояние от ЛЖ электрода до зоны поздней активации при модельной блокаде левой ножки пучка Гиса (БЛНПГ), мм
• DLvInfarct - расстояние от ЛЖ электрода до зоны постинфарктного рубца/фиброза, мм
3. Признаки, рассчитанные в персонализированных моделях возбуждения желудочков в БиВ и БЛНПГ режимах активации для каждого пациента (см. таблица, фиг.1):
• ТАТ95 - время активации 95% миокарда желудочков, мс
• QRSd - максимальная ширина QRS комплекса, мс
• ATRVLV - индекс межжелудочковой диссинхронии, мс
• mATSTLV - индекс внутрижелудочковой диссинхронии, мс
• IntAVSTLV - интегральный индекс внутрижелудочковой диссинхронии.
На выходе классификатора (или прогностической модели) формируется оценка вероятности успешности СРТ, т.е. более 10% увеличения ФВ. Далее результат классификатора называет ранжирующий балл (англ. ML-score) прогноза ответа на СРТ. В итоге, в ML-классификатор вошли следующие признаки:
- ИМТ - индекс массы тела;
- ФВ_ЛЖ - фракция выброса ЛЖ, %;
- КДР_ЛЖ - конечно-диастолический размер ЛЖ, мм;
- ATRVLV_LBBB - индекс межжелудочковой диссинхронии при БЛНПГ, мс;
- ATRVLV_BiV - индекс межжелудочковой диссинхронии при БиВ стимуляции, мс;
- TAT95_LBBB/MTV - время 95% активации желудочков при БЛНПГ нормированное на объем миокардиальной ткани, мс/мл;
- DLvInfarct - расстояние от ЛЖ электрода до зоны инфаркта/фиброза, мм.
В таблице на фиг. 2 приведены признаки, вошедшие в ML-классификатор и соответствующие коэффициенты логистической регрессии.
Была получена формула ML-классификатора:
F=-0.19*ИМТ-15.33* ФВ_ЛЖ_до_СРТ+0.08* КДР_ЛЖ_до_СРТ-0.019* ATRVLV _BiV-0.04* ATRVLV _LBBB+3.96* TAT95_ LBBB /MTV+0.03* DLvInfarct+2.76
ML-балл=1/(1+e-F)
e - математическая константа приблизительно равная 2.71828.
В таблице на фиг. 3 отображены данные, показывающие качество классификатора.
Для непосредственно прогнозирования эффективности СРТ кандидату на данный вид лечения перед имплантацией устройства помимо проведения стандартных исследований выполняют также ЭКГ, компьютерную томографию (КТ) и магнитно-резонансную томографию (МРТ) торса с описанием и сегментацией повреждений миокарда (постинфарктных рубцов, фиброза). Далее по сегментированным изображениям КТ и МРТ строится цифровая геометрическая модель в форме конечно-элементной сетки желудочков сердца, а также туловища и легких (см. статью [Khamzin, 2021] с подробным описанием технологии построения и расчета персонифицированных моделей сердца). В полученной персонифицированной геометрической модели желудочков сердца ЭКГ задается ход миокардиальных волокон (Bayer et al., 2012), размечаются непроводящие участки постинфарктных рубцов и участки фиброза со сниженной проводимостью и проводятся расчеты активации желудочков с использованием эйкональной электрофизиологической модели [Keener, 1991]. Далее моделируют различные комбинации размещения на поверхности ЛЖ с полюсами электрода, установленного поочередно в центр каждого из сегментов свободной стенки ЛЖ на эпикардиальной поверхности (сегменты 1,6,5,4,7,12,11,10,13,16,15 согласно 17-сегментной AHA схемы ЛЖ (bull - eye) [Cerqueira et al., 2002]). Если электроды попадают в зону постинфарктного рубца, то данный сегмент исключается из рассмотрения. Размещение ПЖ электрода осуществляют по стандартной методике в трех возможных положениях (базальная, срединная и верхушечная область эндокардиальной поверхности межжелудочковой перегородки ПЖ). На основе геометрической модели проводят первый расчет персонифицированной электрофизиологической модели возбуждения желудочков сердца в режиме имитации естественного ритма при БЛНПГ с вычислением:
ATRVLV_LBBB (1) - индекс межжелудочковой диссинхронии при БЛНПГ;
TAT95_LBBB/MTV (1) - время 95% активации желудочков при БЛНПГ нормированное на объем миокардиальной ткани,
а также в режиме БиВ стимуляции для различных размещений электродов с вычислением для каждой комбинации:
ATRVLV_BiV (1) - индекс межжелудочковой диссинхронии при БиВ стимуляции и DLvInfarct (1) - расстояние от ЛЖ электрода до зоны инфаркта/фиброза,
Результаты моделирования для каждой комбинации расположения электродов подаются на вход ML-классификатора:
F=-0.19*ИМТ-15.33* ФВ_ЛЖ_до_СРТ+0.08* КДР_ЛЖ_до_СРТ-0.019* ATRVLV _BiV-0.04* ATRVLV _LBBB+3.96* TAT95_LBBB/MTV+0.03* DLvInfarct+2.76
и рассчитывается соответствующий ML-балл для прогноза успеха СРТ ML-балл=1/(1+е-F),
Таким образом, получается первоначальный набор значений ML-балла на поверхности ЛЖ. Этот набор используют для дальнейшей интерполяции значений ML-балла на всей доступной для стимуляции поверхности ЛЖ. Интерполяция проводится методом регрессии на основе гауссовских процессов (GP регрессия) [Rasmussen, 2010]. В итоге получается регрессионная модель, предсказывающая значение ML-балла в зависимости от местоположения ПЖ и ЛЖ электродов. Выбор оптимального местоположения ЛЖ электрода, соответствующего максимальному значению ML-балла, производится с помощью метода байесовской оптимизации [Mockus, 2012]. Метод байесовской оптимизации заключается в итеративном выборе точки стимуляции, в которой так называемая "функция выбора" (или функция выгоды) имеет максимальное значение. В качестве функции выбора используется функция вида L=μ+k*σ, где μ - ожидаемое значение ML-балла предсказанное регрессионной моделью на предыдущем этапе, σ - среднеквадратичное отклонение значений целевой функции от оценки целевой функции, полученной на предыдущем этапе. Таким образом, метод позволяет найти баланс между, с одной стороны, поиском точек, которые позволят уточнить GP регрессионную модель (точки с большим значением ошибки, т.е. большим σ), а с другой стороны с поиском точек, в которых значение регрессионной функции - максимально (точки с максимальным μ). Коэффициент к позволяет сбалансировать обе стратегии. Мы использовали в нашем методе k=2. То есть после получения первоначального набора значений ML-балла на поверхности ЛЖ строят регрессионную модель при стимуляции из центров не инфарктных сегментов со стороны эпикарда свободной стенки ЛЖ. Затем на основании функции выбора байесовской оптимизации находится новая точка стимуляции, в которой рассчитываются характеристики (ATRVLV_LBBB (2); TAT95_LBBB/MTV (2); ATRVLV_BiV (2); DLvInfarct (2)) для ML-классификатора и ML-балл. Далее найденная точка добавляется к существующему набору значений, то есть формируется новый предсказывающий набор значений, после чего регрессионная модель переобучается и вся процедура нахождения новой точки повторяется до тех пор пока две последние итерации не предсказали одну и ту же точку, такая точка считается оптимальной для установки левожелудочкового электрода, при значении ML-балла больше или равном 0,5 прогнозируют, что претендент на СРТ будет респондером, а при значении ML-балла меньше 0,5 прогнозируют, что претендент на СРТ будет нереспондером.
Координаты ПЖ и ЛЖ электродов передаются в виде визуализации на персонифицированной геометрии ЛЖ.
Таким образом, правильный выбор конфигурации стимулирующих устройств, обеспечивающих наиболее качественную синхронизацию активности желудочков с учетом их структурно-анатомических и функциональных особенностей, является одним из существенных факторов, влияющих на успешность СРТ. Разработанные нами персонифицированные модели электрической активности сердца позволили нам провести in-silico исследование различных подходов для решения этой задачи. Используя разработанные на основе индивидуальных клинических данных модели сердец 57 пациентов с имплантированными устройствами СРТ, мы показали, что решения модели являются чувствительными к положению электродов. Оптимизация расположения право- и левожелудочкового (ПЖ, ЛЖ) электродов с точки зрения минимизации различных показателей электрической активации и диссинхронии желудочков дает значимые преимущества по сравнению с известным клиническим расположением электродов. Целевой выбор расположения электродов в модели позволяет значимо уменьшить полное время активации желудочков, ширину QRS комплексов, индексы межжелудочковой и внутрижелудочковой диссинхронии, а также увеличить вероятность успешности СРТ.
Разработан принципиально новый подход, заключающийся в использовании комбинированных клинических и модельных данных для прогноза успешности СРТ. Наряду с имеющимися дооперационными клиническими данными пациентов мы использовали результаты расчетов персонифицированных моделей электрической активности желудочков сердца в качестве in-silico предсказаний результативности виртуальной стимуляции желудочков для конкретного пациента, которые можно получить до имплантации ему устройства. Впервые объединенный гибридный набор реальных и расчетных данных был нами использован для обучения модели классификации респондеров и нереспондеров на терапию [Khamzin, 2021].
Клинические примеры
1. Пациент А.
При стандартной методике выбора места установки стимулирующих электродов, используемой в клинике, пациент является нереспондером. Отсутствием ответа на сердечную ресинхронизирующую терапию считается если увеличение фракции выброса ЛЖ через год после имплантации составляет менее 10%. У данного пациента зафиксировано увеличение фракции выброса всего на 7%.
Из дооперационных клинических протоколов получены характеристики:
ИМТ=27.3;
ФВ ЛЖ (%)=24;
КДР ЛЖ (мм)=72.
Выполняют КТ, МРТ, по сегментированным изображениям которых строят цифровую геометрическую модель туловища, легких и сердца в форме конечно-элементной сетки желудочков сердца, в которой задают ход миокардиальных волокон, размечают непроводящие участки постинфарктных рубцов и участки фиброза со сниженной проводимостью. Далее моделируют различные комбинации размещения электродов на поверхности ЛЖ, на основе геометрической модели проводят первый расчет персонифицированной электрофизиологической модели возбуждения желудочков сердца в режиме имитации естественного ритма при блокаде левой ножки пучка Гиса (БЛНПГ), а также в режиме бивентрикулярной стимуляции для различных комбинаций размещения электродов.
Из персонифицированной модели при расположении стимулирующих электродов, поставленных при стандартной методике, получены характеристики:
ATRVLV_LBBB (мс)=48.14
ATRVLV_BiV (мс)=-18.83
ТАТ95_LBBB/MTV (мс/мл)=0.25
DLvInfarct (мм)=20.03
Рассчитываем ML-балл:
F=-0.19*ИМТ-15.33* ФВ ЛЖ_до_СРТ+0.08* КДР_ЛЖ_до_СРТ-0.019* ATRVLV _BiV-0.04* ATRVLV _LBBB+3.96* TAT95_ LBBB /MTV+0.03* DLvInfarct+2.76
ML-балл=1/(1+e-F)=0.39<0.5
Классификатор правильно предсказывает пациента А как нереспондера с точки зрения вероятности ответа на СРТ.
В таблице на фиг. 4 представлена работа алгоритма поэтапно. На первом этапе выполняется расчет регрессионной модели при стимуляции из центров неинфарктных сегментов со стороны эпикарда свободной стенки левого желудочка (сегменты 1,4,5,6,10,11,12). Затем на основании функции выбора находится новая точка стимуляции (координаты [3.60, -155.73, -204.87]), где ML-балл имеет максимальное значение (0.62), рассчитываются значения характеристик ML-классификатора. Затем проводится следующая итерация алгоритма, до тех пор пока новая найденная точка не совпадает с предыдущей найденной точкой (ср. 5 и 6 итерации алгоритма).
При оптимизации положения стимулирующих электродов характеристики, рассчитываемые с помощью персонифицированной модели, следующие:
ATRVLV_LBBB (мс)=48.14
ATRVLV_BiV (мс)=4.71
ТАТ95_LBBB/MTV (мс/мл)=0.25
DLvInfarct (мм)=53.45
ML-балл=0.78>0.5
Пациент А прогнозируется как респондер на СРТ. Рекомендованное расположение ЛЖ электрода отличается от выбранного при стандартной методике: при оптимальном расположении координаты ЛЖ электрода попадают в сегмент №4 ЛЖ (базальный уровень задней стенки ЛЖ), в то время как при стандартной методике в сегмент №11 ЛЖ (срединный уровень задне-боковой стенки ЛЖ). ПЖ электрод при оптимизации выбран такой же, что и при стандартной методике.
2. Пациент Б.
Способ осуществляют аналогично описанному в примере 1.
При стандартной методике выбора расположения стимулирующих электродов пациент является респондером. У него зафиксировано увеличение фракции выброса ЛЖ на 13% после операции через 1 год.
Из дооперационных клинических протоколов получены характеристики:
ИМТ=17.6;
ФВ ЛЖ(%)=16;
КДР_ЛЖ (мм)=59.
Из персонифицированной модели при расположении стимулирующих электродов, поставленных при стандартной методике получены характеристики:
ATRVLV_LBBB (мс)=74.57
ATRVLV_BiV (мс)=-21.85 TAT95_LBBB/MTV (мс/мл)=0.99 DLvInfarct (мм)=53.17
Рассчитываем ML-балл:
F=-0.19*ИМТ-15.33* ФВ ЛЖ_до_СРТ+0.08* КДР_ЛЖ_до_СРТ-0.019* ATRVLV_BiV-0.04* ATRVLV _LBBB+3.96* TAT95_ LBBB /MTV+0.03* DLvInfarct+2.76
ML-балл=1/(1+e-F)=0.99>0.5
Подтверждается, что классификатор правильно определяет пациента как респондера.
При оптимизации положения стимулирующих электродов, рассчитываемые характеристики с помощью персонифицированной модели:
ATRVLV_LBBB (мс)=74.57
ATRVLV_BiV (мс)=11.09
ТАТ95_LBBB/MTV (мс/мл)=0.99
DLvInfarct (мм)=61.29
ML-балл=0.99>0,5
Пациент прогнозируется как респондер на СРТ при оптимальном расположении электродов. При оптимальном расположении координаты ЛЖ электрода попадают в сегмент №12 ЛЖ (срединный отдел переднебоковой стенки), такое же расположение и при стандартной методике. ПЖ электрод при оптимизации выбран такой же, что и при стандартной методике.
3. Пациент В.
Способ осуществляют аналогично вышеописанным примерам
При стандартной методике выбора расположения стимулирующих электродов не наблюдалось ответа на СРТ. У данного пациента зафиксировано увеличение фракции выброса ЛЖ всего на 3%.
Из дооперационных клинических протоколов получены характеристики:
ИМТ=32.8;
ФВ ЛЖ(%)=0.35;
КДР_ЛЖ (мм)=71.
Из персонифицированной модели при расположении стимулирующих электродов, поставленных при стандартной методике получены характеристики:
ATRVLV_LBBB (мс)=34.53
ATRVLV_BiV (мс)=-15.31
ТАТ95_LBBB/MTV (мс/мл)=0.4
DLvInfarct(мм)=-1 (нет инфарктных рубцов и фиброзных зон)
Рассчитываем ML-балл:
F=-0.19*ИМТ-15.33* ФВЛЖ_до_СРТ+0.08* КДР_ЛЖ_до_СРТ-0.019* ATRVLV _BiV-0.04* ATRVLV_LBBB+3.96* TAT95_ LBBB /MTV+0.03* DLvInfarct+2.76
ML-балл=1/(1+e -F)=0.11<0.5
Классификатор правильно прогнозирует пациента как нереспондера при стандартном расположении электродов.
При оптимизации положения стимулирующих электродов, рассчитываемые характеристики с помощью персонифицированной модели:
ATRVLV_LBBB (мс)=34.53
ATRVLV_BiV (мс)=0.83
ТАТ95_LBBB/MTV (мс/мл)=0.4
DLvInfarct (мм)=-1
ML-балл=0.16<0.5
Пациент прогнозируется как нереспондер на СРТ даже при оптимальном расположении электродов. При оптимальном расположении координаты ЛЖ электрода попадают в сегмент №1 ЛЖ (базальный отдел передней стенки ЛЖ), в то время как при стандартной методике в сегмент №5 ЛЖ (базальный отдел заднебоковой стенки ЛЖ). ПЖ электрод при оптимизации выбран такой же, что и при стандартной методике.
Результат предполагает неэффективность проведения СРТ для данного пациента и исключение его из списка кандидатов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования «супер-ответа» на сердечную ресинхронизирующую терапию у пациентов с полной блокадой левой ножки пучка Гиса и хронической сердечной недостаточностью различной этиологии | 2023 |
|
RU2813796C1 |
| Способ прогнозирования положительного ответа на сердечную ресинхронизирующую терапию у пациентов с электрокардиографическими критериями блокады левой ножки пучка Гиса по Штраусу | 2024 |
|
RU2830640C1 |
| Способ прогнозирования ответа на сердечную ресинхронизирующую терапию у пациентов с хронической сердечной недостаточностью | 2019 |
|
RU2721821C1 |
| СПОСОБ ПРЕДСКАЗАНИЯ СУПЕРОТВЕТА НА СЕРДЕЧНУЮ РЕСИНХРОНИЗИРУЮЩУЮ ТЕРАПИЮ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2019 |
|
RU2746530C2 |
| Способ прогнозирования эффективности электрокардиостимуляционной ресинхронизирующей терапии у больных с дилатационной кардиомиопатией в ранний послеоперационный период | 2020 |
|
RU2801127C2 |
| СПОСОБ ПРЕДСКАЗАНИЯ ОТВЕТА НА СЕРДЕЧНУЮ РЕСИНХРОНИЗИРУЮЩУЮ ТЕРАПИЮ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2018 |
|
RU2716479C1 |
| СПОСОБ ПРЕДСКАЗАНИЯ СУПЕРОТВЕТА НА СЕРДЕЧНУЮ РЕСИНХРОНИЗИРУЮЩУЮ ТЕРАПИЮ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2016 |
|
RU2623487C1 |
| Способ прогнозирования положительного ответа на кардиоресинхронизирующую терапию у пациентов с хронической сердечной недостаточностью II и III функционального класса | 2022 |
|
RU2786467C1 |
| СПОСОБ ВЫБОРА ХИРУРГИЧЕСКОГО СПОСОБА ДОСТАВКИ ЛЕВОЖЕЛУДОЧКОВОГО ЭЛЕКТРОДА ПРИ ЛЕЧЕНИИ СИНДРОМА ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2010 |
|
RU2493779C2 |
| Способ определения выраженности фиброзного поражения миокарда с помощью МРТ для отбора кандидатов на проведение сердечной ресинхронизирующей терапии | 2018 |
|
RU2685643C1 |

Изобретение относится к медицине, а именно к способу прогнозирования эффективности сердечной ресинхронизирующей терапии у больных с хронической сердечной недостаточностью. При этом претенденту на ресинхронизирующую терапию выполняют медицинское обследование, из которого берут данные ИМТ, ФВ_ЛЖ, КДР_ЛЖ. По сегментированным изображениям КТ и МРТ строят цифровую геометрическую модель туловища, легких и сердца в форме конечно-элементной сетки желудочков сердца. Задают в геометрической модели ход миокардиальных волокон. Размечают непроводящие участки постинфарктных рубцов и участки фиброза со сниженной проводимостью. Моделируют комбинации размещения электродов на поверхности ЛЖ. На основе геометрической модели проводят первый расчет персонифицированной электрофизиологической модели возбуждения желудочков сердца в режиме имитации естественного ритма при блокаде левой ножки пучка Гиса, а также в режиме бивентрикулярной стимуляции. Полученные характеристики подставляют в ML-классификатор. Рассчитывают первый набор значений ML-балла на поверхности ЛЖ. Строят регрессионную модель, предсказывающую второй набор значений ML-балла для скорректированного алгоритмом второго набора комбинаций размещения электродов на поверхности ЛЖ. С помощью байесовской оптимизации производят выбор точки стимуляции на поверхности ЛЖ, где ML-балл имеет максимальное значение. Для этой точки производят расчет характеристик ML-классификатора. Переобучают регрессионную модель по крайней мере два раза до достижения показателей алгоритма, при которых две последние итерации предсказали одну и ту же точку, для которой фиксируют значение ML-балла. При значении ML-балла больше или равном 0,5 прогнозируют, что претендент на ресинхронизирующую терапию будет респондером. При значении ML-балла меньше 0,5 прогнозируют, что претендент на ресинхронизирующую терапию будет нереспондером. Обеспечивается прогнозирование эффективности, целесообразности и оправданности проведения СРТ с использованием оптимизации расположения стимулирующих электродов, что снижает количество пациентов без эффекта от СРТ. 4 ил., 3 пр.
Способ прогнозирования эффективности электрокардиостимуляционной ресинхронизирующей терапии, отличающийся тем, что претенденту на ресинхронизирующую терапию выполняют медицинское обследование, из которого берут данные ИМТ, ФВ_ЛЖ, КДР_ЛЖ, также выполняют КТ, МРТ, по сегментированным изображениям которых строят цифровую геометрическую модель туловища, легких и сердца в форме конечно-элементной сетки желудочков сердца, в которой задают ход миокардиальных волокон, размечают непроводящие участки постинфарктных рубцов и участки фиброза со сниженной проводимостью, далее моделируют комбинации размещения электродов на поверхности ЛЖ, на основе геометрической модели проводят первый расчет персонифицированной электрофизиологической модели возбуждения желудочков сердца в режиме имитации естественного ритма при блокаде левой ножки пучка Гиса (БЛНПГ) с вычислением:
ATRVLV_LBBB (1) - индекса межжелудочковой диссинхронии при БЛНПГ;
TAT95_LBBB/MTV (1) - времени 95% активации желудочков при БЛНПГ, нормированное на объем миокардиальной ткани,
а также в режиме бивентрикулярной стимуляции для различных комбинаций размещения электродов с вычислением для каждой комбинации электродов:
ATRVLV_BiV (1) - индекса межжелудочковой диссинхронии при БиВ стимуляции и
DLvInfarct (1) - расстояния от ЛЖ электрода до зоны инфаркта/фиброза,
далее полученные характеристики подставляют в ML-классификатор:
F=-0.19*ИМТ-15.33*ФВ_ЛЖ_до_СРТ+0.08*КДР_ЛЖ_до_СРТ-0.019*ATRVLV_BiV-0.04*ATRVLV_LBBB+3.96*TAT95_LBBB/MTV+0.03*DLvInfarct+2.76,
рассчитывают первый набор значений ML-балла на поверхности ЛЖ
ML-балл=1/(1+е-F),
далее строят регрессионную модель, предсказывающую второй набор значений ML-балла для скорректированного алгоритмом второго набора комбинаций размещения электродов на поверхности ЛЖ, после чего с помощью байесовской оптимизации производят выбор точки стимуляции на поверхности ЛЖ, где ML-балл имеет максимальное значение, далее для этой точки производят расчет характеристик ML-классификатора: ATRVLV_LBBB (2); TAT95_LBBB/MTV (2); ATRVLV_BiV (2); DLvInfarct (2), после чего переобучают регрессионную модель по крайней мере два раза до достижения показателей алгоритма, при которых две последние итерации предсказали одну и ту же точку, для которой фиксируют значение ML-балла, и при значении ML-балла больше или равном 0,5 прогнозируют, что претендент на ресинхронизирующую терапию будет респондером, а при значении ML-балла меньше 0,5 прогнозируют, что претендент на ресинхронизирующую терапию будет нереспондером.
| WO 2021090659 A1, 14.05.2021 | |||
| Пневматическая шина | 2015 |
|
RU2633457C1 |
| US 10311978 B2, 04.06.2019 | |||
| WO 2010052303 A1, 14.05.2010 | |||
| JP 5660849 B2, 28.01.2015 | |||
| US 6963777 B2, 08.11.2005 | |||
| СПОСОБ ПРЕДСКАЗАНИЯ СУПЕРОТВЕТА НА СЕРДЕЧНУЮ РЕСИНХРОНИЗИРУЮЩУЮ ТЕРАПИЮ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2019 |
|
RU2746530C2 |
Авторы
Даты
2023-11-01—Публикация
2022-11-23—Подача