Изобретение относится к биотехнологии, в частности к конструированию вакцин, и может быть использовано в учреждениях, занимающихся созданием вакцинных препаратов для профилактики эшерихиоза у животных.
В настоящее время есть исследования по использованию биопрепаратов, которые включают сразу три вида токсинов патогенных эшерихий: термолабильный (LT) и термостабильный (ST) и шигаподобный (STX) токсины, как в чистом виде, так и в сочетании с адъювантами (Караев Я.М. Иммуногенные и протективные свойства эшерихиозного анатоксина: дис. … канд. вет. наук / Я.М. Караев. - Краснодар: КубГАУ, 2009. - 132 с; Тищенко А.С. Влияние адъювантов на иммуногенные свойства эшерихиозного анатоксина: дис. … канд. вет. наук / А.С. Тищенко. - Краснодар: КубГАУ, 2011. - 124 с.).
Однако этими исследованиями было установлено, что эшерихиозный анатоксин стимулирует клеточные и гуморальные звенья иммунитета в первые сутки после введения препаратов, а использование адъювантов хоть и усиливает иммунный ответ, но на непродолжительное время.
Учитывая данные обстоятельства, необходимо искать новые способы повышения иммуногенной активности вакцинных препаратов па основе инактивированных токсинов кишечной палочки.
Известна вакцина против эшерихиоза животных (патент РФ №2043771, кл. A61K 39/ 108, 1995 г.) изготовленная из соматических - O78, O141; белковых адгезивных - К88, К99, 987Р, F41; капсульных полисахаридных антигенов - К80. К87, а также включает ТЛ и ГС-анатоксины. В настоящее время данная вакцина прошла модернизацию путем добавления штаммов эшерихий и включением помимо ТЛ и ТС шигаподобных токсинов (VT1 и VT2 анатоксины) кишечной палочки, инактивированных формалином в количестве 0,4% с добавлением в качестве адъюванта геля гидрата окиси алюминия в количестве 25% В 1 см вакцины содержится 10 млрд микробных тел эшерихий. Коммерческое название - Вакцина против эшерихиоза животных Вероколивак К88, К99, 987Р, F41, ТЛ-, ТС-, VT1 и VT2 анатоксины (организация-производитель ФГУП «Армавирская биофабрика», Россия) (Вакцинопрофи-лактика эшерихиоза сельскохозяйственных животных // http://www.armbio.info/verokolivak.html; Вакцина против эшерихиоза животных // http://www.armbio.info/catalog/1006-3).
Недостатком данной усовершенствованной вакцины является то, что в ней содержится очень большое количество балластных антигенов в виде целых клеток Е. coli и нерастворимого минерального адъюванта, а это негативно сказывается на формировании у животных иммунной защиты, а так же развития у привитых животных побочных реакций и осложнений. Кроме того, способ получения такой вакцины очень сложен, поскольку требует раздельного культивирования 18 штаммов эшерихий.
Известно применение гидрата окиси алюминия и минерального масла по-отдельности в качестве адъювантов для усиления иммуногенности эшерихиозного анатоксина, содержащим инактивированные токсины (TL, TS, STX) Е. coli (Терехов, В.И. Влияние различных адъювантов на иммуноген-ные свойства эшерихиозного анатоксина / В.И. Терехов, Я.М. Караев, А.С. Тищенко, А.В. Иванов // Тр. / КубГАУ. - 2009. - Вып. №1 (ч.1) Серия: Ветеринарные науки. - С. 100-102.; Тищенко Л.С. Влияние адъювантов на имму-ногенные свойства эшерихиозного анатоксина: дис. канд. вет. наук / А.С. Тищенко. - Краснодар: КубГАУ, 2011. - 124 с.; Тищенко А.С. Иммуногенные свойства эшерихиозного полианатоксина в сочетании с гидратом окиси алюминия / Итоги научно-исследовательской работы за 2016 год: сб. ст.по материалам 72-й науч. - практ. конф. преподавателей. - Краснодар: КубГАУ, 2017. - С. 199-200; Тищенко А.С., Терехов В.И., Мартыненко Я.Н. Влияние минерального и масляного адъювантов на иммуногенность комплексного эшерихиозного анатоксина / Инновационные технологии в сельском хозяйстве: материалы III Междунар. науч. конф. (г. Казань, май 2017 г. ). - Казань: Бук, 2017. - С. 34-39; Киященко А.А., Велик А.Р., Тищенко А.С. Иммуногенные свойства эшерихиозного полианатоксина при совместном использовании с масляным адъювантом / В сборнике: Вестник научно-технического творчества молодежи Кубанского ГАУ. Краснодар: КубГАУ, 2017. - С. 32-35.; Тищенко А.С., Мусатова Н.С Изменение показателей крови у кроликов после применения комплексного эшерихиозного анатоксина в сочетании с адъювантами / В сборнике: Проблемы и перспективы развития науки и образования в XXI веке. Материалы Международной (заочной) научно-практической конференции. - 2017. - С. 69-73).
Недостатком известных исследований является то, что эшерихиозный анатоксин с использованием в качестве адъювантов по-отдельности гидрата окиси алюминия и минерального масла обладали непродолжительным иммунным ответом, что отражалось на эффективности специфической профилактики и продолжительности поствакцинальной защиты у животных против токсинов кишечной палочки. Кроме того, биологической моделью в этих исследованиях выступали белые крысы и кролики и неизвестно, как будут проявлять себя компоненты вакцины на телятах и поросятах.
Известно использование адъюванта (патент РФ №2510845, кл. A61K 39/39, 2014 г.) включающий эмульгатор в виде кремнийорганического соединения и масляную основу. Для вакцины типа «вода в масле» адъювант содержит биологически инертное кремнийорганические соединения цетил-ПЭГ/ППГ-10/1-диметикон, для вакцины «вода в масле в воде» - ПЭГ/ППГ-18/18-диметикон, для вакцины типа «масло в воде» ПЭГ-12-диметикон в концентрации от 1,5 до 3% масс.Предложенное изобретение позволяет повысить стабильность эмульсионных вакцин, повысить безопасность эмульсионных вакцин, а также обеспечить прогнозируемое время иммунного ответа.
Известно техническое решение (патент РФ №2644654, кл. А61К 39/105, 2018 г.) заключающееся в получении вакцины против кампилобактериоза содержащей в качестве адъюванта 2%-ную суспензию AL(ОН)3 и масляный адъювант, состоящий из эмульгатора (биологически инертное кремнийорганическое соединение цетил-ПЭГ/ППГ-10/1-диметикон) - 1,5% и масляной основы - вакцинное масло "М" по ТУ 38101 1224 - 98,5%) и вспомогательные компоненты.
Известную вакцину используют для кампилобактериоза у КРС, свиней, овец и птиц, который сопровождается поражением репродуктивных органов, вагинитами, частыми перекрытиями, временным бесплодием, массовыми абортами, метритами, задержанием последа, рождением нежизнеспособного приплода; у кур - снижением приростов массы бройлеров, яйценоскости кур-несушек и падежом цыплят.
Недостатком известного технического решения является то, что его не возможно использовать для лечения эшерихиоза у молодняка сельскохозяйственных животных, т.к. для получения культуральной среды применяют культуру (колонии) возбудителя кампилобактериоза и для смыва культуры возбудителя и для инактивации биомассы используют вспомогательные компоненты: 0,9%-ный раствор NaCl и теотропин, которые могут вызвать побочные явления.
Наиболее близким по технической сущности является техническое решение, является вакцина против эшерихиоза телят и поросят (патент РФ №2764600, кл. А61К 39/108, 2022 г.) включающая бесклеточную культуральную среду, содержащую инактивированные термолабильные, термостабильные и шигаподобные токсины Escherichia coli, полученные при смешивании в равных соотношениях эпизоотических штаммов Escherichia coli, обладающих генами термолабильного, термостабильного и шигапо-добного токсинов, инактивированных формалином до его конечной концентрации 0,4%, с последующим отделением бактериальной массы с помощью стерилизующей фильтрации и адъюванты.
Недостаточная эффективность специфической профилактики эшерихиоза у телят и поросят.
Техническим результатом изобретения является повышение эффективности специфической профилактики эшерихиоза у телят и поросят и расширение арсенала вакцин против эшерихиоза у телят и поросят.
Технический результат достигается тем, что в вакцине против эшерихиоза телят и поросят, включающей бесклеточную культуральную среду, содержащую инактивированные термолабильные, термостабильные и шигаподобные токсины Escherichia coli, полученные при смешивании в равных соотношениях эпизоотических штаммов Escherichia coli, обладающих генами термолабильного, термостабильного и шигаподобного токсинов, инактиви-рованных формалином до его конечной концентрации 0,4%, с последующим отделением бактериальной массы с помощью стерилизующей фильтрации и адьюванты, согласно изобретению в качестве адъювантов содержит 2%-ную суспензию AL(ОН)3 и масляный адъювант, состоящий из эмульгатора в качестве которого используют биологически инертное кремнийорганическое соединение цетил-ПЭГ/ППГ-10/1-диметикон в количестве 1,5% и масляной основы - вакцинное масло "М" по ТУ 381011224 - 98,5%), которые внесены в бесклеточную культуральную среду, содержащую инактивированные термолабильные, термостабильные и шигаподобные токсины Escherichia coli, полученные при смешивании в равных соотношениях эпизоотических штаммов Escherichia coli поочередно с последующим перемешиванием, при следующем соотношении компонентов, мас. %:
Новизна технического решения состоит в том, что за счет совместного использования бесклеточных культур эпизоотических штаммов Escherichia coli, продуцирующих термолабильный, термостабильный и шигаподобный токсины, инактивированных формалином и адъювантов: 2%-ной суспензией AL(OH)3 и масляным адъювантом достигается повышение иммуногенных свойств вакцины и эффективности профилактики эшерихиоза у животных, а также безвредность биопрепарата за счет отсутствия после применения поствакцинальных реакций.
В патентной и научно-технической литературе не обнаружена аналогичная заявляемой совокупность признаков, что позволяет судить об изобретательском уровне заявляемого предложения.
Предложенная вакцина соответствует критерию «промышленная применимость» поскольку легко воспроизводима, не требует сложного технологического оборудования и условий.
Полученную вакцину фасуют по 100 мл в стерильные флаконы, укупоривают и проверяют на стерильность и безвредность. По внешнему виду готовая вакцина представляет собой прозрачную опалесцирующую жидкость соломенного цвета с выпадающим беловато-сероватым осадком на дне, который при встряхивании флакона легко разбивается, образуя равномерную взвесь. Срок хранения в сухом и темном помещении при температуре 4-10°С - 1 год.
Полученную вакцину проверяли па стерильность и безвредность.
При контрольных высевах анатоксина па МПА, МПБ, среду Китта-Тароцци, Сабуро, Эндо рост бактериальной и грибной флоры отсутствовал, что свидетельствовало о стерильности препарата.
При внутрибрюшинном введении препарата в дозе 0,3 мл белым мышам массой 20-22 г угнетения и гибели их в течение 10 дней не отмечали, что является показателем безвредности препарата.
Эффективность вакцины против эшерихиоза зависит от свойств подобранных эпизоотических штаммов Escherichia coli, последовательности приготовления и процентного соотношения компонентов входящий в ее состав, таких как:
- гидрат окиси алюминия (2%-ная суспензия AL(ОН)3) - 18 мл (18%), 19 мл (19%), 20 мл (20%), 21 мл (21%), 22 мл (22%).
- масляный адъювант, состоящий из эмульгатора (биологически инертное кремнийорганическое соединение цетил-ПЭГ/ППГ-10/1 - диметикон) - 1,5% и масляной основы - вакцинное масло "М" по ТУ 381011224 - 98,5% (патент РФ №2510845)) - 48 мл (48%); 49 мл (49%); 50 мл (50%); 51 мл (51%) и 52 мл (52%).
Количественные значения ввода адъювантов подобраны экспериментальным путем, при этом учитывалась иммуногенная активность гидроокись алюминиевой масляной анатоксин-вакцины. При вводе гидрата окиси алюминия в объеме 18%>и масляного адъюванта 48% иммуногенная активность снижалась, и была не достаточной для длительного сохранения поствакцинального иммунитета. При вводе минерального адъюванта в объеме 22%, а масляного 52% увеличения продукции специфических антител более значения, чем при их вводе в объеме 19-21% и 49-51% соответственно, не происходило, а экономические затраты возрастали. Кроме того, вслед за повышением ввода гидрата окиси алюминия возрастала опасность развития местной воспалительной реакции из-за раздражения тканей.
Приведено пять примеров (1-5) зависимости эффективности вакцины против эшерихиоза телят и поросят от соотношения заявленных компонентов из расчета на 100 мл вакцины и два примера (6, 7) демонстрирующие эффективность использования заявляемого изобретения.
Для примеров 1-5 использовали эпизоотические штаммы Escherichia coli, обладающие генами термолабильного, термостабильного и шигаподоб-ного токсинов, проводили их культивирование на питательном бульоне при температуре 37°С в течение 6-7 дней с ежедневным двукратным перемешиванием, затем их инактивировали формалином до его конечной концентрации 0,4% в течение 14 суток с ежедневным двукратным перемешиванием, после чего отбирали и смешивали культуры в равных соотношениях, отделяли бактериальную массу с помощью стерилизующей фильтрации, для получения бесклеточной культуральной среды, в которую поочередно с последующим перемешиванием вносили адъюванты со следующими объемными количествами и процентным соотношением:
Пример 1 - при следующем соотношении компонентов, масс. %:
При данном соотношении компонентов вакцина обладает слабой протективной активностью и защищает от эшерихиозной инфекции, обусловленной патогенными Escherichia coli телят в 75%, а поросят в 72% случаев.
Пример 2. При следующем соотношении компонентов, масс. %:
При данном соотношении компонентов вакцина защищает от эшерихиозной инфекции, обусловленной патогенными Escherichia coli, в 86%, а поросят в 82%) случаев.
Пример 3. При следующем соотношении компонентов, масс. %:
При данном соотношении компонентов вакцина защищает от эшерихиозной инфекции, обусловленной патогенными Escherichia coli, в 92%, а поросят в 87%о случаев.
Пример 4. При следующем соотношении компонентов, масс. %:
При данном соотношении компонентов вакцина защищает от эшерихиозной инфекции, обусловленной патогенными Escherichia coli, в 94%, а поросят в 90%) случаев.
Пример 5. При следующем соотношении компонентов, масс. %:
При данном соотношении компонентов вакцина защищает от эшерихиозной инфекции, обусловленной патогенными Escherichia coli, в 84%, а поросят в 80% случаев. На месте введения у отдельных животных, особенно из числа поросят развились плотные болезненные припухлости и повышение температуры тела.
Вакцину против эшерихиоза животных производят следующим образом.
Первоначальные этапы получения эшерихиозной вакцины осуществляли по патенту РФ на изобретение №2432174 от 27.10.2011, МПК A61L 39/108, C12N 1/20, А61Р 1/00. Предварительно из эпизоотических штаммов Escherichia coli отобрали штаммы, обладающие генами термолабильного, термостабильного и шигаподобного токсинов. Для этого использовали тест-системы «АмплиСенс E. coli-tox» (Центральный научно-исследовательский институт эпидемиологии МЗ РФ, г. Москва). Подтверждение токсинообразования на искусственной питательной среде осуществляли с помощью биотеста на инфузориях-стилонихиях (патент РФ на изобретение 2262529 от 20.10.2005, МПК C12N 1/10, C12Q 1/10). По известному патенту, для испытания по выживаемости инфузорий использовали культуру кишечной палочки, выращенную на бульоне Хоттингера со сроком инкубации 1-3 суток, затем среду с инфузориями смешивали с бульонной культурой кишечной палочки в соотношении 3:1. При наличии в культуральной среде экзотоксинов, количество погибших инфузорий должно быть не менее 70-80%, в то время как количество погибших инфузорий в контрольной пробе, не содержащей токсин, не должно превышать 5%. Отобранные штаммы по отдельности засевали в пробирки с 10 мл питательного бульона для накопления токсинов кишечной палочки, в состав которой входят кислотный гидролизат крови (9-11%), аутолизат пекарских дрожжей (9-11%), пептон (0,9-1,1%)), натрия хлорид (0,4-0,6%), двузамещенный фосфорнокислый натрий (0,05-0,15%)) и калия хлорид (0,01-0,03%) (патент РФ на изобретение 2342425 от 27.12.2008, МПК C12N 1/20, C12Q 1/04). Затем их помещали в термостат и культивировали при 37°С в течение 6-8 ч до появления легкой мути, свидетельствующей о росте микроорганизмов. Далее полученные культуры переносили в колбы с 200-300 мл аналогичного питательного бульона и инкубировали при 37°С в течение: продуцирующие термолабильный и термостабильный - 6 суток, а продуцирующие шигаподобный токсин - 7 суток. Ежедневно 2 раза в сутки колбы встряхивали. Перед окончанием инкубирования из каждой колбы отобрали по 10 мл культуральной жидкости, центрифугировали при 10 тыс. об/мин в течение 30 мин и определяли методом биотестирования на инфузориях наличия токсинов. При наличии токсинов в оставшиеся культуры добавили формалин до концентрации 0,3-0,4%). Инактивацию культур проводили в течение 14 суток при температуре 37°С с ежедневным двукратным перемешиванием. После завершения инактивации равные объемы культур объединяли, получив, таким образом, комплексный препарат, содержащий 3 вида антигенов. С помощью стерилизующей фильтрации отделили микробную массу от среды культивирования, получая, таким образом, бесклеточную культуральную среду Escherichia coli (эшерихиозный антигенный токсоид-ный компонент). Далее в бесклеточную культуральную среду Escherichia coli: вносили адъюванты: 2%-ную суспензию AL(ОН)3 и масляный адъювант, состоящий из эмульгатора (биологически инертное кремнийорганическое соединение цетил-ПЭГ/ППГ-10/1 - диметикон) - 1,5% и масляной основы -вакцинное масло "М" по ТУ 381011224 - 98,5% (патент РФ №2510845)) при следующем соотношении компонентов, об %:
Подтверждение эффективности использования вакцины для профилактики эшерихиоза у телят и поросят приведены в опытах 1 и 2.
Использование вакцины позволяет обеспечить защиту телят и поросят от эшерихиозной инфекции продолжительностью не менее 6 месяцев (срок наблюдения).
Для доказательства эффективности предлагаемой вакцины, были проведены исследования на белых крысах, телятах и поросятах. Удовлетворительный результат был получен за счет оптимизации ввода растворов гидрата окиси алюминия и масляного адъюванта, что демонстрируется следующими опытами.
Опыт 1 - представлены результаты исследований проведенных на белых крысах.
Было сформировано 4 группы белых крыс по 6 гол в каждой, которым внутримышечно однократно инъецировали по 0,15 мл препарата, в первой группе использовали эшерихиозную вакцину (ЭВ) без адъюванта, во второй - эшерихиозную вакцину с гидратом окиси алюминия (ЭВ+ГОА), в третьей - эшерихиозную вакцину с масляным адъювантом (ЭВ+МА), в четверной -эшерихиозную вакцину с гидратом окиси алюминия и масляным адъювантом (ЭВ+ГОА+МА). Спустя 7, 14, 28, 56, 90 и 120 дней в реакции непрямой ге-магглютинации определяли титр антител к токсинам Е. coli результаты опыта отражены в таблице 1.
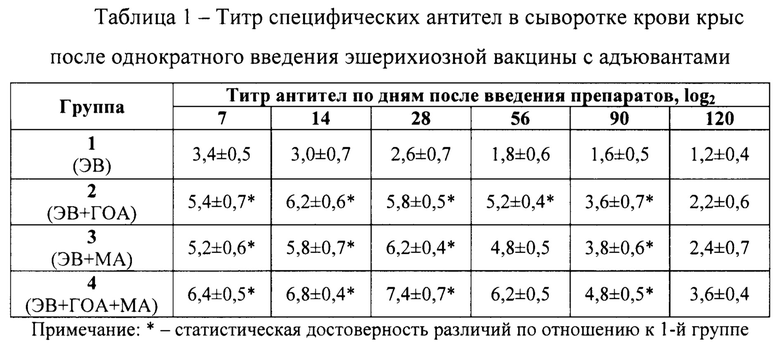
Из данных таблицы видно, что у животных всех групп после ввода им вакцины в течение 7 дней вырабатываются антитела. Однако, в группах 2 и 3 где он вводился с адъювантами, уровень антител был в 1,6 раза выше, чем у животных, которым вакцина вводилась без гидрата окиси алюминия и масляного адъюванта, а у животных группы 4 уровень антител был в 1,8 раза более высоким. В последующие дни у животных 1 группы уровень антител снижался, а вот у животных из опытных групп он повышался, во 2-й - до 14 дня, 3-й и 4-й группе - до 28 дня, превысив показатели 1 группы в 2,1, 2,4 и 2,8 раза соответственно. На 56 день исследования титр антител в опытных группах оставался по-прежнему высоким, максимальное значение регистрировали в группе 4 - 6,2±0,5, что в 3,4 раза превышало значение в 1 группе, и 1,2-1,3 раза значений опытных групп 2 и 3. В последующем во всех группах установили постепенное снижение антител к 120 дню до значения 1,2±0,7, 2,2±0,6, 2,4±0,7 и 3,6±0,4 log2 соответственно. У животных 4 группы уровень антитоксических антител оставался самым высоким даже спустя 120 дней после иммунизации и был достаточным для защитного действия от токсинов Е. coli.
Опыт 2 - представлены результаты исследований проведенных на телятах и поросятах.
Для проведения исследований вакцину прививали стельным коровам и нетелям дважды подкожно. Первый раз за 45, а второй раз за 15 дней до отела в дозе 10 мл. Телят также прививали дважды, первый раз в возрасте 13-15 дней, а второй через 19-21 день в дозе 2 мл соответственно.
Супоросным свиноматкам вакцину вводили внутримышечно дважды, первый раз за 40 дней, а второй раз за 15 дней до опороса в дозе 5 мл; поросят прививали первый раз в возрасте 10-12 дней в дозе 0,25 мл, а второй за 5 дней до отъема поросят от свиноматки в дозе 0,5 мл.
Пример конкретного использования вакцины для профилактики эшерихиоза у телят и поросят.
Использование заявляемой вакцины для телят
В хозяйстве Краснодарского края, неблагополучном по эшерихиозу телят, провели производственное испытание заявляемой вакцины. По данным ветеринарной лаборатории диарею у молодняка крупного рогатого скота в данном хозяйстве вызывают патогенные штаммы кишечной палочки. Эффективность вакцины, изготовленной по заявляемому способу, сравнивали с эффективностью прототипа, для этого было сформировано 3 группы стельных коров по 25 голов в каждой.
Первую группу коров иммунизировали заявляемой вакциной первый раз за 45 дней, второй раз за 15 дней до отела в дозе 10 мл. Полученных от этих коров телят также иммунизировали заявляемой вакциной первый раз в возрасте 13-15 дней, а второй через 19-21 день в дозе 2 мл. Вакцину вводили подкожно в область верхней трети шеи.
Вторую группу коров и полученных от них телят иммунизировали эшерихиозной вакциной с гидратом окиси алюминия по схеме и в дозах аналогичных в первой группе.
Третью группу коров и полученных от них телят иммунизировали эшерихиозной вакциной с масляным адъювантом по схеме и в дозах аналогичных в первой группе.
Четвертую группу коров и полученных от них телят иммунизировали эшерихиозной вакциной без адъювантов по схеме и в дозах аналогичных в первой группе.
Пятая группа коров была контрольной, они и полученные от них телята не иммунизировались.
Использование заявляемой вакцины для поросят
Для обоснования эффективности использования вакцины для профилактики эшерихиоза у поросят, в хозяйстве длительно неблагополучном по эшерихиозу были сформированы 5 групп супоросных свиноматок по 5 животных в каждой.
В первой группе свиноматок и полученных от них поросят иммунизировали предлагаемой вакциной (ЭВ+ГОА+МА). Свиноматок иммунизировали первый раз за 40 дней до опороса в дозе 5 мл, второй раз - за 15 дней в дозе 5 мл внутримышечно в область основания ушной раковины. Поросят иммунизировали дважды первый раз в возрасте 10-12 дней в дозе 0,25 мл, а второй за 5 дней до отъема поросят от свиноматки в дозе 0,5 мл внутримышечно в области внутренней поверхности бедра.
Вторую группу свиноматок и полученных от них поросят иммунизировали эшерихиозной вакциной с гидратом окиси алюминия (ЭВ+ГОА) по схеме и в дозах аналогичных в первой группе.
Третью группу свиноматок и полученных от них поросят иммунизировали эшерихиозной вакциной с масляным адъювантом (ЭВ+МА) по схеме и в дозах аналогичных в первой группе.
Четвертую группу свиноматок и полученных от них поросят иммунизировали эшерихиозной вакциной без адъювантов (ЭВ) по схеме и в дозах аналогичных в первой группе.
Пятая группа свиноматок была контрольной, они и полученные от них поросята не иммунизировались.
Результаты исследований эффективности заявляемой вакцины для телят
Эффективность вакцин оценивали по достижении телятами 3-месячного возраста и перевода их другой корпус на групповое содержание. Критериями оценки служили показатели заболеваемости и летальности.
Результаты опыта отражены в таблице 2, из материалов которой, видно, что в первой группе эшерихиозная инфекция была зарегистрирована у 3 телят, при этом диарею у них удалось купировать в течение 3 дней, а на 5 день телята полностью выздоровели. Таким образом, профилактическая эффективность заявляемой вакцины составила 88%, сохранность 100%.
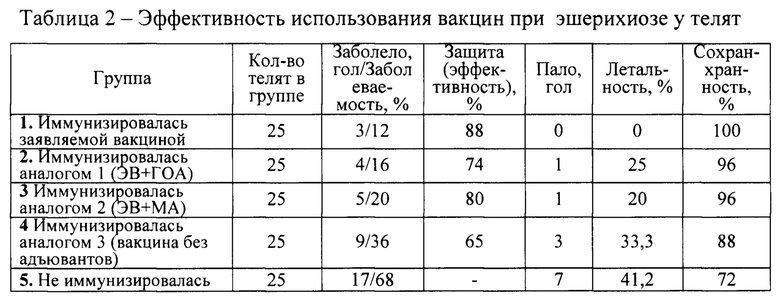
Во 2-ой группе эшерихиозная инфекция была зарегистрирована у 4 телят, причем у одного теленка она протекала очень тяжело и закончилась гибелью животного. Профилактическая эффективность аналога составила 74%, сохранность 96%.
В третьей группе эшерихиозная инфекция была зарегистрирована у 5 телят, у 1 теленка она протекала очень тяжело и закончилась гибелью животных. Профилактическая эффективность аналога составила 80%, сохранность 96%.
В четвертой группе эшерихиозная инфекция была зарегистрирована у 9 телят, из них у троих телят она протекала очень тяжело и закончилась гибелью животных. Профилактическая эффективность прототипа составила 65%, сохранность 88%.
В контрольной группе заболеваемость телят острой кишечной инфекцией составила 68%, а сохранность 72%.
Иммуногенные свойства эшерихиозной вакцины изучали у телят, полученных от вакцинированных стельных коров. Сыворотку крови для определения наличия антитоксических антител в реакции диффузной преципитации отбирали через 7, 14, 28 и 56 дней после последней их вакцинации.
Влияние применения вакцин на титр антител у телят представлены в таблице 3.
Из материалов таблицы 3 видно, что иммунизация коров и телят заявляемым способом обеспечивает более напряженный и продолжительный специфический иммунитет против эшерихиозной инфекции.
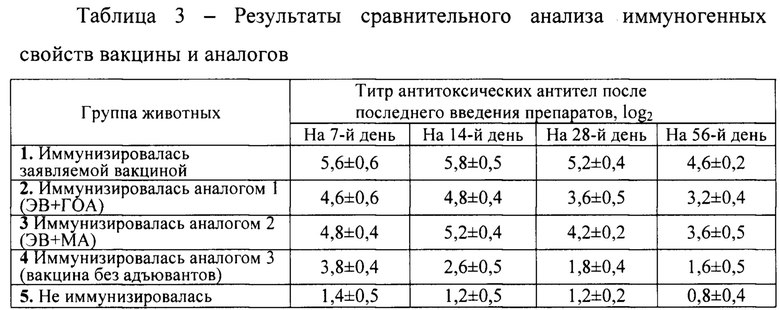
Об этом свидетельствуют количество антител к токсинам кишечной палочки у телят, которых у животных первой группы в 1,1-1,8 раз больше, чем у животных из второй и третьей группы, и 1,5-7,3 раза больше, чем у животных четвертой и пятой групп.
Результаты исследований эффективности заявляемой вакцины для поросят
За поросятами в течение 90 дней вели клиническое наблюдение, учитывали количество заболевших и павших животных. Результаты проведенного исследования представлены в таблице 4.
Из материалов таблицы 4 видно, что в 1-й группе от 5 свиноматок было 5 получено 55 поросят, из которых заболело 8 голов и пало 2. Заболеваемость по группе составила 14,5%, смертность 3,6%. Следовательно, профилактическая эффективность заявляемого способа составила 85,5% при сохранности поросят в группе 96,4%.
Во 2-й группе, где свиноматки иммунизировались вакциной с гидратом окиси алюминия, родилось 54 поросенка, из которых 12 заболело и 5 пало. Заболеваемость по этой группе составила 22,2%, смертность 9,2%, профилактическая эффективность 77,8%), при сохранности 90,8%.
В 3-й группе, где свиноматки иммунизировались вакциной с масляным адъювантом, было получено 53 поросенка, из них 11 заболело, 4 пало. Заболеваемость составила 20,7%, смертность 7,5%, профилактическая эффективность 79,3%), а сохранность 92,5%.
В четвертой группе, где свиноматки вакцинировались вакциной без адъювантов, родилось 55 поросят, из них 19 заболело, 8 пало. Заболеваемость составила 34,5%, смертность 14,5%, профилактическая эффективность 65,5%), а сохранность 85,5%).
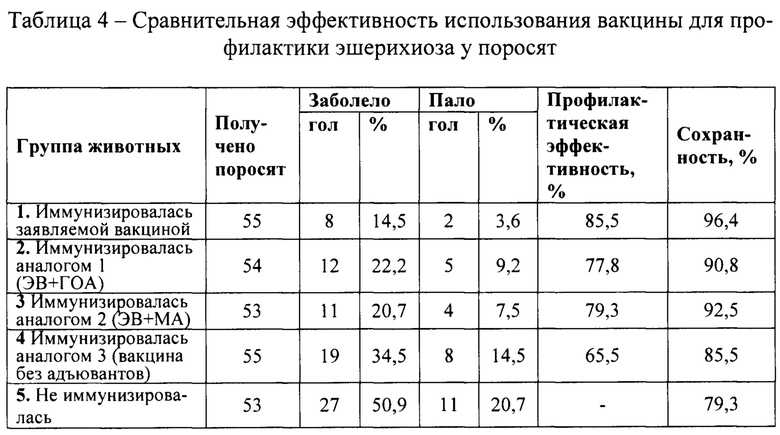
В 5-й группе было получено 53 поросенка, из них 27 заболело, 11 пало. Заболеваемость составила 50,9%, смертность 20,7%, сохранность 79,3%.
Следовательно, применение вакцины против эшерихиоза, позволило более эффективно профилактировать заболевание поросят с эшерихиозной инфекцией. При этом заболеваемость снизилась по сравнению с аналогом на 7,7%, аналогом 2 на 6,2%, аналогом 3 на 20%, а в сравнении с группой (контроль) на 36,4%, при этом падеж сократился в 1,4-5,5 раза, что свидетельствует о высокой эффективности заявляемой вакцины.
Иммуногенные свойства эшерихиозной вакцины изучали у поросят, полученных от вакцинированных супоросных свиноматок. Сыворотку крови для определения наличия антитоксических антител в реакции диффузной преципитации отбирали через 7, 14, 28 и 56 дней после последней их вакцинации.
Влияние применения вакцин на титр антител у поросят представлены в таблице 5.
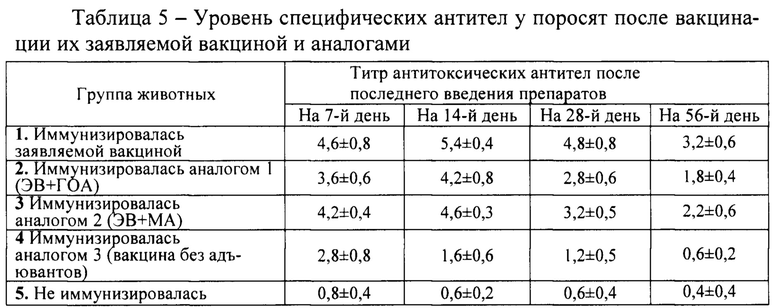
Из материалов таблицы 5 видно, что иммунизация свиноматок и поросят заявляемым способом обеспечивает более напряженный и продолжительный специфический иммунитет против эшерихиозной инфекции. Об этом свидетельствуют количество антител к токсинам кишечной палочки у поросят, которых у животных первой группы в 1,2-9 раз больше, чем у животных из остальных опытных групп.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гидроокись алюминиевой масляной вакцины против эшерихиоза телят и поросят | 2022 |
|
RU2813752C1 |
| Вакцина против эшерихиоза телят и поросят | 2021 |
|
RU2764600C1 |
| Способ профилактики эшерихиоза у поросят | 2021 |
|
RU2766549C1 |
| Способ профилактики эшерихиоза у поросят | 2022 |
|
RU2814593C1 |
| Способ профилактики эшерихиоза у телят | 2021 |
|
RU2766249C1 |
| Способ профилактики эшерихиоза у телят | 2022 |
|
RU2813771C1 |
| Способ получения вакцины ассоциированной против колибактериоза, стрептококкоза и энтерококковой инфекции телят и поросят | 2017 |
|
RU2650628C1 |
| Способ профилактики острых кишечных заболеваний у поросят | 2017 |
|
RU2649831C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭШЕРИХИОЗНОГО АНАТОКСИНА | 2010 |
|
RU2432174C1 |
| Способ профилактики острых кишечных заболеваний у телят | 2017 |
|
RU2650604C1 |
Изобретение относится к биотехнологии. Предложена вакцина против эшерихиоза телят и поросят, включающая бесклеточную культуральную среду, содержащую инактивированные термолабильные, термостабильные и шигаподобные токсины Escherichia coli, полученные при смешивании в равных соотношениях эпизоотических штаммов Escherichia coli, обладающих генами термолабильного, термостабильного и шигаподобного токсинов, инактивированных формалином до его конечной концентрации 0,4%, с последующим отделением бактериальной массы с помощью стерилизующей фильтрации и адъюванты, при этом в качестве адъювантов содержит 2%-ную суспензию Al(ОН)3 и масляный адъювант, состоящий из эмульгатора, в качестве которого использовано биологически инертное кремнийорганическое соединение цетил-ПЭГ/ППГ-10/1-диметикон в количестве 1,5% и масляной основы - вакцинного масла «М» - 98,5%, которые внесены в бесклеточную культуральную среду поочередно с последующим перемешиванием, при следующем соотношении компонентов, мас.%: 2%-ная суспензия Al(OH)3 19-21; масляный адъювант 49-51; бесклеточная культуральная среда, содержащая инактивированные термолабильные, термостабильные и шигаподобные токсины Escherichia coli до 100. Изобретение обеспечивает расширение арсенала вакцинных препаратов для профилактики эшерихиоза у животных. 5 табл., 5 пр.
Вакцина против эшерихиоза телят и поросят, включающая бесклеточную культуральную среду, содержащую инактивированные термолабильные, термостабильные и шигаподобные токсины Escherichia coli, полученные при смешивании в равных соотношениях эпизоотических штаммов Escherichia coli, обладающих генами термолабильного, термостабильного и шигаподобного токсинов, инактивированных формалином до его конечной концентрации 0,4%, с последующим отделением бактериальной массы с помощью стерилизующей фильтрации и адъюванты, при этом в качестве адъювантов содержит 2%-ную суспензию Al(ОН)3 и масляный адъювант, состоящий из эмульгатора, в качестве которого использовано биологически инертное кремнийорганическое соединение цетил-ПЭГ/ППГ-10/1-диметикон в количестве 1,5% и масляной основы - вакцинного масла «М» - 98,5%, которые внесены в бесклеточную культуральную среду поочередно с последующим перемешиванием, при следующем соотношении компонентов, мас.%:
| Вакцина против эшерихиоза телят и поросят | 2021 |
|
RU2764600C1 |
| Способ получения гидроокись алюминиевой масляной тео-вакцины против кампилобактериоза | 2016 |
|
RU2644654C2 |
| ТИЩЕНКО А.С | |||
| и др | |||
| "Влияние минерального и масляного адъювантов на иммуногенность комплексного эшерихиозного анатоксина"; III Международная научная конференция "Инновационные технологии в сельском хозяйстве", 2017, Казань, с.34-39. | |||
Авторы
Даты
2023-11-07—Публикация
2022-11-17—Подача