Область техники, к которой относится изобретение
Настоящее изобретение относится к инъекционным фармацевтическим композициям с замедленным высвобождением, в частности к инъекционным фармацевтическим композициям с замедленным высвобождением, содержащим производные налтрексона. Настоящее изобретение также относится к способу лечения расстройства, связанного с употреблением опиоидов (OUD), или расстройства, связанного с употреблением алкоголя (AUD, также известного как алкоголизм), путём введения инъекционных фармацевтических композиций с замедленным высвобождением нуждающемуся в этом субъекту.
Уровень техники
Налтрексон, 17-(циклопропилметил)-4,5α-эпокси-3,14-дигидроксиморфинан-6-он, является производным тебаина, который принадлежит к семейству опиоидных алкалоидов. Структура налтрексона представлена ниже формулой I с молекулярной массой 341,40.

Формула I (налтрексон)
Как конкурентный антагонист с высоким сродством к μ-рецептору, налтрексон обладает большей эффективностью при конкуренции с другими полными агонистами, такими как морфин или героин и т.д. Обладая антагонистическим эффектом в два раза большим, чем налоксон, налтрексон показан для лечения расстройства, связанного с употреблением опиоидов, и алкоголизм в нескольких лекарственных формах, например Ревия (таблетка для перорального приема) и Вивитрол (внутримышечная инъекция). Клиническая доза (Cmax) вивитрола составляет 380 мг, что в 3-4 раза превышает ежедневную пероральную дозу налтрексона (т.е. 50 мг) в течение 28 дней. Кроме того, описаны различные продукты налтрексона гидрохлорида, которые включают в себя комбинации налтрексона гидрохлорида и других соединений, например Контрейв (таблетка для перорального приема, 8 мг налтрексона гидрохлорида и 90 мг бупропиона гидрохлорида), Эмбеда (пероральная капсула, с соотношеним 25:1 налтрексона гидрохлорида и сульфата морфина) и Троксика ER (пероральная капсула, 1,2 мг налтрексона гидрохлорида и 10 мг оксикодона гидрохлорида). Эти продукты показаны при ожирении или умеренной или сильной боли. В качестве неселективного опиоидного антагониста без агонистической активности налтрексон используется в комбинации с полным опиоидным агонистом (например, метадоном) или частичным опиоидным агонистом (например, бупренорфином) для снижения злоупотребления опиоидами в ходе курса лечения.
В предыдущих исследованиях были раскрыты различные производные налтрексона. Среди них чаще всего модифицируют 3-гидроксильную группу, образуя сложноэфирные связи. Эти производные сложных эфиров синтезируют и сравнивают с налтрексоном и его гидрохлоридной солью. В 1987 году Hussain et al. опубликовали в журнале J. Pharm. Sci. (1987), 75 (5), 356-358 статью о производных налтрексона на основе 3-алкиловых эфиров, как показано в формуле II ниже, где R представляет собой антранилат, ацетилсалицилат, бензоат или пивалат. Эти производные получают в виде пролекарств в попытке улучшить физико-химические характеристики налтрексона и повысить биодоступность при пероральном введении у собак.
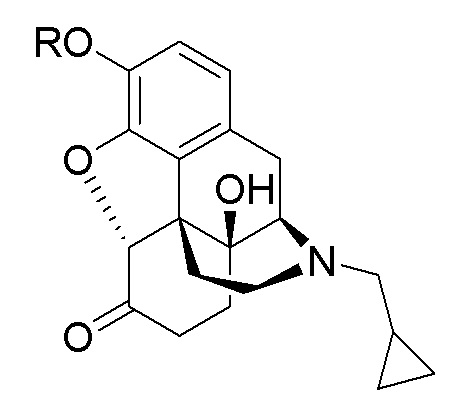
Формула II
Stinchcomb et al. раскрыли в журнале J. Pharm. Sci. (2002), 91 (12), 2571-2578, пролекарство налтрексон-3-алкиловый сложный эфир, имеющее вышеприведенную формулу II, где R представляет собой ацетат, пропаноат, бутаноат, пентаноат, гексаноат или гептаноат. Эти производные налтрексона улучшили физико-химические характеристики налтрексона и увеличили скорость проникновения через кожу человека in vitro. Степень регенерации налтрексона в интактной коже колебалась от 28 до 91%.
Valiveti et al. раскрыли в журнале J. Control. Release (2005), 102 (2), 509-520 in vivo трансдермальную доставку безволосым морским свинкам трех пролекарств на основе 3-O-алкилового сложного эфира налтрексона, показанных в формуле II выше, где R представляет собой ацетат, пропионат или гексаноат. Фармакокинетические параметры налтрексона и пролекарств налтрексона на основе 3-O-алкилового сложного эфира были определены после внутривенного введения и местного применения трансдермальных терапевтических систем (TTS) у морских свинок. Результаты исследований in vivo показали средние стационарные концентрации налтрексона в плазме. Эти концентрации налтрексона в плазме сохранялись в течение 48 часов.
Кроме того, несколько С3-этерифицированных производных налтрексона и их применения были раскрыты в различных патентах. Например, в Европейском патенте No. 2064215 B1, выданном Zynerba Pharmaceuticals Inc., описаны пролекарства налтрексона, представленные формулой II выше, где R представляет собой пивалоат, изовалерат, 2-этилбутират, изобутират, изопропилоксикарбоноат или трет-бутилоксикарбоноат. Налтрексон и его пролекарства в качестве опиоидных антагонистов применяли в комбинации с опиоидными агонистами, такими как бупренорфин или его пролекарства, которые вводили трансдермально для лечения расстройства, связанного с употреблением опиоидов, или алкоголизма.
Производные сложных эфиров налтрексона также раскрыты в патенте США No. 6569449 В1, выданном Исследовательскому фонду Университета Кентукки. В этом патенте США налтрексон был модифицирован сложными эфирами, показанными выше Формулой II, где R представляет собой валерат или гептаноат. Исследование диффузии in vitro показало примерно восьмикратное по сравнению с налтрексоном увеличение кумулятивного количества налтрексона, когда пролекарство, валероил-налтрексон, доставлялось трансдермально через образец кожи. Этот препарат для трансдермальной доставки эффективного количества налтрексона использовали для лечения расстройства, связанного с употреблением опиоидов, и алкоголизма.
Существует множество вариантов реализации замедленного длительного высвобождения налтрексона, показанных для лечения расстройства, связанного с употреблением опиоидов, и алкоголизма. Например, Южный научно-исследовательский институт (Southern Research Institute) разработал композицию микросфер налтрексона для инъекций, которая включает в себя налтрексон в матрице поли-(D,L-лактида) и остаточное количество этилацетата. Эта композиция также была раскрыта в патенте США No.6306425 B1. В этом патенте США людям внутримышечно вводили композиции для клинических исследований, и было показано, что такое введение композиций поддерживает профиль высвобождения налтрексона в течение 31 дня.
Технология получения микросфер была раскрыта в нескольких патентах, выданных Alkermes. Например, в патенте США No.6264987 B1 описаны продукты из микрочастиц с контролируемым высвобождением, содержащие налтрексон и полимеры с выбранной молекулярной массой. Кроме того, в патенте США No.7799345 В2 описана суспензия для инъекций, которая представляет собой смесь налтрексона, микрочастиц и водного носителя для инъекций, в котором носитель для инъекций состоит из воды, агента, повышающего вязкость, смачивающего агента и агента, регулирующего тоничность. Кроме того, в патенте США No.7919499 B2 описана инъекционная суспензия микросфер налтрексона, то есть Vivitrex, в которой используется запатентованная технология Medisorb. Композиция применялась для лечения алкоголизма и вводилась ежемесячно внутримышечно.
Компания BioCorRx Inc. разработала имплантат налтрексона с замедленным высвобождением, BICX102, который использовался для лечения расстройства, связанного с употреблением опиоидов, и алкоголизма. Имплантат может быть хирургическим путём внедрён в плечо пациента, обеспечивая 3-х и 6-ти месячные профили высвобождения. Кроме того, BioCorRx Inc. также разработала налтрексон для инъекций, BICX101. Этот препарат представляет собой суспензию для внутримышечных или подкожных инъекций, в которой используется запатентованная технология микродоставки TheraKine, поддерживающая терапевтические уровни в плазме крови до 3 месяцев. Эта технология также была раскрыта в публикации патента США No.2017/0065579 A1.
Akala et al. раскрыли в публикации в журнале Drug Dev. Ind. Pharm. (2011), 37 (6), 673-684 нагруженные налтрексоном микросферы из поли-(D,L-лактида-когликолида). Исследования доступности in vitro показали, что препарат способен к замедленному высвобождению в течение периода времени от 30 до 150 дней. Такие системы доставки лекарств будут полезны больным алкоголизмом.
Liu et al. раскрыли в публикации в журнале Drug Dev. Ind. Pharm. (2006), 32 (1), 85-94, полилактидные микросферы с налтрексоном, которые подкожно вводили крысам. Уровни в плазме крови крыс показали, что концентрация налтрексона постоянно превышала 2 нг/мл в течение 28 дней. Биоразлагаемые депо-системы могут обеспечить долгосрочное лечение опиоидной зависимости.
Препараты с замедленным высвобождением налтрексона были получены для лечения в соответствующей области техники. Однако у этих препаратов все ещё существуют недостатки, такие как сложные процессы производста, недоступная процедура введения, низкая загрузка лекарственного средства и колебания профиля высвобождения. Эффективные уровни концентрации вивитрола в плазме крови в клиническом исследовании были ограничены одним месяцем. Таким образом, настоящее изобретение относится к композициям налтрексона, содержащим производные 3-ацил-налтрексона, с различной продолжительностью терапевтического действия от одной недели до нескольких месяцев для пациентов, нуждающихся в различных терапевтических схемах лечения. Например, настоящее изобретение относится к композициям налтрексона, имеющим длительное время действия после одной однократной инъекции, для лечения расстройства, связанного с употреблением опиоидов, или алкоголизма.
Сущность изобретения
Настоящее изобретение относится к инъекционной фармацевтической композиции с замедленным высвобождением, содержащей производное 3-ацил-налтрексона или его фармацевтически приемлемую соль и биосовместимый растворитель.
В одном варианте осуществления настоящего изобретения инъекционная фармацевтическая композиция с замедленным высвобождением дополнительно содержит биосовместимый полимерный материал.
В одном варианте осуществления настоящего изобретения фармацевтически приемлемая соль 3-ацилналтрексона может быть в форме соли HCl, формиата и ацетата, но не ограничивается этим.
Инъекционная фармацевтическая композиция с замедленным высвобождением настоящего изобретения обеспечивает замедленное высвобождение пролекарства 3-ацилнатрексона в течение периода времени, по меньшей мере, от одной недели до нескольких месяцев. Следовательно, инъекционные фармацевтические композиции с замедленным высвобождением настоящего изобретения обеспечивают доступную процедуру введения, профиль замедленного высвобождения и длительное терапевтическое действие.
Настоящее изобретение также относится к способу лечения расстройства, связанного с употреблением опиоидов, включающему в себя введение инъекционной фармацевтической композиции с замедленным высвобождением нуждающемуся в этом субъекту.
Настоящее изобретение также относится к способу лечения алкоголизма, включающему в себя введение инъекционной фармацевтической композиции с замедленным высвобождением нуждающемуся в этом субъекту.
Другие аспекты настоящего изобретения станут очевидными из прилагаемых чертежей и следующего подробного описания.
Краткое описание чертежей
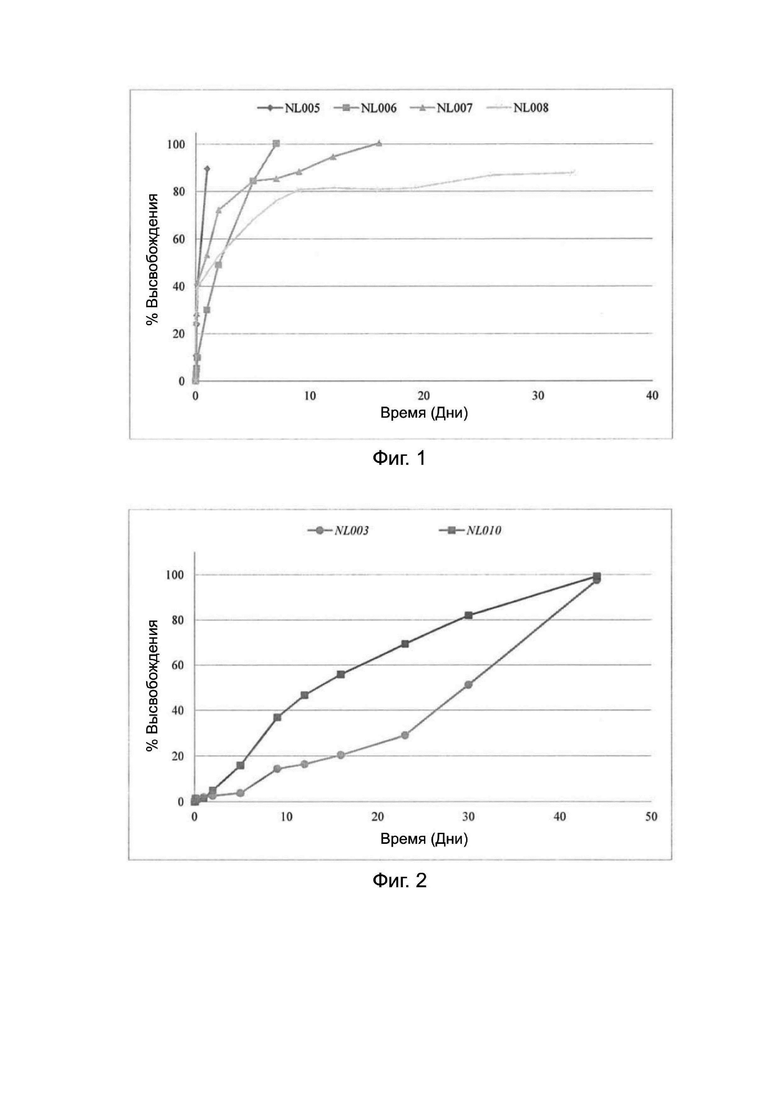
На фиг. 1 показаны in vitro профили растворения инъекционных фармацевтических композиций с замедленным высвобождением, содержащих различные производные налтрексона, в соответствии с Примером 2 настоящего изобретения.
На фиг. 2 показаны in vitro профили растворения инъекционных фармацевтических композиций с замедленным высвобождением, содержащих налтрексона гексаноат, растворенных в различных органических растворителях, в соответствии с Примером 2 настоящего изобретения.
На фиг. 3 показаны средние уровни налтрексона в плазме крови после подкожной инъекции NL023 в дозе 10,3 мг налтрексона на килограмм мини-свиньям в соответствии с вариантами осуществления настоящего изобретения.
На фиг. 4 показаны средние уровни налтрексона в плазме крови после подкожной инъекции NL024 в дозе 10,3 мг налтрексона на килограмм мини-свиньям в соответствии с вариантами осуществления настоящего изобретения.
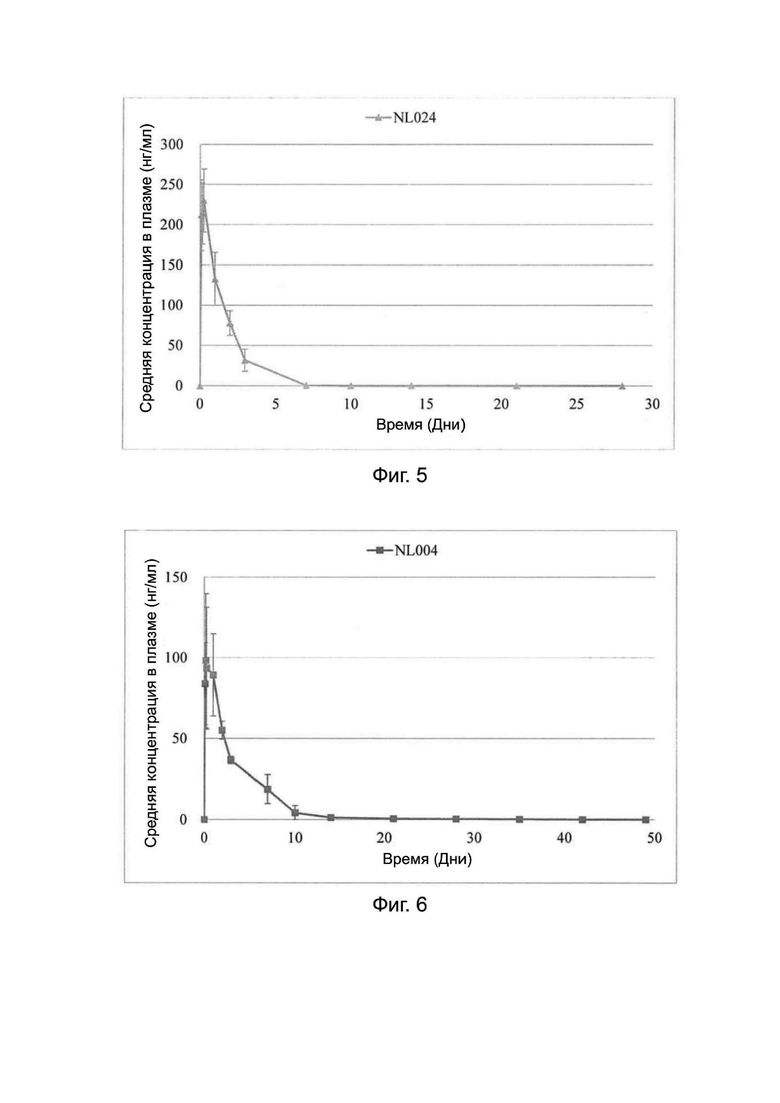
На фиг. 5 показаны средние уровни налтрексона в плазме крови после подкожной инъекции NL024 в дозе 60 мг налтрексона на килограмм крысам в соответствии с вариантами осуществления настоящего изобретения.
На фиг. 6 показаны средние уровни налтрексона в плазме крови после подкожной инъекции NL004 в дозе 120 мг налтрексона на килограмм крысам в соответствии с вариантами осуществления настоящего изобретения.
На фиг. 7 показаны средние профили высвобождения налтрексона после подкожной инъекции NL023 и NL024 в дозе 10,3 мг налтрексона на килограмм мини-свиньям в соответствии с вариантами осуществления настоящего изобретения.
На фиг. 8 показаны профили среднего высвобождения налтрексона после подкожной инъекции NL004 в дозе 120 мг налтрексона на килограмм и NL024 в дозе 60 мг налтрексона на килограмм крысам в соответствии с вариантами осуществления настоящего изобретения.
Подробное описание изобретения
В одном варианте осуществления настоящее изобретение относится к композициям производных налтрексона, которые имеют более длительное терапевтическое действие после введения одной разовой дозы для лечения. Лечение включает в себя расстройство, связанное с употреблением опиоидов (OUD), и расстройство, связанное с употреблением алкоголя (AUD, также известное как алкоголизм).
В одном варианте осуществления настоящего изобретения инъекционная фармацевтическая композиция с замедленным высвобождением содержит 3-ацил-налтрексон или его фармацевтически приемлемую соль и биосовместимый растворитель. В одном варианте осуществления настоящего изобретения инъекционная фармацевтическая композиция с замедленным высвобождением содержит 3-ацилналтрексон или его фармацевтически приемлемую соль в нижнем пределе 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50% по массе, и инъекционная фармацевтическая композиция с замедленным высвобождением содержит 3-ацил-налтрексон или его фармацевтически приемлемую соль в верхнем пределе 99%, 95%, 90%, 85%, 80%, 75%, 70%, 65%, 60%, 55% или 50% по массе в расчете на общую массу инъекционной фармацевтической композиции с замедленным высвобождением. Например, 3-ацилналтрексон или его фармацевтически приемлемая соль присутствует в количестве от 1% до 99% по массе, от 1% до 90% по массе, от 5% до 90% по массе, от 5% до 80% по массе, от 10% до 70% по массе или от 10% до 60% по массе в расчете на общую массу инъекционной фармацевтической композиции с замедленным высвобождением.
В другом варианте осуществления настоящего изобретения инъекционная фармацевтическая композиция с замедленным высвобождением представляет собой инъекционную фармацевтическую композицию с замедленным высвобождением на основе полимера, содержащую биосовместимый полимерный материал. В одном варианте осуществления настоящего изобретения инъекционная фармацевтическая композиция с замедленным высвобождением содержит биосовместимый полимерный материал в нижнем пределе 1%, 2%, 3%, 4%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50% по массе, и инъекционная фармацевтическая композиция с замедленным высвобождением содержит биосовместимый полимерный материал в верхнем пределе 95%, 90%, 85%, 80%, 75%, 70%, 65%, 60%, 55%, 50%, 45%, 40%, 35%, 30%, 25%, 20%, 15%, 10%, 9%, 8%, 7%, 6% или 5% по массе в расчете на общую массу инъекционной фармацевтической композиции с замедленным высвобождением. Например, биосовместимый полимерный материал присутствует в количестве от 1% до 10% по массе, от 1% до 8% по массе, от 3% до 8% по массе или от 5% до 7% по массе, в расчете на общую массу инъекционной фармацевтической композиции с замедленным высвобождением.
В одном варианте осуществления настоящего изобретения 3-ацилналтрексон или его фармацевтически приемлемая соль содержит сложноэфирную группу, образованную между 3-гидрокси (фенольной) группой налтрексона и реагентом алкилкарбонилирования или арилкарбонилирования (ацилирования).
В одном варианте осуществления настоящего изобретения реагент алкилкарбонилирования или арилкарбонилирования (т.е. ацилирования) имеет формулу R-CO-X, где R представляет собой алкильный или арильный остаток, который может быть ацилхлоридом, ацилангидридом или ацилактивным сложным эфиром. Алкильная часть алкилкарбонильной группы может быть алкильной группой с прямой или разветвленной цепью. В одном варианте осуществления изобретения алкильная часть может содержать подходящее количество атомов углерода, например от 1 до 20 (C1-C20), от 1 до 12 (C1-C12), от 1 до 10 (C1-C10), от 1 до 6 (C1-C6), от 1 до 5 (C1-C5), от 1 до 4 (C1-C4) или от 1 до 2 (C1-C2). Примеры алкилкарбонильных (ацильных) групп включают в себя без ограничений ацетил, бутирил, валерил, гексаноил, деканоил или лауроил. Арильная часть арилкарбонильной группы включает в себя арильную группу или арилалкильную группу, и алкильная часть является такой, как указано выше. Арильная часть арилкарбонильной группы может содержать C6-C18 ароматическое кольцо, такое как фенильная группа или нафтильная группа. В другом варианте осуществления настоящего изобретения фармацевтически приемлемая соль 3-ацилналтрексона может представлять собой соль HCl, формиат, ацетат, соли памоевой кислоты, лимонной кислоты, винной кислоты и малеиновой кислоты, но не ограничивается этим.
В одном варианте осуществления настоящего изобретения 3-ацилналтрексон может быть синтезирован обычными методами. Налтрексон или его соль можно приобрести у нескольких коммерческих источников, таких как Sigma-Aldrich. Чтобы получить производное налтрексона, проводят реакцию налтрексона (или его соли) с ацилхлоридом в присутствии ненуклеофильного основания (например, триэтиламина) с образованием сложноэфирной связи. Продукт (3-ацилналтрексон или 3-алкилкарбонилналтрексон) можно очистить обычными методами, такими как колоночная хроматография.
В одном варианте осуществления настоящего изобретения 3-ацилналтрексон, включая 3-алкилкарбонилналтрексон или 3-арилкарбонилналтрексон, или его соль, можно использовать в качестве пролекарства, которое затем превращается в исходное соединение, налтрексон, т.е. фармацевтически активное соединение.
В одном варианте осуществления настоящего изобретения биосовместимый растворитель может представлять собой органический растворитель, такой как N-метил-2-пирролидон (NMP), этилацетат, этанол (EtOH), бутанол, 2-бутанол, изопропанол (IPA), изобутанол, глицерин, бензилбензоат (BnBzO), диметилсульфоксид (DMSO), пропиленгликоль (PG), диметилгликоль, N,N-диметилацетамид (DMAc), бензиловый спирт, сложный эфир, простой эфир, амид, карбонат, лактам, сульфонил или их комбинацию.
В одном варианте осуществления настоящего изобретения в качестве вспомогательных веществ используются биосовместимые полимерные материалы, такие как поли-(D,L-лактид) (PLA) и поли-(D,L-лактид/гликолид) (PLGA). В одном варианте осуществления настоящего изобретения PLA и PLGA находятся в молярном соотношении 75:25. В другом варианте осуществления настоящего изобретения PLA и PLGA находятся в молярном соотношении 50:50.
В одном варианте осуществления настоящего изобретения инъекционная фармацевтическая композиция с замедленным высвобождением предназначена для подкожной, внутримышечной или внутрикожной инъекции.
Варианты осуществления настоящего изобретения будут дополнительно проиллюстрированы следующими примерами. Однако специалисту в данной области техники должно быть понятно, что эти примеры предоставлены только для иллюстрации и что другие модификации и вариации возможны, при условии, что они не выходят за рамки объема настоящего изобретения.
Пример 1: Получение производных налтрексона
Производные налтрексона синтезировали с использованием традиционных методов, как описано ниже. Налтрексон HCl смешивали с дихлорметаном в трехгорлой круглодонной колбе с образованием суспензии с последующим помещением на ледяную баню для охлаждения. Затем в трехгорлую круглодонную колбу при перемешивании медленно добавляли триэтиламин с последующим добавлением ацилхлорида, содержащего от 1 до 20 атомов углерода. Реакцию этерификации проводили в атмосфере азота при температуре окружающей среды. Реакционную смесь нейтрализовали насыщенным водным раствором бикарбоната натрия. Органический слой промывали рассолом и затем сушили сульфатом натрия с последующим концентрированием при пониженном давлении. Неочищенное налтрексоновое производное 3-ацилналтрексона очищали колоночной хроматографией на силикагеле.
Пример 2: Получение инъекционных фармацевтических композиций с замедленным высвобождением
Добавляют от 15 до 70 мас.% производного налтрексона в стеклянный флакон и растворяют в одном или комбинации двух или более биосовместимых органических растворителей, таких как N-метил-2-пирролидон (NMP), этилацетат, этанол (EtOH ), бутанол, 2-бутанол, изопропанол (IPA), изобутанол, глицерин, бензилбензоат (BnBzO), диметилсульфоксид (DMSO), пропиленгликоль (PG), диметилгликоль, N,N-диметилацетамид (DMAc) и бензиловый спирт.
В качестве альтернативы, от 15 до 70 мас.% производного налтрексона и биосовместимых полимерных материалов (D,L-лактид) и поли (D,L-лактид/гликолид) в молярном соотношении 75:25 или 50:50 добавляли в стеклянный флакон, а затем растворяли в одном или комбинации двух или более биосовместимых органических растворителей, таких как N-метил-2-пирролидон, этилацетат, этанол, бутанол, 2-бутанол, изопропанол, изобутанол, глицерин, бензилбензоат, диметилсульфоксид, пропиленгликоль, диметилгликоль, N,N-диметилацетамид и бензиловый спирт.
Смесь постоянно перемешивали при температуре окружающей среды или слегка нагревали до растворения всех ингредиентов. Полученные инъекционные фармацевтические композиции с замедленным высвобождением перечислены ниже в Таблице 1.
(мас.%)
(мас.%)
(мас.%)
Пример 3: Испытание in vitro на растворимость инъекционных фармацевтических композиций с замедленным высвобождением
Каждую из композиций NL003, NL005, NL006, NL007, NL008 и NL010, полученных в Примере 2, соответственно оценивали на предмет её профиля растворения in vitro. Каждую из композиций NL005, NL006, NL007 и NL008 смешивали со средой растворения фосфатно-солевым буфером, содержащим 0,1% додецилсульфата натрия и 0,02% азида натрия, в одной пробирке, и каждую из композиций NL003 и NL010 смешивали со средой растворения фосфатно-солевым буфером, содержащим 0,2% додецилсульфата натрия и 0,02% азида натрия в одной пробирке. Каждую из пробирок встряхивали со скоростью 60 об/мин на водяной бане при температуре 37°C. Из каждой из пробирок отбирали 1 мл образца в определенные моменты времени и применяли ВЭЖХ для анализа производных налтрексона и свободного основания налтрексона. В каждую из пробирок снова добавляли 1 мл свежей среды растворения. Профили скоростей растворения композиций NL005, NL006, NL007 и NL008 показаны в Таблице 2 и на фиг. 1, а композиций NL003 и NL010 показаны в Таблице 3 и на фиг. 2. Результаты показали, что композиции NL003, NL006, NL007, NL008 и NL010 могут длительно высвобождать производные налтрексона от одной недели до более чем одного месяца.
Пример 4: Фармакокинетические профили инъекционных фармацевтических композиций с замедленным высвобождением у мини-свиней
Композиции, полученные в Примере 2, вводили подкожно самцам минисвиней породы Lanyu в дозе 10,3 мг налтрексона на килогамм массы тела. Образцы крови отбирали из внешних яремных вен в определенные моменты времени. Образцы плазмы отделяли на центрифуге и хранили в замороженных условиях для последующего анализа. ЖХ-МС/МС использовали для анализа концентраций налтрексона в образцах плазмы крови. Фармакокинетический профиль композиции NL023 показан в Таблице 4 и на фиг. 3. Результаты показали, что композиция NL023 может обеспечивать замедленное высвобождение налтрексона в течение 2 месяцев. Фармакокинетический профиль композиции NL024 показан в Таблице 5 и на фиг. 4. Результаты показали, что композиция NL024 может обеспечивать замедленное высвобождение налтрексона в течение одного месяца.
Пример 5: Фармакокинетические профили инъекционных фармацевтических композиций с замедленным высвобождением у крыс
Композиции, полученные в Примере 2, вводили подкожно самцам крыс линии CD (SD) IGS в дозе 60 и 120 мг налтрексона на килограмм массы тела. Образцы крови отбирали из хвостовых вен в определенные моменты времени. Образцы плазмы крови отделяли на центрифуге и хранили в замороженных условиях для последующего анализа. ЖХ-МС/МС использовали для анализа концентраций налтрексона в образцах плазмы крови. Фармакокинетический профиль композиции NL024 показан в Таблице 6 и на фиг. 5. Фармакокинетический профиль композиции NL004 показан в Таблице 7 и на фиг. 6.
Пример 6: Профили высвобождения in vivo инъекционных фармацевтических композиций с замедленным высвобождением у мини-свиней и крыс
Фармакокинетические данные у мини-свиней и крыс анализировали для площади под кривой в определенный момент времени (area under curve, AUC0-t) и площади под кривой зависимости концентрации в плазме крови от времени с момента 0, экстраполированного до бесконечности (AUC0-∞). Процент высвобождения налтрексона в профиле высвобождения оценивали по отношению AUC0-t к AUC0-∞.

Профили высвобождения in vivo композиции NL023 и NL024 у мини-свиней показаны в Таблице 8 и на фиг. 7. Профили высвобождения in vivo композиции NL004 и NL024 у крыс показаны в Таблице 9 и на фиг. 8. Профили высвобождения у двух разных животных моделях показали, что композиции могут постоянно высвобождать налтрексон в течение различных периодов времени от одной недели до 2 месяцев.
Таким образом, инъекционные композиции с замедленным высвобождением настоящего изобретения могут поддерживать длительное терапевтическое действие и обеспечивать высокую нагрузку лекарственным средством после введения однократной дозы. Система введения подкожной инъекции может быть менее болезненной, чем внутримышечная инъекция, и для нее требуется относительно небольшой объем препарата. Кроме того, профили высвобождения при растворении и фармакокинетические профили у минисвиней этих композиций также доказали, что производные налтрексона могут применяться в качестве пролекарств и превращаться в исходное соединение, налтрексон, для лечения, по меньшей мере, от одной недели до нескольких месяцев.
Хотя настоящее изобретение было описано относительно ограниченного числа вариантов его осуществления, специалисты в данной области техники, пользуясь преимуществом настоящего раскрытия, поймут, что могут быть разработаны другие варианты осуществления изобретения, которые не выходят за пределы раскрытого здесь объема настоящего изобретения. Соответственно, объем настоящего изобретения должен определяться только прилагаемой формулой изобретения.


Предложена инъекционная фармацевтическая композиция с замедленным высвобождением, включающая в себя 3-ацилналтрексон или его фармацевтически приемлемую соль, биосовместимый органический растворитель и, необязательно, биосовместимый полимерный материал. Также предложен способ лечения расстройства, связанного с употреблением опиоидов, или алкоголизма, включающий в себя введение инъекционной фармацевтической композиции с замедленным высвобождением нуждающемуся в этом субъекту. Фармацевтическая композиция обеспечивает профиль замедленного высвобождения после одной однократной инъекции, а уровни налтрексона в плазме крови у мини-свиней могут обеспечивать замедленное высвобождение в течение 2 месяцев. 2 н. и 4 з.п. ф-лы, 6 пр., 9 табл., 8 ил.
1. Инъекционная фармацевтическая композиция с замедленным высвобождением, содержащая 3-ацилналтрексон или его фармацевтически приемлемую соль и биосовместимый органический растворитель, где 3-ацилналтрексон содержит алкилкарбонильную группу или арилкарбонильную группу, и где алкилкарбонильная группа имеет алкильную часть, содержащую прямую или разветвленную цепь, имеющую от 2 до 20 атомов углерода, и где арилкарбонильная группа имеет арильную часть, содержащую ароматическую группу, имеющую от 6 до 18 атомов углерода, и где биосовместимый органический растворитель выбран из группы, состоящей из N-метил-2-пирролидона, N,N-диметилацетамида и их комбинации.
2. Инъекционная фармацевтическая композиция с замедленным высвобождением по п. 1, где 3-ацилналтрексон или его фармацевтически приемлемая соль присутствует в количестве от 1 до 99% по массе в расчете на общую массу инъекционной фармацевтической композиции с замедленным высвобождением.
3. Инъекционная фармацевтическая композиция с замедленным высвобождением по п. 1, дополнительно содержащая биосовместимый полимерный материал, где биосовместимый полимерный материал представляет собой поли-(D,L-лактид) (PLA).
4. Инъекционная фармацевтическая композиция с замедленным высвобождением по п. 3, где биосовместимый полимерный материал присутствует в количестве от 1 до 10% по массе в расчете на общую массу инъекционной фармацевтической композиции с замедленным высвобождением.
5. Способ лечения расстройства, связанного с употреблением опиоидов, или алкоголизма, включающий в себя введение инъекционной фармацевтической композиции с замедленным высвобождением по п. 1 нуждающемуся в этом субъекту, где инъекционная фармацевтическая композиция с замедленным высвобождением обеспечивает профиль замедленного высвобождения в течение по меньшей мере одной недели.
6. Способ по п. 5, отличающийся тем, что инъекционную фармацевтическую композицию с замедленным высвобождением вводят путем подкожной, внутримышечной или внутрикожной инъекции.
| WO 2005107753 A2, 2005.11.17 | |||
| US 6569449 B1, 2003.05.27 | |||
| Emmamuel O | |||
| AKALA et al., Studies on in vitro availability, degradation, and thermal properties of naltrexone-loaded biodegradable microspheres, Drug Dev Ind Pharm., 37(6), 2011, pages 673-684 | |||
| VALIVETI, Satyanarayana et al., In vivo evaluation of 3-O-alkyl ester transdermal prodrugs of |
Авторы
Даты
2023-11-07—Публикация
2019-12-26—Подача