Изобретение относится к медицине, а именно к офтальмохирургии, и может быть использовано в качестве эффективного способа хирургического лечения птеригиума.
Как известно, в южных регионах России частота встречаемости птеригиума может достигать до 11% [Маложен С.А. Птеригиум: этиология, патогенез, лечение / Маложен С.А. [и др.]// Вестник офтальмологии. - 2017. - № 5. - С. 76-83]. В климатических областях с высоким уровнем ультрафиолетового спектра солнечного излучения и сухим ветреным климатом (фактор риска развития птеригиума), заболевание встречается гораздо чаще, достигая 22 %. К другим провоцирующим факторам развития данной патологии относят синдром сухого глаза, особенности профессиональной деятельности (повышенный уровень пыли, работа на открытом воздухе более 4-5 часов в день), а также оперативные вмешательства на глазном яблоке [Павлова О.Н. Методы лечения и профилактики птеригиума. / Павлова О.Н. [и др.]// Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье. - 2019.- №3. - C. 65-73].
Пусковым механизмом в патогенезе птеригиума является частичная гибель стволовых клеток эпителия роговицы с развитием частичной лимбальной недостаточности, что приводит к росту фиброваскулярной ткани по поверхности роговицы [Zaidi, F., Bloom, P. & Corbett, M. Limbal stem cell deficiency: a clinical chameleon. Eye 17, 837-839 (2003)]. Такое локальное рубцевание глазной поверхности лежит в основе изменения кривизны и, как следствие, преломляющих свойств роговицы, что клинически проявляется в развитии астигматизма высоких степеней со снижением остроты зрения до 0,1 и ниже. По мере своего увеличения в размерах и врастания новообразованных сосудов птеригиум становится все более заметным и приводит к косметическому дефекту, резко снижая и без того низкую остроту зрения, а также качество жизни пациентов.
Единственным эффективным методом лечения птеригиума является его удаление различными хирургическими способами. В настоящее время применяются барьерные методы лечения, которые подразумевают удаление птеригиума с замещением дефекта бульбарной конъюнктивы различными тканями. Однако вероятность рецидива достигает в 89% случаев, при этом до 97% рецидивов регистрируются в течение первого года после операции и требуют повторного вмешательства [Ghiasian L. Recurrent Pterygium: A Review. / Ghiasian L. [et al.] // J Curr Ophthalmol. -2022. - №33(4). - P. 367-378].
Таким образом, на сегодняшний день отсутствует эффективный способ хирургического лечения птеригиума, а существующие методики не исключают рецидива его роста в послеоперационном периоде. В этой связи поиск новых способов малотравматичного, простого и надежного хирургического лечения птеригиума остается актуальной проблемой современной офтальмохирургии.
Известен способ лечения птеригиума на основе аутопластики [патент РФ №RU 2 269 988 С2 МПК, опубл. 20.02.2006], который заключается в использовании конъюнктивы нижне - наружного квадранта для замещения дефекта ткани. Техника операции заключается в следующем. Под эпибульбарной анестезией отсепаровывают и иссекают тело птеригиума с прилежащей тканью на 2 мм от основания и по 1 мм в стороны. После отделения головки птеригиума тупым путем очищают роговичный эпителий до здоровых тканей. Из нижне-наружного отдела конъюнктивального свода на 2 мм ниже лимба иссекают донорскую ткань для получения трансплантата. Размер фрагмента рассчитывают с учетом размера дефекта конъюнктивы плюс 1 мм по всему периметру выкраиваемого участка из-за его сокращения в зоне пересадки. Конъюнктиву донорского участка ушивают непрерывным швом. Полученный трансплантат укладывают на ложе и фиксируют к конъюнктиве непрерывным швом 8/0.
Данный способ хирургического лечения позволяет снизить частоту рецидивирования до 33% и сократить сроки реабилитационного периода за счет снижения травматичности хирургического вмешательства [Nuzzi R, Tridico F. How to minimize pterygium recurrence rates: clinical perspectives. Clin Ophthalmol. 2018 Nov 19;2347-2362].
Однако, несмотря на свои преимущества, недостатками предлагаемого способа являются трудоемкость операции, что приводит к увеличению времени оперативного вмешательства. Наличие косметического дефекта и выраженный дискомфорт в послеоперационном периоде за счет немалого объема иссекаемых тканей существенно влияют на уровень комфорта и качество жизни пациентов. Кроме того, взятие аутотрансплантата в нижнем своде ограничено его размерами и не всегда доступно формирование участка необходимых размеров. В области забора трансплантата отмечаются изменение структуры конъюнктивы и потеря ее эластичности по сравнению с нетронутыми участками, что обусловливает склонность к дальнейшему рубцеванию и снижает эффективность проводимой операции [Young AL, Kam KW. Pterygium: Surgical Techniques and Choices. Asia Pac J Ophthalmol (Phila). 2019 Nov-Dec;8(6):422-423].
Использование метода аутоконъюнктивальной трансплантации также ограничено в случаях большой зоны иссекаемых тканей (при широком, мясистом птеригиуме), особенно при хирургическом лечении рецидивов заболевания [Kucukerdonmez, C., Karalezli, A., Akova, Y. et al. Amniotic membrane transplantation using fibrin glue in pterygium surgery: a comparative randomised clinical trial. Eye 24, 558-566 (2010)].
Приведенные недостатки частично устранены в способе хирургического лечения птеригиума с трансплантацией нативной амниотической мембраны и ее фиксацией шовным материалом [Katbaab A, Anvari Ardekani HR, Khoshniyat H, Jahadi Hosseini HR. Amniotic membrane transplantation for primary pterygium surgery. J Ophthalmic Vis Res. 2008 Jan;3(1):23-7].
Данный метод отличается от предыдущего тем, что фрагмент амниотической мембраны, соответствующий размерам подготовленного ложа, размещается в зоне иссеченного птеригиума поверх обнаженной склеры базальной мембраной вверх и фиксируется с помощью швов (викрил 8-0 или нейлон 10-0) к эписклере и окружающей конъюнктиве, выступая в качестве биологического «бандажа» и защищая подлежащие ткани. К основным преимуществам амниопластики относят низкую иммуногенность и отсутствие реакций отторжения, значительное ускорение эпителизации и восстановление морфологии эпителиального покрова, что обеспечивает снижение частоты рецидивов до 26,9 % [Скачков Д.П. Применение биологических свойств амниотической оболочки в хирургическом лечении патологии роговицы / Скачков Д.П. [и др.]// Дальневосточный медицинский журнал. - 2013. - №4. - С. 41-43].
Тем не менее, использование шовного способа фиксации амниотической мембраны имеет свои недостатки, а именно:
1) наложение швов является трудоемкой процедурой и существенно удлиняет время оперативного вмешательства;
2) работа с материалами на микрохирургическом уровне подразумевает высокие навыки и мастерство хирурга;
3) использование шовных материалов шириной 0,06-0,08 мм требует осторожности и аккуратности во избежание разрыва нити;
4) использование амниотической мембраны толщиной около 0,4 мм и ее фиксация с помощью шовного материала связаны с риском ее интраоперационного повреждения;
5) наружные концы нитей вызывают раздражение и усиливают дискомфорт в послеоперационном периоде, что снижает качество жизни пациентов и требует назначения дополнительной (корнеопротекторной) терапии;
6) наружные концы нитей могут травмировать участок амниотической мембраны, особенно при мигательных движениях, и привести к его расслоению или отторжению;
7) избыточное слезотечение, возникающее при ирритации нитями, может привести к преждевременному лизису амниона за счет ферментов слезы при попадании ее под фиксированный швами фрагмент;
8) наложение швов ассоциировано с большим риском послеоперационного инфицирования и образованию гранулем [Mahdy, Reda A.; Wagieh, Mostafa M. (2012). Safety and Efficacy of Fibrin Glue versus Vicryl Sutures in Recurrent Pterygium with Amniotic Membrane Grafting. Ophthalmic Research, 47(1), 23-26].
Наиболее близким к заявленному изобретению является способ, выбранный нами в качестве прототипа и заключающийся в использовании фибринового клея - герметика «Tisseel VH» (Baxter Healthcare Corp, Deerfield, IL) для фиксации фрагмента амниотической мембраны [Kucukerdonmez C. Amniotic membrane transplantation using fibrin glue in pterygium surgery: a comparative randomised clinical trial. / Kucukerdonmez C. [et al.]// Eye. - 2010. -№24(4). - P. 558-566].
Авторы предлагают использование двухкомпонентного фибринового клея - герметика для фиксации амниотической мембраны и описывают следующую технику его приготовления: первый компонент герметика представляет собой концентрат плазмы крови, содержащей человеческий фибриноген (70-110 г), фибронектин (2-9 мг), фактор XIII (10-50 МЕ), плазминоген (40-120 мкг) и раствор бычьего апротинина. Второй компонент приготавливается путем смешивания бычьего тромбина и раствора хлорида кальция. Перед нанесением компонентов для поддержания температурного режима производят нагревание первого компонента и тромбина. Далее тромбин смешивают с раствором хлорида кальция для получения второго компонента.
После иссечения птеригиума и высушивания с помощью губки оголенного участка склеры на глазную поверхность наносят фибриновый клей. Для нанесения клея на поверхность глаза используется двойная инъекционная система «Duploject» (Baxter AG, Вена, Австрия), в которой раствор первого и второго компонента из разных шприцов смешиваются друг с другом непосредственно во время аппликации за счет объединяющей канюли на конце устройства [Panda A, Kumar S, Kumar A, Bansal R, Bhartiya S. Fibrin glue in ophthalmology. Indian J Ophthalmol. 2009 Sep-Oct;57(5):371-9]. После аппликации клея в подготовленное ложе переносили сформированный фрагмент амниотической мембраны, с помощью инструментов убирали излишки клеевой композиции.
К недостаткам данного метода относят:
1) отсутствие зарегистрированного способа хирургического лечения птеригиума с использованием нативной амниотической мембраны и фибринового клея в Российской Федерации;
2) наличие в составе клеевой композиции аллогенного (чужеродного) концентрата (первого компонента), что диктует необходимость тщательного исследования донорского материала на предмет гемоконтактных инфекций;
3) увеличение времени приготовления клеевой композиции и необходимость соблюдения производственных норм при получении компонента клея из донорской плазмы;
4) проявление возможных аллергических реакций на белок апротинин, которые имеет бычье происхождение и, следовательно, считается аллергеном;
5) высокая концентрация фибрина первого компонента определяет пропорционально большую интенсивность процессов рубцевания конъюнктивы, и, соответственно, больший риск развития рецидива птеригиума;
6) высокая концентрация фибрина первого компонента определяет пропорционально большую интенсивность помутнения роговицы в послеоперационном периоде;
7) необходимость поддержания определенной температуры во время приготовления клеевой композиции делает процедуру более энергозатратной и сложной в осуществлении;
8) потребность в использовании специального дорогостоящего оборудования (термо - устройство, система «Duploject» для нанесения компонентов) приводит к снижению уровня доступности данного метода.
В основу настоящего изобретения положена идея создания быстрого, малотравматичного, а главное - эффективного способа лечения птеригиума. Это достигается путем использования биологических свойств нативной амниотической мембраны, а также разработанного и запатентованного [патент РФ №RU 2 704 256 С1 МПК, опубл. 18.02.2019] двухкомпонентного аутофибринового клея (ДАФК) как наиболее простого и надежного способа фиксации тканей.
Решение поставленной задачи обеспечивается тем, что в способе хирургического лечения птеригиума, заключающемся в предварительной эпибульбарной и субконъюнктивальной анестезии, иммобилизации головки птеригиума пинцетом и отсепаровки ее от роговичной поверхности с помощью расслаивателя с последующим иссечением ножницами до неизменной стромы роговицы и конъюнктивы с формированием ложа для амниотической мембраны, затем из нативной амниотической мембраны формируют участок прямоугольной формы шириной 2 мм, по длине соответствующий размерам сектора иссечения птеригиума в лимбальной зоне, далее проводят инстилляцию заранее подготовленных первого и второго компонентов ДАФК в ложе для амниотической мембраны в объеме 2-3 капли 0,1 мл, и их экспозицию в течение 2-х минут, после чего фрагмент амниотической мембраны перемещают в подготовленное ложе, проводят повторную инстилляцию компонентов ДАФК на уложенный фрагмент амниотической мембраны и экспозицию в течение 2-х минут, после чего операция завершают наложением мягкой контактной линзы на глазную поверхность.
Основными достоинствами предлагаемого нами способа хирургического лечения птеригиума являются:
1) использование запатентованного [патент РФ №RU 2 704 256 С1 МПК, опубл. 18.02.2019] двухкомпонентного аутофибринового клея, обеспечивающего высокую прочность склеивания тканей, обеспечение гемостаза и купирование воспалительной реакции в месте нанесения клеевой композиции;
2) полное исключение контаминации и переноса гемоконтактных инфекций за счет использования плазмы крови пациента;
3) использование минимального объема свежезабранной плазмы крови пациента, что ускоряет процедуру приготовления клеевой композиции;
4) отсутствие синтетических компонентов в составе двухкомпонентного аутофибринового клея и полное исключение аллергических реакций;
5) меньшая частота развития рубцевания конъюнктивы в месте оперативного вмешательства за счет использования физиологических концентраций фибрина, обеспечивающих более контролируемые процессы регенерации тканей;
6) меньшая частота развития помутнений роговицы за счет использования физиологических концентраций фибрина и создания условий для быстрой регенерации;
7) простота приготовления клеевой композиции и отсутствие потребности в создании специальных температурных условий;
8) использование более доступного оборудования (стерильные пробирки для получения обогащенной тромбоцитами плазмы и центрифуга), что значительно упрощает методику приготовления данной клеевой композиции.
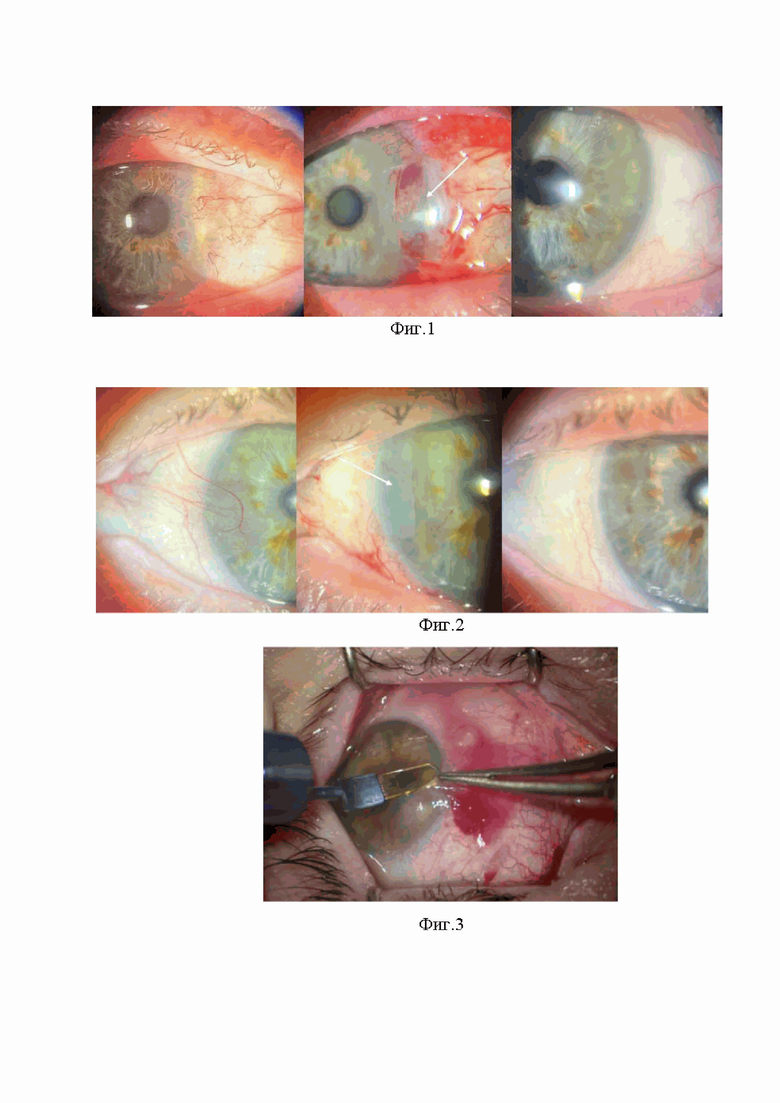
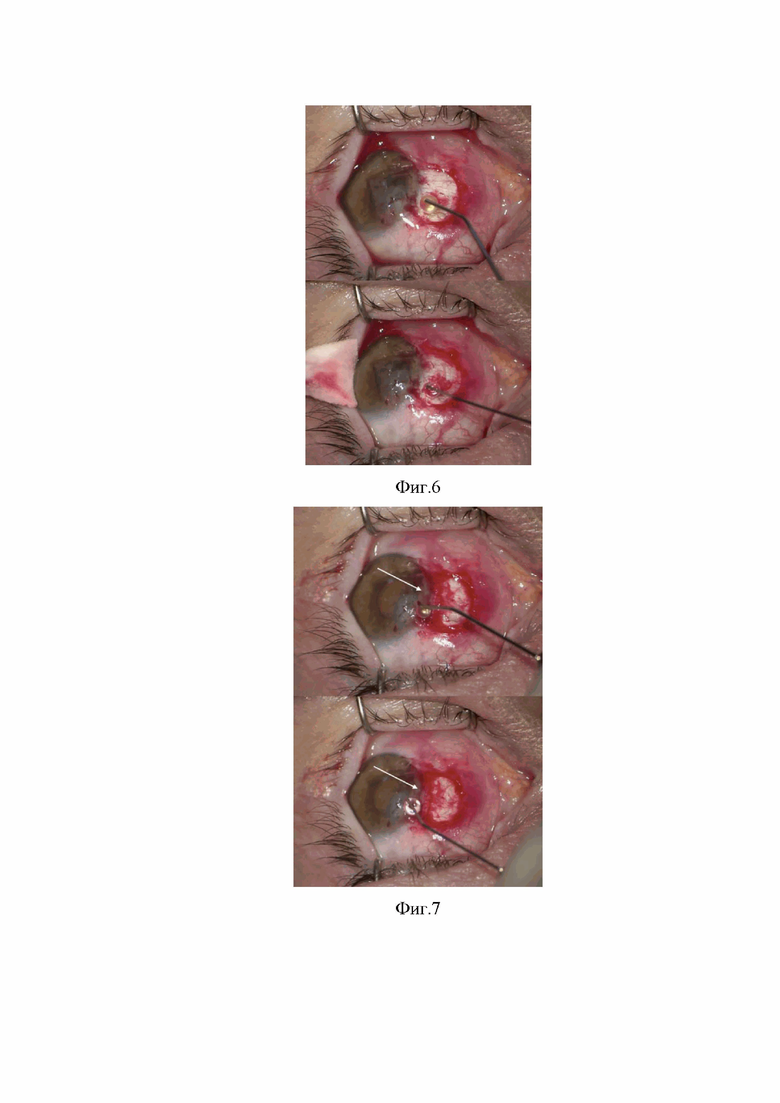
Изобретение поясняется фиг. 1 и фиг. 2, на которой представлены фото глазной поверхности правого (фиг. 1) и левого (фиг. 2) глаза в динамике. На фиг. 3 показана отсепаровка головки птеригиума от роговичной поверхности с помощью расслаивателя. На фиг. 4 показано иссечение головки птеригиума ножницами до неизменной стромы роговицы и конъюнктивы. На фиг. 5 показано формирование фрагмента амниотической мембраны прямоугольной формы шириной 2 мм, по длине соответствующего размерам сектора иссечения птеригиума в лимбальной зоне. На фиг. 6 показана экспозиция компонентов ДАФК в течение 2-х минут. На фиг. 7 показана повторная инстилляция компонентов ДАФК на уложенный фрагмент АМ.
Эффективность предлагаемого нами способа лечения птеригиума иллюстрирует следующий клинический случай. Пациент З. обратился в клинику офтальмологии ВМедА им. С.М. Кирова с жалобами на ощущение инородного тела, слезотечение, периодическое покраснение обоих глаз. Из анамнеза известно, что данные жалобы беспокоят на протяжении трех лет, при осмотре офтальмолога в ходе прохождения диспансеризации в поликлинике по месту жительства выявлено нарастание конъюнктивы на роговицу с носовой стороны на обоих глазах, выставлен диагноз: птеригиум второй степени обоих глаз. В клинике офтальмологии ВМедА им. С.М. Кирова было проведено хирургическое лечение в объеме удаления птеригиума с пластикой амниотической мембраной и фиксацией ДАФК на правом глазу, через 3 месяца - аналогичный объем хирургического вмешательства на правом глазу. После удаления птеригиума пациент отмечает снижение выраженности дискомфорта на обоих глазах и не предъявляет жалоб.
Из преимуществ нашего метода хирургического лечения в данном клиническом примере можно отметить малую продолжительность операции (на правом глазу длительность вмешательства составила 20 минут, на левом - 14 минут), отсутствие жалоб со стороны пациента в послеоперационном периоде (2 балла по 10-ти балльной шкале, где 0 баллов - отсутствие дискомфорта, 10 баллов - максимальный дискомфорт), использование минимальной консервативной терапии (местная антибактериальная и противовоспалительная терапия, препараты искусственной слезы), сокращение длительности послеоперационного периода до 8 суток в случае первого оперативного вмешательства и до 3 суток в случае оперативного вмешательства на парном глазу, а также сокращение сроков эпителизации до 7 суток в обоих случаях, что в совокупности обеспечило быструю реабилитацию пациента и позволило проводить дальнейшие хирургические вмешательства (удаление птеригиума на парном (левом) глазу спустя 3 месяца, а также факоэмульсификация катаракты с имплантацией интраокулярной линзы на правом глазу). На контрольных осмотрах при биомикроскопии в течение первых 3-х суток после операции отмечались признаки незначительного послеоперационного воспаления (умеренная поверхностная инъекция глазного яблока), которые были полностью купированы к 7-му дню после оперативного вмешательства.
Фото глазной поверхности правого (фиг. 1) и левого (фиг. 2) глаза в динамике демонстрируют наличие конъюнктивальной складки, нарастающей через лимбальную зону на роговицу, до операции, наличие фрагмента амниотической мембраны с четкими границами в бывшей зоне роста птеригиума, фиксированного ДАФК, на первые сутки после операции (отмечен стрелкой), отсутствие признаков воспаления и рецидива роста птеригиума через год после операции на правом глазу и через 9 месяцев после операции на левом глазу.
В настоящее время пациент не предъявляет жалоб со стороны органа зрения, острота зрения на обоих глазах составляет 1,0, рецидива роста птеригиума не наблюдается. Таким образом, проведение оперативного вмешательства на обоих глазах по предложенной методике в данном случае привело к купированию дискомфорта и увеличению качества жизни пациента, быстрой его реабилитации и возвращению к привычной жизни.
Техническим результатом является повышение эффективности хирургического лечения птеригиума за счет сокращения длительности оперативного вмешательства, уменьшения сроков эпителизации, повышением комфорта пациентов в послеоперационном периоде, а также снижения риска рецидивирования птеригиума.
Технический̆ результат достигается тем, что заранее проводится заготовка первого и второго компонентов ДАФК, которые набираются в 2 разных стерильных шприца объемом 1 мл. После проведения обезболивания: эпибульбарно - инстилляции анестетика (инокаин), субконъюнктивально - 0,2 мл 2% раствора лидокаина проводится иммобилизация головки птеригиума пинцетом, отсепаровка ее от роговичной поверхности с помощью расслаивателя (фиг. 3), иссечение ножницами до неизменной стромы роговицы и конъюнктивы (фиг. 4). Далее из амниотической мембраны формируется фрагмент прямоугольной формы шириной 2 мм, по длине соответствующего размерам сектора иссечения птеригиума в лимбальной зоне (отмечен стрелкой, фиг. 5). Производят инстилляцию первого и второго компонентов ДАФК в подготовленное ложе для амниотической мембраны в объеме 2-3 капли (0,1 мл), и их экспозицию в течение 2-х минут (фиг. 6), после чего фрагмент амниотической мембраны перемещают в подготовленное ложе. Далее следует повторная инстилляция компонентов ДАФК на уложенный фрагмент амниотической мембраны (отмечен стрелкой, фиг. 7), экспозиция в течение 2-х минут. Операция завершается наложением мягкой контактной линзы.
Данный способ зарекомендовал себя как эффективный и атравматичный способ хирургического лечения птеригиума.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕЦИДИВИРУЮЩЕГО ПТЕРИГИУМА | 2023 |
|
RU2821131C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ФИКСАЦИИ АМНИОТИЧЕСКОЙ МЕМБРАНЫ ПРИ ЛЕЧЕНИИ ХРОНИЧЕСКИХ ЭРОЗИЙ РОГОВИЦЫ | 2023 |
|
RU2807860C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПТЕРИГИУМА 3 - 5 СТЕПЕНИ | 2018 |
|
RU2698445C1 |
| Способ хирургического лечения рецидивирующего птеригиума | 2017 |
|
RU2655271C1 |
| Способ хирургического лечения птеригиума | 2016 |
|
RU2611939C1 |
| СПОСОБ ПРОФИЛАКТИКИ РЕЦИДИВА ПТЕРИГИУМА | 2016 |
|
RU2646125C1 |
| Способ хирургического удаления птеригиума роговицы с пластикой дефекта при помощи интактной бульбарной конъюнктивы | 2020 |
|
RU2736914C1 |
| Способ реконструкции эпителиального слоя роговицы при синдроме лимбальной недостаточности у пациентов с истонченной роговицей | 2021 |
|
RU2766166C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕЦИДИВИРУЮЩЕГО ПТЕРИГИУМА | 2008 |
|
RU2354338C1 |
| Способ восстановления эпителиального слоя роговицы при одностороннем синдроме лимбальной недостаточности | 2020 |
|
RU2741411C1 |

Изобретение относится к медицине, а именно, к офтальмохирургии. Осуществляют предварительную эпибульбарную и субконъюнктивальную анестезию, иммобилизацию головки птеригиума пинцетом и отсепаровку ее от роговичной поверхности с помощью расслаивателя с последующим иссечением ножницами до неизменной стромы роговицы и конъюнктивы с формированием ложа для фрагмента нативной амниотической мембраны прямоугольной формы шириной 2 мм, по длине соответствующего размерам сектора иссечения птеригиума в лимбальной зоне. Вначале проводят инстилляцию заранее подготовленных первого и второго компонентов двухкомпонентного аутофибринового клея в ложе для амниотической мембраны в объеме 2-3 капли - 0,1 мл, их экспозицию в течение 2-х минут, после чего фрагмент амниотической мембраны перемещают в подготовленное ложе. Проводят повторную инстилляцию первого и второго компонентов двухкомпонентного аутофибринового клея на уложенный фрагмент амниотической мембраны и экспозицию в течение 2-х минут. После чего операцию завершают наложением мягкой контактной линзы на глазную поверхность. Способ позволяет сократить длительность оперативного вмешательства, уменьшить сроки эпителизации, повысить комфорт пациентов в послеоперационном периоде, а также снизить риск рецидивирования птеригиума. 1 пр., 7 ил.
Способ хирургического лечения птеригиума, заключающийся в предварительной эпибульбарной и субконъюнктивальной анестезии, иммобилизации головки птеригиума пинцетом и отсепаровки ее от роговичной поверхности с помощью расслаивателя с последующим иссечением ножницами до неизменной стромы роговицы и конъюнктивы с формированием ложа для фрагмента нативной амниотической мембраны прямоугольной формы шириной 2 мм, по длине соответствующего размерам сектора иссечения птеригиума в лимбальной зоне, отличающийся тем, что вначале проводят инстилляцию заранее подготовленных первого и второго компонентов двухкомпонентного аутофибринового клея в ложе для амниотической мембраны в объеме 2-3 капли - 0,1 мл, их экспозицию в течение 2-х минут, после чего фрагмент амниотической мембраны перемещают в подготовленное ложе, проводят повторную инстилляцию первого и второго компонентов двухкомпонентного аутофибринового клея на уложенный фрагмент амниотической мембраны и экспозицию в течение 2-х минут, после чего операцию завершают наложением мягкой контактной линзы на глазную поверхность.
| Kucukerdonmez C | |||
| et al | |||
| Amniotic membrane transplantation using fibrin glue in pterygium surgery: a comparative randomised clinical trial | |||
| Eye (Lond) | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Singh P, et al | |||
| A randomized controlled prospective study to assess the role of subconjunctival bevacizumab in primary pterygium surgery in Indian patients | |||
| Indian J | |||
Авторы
Даты
2023-11-21—Публикация
2023-05-16—Подача