Область техники
Настоящее изобретение относится к металлическому материалу для медицинского устройства, способу изготовления металлического материала для медицинского устройства и медицинскому устройству.
Уровень техники
Пленка алмазоподобного углерода (АПУ) известна как аморфная углеродная пленка и имеет твердую, плотную и неактивную поверхность, и поэтому ее применяют в различных областях.
Например, были изучены методы придания таких характеристик, как стойкость к истиранию, коррозионная стойкость и гладкость поверхности, поверхности основы с использованием неорганического материала, такого как металл или керамика, или органического материала, такого как полимер, путем формирования пленки АПУ на поверхности основы. В частности, известна металлическая форма или металлический инструмент, долговечность которых повышают посредством нанесения покрытия из пленки АПУ на металлическую поверхность, чтобы покрыть металлическую поверхность пленкой АПУ. Кроме того, пленку АПУ также используют для изготовления медицинских инструментов (стентов и т.п.). Например, было изучено повышение долговечности посредством нанесения пленки АПУ на поверхность металла, используемого для медицинских инструментов.
В качестве конкретного примера в патенте Японии (JP-B2) №5536168 раскрыт супергидрофильный материал, включающий пленку АПУ, имеющий гидрофильную функциональную группу на поверхности основы, где для улучшения адгезии между основой и пленкой АПУ обеспечен промежуточный слой между основой и пленкой АПУ.
Кроме того, в патенте Японии (JP-B2) №5661632 описан стент, включающий слой основы, поверхность которой выполнена из металлического материала, слой углеродного соединения, изготовленный из карбида кремния, первый слой алмазоподобного углерода, содержащий по меньшей мере кремний и не содержащий фтора, и второй слой алмазоподобного углерода (слой F-АПУ), содержащий фтор, где концентрация кремния, содержащегося в первом слое алмазоподобного углерода, в атомных процентах составляет 1% или более и 10% или менее.
Сущность изобретения
Техническая задача
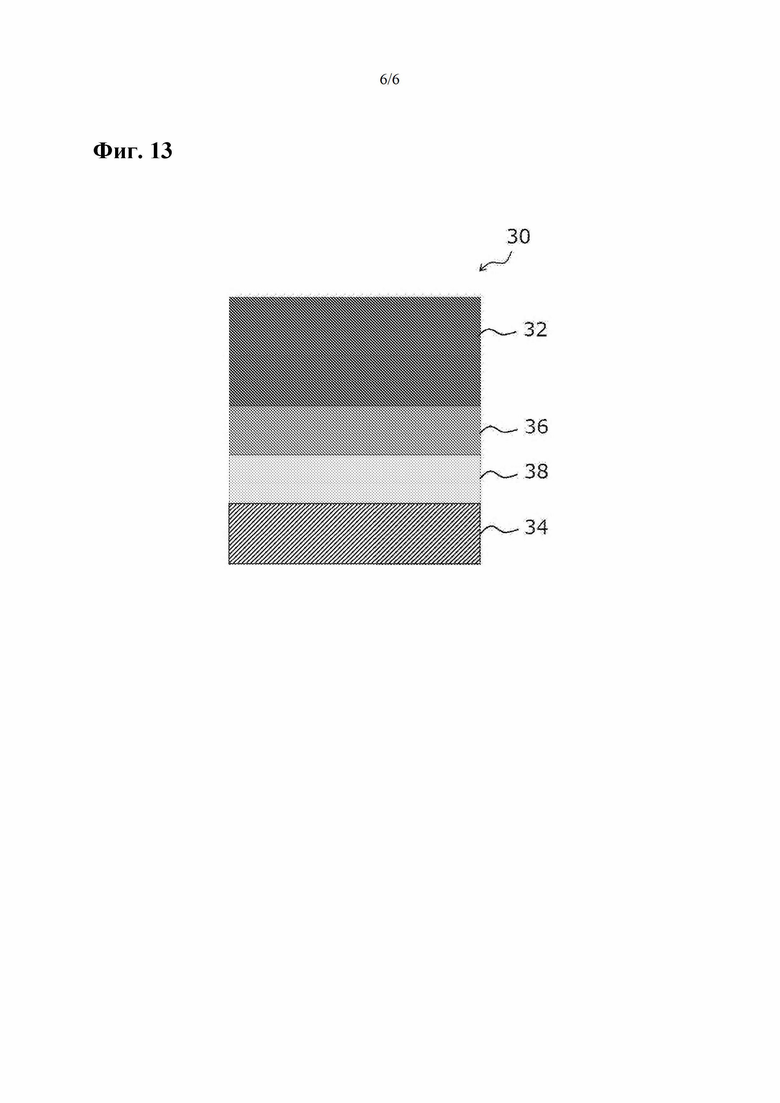
Как описано выше, методы с использованием пленки из алмазоподобного углерода (пленка АПУ) изучали также в устройствах для медицинского применения (далее -медицинские устройства), таких как стенты. В традиционных способах считается, что стент, описанный в JP-B2 №5661632, подавляет появление трещин и отслоений посредством обеспечения первого слоя АПУ, не содержащего фтора, между слоем соединения углерода и слоем F-АПУ. В качестве обычного медицинского устройства, в котором используют пленку АПУ, известно устройство, имеющее слоистую структуру из слоя 32 F-АПУ, слоя 36 Si-АПУ, слоя 38 SiC и основы 34, как показано на фиг. 13.
Медицинские устройства обычно используются в течение длительного периода времени после их имплантации в живой организм.
Поэтому в живом организме требуются стабильные рабочие характеристики, чтобы медицинские изделия могли непрерывно и стабильно следовать за движением живого организма в течение длительного периода времени, и медицинские изделия гибко деформируются под действием различных напряжений, различных по силе или направлению при следовании за движением. Однако традиционные методы в действительности не обеспечивают гибкости, способной ослаблять различные напряжения, а также способности отслеживать каждое движение живого организма.
Настоящее изобретение было сделано с учетом вышеизложенного.
Задача, решаемая одним воплощением настоящего изобретения, состоит в обеспечении металлического материала для медицинского устройства, обладающего способностью стабильно следовать за движением живого организма и гибкостью для гибкого деформирования под действием различных напряжений во время следования, а также способа изготовления такого материала.
Задача, решаемая с помощью другого воплощениях настоящего изобретения, состоит в обеспечении медицинского устройства, обладающего способностью стабильно следовать за движением живого организма и гибкостью для гибкого деформирования под действием различных напряжений во время следования.
Решение задачи
Конкретные средства решения указанных задач включают следующие аспекты.
1. Металлический материал для медицинского устройства, включающий: металлический слой и слой алмазоподобного углерода, нанесенный на металлический слой и содержащий фтор и кремний.
2. Металлический материал для медицинского устройства согласно (1), в котором общая концентрация фтора, содержащегося в слое алмазоподобного углерода, составляет от 7 ат. % до 10 ат. % по отношению к общей концентрации углерода, фтора и кремния.
3. Металлический материал для медицинского устройства согласно (1) или (2), в котором общая концентрация кремния, содержащегося в слое алмазоподобного углерода, составляет от 17 ат. % до 25 ат. % по отношению к общей концентрации углерода, фтора и кремния.
4. Металлический материал для медицинского устройства согласно любому из (1)-(3), в котором в слое алмазоподобного углерода концентрация фтора на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, больше, чем концентрация фтора на поверхности на стороне, обращенной к металлическому слою, по толщине слоя алмазоподобного углерода.
5. Металлический материал для медицинского устройства согласно (4), в котором в слое алмазоподобного углерода отношение Cf концентрации фтора на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, к концентрации фтора на поверхности на стороне, обращенной к металлическому слою, удовлетворяет соотношению 1<Cf≤155.
6. Металлический материал для медицинского устройства согласно (4) или (5), в котором концентрация фтора, содержащегося в слое алмазоподобного углерода, постепенно увеличивается от стороны, обращенной к металлическому слою, к стороне, противоположной стороне, обращенной к металлическому слою, по толщине слоя алмазоподобного углерода.
7. Металлический материал для медицинского устройства согласно любому из (1)-(6), в котором в слое алмазоподобного углерода концентрация кремния на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, меньше, чем концентрация кремния на поверхности на стороне, обращенной к металлическому слою, по толщине слоя алмазоподобного углерода.
8. Металлический материал для медицинского устройства согласно (7), в котором в слое алмазоподобного углерода отношение Cs концентрации кремния на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, к концентрации кремния на поверхности на стороне, обращенной к металлическому слою, удовлетворяет соотношению 0,015≤Cs<1.
9. Металлический материал для медицинского устройства согласно (7) или (8), в котором концентрация кремния, содержащегося в слое алмазоподобного углерода, постепенно уменьшается от стороны, обращенной к металлическому слою, к стороне, противоположной стороне, обращенной к металлическому слою, по толщине слоя алмазоподобного углерода.
10. Металлический материал для медицинского устройства согласно любому из (1)-(9), в котором отношение (DF:DS) концентрации DF фтора к концентрации DS кремния на поверхности слоя алмазоподобного углерода на стороне, противоположной стороне, обращенной к металлическому слою, составляет от 1:1 до 90:1.
11. Металлический материал для медицинского устройства согласно любому из (1)-(10), в котором слой алмазоподобного углерода расположен в качестве самого внешнего слоя на металлическом слое.
12. Металлический материал для медицинского устройства согласно любому из (1)-(11), в котором металлический слой содержит по меньшей мере один металл, выбранный из группы, состоящей из титана, никеля, кобальта, хрома, тантала, платины, золота, их сплавов и нержавеющей стали.
13. Металлический материал для медицинского устройства согласно (12), в котором металлический слой содержит никель-титановый сплав, кобальт-хромовый сплав или нержавеющую сталь.
14. Металлический материал для медицинского устройства согласно любому из (1)-(13), где металлический материал используют в стенте.
15. Металлический материал для медицинского устройства согласно (14), где стент представляет собой стент для системного кровеносного сосуда.
16. Медицинское устройство, включающее металлический материал для медицинского устройства согласно любому из (1)-(15).
17. Медицинское устройство согласно (16), представляющее собой стент.
18. Медицинское устройство согласно (17), где стент представляет собой стент для кровеносного сосуда нижней конечности.
19. Способ изготовления металлического материала для медицинского изделия, включающий формирование слоя алмазоподобного углерода, содержащего фтор и кремний, на металлическом слое посредством осаждения из паровой фазы, способом выращивания из паровой фазы с использованием смешанного исходного материала, полученного смешиванием силанового соединения и фторсодержащего алифатического углеводорода в качестве исходных материалов.
Преимущественные эффекты изобретения
Согласно одному воплощению настоящего изобретения предложен металлический материал для медицинского устройства, обладающий способностью стабильно следовать за движением живого организма и гибкостью для гибкого деформирования под действием различных напряжений во время следования, а также способ изготовления такого материала. Ожидается, что металлический материал для медицинского устройства по настоящему изобретению является совместимым при непрерывном использовании в течение длительного периода времени.
Согласно другому воплощению настоящего изобретения предложено медицинское устройство, обладающее способностью стабильно следовать за движением живого организма и гибкостью для гибкого деформирования под действием различных напряжений во время следования. Ожидается, что медицинское устройство по настоящему изобретению является совместимым при непрерывном использовании в течение длительного периода времени.
Краткое описание чертежей
Фиг. 1 представляет собой фотографию СЭМ (сканирующей электронной микроскопии), иллюстрирующую состояние адгезии тромбоцитов в испытуемом образце примера 3, в котором однослойный слой АПУ сформирован на основе из сплава NiTi.
Фиг. 2 представляет собой фотографию СЭМ, иллюстрирующую состояние адгезии тромбоцитов на основе из сплава NiTi, где не сформирован слой АПУ.
Фиг. 3 представляет собой фотографию СЭМ, иллюстрирующую состояние отслаивания (способность следования) в испытуемом образце примера 3, в котором на проволоке из сплава NiTi сформирован однослойный слой АПУ.
Фиг. 4 представляет собой фотографию СЭМ, иллюстрирующую состояние адгезии тромбоцитов в испытуемом образце примера 7, в котором однослойной слой АПУ сформирован на основе из SUS316L (нержавеющая сталь).
Фиг. 5 представляет собой фотографию СЭМ, иллюстрирующую состояние адгезии тромбоцитов на основе из нержавеющей стали, на которой не сформирован слой АПУ.
Фиг. 6 представляет собой фотографию СЭМ, иллюстрирующую состояние адгезии тромбоцитов в испытуемом образце сравнительного примера 1, в котором слой АПУ, имеющий многослойную структуру, сформирован на основе из сплава NiTi.
Фиг. 7 представляет собой фотографию СЭМ, иллюстрирующую состояние адгезии тромбоцитов в испытуемом образце сравнительного примера 2, в котором слой АПУ, имеющий многослойную структуру, сформирован на основе из SUS316L (нержавеющая сталь).
Фиг. 8 представляет собой фотографию СЭМ, иллюстрирующую состояние отслаивания (способность следования) в испытуемом образце сравнительного примера 1, в котором слой АПУ, имеющий многослойную структуру, сформирован на проволоке из сплава NiTi.
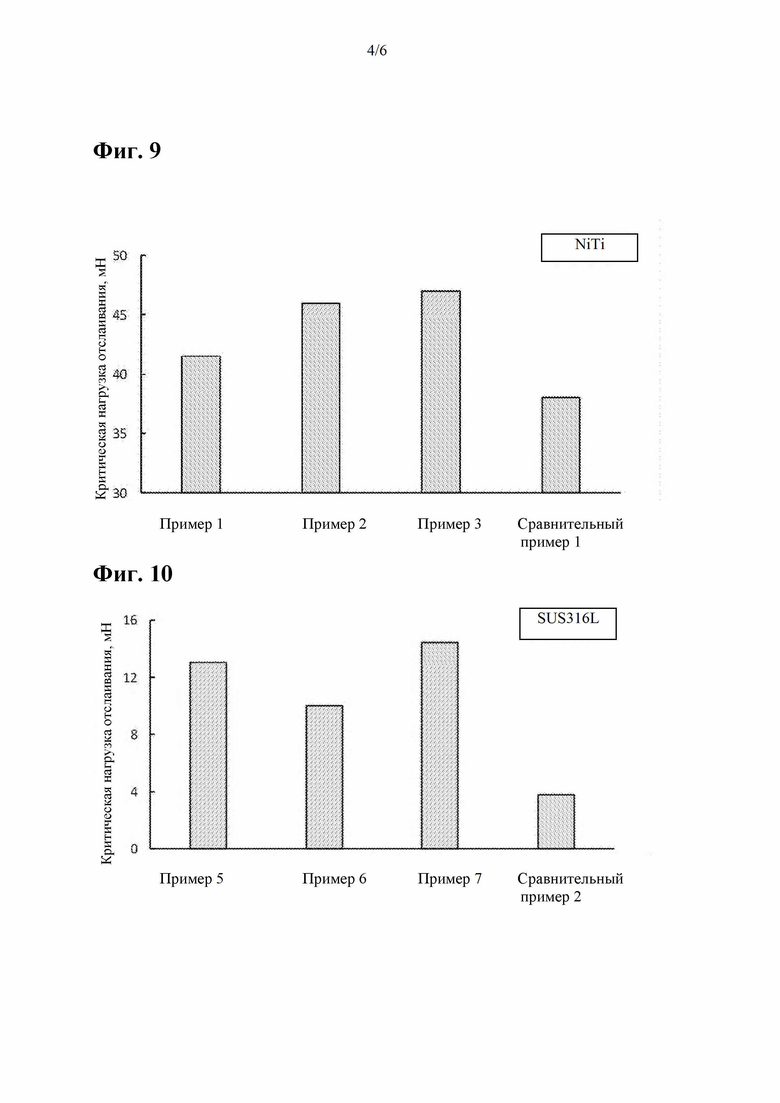
Фиг. 9 представляет собой график, иллюстрирующий адгезию (к основе из сплава NiTi) слоев АПУ в примерах 1-3 и сравнительном примере 1 в сравнении.
Фиг. 10 представляет собой график, иллюстрирующий адгезию (к основе из нержавеющей стали) слоев АПУ в примерах 5-7 и сравнительном примере 2 в сравнении.
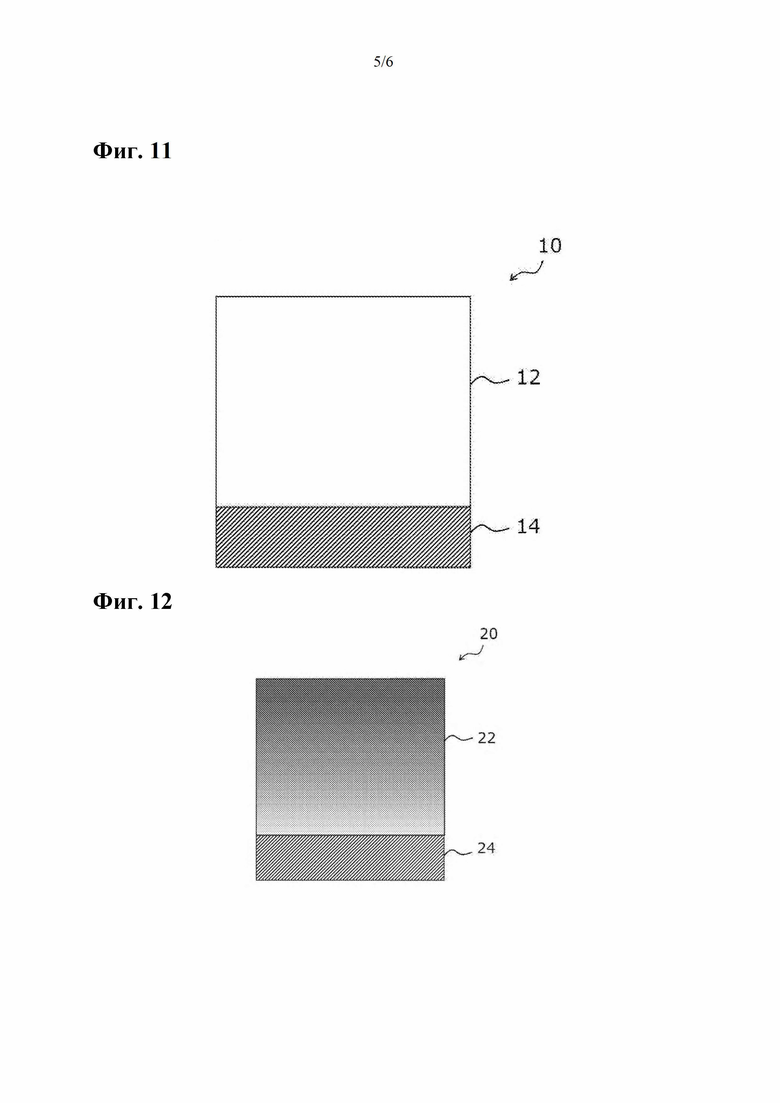
Фиг. 11 представляет собой схематический вид в разрезе, иллюстрирующий пример металлического материала для медицинского устройства по настоящему изобретению.
Фиг. 12 представляет схематический вид в разрезе, иллюстрирующий другой пример металлического материала для медицинского устройства по настоящему изобретению.
Фиг. 13 представляет схематический вид в разрезе, иллюстрирующий традиционный металлический материал для медицинского устройства.
Описание воплощений
Далее подробно описаны металлический материал для медицинского устройства, способ его изготовления и медицинское устройство по настоящему изобретению. Описание компонентов, раскрытых ниже, может быть выполнено на основе репрезентативного воплощения настоящего изобретения, но настоящее изобретение не ограничивается таким воплощением.
В настоящем описании «от X до Y», указывающее на численный диапазон, используют для обозначения включения численных значений X и Y, указанных до и после численного диапазона, в качестве нижнего предельного значения и верхнего предельного значения, соответственно.
В численном диапазоне, описанном поэтапно в настоящем описании, верхнее предельное значение или нижнее предельное значение, описанное в одном численном диапазоне, может быть заменено верхним предельным значением или нижним предельным значением другого численного диапазона, описанного поэтапно. Кроме того, в численном диапазоне, описанном в настоящем описании, верхнее предельное значение или нижнее предельное значение численного диапазона может быть заменено значением, указанным в примерах.
В настоящем изобретении термин «стадия» охватывает не только независимую стадию, но также стадию, которую нельзя четко отличить от других стадий, при условии, что намеченная цель стадии достигнута.
В настоящем описании в случае, когда в слое присутствует множество веществ, соответствующих каждому компоненту, количество каждого компонента композиции означает общее количество множества веществ, присутствующих в композиции, если не указано иное.
В настоящем описании сочетание предпочтительных воплощений представляет собой более предпочтительное воплощение.
Металлический материал для медицинского устройства
Металлический материал для медицинского устройства по настоящему изобретению включает металлический слой и слой алмазоподобного углерода (далее также называемый просто «слой АПУ»), нанесенный на металлический слой и содержащий фтор и кремний. Металлический материал для медицинского устройства по настоящему изобретению может дополнительно включать другой слой, такой как промежуточный слой, при необходимости.
В металлическом материале для медицинского устройства по настоящему изобретению, поскольку слой АПУ, нанесенный на металлический слой, представляет собой слой алмазоподобного углерода, содержащего фтор (F) и кремний (Si), металлический материал обладает превосходной стабильностью для стабильного следования движению живого организма и обладает гибкостью для гибкого деформирования под действием различных напряжений, возникающих в соответствии с движением живого организма при следовании за движением живого организма. Это обеспечивает превосходную стабильность в живом организме.
Причина, по которой проявляются эффекты настоящего изобретения, не всегда ясна, но оценивается следующим образом.
В качестве слоя АПУ в металлическом материале для медицинского устройства по настоящему изобретению используют алмазоподобный углерод, содержащий фтор (F) и кремний (Si). Как правило, алмазоподобный углерод считается твердым и обладает превосходными поверхностными свойствами, но в живом организме алмазоподобный углерод, вероятно, может стать мишенью для атаки тромбоцитов и т.п. как инородное вещество. Кроме того, движение живого организма меняется, и дополнительно к напряжению изгиба и напряжению растяжения часто накладывается напряжение кручения. Для непрерывного и стабильного использования в живом организме в течение длительного периода времени даже в таких условиях требуется гибкость, обеспечивающая возможность стабильно следовать за движением живого организма и гибко деформироваться под действием различных напряжений, воспринимаемых при следовании за движением.
Традиционно известно использование F для придания биосовместимости слою АПУ на самой внешней стороне, и известно использование Si для улучшения адгезии слоя АПУ к основе.
Чтобы справиться с напряжением, вызванным движением живого организма, важно иметь гибкость, позволяющую легко следовать за напряжением и ослаблять напряжение. При всего лишь обеспечении слоя, содержащего F или Si, межслойная адгезия, как правило, оказывается недостаточной, и даже если свойства, зависящие от состава, могут частично проявляться, считают, что баланс между способностью следовать за движением живого организма и релаксацией напряжения (гибкостью) во время следования не является подходящим по материалу в целом. Поэтому эффект подавления растрескивания или отслаивания при восприятии различных напряжений является небольшим.
В настоящем изобретении при использовании алмазоподобного углерода, содержащего F и Si, можно придать слою АПУ способность стабильно следовать за движением живого организма и гибкость для гибкого деформирования под действием различных напряжений при следовании за движением.
В результате металлический материал для медицинского устройства по настоящему изобретению может выдерживать длительное непрерывное использование.
Металлический слой
Металлический материал для медицинского устройства по настоящему изобретению включает металлический слой.
В одном аспекте металлический слой может представлять собой основу, составляющую металлический материал для медицинского устройства (т.е. в аспекте, в котором основа представляет собой металл). Кроме того, в одном аспекте металлический слой может быть включен как часть основы, составляющей металлический материал для медицинского устройства (например, в аспекте, в котором материал (полимер, силиконовый каучук и т.п.), отличающийся от желательного металла, используют для основы).
Примеры металла в металлическом слое включают железо, медь, титан, никель, кобальт, хром, алюминий, цинк, марганец, тантал, вольфрам, платину и золото. Среди металлов предпочтительным является по меньшей мере один металл, выбранный из группы, состоящей из титана, никеля, кобальта, хрома, тантала, платины и золота.
Металл может представлять собой сплав вышеуказанных металлов.
Примеры металлического сплава включают никель-титановый сплав, кобальт-хромовый сплав, медно-алюминиево-марганцевый сплав, медно-цинковый сплав, никель-алюминиевый сплав и нержавеющую сталь. Среди сплавов предпочтительными являются никель-титановый сплав, кобальт-хромовый сплав или нержавеющая сталь.
В качестве нержавеющей стали, например, SUS316L является предпочтительной с точки зрения коррозионной стойкости.
Среди перечисленного более предпочтительным является по меньшей мере один металл, выбранный из группы, состоящей из титана, никеля, кобальта, хрома, тантала, платины, золота, их сплавов и нержавеющей стали, и еще более предпочтительным является по меньшей мере один металл, выбранный из группы, состоящей из титана, никеля, кобальта, хрома, их сплавов и нержавеющей стали.
Среди перечисленного особенно предпочтительным является слой, содержащий никель-титановый сплав, кобальт-хромовый сплав или нержавеющую сталь, или слой, состоящий из никель-титанового сплава, кобальт-хромового сплава или нержавеющей стали.
Следует отметить, что в случае, когда металлический слой представляет собой слой, состоящий из никель-титанового сплава, кобальт-хромового сплава или нержавеющей стали, металлический слой может содержать металлы, отличающиеся от никеля, титана, кобальта, хрома и нержавеющей стали при условии, что эффекты металлического материала для медицинского устройства и медицинского устройства по настоящему изобретению существенно не ухудшаются.
Толщина металлического слоя конкретно не ограничена и может быть подходящим образом выбрана в соответствии с местом применения медицинского устройства в живом организме, сроком службы и т.п. В случае, когда металлический слой имеет форму плоской пластины, толщина металлического слоя может быть выбрана в соответствии с применением, формой и т.п. Например, в случае стента толщина металлического слоя может составлять, например, от 50 мкм до 250 мкм. Например, в случае фиксирующей пластины толщина металлического слоя может составлять, например, от 100 мкм до 2000 мкм. Кроме того, в случае, когда металлический слой имеет такую форму, как квадратная, круглая, полукруглая, форму блока, форму куска или неправильную форму (например, фиксирующее устройство, такое как болт или винт, искусственное сердце или искусственный тазобедренный сустав), толщина может быть выбрана в соответствии с необходимой формой или т.п.
Металлический слой можно получать любым способом, и для него можно использовать коммерческие продукты, доступные на рынке.
Слой алмазоподобного углерода
Металлический материал для медицинского устройства по настоящему изобретению включает слой АПУ на основе.
Слой АПУ в настоящем изобретении представляет собой алмазоподобный углеродный слой, содержащий фтор (F) и кремний (Si). Поскольку используют алмазоподобный углерод, содержащий F и Si, может проявляться способность стабильно следовать за движением живого организма и гибкость для гибкого деформирования под действием различных напряжений при следовании.
Слой алмазоподобного углерода может представлять собой слой, сформированный любым способом, при условии, что в этом способе используют F и Si. Слой алмазоподобного углерода может быть сформирован с использованием известного способа, такого как способ осаждения из паровой фазы или способ напыления. Слой алмазоподобного углерода в настоящем изобретении предпочтительно формируют способом выращивания из паровой фазы.
Способ формирования слоя АПУ способом выращивания из паровой фазы подробно описан в разделе, посвященном способу изготовления металлического материала для медицинского устройства, описанному ниже.
Концентрация F
Общая концентрация фтора, содержащегося в слое АПУ, предпочтительно составляет от 7 ат. % до 10 ат. % и более предпочтительно от 7 ат. % до 8,5 ат. % по отношению к общей концентрации углерода, фтора и кремния.
Концентрацию фтора, содержащегося в слое АПУ, можно измерить с помощью метода рентгеновской фотоэлектронной спектроскопии (РФС). В частности, концентрацию фтора определяют с помощью устройства РФС, измеряя содержание таких элементов, как углерод (С), F, Si и, при необходимости, кислород (О), которые присутствуют на поверхности слоя АПУ, содержащего F и Si.
В слое АПУ концентрация фтора (далее концентрация фтора может обозначаться как «концентрация F») на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, предпочтительно больше, чем концентрация F на поверхности на стороне, обращенной к металлическому слою, по толщине слоя АПУ. В частности, в случае, когда слой АПУ является самым внешним слоем на металлическом слое, предпочтительно концентрация F на поверхности (т.е. на самой внешней поверхности) на стороне, противоположной стороне, обращенной к металлическому слою, больше, чем концентрация F на поверхности на стороне, обращенной к металлическому слою, и более предпочтительно концентрация F на самой внешней поверхности слоя АПУ является наибольшей по толщине слоя АПУ.
В слое АПУ отношение Cf (=CF1/CF0) концентрации F (CF1) на поверхности (предпочтительно на самой внешней поверхности в случае, когда слой АПУ является самым внешним слоем) на стороне, противоположной стороне, обращенной к металлическому слою, к концентрации F (CF0) на поверхности на стороне, обращенной к металлическому слою, предпочтительно удовлетворяет соотношению 1<Cf≤155. То есть предпочтительно концентрация F увеличивается от внутренней стороны слоя АПУ, прилегающей к металлическому слою, наружу в направлении наслоения металлического слоя и слоя АПУ металлического материала для медицинского устройства. Это придает металлическому материалу для медицинского устройства превосходные гибкость и биосовместимость.
Отношение Cf более предпочтительно удовлетворяет соотношению формулы 1 и еще более предпочтительно удовлетворяет соотношению формулы 2.
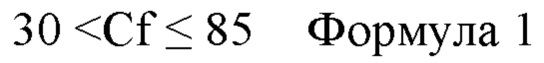
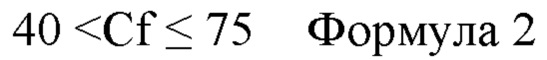
В одном аспекте слой АПУ может иметь концентрацию F, содержащегося в слое АПУ, ступенчато увеличивающуюся от стороны, обращенной к металлическому слою, к стороне, противоположной стороне, обращенной к металлическому слою, по толщине слоя АПУ. Предпочтительно это аспект, в котором концентрация F, содержащегося в слое АПУ, постепенно увеличивается от стороны, обращенной к металлическому слою, к стороне, противоположной стороне, обращенной к металлическому слою. Ступенчатое увеличение означает, что концентрация F увеличивается при постоянной или произвольной разнице концентраций. В последнем аспекте предпочтительно концентрация F постепенно увеличивается в направлении от металлического слоя (направление наружу), от внутренней стороны слоя АПУ, прилегающей к металлическому слою, в направлении наслоения металлического слоя и слоя АПУ металлического материала для медицинского устройства. В результате металлический материал для медицинского изделия обладает гибкостью для гибкого деформирования под действием различных напряжений, вызванных движением живого организма, при сохранении биосовместимости металлического материала для медицинского изделия, а также имеет превосходный эффект подавления растрескивания и отслаивания.
Концентрация Si
Общая концентрация кремния, содержащегося в слое АПУ, предпочтительно составляет от 17 до 25 ат. % и более предпочтительно от 20 до 25 ат. % по отношению к общей концентрации углерода, фтора и кремния.
Концентрацию кремния, содержащегося в слое АПУ, можно измерить с помощью метода анализа рентгеновской фотоэлектронной спектроскопии (РФС), аналогично концентрации F, описанной выше.
В слое АПУ концентрация кремния (далее концентрация кремния может сокращенно обозначаться «концентрация Si») на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, предпочтительно меньше, чем концентрация Si на поверхности на стороне, обращенной к металлическому слою, по толщине слоя АПУ. В частности, в случае, когда слой АПУ является самым внешним слоем на металлическом слое, концентрация Si на поверхности на стороне, обращенной к металлическому слою, предпочтительно больше, чем концентрация Si на поверхности (то есть на самой внешней поверхности) на стороне, противоположной стороне, обращенной к металлическому слою.
В слое АПУ отношение Cs (=CS1/CS0) концентрации Si (CS1) на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, к концентрации Si (CS0) на поверхности на стороне, обращенной к металлическому слою, предпочтительно удовлетворяет соотношению 0,015≤Cs<1. To есть предпочтительно концентрация Si увеличивается по направлению внутренней стороны слоя АПУ, прилегающей к металлическому слою, в направлении наслоения металлического слоя и слоя АПУ металлического материала для медицинского изделия. Это придает металлическому материалу превосходную деформируемость при деформировании вслед за движением живого организма.
Деформируемость относится к способности изменять форму в соответствии с изгибом, растяжением, кручением и т.п., которое металлический материал для медицинского устройства воспринимает вследствие движения живого организма.
Отношение Cs более предпочтительно удовлетворяет соотношению формулы 3 и еще более предпочтительно удовлетворяет соотношению формулы 4.
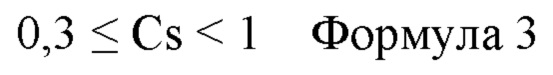
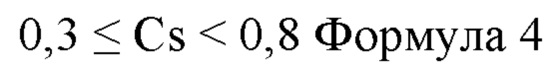
В одном аспекте слой АПУ может иметь концентрацию Si, содержащегося в слое АПУ, которая уменьшается ступенчато от стороны, обращенной к металлическому слою, к стороне, противоположной стороне, обращенной к металлическому слою, по толщине слоя АПУ. Предпочтительно это аспект, в котором концентрация Si, содержащегося в слое АПУ, постепенно уменьшается от стороны, обращенной к металлическому слою, к стороне, противоположной стороне, обращенной к металлическому слою. Ступенчатое уменьшение означает, что концентрация F уменьшается при постоянной или произвольной разнице концентраций. В последнем аспекте предпочтительно концентрация Si постепенно увеличивается к внутренней стороне слоя АПУ, прилегающей к металлическому слою, в направлении наслоения металлического слоя и слоя АПУ металлического материала для медицинского устройства. В результате достигают деформируемости, при которой металлический материал медицинского устройства деформируется под действием такой силы, как изгиб, растяжение или кручение, которую воспринимает металлический материал медицинского устройства вследствие движения живого организма, и эффект подавления растрескивания и отслоения является превосходным.
Отношение (DF:DS) концентрации F DF к концентрации Si DS на поверхности слоя АПУ на стороне, противоположной стороне, обращенной к металлическому слою, предпочтительно составляет от 1:1 до 90:1, более предпочтительно от 1:1 до 80:1 и еще более предпочтительно от 1:1 до 50:1.
Когда отношение (DF:DS) на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, находится в указанном диапазоне, получают композицию, в которой F содержится больше, чем Si в определенном диапазоне на поверхности слоя АПУ, наиболее удаленной от металлического слоя. Это дает возможность более гибкого деформирования под действием различных напряжений, следуя движению живого организма. Это более заметно в случае, когда слой АПУ является самым внешним слоем металлического материала для медицинского устройства.
Как описано выше, слой АПУ предпочтительно обеспечивают как самый внешний слой на металлическом слое с точки зрения способности более гибко деформироваться под действием различных напряжений, следуя движению живого организма.
Толщина АПУ в настоящем изобретении предпочтительно мала с точки зрения применения медицинских устройств. Например, толщина предпочтительно составляет от 10 нм или более до менее 1000 нм, более предпочтительно от 100 нм до 500 нм и еще более предпочтительно от 150 нм до 250 нм.
Металлический материал для медицинского устройства по настоящему изобретению может быть любым при условии, что металлический материал включает слой АПУ, содержащий F и Si, на металлическом слое. В качестве конкретного металлического материала для медицинского устройства можно использовать материал, имеющий следующую слоистую структуру.
(1) Содержащий слой F и Si слой АПУ / металлический слой
(2) Содержащий F и Si слой АПУ / не содержащий F и Si слой АПУ / металлический слой
(3) Содержащий F и Si слой АПУ / содержащий Si слой АПУ / металлический слой
(4) Содержащий F и Si слой АПУ / промежуточный слой, отличающийся от слоя АПУ / металлический слой.
Среди вышеперечисленного, с точки зрения гибкости и стабильности в живом организме, предпочтительным является материал, в котором слой АПУ и металлический слой находятся в контакте друг с другом, и слой АПУ является самым внешним слоем металлического материала для медицинского устройства, и вышеуказанный материал (1) является особенно предпочтительным.
Пример металлического материала для медицинского устройства по настоящему изобретению показан на фиг. 11.
Металлический материал 10 для медицинского устройства, показанный на фиг. 11, является примером вышеприведенного материала (1), и содержащий F и Si слой 12 АПУ нанесен на металлический слой 14. В случае материала (2) получают слоистую структуру, в которой не содержащий F и Si слой АПУ расположен между слоем 12 АПУ и металлическим слоем 14 на фиг. 11.
Другой пример металлического материала для медицинского устройства по настоящему изобретению показан на фиг. 12.
Металлический материал 20 для медицинского устройства, показанный на фиг. 12, является другим примером вышеуказанного материала (1), и содержащий F и Si слой 22 АПУ, имеющий концентрацию F, постепенно увеличивающуюся со стороны, обращенной к металлическому слою 24 (то есть со стороны, прилегающей к металлическому слою), к стороне, противоположной стороне, обращенной к металлическому слою (то есть к стороне, удаленной от металлического слоя), по толщине слоя АПУ, нанесен на металлический слой 24. То есть по толщине слоя АПУ концентрация F на поверхности на стороне, противоположной стороне, прилегающей к металлическому слою, больше, чем концентрация F на поверхности на стороне, прилегающей к металлическому слою 24. В этом аспекте концентрация Si постепенно уменьшается от стороны, обращенной к металлическому слою 24, к стороне, противоположной стороне, обращенной к металлическому слою 24, по толщине слоя АПУ.
Следует отметить, что в многослойной структуре, описанной выше, «не содержащий F и Si слой АПУ», относится к слою АПУ, который может содержать другие атомы, при условии, что F и Si в нем не содержатся. «Не содержащий F и Si» означает, что содержание F и Si по отношению к общему числу атомов углерода, фтора и кремния в слое АПУ составляет менее 1,0 ат. %.
«Содержащий Si слой АПУ» относится к слою АПУ, который содержит Si и может содержать атомы, отличные от F и Si, при условии, что F в нем не содержится. «Не содержащий F» означает, что содержание F по отношению к общему числу атомов углерода, фтора и кремния в слое АПУ составляет менее 1,0 ат. %.
Примеры «промежуточного слоя, отличающегося от слоя АПУ», включают слой, содержащий карбид кремния (SiC), карбид титана (TiC), карбид хрома (Cr3C2), карбид титана и кремния (Ti3SiC2) и т.п.
Применение металлического материала для медицинского устройства по настоящему изобретению не ограничено особым образом.
Примеры применения металлического материала для медицинского устройства включают стенты, катетеры, эндоскопы и фиксирующие устройства, такие как болты и винты.
Стент подходит в качестве стента для кровеносного сосуда. Стент относится к медицинскому устройству, которое расширяет трубчатую часть (например, кровеносный сосуд) человеческого тела изнутри просвета. Стент в качестве металлического материала для медицинского устройства по настоящему изобретению используют для системного кровеносного сосуда человеческого тела (стент для системного кровеносного сосуда), и он подходит для применения в кровеносном сосуде, таком как церебральный кровеносный сосуд, легочный кровеносный сосуд, кровеносный сосуд сердечно-сосудистой системы (например, коронарная артерия), магистральный кровеносный сосуд (например, верхняя брыжеечная артерия, общая печеночная артерия) и кровеносный сосуд нижней конечности (например, вена нижней конечности).
Среди перечисленного металлический материал для медицинского устройства по настоящему изобретению предпочтительно применяют в кровеносном сосуде, совершающем много движений, таких как изгиб, растяжение и кручение, с точки зрения более эффективного проявления эффекта, и предпочтительно его используют, например, в качестве стента для кровеносного сосуда сердечно-сосудистой системы или кровеносного сосуда нижней конечности.
Способ изготовления металлического материала для медицинского устройства
Способ изготовления металлического материала для медицинского устройства по настоящему изобретению включает стадию (далее стадия формирования слоя АПУ) формирования алмазоподобного углеродного слоя (слоя АПУ), содержащего фтор и кремний, на металлическом слое с помощью способа выращивания из паровой фазы с использованием смешанного исходного материала, полученного путем смешивания силанового соединения и фторсодержащего алифатического углеводорода в качестве исходных материалов. Способ изготовления металлического материала для медицинского устройства по настоящему изобретению может дополнительно включать другие стадии, при необходимости.
Стадия формирования слоя АПУ
На стадии формирования слоя АПУ в настоящем изобретении слой алмазоподобного углерода, содержащий фтор и кремний, формируют на металлическом слое посредством осаждения из паровой фазы, способом выращивания из паровой фазы с использованием смешанного исходного материала, полученного путем смешивания силанового соединения и фторсодержащего алифатического углеводорода.
Способ выращивания из паровой фазы включает способ химического осаждения из паровой фазы (способ ХПО), способ физического осаждения из паровой фазы (способ ФПО) и т.п.
Примеры способа ХПО включают способ усиленного плазмой химического осаждения из паровой фазы (способ УП-ХПО) и способ термического химического осаждения из паровой фазы. Тонкая пленка, содержащая F, Si и С, может быть сформирована путем синтеза тонкой пленки с использованием способа УП-ХПО.
Способ УП-ХПО представляет собой тип способа химического осаждения из паровой фазы (ХПО), в котором используют газ в качестве исходного материала, и представляет собой способ, в котором газообразный исходный материал вводят в вакуумный сосуд, и генерируют плазму, вызывающую химическую реакцию, тем самым осаждая пленку. Способ ХПО представляет собой общий термин для способа осаждения пленки на основу с использованием химической реакции.
В качестве источника энергии для осуществления химической реакции используют тепло, плазму, лазер и т.п. В способе ХПО в качестве исходного материала используют газ. Следовательно, качество пленки, которая может быть сформирована, можно свободно изменять путем подбора газообразного исходного материала, и по желанию можно добавлять различные элементы.
В настоящем изобретении слой АПУ может быть подходящим образом сформирован способом ХПО. В результате условия формирования пленки (например, различные параметры) можно регулировать по желанию, и они подходят для формирования слоя АПУ, в котором концентрация F и концентрация Si изменяются по толщине слоя АПУ.
В способе УП-ХПО газообразный углеводород или газ, содержащий добавляемый элемент, направляют в качестве газообразного исходного материала в вакуумный сосуд, и генерируют плазму, вызывающую химическую реакцию, осаждая при этом пленку. В качестве энергии для генерирования плазмы подходящим образом используют мощность постоянного тока и мощность переменного тока, такую как высокочастотная и микроволновая. В способе УП-ХПО химические вещества, имеющие высокую степень активации, могут реагировать с использованием плазмы, и реакцию можно проводить при низкой температуре.
Слой АПУ в настоящем изобретении может быть сформирован с использованием устройства для химического осаждения из паровой фазы с высокочастотной индуктивно связанной плазмой (ИСП-ХПО), используя высокую частоту. В качестве устройства ИСП-ХПО можно использовать, например, YH-100NX производства ONWARD GIKEN Co., Ltd.
В устройстве ИСП-ХПО плазму генерируют между кольцеобразными электродами посредством высокочастотного разряда, и напряжение смещения прикладывают к фиксирующему приспособлению, на которое помещают основу, так что адсорбируются ионизированные или возбужденные химические частицы для осаждения и образования пленки. В качестве условий формирования пленки можно регулировать такие параметры, как время обработки, высокочастотный выход, напряжение смещения, расход газообразного исходного материала, амплитуда высокочастотного импульса, амплитуда импульса смещения и высокочастотное напряжение, напряжение смещения и расход газообразного исходного материала во время воспламенения плазмы.
Примеры способа ФПО включают способ плазменной ионной имплантации, способ вакуумного осаждения из паровой фазы и способ напыления.
В качестве исходного матриала используют смешанный исходный материал, полученный путем смешивания силанового соединения и фторсодержащего алифатического углеводорода.
В качестве силанового соединения кремнийорганическое соединение, содержащее углерод, является предпочтительным. Примеры кремнийорганического соединения включают соединение, представленное следующей формулой S.

В формуле S каждый из R представляет собой алкильную группу, содержащую от 1 до 4 атомов углерода, а х представляет собой целое число от 1 до 4.
Примеры соединения, представленного формулой S, включают тетраметилсилан, тетраэтилсилан, триметилсилан, диэтилсилан, метилдиэтилсилан и диэтилдиметилсилан.
В качестве фторсодержащего алифатического углеводорода фторсодержащий алифатический углеводород, содержащий от 1 до 4 атомов углерода, является предпочтительным и более предпочтительным является перфторуглеводород, содержащий от 1 до 4 атомов углерода. Примеры фторсодержащих алифатических углеводородов включают тетрафторметан (CF4), гексафторэтан (C2F6), октафторпропан и перфторбутан (C4F10).
В качестве исходного материала дополнительно можно использовать углеводород.
В случае способа ХПО насыщенный углеводород (например, метан (CH4), этан (С2Н6) и т.п.), ненасыщенный углеводород (например, ацетилен (С2Н2), бензол (С6Н6) и т.п.) или тому подобное можно использовать в качестве углеводорода.
В случае способа ФПО в качестве углеводорода можно использовать твердый углерод.
На стадии формирования слоя АПУ силановое соединение испаряется, и испаренное силановое соединение и фторсодержащий алифатический углеводород (могут быть добавлены ненасыщенные углеводороды) вводят в камеру для формирования пленки. В это время предпочтительно регулировать и постепенно изменять парциальное давление силанового соединения и фторсодержащего алифатического углеводорода. Смешанный исходный материал, состоящий из силанового соединения и фторсодержащего алифатического углеводорода, может образовывать слой АПУ в настоящем изобретении путем регулирования и смешивания силанового соединения и фторсодержащего алифатического углеводорода в произвольном соотношении. Например, это может быть выполнено следующим образом.
Так, силановое соединение и фторсодержащий алифатический углеводород сначала подают на поверхность металлического слоя при содержании в смеси силанового соединения ≥ содержанию в смеси фторсодержащего алифатического углеводорода и адсорбируют и осаждают. В начале формирования пленки можно использовать только силановое соединение без использования смешанного материала. Затем пленку непрерывно формируют посредством адсорбции и осаждения при уменьшении (предпочтительно постепенном уменьшении) содержания в смеси силанового соединения и увеличении (предпочтительно постепенном увеличении) содержания в смеси фторсодержащего алифатического углеводорода.
При формировании пленки таким образом получают слой АПУ, который имеет распределение состава, при котором количество F увеличивается (предпочтительно, количество F постепенно увеличивается) и количество Si уменьшается (предпочтительно, количество Si постепенно уменьшается) в направлении осаждения (по толщине осаждаемого слоя) от стороны металлического слоя.
Другие стадии
В случае, когда основу используют в качестве металлического слоя, способ изготовления металлического материала для медицинского устройства по настоящему изобретению может включать стадию травления основы в качестве еще одной стадии. Путем травления адгезия к слою АПУ может быть дополнительно улучшена.
В качестве способа травления можно использовать способ сухого травления, такой как способ травления ионным пучком или способ плазменного травления.
Примеры газа, используемого для травления, включают инертные газы (примеры: гелий (Не), неон (Ne), аргон (Ar), криптон (Kr) и ксенон (Хе)), газ на основе галогена, содержащий атом галогена (примеры: CCl4, CClF3, AlF3 и AlCl3), О2, N2, СО и СО2.
Газ можно использовать по отдельности, или он может представлять собой смесь двух или более газов.
Стадия травления предпочтительно представляет собой стадию плазменного травления поверхности подложки.
Способ изготовления металлического материала для медицинского устройства по настоящему изобретению может включать стадию дополнительного формирования слоя покрытия, содержащего лекарственное средство, на слое АПУ в качестве еще одной стадии.
Слой, высвобождающий лекарственное средство (например, полимерный слой, включающий лекарственное средство и полимер), содержащий целевое лекарственное средство, может быть обеспечен по меньшей мере на части слоя АПУ. Это позволяет придать функцию высвобождения лекарственного средства, при этом обеспечивая превосходное следование движению и гибкость, как описано выше.
Лекарственное средство можно выбирать в соответствии с такой целью, как уничтожение клетки-мишени.
Медицинское устройство
Медицинское устройство по настоящему изобретению включает вышеуказанный металлический материал для медицинского устройства по настоящему изобретению.
Примеры медицинского устройства по настоящему изобретению включают стент, катетер, эндоскоп, фиксирующее устройство, такое как болт или винт, искусственное сердце, искусственный тазобедренный сустав и фиксирующую пластину. Медицинское устройство по настоящему изобретению подходит в качестве стента, подходит в качестве стента, используемого для системного кровеносного сосуда человеческого тела, и больше подходит в качестве стента, используемого для кровеносного сосуда нижней конечности, церебрального кровеносного сосуда, легочного кровеносного сосуда, кровеносного сосуда сердечно-сосудистой системы или магистрального кровеносного сосуда.
Нижняя конечность относится ко всей ноге от тазобедренного сустава до кончика пальца и включает три основных сустава: тазобедренный сустав, коленный сустав, голеностопный сустав и часть пальца ноги.
Примеры
Далее настоящее изобретение описано более конкретно со ссылкой на примеры, но настоящее изобретение не ограничивается нижеследующими примерами, если только они не выходят за рамки сущности настоящего изобретения.
Пример 1
1. Получение основы (металлического слоя)
В качестве основы были получены основа из сплава NiTi и основа из кремния (Si) для анализа химического состава и оценки адгезии. Кроме того, для оценки совместимости с кровью была получена основа из сплава NiTi. Кроме того, для оценки способности следования с использованием основы, принимаемой в качестве стента, была получена проволока NiTi. Толщина основы 380 мкм, диаметр проволоки 150 мкм.
2. Получение газообразного исходного материала
В качестве исходного материала для получения газообразного исходного материала были получены следующие соединения.
Силановое соединение: тетраметилсилан (Si(CH3)4)
Фторсодержащее алифатическое соединение: октафторпропан (C3F8)
3. Формирование слоя АПУ
Слой АПУ, содержащий F и Si, формировали на основе или проволоке в соответствии со следующей процедурой.
(1) Обработка травлением
Сначала для улучшения адгезии поверхности основы поверхность каждой основы подвергали поверхностной обработке путем плазменного травления при следующих условиях.
Условия травления
Устройство для травления: YH-100NX (производства ONWARD GIKEN Co., Ltd.)
Газ для травления: газообразный аргон (Ar)
Время травления: от 10 до 1000 секунд
Расход газа: 10 мл/мин.
(2) Формирование пленки
Было подготовлено устройство YH-100NX для осаждения из паровой фазы с высокочастотной индуктивно связанной плазмой (ИСП-ХПО) производства ONWARD GIKEN Co., Ltd., и каждую основу последовательно размещали внутри его камеры. Испаренный тетраметилсилан (ТМС; соединение силана) и октафторпропан (ОФП/называемый также октафторид пропана; фторсодержащий алифатический углеводород) вводили для формирования пленки на поверхности каждой основы.
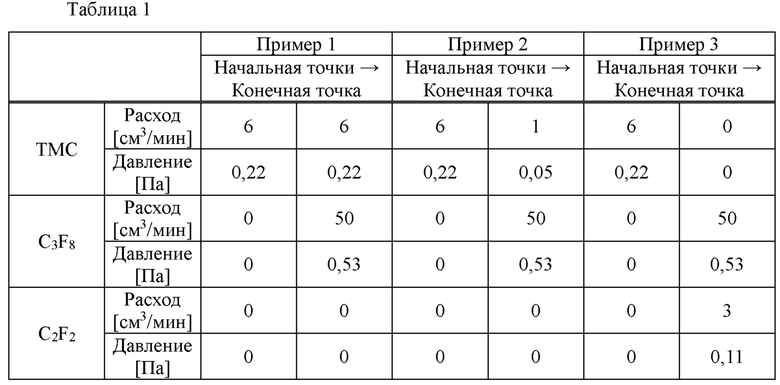
Формирование пленки осуществляли, регулируя парциальное давление PSi ТМС и парциальное давление PF ОФП, вводимых в камеру. В частности, как показано в таблице 1, ТМС сначала вводили при расходе 6 см3/мин (PSi: 0,22 Па), а ОФП вводили путем постепенного увеличения расхода до 50 см3/мин (PF: 0,53 Па) при поддержании расхода ТМС.
Как описано выше, был получен медицинский материал (металлический материал для медицинского устройства), в котором на основе или проволоке был сформирован слой АПУ толщиной 200 нм. Элементный состав углерода, фтора и кремния в слое АПУ измеряли следующим методом.
4. Измерения и оценка
Для слоя АПУ, сформированного на основе или проволоке, проводили следующие измерения и оценки.
1. Концентрация F и концентрация Si
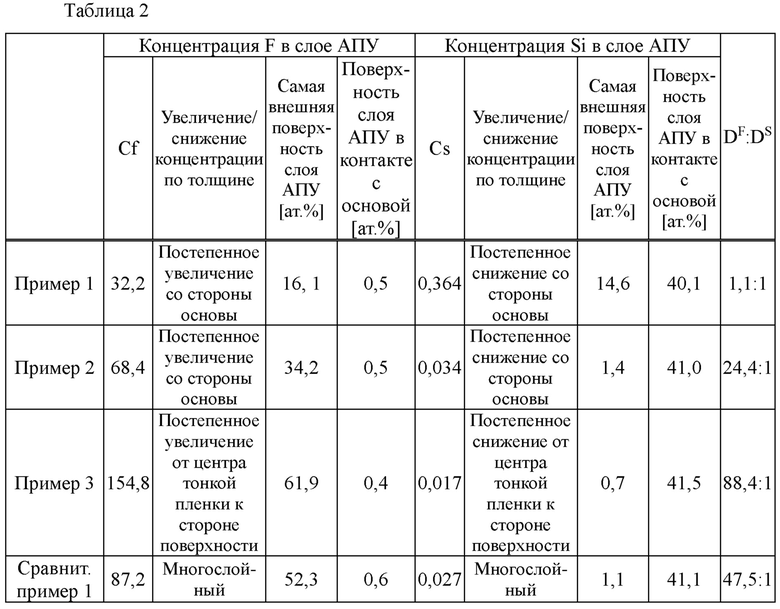
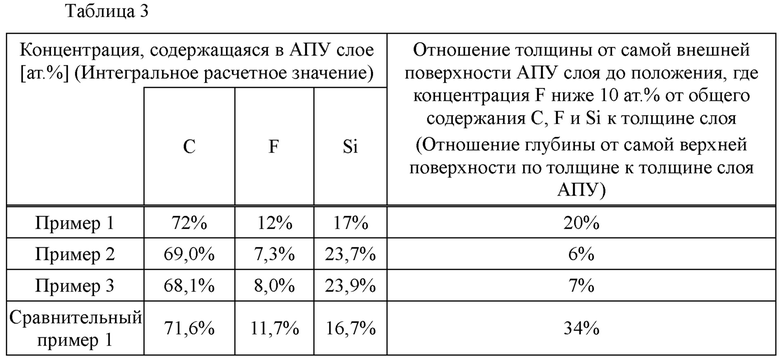
Концентрацию F и концентрацию Si определяли путем проведения анализа химического состава следующим методом с использованием образца для испытаний, в котором слой АПУ был сформирован на основе из Si или основе из сплава NiTi. Результаты измерений представлены в таблицах 2 и 3.
С помощью устройства для РФС (JPS-9010TR производства JEOL Ltd.) содержание элементов (содержание С, F, Si и О) определяли по спектру, измеренному на внешней поверхности слоя АПУ и на поверхности слоя АПУ, находящегося в контакте с основой и по толщине слоя АПУ. Следует отметить, что самой внешней поверхностью слоя АПУ является поверхность слоя АПУ на стороне, противоположной стороне, контактирующей с основой.
Конкретные операции заключаются в следующем.
a) MgKα использовали в качестве источника рентгеновского излучения, и анализ С, F, Si и О на каждой поверхности необработанного слоя АПУ, сформированного на каждой основе, проводили в условиях генерирования рентгеновского излучения 10 кВ и 10 мА.
b) Затем каждую поверхность слоя АПУ подвергали травлению в течение 10 секунд с использованием кластерного ионного пучка газообразного Ar.
c) С, F, Si и О внутри слоя АПУ, протравленного на вышеуказанной стадии (b), анализировали таким же образом, как и на вышеуказанной стадии (а).
d) Содержание элементов на поверхности и внутри слоя АПУ определяли по спектрам, полученным в ходе соответствующих измерений. Содержание элементов рассчитывали методом корреляции коэффициента чувствительности по площади спектра каждого элемента, полученного при измерении.
Следует отметить, что содержание элементов на поверхности слоя АПУ, контактирующей с основой, и содержание элементов по толщине слоя АПУ определяли путем измерения внутренней части слоя посредством травления слоя АПУ. Содержание элементов по толщине слоя АПУ определяли путем травления слоя АПУ с заданными интервалами по толщине, измерения распределения элементов по толщине внутри слоя и в направлении плоскости, параллельной самой внешней поверхности, и выполнения интегрального расчета количества углерода, фтора и кремния от самой внешней поверхности по толщине в слое АПУ.
Кроме того, при измерении распределения элементов на самой внешней поверхности слоя АПУ и по толщине слоя АПУ использовали слой АПУ, сформированный с использованием кремниевой (Si) основы в качестве основы. При измерении на поверхности слоя АПУ, находящейся в контакте с основой, использовали слой АПУ, сформированный с использованием основы из сплава NiTi в качестве основы.
2. Адгезия
Адгезию слоя АПУ к основе из сплава NiTi оценивали с помощью испытания нанесением царапин. В частности, критическая нагрузка на отслаивание слоя АПУ была получена 5 раз в соответствии с нижеследующей процедурой с использованием тестера с нанесением нано-царапин (CSR5000 производства RHESCA CORPORATION), и среднее значение из 5 раз рассчитывали как показатель для оценки адгезии. Результаты оценки представлены в таблице 4 и на фиг. 9.
Методика проведения испытания
1) Используя алмазный индентор с диаметром наконечника ϕ 5 мкм, сканировали поверхность слоя АПУ, сформированного на основе из сплава NiTi, при следующих условиях.
Условия испытаний
Максимальная нагрузка: 100 мН
Скорость приложения нагрузки: 1,67 мН/с
Длина царапины: 600 мкм
Количество испытаний: 5 раз
(2) Измеряли начальную точку отслаивания слоя АПУ, возникающего во время сканирования, и рассчитывали критическую нагрузку отслаивания.
(3) На основании результатов по критической нагрузке отслаивания была проведена оценка в соответствии со следующими критериями оценки.
Критерии оценки
А: Продемонстрирована особенно превосходная адгезия.
В: Адгезия проявлялась до такой степени, что не затруднялось практическое использование.
С: Плохая адгезия.
3. Способность к следованию
Способность слоя АПУ к следованию деформации NiTi проволоки оценивали с помощью наблюдения под электронным микроскопом. В частности, в качестве испытуемого образца использовали образец с наиболее легко деформируемым слоем АПУ, сформированным на NiTi проволоке, и этот испытуемый образец изгибали под углом изгиба 120°. Затем испытуемый образец в изогнутом состоянии наблюдали с помощью сканирующего электронного микроскопа (СЭМ) и оценивали способность слоя АПУ к следованию в состоянии, деформированном изгибом, в соответствии со следующими критериями оценки. Результаты оценки представлены в таблице 4.
Критерии оценки
А: Продемонстрированы высокая гибкость и особенно превосходная способность к следованию.
В: Гибкость была немного недостаточной и не наблюдалось отслаивания слоя АПУ, но в слое АПУ наблюдались трещины.
С: Плохая гибкость и в слое АПУ наблюдался отслоившийся участок.
4. Совместимость с кровью
К основе из сплава NiTi или основе со слоем АПУ, где слой АПУ сформирован на основе из сплава NiTi, полученным в качестве образцов, прикрепляли тромбоциты и проводили испытание на адгезию тромбоцитов для оценки антитромбогенности образца, чтобы оценить совместимость с кровью. Поскольку основной причиной образования тромбов на биологическом материале в кровеносном сосуде является свертывание крови, вызванное характеристикой поверхности материала, называемой внутренним фактором свертывания крови, можно сказать, что совместимость с кровью тем выше, чем меньше количество прикрепленных тромбоцитов.
Испытание проводили по следующей методике с использованием основы из сплава NiTi и основы со слоем АПУ. Результаты представлены в таблице 4.
Методика проведения испытания
1) Обогащенную тромбоцитами плазму (ОТП), выделенную из крови здорового взрослого человека, капали и наносили в количестве 1 мл на каждую из основы из сплава NiTi и основы со слоем АПУ, где слой АПУ сформирован на основе из сплава NiTi, и выдерживали в условиях 37°С и парциальном давлении СО2 5% в атмосфере в течение 60 минут с использованием СО2-инкубатора.
Обогащенная тромбоцитами плазма (ОТП) представляет собой раствор богатой тромбоцитами крови, отделенный от крови.
2) После инкубации кровь на основе из сплава NiTi или образце осторожно отсасывали и промывали физиологическим раствором.
3) После обезвоживания и фиксации тромбоцитов, прилипших к поверхности основы из сплава NiTi или к поверхности слоя АПУ основы со слоем АПУ, тромбоциты, прилипшие к поверхности основы из сплава NiTi или к поверхности слоя АПУ основы со слоем АПУ, наблюдали с помощью дифференциального интерференционного микроскопа, который представлял собой вид оптического микроскопа.
4) Состояние адгезии тромбоцитов, наблюдаемое на микрофотографии, оценивали в соответствии со следующими критериями оценки.
Критерии оценки
А: Адгезия тромбоцитов чрезвычайно мала.
В: Наблюдается адгезия тромбоцитов.
С: Наблюдается заметная адгезия тромбоцитов.
Пример 2
Слой АПУ формировали так же, как в примере 1, за исключением того, что формирование пленки осуществляли путем регулирования парциального давления PSi ТМС и парциального давления PF ОФП, вводимых в камеру, таким образом, чтобы соотношение содержания фтора и кремния изменялось по толщине слоя АПУ, как показано в таблице 1, и далее выполняли измерения и оценку. В частности, образование пленки выполняли, сначала вводя ТМС при расходе 6 см3/мин (PSi: 0,22 Па) и постепенно увеличивая расход ОФП до 50 см3/мин (PF: 0,53 Па) при постепенном снижении расхода ТМС. Результаты измерения и оценки представлены в таблицах 2 и 3, а также на фиг. 9.
Пример 3
Слой АПУ формировали так же, как в примере 1, за исключением того, что формирование пленки осуществляли путем регулирования парциального давления PSi ТМС, парциального давления PF ОФП и парциального давления РС ацетилена, вводимых в камеру, таким образом, чтобы соотношение содержания углерода, фтора и кремния изменялось по толщине слоя АПУ, как показано в таблице 1, и далее проводили измерения и оценку.
В частности, формирование пленки проводили, сначала вводя ТМС при расходе 6 см3/мин (PSi: 0,22 Па) и постепенно увеличивая расход ОФП до 50 см3/мин (PF: 0,53 Па) и постепенно увеличивая расход ацетилена до 3 см3/мин (PF: 0,11 Па) при постепенном снижении расхода ТМС.
Результаты измерений и оценок представлены в таблицах 2 и 3, на фиг. 1 (фиг. 2 для сравнения), фиг. 3 и фиг. 9. На фиг. 9 белый участок, видимый в поле зрения, представляет собой области, где происходит отслаивание.
Пример 4
Слой АПУ формировали так же, как в примере 1, за исключением того, что тип основы был изменен, вместо сплава NiTi использовали сплав CoCr в примере 1, и далее проводили измерения и оценку. Результаты измерений и оценки представлены в таблице 4.
Примеры 5-7
Слой АПУ формировали так же, как и в примере 1, за исключением того, что тип основы был изменен, вместо сплава NiTi в каждом из примеров 1-3 использовали SUS316L (нержавеющую сталь), и далее проводили измерения и оценку. Результаты измерений и оценки представлены в таблице 4, на фиг. 4 (фиг. 5 для сравнения) и фиг. 10.
Сравнительный пример 1 В качестве основы получали основу из сплава NiTi так же, как в примере 1. После обработки поверхности основы путем бомбардирования аргоном в течение примерно 10 минут формировали слой SiC толщиной примерно 100 нм с использованием тетраметилсилана (ТМС) в качестве газообразного исходного материала. Затем, используя тетраметилсилан (ТМС) и ацетилен (C2H2) в качестве газообразных исходных материалов, в качестве первого слоя АПУ на поверхности слоя SiC формировали слой Si-АПУ, имеющий толщину примерно 100 нм. После этого с использованием перфторпропана (C3F8) и ацетилена (С2Н2) в качестве газообразных исходных материалов формировали фторсодержащий слой АПУ (слой F-АПУ) толщиной примерно 200 нм в качестве второго слоя АПУ на поверхности слоя Si-АПУ. Следует отметить, что при формировании слоя SiC, слоя Si-АПУ и слоя F-АПУ расход каждого газа, время реакции и т.п. регулировали соответствующим образом, чтобы получить каждый слой, имеющий вышеуказанную толщину.
Как описано выше, как показано на фиг. 13, был изготовлен стент, имеющий слоистую структуру из слоя F-АПУ, слоя Si-АПУ, слоя SiC и основы. Изготовленный стент измеряли и оценивали так же, как в примере 1. Результаты измерений и оценки показаны в таблицах 3 и 4, на фиг. 6, фиг. 8 и фиг. 9. На фиг. 8 белый участок в поле наблюдения представляет собой область, где происходит отслаивание.
Сравнительный пример 2
Измерение и оценку проводили так же, как и в сравнительном примере 1, за исключением того, что тип основы был изменен, вместо сплава NiTi в сравнительном примере 1 использовали SUS316L (нержавеющую сталь). Результаты измерений показаны на фиг. 7 и 10.
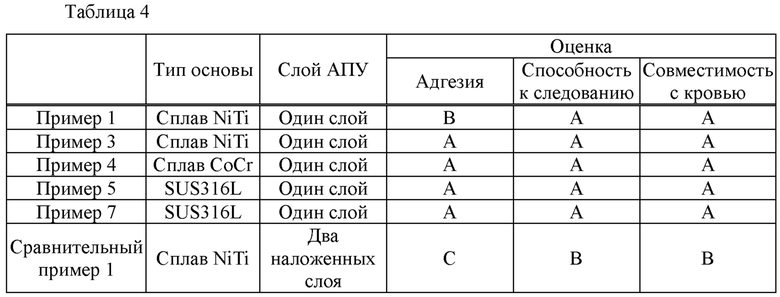
Как показано в таблице 4, в каждом из примеров, в которых концентрация фтора (F) и концентрация кремния (Si) в однослойном слое АПУ постепенно изменялись по толщине, были получены хорошие результаты в отношении адгезии, способности к следованию и совместимости с кровью по сравнению со сравнительным примером 1, имеющим многослойную структуру, включающую F и Si в отдельных слоях.
Как видно из сравнения фиг. 1 (пример 3) и фиг. 6 (сравнительный пример 1), было подтверждено, что в испытуемом образце (металлический материал для медицинского устройства) примера 3, имеющем однослойный слой АПУ на основе из сплава NiTi количество прилипших тромбоцитов было значительно снижено по сравнению со сравнительным примером 1, в котором слой АПУ имел многослойную слоистую структуру. Следует отметить, что в основе из сплава NiTi, не имеющей слоя АПУ, в качестве контрольного примера, ясно, что степень адгезии тромбоцитов является заметной, как показано на фиг. 2. Как видно из сравнения фиг. 4 (пример 7) и фиг. 7 (сравнительный пример 2), сходные результаты были получены для примера 7 и сравнительного примера 2, в которых основа из сплава NiTi была заменена на основу SUS316L (нержавеющая сталь). Кроме того, это также ясно из сравнения фиг. 4 (пример 7) и фиг. 5 (контрольный пример без слоя АПУ). То есть, как и в случае использования основы из сплава NiTi, видно, что в случае наличия однослойного слоя АПУ на основе из нержавеющей стали (испытуемый образец (металлический материал для медицинского устройства) примера 7), количество прилипших тромбоцитов значительно снижено по сравнению со случаем использования основы из нержавеющей стали, не имеющей слоя АПУ.
Кроме того, как видно из сравнения фиг. 3 (пример 3) и фиг. 8 (сравнительный пример 1), в стенте с использованием проволоки из сплава NiTi было подтверждено, что в испытуемом образце примера 3 (металлический материал для медицинского устройства), имеющем однослойный слой АПУ на проволоке из сплава NiTi, отслаивание слоя АПУ было подавлено, и способность к следованию была превосходной по сравнению со сравнительным примером 1, в котором слой АПУ имел многослойную структуру.
Что касается адгезии слоя АПУ, как показано в таблице 4 и на фиг. 9 и 10, примеры 1-3 и примеры 5-7, в которых концентрация фтора (F) и концентрация кремния (Si) в однослойном слое АПУ постепенно изменялись по толщине, были превосходными по сравнению со сравнительным примером 1 или сравнительным примером 2, каждый из которых имеет многослойную структуру, включающую F и Si в отдельных слоях.
| название | год | авторы | номер документа |
|---|---|---|---|
| Стент | 2021 |
|
RU2830414C2 |
| МЕДИЦИНСКОЕ УСТРОЙСТВО (ВАРИАНТЫ) | 2012 |
|
RU2704539C2 |
| АНТИФРИКЦИОННЫЕ ПОКРЫТИЯ С УЛУЧШЕННЫМИ СВОЙСТВАМИ АБРАЗИВНОГО ИЗНОСА И ИСТИРАНИЯ, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2653379C2 |
| МЕДИЦИНСКОЕ УСТРОЙСТВО (ВАРИАНТЫ) | 2019 |
|
RU2766742C2 |
| СОПОЛИМЕР И МЕДИЦИНСКИЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ ЕГО | 2017 |
|
RU2757274C2 |
| КОМПОЗИЦИЯ ПОКРЫТИЯ И МЕДИЦИНСКОЕ УСТРОЙСТВО | 2013 |
|
RU2605291C2 |
| Медицинское устройство с поверхностью, содержащей металл противомикробного действия | 2013 |
|
RU2651463C1 |
| Муфтовое устройство с покрытием для эксплуатации в газонефтяных скважинах | 2015 |
|
RU2608454C1 |
| АНТИТРОМБОТИЧЕСКИЙ МЕТАЛЛИЧЕСКИЙ МАТЕРИАЛ | 2016 |
|
RU2711652C2 |
| Медицинское устройство с поверхностью, содержащей оксид галлия | 2013 |
|
RU2636515C1 |



Изобретение относится к металлическому материалу для медицинского устройства, медицинскому устройству, включающему указанный металлический материал и способу изготовления металлического материала для медицинского устройства. Металлический материал для медицинского устройства включает металлический слой и слой алмазоподобного углерода, расположенный на металлическом слое и содержащий фтор и кремний. В изобретении рассматривается медицинское устройство, такое как стент, в частности стент для кровеносного сосуда нижней конечности с использованием вышеуказанного материала. Способ включает формирование слоя алмазоподобного углерода, содержащего фтор и кремний, на металлическом слое посредством осаждения из паровой фазы, способом выращивания из паровой фазы с использованием смешанного исходного материала, полученного путем смешивания силанового соединения и фторсодержащего алифатического углеводорода в качестве исходных материалов. Изобретение обеспечивает получение медицинского материала для медицинского устройства, обладающего способностью следовать за движением живого организма и гибкостью для гибкого деформирования под действием различных напряжений во время следования. 3 н. и 16 з.п. ф-лы, 13 ил., 4 табл.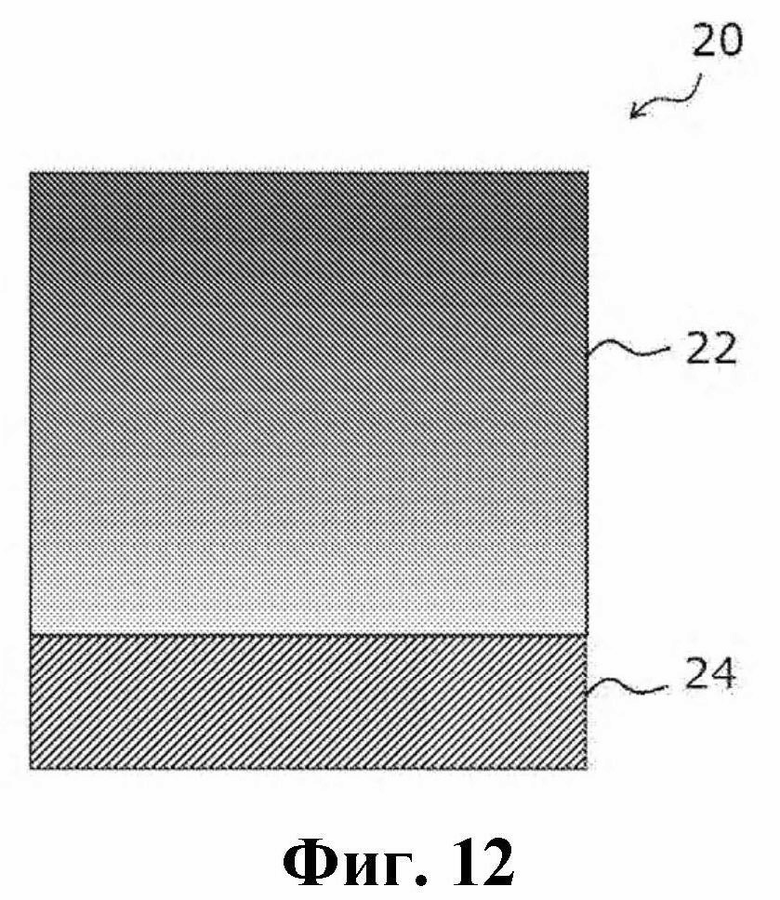
1. Металлический материал для медицинского устройства, включающий:
металлический слой и
слой алмазоподобного углерода, нанесенный на металлический слой и содержащий фтор и кремний.
2. Металлический материал для медицинского устройства по п. 1, в котором общая концентрация фтора, содержащегося в слое алмазоподобного углерода, составляет от 7 до 10 ат. % по отношению к общей концентрации углерода, фтора и кремния.
3. Металлический материал для медицинского устройства по п. 1, в котором общая концентрация кремния, содержащегося в слое алмазоподобного углерода, составляет от 17 до 25 ат. % по отношению к общей концентрации углерода, фтора и кремния.
4. Металлический материал для медицинского устройства по п. 1, в котором в слое алмазоподобного углерода концентрация фтора на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, больше, чем концентрация фтора на поверхности на стороне, обращенной к металлическому слою, по толщине слоя алмазоподобного углерода.
5. Металлический материал для медицинского устройства по п. 4, в котором в слое алмазоподобного углерода отношение Cf концентрации фтора на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, к концентрации фтора на поверхности на стороне, обращенной к металлическому слою, удовлетворяет соотношению 1<Cf≤155.
6. Металлический материал для медицинского устройства по п. 4, в котором концентрация фтора, содержащегося в слое алмазоподобного углерода, постепенно увеличивается от стороны, обращенной к металлическому слою, к стороне, противоположной стороне, обращенной к металлическому слою, по толщине слоя алмазоподобного углерода.
7. Металлический материал для медицинского устройства по п. 1, в котором в слое алмазоподобного углерода концентрация кремния на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, меньше, чем концентрация кремния на поверхности на стороне, обращенной к металлическому слою, по толщине слоя алмазоподобного углерода.
8. Металлический материал для медицинского устройства по п. 7, в котором в слое алмазоподобного углерода отношение Cs концентрации кремния на поверхности на стороне, противоположной стороне, обращенной к металлическому слою, к концентрации кремния на поверхности на стороне, обращенной к металлическому слою, удовлетворяет соотношению 0,015≤Cs<1.
9. Металлический материал для медицинского устройства по п. 7, в котором концентрация кремния, содержащегося в слое алмазоподобного углерода, постепенно уменьшается от стороны, обращенной к металлическому слою, к стороне, противоположной стороне, обращенной к металлическому слою, по толщине слоя алмазоподобного углерода.
10. Металлический материал для медицинского устройства по п. 1, в котором отношение (DF:DS) концентрации DF фтора к концентрации DS кремния на поверхности слоя алмазоподобного углерода на стороне, противоположной стороне, обращенной к металлическому слою, составляет от 1:1 до 90:1.
11. Металлический материал для медицинского устройства по п. 1, в котором слой алмазоподобного углерода расположен в качестве самого внешнего слоя на металлическом слое.
12. Металлический материал для медицинского устройства по п. 1, в котором металлический слой содержит по меньшей мере один металл, выбранный из группы, состоящей из титана, никеля, кобальта, хрома, тантала, платины, золота, их сплавов и нержавеющей стали.
13. Металлический материал для медицинского устройства по п. 12, в котором металлический слой содержит никель-титановый сплав, кобальт-хромовый сплав или нержавеющую сталь.
14. Металлический материал для медицинского устройства по п. 1, который используют в стенте.
15. Металлический материал для медицинского устройства по п. 14, где стент представляет собой стент для системного кровеносного сосуда.
16. Медицинское устройство, включающее металлический материал для медицинского устройства по любому из пп. 1-15.
17. Медицинское устройство по п. 16, представляющее собой стент.
18. Медицинское устройство по п. 17, где стент представляет собой стент для кровеносного сосуда нижней конечности.
19. Способ изготовления металлического материала для медицинского изделия, включающий формирование слоя алмазоподобного углерода, содержащего фтор и кремний, на металлическом слое посредством осаждения из паровой фазы, способом выращивания из паровой фазы с использованием смешанного исходного материала, полученного путем смешивания силанового соединения и фторсодержащего алифатического углеводорода в качестве исходных материалов.
| D.W.REN, Q.ZHAO, Anti-bacterial property of Si and F doped diamond-like carbon coatings | |||
| Surface and Coatings Technology, 15 July 2013 | |||
| JP 2001029447 A 06.02.2001 | |||
| JP 2012041629 A, 01.03.2012 | |||
| US 8900291 B2, 02.12 | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| US 6572651 B1, 03.06.2003 | |||
| US 8435287 B2, 07.05.2013 | |||
| CN 107502860 A, 22.12.2017 | |||
| Стент повышенной гибкости | 2014 |
|
RU2635474C1 |
Авторы
Даты
2023-12-05—Публикация
2020-11-09—Подача