Область техники, к которой относится изобретение
Настоящее изобретение относится к способам предотвращения или лечения нарушений метаболизма глюкозы и, в частности, относится к способам долгосрочного предотвращения или лечения нарушений метаболизма глюкозы путем введения нуждающемуся в этом субъекту бета-лактамного соединения или его фармацевтически приемлемой соли.
Уровень техники
Энергия необходима для нормального функционирования органов тела. Многие ткани используют жир или белок в качестве источника энергии, но другие, такие как головной мозг и эритроциты, используют только глюкозу. Следовательно, глюкоза является наиболее важным источником клеточной энергии, и, следовательно, ее метаболизм строго регулируется.
Высокий уровень глюкозы в крови стимулирует секрецию инсулина, который вырабатывается бета-клетками поджелудочной железы. Инсулин, секретируемый в кровь, активирует поглощение глюкозы мышцами и жировыми клетками, что приводит к накоплению гликогена и триглицеридов и синтезу белков, и, таким образом, уровень глюкозы в крови поддерживается на должном уровне. Нарушения этой регуляторной сети могут привести к диабету и связанным с ним синдромам.
Нарушения метаболизма глюкозы могут привести к гипергликемии, гиперинсулинемии или непереносимости глюкозы. Примером патологии, которая часто связана с аберрантным уровнем глюкозы, является инсулинорезистентность, при которой печеночные, жировые и мышечные клетки теряют способность реагировать на нормальный уровень инсулина в крови. Ожирение и инсулинорезистентность имеют сложную взаимосвязь, которая приводит к развитию различных типов метаболических нарушений, таких как диабет 2 типа. Триглицериды, накопленные в адипоцитах, и свободные жирные кислоты, выделяемые этими клетками, являются предшественниками холестерина, которые играют важную роль в развитии и прогрессировании диабета и связанных с ним нарушений.
Считается, что пациенты имеют нарушения метаболизма, предшествующие диабету, в течение определенного периода времени до окончательного клинического диагноза диабета. Нарушенная гликемия натощак (НГН, 100-126 мг/дл) и нарушенная толерантность к глюкозе (НТГ, 140-200 мг/дл) являются двумя основными тестами для диагностики преддиабета. Уровень глюкозы в крови у людей с преддиабетом выше нормы, но недостаточно высок, чтобы считаться диабетом. Преддиабет несет в себе более высокий риск развития диабета в будущем, а также сердечных заболеваний. Преддиабет можно контролировать с помощью диеты и физических упражнений; например, снижение массы тела на 5-10% с помощью диеты и физических упражнений может значительно снизить риск развития диабета в будущем. Также может потребоваться медицинское вмешательство, чтобы преддиабетическое состояние не переросло в диабет.
Для поддержания уровня глюкозы в крови на постоянном уровне в течение дня, например, до и после еды, а также во время сна с продолжительным голоданием, используются лекарства с различным началом, пиком и продолжительностью лечебного воздействия. Например, по данным Управления по контролю качества пищевых продуктов и лекарственных препаратов США (FDA), существует четыре типа лечения инсулином, включающие в себя (i) инсулин быстрого действия, который начинает действовать всего через 15 минут после приема и достигает пика в течение 30-90 минут, его действие длится в течение трех-пяти часов, (ii) инсулин короткого действия, который активируется примерно через 30-60 минут и достигает пика через два-четыре часа, его действие длится от пяти до восьми часов, (iii) инсулин средней продолжительности действия, который начинает функционировать через один - три часа и достигает пика через восемь часов при продолжительности действия на этом уровне от 12 до 16 часов, и (iv) инсулин длительного действия, которому требуется больше всего времени для начала функционирования, но его действие может продолжаться до 24 часов.
Несмотря на множество вариантов лечения, лечение нарушений метаболизма глюкозы по-прежнему представляет собой проблему. Пациенты не всегда достигают своих целевых показателей гликемии, и соблюдение плана лечения, основанного на частом введении дозы и дозировании в зависимости от приема пищи, оставляет место для человеческой ошибки. Лечение с длительным действием предпочтительнее, потому что количество инъекций при лечении для контроля уровня глюкозы меньше, что улучшает качество жизни пациентов и их приверженность лечению. Однако в настоящее время инсулин с самым продолжительным действием имеет период действия 42 часа и по-прежнему требует ежедневных инъекций.
Следовательно, все еще существует неудовлетворенная потребность в композициях и способах, пригодных для терапии нарушений метаболизма глюкозы длительного действия.
Сущность изобретения
Ввиду вышеизложенного настоящее изобретение относится к бета-лактамному соединению или его фармацевтически приемлемой соли, которое может предотвращать или лечить нарушение метаболизма глюкозы с эффектом длительного действия.
В одном варианте осуществления настоящее изобретение относится к способу долгосрочного предотвращения или лечения нарушений метаболизма глюкозы у нуждающегося в этом субъекта. Данный способ включает в себя введение субъекту эффективного количества бета-лактамного соединения или его фармацевтически приемлемой соли.
В одном варианте осуществления настоящего изобретения бета-лактамное соединение для применения в долгосрочном предотвращении или лечении нарушения метаболизма глюкозы представляет собой соединение, представленное формулой (I), или его фармацевтически приемлемую соль:
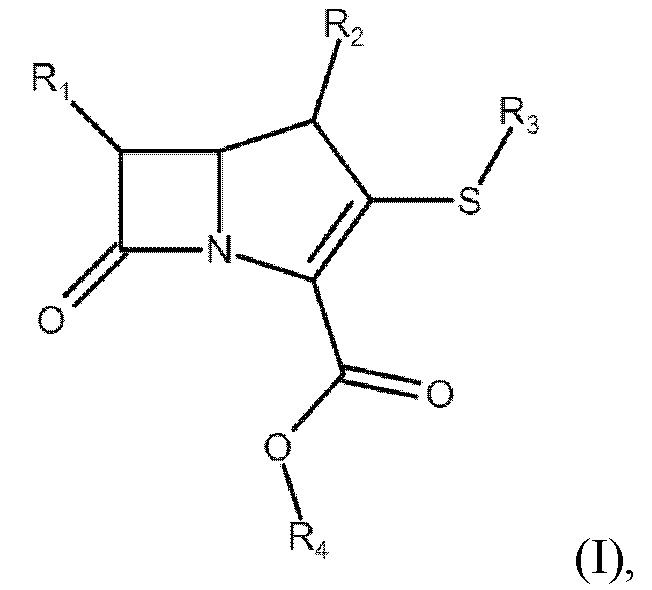
где:
R1 и R3 независимо представляют собой H или замещенную или незамещенную группу, выбранную из группы, состоящей из алкила, алкенила, алкинила, гидроксиалкила, фторалкила, хлоралкила, бромалкила, йодоалкила, перфторалкила, арила, гетероарила, циклоалкила, циклоалкенила, карбоксила, аралкила, аралкенила, аралкинила, гетероаралкила, гетероаралкенил, гетероаралкинила, гетероциклила, ацила, бензила, фенила, аминокарбонила, аминоалкила, амино, гидроксила, алкокси, ацилокси, силилокси, амидо, имидоила, карбамоила, галогена, тио, тиоэфира, сульфо, сульфонола, сульфамоила, тиазолила, тиазолидинила, пирролила, пирролидинила, триазолила, азетидинила и сульфонамидо;
R2 представляет собой H или (C1-C6)-алкил; и
R4 представляет собой H или (C1-C6)-алкил, или щелочной металл, или щелочноземельный металл, где щелочной металл или щелочноземельный металл представляет собой натрий, калий, литий, цезий, рубидий, барий, кальций или магний.
В одном варианте осуществления настоящего изобретения соединение формулы (I) может представлять собой соединение, представленное нижеприведенной формулой (II):
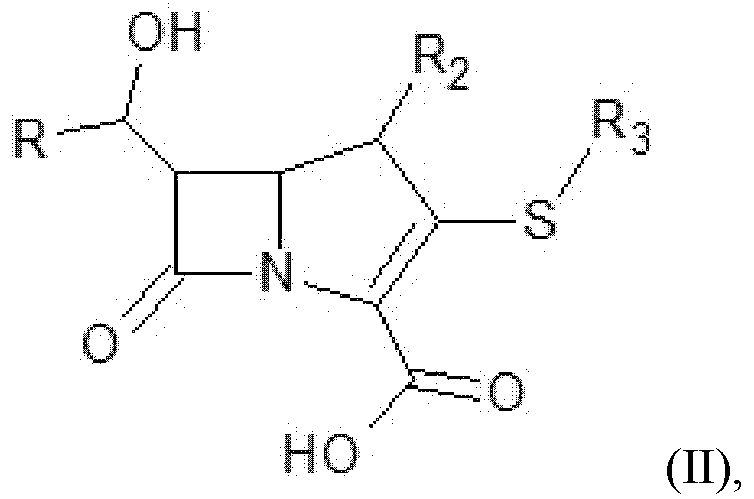
где R определен как R1 выше, и R2 и R3 имеют значения, определенные выше.
В одном варианте осуществления настоящего изобретения в формуле (I) или (II) R3 может быть представлен одной из приведенных ниже формул (I-a) - (I-l):


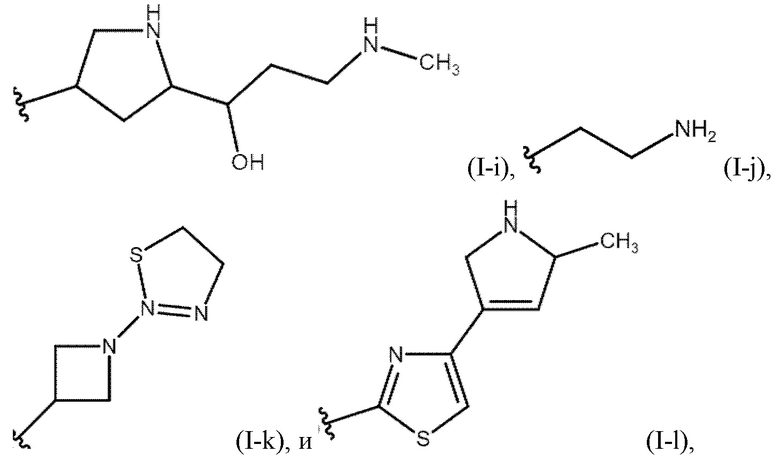
где:
R9 и R13 независимо представляют собой H или (C1-C6)-алкил, или щелочной металл, или щелочноземельный металл, где щелочной металл или щелочноземельный металл представляет собой натрий, калий, литий, цезий, рубидий, барий, кальций или магний;
R10 и R11 независимо представляют собой H, галоген, циано, (C1-C6)-алкил, нитро, гидрокси, карбокси, (C1-C6)-алкокси, (C1-C6)-алкоксикарбонил, аминосульфонил, (C1-C6)-алкиламиносульфонил, ди-(C1-C6)-алкиламиносульфонил, карбамоил, (C1-C6)-алкилкарбамоил, ди-(C1-C6)-алкилкарбамоил, трифторметил, сульфоновую кислоту, амино, (C1-C6)-алкиламино, ди-(C1-C6)-алкиламино, (C1-C6)-алканоиламино, (C1-C6)-алканоил(N-(C1-C6)-алкил)амино, (C1-C6)-алкансульфонамидо или (C1-C6)-алкил-S(O)n, где n равно от 0 до 2; и
R12 представляет собой H или (C1-C6)-алкил.
В одном варианте осуществления настоящего изобретение соединение формулы (II) может представлять собой соединение, представленное следующей формулой:
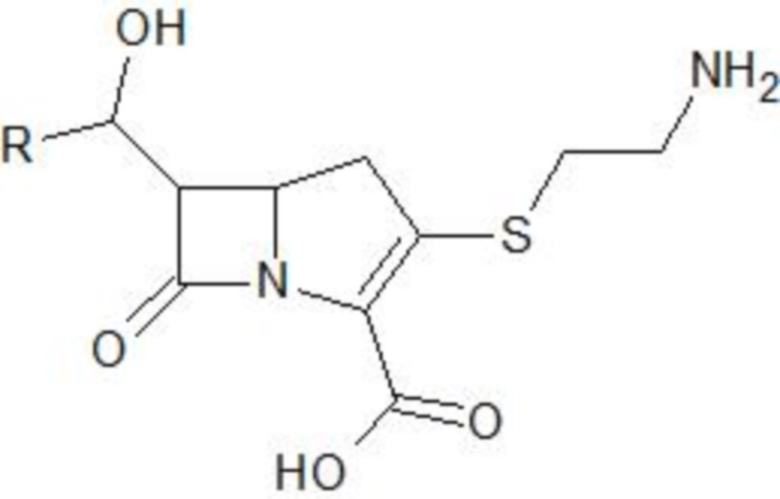 (IIA),
(IIA),
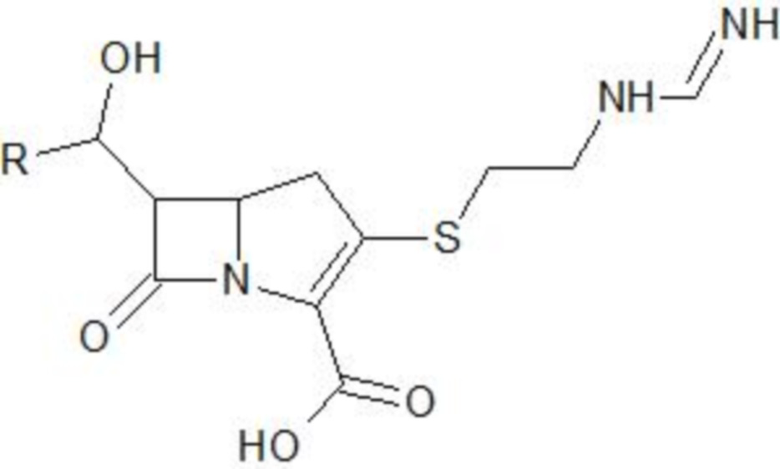 (IIB),
(IIB),  (IIC), или
(IIC), или
 (IID),
(IID),
где R определен как R1 выше.
В одном из вариантов осуществления настоящего изобретения соединение для применения в долгосрочном предотвращении или лечении нарушения метаболизма глюкозы представляет собой соединение, представленное формулой (III), или его фармацевтически приемлемую соль:
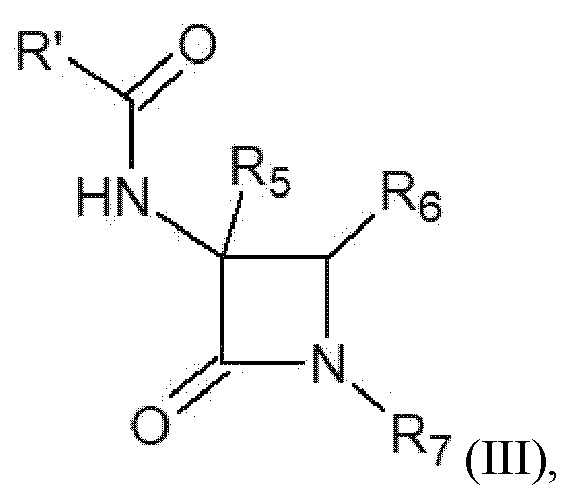
где:
R’ представляет собой H или замещенную или незамещенную группу, выбранную из группы, состоящей из алкила, алкенила, алкинила, гидроксиалкила, фторалкила, хлоралкила, бромалкила, йодоалкила, перфторалкила, арила, фенила, феноксила, бензила, нафталинила, изоксазолила, пиперазинила, оксопиперазинила, пирролидинила, пиразолила, пиридиазинила, гетероарила, пиридинила, циклопентапиридинила, хинолинила, циклоалкила, циклоалкенила, карбоксила, аралкила аралкенила, аралкинила, гетероаралкила, гетероаралкенила, гетероаралкинила, гетероциклила, ацила, аминокарбонила, аминоалкила, амино, имино, алкиламино, имидазолилила, оксоимидазолидинила, циано, фуранила, гидроксила, алкокси, ацилокси, силилокси, амидо, имидоила, карбамоила, триазинанила, триазолила, тетразолила, галогена, тио, тиоэфира, тиенила, тиэтанила, тиофенила, тиазолила, тиадиазолила, сульфо, сульфанила, сульфонила, фосфонила, сульфонола и сульфонамидо;
R5 представляет собой H или замещенный или незамещенный алкокси; и
R6 связан с R7 с образованием замещенного или незамещенного 5- или 6-членного гетероцикла.
В одном варианте осуществления настоящего изобретения соединение формулы (III) может представлять собой соединение, представленное следующей формулой:

где R’ и R5 определены выше, и R8 определен как R’.
В одном варианте осуществления настоящего изобретения в формуле (IIIA) R’ представляет собой замещенную группу, выбранную из группы, состоящей из алкила, гидроксиалкила, арила, гетероарила и аралкила.
В одном варианте осуществления настоящего изобретения в формуле (IIIB) R5 представляет собой H или метокси, и R8 представляет собой замещенную группу, выбранную из группы, состоящей из гетероарила, гетероциклила, алкокси и тио.
В одном варианте осуществления настоящего изобретения бета-лактамное соединение для применения в долгосрочном предотвращении или лечении нарушения метаболизма глюкозы может представлять собой один или несколько пенициллинов, цефалоспоринов и карбапенемов. В другом варианте осуществления изобретения бета-лактамное соединение выбрано из группы, состоящей из эртапенема, дорипенема, имипенема, меропенема, биапенема, панипенема, томопенема, ленапенема, тебипенема, разупенема, тиенпенема, пенициллина G, пенициллина O, пенициллина N, пенициллина K, пенициллина V, фенетициллина, пропациллина, ампициллина, амоксициллина, азлоциллина, карбенициллина, эпициллина, метициллина, мезлоциллина, оксациллина, пиперациллина, клоксациллина, диклоксациллина, флуклоксациллина, сульбенициллина, тикарциллина, нафциллина, метампициллина, оксациллина, цефтриаксона, цефалотина, цефокситин, цефотетана, цефтазидима, цефотаксима, цефепима, цефацетрила, цефадроксила, цефалексина, цефалоглицина, цефалония, цефалоридина, цефапирин, цефатризина, цефазафлура, цефазедона, цефазолина, цефрадина, цефроксадина, цефтезола, цефаклора, цефоницида, цефпрозила, цефуроксима, цефузонама, цефметазола, цефбуперазона, цефминокса, цефотиама, цефкапена, цефдалоксима, цефдинира, цефдиторена, цефетамета, цефиксима, цефменоксима, цефодизима, цефовецина, цефпимизола, цефподоксима, цефтерама, цефтибутена, цефтиофура, цефтиолена, цефтизоксима, цефоперазона, цефклидина, цефидерокола, цефлупренама, цефозелиса, цефозопрана, цефпирома, цефкинома, цефтобипрола, цефтаролина, цефтолозана, цефапарола, цефматилена, цефсумида и их комбинации.
В одном варианте осуществления настоящего изобретения долгосрочное предотвращение или лечение нарушения метаболизма глюкозы представляет собой предотвращение или лечение симптома нарушения метаболизма глюкозы в течение более двух дней после введения соединения (т.е. после прекращения введения соединения). В другом варианте осуществления изобретения долгосрочное предотвращение или лечение нарушения метаболизма глюкозы продолжается в течение, по меньшей мере, одной недели после введения соединения. В еще одном варианте осуществления изобретения долгосрочный эффект длится, по меньшей мере, 6 недель после введения соединения. В еще одном варианте осуществления изобретения долгосрочный эффект продолжается от 6 до 10 недель после введения соединения.
В одном варианте осуществления настоящего изобретения нарушение метаболизма глюкозы представляет собой ожирение, избыточный вес, гипергликемию, гиперинсулинемию, непереносимость глюкозы, диабет 1 типа или диабет 2 типа. В другом варианте осуществления изобретения нарушение метаболизма глюкозы представляет собой гипергликемию, и введение снижает уровень глюкозы в плазме крови у субъекта. В еще одном варианте осуществления изобретения нарушение метаболизма глюкозы представляет собой непереносимость глюкозы, и введение увеличивает толерантность к глюкозе у субъекта.
В одном варианте осуществления настоящего изобретения субъектом является млекопитающее. В другом варианте осуществления изобретения субъектом является человек.
В одном варианте осуществления настоящего изобретения субъект страдает диабетом 1 типа. В другом варианте осуществления изобретения субъект страдает диабетом 2 типа.
Краткое описание чертежей
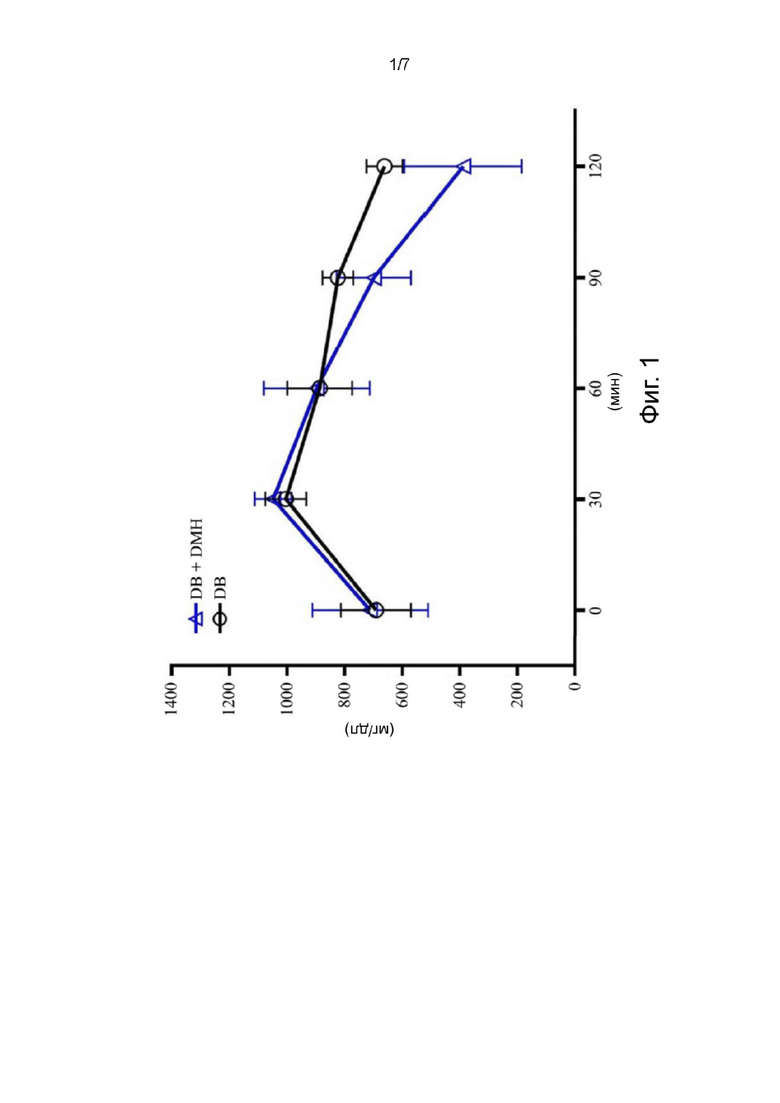
На Фигуре 1 показаны концентрации глюкозы в крови через 3 недели после лечения эртапенемом. DB: db/db мыши, которым перорально вводили дистиллированную воду и внутрибрюшинно (в.б.) вводили физиологический раствор. DB + DMH: db/db мыши, получавшие эртапенем (0,41 мг/г м.т./сутки), в.б.
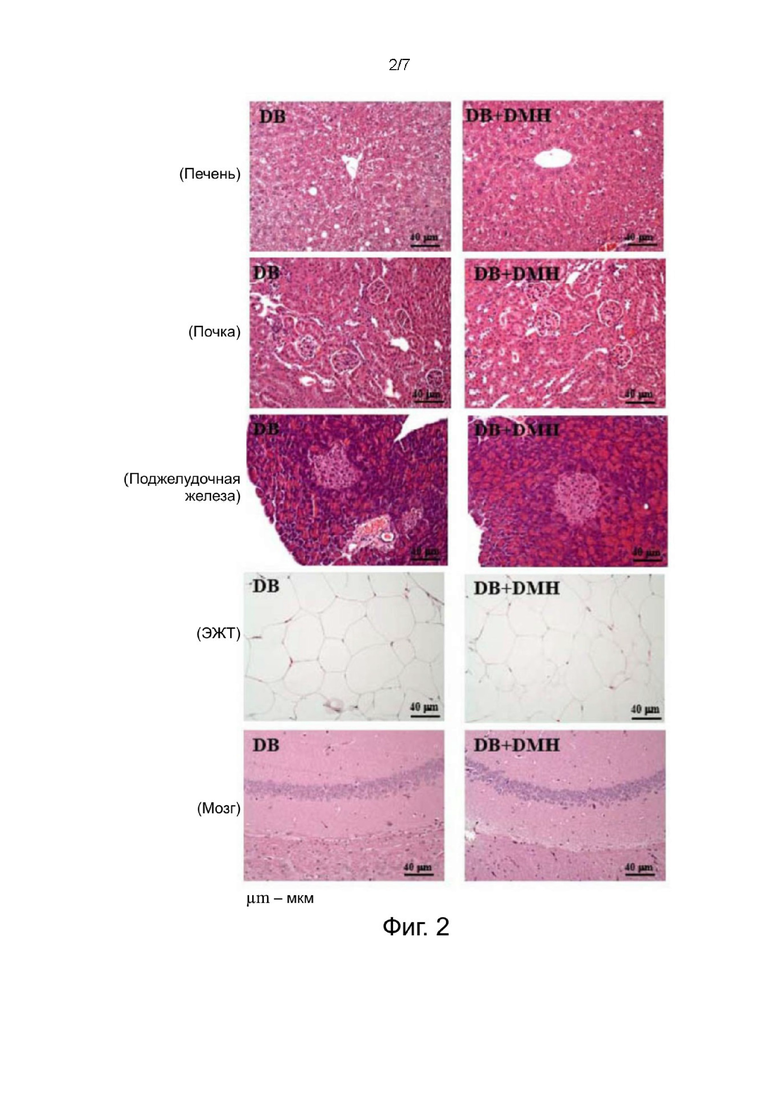
На Фигуре 2 показана гистология различных тканей после лечения эртапенемом. DB: db/db мыши, которым перорально вводили дистиллированную воду и внутрибрюшинно (в.б.) вводили физиологический раствор. DB + DMH: db/db мыши, получавшие эртапенем (0,41 мг/г м.т./сутки), в.б. Масштабная линейка: 40 мкм. ЭЖТ: эпидидимальная жировая ткань.
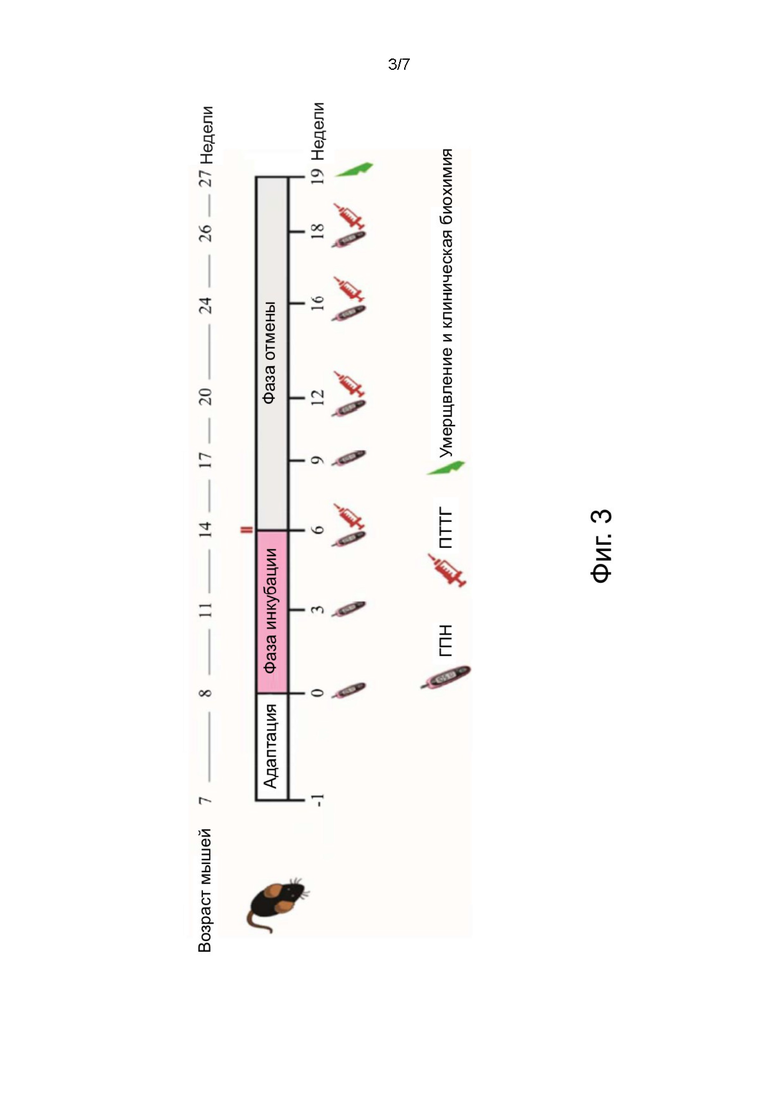
На Фигуре 3 показана схема времени лечения, возраст мышей и время сбора данных. Уровень глюкозы в плазме натощак (ГПН) измеряли в указанные недели, с помощью глюкометра OneTouch UltraEasy. Пероральный тест на толерантность к глюкозе (ПТТГ) проводили в указанные недели с помощью шприцев. Уровни некоторых воспалительных маркеров печени и почек определяли на 19 неделе (указано стрелкой). Введение всех препаратов прекращали на 6 неделе.
На Фигуре 4 показаны концентрации глюкозы в крови на 6, 12, 16 и 18 неделе после лечения.  : m/m мыши, которым перорально вводили дистиллированную воду и внутрибрюшинно (в.б.) вводили физиологический раствор.
: m/m мыши, которым перорально вводили дистиллированную воду и внутрибрюшинно (в.б.) вводили физиологический раствор.  : db/db мыши, которых лечили так же, как m/m мышей.
: db/db мыши, которых лечили так же, как m/m мышей.  : db/db мыши, которым перорально вводили метформин (МЕТ) (0,3 мг/г м.т./сутки).
: db/db мыши, которым перорально вводили метформин (МЕТ) (0,3 мг/г м.т./сутки).  : db/db мыши, получавшие эртапенем (0,1 мг/г м.т./сутки), в.б.
: db/db мыши, получавшие эртапенем (0,1 мг/г м.т./сутки), в.б.  : db/db мыши, получавшие эртапенем (0,2 мг/г м.т./сутки), в.б.
: db/db мыши, получавшие эртапенем (0,2 мг/г м.т./сутки), в.б.  : db/db мыши, получавшие эртапенем (0,4 мг/г м.т./сутки), в.б.
: db/db мыши, получавшие эртапенем (0,4 мг/г м.т./сутки), в.б.
На Фигуре 5 показана гистология четырех различных тканей после лечения. G1: m/m мыши, вода неограниченно, физиологический раствор (10 мкл/г м.т.) в.б., ежедневно; G2: db/db, мыши, вода неограниченно, физиологический раствор (10 мкл/г м.т.) в.б., ежедневно; G3: db/db мыши, метформин (MET) перорально (0,3 мг/г мт/сутки); G4: db/db мыши, эртапенем (0,1 мг/г м.т./сутки) в.б.; G5: db/db мыши, эртапенем (0,2 мг/г м.т./сутки) в.б.; G6: db/db мыши, эртапенем (0,4 мг/г м.т./сутки) в.б. Масштабная линейка: 40 мкм. ЭЖТ: эпидидимальная жировая ткань.
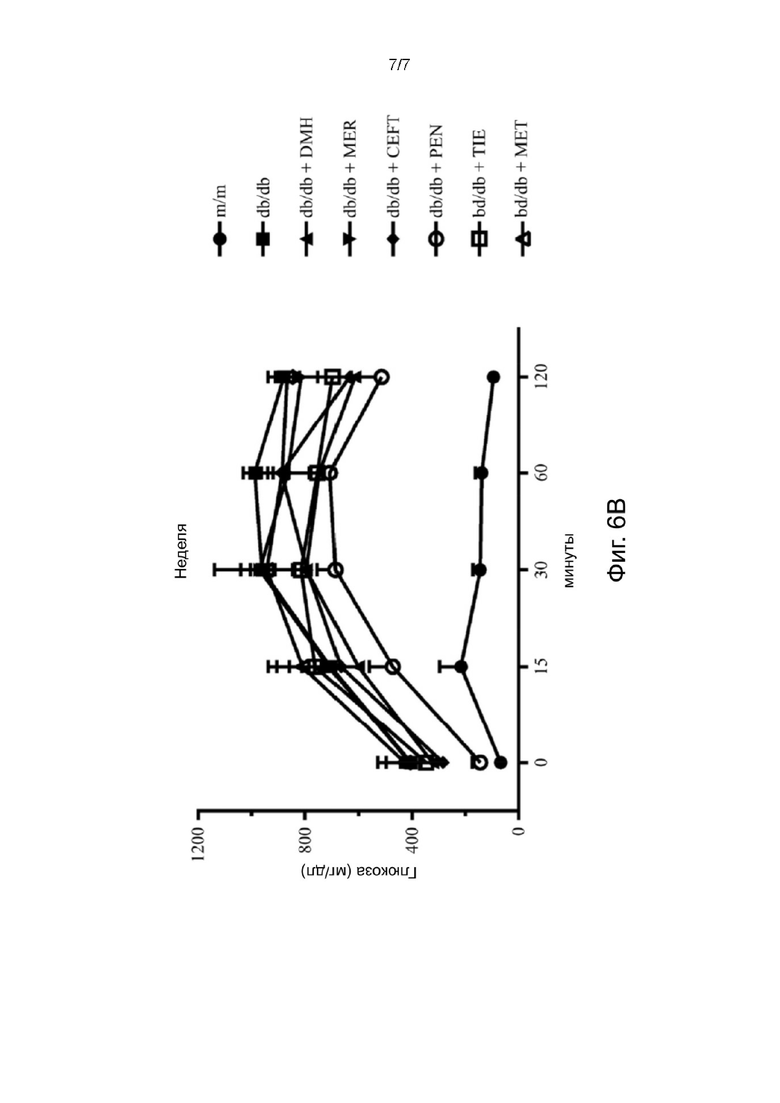
На Фигурах 6A и 6B показаны концентрации глюкозы в крови на 6-й неделе (Фигура 6A) и 9-й неделе (Фигура 6B) после лечения.  : m/m мыши, которым перорально вводили дистиллированную воду и внутрибрюшинно (в.б.) вводили физиологический раствор.
: m/m мыши, которым перорально вводили дистиллированную воду и внутрибрюшинно (в.б.) вводили физиологический раствор.  : db/db мыши, которых лечили так же, как m/m мышей.
: db/db мыши, которых лечили так же, как m/m мышей.  : db/db мыши, получавшие эртапенем (DMH) (0,41 мг/г м.т./сутки) в.б.
: db/db мыши, получавшие эртапенем (DMH) (0,41 мг/г м.т./сутки) в.б.  мыши, получавшие меропенема гидрат (MER) (0,205 мг/г м.т./сутки)
мыши, получавшие меропенема гидрат (MER) (0,205 мг/г м.т./сутки)  мыши, получавшие цефтриаксон (CEFT) (0,82 мг/г м.т./сутки) в.б.
мыши, получавшие цефтриаксон (CEFT) (0,82 мг/г м.т./сутки) в.б.  : db/db мыши, получавшие пенициллин G (PEN) (1,473 мг/г м.т./сутки).
: db/db мыши, получавшие пенициллин G (PEN) (1,473 мг/г м.т./сутки).  : db/db мыши, получавшие тиенам (TIE) (0,41 мг/г м.т./сутки).
: db/db мыши, получавшие тиенам (TIE) (0,41 мг/г м.т./сутки).  : db/db мыши, которым перорально вводили метформин (МЕТ) (0,3 мг/г м.т./сутки).
: db/db мыши, которым перорально вводили метформин (МЕТ) (0,3 мг/г м.т./сутки).
Подробное описание изобретения
Следующие ниже примеры используются для иллюстрации настоящего изобретения. Специалист в данной области техники сможет легко понять другие преимущества и эффекты настоящего изобретения, основываясь на раскрытии описания. Настоящее изобретение также может быть реализовано или применено, как описано в различных примерах. Можно модифицировать или изменить следующие примеры для выполнения настоящего изобретения без нарушения его сущности и объема для различных аспектов и приложений.
Кроме того, следует отметить, что используемые в настоящем изобретении формы единственного числа термина включают в себя множественное число термина, если явно и недвусмысленно не ограничены одним термином в единственном числе. Термин «или» используется взаимозаменяемо с термином «и/или», если из контекста явно не следует иное.
Термин «пациент» или «субъект», используемый здесь взаимозаменяемо в контексте терапии, относится к человеку или животному, не являющемуся человеком, как реципиенту терапии или профилактического лечения.
Используемый здесь термин «толерантность к глюкозе» относится к способности субъекта контролировать уровень глюкозы в плазме крови и/или инсулина в плазме крови при колебаниях потребления глюкозы. Например, толерантность к глюкозе включает в себя способность снижать уровень глюкозы в плазме крови обратно до уровня до приема глюкозы в течение примерно 120 минут или около того.
Используемый здесь термин «преддиабет» относится к состоянию, которое может быть определено с помощью теста на глюкозу в плазме натощак (ГПН) или перорального теста на толерантность к глюкозе (ПТТГ). Оба эти теста требуют, чтобы человек не ел с вечера. В тесте ГПН уровень глюкозы в крови человека сначала измеряется утром перед едой. В ПТТГ уровень глюкозы в крови человека проверяется после голодания и еще раз через 2 часа после употребления напитка, богатого глюкозой. У здорового человека нормальный результат теста на ГПН будет показывать уровень глюкозы ниже примерно 100 мг/дл. Субъект с преддиабетом может иметь уровень ГПН от примерно 100 мг/дл до примерно 125 мг/дл. Если уровень глюкозы в крови повышается примерно до 126 мг/дл или выше, то субъекту ставят диагноз «диабет». В ПТТГ уровень глюкозы в крови субъекта измеряется после голодания и через 2 часа после употребления напитка, богатого глюкозой. Нормальный уровень глюкозы в крови у здорового человека ниже примерно 140 мг/дл через 2 часа после приема напитка. У субъекта с преддиабетом уровень глюкозы в крови через 2 часа составляет от примерно 140 мг/дл до примерно 199 мг/дл. Если уровень глюкозы в крови через 2 часа повышается до 200 мг/дл или выше, то субъекту ставят диагноз «диабет».
Настоящее изобретение относится к способу лечения пациента, страдающего гипергликемией, гиперинсулинемией, непереносимостью глюкозы и т.д. Такие состояния также обычно связаны со многими другими нарушениями метаболизма глюкозы. По существу, пациенты с нарушениями метаболизма глюкозы могут быть кандидатами на лечение в соответствии со способами настоящего изобретения.
Термин «нарушение метаболизма глюкозы» включает в себя любое расстройство, характеризующееся клиническим симптомом или комбинацией клинических симптомов, которые связаны с повышенным уровнем глюкозы и/или повышенным уровнем инсулина у субъекта по сравнению со здоровым человеком. Повышенные уровни глюкозы и/или инсулина могут проявляться в следующих нарушениях и/или состояниях: диабет 2 типа (например, диабет с инсулинорезистентностью), гестационный диабет, инсулинорезистентность, нарушение толерантности к глюкозе, гиперинсулинемия, нарушение метаболизма глюкозы, преддиабет, метаболические нарушения (например, метаболический синдром, также называемый синдромом X), ожирение или расстройство, связанное с ожирением.
Примером подходящего пациента может быть пациент, страдающий гипергликемией и/или гиперинсулинемией, и у которого также диагностирован сахарный диабет (например, диабет 2 типа). Термин «диабет» относится к прогрессирующему заболеванию углеводного обмена, включающему в себя неадекватную выработку или использование инсулина, и характеризующемуся гипергликемией и глюкозурией.
Используемый здесь термин «гипергликемия» означает состояние, при котором в плазме крови циркулирует повышенное количество глюкозы по сравнению со здоровым человеком, и его можно диагностировать с помощью способов, известных в данной области техники. Например, гипергликемия может быть диагностирована как наличие уровня глюкозы в крови натощак от 5,6 мМ до 7 мМ (преддиабет) или более 7 мМ (диабет).
Используемый здесь термин «гиперинсулинемия» означает состояние, при котором наблюдаются повышенные уровни циркулирующего инсулина, в то время как уровни глюкозы в крови могут быть повышены или оставаться нормальными. Гиперинсулинемия может быть вызвана резистентностью к инсулину, которая связана с дислипидемией, такой как высокий уровень триглицеридов, высокий уровень холестерина, высокий уровень липопротеинов низкой плотности (ЛПНП) и низкий уровень липопротеинов высокой плотности (ЛПВП), высокое содержание мочевой кислоты, синдром поликистозных яичников, диабет 2 типа и ожирение. Гиперинсулинемия может быть диагностирована как уровень инсулина в плазме выше примерно 2 мкЕд/мл.
Пациент, страдающий любым из вышеперечисленных расстройств, может быть подходящим кандидатом, нуждающимся в терапии в соответствии с настоящим изобретением, чтобы получить лечение нарушений метаболизма глюкозы. Введение β - лактамных соединений настоящего изобретения такому субъекту может восстановить гомеостаз глюкозы, а также может уменьшить один или несколько симптомов, связанных с этими расстройствами.
Кандидаты на лечение с применением способов настоящего изобретения могут быть определены с использованием диагностических методов, известных в данной области техники, например путем определения уровня глюкозы и/или инсулина в плазме крови. К кандидатам на лечение относятся те, у кого уровень глюкозы/инсулина в плазме крови был выше нормального или у них наблюдается более высокий, чем нормальный, уровень. К таким пациентам относятся пациенты, у которых концентрация глюкозы в крови натощак (когда тест проводится после 8-10 часов голодания) выше примерно 100 мг/дл, например выше примерно 110 мг/дл, выше примерно 120 мг/дл, от примерно 150 мг/дл до примерно 200 мг/дл или более. Лица, подходящие для лечения, также включают тех, у кого концентрация глюкозы в крови через 2 часа после приема пищи или концентрация после теста на толерантность к глюкозе (например, через 2 часа после приема напитка, богатого глюкозой), выше, чем примерно 140 мг/дл, например, от примерно 150 мг/дл до 200 мг/дл или более. Концентрация глюкозы также может быть выражена в ммоль/л, ее можно получить, разделив концентрацию в мг/дл на коэффициент 18.
Субъекты, имеющие нарушения метаболизма глюкозы, подозреваемые в их наличии или подверженные риску их развития, рассматриваются как подходящие для описанного здесь лечения.
Используемый здесь термин «лечение» относится к ситуации, когда достигается, по меньшей мере, облегчение симптомов, связанных с состоянием, поражающим субъекта, где облегчение относится, по меньшей мере, к уменьшению величины параметра, например симптома, связанного с подвергающимся лечению состоянием. Таким образом, лечение включает в себя ситуацию, когда состояние или, по крайней мере, симптом, связанный с ним, уменьшается, или его удается избежать. Лечение включает в себя: (i) взаимозаменяемое с предотвращением снижение риска развития клинических симптомов, включая предотвращение развития клинических симптомов, например, предотвращение прогрессирования заболевания до вредного или иного нежелательного состояния; и (ii) ингибирование, то есть остановку развития или дальнейшего развития клинических симптомов, например, смягчение или полное подавление активного заболевания (например, снижение уровня инсулина и/или глюкозы в кровотоке, повышение толерантности к глюкозе для минимизации колебаний уровня глюкозы и/или защита от заболеваний, вызванных нарушением гомеостаза глюкозы).
Способы, связанные к нарушениям метаболизма глюкозы, описанные в настоящем изобретении, включают в себя, например, применение описанных выше β - лактамных соединений для лечения самостоятельно или в комбинации с другими видами терапии. Способ включает в себя введение субъекту β - лактамного соединения настоящего изобретения (например, подкожно, внутримышечно или внутривенно). Как отмечалось выше, эти способы применимы в контексте лечения или предотвращения широкого спектра нарушений, связанных с метаболизмом глюкозы.
Способы настоящего изобретения включают в себя введение β - лактамного соединения настоящего изобретения субъекту, страдающему нарушением метаболизма глюкозы. Способы настоящего изобретения включают в себя введение соединения, представленного формулой (I), (II) или (III), как описано выше, в контексте множества состояний, включая нарушения, приведенные в примерах выше (как для их предотвращения, так и в качестве терапии после постановки диагноза).
В одном варианте осуществления изобретения β - лактамное соединение настоящего изобретения для применения в долгосрочном предотвращении или лечении нарушения метаболизма глюкозы может представлять собой карбапенемы, представленные формулой (IIA), (IIB), (IIC) или (IID), такие как эртапенем, дорипенем, имипенем, меропенем, биапенем и панипенем.
В одном варианте осуществления изобретения β-лактамное соединение настоящего изобретения для применения в долгосрочном предотвращении или лечении нарушения метаболизма глюкозы может представлять собой пенициллины, представленные формулой (IIIA), такие как пенициллин G, пенициллин O, пенициллин N, пенициллин K, пенициллин V, фенетициллин, пропациллин, ампициллин, амоксициллин, азлоциллин, карбенициллин, эпициллин, метициллин, мезлоциллин, оксациллин, пиперациллин, клоксациллин, диклоксациллин, флуклоксациллин, сульбенициллин, тикарциллин, нафциллин, метампициллин и оксациллин.
В одном варианте осуществления изобретения β-лактамное соединение настоящего изобретения для применения в долгосрочном предотвращении или лечении нарушения метаболизма глюкозы может представлять собой цефалоспорины, представленные формулой (IIIB), такие как цефтриаксон, цефалотин, цефокситин, цефотетан, цефтазидим, цефотаксим, цефепим, цефацетрил, цефадроксил, цефалексин, цефалоглицин, цефалоний, цефалоридин, цефапирин, цефатризин, цефазафлур, цефазедон, цефазолин, цефрадин, цефроксадин, цефтезол, цефаклор, цефоницид, цефпрозил, цефуроксим, цефузонам, цефметазол, цефбуперазон, цефминокс, цефотиам, цефкапен, цефдалоксим, цефдинир, цефдиторен, цефетамет, цефиксим, цефменоксим, цефодизим, цефовецин, цефпимизол, цефподоксим, цефтерам, цефтибутен, цефтиофур, цефтиолен, цефтизоксим, цефоперазон, цефклидин, цефидерокол, цефлупренам, цефозелис, цефозопран, цефпиром, цефхином, цефтобипрол, цефтаролин, цефтолозан, цефапарол, цефматилен и цефсумид.
В способах настоящего изобретения β - лактамное соединение можно вводить в форме фармацевтической композиции. Фармацевтическая композиция может содержать одно или несколько описанных здесь β - лактамных соединений и/или дополнительный терапевтический агент для лечения расстройства, как проиллюстрировано выше. Фармацевтическая композиция может вводиться субъекту (например, пациенту-человеку), например, для достижения и/или поддержания гомеостаза глюкозы, например, для снижения уровня глюкозы в кровотоке и/или для снижения уровня инсулина до диапазона, свойственного здоровому человеку. Субъекты, нуждающиеся в лечении, включают в себя субъектов, страдающих нарушением метаболизма глюкозы, как описано здесь.
В одном варианте осуществления изобретения фармацевтические композиции настоящего изобретения дополнительно содержат фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или сольват и могут быть приготовлены в виде подходящих лекарственных форм. Примерами подходящих лекарственных форм являются таблетки, капсулы, таблетки с покрытием, гранулы, растворы и сиропы для перорального введения; лечебные пластыри, пасты, кремы и мази для трансдермального введения; свечи для ректального введения; и стерильные растворы для введения путем инъекции или в виде аэрозоля.
Другими примерами подходящих лекарственных форм являются формы с замедленным высвобождением, основанные, например, на липосомах, для введения пероральным или инъекционным путем.
Лекарственные формы могут также содержать другие стандартные ингредиенты, например консервант, стабилизатор, поверхностно-активное вещество, буфер, регулирующая осмотическое давление соль, эмульгатор, подсластитель, краситель, ароматизатор и тому подобное.
Кроме того, когда требуется для определенных видов лечения, фармацевтическая композиция настоящего изобретения может также содержать другие фармакологически активные ингредиенты, одновременное введение которых является полезным.
Количество бета-лактамного соединения настоящего изобретения может варьироваться в широком диапазоне в зависимости, например, от типа заболевания, подлежащего лечению, тяжести заболевания, массы тела пациента, лекарственной формы, выбранного пути введения, количества ежедневных введений и эффективности выбранного бета-лактамного соединения. Однако специалист в данной области техники при необходимости может определить оптимальное количество простым и обычным способом на основе настоящего изобретения.
В способах настоящего изобретения терапевтически эффективное количество бета-лактамного соединения вводят нуждающемуся в этом субъекту. Другими словами, бета-лактамное соединение вызывает возврат уровня глюкозы и/или инсулина в плазме крови к нормальному уровню как у здорового человека, когда соединение доставляется в кровоток в эффективном количестве пациенту, который ранее до лечения не имел нормальный уровень глюкозы/инсулина как у здорового человека. Вводимое количество варьируется в зависимости от цели введения, здоровья, физического состояния и возраста человека, подлежащего лечению, активности используемых соединений, оценки лечащим врачом медицинской ситуации, состояния субъекта, массы тела субъекта, тяжести нарушения регуляции глюкозы/инсулина и стадии заболевания, а также других соответствующих факторов. Величина дозы также будет определяться существованием, природой и степенью любых неблагоприятных побочных эффектов, которые могут сопровождать введение соединения.
Ожидается, что это количество будет находиться в относительно широком диапазоне, который может быть определен с помощью обычных испытаний. Например, количество соединения, применяемого для восстановления гомеостаза глюкозы, не превышает примерно того количества, которое в противном случае могло бы быть необратимо токсичным для субъекта (т.е. максимально переносимая доза). В других случаях количество примерно или даже значительно ниже порога токсичности, но все же находится в диапазоне эффективных концентраций или даже на уровне пороговой дозы.
Также подходящие дозы и схемы приема могут быть определены путем сравнения с показателями метаболизма глюкозы. Такие дозы включают в себя дозы, которые приводят к стабилизированным уровням глюкозы и инсулина, например, сравнимым со здоровым индивидуумом, без значительных побочных эффектов. Дозированное лечение может представлять собой схему однократного приема или схему многократного приема (например, включая возрастающие и поддерживающие дозы). Как указано ниже, фармацевтическую композицию можно вводить в сочетании с другими агентами, и, таким образом, дозы и схемы могут варьироваться в этом контексте, а также соответствовать потребностям субъекта.
Индивидуальные дозы обычно не меньше количества, необходимого для оказания измеримого воздействия на субъекта, и могут быть определены на основе фармакокинетики и фармакологии всасывания, распределения, метаболизма и выведения («ADME») соединений или их побочных продуктов, и, следовательно, на основе расположения композиции в субъекте. Сюда входит рассмотрение пути введения, а также величины дозы, которая может быть скорректирована для энтерального (вводится через пищеварительный тракт для системных или местных эффектов, когда сохраняется в части пищеварительного тракта) или парентерального (вводится путями, отличными от пищеварительного тракта для системных или местных эффектов) введений. Например, введение соединений обычно осуществляется путем инъекции и часто внутривенно, внутримышечно или путем их комбинации.
Термин «в эффективном количестве» означает, что существует обнаруживаемая разница между уровнем индикатора, измеренным до и после введения количества конкретной терапии. Индикаторы включают в себя без ограничений глюкозу и инсулин. Например, это может означать, что введение этого количества индивидууму, либо в виде разовой дозы, либо в составе серии одинаковых или разных композиций, эффективно для восстановления гомеостаза метаболизма глюкозы, оцениваемого по уровню глюкозы и/или инсулина у субъекта. Как отмечалось выше, терапевтически эффективное количество может быть скорректировано в связи со схемой приема и диагностическим анализом состояния субъекта (например, мониторинг уровня глюкозы и/или инсулина в плазме крови) и тому подобное.
Лекарственные формы фармацевтической композиции настоящего изобретения могут быть приготовлены согласно методикам, которые хорошо известны химикам-фармацевтам, включая смешивание, гранулирование, прессование, растворение, стерилизацию и тому подобное.
Термины «долгосрочное» или «долгосрочный эффект», используемые здесь взаимозаменяемо, означают эффект предотвращения или лечения нарушения метаболизма глюкозы, продолжающийся, по меньшей мере, 24 часа, по меньшей мере, 48 часов, по меньшей мере, 72 часа, по меньшей мере, 96 часов, по меньшей мере, одну неделю, по меньшей мере, две недели, по меньшей мере, три недели, по меньшей мере, четыре недели, по меньшей мере, пять недель, по меньшей мере, шесть недель, по меньшей мере, семь недель, по меньшей мере, восемь недель, по меньшей мере, девять недель, по меньшей мере, десять недель, по меньшей мере, одиннадцать недель или, по меньшей мере, двенадцать недель даже после прекращения приема лекарственного средства β - лактамного соединения. В одном варианте осуществления изобретения β - лактамные соединения настоящего изобретения не только применимы для предотвращения или лечения нарушения метаболизма глюкозы, но также проявляют эффект длительного действия в отношении предотвращения или лечения нарушения метаболизма глюкозы даже после введения нуждающемуся в этом субъекту, при этом долгосрочный эффект может длиться, по меньшей мере, два дня, по меньшей мере, одну неделю, по меньшей мере, две недели, по меньшей мере, три недели, по меньшей мере, четыре недели, по меньшей мере, пять недель, по меньшей мере, шесть недель, по меньшей мере, семь недель, по меньшей мере, восемь недель, по меньшей мере, девять недель, по меньшей мере, десять недель, по меньшей мере, одиннадцать недель или, по меньшей мере, двенадцать недель.
Примеры
Следующие ниже примеры представлены для того, чтобы предоставить средним специалистам в данной области техники полное раскрытие и описание того, как осуществить и применять настоящее изобретение, и не предназначены для ограничения объема того, что следует рассматривать как изобретение, или для обозначения того, что приведенные ниже эксперименты являются всеми или единственными выполненными экспериментами. Авторами настоящего изобретения были предприняты усилия для обеспечения точности используемых чисел (например, количества, веса, температуры и т.д.), но следует учитывать некоторые экспериментальные ошибки и отклонения.
Материалы и методы
Материалы и методы, использованные в следующих примерах, подробно описаны ниже. Материалы, используемые в настоящем изобретении, но не аннотированные здесь, являются коммерчески доступными.
(1) Животные
В следующих примерах db/db мышей с дефектом гена лептинового рецептора (Lepr), которые проявляют резистентность к инсулину, аналогично пациентам с диабетом 2 типа, использовали для исследования действия соединений-кандидатов на регуляцию гомеостаза глюкозы в крови.
db/db мышей (BKS.Cg-Dock7m+/+Leprdb/JNarl) и m/m мышей (BKS.Cg-Dock7m+/Dock7m+) в возрасте от четырех до пяти недель получали из Национального центра лабораторных животных (Нанган, Тайбэй, Тайвань). Этих животных содержали в помещении с 12-часовым циклом темнота-свет при температуре 24 ± 2°C и влажности 65 ± 5%, им давали пищу (№ 5001; PMI Nutrition International, Брентвуд, Миссури) и воду без ограничений. Для экспериментов средняя масса тела m/m мышей составляла приблизительно 20 г, а db/db мышей - приблизительно 30 г.
Массу тела мышей (м.т.) и количество потребляемой воды и корма регистрировали еженедельно в течение всего периода исследования.
(2) Измерение уровня глюкозы в плазме натощак (ГПН).
У каждой мыши брали пробы крови из хвостовой вены и измеряли уровни ГПН с помощью глюкометра (OneTouch UltraEasy, Johnson & Johnson, США) в определенный момент времени.
(3) Пероральный тест на толерантность к глюкозе (ПТТГ)
Для ПТТГ все мыши перед тестом голодали в течение 16 часов, но имели неограниченный доступ к воде. Кровь брали из хвостовой вены, измеряли уровни ГПН и записывали их как базовые уровни глюкозы в крови. После измерений ГПН мышам перорально вводили 2 мг/г глюкозы (20% раствор глюкозы) и измеряли уровни глюкозы в крови через 15, 30, 60 и 120 минут после кормления. Общую площадь под кривой (AUC) в ПТТГ строили и рассчитывали при помощи программы Area Under Coordinates (сервер StatsToDo, кафедра акушерства и гинекологии, Китайский университет Гонконга).
(4) Прочие анализы
Воспалительные маркеры, такие как сывороточная аспартатаминотрансфераза (AST), аланинаминотрансфераза (ALT), азот мочевины крови (BUN), креатинин (Cr) и гемоглобин A1c (HbA1c), измеряли с помощью химического автоматического анализатора BMC-Hitachi 717.
Для гистопатологической оценки всех мышей умерщвляли асфиксией 95% CO2 в конце периода исследования. Их головной мозг, печень, почки, поджелудочную железу и эпидидимальную жировую ткань извлекали, фиксировали в 10% забуференном фосфатом формалине и заливали парафином. Ткани, залитые парафином, разрезали на срезы толщиной 4 мкм, которые затем окрашивали гематоксилином и эозином (т.е. окрашивание H&E).
(5) Статистический анализ
Результаты, рассчитанные, по меньшей мере, для 6 мышей в каждой экспериментальной группе, были показаны как средние значения ± стандартная ошибка среднего (СОС). Значение P <0,05 считалось значимым (дисперсионный анализ с последующим тестом Дункана). Медикаментозное лечение считалось эффективным (значение P <0,05) для снижения уровня глюкозы в крови, если уровни ГПН после лечения были значимо ниже, чем до лечения, или если значения пероральной толерантности к глюкозе (ПТГ) после лечения были значимо выше, чем до лечения.
Пример 1: Влияние лечения эртапенемом на нарушение метаболизма глюкозы.
В этом примере влияние эртапенема (далее также сокращенно «DMH») на нарушение метаболизма глюкозы исследовали в сравнении с метформином (Met), известной фармакотерапией первой линии для лечения диабета 2 типа.
Двенадцать db/db мышей в возрасте 7 или 8 недель были случайным образом распределены на 2 группы, и им внутрибрюшинно (в.б.) вводили эртапенем или не вводили его (т.е. группы DB + DMH или DB, соответственно). Лечение каждой группы подробно описано в Таблице 1 ниже.
Таблица 1. Мыши были распределены на 2 группы для различного лечения.
Каждой мыши вводили физиологический раствор или эртапенем внутрибрюшинно один раз в день, и такое лечение длилось в общей сложности три недели. Тесты и результаты описывали следующим образом.
(1-1) Лечение эртапенемом уменьшило потребление корма и воды
Как показано в Таблице 2 ниже, было обнаружено, что мыши, получавшие эртапенем (т.е. группа DB + DMH), имели пониженное потребление корма и воды в течение всего периода исследования (P <0,05). Этот результат ясно показал, что эртапенем эффективен в контроле потребления корма и воды у мышей с диабетом.
Таблица 2. Среднее потребление корма и воды среди групп мышей
Группы
(г/мышь/сутки)
(мл/мышь/сутки)
*P < 0,05
(1-2) Лечение эртапенемом увеличивало пероральную определяемую толерантность к глюкозе
ПТТГ выполняли на 3-й неделе, то есть в конце лечения эртапенемом. Как показано на Фигуре 1, концентрация глюкозы в группе DB + DMH была значимо ниже, чем в группе DB, в моменты времени 90 и 120 минут.
Кроме того, общая площадь под кривой (AUC) в ПТТГ была построена и рассчитана, как показано в Таблице 3. Результаты показали, что AUC мышей, получавших эртапенем (группа DB + DMH), была значимо меньше (P <0,05), чем у мышей, не получавших лечение (группа DB).
Таблица 3. AUC ПТТГ двух групп мышей
Группы
*P < 0,05
(1-3) Анализ биохимических параметров плазмы крови
AST и ALT, ранее называемые сывороточной глутаминовой щавелевоуксусной трансаминазой (GOT) и сывороточной глутаминовой пировиноградной трансаминазой (GPT), соответственно, являются воспалительными маркерами печени. BUN и Cr являются маркерами воспаления почек. Эти маркеры и HbA1c измеряли на 3-й неделе, то есть в конце лечения эртапенемом. Результаты представлены в Таблице 4. Было обнаружено, что уровни AST, ALT, BUN и HbA1c у мышей с диабетом были значительно снижены при лечении эртапенемом.
Таблица 4. Биохимические параметры плазмы крови мышей двух групп
Группы
(Ед/л)
(Ед/л)
(мг/дл)
(%)
*P < 0,05
(1-4) Гистологические изменения при лечении эртапенемом
В конце периода исследования всех мышей умерщвляли, извлекали у них мозг, печень, почки, поджелудочную железу и эпидидимальную жировую ткань и гистологически исследовали на предмет повреждений.
Как показано на Фигуре 2, результаты показали отсутствие гистологических изменений поджелудочной железы, эпидидимальной жировой ткани и мозга всех мышей.
Кроме того, в тканях печени двух групп наблюдались очень слабые или незначительные уровни накопления гликогена в цитоплазме гепатоцитов вокруг области центральной вены. Тяжесть и частота такого накопления гликогена в группе DB + DMH меньше, чем в группе DB.
В тканях почек у некоторых мышей наблюдались дегенерация и некроз эпителиальных клеток почечных канальцев, минеральные и гиалиновые отложения, в то время как тяжесть и частота таких гистологических изменений значимо не различались между двумя группами.
В целом, после лечения эртапенемом не наблюдалось серьезных повреждений головного мозга, печени, почек, поджелудочной железы и эпидидимальной жировой ткани.
Пример 2: Влияние лечения эртапенемом на нарушение метаболизма глюкозы после прекращения лечения
Чтобы изучить эффекты лечения эртапенемом и метформином (Met) после прекращения лечения, восемь 8-недельных m/m мышей использовали в качестве нормального контроля (G1) и сорок 8-недельных db/db мышей случайным образом распределяли на 5 групп (от G2 до G6). Каждая группа получает различное лечение, как описано ниже в Таблице 5.
Таблица 5. Мыши были распределены на 6 групп для различного лечения.
Лечение длилось в общей сложности шесть недель, и введение всех лекарственных препаратов было прекращено через шесть недель. Тесты проводились в моменты времени с соответствующим возрастом мышей, как показано на схеме на Фигуре 3. Тесты и результаты были описаны следующим образом.
(2-1) Лечение эртапенемом снижает массу тела
Как показано в Таблице 6 ниже, было обнаружено, что мыши G1 имели самую низкую массу тела в течение всего периода исследования (P<0,05). Не было обнаружено значимых изменений массы тела среди мышей, получавших метформин (G3), и в других группах подопытных мышей.
Однако мыши G4 имели значимо меньшую массу тела, чем мыши G2 и G3 в течение недель 2-9, а мыши G6 имели меньшую массу тела, чем мыши G2 (в течение недель 3-7 и 9) и мыши G3 (в течение недель 3-9). Эти данные показали, что лечение эртапенемом (0,1 мг/г м.т. и 0,4 мг/г м.т.) имело положительный эффект снижения массы тела у db/db мышей. Этот эффект имел место из-за того, что db/db мыши уменьшили потребление корма и воды при лечении эртапенемом.
Таблица 6. Масса тела среди групп мышей
a
a
a
a
a
a
a
b
b
c
d
c
c
cd
+ 0,3 Met
b
b
bc
cd
c
c
d
+ 0,1 DMH
b
b
b
b
b
b
b
+ 0,2 DMH
b
b
bc
bc
bc
bc
bc
+ 0,4 DMH
b
b
bc
b
b
b
b
a
a
a
a
a
a
a
cd
bc
cd
b
b
b
b
+ 0,3 Met
d
c
d
b
b
b
b
+ 0,1 DMH
b
b
b
b
b
b
b
+ 0,2 DMH
bc
bc
bcd
b
b
b
b
+ 0,4 DMH
b
b
bc
b
b
b
b
a
a
a
a
a
a
b
b
b
b
b
b
+ 0,3 DMH
b
b
b
b
b
b
+ 0,1 DMH
b
b
b
b
b
b
+ 0,2 DMH
b
b
b
b
b
b
+ 0,4 DMH
b
b
b
b
b
b
В Таблице 6 представлены значения группового среднего ± СОС массы тела, и разница в значении была значимой (P <0,05) между разными курсивными буквами. Например, при сравнении значений, представленных a с b, существует статистическая значимость (P <0,05) в различии массы тела между ними; и при сравнении значений, представленных буквой b и c, между ними также существует статистическая значимость (P <0,05) по массе тела. Кроме того, значение, представленное bc, значимо отличалось от значений, представленных буквой «а» или «d».
(2-2) Лечение эртапенемом снижает уровень глюкозы в крови
Измерение ГПН проводили у мышей в возрасте 8, 11, 14, 17, 20, 24 и 26 недель, при этом уровни ГПН у 8-недельных мышей были установлены как уровни на неделе 0. Таким образом, уровни ГПН У мышей в возрасте 11, 14, 17, 20, 24 и 26 недель представляли собой уровни у мышей через 3, 6, 9, 12, 16 и 18 недель после лечения, соответственно. Уровни ГПН в каждой группе мышей представлены ниже в Таблице 7.
Таблица 7. Средние уровни ГПН у мышей
+ 0,3 Met
+ 0,1 DMH
+ 0,2 DMH
+ 0,4 DMH
В Таблице 7 показаны значения групповых средних ± СОС уровней ГПН, и разница между значениями была значимой (P <0,05), как объяснено выше.
Как показано в Таблице 7 выше, у мышей G1 были самые низкие уровни ГПН во всех точках измерения (P <0,05).
На 3 неделе уровни ГПН у мышей G3, G4 и G6 были значимо ниже, чем у мышей G2 (P <0,05), что свидетельствует о том, что лечение эртапенемом (0,1 мг/г м.т. и 0,4 мг/г м.т.) было столь же эффективным для снижения уровня глюкозы в крови у db/db мышей, как лечение метформином (0,3 мг/г м.т.).
На 6 неделе уровни ГПН у мышей G3, G4, G5 и G6 были значимо ниже, чем у мышей G2 (P <0,05), что указывает на то, что эртапенем во всех концентрациях оказывал такое же действие на уровень глюкозы в крови у db/db мышей со спонтанным диабетом 2 типа, что и метформин (0,3 мг/г м.т.).
На 9, 12, 16 и 18 неделе уровни ГПН у мышей, получавших метформин (G3), были такими же, как у не получавших лечение db/db мышей (G2). Это возможно, поскольку метформин имеет период полувыведения из плазмы всего около 6 часов и выводится из крови в течение 24 часов.
Неожиданно, на 9 неделе уровни ГПН у мышей G6 были значимо ниже, чем у мышей G2 (P <0,05) и G3 (P = 0,0059), а у мышей G4 и G5 также были ниже, чем у мышей G3 (P <0,05). На 12-й неделе уровни ГПН у мышей G4, G5 и G6 были все еще ниже, чем у мышей G2, и не было значимых различий в уровнях ГПН среди мышей G4, G5 и G6. Эти результаты ясно показали, что действие эртапенема является длительным и продолжительным.
Эти результаты ясно показали, что эртапенем так же эффективен, как и метформин, в контроле уровня глюкозы в крови, и что действие эртапенема по снижению уровня глюкозы в крови длился не менее 6 недель у мышей, даже несмотря на то, что лечение эртапенемом было прекращено.
(2-3) Лечение эртапенемом повышает толерантность к глюкозе при пероральном введении
ПТТГ проводился на 6, 12, 16 и 18 неделе после лечения (возраст мышей 14, 20, 24 и 26 недель).
Как показано в таблице 8 и на Фигуре 4, эртапенем значимо повышал толерантность к глюкозе при пероральном введении (ТГ) db/db мышей в большинстве точек времени в течение нескольких недель 6 и 12. Однако не было обнаружено никаких значимых изменений в ТГ у мышей, получавших метформин, и только небольшие изменения наблюдались среди групп db/db мышей в большинстве точек измерения на 16 и 18 неделе.
Таблица 8. Уровни ПТТГ среди групп на 6, 12, 16 и 18 неделе
+ 0,3 Met
+ 0,1 DMH
+ 0,2 DMH
+ 0,4 DMH
+ 0,3 Met
+ 0,1 DMH
+ 0,2 DMH
+ 0,4 DMH
+ 0,3 Met
+ 0,1 DMH
+ 0,2 DMH
+ 0,4 DMH
+ 0,3 Met
+ 0,1 DMH
+ 0,2 DMH
+ 0,4 DMH
В Таблице 8 приведены значения групповых средних ± СОС уровней ПТТГ. Разница между значениями была значимой (P <0,05), если выделенные курсивом буквы в надстрочном индексе не перекрывались, как объяснено выше.
Затем строили и рассчитывали общую площадь под кривой (AUC) в ПТТГ, как показано ниже в Таблице 9. Результаты показали, что AUC мышей, получавших эртапенем (G4 и G5), были значимо меньше (P<0,05), чем у мышей, получавших метформин (G3), и не получавших лечение db/db мышей (G2) на 6, 12 и 16 неделях. Не было статистической значимости в значениях AUC между группами G2 и G3 в любых точках измерения.
Таблица 9. AUC ПТТГ шести групп мышей
В Таблице 9 выше перечислены значения групповых средних ± СОС для AUC ПТТГ, и разница между значениями была значимой (P <0,05), если выделенные курсивом буквы в надстрочном индексе не перекрывались, как объяснено выше.
Эти результаты продемонстрировали, что эртапенем эффективно увеличивал толерантность к глюкозе при пероральном введении у db/db мышей даже после прекращения лечения в течение 10 недель.
(2-4) Уровни воспалительных маркеров при лечении DMH
Уровни воспалительных маркеров измеряли на 19 неделе. Глюкоза крови (GLU) и креатинин (Cr) были одинаковыми среди мышей в опытных группах (от G2 до G6), но были выше, чем у мышей из группы G1. Не было обнаружено значимых изменений других воспалительных маркеров среди мышей в опытных группах (G2 - G6).
(2-5) Гистологические изменения после лечения DMH
Гистологически исследовали печень, почки, поджелудочную железу и эпидидимальную жировую ткань мышей на предмет повреждений.
Как показано на Фигуре 5, результаты исследования показали отсутствие гистологических изменений в поджелудочной железе у всех мышей. Было обнаружено, что следовые количества гликогена накапливаются в гепатоцитах, окружающих центральную вену, у db/db мышей, но не у m/m мышей.
Не было обнаружено гистологических изменений в почках m/m мышей, но у некоторых db/db мышей наблюдались дегенерация и некроз эпителиальных клеток почечных канальцев, минеральные и гиалиновые отложения. Эти гистологические изменения были более очевидны у мышей, получавших метформин, чем у мышей, получавших эртапенем.
В эпидидимальной жировой ткани жировые капли были больше у db/db мышей, чем у m/m мышей, и гистологических различий между группами не наблюдалось.
После лечения эртапенемом не наблюдалось значительных повреждений печени, почек, поджелудочной железы и эпидидимальной жировой ткани.
Пример 3: Влияние лечения бета-лактамного соединения на нарушение метаболизма глюкозы после прекращения лечения.
Чтобы изучить влияние бета-лактамных соединений после прекращения лечения, шесть 8-недельных m/m мышей использовали в качестве нормального контроля (G7), и 42 7- или 8-недельных db/db мышей случайным образом распределили на 7 групп (от G8 до G14). Каждая группа получала различное лечение, как описано в ниже Таблице 10.
Таблица 10. Мыши были распределены на 8 групп для различного лечения
В частности, лечение, полученное каждой группой, было следующим:
G7: m/m мыши, вода без ограничений, физиологический раствор в.б. (10 мкл/г м.т.) ежедневно;
G8: db/db мыши, вода без ограничений, физиологический раствор в.б. (10 мкл/г м.т.) ежедневно;
G9: db/db мыши, эртапенем (DMH) в.б. (0,41 мг/г м.т., что эквивалентно 0,033 г/кг для человека) ежедневно;
G10: db/db мыши, меропенем гидрат (MER), в.б. (0,205 мг/г м.т., что эквивалентно 0,017 г/кг для человека) ежедневно;
G11: db/db мыши, цефтриаксон (CEFT) в.б. (0,82 мг/г м.т., что эквивалентно 0,067 г/кг для человека) ежедневно;
G12: db/db мыши, пенициллин G (PEN) в.б. (1,473 мг/г м.т., что эквивалентно 0,12 г/кг для человека) ежедневно;
G13: db/db мыши, тиенам (TIE) в.б. (0,41 мг/г м.т., что эквивалентно 0,033 г/кг для человека) ежедневно; и
G14: db/db мыши, метформин (MET) перорально (0,3 мг/г м.т.) ежедневно.
Лечение длилось в общей сложности три недели; то есть введение всех лекарственных препаратов было прекращено через три недели. Тесты или измерения проводили в заранее определенные моменты времени, включая начало введения лекарственного препарата (также обозначенное как исходный уровень или 0 неделя), момент времени, когда введение лекарственного препарата продолжалось в течение 3 недель (также обозначен как неделя 3), момент времени через 3 недели после того как введение лекарственного препарата было прекращено (также обозначен как неделя 6), и момент времени через 6 недель после того как введение лекарственного препарата было прекращено (также обозначен как неделя 9). Тесты и результаты были описаны следующим образом.
(3-1) Влияние лечения бета-лактамным соединением на массу тела
Как показано ниже в Таблице 11, было обнаружено, что, за исключением контрольной группы, мыши G12 имели самую низкую массу тела в течение всего периода исследования (P <0,05)
Таблица 11. Масса тела среди групп мышей
Неделя
m/m
db/db
db/db
+DMH
db/db
+MER
db/db
+CEFT
db/db
+PEN
db/db
+TIE
db/db
+MET
В Таблице 11 выше представлены значения группового среднего ± СОС массы тела, и разница между значениями была значимой (P <0,05), если выделенные курсивом буквы в надстрочном индексе не перекрывались, как объяснено выше.
(3-2) Влияние лечения бета-лактамным соединением на потребление корма и воды
Как показано ниже в Таблице 12, было обнаружено, что лечение DMH, CEFT и PEN значимо снижало потребление корма у db/db мышей (P <0,05), а лечение DMH, CEFT, TIE и PEN значимо снижало потребление воды у db/db мышей (P <0,05).
Таблица 12. Среднее потребление корма и воды среди групп мышей
Группы
(г/мышь/сутки)
(мл/мышь/сутки)
В Таблице 12 выше представлены значения группового среднего ± СОСО потребления корма и воды, и разница между значениями была значимой (P <0,05), если выделенные курсивом буквы в надстрочном индексе не перекрывались, как объяснено выше.
(3-3) Влияние лечения бета-лактамным соединением на толерантность к глюкозе при пероральном введении
ПТТГ проводили на 6-й и 9-й неделе, то есть в моменты времени, на 3-й и 6-й неделе после прекращения введение лекарственного препарата, соответственно.
Как показано на Фигуре 6А, концентрации глюкозы в группах G9 и G12 были значимо ниже, чем в группе G8, в моменты времени 30 мин и 60 мин; также, как показано на Фигуре 6B, концентрации глюкозы в группах G9 и G12 были значимо ниже, чем в группе G8 в моменты времени 30 мин, 60 мин и 120 мин, что позволяет предположить, что DMH и PEN по-прежнему эффективны в регуляции гомеостаза глюкозы в крови, даже если прием лекарственных средств был прекращен, по меньшей мере, на 3 недели.
Кроме того, строили и рассчитывали общую AUC в ПТТГ, как показано в Таблице 13 ниже. Результаты показали, что AUC в случае лечения бета-лактамным соединением (т.е. группы G9 - G13) были меньше (P <0,05), чем у не получавших лечение мышей (группа G8), даже после того, как лечение было прекращено, по меньшей мере, на 3 недели.
Таблица 13. AUC ПТТГ восьми групп мышей
Группы
В Таблице 13 выше перечислены значения группового среднего ± СОС для AUC ПТТГ, и разница между значениями была значимой (P <0,05), если выделенные курсивом буквы в надстрочном индексе не перекрывались, как объяснено выше.
(3-4) Анализ биохимических параметров плазмы крови
Концентрации AST, ALT, BUN, Cr и HbA1c в плазме крови каждой группы мышей измеряли на 9 неделе, то есть через 6 недель после прекращения лечения. Результаты суммированы ниже в Таблице 14.
Было обнаружено, что уровни AST, ALT, BUN, Cr и HbA1c у мышей с диабетом были снижены при лечении бета-лактамными соединениями. Например, DMH может снижать уровни AST, ALT и HbA1c; MER может снижать уровень AST; CEFT может снижать уровни AST, ALT, BUN, Cr и HbA1c; PEN может снижать уровень ALT, BUN, Cr и HbA1c; и TIE может снижать уровень HbA1c даже после прекращения лечения на 6 недель.
Таблица 14. Биохимические параметры плазмы крови в каждой группе мышей
Группы
(Ед/л)
(Ед/л)
(мг/дл)
(%)
В Таблице 14 выше перечислены значения группового среднего ± СОС каждого параметра, и разница между значениями была значимой (P <0,05), если выделенные курсивом буквы в надстрочном индексе не перекрывались, как объяснено выше.
Из вышеизложенного можно видеть, что бета-лактамные соединения настоящего изобретения проявляют эффект длительного действия в улучшении нарушения метаболизма глюкозы и, таким образом, могут быть применимы для улучшения качества жизни пациентов и их приверженности лечению при нарушении метаболизма глюкозы.
Хотя некоторые из вариантов осуществления настоящего раскрытия были подробно описаны выше, тем не менее, специалисты в данной области техники могут внести различные модификации и изменения в показанные конкретные варианты осуществления изобретения без существенного отклонения от идеи и преимуществ настоящего изобретения. Такие модификации и изменения включены в сущность и объемом настоящего изобретения в соответствии с прилагаемой формулой изобретения.



Изобретение относится к способу долгосрочного лечения сахарного диабета 2 типа у нуждающегося в этом субъекта. Способ лечения включает введение субъекту соединения, которое представляет собой карбапенем, в эффективном количестве. При этом долгосрочное лечение диабета 2 типа представляет собой лечение симптома диабета 2 типа в течение по крайней мере одной недели после введения соединения. Изобретение обеспечивает лечение диабета 2 типа с длительным действием, которое длится по крайней мере одну неделю даже после прекращения приема лекарственного препарата, что позволяет улучшить качество жизни пациентов и их приверженность лечению. 5 з.п. ф-лы, 6 ил., 14 табл., 3 пр.
1. Способ долгосрочного лечения сахарного диабета 2 типа у нуждающегося в этом субъекта, где соединение, которое представляет собой карбапенем, вводят субъекту в эффективном количестве, где долгосрочное лечение диабета 2 типа представляет собой лечение симптома диабета 2 типа в течение по крайней мере одной недели после введения соединения.
2. Способ по п. 1, где соединение является эртапенем, дорипенем, имипенем, меропенем, биапенем, панипенем, томопенем, ленапенем, тебипенем, разупенем или тиенпенем.
3. Способ по п. 1, где долгосрочное лечение длится, по меньшей мере, 6 недель после введения.
4. Способ по п. 1, где долгосрочное лечение длится от 6 до 10 недель после введения.
5. Способ по п. 1, где субъектом является млекопитающее.
6. Способ по п. 1, где субъектом является человек.
| WO 1993015078 A1, 05.08.1993 | |||
| WO 2017165599 A1, 28.09.2017 | |||
| WO 2016030500 A2, 03.03.2016 | |||
| WO 2013042121 A1, 28.03.2013 | |||
| K.H | |||
| MIKKELSEN ET AL | |||
| Effect of antibiotics on gut microbiota, glucose metabolism and body weight regulation: a review of the literature | |||
| Diabetes, Obesity and Metabolism | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| K.H | |||
Авторы
Даты
2024-01-12—Публикация
2020-01-20—Подача