ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к химии органических соединений, фармакологии, медицине, а именно изобретение относится к соединениям для применения с целью ингибирования активности цитохрома P450 11B2 человека (CYP11B2) и их применению в лечении и/или профилактике различных заболеваний и расстройств, которые опосредованы или поддерживаются активностью гормона альдостерона. Настоящее изобретение также относится к фармацевтическим композициям, содержащим соединения по изобретению, и способам получения этих соединений.
УРОВЕНЬ ТЕХНИКИ
Альдостерон - это стероидный гормон, основная физиологическая роль которого заключается в поддержании баланса натрия и калия путем регулирования катионного обмена (реабсорбции Na+ и секреции K+) в дистальном нефроне, что, в свою очередь, приводит к повышению кровяного давления. Помимо физиологической роли, альдостерон также вовлечен в патогенез заболеваний или патологических состояний, вызванных (первичный гиперальдостеронизм) и/или сопровождающихся его гиперсинтезом (вторичный гиперальдостеронизм), включая ряд заболеваний сердечно-сосудистой системы, почек и метаболический синдром.
Современные подходы к терапии состояний, вызванных и/или сопровождающихся гиперсинтезом альдостерона, включают воздействие на различные уровни ренин-ангиотензин-альдостероновой системы (РААС). Современные стандарты медицинской помощи представлен такими классами лекарственных средств, как ингибиторы ренина (ИР), блокаторы рецепторов ангиотензина II (БРА), ингибиторы ангиотензин-превращающего фермента (ИАПФ) и блокаторы минералокортикоидных рецепторов (МР). Однако у 25-50% пациентов, получавших ИР, БРА и ИАПФ по отдельности или в комбинации, уровни альдостерона в сыворотке в конечном итоге возвращаются к уровням до лечения или выше (прорыв альдостерона) (Bomback et al., 2007, Nature Clinical Practice. Nephrology, 3, 486-492; Bomback et al., 2012, J Am Soc Hypertens, 6(5):338-45), а введение блокаторов МР приводит к компенсаторному повышению уровней альдостерона в сыворотке (Pitt at al., 2013, Eur Heart J, 34:2453-2463; Calhoun et al., 2011, Circulation, 124, 1945-1955). В связи с этим на сегодняшний день по-прежнему отсутствует решение, которое сможет полностью охватить все патологические эффекты альдостерона у человека, включая как МР-опосредованные, так и не-МР-опосредованные эффекты. К последним относятся следующие: а) действуя через рецепторы GPER, альдостерон осуществляет так называемый “быстрый эффект”, приводящий к апоптозу и препятствованию пролиферации эндотелиальных и гладкомышечных клеток сосудов [Namsolleck et al., 2014, Nephrology, Dialysis, Transplantation, 29(Suppl. 1), i62-i68), нарушению вазоконстрикции (Feldman et al., 2013, Clinical and Experimental Pharmacology & Physiology, 40, 916-921) и воспалению эндотелия [Ziwei Tang et al., 2021, International Journal of Endocrinology, Volume 2021, Article ID 5575927]. Помимо этого, недавние исследования in vitro и ex vivo показали, что альдостерон также посредством активации GPER усиливает экспрессию гена CYP11B2 и, следовательно, усиливает свой собственный биосинтез и высвобождение (Caroccia et al., 2019, The Journal of Clinical Endocrinology & Metabolism, Volume 104, Issue 12, 6316-6324); б) повреждение бета-клеток поджелудочной железы (Luther et al., 2011, Diabetologia, 54, 2152-2163; Fang Chen et al., 2015, Scientific Reports volume 5, Article number: 13215 (2015), которое может привести к толерантности к глюкозе; c) взаимодействие с рецепторами IGF-I в гладкомышечных клетках сосудов со стимуляцией выработки эластина фибробластами (Mitts et al., 2010, Journal of Investigative Dermatology, Volume 130, Issue 10, 2396-2406), что может привести, в частности, к ремоделированию сосудов и указывать на механизм, с помощью которого альдостерон может ускорить развитие атеросклероза (Cascella et al., 2010, Endocrinology, 151(12):5851-64); d) индукция сужения сосудов через зависимые от протеинкиназы C пути, возможно, через мембранные рецепторы, что приводит к ухудшению сократительной и метаболической функций сердца в ишемизированных сердцах, поэтому повышение уровня альдостерона в плазме или в сердечной ткани может оказывать неблагоприятное действие при ишемической болезни сердца (Fujita et al., 2005, Hypertension, 46(1):113-7); e) MP-независимая активация калиевого тока (IK1) альдостероном, как показано, является основным механизмом, объясняющим увеличение желудочковой аритмии и внезапной сердечной смерти, сопровождающейся высоким уровнем альдостерона во время инфаркта миокарда с подъемом сегмента ST (STEMI) (Alexandre et al., 2015, PLoS One v.10(7); f) димеризация рецептора ангиотензина II типа (AT1) альдостероном может играть важную роль в патологических состояниях, включая гипертонию и атеросклероз (Sinphitukkul et al., 2019, Arch Med Sci, 15(6):1589-1598). Помимо этого, альдостерон продемонстрировал негеномный эндотелий-независимый сосудосуживающий эффект, также опосредованный через рецептор AT1 (Yamada et al., 2008, Cardiovasc Res, 79(1):169-78).
На основании вышеизложенного следует, что ингибирование синтеза альдостерона будет иметь терапевтическое преимущество перед существующими методами терапии, а также позволит преодолеть ограничения существующих стандартов оказания медицинской помощи.
Альдостерон синтезируется одним ферментом CYP11B2 (альдостеронсинтаза), который катализирует 3-ступенчатую конверсию 11-дезоксикортикостерона (11-DOC) в альдостерон через кортикостерон и 18-гидроксикортикостерон, поэтому CYP11B2 представляет собой потенциальную терапевтическую мишень для ингибирования синтеза альдостерона, что может иметь фармакодинамический профиль отличный от того, который наблюдается у других модуляторов РААС.
Из вышеизложенного очевидным образом следует, что агенты, способные ингибировать CYP11B2 (альдостеронсинтаза) могут применяться для лечения и/или профилактики заболевания или состояния, которое опосредовано или поддерживается гиперсинтезом альдостерона. Трансляция данных c in vitro исследований по ингибированию альдостеронсинтазы на результаты in vivo испытаний как на грызунах так и приматах продемонстрирована как минимум для 7 соединений, имеющих разную химическую структуру, и более того, для 3 из них показано действие по снижению уровня альдостерона в клинических испытаниях: LCI699 (Novartis), RO6836191 (Roche) и LY3045697 (Ely Lilly) [Aldosterone synthase inhibitors for cardiovascular diseases: A comprehensive review of preclinical, clinical and in silico data. Lenzini L et. al. Pharmacol Res. 2021 jan;163:105332. doi:10.1016/j.phrs.2020.105332; PMID: 33271294], [Inhibitors of Aldosterone Synthase. Weldon SM, Brown NF. Vitam Horm. 2019;109:211-239. doi: 10.1016/bs.vh.2018.10.002; PMID: 30678857; клинические испытания NCT00817635, NCT01995383, NCT01821703]. Следовательно, ингибирование активности альдостеронсинтазы в условиях in vitro будет также наблюдаться и в in vivo.
Более того, было показано, что CYP11B2-специфичная молекула может быть использована в качестве диагностического маркера различных заболеваний, связанных со сверхэкспрессией CYP11B2 [Development of [18F]AldoView as the First Highly Selective Aldosterone Synthase PET Tracer for Imaging of Primary Hyperaldosteronism. Sander K et al. J Med Chem. 2021; 8;64(13):9321-9329. doi: 10.1021/acs.jmedchem.1c00539. PMID: 34137616].
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В своих множественных вариантах воплощения настоящее изобретение представляет собой новые химические соединения, способные ингибировать активность фермента CYP11B2 человека, и их биологическая активность была исследована. Таким образом, изобретение относится к соединениям, фармацевтическим композициям, содержащим эти соединения, применению соединений, способам их применения при лечении, профилактике, диагностике различных заболеваний и расстройств, а также способам получения этих соединений.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Раскрытые здесь соединения ингибируют активность фермента CYP11B2 человека, и их биологическая активность была исследована.
Таким образом, изобретение относится к соединениям, фармацевтическим композициям, содержащим эти соединения, применению этих соединений, способам их применения при лечении различных заболеваний и расстройств, а также способам получения этих соединений.
В одном варианте воплощения настоящее изобретение обеспечивает соединение общей формулы (I):
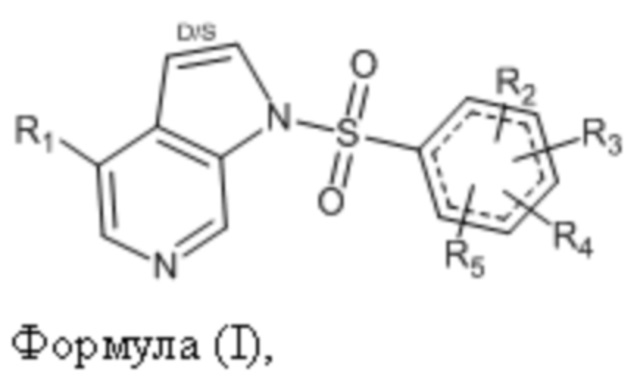
или его фармацевтически приемлемую соль, сольват или гидрат, где:
R1 представляет собой 5-6-членный гетероарил, содержащий 0-1 атома кислорода, 0-1 серы и/или 0-4 азота, необязательно замещенный 1-5 заместителями R1a,
R1a выбирается независимо и представляет собой водород, дейтерий, галоген, (C1-C3)алкил, (C3-C5)циклоалкил, -C(=O)-CH3, частично или полностью галогенированный (C1-C3)алкил, (C1-C3)алкилсульфонил, циано, N,N-диметиламин, N-метиламин;
R2, R3, R4, R5 каждый выбирается независимо и представляет собой:
- (i) водород, дейтерий, галоген, (C1-C3)-алкил, (C3-C5)-циклоалкил, -C(=O)-CH3, частично или полностью галогенированный (C1-C3)алкил, или
- (ii) -OH, -SH, или
- (iii) -(C1-C3)-алкокси, 3-7-членный гетероциклил, содержащий 0-2 атома азота, 0-1 атома кислорода и/или 0-1 серы, (C3-C7)-циклоалкил, -S-(C1-C3)-алкил, -(C3-C7)-циклоалкил-S-(C1-C3)-алкил, причем каждая из вышеуказанных групп необязательно частично или полностью замещена заместителями, выбранными из -OH, 1-4 атома галогена, (C1-C3)-алкокси, (C3-C7)-циклоалкила, 3-7-членного гетероцикла, содержащего один атом кислорода, -NH2, (C1-C3)-алкиламино, ди(C1-C3)-алкиламино или 3-7-членный гетероцикл, содержащий один атом азота и необязательно 1-2 гетероатома кислорода и/или серы; или
- (iv) -NRaRb, где каждый Ra и Rb:
- независимо представляет собой водород, дейтерий, (C3-C7)-циклоалкил, -(C1-C3)-алкил-N(CH3)2, (C1-C3)-алкил, частично или полностью галогенированный (C1-C3)-алкил, 3-7-членный гетероциклил, содержащий 0-1 атом кислорода, 0-1 атом серы и/или 0-4 атом азота, необязательно замещенный 1-2 заместителями, выбранными из (C1-C3)-алкила или частично или полностью галогенированного (C1-C3)-алкила, 5-7-членный гетероарил, содержащий 0-1 атом кислорода, 0-1 атом серы и/или 0-4 атом азота, причем указанный гетероарил необязательно замещен 1-2 заместителями, выбранными из (C1-C3)-алкила или частично или полностью галогенированного (C1-C3)-алкила,
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 4-7-членный гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-2 заместителями, выбранными из (C1-C3)-алкила, частично или полностью галогенированным (C1-C3)-алкилом, или
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 6-14-членный бициклический гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-4 заместителями, выбранными из дейтерия, галогена, (C1-C3)-алкила, частично или полностью галогенированного (C1-C3)-алкила, (C2-C3)-алкенила, (C2-C3)-алкинила и (C1-C3)-алкокси;
D/S - означает наличие двойной или одинарной связи;
пунктирные связи означают, что кольца ароматические.
В другом варианте воплощения настоящее изобретение включает соединения формулы (I), как определено выше, по меньшей мере два из R2, R3, R4 и R5 отличны от водорода.
В другом варианте воплощения настоящее изобретение включает соединения формулы (I), как определено выше, по меньшей мере три из R2, R3, R4 и R5 отличны от водорода.
В другом варианте воплощения в соединениях формулы (I), как определено выше, R2, R3, R4 и R5 каждый выбирается независимо и представляют собой:
- (i) водород, дейтерий, галоген, (C1-C3)-алкил, (C3-C5)-циклоалкил, -C(=O)-CH3, частично или полностью галогенированный (C1-C3)-алкил;
- (ii) группу, выбранную из (C1-C3)-алкокси, (C3-C7)циклоалкила, галогегенированной (C1-C3)алкокси группы, содержащей 1-4 атома галогена;
- (iii) -NRaRb, где каждый Ra и Rb:
- независимо представляет собой водород, дейтерий, (C3-C7)-циклоалкил, -(C1-C3)-алкил-N(CH3)2, (C1-C3)-алкил, частично или полностью галогенированный (C1-C3)-алкил, 3-7-членный гетероциклил, содержащий 0-1 атом кислорода, 0-1 атом серы и/или 0-4 атома азота, необязательно замещенный 1-2 заместителями, выбранными из (C1-C3)-алкила, частично или полностью галогенированного (C1-C3)-алкил, 5-7-членный гетероарил, содержащий 0-1 атом кислорода, 0-1 атом серы и/или 0-4 атома азота, необязательно замещенный 1-2 заместителями, выбранными из (C1-C3)-алкила, частично или полностью галогенированного (C1-C3)-алкила,
- альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 4-7-членный гетероциклил, необязательно замещенный 1-2 заместителя, выбранными из (C1-C3)-алкила, частично или полностью галогенированного (C1-C3)-алкила, или
- Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 6-14-членный бициклический гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-4 заместителями, выбранными из дейтерия, галогена, (C1-C3)-алкила, частично или полностью галогенированного (C1-C3)-алкила, (C2 C3)-алкенила, (C2-C3)-алкинила и (C1-C3)-алкокси.
В другом варианте воплощения в соединениях формулы (I), как определено выше, по меньшей мере один из R2, R3, R4 и R5 находятся в пара-положении и каждый выбирается независимо и представляет собой:
-OH, -SH, (C1-C3)-алкокси, 3-7-членный гетероциклил, содержащий 0-1 атома кислорода и/или 0-1 серы, (C3-C7)-циклоалкил, -S-(C1-C3)-алкил, (C3-C7)-циклоалкил-S-(C1-C3)-алкил, причем каждая из вышеуказанных групп необязательно частично или полностью замещена заместителями, выбранными из -OH, 1-4 атома галогена, (C1-C3)-алкокси, (C3-C7)-циклоалкила, 3-7-членного гетероцикла, содержащего один атом кислорода, -NH2, (C1-C3)-алкиламино, ди(C1-C3)-алкиламино или 3-7-членный гетероцикл, содержащий один атом азота и необязательно 1-2 гетероатома кислорода и серы; или
- NRaRb, где каждый Ra и Rb:
- независимо представляет собой водород, дейтерий, (C3-C7)-циклоалкил, -(C1-C3)-алкил-N(CH3)2, (C1-C3)-алкил, частично или полностью галогенированный (C1-C3)-алкил, 3-7-членный гетероцикл, содержащий 0-1 атома кислорода, 0-1 серы и/или 0-4 азота, необязательно замещенный 1-2 заместителями, выбранными из (C1-C3)-алкила или частично или полностью галогенированного (C1-C3)-алкила, 5-7-членный гетероарил, причем указанный гетероарил необязательно замещен 1-2 заместителями, выбранными из (C1-C3)-алкила или частично или полностью галогенированного (C1-C3)-алкила,
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 4-7-членный гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-2 заместителями, выбранными из (C1-C3)-алкила, частично или полностью галогенированного (C1-C3)-алкила, или
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 6-14-членный бициклический гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-4 заместителями, выбранными из дейтерия, галогена, (C1-C3)-алкила, частично или полностью галогенированного (C1-C3)-алкила, (C2-C3)-алкенила, (C2-C3)-алкинила или (C1-C3)-алкокси.
В другом варианте воплощения в соединениях формулы (I), как определено выше, R1 представляет собой группу, выбранную из пиридинила, пиразинила, пиримидинила, пиридазинила, оксазила, необязательно замещенную группой, выбранной из метила, метилсульфонила, галогена, такого как фтор, метиламино, циано и циклопропил.
В другом варианте воплощения в соединениях формулы (I), как определено выше, два радикала из R2, R3, R4 и R5 находятся в мета-положении и представляют собой группу, выбранную из метила или галогена, один из R2, R3, R4 и R5 представляет собой водород и один из R2, R3, R4 и R5 находится в пара-положении и представляет собой группу, выбранную из метокси, изопропокси, циклопропилметокси, дифторэтокси, NH2, -N(CH3)2, циклопропиламино, -N(CH3)-циклобутил, N-метилтиазолил, метилпиперидиниламино, -NH-(C1-C3)-алкил-N(CH3)2, морфолинил, метилпиперазинил, азетидинил, необязательно замещенный метилом, тиоморфолинил, гексагидропирролопирролил, необязательно замещенный метилом, диазаспирононанил, октагидропирролопиридинил, необязательно замещенный метилом.
В другом варианте воплощения настоящее изобретение включает соединение Формулы (Ia):

или его фармацевтически приемлемую соль, сольват или гидрат, где:
R1 как определено выше,
R6 выбирается независимо и представляет собой:
- -OH, -SH, -(C1-C3)-алкокси, 3-7-членный гетероциклил, содержащий 0-1 атома кислорода и/или 0-1 серы, (C3-C7)-циклоалкил, -S-(C1-C3)-алкил, (C3-C7)-циклоалкил-S-(C1-C3)-алкил, причем каждая из вышеуказанных групп необязательно частично или полностью замещена заместителями, выбранными из -OH, 1-4 атома галогена, (C1-C3)-алкокси, (C3-C7)-циклоалкила, 3-7-членного гетероцикла, содержащего один атом кислорода, -NH2, (C1-C3)-алкиламино, ди(C1-C3)-алкиламино или 3-7-членный гетероцикл, содержащий один атом азота и необязательно 1-2 гетероатома выбирают из кислорода и серы, или
- -NRaRb, где каждый Ra и Rb:
- независимо представляет собой водород, дейтерий, (C3-C7)-циклоалкил, -(C1-C3)-алкил-N(CH3)2, (C1-C3)-алкил, частично или полностью галогенированный (C1-C3)-алкил, 3-7-членный гетероцикл, содержащий 0-1 атома кислорода, 0-1 серы и/или 0-4 азота, необязательно замещенный 1-2 заместителями, выбранными из (C1-C3)-алкила или частично или полностью галогенированного (C1-C3)-алкила, 5-7-членный гетероарил, причем указанный гетероарил необязательно замещен 1-2 заместителями, выбранными из (C1-C3)-алкила или частично или полностью галогенированного (C1-C3)-алкила,
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 4-7-членный гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-2 заместителями, выбранными из (C1-C3)-алкила, частично или полностью галогенированным (C1-C3)-алкилом, или
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 6-14-членный бициклический гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-4 заместителями, выбранными из дейтерия, галогена, (C1-C3)-алкила, частично или полностью галогенированного (C1-C3)-алкила, (C2-C3)-алкенила, (C2-C3)-алкинила или (C1-C3)-алкокси.
В другом варианте воплощения настоящее изобретение включает соединение Формулы (IIa):

или его фармацевтически приемлемую соль, сольват или гидрат, где:
R1 и R6 как определено выше.
В другом варианте воплощения настоящее изобретение включает соединение Формулы (Ib):

или его фармацевтически приемлемую соль, сольват или гидрат, где:
Q1, Q2, Q3, Q4, Q5 каждый выбирается независимо и представляет собой азот или углерод, причем не более двух из Q1, Q2, Q3, Q4 и Q5 представляют собой азот, и указанный углерод необязательно замещен 1-5 группами R1a,
R1a такой же, как описано выше,
R2, R3, R4, R5 такие же, как описано выше;
пунктирные связи означают, что кольца ароматические.
В другом варианте воплощения настоящее изобретение включает соединение Формулы (Ic):
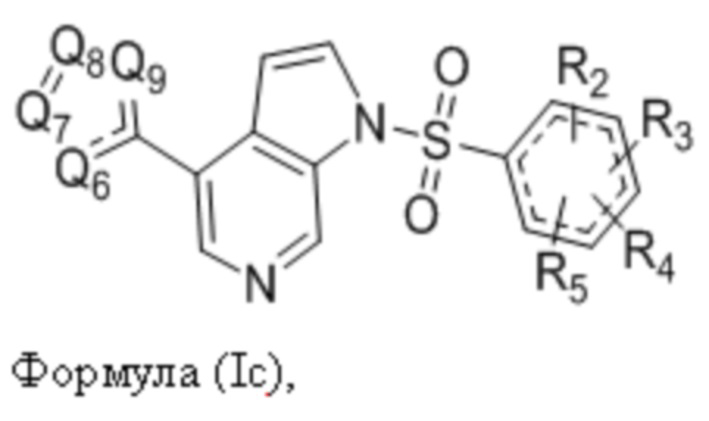
или его фармацевтически приемлемую соль, сольват или гидрат, где:
Q6, Q7, Q8, Q9 каждый выбирается независимо и представляют собой кислород, углерод или азот, причем не более двух из Q6, Q7, Q8 и Q9 представляют собой азот или кислород, и указанный углерод необязательно замещен 1-4 группами R1a,
R1a такой же, как описано выше,
R2, R3, R4, R5 такие же, как описано выше;
пунктирные связи означают, что кольца ароматические.
В другом варианте воплощения настоящее изобретение включает соединение Формулы (Id):

или его фармацевтически приемлемую соль, сольват или гидрат, где:
Q1, Q2, Q3, Q4, Q5, R1a и R6 как определено выше.
В другом варианте воплощения настоящее изобретение включает соединение Формулы (Ie):
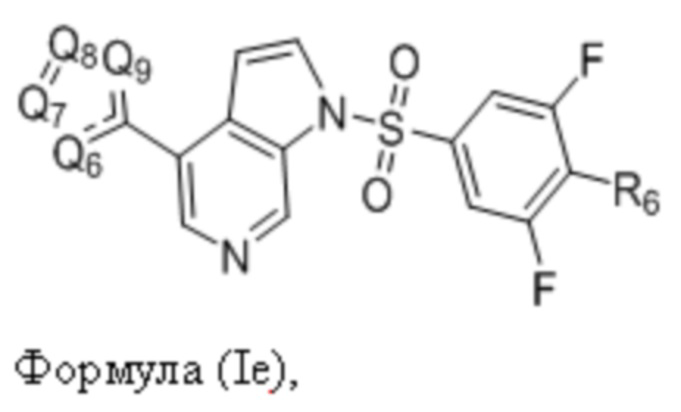
или его фармацевтически приемлемую соль, сольват или гидрат, где:
Q6, Q7, Q8, Q9, R1a и R6 как определено выше.
В другом варианте воплощения настоящее изобретение включает соединение Формулы (If):

или его фармацевтически приемлемую соль, сольват или гидрат, где:
R1 и R6 как определено выше.
В другом варианте воплощения настоящее изобретение включает соединение Формулы (IIb):

или его фармацевтически приемлемую соль, сольват или гидрат, где:
Q1, Q2, Q3, Q4, Q5, R2, R3, R4 и R5 как определено выше;
пунктирные связи означают, что кольца ароматические.
В другом варианте воплощения настоящее изобретение включает соединение Формулы (IId):

или его фармацевтически приемлемую соль, сольват или гидрат, где:
Q1, Q2, Q3, Q4, Q5 и R6 как определено выше.
В частных вариантах воплощения настоящее изобретение включает соединения, выбранные из группы (названия приведены в соответствии с IUPAC):
1-(4-метокси-3,5-диметилфенил)сульфонил-4-(5-метил-2-пиридил)пирроло[2,3-c]пиридин
1-((4-метокси-3,5-диметилфенил)сульфонил)-4-(5-метилпиразин-2-ил)-1H-пирроло[2,3-с] пиридин
1-((4-метокси-3,5-диметилфенил)сульфонил)-4-(5-метилпиримидин-2-ил)-1H-пирроло[2,3-c]пиридин
1-(4-метокси-3,5-диметилфенил)сульфонил-4-(6-метилпиридазин-3-ил)пирроло[2,3-с] пиридин
1-(4-метокси-3,5-диметилфенил)сульфонил-4-(5-метилсульфонил-2-пиридил)пирроло[2,3-с] пиридин
1-((3,5-дифтор-4-изопропоксифенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин
1-((4-(циклопропилметокси)-3,5-дифторфенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин
1-((4-(2,2-дифторэтокси)-3,5-дифторфенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин
2,6-дифтор-N,N-диметил-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)анилин
4-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)морфолин
2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)анилин
1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин
N-циклопропил-2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло [2,3-c] пиридин-1-ил)сульфонил)анилин
N-циклобутил-2,6-дифтор-N-метил-4 - ((4- (пиридин-2-ил) -1H-пирроло [2,3-c] пиридин-1-ил) сульфонил) анилин
2,6-дифтор-N,N-диметил-4-((4-(пиридин-2-ил)-2,3-дигидро-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил) анилин
2,6-дифтор-4-((4-(пиридин-2-ил)-2,3-дегидро-H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенол
1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-4-(пиридин-2-ил)-2,3-дигидро-1Н-пирроло[2,3- с] пиридин
1-((3,5-дифтор-4-метоксифенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин
1-((3,5-дифтор-4-(3-метилазетидин-1-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин
N-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)-N,4-диметилтиазол- 2-амин
N-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)-1-метилпиперидин-4- амин
N1-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)-N2,N2-диметилэтан- 1,2-диамин
4-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)тиоморфолин
1-((3,5-дифтор-4-(5-метилгексагидропирроло[3,4-c]пиррол-2(1H)-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло [2,3-с]пиридин
1-((3,5-дифтор-4-(5-метилоктагидро-2H-пирроло[3,4-c]пиридин-2-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1H- пирроло[2,3-c]пиридин
2-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)-2,7-диазаспиро[4.4] нонан
2-(1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1H-пирроло[2,3-c]пиридин-4-ил)оксазол-4-карбонитрил
5-(1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1H-пирроло[2,3-c]пиридин-4-ил)пиколинитрил
1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-4-(5-фторпиримидин-2-ил)-1H-пирроло[2,3-c]пиридин
5-(1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1H-пирроло[2,3-c]пиридин-4-ил)-N-метилпиразин- 2-амин
4-(5-циклопропилпиридин-2-ил)-1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1H-пирроло[2,3-c]пиридин
2,6-дифтор-4-((4-(5-метилпиразин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)анилин
2,6-дифтор-N,N-диметил-4-((4-(5-метилпиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)анилин
Соединения по изобретению могут существовать в виде различных стереоизомеров, диастереомеров или энантиомеров или их смесей. Все эти формы являются частью изобретения.
Данное изобретение также относится к применению соединений по изобретению для ингибирования CYP11B2.
Настоящее изобретение также относится к применению соединений по изобретению для снижения уровня альдостерона у субъекта.
В частных вариантах воплощения изобретения субъект представляет собой человека.
Изобретение также включает фармацевтическую композицию для лечения и/или профилактики заболевания или состояния, которое опосредовано или поддерживается гиперсинтезом альдостерона, включающая терапевтически или профилактически эффективное количество соединения по изобретению и, по меньшей мере, одно фармацевтически приемлемое вспомогательное вещество.
В частных вариантах воплощения изобретения фармацевтически приемлемое вспомогательное вещество представляет собой носитель, адъювант и/или растворитель.
В частных вариантах воплощения изобретения заболевание выбрано из группы, включающей первичный гиперальдостеронизм (синдром Конна), хроническую сердечную недостаточность, хроническую сердечную недостаточность с сохраненной фракцией выброса, дисфункцию левого желудочка, гипертрофию левого желудочка, артериальную гипертензию, резистентную артериальную гипертензию, легочную артериальную гипертензию, коронарную болезнь сердца, цирроз печени, метаболический синдром, хроническую болезнь почек, гломерулосклероз, гломерулонефрит, нефритический синдром, фокальный сегментарный гломерулосклероз, диабетическую нефропатию, ремоделирование сердца и сосудов, постинфарктный кардиосклероз, атеросклероз, повышенное коллагенообразование, дисфункцию эндотелия, гипокалиемию или инсулинорезистентность.
В частных вариантах воплощения изобретения первичный гиперальдостеронизм представляет собой синдром Конна, включающий следующие заболевания или состояния: альдостеронпродуцирующая аденома, идиопатический гиперальдостеронизм, одно- или билатеральная гиперплазия надпочечников, семейный гиперальдостеронизм первого и второго типа, альдостеронпродуцирующая карцинома и альдостеронэктопированный.
Данное изобретение также относится к способу снижения уровня альдостерона у субъекта, включающему введение субъекту терапевтически эффективного количества соединения по изобретению.
Изобретение также включает способ лечения и/или профилактики заболевания или состояния, которые опосредовано или поддерживается гиперсинтезом альдостерона, у субъекта, включающий введение терапевтически или профилактически эффективного количества соединения по изобретению.
В частных вариантах воплощения изобретения заболевание или состояние выбрано из группы, включающей первичный гиперальдостеронизм (синдром Конна), хроническую сердечную недостаточность, хроническую сердечную недостаточность с сохраненной фракцией выброса, дисфункцию левого желудочка, гипертрофию левого желудочка, артериальную гипертензию, резистентную артериальную гипертензию, легочную артериальную гипертензию, коронарную болезнь сердца, цирроз печени, метаболический синдром, хроническую болезнь почек, гломерулосклероз, гломерулонефрит, нефритический синдром, фокальный сегментарный гломерулосклероз, диабетическую нефропатию, ремоделирование сердца и сосудов, постинфарктный кардиосклероз, атеросклероз, повышенное коллагенообразование, дисфункцию эндотелия, гипокалиемию или инсулинорезистентность.
В частных вариантах воплощения изобретения первичный гиперальдостеронизм представляет собой синдром Конна, включающий следующие заболевания или состояния: альдостеронпродуцирующая аденома, идиопатический гиперальдостеронизм, одно- или билатеральная гиперплазия надпочечников, семейный гиперальдостеронизм первого и второго типа, альдостеронпродуцирующая карцинома и альдостеронэктопированный.
В частных вариантах воплощения изобретения субъект представляет собой человека.
Изобретение также включает способ диагностики или тераностики заболевания или состояния у субъекта, которые опосредовано или поддерживается активностью CYP11B2, включающий введение эффективного количества соединения по изобретению.
Настоящее изобретение также относится к применению соединений по изобретению для получения ингибитора CYP11B2.
Настоящее изобретение также относится к применению соединений изобретения для получения средства для снижения уровня альдостерона у субъекта.
Настоящее изобретение также относится к применению соединений по изобретению для получения фармацевтической композиции для лечения и/или профилактики заболевания или состояния, которое опосредовано или поддерживается гиперсинтезом альдостерона, включающей терапевтически или профилактически эффективное количество соединение по изобретению и по меньшей мере один фармацевтически приемлемое вспомогательное вещество.
Технический результат настоящего изобретения заключается в разработке химических соединений, характеризующихся высокой эффективностью в ингибировании активности цитохрома 11B2 человека (CYP11B2). Указанные соединения являются перспективными для профилактики и/или терапии заболеваний или патологических состояний или расстройств, которые опосредованы или поддерживаются гиперсинтезом альдостерона.
Подробное раскрытие изобретения
Определения (термины)
Для лучшего понимания настоящего изобретения ниже приведены некоторые термины, использованные в настоящем описании изобретения. Следующие определения применяются в данном документе, если иное не указано явно. Кроме того, если не указано иное, все вхождения функциональных групп выбираются независимо, на что может указывать использование косого штриха для определения, что два вхождения могут быть как одинаковыми, так и разными (например, R и т.п.). В описании данного изобретения термины «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из».
Термин «алкил» в настоящем документе сам по себе или как часть другого заместителя, относится к насыщенным углеводородным группам с прямой или разветвленной цепью, включая углеводородные группы, имеющие указанное число атомов углерода, относится к группам, обычно имеющим от одного до десяти атомов углерода. Например, термин -C1-3-алкил означает, метил, этил, пропил, изопропил и т.д.
Термин «алкенил», используемый здесь, относится к линейной или разветвленной алифатической группе на основе углеводорода, содержащей, если не указано иное, от 1 до 6 атомов углерода и по меньшей мере ненасыщенность. В качестве примеров можно упомянуть, но не ограничиваясь ими, винильную группу и т.п.
Термин «алкинил», используемый здесь, относится к линейной или разветвленной алифатической группе на основе углеводорода, содержащей, если не указано иное, от 1 до 6 атомов углерода и по меньшей мере тройную связь. В качестве примеров можно упомянуть, но не ограничиваясь этим, ацетиленильную группу и т.п.
Термин «частично или полностью галогенированный» включает разветвленные или неразветвленные углеводородные цепи, в которых один или несколько атомов водорода замещены на галоген. Примеры галогеналкильных групп включают, но не ограничиваются, следующие группы: трифторметил, трихлорметил, -C(CF3)2CH3 и т.п
Термин «галоген» сам по себе или в части другого термина относится к атому фтора, хлора, брома или йода.
Термин «алкокси» относится к алкильным группам, соответствующим определению, приведенному выше, и которые присоединяются к молекуле посредством мостикового атома кислорода. Например, термин «алкокси» означает -O-алкил, где алкильная группа содержит от 1 до 3 атомов углерода в виде линейной (неразветвленной) или разветвленной цепи. В качестве иллюстрации алкокси группы включают, но не
Термин «алкиламино» относится к алкильным группам, определенным выше, которые присоединены к молекуле через мостиковый атом азота. Например, термин «алкиламино» означает -NH-алкил или -N(-алкил)2, где алкильная группа содержит от 1 до 3 атомов углерода в виде линейной (прямой) или разветвленной цепи. В качестве иллюстрации алкиламино группы включают, но не ограничиваются ими, следующие группы: метиламино, N,N-диметиламино, этиламино и т.д.
Термин «алкилтиоэфир» (-S-(C1-C3)-алкил) относится к алкильным группам, определенным выше, которые присоединены к молекуле через мостиковый атом серы. Например, термин «алкилтиоэфир» означает -S-алкил, где алкильная группа содержит от 1 до 3 атомов углерода в виде линейной (прямой) или разветвленной цепи. В качестве иллюстрации алкилтиоэфирные группы включают, но не ограничиваются ими, следующие группы: метилтиоэфир, этилтиоэфир, н-пропилтиоэфир и т.д.
Термин «бициклический», используемый в данном документе, означает бициклическую одновалентную углеводородную группу, содержащую от шести до четырнадцати атомов углерода, в которой два кольца конденсированы, спироконденсированы или образуют мостиковую структуру, или комбинацию этих форм. При использовании для модификации гетероцикла бициклическая группа может содержать от одного до четырех гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы. Примеры бициклической структуры включают, но не ограничиваются, данными примерами:
 .
.
Термин «гетероарил» в значении используемого здесь изобретения означает 5 - или 6-членное ароматическое кольцо в соответствии с правилом ароматичности Хюккеля: циклическая, плоская молекула имеет 4n+2 π (Pi) электрона, содержащая от одного до 4 гетероатомов, выбранных из атомов азота, кислорода и/или серы. Примеры гетероарила включают пиридинил, пиримидинил, пиразинил, пиридазинил, пиразолил, триазинил, тиофенил, фуранил, имидазолил, оксазолил, тиазолил, изоксазолил, истиотиазолил, триазолил, тетразолил и т.п.Термин «гетероарил» может использоваться эквивалентно с терминами «гетероарильный цикл» или «гетероароматический».
Термин «гетероцикл» в значении изобретения, используемом здесь, означает 5 -, 7-членное неароматическое кольцо, содержащее от одного до 4 гетероатомов, выбранных из атомов азота, кислорода и/или серы. Определение также включает частично насыщенные кольца. Примеры гетероцикла включают азепин, пирролидин, пиперидин, азепин, азетидин, оксиран, тетрагидрофуран, тетрагидропиран, оксепан, пиперазин, морфолин, тиоморфолин, диазепин, оксазепан, тиазепин, гомопиперазин, гомоморфолин и тому подобное. Термин «гетероцикл», «гетероциклил» или «гетероциклический», также относятся к циклам, насыщенным или частично ненасыщенным, которые могут быть замещенными.
Данное изобретение содержит только такие комбинации заместителей и производных, которые образуют стабильное или химически возможное соединение. Стабильным или химически возможным соединением называется такое соединение, стабильности которого достаточно для его синтеза и аналитического детектирования. Предпочтительные соединения данного изобретения являются достаточно стабильными и не разлагаются при температуре до 40°C в отсутствие химически активных условий, в течение по крайней мере одной недели.
Если не указано иначе, приведенные в материалах заявки структуры соединений также подразумевают и все стереоизомеры, то есть R- и S- изомеры для каждого ассиметричного центра. Кроме того, отдельные стереохимические изомеры, равно как и энантиомеры и диастереомерные смеси настоящих соединений, также являются предметом данного изобретения. Таким образом, данное изобретение охватывает каждый диастереомер или энантиомер, свободный в значительной степени от других изомеров (>90%; более предпочтительно,>95% мольной чистоты), так же, как и смесь таких изомеров.
Конкретный оптический изомер может быть получен разделением рацемической смеси в соответствии со стандартной процедурой, например, путем получения диастереоизомерных солей путем обработки оптически активной кислотой или основанием с последующим разделением смеси диастереомеров кристаллизацией с последующим выделением оптически активных оснований из этих солей. Примерами соответствующих кислот являются винная, диацетилвинная, дибензоилвинная, дитолуолвинная и камфорсульфоновая кислота. Другая методика разделения оптических изомеров заключается в использовании хиральной хроматографической колонки. Кроме того, другой метод разделения включает синтез ковалентных диастереомерных молекул путем реакции соединений изобретения с оптически чистой кислотой в активированной форме или оптически чистым изоцианатом. Полученные диастереомеры можно разделить обычными способами, например, хроматографией, дистилляцией, кристаллизаций или сублимацией, а затем гидролизовать для получения энантиомерно чистого соединения.
Оптически активные соединения данного изобретения могут быть получены с использованием оптически активных исходных материалов. Такие изомеры могут находиться в форме свободной кислоты, свободного основания, эфира или соли.
Термин «сольват» относится к ассоциации или комплексу из одной или нескольких молекул растворителя и соединения по изобретению. Примеры растворителей, образующих сольваты, включают, но ими не ограничиваются, воду, изопропанол, этанол, метанол, ДМСО, этилацетат, уксусную кислоту и этаноламин.
Термин «гидрат» относится к комплексу, где молекулами растворителя является вода.
Соединения, составляющие суть данного изобретения, могут существовать в меченой радиоизотопом форме, т.е. указанные соединения могут содержать один или несколько атомов, чья атомная масса или массовое число отличается от атомной массы или массового числа наиболее распространенных природных изотопов. Радиоизотопы водорода, углерода, фосфора, хлора включают 3H, 14C, 32P, 35S, и 36Cl, соответственно. Соединения данного изобретения, которые содержат такие радиоизотопы и/или другие радиоизотопы других атомов, находятся в сфере настоящего изобретения. Тритиевые, т.е. 3H и углеродные, т.е. 14С радиоизотопы являются особенно предпочтительными благодаря простоте приготовления и обнаружения.
Соединения настоящего изобретения, меченые радиоактивными изотопами, могут быть получены с помощью методов, хорошо известных специалистам в данной области. Меченые соединения могут быть получены с помощью процедур, описанными здесь, простой заменой немеченых реагентов соответствующими мечеными реагентами.
Соединения настоящего изобретения могут существовать в свободной форме или, если требуется, в виде фармацевтически приемлемой соли или другого производного. Используемый здесь термин «фармацевтически приемлемая соль» относится к таким солям, которые, в рамках проведенного медицинского заключения, пригодны для использования в контакте с тканями человека и животных без излишней токсичности, раздражения, аллергической реакции и т.д., и отвечают разумному соотношению пользы и риска. Фармацевтически приемлемые соли аминов, карбоновых кислот, фосфонатов и другие типы соединений хорошо известны в медицине. Соли могут быть получены in situ в процессе выделения или очистки соединений изобретения, а также могут быть получены отдельно, путем взаимодействия свободной кислоты или свободного основания соединения изобретения с подходящим основанием или кислотой, соответственно. Примером фармацевтически приемлемых, нетоксичных солей кислот могут служить соли аминогруппы, образованные неорганическими кислотами, такими как соляная, бромоводородная, фосфорная, серная и хлорная кислоты, или органическими кислотами, такими как уксусная, щавелевая, малеиновая, винная, янтарная или малоновая кислоты, или полученные другими методами, используемыми в данной области, например, с помощью ионного обмена. К другим фармацевтически приемлемым солям относятся адипинат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептанат, гексанат, гидройодид, 2-гидрокси-этансульфонат, лактобионат, лактат, лаурат, лаурил сульфат, малат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, п-толуолсульфонат, ундеканат, валериат и подобные. Типичные соли щелочных и щелочноземельных металлов содержат натрий, литий, калий, кальций, магний и другие. Кроме того, фармацевтически приемлемые соли могут содержать, если требуется, нетоксичные катионы аммония, четвертичного аммония и амина, полученные с использованием таких противоионов, как галогениды, гидроксиды, карбоксилаты, сульфаты, фосфаты, нитраты, низшие алкил сульфонаты и арил сульфонаты.
Под «терапевтически эффективным количеством» подразумевается такое количество соединения, вводимого или доставляемого пациенту, при котором у пациента с наибольшей вероятностью проявится желаемая реакция на лечение (профилактику). Точное требуемое количество может меняться от субъекта к субъекту в зависимости от возраста, массы тела и общего состояния пациента, тяжести заболевания, методики введения препарата, комбинированного лечения с другими препаратами и т.п.
Термин «пациент» («субъект») охватывает все виды млекопитающих, предпочтительно человека, которые используют соединения в рамках данного изобретения как путем самостоятельного введения, так и/или введения пациенту другим лицом для лечения и/или профилактики заболевания или медицинского состояния.
Термины «лечение», «терапия» охватывают лечение патологических состояний у млекопитающих, предпочтительно у человека, и включают: а) блокирование (приостановку) течения заболевания, б) облегчение тяжести заболевания, т.е. индукцию регрессии заболевания.
Термин «профилактика», «предотвращение», «превентивная терапия» охватывает устранение факторов риска, а также профилактическое лечение субклинических стадий заболевания у человека, направленное на уменьшение вероятности возникновения клинических стадий заболевания. Пациенты для профилактической терапии отбираются на основе факторов, которые, на основании известных данных, влекут увеличение риска возникновения клинических стадий заболевания по сравнению с общим населением. К профилактической терапии относится а) первичная профилактика и б) вторичная профилактика. Первичная профилактика определяется как профилактическое лечение у пациентов, клиническая стадия заболевания у которых еще не наступила. Вторичная профилактика - это предотвращение повторного наступления того же или близкого клинического состояния заболевания.
Термин «уменьшение риска» охватывает терапию, которая снижает частоту возникновения клинической стадии заболевания. Примерами уменьшения риска заболевания является первичная и вторичная профилактика заболевания.
Осуществление изобретения
Примеры
Конкретные соединения по изобретению, раскрытые в настоящем документе, приводятся для целей иллюстрирования настоящего изобретения, чтобы изобретение могло быть более полно понято. В таблице 1 показаны частные примеры соединений по изобретению, которые могут быть получены методами, описанными в общих схемах синтеза, примерах и известных методах в данной области техники. Перечисленные методы не являются исчерпывающими и допускают введение разумных модификаций. Указанные реакции должны проводиться с использованием подходящих растворителей и материалов. При реализации данных общих методик для синтеза конкретных веществ необходимо учитывать присутствующие в веществах функциональные группы и их влияние на протекание реакции. Для получения некоторых веществ необходимо изменить порядок стадий либо отдать предпочтение одной из нескольких альтернативных схем синтеза. Соединения, приведенные ниже, не должны рассматриваться как единственные примеры в рамках настоящего изобретения, и никоим образом не ограничивают изобретение.
В частных вариантах воплощения изобретения соединения общей Формулы I представляют собой соединения №1-14 и 18-33, указанные в таблице 1 ниже, а также их фармацевтически приемлемые соли и/или стереоизомеры.
В частных вариантах воплощения изобретения соединения общей формулы IIa изобретение относится к соединениям №15-17, изображенным в таблице 1 ниже, и их фармацевтически приемлемым солям и стереоизомерам.
В частных вариантах воплощения изобретения соединения общей формулы IIb изобретение относится к соединениям №15-17, изображенным в таблице 1 ниже, и их фармацевтически приемлемым солям и стереоизомерам.
В частных вариантах воплощения изобретения соединения общей формулы IId изобретение относится к соединениям №15-17, изображенным в таблице 1 ниже, и их фармацевтически приемлемым солям и стереоизомерам.
В частных вариантах воплощения изобретения соединения общей формулы Ia изобретение относится к соединению №6-14, 18-33, изображенному в таблице 1 ниже, и их фармацевтически приемлемым солям и стереоизомерам.
В частных вариантах воплощения изобретения соединения общей формулы Ib изобретение относится к соединениям №6-14, 18-26 и 28-33, изображенным в таблице 1 ниже, и их фармацевтически приемлемым солям и стереоизомерам.
В частных вариантах воплощения изобретения соединения общей формулы Ic изобретение относится к соединению №27, изображенному в таблице 1 ниже, и его фармацевтически приемлемым солям и стереоизомерам.
В частных вариантах воплощения изобретения соединения общей формулы Id изобретение относится к соединениям №6-14, 18-26 и 28-33, изображенным в таблице 1 ниже, и их фармацевтически приемлемым солям и стереоизомерам.
В частных вариантах воплощения изобретения соединения общей формулы Ie изобретение относится к соединению №27, изображенному в таблице 1 ниже, и его фармацевтически приемлемым солям и стереоизомерам.
В частных вариантах воплощения изобретения соединения общей формулы If изобретение относится к соединениям №1-5, изображенным в таблице 1 ниже, и его фармацевтически приемлемым солям и стереоизомерам.


с] пиридин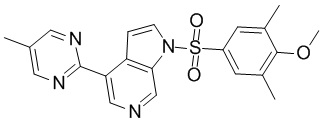
пиридин
с] пиридин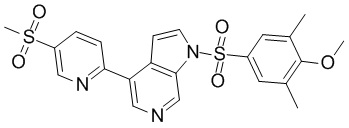
с] пиридин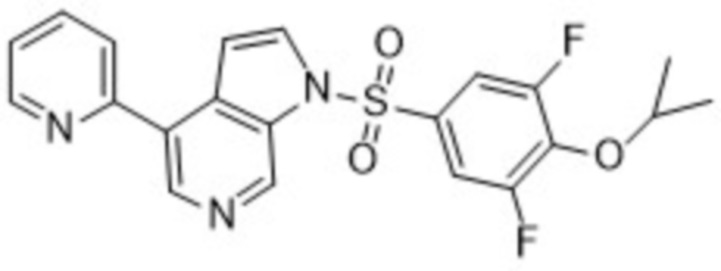
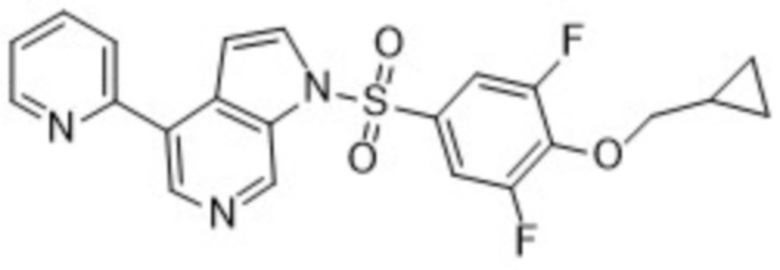


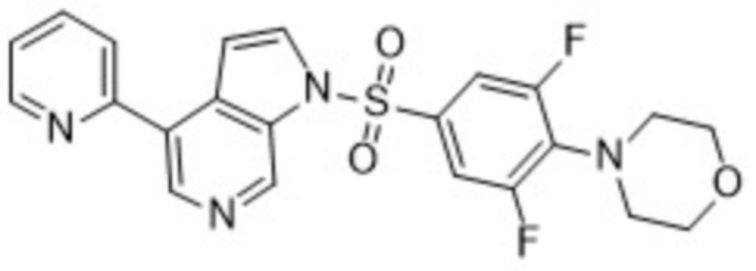

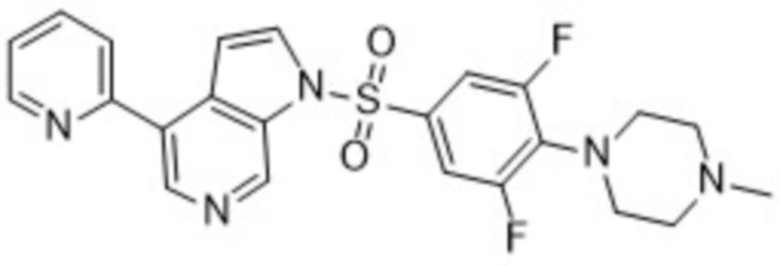




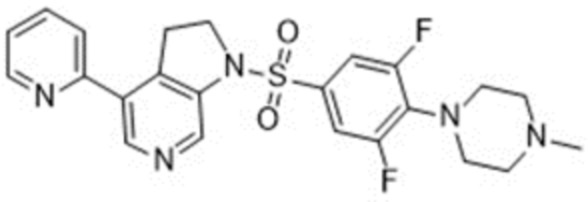







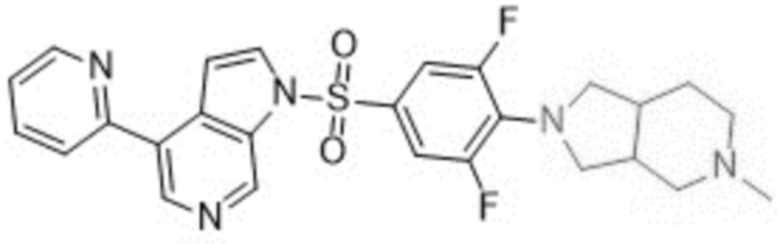
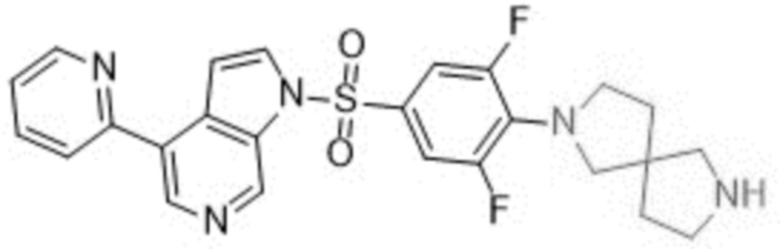



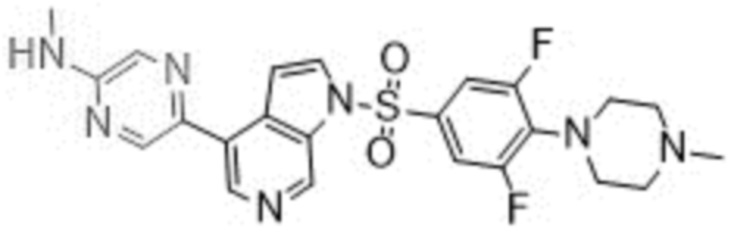



Общие способы синтеза
Оптимальные условия реакции и время реакции могут варьироваться в зависимости от конкретных используемых реагентов. Если не указано иное, растворители, температуры, давления и другие условия реакции могут быть без труда выбраны специалистом в данной области.
Общая формула интермедиатов для синтеза (R1, R2, R3, R4, и R5 определены как указано выше):

Интермедиаты
Интермедиат X (общая структура) для синтеза, бром производные (Интермедиаты Y) и производные сульфонилхлорида (Интермедиаты Z) либо доступны на рынке, либо легко получены методами, известными специалистам в данной области.
Синтез соединений по изобретению.
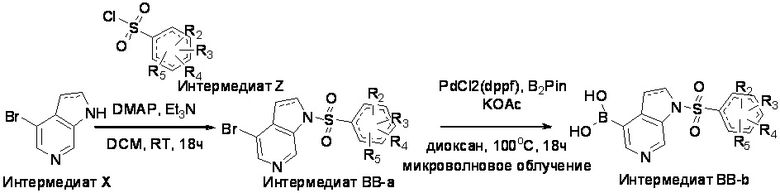
Схема 1. Общая схема синтеза интермедиатов для синтеза целевых соединений по изобретению.
Получение интермедиата BB-a
К раствору интермедиада X (1 экв.) в DCM (дихлорметане) добавляли DMAP (4(диметиламино)пиридин) (0.1 экв.), триэтиламин (2 экв.) и интермедиат Z (1.3 экв.). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь нейтрализовали водой и экстрагировали DCM (дихлорметаном). Органическую фазу промывали соляным раствором, затем сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем с получением интермедиата BB-a.
Получение Интермедиата BB-b
К раствору Интермедиата BB-a (1 экв.) в 1,4-диоксане добавляли B2Pin2 (бис(пинаколато)диборона) (1.5 экв.), ацетат калия (3 экв.) и после дегазировали в присутствии PdCl2(dppf) (бис(дифенилфосфино)ферроцен]дихлорпалладия(II)) (0.5 экв. 370 мг, 0,51 ммоль). Реакционную смесь нагревали при 100°С в условиях микроволнового излучения в течение 6 часов. Реакционной смеси давали остыть до комнатной температуры и фильтровали через слой целита. К фильтрату добавляли этилацетат и воду. Слои разделяли и водную фазу экстрагировали этилацетатом. Объединенный органический слой промывали соляным раствором, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением интермедиата BB-b, который использовали на следующей стадии без дополнительной очистки.
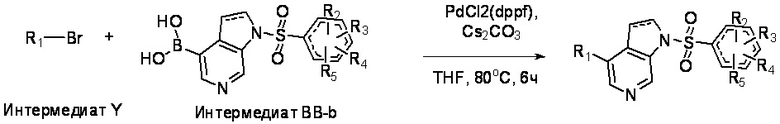
Схема 2. Общая схема синтеза целевых соединений по изобретению.
Получение соединения по изобретению.
К раствору Интермедиата BB-b (1 экв.) в смеси THF (тетрагидрофуран)/вода (10/1) добавляли интермедиат Y (1.2 экв.), карбонат цезия (2 экв.) и после дегазировали в присутствии PdCl2(dppf) (бис(дифенилфосфино)ферроцен]дихлорпалладия(II)) (0.5 экв.). Реакционную смесь перемешивали при 80°С в течение 6 часов. Реакционной смеси давали остыть до комнатной температуры и фильтровали через слой целита. К фильтрату добавляли этилацетат и воду. Слои разделяли и водную фазу экстрагировали этилацетатом. Объединенный органический слой промывали соляным раствором, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем.

Схема 3. Схема синтеза интермедиата для синтеза целевого соединения 1 по изобретению.
Получение 4-бром-1-(4-метокси-3,5-диметилфенил)сульфонилпирроло[2,3-c]пиридина (BB-a1)
К раствору 4-бром-1Н-пирроло[2,3-с]пиридина (500 мг, 2,54 ммоль) в DCM (дихлорметане) (8,0 мл) добавляли DMAP (4(диметиламино)пиридин) (31 мг, 0,25 ммоль), триэтиламин (707 мкл, 5,08 ммоль) и 4-метокси-3,5-диметилбензолсульфонилхлорид (Интермедиат Z1) (774 мг, 3,30 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь нейтрализовали водой и экстрагировали DCM (дихлорметаном). Органическую фазу промывали соляным раствором, затем сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем, используя в качестве элюента смесь циклогексан/этилацетат от 100/0 до 90/10, с получением 4-бром-1-((4-метокси-3,5-диметилфенил)сульфонил)-1H-пирроло[2,3-с]пиридин (BB-a1) (1,05 г, количественный выход) в виде бесцветного масла.
Получение [1-(4-метокси-3,5-диметилфенил)сульфонилпирроло[2,3-c]пиридин-4-ил]бороновой кислоты (BB-b1)
К раствору 4-бром-1-((4-метокси-3,5-диметилфенил)сульфонил)-1H-пирроло[2,3-c]пиридина (BB-a1) (1,05 г, 2,53 ммоль) в 1,4-диоксане (15,2 мл) добавляли B2Pin2 (бис(пинаколато)диборона) (963 мг, 3,80 ммоль), ацетат калия (744 мг, 7,59 ммоль) и после дегазировали в присутствии PdCl2(dppf) (бис(дифенилфосфино)ферроцен]дихлорпалладия(II)) (370 мг, 0,51 ммоль). Реакционную смесь нагревали при 100°С в условиях микроволнового излучения в течение 6 часов. Реакционной смеси давали остыть до комнатной температуры и фильтровали через слой целита. К фильтрату добавляли этилацетат и воду. Слои разделяли и водную фазу экстрагировали этилацетатом. Объединенный органический слой промывали соляным раствором, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением (1-((4-метокси-3,5-диметилфенил)сульфонил)-1H-пирроло[2,3-c]пиридин-4-ил)бороновую кислоту (BB-b1) (1,99 г, выход 99%) в виде коричневого масла, которое использовали на следующей стадии без дополнительной очистки.
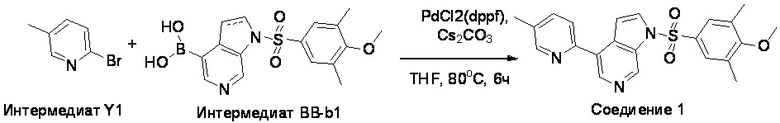
Схема 4. Схема синтеза целевого соединения 1 по изобретению.
Получение 1-(4-метокси-3,5-диметилфенил)сульфонил-4-(5-метил-2-пиридил)пирроло[2,3-c]пиридина (Соединение 1)
К раствору (1-((4-метокси-3,5-диметилфенил)сульфонил)-1H-пирроло[2,3-c]пиридин-4-ил)бороновой кислоты (BB-b1) (200 мг, 45% мас., 0,25 ммоль) в ТГФ (тетрагидрофуране) (1,1 мл) и воде (0,11 мл) добавляли 2-бром-5-метилпиридин (53,7 мг, 0,31 ммоль), карбонат цезия (163 мг, 0,50 ммоль) и после дегазировали в присутствии PdCl2(dppf) (бис(дифенилфосфино)ферроцен]дихлорпалладия(II)) (9,14 мг, 0,13 ммоль). Реакционную смесь перемешивали при 80°С в течение 6 часов. Реакционной смеси давали остыть до комнатной температуры и фильтровали через слой целита. К фильтрату добавляли этилацетат и воду. Слои разделяли и водную фазу экстрагировали этилацетатом. Объединенный органический слой промывали соляным раствором, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем, используя в качестве элюента смесь циклогексан/этилацетат от 100/0 до 60/40. Полученное твердое вещество растирали в диэтиловом эфире, фильтровали и сушили с получением 1-((4-метокси-3,5-диметилфенил)сульфонил)-4-(5-метилпиридин-2-ил)-1H-пирроло[2,3-c]пиридин (Соединение 1) (10,4 мг, выход 9,7%) в виде белого твердого вещества.
Соединения 2-33 получены аналогично методике выше, но с использованием характеристического бром производного интермедиата Y и сульфонилхлоридного производного интермедиата Z.
Экспериментальный анализ
LC-MS анализ соединений по изобретению
Масс-спектры (LCMS) соединений 16 и 18 были записаны на ВЭЖХ-системе серии Agilent 1260 с DAD\ELSD. в сочетании с масс-спектрометром Agilent LC\MSD (G6120B) для преобладающих пиков указывается отношение массы к заряду (m/z) и относительная интенсивность (%). Все данные LC/MS были получены с использованием положительного/отрицательного переключения режимов. ВЭЖХ проводили с использованием колонки с обращенной фазой Agilent Poroshell 120 SB-C18 4, 6x30 мм 2,7 мкм с UHPLC Guard Infinity Lab Poroshell 120 SB-C18 4,6 х 5 мм 2,7 мкм. В качестве подвижной фазы использовали ацетонитрил в воде, содержащей муравьиную кислоту.
Аналитическую ВЭЖХ соединений 1-15, 17 и 19-33 проводили на колонке X-Select CSH C18 XP (2,5 мкм, 30× 4,6 мм, внутренний диаметр), элюируя 0,1% муравьиной кислоты в воде (растворитель A) и 0,1% муравьиной кислоты в ацетонитриле (растворитель B), используя следующую схему элюирования: градиент 0-3 минуты: от 5% до 100% B, 3-4 минуты 100% B, при скорости потока 1,8 мл/мин при 40°C. Масс-спектры (МС) записывали на масс-спектрометре Waters ZQ (сканирование 200-900 мкм) с использованием положительной ионизации электрораспылением [ES+для получения молекулярных ионов M+H+] или отрицательной ионизации электрораспылением [ES- для получения [M-H]-молекулярных ионов] с напряжением конуса 20 В.
Пример 1.
Соединение 1: 1-(4-метокси-3,5-диметилфенил)сульфонил-4-(5-метил-2-пиридил)пирроло[2,3-c]пиридин; MW=407.49; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 408.4 [M+H]+.
Пример 2.
Соединение 2: 1-((4-метокси-3,5-диметилфенил)сульфонил)-4-(5-метилпиразин-2-ил)-1H-пирроло[2,3-с] пиридин; MW=408.47; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 409.4 [M+H]+.
Пример 3.
Соединение 3: 1-((4-метокси-3,5-диметилфенил)сульфонил)-4-(5-метилпиримидин-2-ил)-1H-пирроло[2,3-c]пиридин; MW=408.47; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 409.4 [M+H]+.
Пример 4.
Соединение 4: 1-(4-метокси-3,5-диметилфенил)сульфонил-4-(6-метилпиридазин-3-ил)пирроло[2,3-с] пиридин; MW=409.3; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 395.2 [M+H]+.
Пример 5.
Соединение 5: 1-(4-метокси-3,5-диметилфенил)сульфонил-4-(5-метилсульфонил-2-пиридил)пирроло[2,3-с] пиридин; MW=471.55; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 472.1 [M+H]+.
Пример 6.
Соединение 6: 1-((3,5-дифтор-4-изопропоксифенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин; MW=429.44; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 430.1 [M+H]+.
Пример 7.
Соединение 7: 1-((4-(циклопропилметокси)-3,5-дифторфенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин; MW=441.45; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 442.3 [M+H]+.
Пример 8.
Соединение 8: 1-((4-(2,2-дифторэтокси)-3,5-дифторфенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин; MW=451.4; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 452.0 [M+H]+.
Пример 9.
Соединение 9: 2,6-дифтор-N,N-диметил-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)анилин; MW=414.43; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 415.1 [M+H]+.
Пример 10.
Соединение 10: 4-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)морфолин; MW=456.47; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 457.1 [M+H]+.
Пример 11.
Соединение 11: 2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)анилин; MW=386.38; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 387.3 [M+H]+.
Пример 12.
Соединение 12: 1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин; MW=469.51; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 470.2 [M+H]+.
Пример 13.
Соединение 13: N-циклопропил-2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло [2,3-c] пиридин-1-ил)сульфонил)анилин; MW=426.44; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 427.4 [M+H]+.
Пример 14.
Соединение 14: N-циклобутил-2,6-дифтор-N-метил-4 - ((4- (пиридин-2-ил) -1H-пирроло [2,3-c] пиридин-1-ил) сульфонил) анилин; MW=454.5; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 455.3 [M+H]+.
Пример 15.
Соединение 15: 2,6-дифтор-N,N-диметил-4-((4-(пиридин-2-ил)-2,3-дигидро-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил) анилин; MW=416.45; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 417.4 [M+H]+.
Пример 16.
Соединение 35: 2,6-дифтор-4-((4-(пиридин-2-ил)-2,3-дегидро-H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенол; MW=389.38; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z *** [M+H]+.
Пример 17.
Соединение 17: 1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-4-(пиридин-2-ил)-2,3-дигидро-1Н-пирроло[2,3- с] пиридин; MW=471.53; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 472.4 [M+H]+.
Пример 18
Соединение 34: 1-((3,5-дифтор-4-метоксифенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин; MW=401.39; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z ** [M+H]+.
Пример 19.
Соединение 19: 1-((3,5-дифтор-4-(3-метилазетидин-1-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин; MW=440.47; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 441.1 [M+H]+.
Пример 20.
Соединение 20: N-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)-N,4-диметилтиазол- 2-амин; MW=497.54; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 498.3 [M+H]+.
Пример 21.
Соединение 21: N-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)-1-метилпиперидин-4- амин; MW=483.54; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 484.1 [M+H]+.
Пример 22.
Соединение 22: N1-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)-N2,N2-диметилэтан- 1,2-диамин; MW=457.5; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 458.4 [M+H]+.
Пример 23.
Соединение 23: 4-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)тиоморфолин; MW=472.53; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 473.3 [M+H]+.
Пример 24.
Соединение 24: 1-((3,5-дифтор-4-(5-метилгексагидропирроло[3,4-c]пиррол-2(1H)-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1H-пирроло [2,3-с]пиридин; MW=495.55; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 496.4 [M+H]+.
Пример 25.
Соединение 25: 2-(2,6-дифтор-4-((4-(пиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)фенил)-2,7-диазаспиро[4.4] нонан; MW=495.55; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 496.2 [M+H]+.
Пример 26.
Соединение 26: 1-((3,5-дифтор-4-(5-метилоктагидро-2H-пирроло[3,4-c]пиридин-2-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1H- пирроло[2,3-c]пиридин; MW=509.58; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 510.2 [M+H]+.
Пример 27.
Соединение 27: 2-(1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1H-пирроло[2,3-c]пиридин-4-ил)оксазол-4-карбонитрил; MW=484.48; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 485.4 [M+H]+.
Пример 28.
Соединение 28: 5-(1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1H-пирроло[2,3-c]пиридин-4-ил)пиколинитрил; MW=494.52; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 495.4 [M+H]+.
Пример 29.
Соединение 29: 1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-4-(5-фторпиримидин-2-ил)-1H-пирроло[2,3-c]пиридин; MW=488.49; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 489.1 [M+H]+.
Пример 30.
Соединение 30: 5-(1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1H-пирроло[2,3-c]пиридин-4-ил)-N-метилпиразин-2-амин; MW=499.54; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 500.2 [M+H]+.
Пример 31.
Соединение 31: 4-(5-циклопропилпиридин-2-ил)-1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1H-пирроло[2,3-c]пиридин; MW=509.58; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 510.4 [M+H]+.
Пример 32.
Соединение 32: 2,6-дифтор-4-((4-(5-метилпиразин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)анилин; MW=401.39; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 402.1 [M+H]+.
Пример 33.
Соединение 33: 2,6-дифтор-N,N-диметил-4-((4-(5-метилпиридин-2-ил)-1H-пирроло[2,3-c]пиридин-1-ил)сульфонил)анилин; MW=428.46; Чистота (по ВЭЖХ)>95%, MS (ESI+), m/z 429.1 [M+H]+.
ХАРАКТЕРИСТИКА БИОЛОГИЧЕСКОЙ АКТИВНОСТИ СОЕДИНЕНИЙ ПО ИЗОБРЕТЕНИЮ
Авторами настоящего изобретения исследовалась активность соединений по изобретению в качестве ингибиторов CYP11B2 при анализе в реконструированной системе, содержащей 0,5 мкМ рекомбинантного CYP11B2, 0,3 мкМ адренодоксинредуктазы человека, 2 мкМ адренодоксина человека, 100 мкМ кортикостерона в качестве контрольной реакции для обнаружения образования продукта с использованием системы ВЭЖХ с УФ-детектором. В реакционную смесь добавляют испытуемого соединения до конечной концентрации ≤2 мкМ. Концентрированную смесь белков, разбавляли буфером до конечного объема 0,5 мл, предварительно инкубировали в течение 10 мин при 37°C с последующим добавлением субстрата. Реакции инициируются добавлением NADPH (никотинамидадениндинуклеотидфосфат) до конечной концентрации 0,25 мМ с регенерирующей системой (глюкозо-6-фосфат и глюкозо-6-фосфатдегидрогеназа) в 25 мМ калий фосфатном буфере, рН 7,4, содержащем 0,1 мМ DTT (дитиотреитол), 0,1% Твин-20,4 мМ MgCl2. и инкубируют при температуре 37°C. Через 30 мин инкубации реакцию прекращают добавлением 5 мл дихлорметана. Органическую фазу выделяют центрифугированием, выпариванием, растворением в этаноле и переносят во флакон для исследований на ВЭЖХ. Колонка C18 Luna 100 Å 250×4, 6 мм использовалась на приборе Agilent Technologies серии 1200 (США) с этанолом в качестве подвижной фазы.
Активность (а) рассчитывается как количество продукта в нмоль в минуту на 1 нмоль CYP.
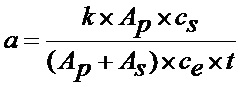 ,
,
где k-поправочный коэффициент (k=1 используется в качестве молярных коэффициентов экстинкции стероидных субстратов и продуктов, аналогичных при длине волны детектирования 254 нм), As - площадь пика субстрата, cs -концентрация субстрата, Ap - площадь пика продукта, ce - концентрация CYP (цитохром Р450), t -время реакции.
Уровень ингибирования активности CYP11B2 выражается в процентах, где 0% определяется как отсутствие ингибирования в реакциях без тестируемого соединения, а 100% - абсолютное ингибирование тестируемым соединением. Соединения всех вариантов воплощения изобретения подходят для ингибирования активности CYP11B2, и предпочтительная подгруппа включает соединения с ингибированием активности CYP11B2 в диапазоне 1-100% (+). В этой подгруппе есть еще одна подгруппа более предпочтительных соединений с ингибированием активности CYP11B2 в диапазоне 20-100% (++). В последней есть еще одна подгруппа более предпочтительных соединений с ингибированием активности CYP11B2 в диапазоне 35-100% (+++). См. таблицу 2. Кодовые номера соединений соответствуют более ранним кодам, приведенным в таблице 1.
ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ
Изобретение также относится к фармацевтическим композициям, которые содержат соединение общей формулы I, Ia, IIa, Ib, IIb, Ic, Id, IId, Ie, If(или про-лекарственную форму, фармацевтически приемлемую соль или другое фармацевтически приемлемое производное) и один или несколько фармацевтически приемлемых носителей, адъювантов, растворителей и/или наполнителей, таких, которые могут быть введены в организм пациента вместе с соединением, составляющим сущность этого изобретения, и которые не разрушают фармакологическую активность этого соединения, и нетоксичны при введении в дозах, достаточных для доставки терапевтического количества соединения.
Фармацевтические композиции, указанные в этом изобретении, содержат соединения этого изобретения вместе с фармацевтически приемлемыми носителями, которые могут включать любые растворители, разбавители, дисперсии или суспензии, поверхностно-активные вещества, изотонические агенты, загустители и эмульгаторы, консерванты, вяжущие вещества, смазки и т.д., Подходящие для конкретной формы дозирования. Материалы, которые могут служить фармацевтическими приемлемыми носителями, включают, но не ограничены, моно - и олигосахариды, а также их производные; желатин; тальк; вспомогательные вещества, такие как масло какао и воск для суппозиториев; масла, такие как арахисовое, хлопковое, кунжутное, оливковое, кукурузное и соевое масло и другие; гликоли, такие как пропиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные вещества, такие как гидроксид магния и гидроксид алюминия; альгиновая кислота; депирогенизированная вода; изотонический раствор, раствор Рингера; спиртовые и фосфатные буферные растворы. Также в составе композиции могут быть другие нетоксичные совместимые смазочные вещества, такие как лаурилсульфат натрия и стеарат магния, а также красители, разделительные жидкости, пленочные агенты, подсластители, вкусовые добавки и ароматизаторы, консерванты и антиоксиданты.
Предметом настоящего изобретения являются также лекарственные формы - класс фармацевтических композиций, структура которых оптимизирована для определенного способа введения в организм в терапевтической эффективной дозе, например, для введения в организм внутривенно, внутримышечно, перорально, подкожно, внутриглазным способом, ингаляционно, интраназально и сублингвально, в рекомендуемых дозировках.
Лекарственные формы этого изобретения могут содержать структуры, полученные методами использования липосом, методами микрокапсулирования, способами получения наноформ лекарственного средства или другими способами, известными в фармацевтике.
При получении композиции, например, в форме таблетки, активное начало смешивают с одним или несколькими фармацевтическими наполнителями, такими как желатин, крахмал, лактоза, стеарат магния, тальк, диоксид кремния, арабская камедь, маннит, микрокристаллическая целлюлоза, гипромеллоза или аналогичные соединения.
Таблетки могут быть покрыты сахарозой, производными целлюлозы или другими веществами, подходящими для нанесения покрытия. Таблетки могут быть получены различными способами, такими как прямое прессование, сухая или влажная грануляция или горячее легирование в горячем состоянии.
Фармацевтическую композицию в виде желатиновой капсулы можно получить, смешивая активное начало с растворителем и заполняя полученной смесью мягкие или твердые капсулы.
Для введения парентеральным способом используются водные суспензии, изотонические физиологические растворы или стерильные растворы для инъекций, совместимые агенты которых содержат фармакологические, например, пропиленгликоль или бутиленгликоль.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
МЕТОДЫ ТЕРАПЕВТИЧЕСКОГО ПРИМЕНЕНИЯ
Соединения настоящего изобретения являются ингибиторами CYP11B2 (альдостеронсинтазы), и поэтому они являются полезными агентами для терапии и/или профилактики заболеваний или состояний, которые могут быть облегчены путем снижения уровня альдостерона. Благодаря своей способности ингибировать альдостеронсинтазу соединения настоящего изобретения полезны для лечения и/или уменьшение риска развития: первичного гиперальдостеронизма (синдрома Конна), хронической сердечной недостаточности, хронической сердечной недостаточности с сохраненной фракцией выброса, дисфункции левого желудочка, гипертрофии левого желудочка, артериальной гипертензии, резистентной артериальной гипертензии, легочной артериальной гипертензии, коронарной болезни сердца, цирроза печени, метаболического синдрома, хронической болезни почек, гломерулосклероза, гломерулонефрита, нефритического синдрома, фокального сегментарного гломерулосклероза, диабетической нефропатии, ремоделирования сердца и сосудов, постинфарктного кардиосклероза, атеросклероза, повышенного коллагенообразования, дисфункции эндотелия, гипокалиемии и инсулинорезистентности.
Эти расстройства хорошо охарактеризованы у человека, но также с аналогичной этиологией присутствуют у других млекопитающих, и их можно лечить фармацевтическими композициями настоящего изобретения.
Для терапевтического применения соединения изобретения могут вводиться с помощью фармацевтической композиции в любой фармацевтической лекарственной форме любым способом введения. Лекарственные формы обычно включают фармацевтически приемлемый носитель, подходящий для выбранной конкретной лекарственной формы. В частности, соединение по изобретению может вводиться ежедневно в течение периода времени, необходимого для лечения и/или профилактики заболеваний, имеющих отношение к пациенту, включая курс терапии, длящийся дни, месяцы, годы или всю жизнь пациента. Способы введения включают, но не ограничиваются внутривенно, внутримышечно, перорально, подкожно, внутриглазным способом, ингаляционно, интраназально и сублингвально. Предпочтительными способами введения являются пероральный и внутривенный.
Изобретение также относится к фармацевтической композиции, содержащей ежедневную дозу указанного соединения в форме фиксированной единицы дозировки, и к комбинации, содержащей указанную фармацевтическую композицию или указанное соединение. В предпочтительном варианте осуществления указанную композицию для применения в соответствии с изобретением вводят один раз в день в дозировке 1 мг или более выбранного соединения по изобретению. Предпочтительная дозировка составляет 1-500 мг.Наиболее предпочтительная дозировка составляет 10-200 мг.
Один или несколько дополнительных фармакологически активных агентов могут вводиться в комбинации с соединением формулы I, Ia, IIa, Ib, IIb, Ic, Id, IId, Ie, If. Как правило, любые дополнительные одиночные или множественные активные агенты, отличные от соединения формулы I, Ia, IIa, Ib, IIb, Ic, Id, IId, Ie, If, включая, но не ограничиваясь, антигипертензивными агентами, антидиабетическими агентами и/или агентами против ожирения, могут использоваться в любой комбинации с соединением формулы I, Ia, IIa, Ib, IIb, Ic, Id, IId, Ie, If в одной или отдельной лекарственной форме, позволяющей одновременное или последовательное терапевтическое действие активных агентов.
МЕТОДЫ ПРИМЕНЕНИЯ В ОБЛАСТИ МЕДИЦИНСКОЙ ДИАГНОСТИКИ
Соединения настоящего изобретения являются ингибиторами CYP11B2 (альдостеронсинтазы) связываясь с активным центром данного фермента, и поэтому они являются полезными агентами для диагностики и тераностики заболеваний или состояний, которые обусловлены повышением уровня альдостерона. Благодаря своей способности высокоаффинно связываться с активным центром альдостеронсинтазы соединения настоящего изобретения полезны для диагностики причин развития ряда заболеваний: первичного гиперальдостеронизма (синдрома Конна), хронической сердечной недостаточности, хронической сердечной недостаточности с сохраненной фракцией выброса, дисфункции левого желудочка, гипертрофии левого желудочка, артериальной гипертензии, резистентной артериальной гипертензии, легочной артериальной гипертензии, коронарной болезни сердца, цирроза печени, метаболического синдрома, хронической болезни почек, гломерулосклероза, гломерулонефрита, нефритического синдрома, фокального сегментарного гломерулосклероза, диабетической нефропатии, ремоделирования сердца и сосудов, постинфарктного кардиосклероза, атеросклероза, повышенного коллагенообразования, дисфункции эндотелия, гипокалиемии и инсулинорезистентности.
Эти расстройства хорошо охарактеризованы у человека, но также с аналогичной этиологией присутствуют у других млекопитающих, и их можно диагностировать фармацевтическими композициями настоящего изобретения.
Для диагностического и тераностического применения соединения изобретения могут вводиться с помощью фармацевтической композиции в любой фармацевтической лекарственной форме любым способом введения. Лекарственные формы обычно включают фармацевтически приемлемый носитель, подходящий для выбранной конкретной лекарственной формы. В частности, соединение по изобретению может вводиться в течение периода времени, необходимого для диагностики и тераностики. Способы введения включают, но не ограничиваются внутривенно, внутримышечно, перорально, подкожно, внутриглазным способом, ингаляционно, интраназально и сублингвально. Предпочтительными способами введения являются пероральный и внутривенный.
Изобретение также относится к фармацевтической композиции используемое для диагностики и тераностики, содержащей дозу указанного соединения в форме фиксированной единицы дозировки, и к комбинации, содержащей указанную фармацевтическую композицию или указанное соединение.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ АЛЬДОСТЕРОНСИНТАЗЫ (CYP11B2) ЧЕЛОВЕКА | 2023 |
|
RU2824362C1 |
| Ингибиторы цитохрома 11В2 человека | 2021 |
|
RU2783521C1 |
| Ингибиторы цитохрома 11В2 человека | 2022 |
|
RU2800378C1 |
| (АЗА)ИНДОЛ-, БЕНЗОТИОФЕН- И БЕНЗОФУРАН-3-СУЛЬФОНАМИДЫ | 2017 |
|
RU2767904C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ИЗОХИНОЛИНА | 2020 |
|
RU2839897C2 |
| ПИРРОЛОПИРРОЛОВЫЕ КОМПОЗИЦИИ В КАЧЕСТВЕ АКТИВАТОРОВ ПИРУВАТКИНАЗЫ (PKR) | 2018 |
|
RU2736217C2 |
| ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ ИНГИБИТОР НАТРИЙЗАВИСИМОГО ПЕРЕНОСЧИКА ФОСФАТА | 2015 |
|
RU2740008C2 |
| АПОПТОЗ-ИНДУЦИРУЮЩИЕ АГЕНТЫ | 2018 |
|
RU2782469C2 |
| ПРОИЗВОДНОЕ АМИНОПИРАЗОЛА | 2010 |
|
RU2580543C9 |
| ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ ИНГИБИТОР НАТРИЙЗАВИСИМОГО ПЕРЕНОСЧИКА ФОСФАТА | 2015 |
|
RU2811864C1 |
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая соединение, фармацевтическую композицию для лечения или профилактики заболевания или состояния, которое опосредовано или поддерживается активностью CYP11B2, включающую вышеуказанное соединение, и способ лечения или профилактики заболевания или состояния, которое опосредовано или поддерживается активностью CYP11B2. Изобретение расширяет арсенал средств, характеризующихся высокой эффективностью в ингибировании активности цитохрома 11В2 человека (CYP11B2). 3 н. и 23 з.п. ф-лы, 2 табл., 33 пр.
1. Соединение общей формулы (I)

или его фармацевтически приемлемая соль, сольват,
где R1 представляет собой 5-6-членный гетероарил, содержащий 0-1 атома кислорода и 1-4 азота, необязательно замещенный 1-5 заместителями R1a,
R1a выбирается независимо и представляет собой водород, галоген, (С1-С3)алкил, (С3-С5)циклоалкил, частично или полностью галогенированный (С1-С3)алкил, (С1-С3)алкилсульфонил, циано, N,N-диметиламин, N-метиламин;
R2, R3, R4, R5, каждый, выбирается независимо и представляет собой:
- (i) водород, галоген, (С1-С3)-алкил, (С3-С5)-циклоалкил, -С(=O)-СН3, частично или полностью галогенированный (С1-С3)алкил, или
- (ii) -ОН, -SH, или
- (iii) -(С1-С3)-алкокси, 3-7-членный гетероциклил, содержащий 1-2 атома азота, 0-1 атома кислорода и/или 0-1 серы, (С3-С7)-циклоалкил, -3-(С1-С3)-алкил, -(С3-С7)-циклоалкил-3-(С1-С3)-алкил, причем каждая из вышеуказанных групп необязательно частично или полностью замещена заместителями, выбранными из -ОН, 1-4 атома галогена, (С1-С3)-алкокси, (С3-С7)-циклоалкила, 3-7-членного гетероцикла, содержащего один атом кислорода, -NH2, (С1-С3)-алкиламино, ди(С1-С3)-алкиламино или 3-7-членный гетероцикл, содержащий один атом азота и необязательно 1-2 гетероатома кислорода и/или серы; или
- (iv) -NRaRb, где каждый Ra и Rb:
- независимо представляет собой водород, дейтерий, (С3-С7)-циклоалкил, -(С1-С3)-алкил-N(СН3)2, (С1-С3)-алкил, частично или полностью галогенированный (С1-С3)-алкил, 3-7-членный гетероциклил, содержащий 0-1 атом кислорода, 0-1 атом серы и/или 1-4 атом азота, необязательно замещенный 1-2 заместителями, выбранными из (С1-С3)-алкила или частично или полностью галогенированного (С1-С3)-алкила, 5-7-членный гетероарил, содержащий 0-1 атом кислорода, 0-1 атом серы и/или 1-4 атом азота, причем указанный гетероарил необязательно замещен 1-2 заместителями, выбранными из (С1-С3)-алкила или частично или полностью галогенированного (С1-С3)-алкила,
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 4-7-членный гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-2 заместителями, выбранными из (С1-С3)-алкила, частично или полностью галогенированным (С1-С3)-алкилом, или
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 6-14-членный бициклический гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-4 заместителями, выбранными из дейтерия, галогена, (С1-С3)-алкила, частично или полностью галогенированного (С1-С3)-алкила, (С2-С3)-алкенила, (С2-С3)-алкинила и (С1-С3)-алкокси;
D/S означает наличие двойной или одинарной связи;
пунктирные связи означают, что кольца ароматические.
2. Соединение по п. 1, где по меньшей мере два радикала из R2, R3, R4 и R5 отличны от водорода.
3. Соединение по п. 2, где по меньшей мере три радикала из R2, R3, R4 и R5 отличны от водорода.
4. Соединение по п. 1, где R2, R3, R4 и R5, каждый, выбирается независимо и представляет собой:
- (i) водород, галоген, (С1-С3)-алкил, (С3-С5)-циклоалкил, -С(=O)-СН3, частично или полностью галогенированный (С1-С3)-алкил;
- (ii) группу, выбранную из (С1-С3)-алкокси, (С3-С7)циклоалкила, галогегенированной (С1-С3)алкокси группы, содержащей 1-4 атома галогена;
- (iii) -NRaRb, где каждый Ra и Rb:
- независимо представляет собой водород, дейтерий, (С3-С7)-циклоалкил, -(С1-С3)-алкил-N(СН3)2, (С1-С3)-алкил, частично или полностью галогенированный (С1-С3)-алкил, 3-7-членный гетероциклил, содержащий 0-1 атом кислорода, 0-1 атом серы и/или 1-4 атома азота, необязательно замещенный 1-2 заместителями, выбранными из (С1-С3)-алкила, частично или полностью галогенированного (С1-С3)-алкил, 5-7-членный гетероарил, содержащий 0-1 атом кислорода, 0-1 атом серы и/или 1-4 атома азота, необязательно замещенный 1-2 заместителями, выбранными из (С1-С3)-алкила, частично или полностью галогенированного (С1-С3)-алкила,
- альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 4-7-членный гетероциклил, необязательно замещенный 1-2 заместителями, выбранными из (С1-С3)-алкила, частично или полностью галогенированного (С1-С3)-алкила, или
- Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 6-14-членный бициклический гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-4 заместителями, выбранными из дейтерия, галогена, (С1-С3)-алкила, частично или полностью галогенированного (С1-С3)-алкила, (С2 С3)-алкенила, (С2-С3)-алкинила и (С1-С3)-алкокси.
5. Соединение по п. 1, где по меньшей мере один из радикалов R2, R3, R4, R5 находится в пара-положении и каждый выбирается независимо и представляет собой:
- -ОН, -SH, (С1-С3)-алкокси, 3-7-членный гетероциклил, содержащий 1-2 атома азота, 0-1 атома кислорода и/или 0-1 серы, (С3-С7)-циклоалкил, -S-(С1-С3)-алкил, (С3-С7)-циклоалкил-S-(С1-С3)-алкил, причем каждая из вышеуказанных групп необязательно частично или полностью замещена заместителями, выбранными из -ОН, 1-4 атома галогена, (С1-С3)-алкокси, (С3-С7)-циклоалкила, 3-7-членного гетероцикла, содержащего один атом кислорода, -NH2, (С1-С3)-алкиламино, ди(С1-С3)-алкиламино или 3-7-членный гетероцикл, содержащий один атом азота и необязательно 1-2 гетероатома кислорода и серы; или
- NRaRb, где каждый Ra и Rb:
- независимо представляет собой водород, дейтерий, (С3-С7)-циклоалкил, -(С1-С3)-алкил-(СН3)2, (С1-С3)-алкил, частично или полностью галогенированный (С1-С3)-алкил, 3-7-членный гетероцикл, содержащий 0-1 атома кислорода, 0-1 серы и/или 1-4 азота, необязательно замещенный 1-2 заместителями, выбранными из (С1-С3)-алкила или частично или полностью галогенированного (С1-С3)-алкила, 5-7-членный гетероарил, причем указанный гетероарил необязательно замещен 1-2 заместителями, выбранными из (С1-С3)-алкила или частично или полностью галогенированного (С1-С3)-алкила,
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 4-7-членный гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-2 заместителями, выбранными из (С1-С3)-алкила, частично или полностью галогенированного (С1-С3)-алкила, или
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 6-14-членный бициклический гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-4 заместителями, выбранными из дейтерия, галогена, (С1-С3)-алкила, частично или полностью галогенированного (С1-С3)-алкила, (С2-С3)-алкенила, (С2-С3)-алкинила или (С1-С3)-алкокси.
6. Соединение по п. 1, где R1 выбирается независимо и представляет собой группу, выбранную из пиридинила, пиразинила, пиримидинила, пиридазинила, оксазила, причем R1 необязательно замещен группой, выбранной из метила, метилсульфонила, галогена, метиламино, циано и циклопропила.
7. Соединение по п. 1, где два радикала из R2, R3, R4, R5 находятся в мета-положении и представляют собой группу, выбранную из метила или галогена, один из R2, R3, R4, R5 представляет собой водород и один из R2, R3, R4, R5 находится в пара-положении и представляет собой группу, выбранную из метокси, изопропилокси, циклопропилметокси, дифторэтокси, -NH2, -N(СН3)2, циклопропиламино, -N(СН3)-цикпобутил, -N(СН3)-метилтиазолил, метилпиперидиниламино, -NH-(С1-С3)-алкил-N(СН3)2, морфолинил, метилпиперазинил, необязательно замещенный метилом азетидинил, тиоморфолинил, необязательно замещенный метилом гексагидропирролопирролил, диазаспирононанил, необязательно замещенный метилом октагидропирролопиридинил.
8. Соединение по п. 1, где соединение формулы (I) представляет собой соединение, структура которого описывается формулой (Ia)

или его фармацевтически приемлемую соль, сольват,
где R1 как определено в п. 1,
R6 выбирается независимо и представляет собой:
- -ОН, -SH, -(С1-С3)-алкокси, 3-7-членный гетероциклил, содержащий 1-2 атома азота, 0-1 атома кислорода и/или 0-1 серы, (С3-С7)-циклоалкил, -S-(С1-С3)-алкил, (С3-С7)-циклоалкил-S-(С1-С3)-алкил, причем каждая из вышеуказанных групп необязательно частично или полностью замещена заместителями, выбранными из -ОН, 1-4 атома галогена, (С1-С3)-алкокси, (С3-С7)-цикпоалкила, 3-7-членного гетероцикла, содержащего один атом кислорода, -NH2, (С1-С3)-алкиламино, ди(С1-С3)-алкиламино или 3-7-членный гетероцикл, содержащий один атом азота и необязательно 1-2 гетероатома выбирают из кислорода и серы, или
- -NRaRb, где каждый Ra и Rb:
- независимо представляет собой водород, дейтерий, (С3-С7)-циклоалкил, -(С1-С3)-алкил-N(СН3)2, (С1-С3)-алкил, частично или полностью галогенированный (С1-С3)-алкил, 3-7-членный гетероцикл, содержащий 0-1 атома кислорода, 0-1 серы и/или 1-4 азота, необязательно замещенный 1-2 заместителями, выбранными из (С1-С3)-алкила или частично или полностью галогенированного (С1-С3)-алкила, 5-7-членный гетероарил, причем указанный гетероарил необязательно замещен 1-2 заместителями, выбранными из (С1-С3)-алкила или частично или полностью галогенированного (С1-С3)-алкила,
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 4-7-членный гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-2 заместителями, выбранными из (С1-С3)-алкила, частично или полностью галогенированным (С1-С3)-алкилом, или
альтернативно Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 6-14-членный бициклический гетероциклил, содержащий 1-2 атома азота и 0-1 атома кислорода и/или 0-1 серы, необязательно замещенный 1-4 заместителями, выбранными из дейтерия, галогена, (С1-С3)-алкила, частично или полностью галогенированного (С1-С3)-алкила, (С2-С3)-алкенила, (С2-С3)-алкинила или (С1-С3)-алкокси.
9. Соединение по п. 1, где соединение формулы (I) представляет собой соединение, структура которого описывается формулой (IIa)
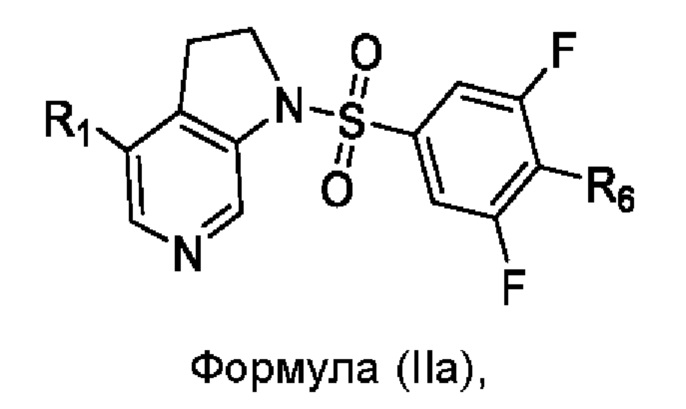
или его фармацевтически приемлемую соль, сольват,
где R1 и R6 как определено в п. 8.
10. Соединение по п. 1, где соединение формулы (I) представляет собой соединение, структура которого описывается формулой (Ib)

или его фармацевтически приемлемую соль, сольват,
где Q1, Q2, Q3, Q4, Q5 каждый выбирается независимо и представляет собой азот или углерод, причем не более двух из Q1, Q2, Q3, Q4 и Q5 представляют собой азот, и указанный углерод необязательно замещен 1-5 заместителями R1a,
R1a как определено в п. 1,
R2, R3, R4, R5, такие как определено в п. 1;
пунктирные связи означают, что кольца ароматические.
11. Соединение по п. 1, где соединение формулы (I) представляет собой соединение, структура которого описывается формулой (Ic)

или его фармацевтически приемлемую соль, сольват,
где Q6, Q7, Q8, Q9, каждый, выбирается независимо и представляют собой кислород, углерод или азот, причем не более двух из Q6, Q7, Q8 и Q9 представляют собой азот или кислород, и указанный углерод необязательно замещен 1-4 группами R1a,
R1a как определено в п. 1,
R2, R3, R4, R5, такие как определено в п. 1;
пунктирные связи означают, что кольца ароматические.
12. Соединение по п. 1, где соединение формулы (I) представляет собой соединение, структура которого описывается формулой (Id)

или его фармацевтически приемлемую соль, сольват, где:
Q1, Q2, Q3, Q4, Q5 такие как определено в п. 10;
R1a как определено в п. 1;
R6 как определено в п. 8.
13. Соединение по п. 1, где соединение формулы (I) представляет собой соединение, структура которого описывается формулой (Ie)
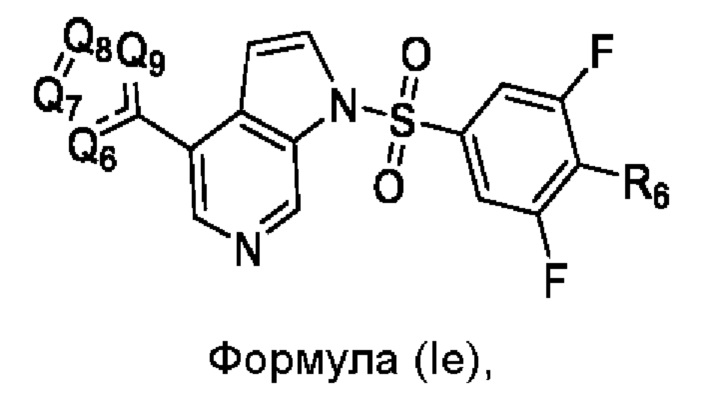
или его фармацевтически приемлемую соль, сольват,
где Q6, Q7, Q8, Q9, такие как определено в п. 11;
R1a как определено в п. 1;
R6 как определено в п. 8.
14. Соединение по п. 1, где соединение формулы (I) представляет собой соединение, структура которого описывается формулой (If)

или его фармацевтически приемлемую соль, сольват,
где R1 как определено в п. 1,
R6 как определено в п. 8.
15. Соединение по п. 1, где соединение формулы (I) представляет собой соединение, структура которого описывается формулой (IIb)
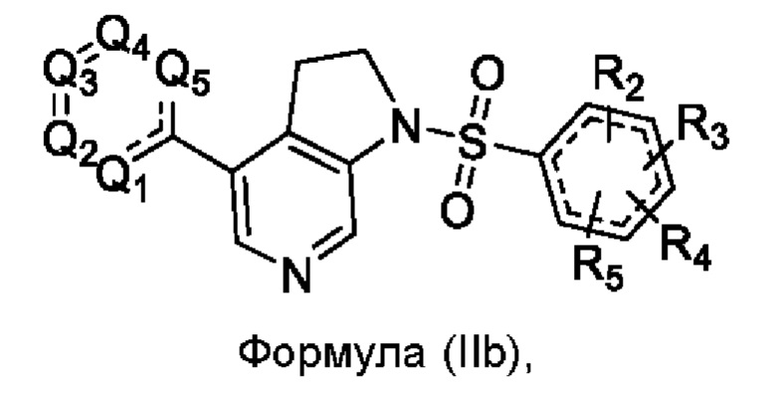
или его фармацевтически приемлемую соль, сольват,
где Q1, Q2, Q3, Q4, Q5, такие как определено в п. 10;
R2, R3, R4 и R5, такие как определено в п. 1;
пунктирные связи означают, что кольца ароматические.
16. Соединение по п. 1, где соединение формулы (I) представляет собой соединение, структура которого описывается формулой (IId)

или его фармацевтически приемлемую соль, сольват,
где Q1, Q2, Q3, Q4, Q5, такие как определено в п. 10;
R6 как определено в п. 8.
17. Соединение по п. 1, выбранное из группы:
1-(4-метокси-3,5-диметилфенил)сульфонил-4-(5-метил-2-пиридил)пирроло[2,3-с]пиридин;
1-((4-метокси-3,5-диметилфенил)сульфонил)-4-(5-метилпиразин-2-ил)-1Н-пирроло[2,3-с]пиридин;
1-((4-метокси-3,5-диметилфенил)сульфонил)-4-(5-метилпиримидин-2-ил)-1Н-пирроло[2,3-с]пиридин;
1-(4-метокси-3,5-диметилфенил)сульфонил-4-(6-метилпиридазин-3-ил)пирроло[2,3-с]пиридин;
1-(4-метокси-3,5-диметилфенил)сульфонил-4-(5-метилсульфонил-2-пиридил)пирроло[2,3-с]пиридин;
1-((3,5-дифтор-4-изопропоксифенил)сульфонил)-4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин;
1-((4-(циклопропилметокси)-3,5-дифторфенил)сульфонил)-4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин;
1-((4-(2,2-дифторэтокси)-3,5-дифторфенил)сульфонил)-4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин;
2,6-дифтор-N,N-диметил-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)анилин;
4-(2,6-дифтор-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)фенил)морфолин;
2,6-дифтор-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)анилин;
1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин;
N-циклопропил-2,6-дифтор-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)анилин;
N-циклобутил-2,6-дифтор-N-метил-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил) сульфонил)анилин;
2,6-дифтор-N,N-диметил-4-((4-(пиридин-2-ил)-2,3-дигидро-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)анилин;
2,6-дифтор-4-((4-(пиридин-2-ил)-2,3-дегидро-Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)фенол;
1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-4-(пиридин-2-ил)-2,3-дигидро-1Н-пирроло[2,3-с]пиридин;
1-((3,5-дифтор-4-метоксифенил)сульфонил)-4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин;
1-((3,5-дифтор-4-(3-метилазетидин-1-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин;
N-(2,6-дифтор-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)фенил)-N,4-диметилтиазол-2-амин;
N-(2,6-дифтор-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)фенил)-1-метилпиперидин-4-амин;
N1-(2,6-дифтор-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)фенил)-N2,N2-диметилэтан-1,2-диамин;
4-(2,6-дифтор-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)фенил)тиоморфолин;
1-((3,5-дифтор-4-(5-метилгексагидропирроло[3,4-с]пиррол-2(1Н)-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин;
1-((3,5-дифтор-4-(5-метилоктагидро-2Н-пирроло[3,4-с]пиридин-2-ил)фенил)сульфонил)-4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин;
2-(2,6-дифтор-4-((4-(пиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)фенил)-2,7-диазаспиро[4.4]нонан;
2-(1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1Н-пирроло[2,3-с]пиридин-4-ил)оксазол-4-карбонитрил;
5-(1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1Н-пирроло[2,3-с]пиридин-4-ил)пиколинитрил;
1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-4-(5-фторпиримидин-2-ил)-1Н-пирроло[2,3-с]пиридин;
5-(1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1Н-пирроло[2,3-с]пиридин-4-ил)-N-метилпиразин-2-амин;
4-(5-циклопропилпиридин-2-ил)-1-((3,5-дифтор-4-(4-метилпиперазин-1-ил)фенил)сульфонил)-1Н-пирроло[2,3-с]пиридин;
2,6-дифтор-4-((4-(5-метилпиразин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)анилин;
2,6-дифтор-N,N-диметил-4-((4-(5-метилпиридин-2-ил)-1Н-пирроло[2,3-с]пиридин-1-ил)сульфонил)анилин.
18. Соединение по любому из пп. 1, 8-16, в котором сольват представляет собой гидрат.
19. Фармацевтическая композиция для лечения или профилактики заболевания или состояния, которое опосредовано или поддерживается активностью CYP11B2, включающая терапевтически или профилактически эффективное количество соединения по любому из пп. 1-18 и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
20. Фармацевтическая композиция по п. 19, характеризующаяся тем, что фармацевтически приемлемое вспомогательное вещество представляет собой носитель, адъювант и/или растворитель.
21. Фармацевтическая композиция по п. 19, характеризующаяся тем, что заболевание выбрано из группы, включающей первичный гиперальдостеронизм, хроническую сердечную недостаточность, хроническую сердечную недостаточность с сохраненной фракцией выброса, дисфункцию левого желудочка, гипертрофию левого желудочка, артериальную гипертензию, резистентную артериальную гипертензию, легочную артериальную гипертензию, коронарную болезнь сердца, цирроз печени, метаболический синдром, хроническую болезнь почек, гломерулосклероз, гломерулонефрит, нефритический синдром, фокальный сегментарный гломерулосклероз, диабетическую нефропатию, ремоделирование сердца и сосудов, постинфарктный кардиосклероз, атеросклероз, повышенное коллагенообразование, дисфункцию эндотелия, гипокалиемию или инсулинорезистентность.
22. Фармацевтическая композиция по п. 21, характеризующаяся тем, что первичный гиперальдостеронизм представляет собой синдром Конна, включающий следующие заболевания или состояния: альдостеронпродуцирующая аденома, идиопатический гиперальдостеронизм, одно- или билатеральная гиперплазия надпочечников, семейный гиперальдостеронизм первого и второго типа, альдостеронпродуцирующая карцинома и альдостеронэктопированный синдром.
23. Способ лечения или профилактики заболевания или состояния, которое опосредовано или поддерживается активностью CYP11B2, у субъекта, включающий введение терапевтически или профилактически эффективного количества соединения по любому из пп. 1-18.
24. Способ по п. 23, характеризующийся тем, что заболевание выбрано из группы, включающей первичный гиперальдостеронизм, хроническую сердечную недостаточность, хроническую сердечную недостаточность с сохраненной фракцией выброса, дисфункцию левого желудочка, гипертрофию левого желудочка, артериальную гипертензию, резистентную артериальную гипертензию, легочную артериальную гипертензию, коронарную болезнь сердца, цирроз печени, метаболический синдром, хроническую болезнь почек, гломерулосклероз, гломерулонефрит, нефритический синдром, фокальный сегментарный гломерулосклероз, диабетическую нефропатию, ремоделирование сердца и сосудов, постинфарктный кардиосклероз, атеросклероз, повышенное коллагенообразование, дисфункцию эндотелия, гипокалиемию или инсулинорезистентность.
25. Способ по п. 24, характеризующийся тем, что первичный гиперальдостеронизм представляет собой синдром Конна, включающий следующие заболевания или состояния: альдостеронпродуцирующая аденома, идиопатический гиперальдостеронизм, одно- или билатеральная гиперплазия надпочечников, семейный гиперальдостеронизм первого и второго типа, альдостеронпродуцирующая карцинома и альдостеронэктопированный синдром.
26. Способ по п. 23, в котором субъект представляет собой человека.
| WO 2016014736 A1, 28.01.2016 | |||
| Соединительная муфта с автоматическими запорными клапанами для трубопроводов | 1929 |
|
SU17952A1 |
| EP 1842543 A1, 10.10.2007 | |||
| WO 2008076862 A2, 26.06.2008. | |||
Авторы
Даты
2024-01-16—Публикация
2022-11-10—Подача