ОБЛАСТЬ ТЕХНИКИ
В целом, примеры вариантов осуществления настоящего раскрытия относятся к анестезирующей композиции и способу введения анестезирующей композиции пациенту, в частности, для анестезирования по меньшей мере части глаза. Раскрытие относится к анестезирующей композиции или препарату для местного применения, которые можно наносить локально на поверхность глаза. В примерах реализации некоторых вариантов осуществления раскрытия предложены способы применения местного анестезирующего препарата, например, в виде капель, для получения высокого уровня анестезии плоской части ресничного тела, достаточного для обеспечения возможности интравитреальной инъекции (инъекции в стекловидное тело) без чрезмерного дискомфорта для пациента. В примерах реализации некоторых вариантов осуществления настоящего раскрытия предложены способы нанесения раствора для наружного применения, содержащего артикаин, направленные на достижение анестезии поверхности глаза и внутренней стороны глазной стенки.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Инъекции фармакологических агентов в полость стекловидного тела с целью лечения различных заболеваний сетчатки и внутриглазных воспалительных заболеваний получили широкое распространение. В 2016 г только CMS (англ. Centers for Medicare & Medicaid Services - Центры обеспечения услуг по программам Медикэр и Медикэйд) компенсировали расходы приблизительно за 2,75 миллионов инъекций. Практически всегда такие инъекции в основном выполняют через плоскую часть ресничного тела. Инъекцию в глаз через плоскую часть ресничного тела при правильной ориентации иглы выполняют позади хрусталика или импланта искусственного хрусталика человека, но перед сетчаткой, что позволяет избежать повреждения хрусталика и сетчатки. Плоская часть ресничного тела представляет собой кольцевую зону, окружающую периметр глаза, на расстоянии от 3,0 до 5,5 мм от края роговицы. Известные агенты для местного применения, такие как пропаракаин, могут обеспечивать анестезию внешней поверхности глаза, но не вызывают онемения или анестезии чрезвычайно чувствительной внутренней стороны плоской части ресничного тела.
Не существует известных разрешенных для применения в медицинской практике местно-анестезирующих средств, вызывающих анестезию внутренней стороны плоской части ресничного тела. В настоящее время врачи сначала вводят лидокаин под конъюктиву (покрывающую ткань глаза), а затем выполняют вторую инъекцию через плоскую часть ресничного тела. В некоторых случаях перед выполнением инъекции в стекловидное тело используют гель с лидокаином. Пациенты часто сообщают о дискомфорте от умеренного до сильного при каждом из этих подходов.
При интравитреальной инъекции возможно возникновение некоторых осложнений, включая эндофтальмит, при котором внутри глаза развивается инфекция. Лечение эндофтальмита часто бывает успешным, однако нередко происходит необратимая потеря зрения, по меньшей мере, до некоторой степени. Терапия включает последующие инъекции в стекловидное тело антибиотиков и/или стероидов и витрэктомию (удаление стекловидного тела). При этом довольно часто возникает слепота или происходит потеря глаза. Офтальмологи стремятся предотвратить осложнения, вызываемые инфекциями, несмотря на то, что многие из используемых анестезирующих средств не всегда являются стерильными.
Обычно артикаин применяют только в виде инъекций. Доступные в настоящее время местные офтальмологические анестезирующие средства действуют на внешней поверхности глаза, но проникают не настолько хорошо, чтобы обеспечить надлежащую анестезию внутренней стороны глазной стенки. Эта область чрезвычайно чувствительна к проникновению, давлению и воздействию лазера или замораживания. Одной из часто выполняемых офтальмологических процедур является введение в глаз различных фармакологических агентов. Для обеспечения равномерной адекватной анестезии, необходимой для такого введения, врач сначала выполняет периокулярную инъекцию анестезирующего агента, выжидает, пока анестезирующее средство подействует, и затем выполняет внутриглазную инъекцию.
Известно об использовании препаратов артикаина, содержащих не более 4% артикаина и сосудосуживающее средство, которым обычно является адреналин, в качестве инъекционного анестезирующего средства, разработанного для инъекции в ткань пациента. Такие препараты широко используют в стоматологии для выполнения стоматологических процедур. Предшествующие композиции, как правило, не подходят либо являются неэффективными для местного применения или нанесения на глаз.
В настоящее время отсутствуют стандартные способы офтальмологической анестезии и препараты для инъекций в стекловидное тело. Кроме того, не существует разрешенных для медицинского применения лекарственных средств, специально предназначенных для воздействия на глаз перед инъекциями в стекловидное тело. Плоская часть ресничного тела представляет собой уникальную область глаза. Стандартные офтальмологические средства местного применения обеспечивают анестезию внешней поверхности глаза. Однако, поскольку инъекционная игла проникает через внутреннюю сторону плоской части ресничного тела в стекловидная полость, пациенты без анестезии испытывают настолько сильную боль, что завершение инъекции становится невозможным.
И хотя предшествующие композиции и препараты, как правило, подходили для предполагаемых целей, по-прежнему сохраняется потребность в улучшенных анестезирующих композициях.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В примерах вариантов осуществления настоящего раскрытия предложена анестезирующая композиция, содержащая артикаин. Анестезирующая композиция подходит для местного офтальмологического применения путем местного нанесения на поверхность глаза для достижения уровня анестезии, достаточного для выполнения инъекций в стекловидное тело и других медицинских манипуляций. Анестезирующую композицию можно вводить в количестве, достаточном для выполнения инъекции в стекловидное тело глаза, без чрезмерного дискомфорта для пациента.
Офтальмологическая композиция для местного применения содержит артикаин в достаточно высокой концентрации, чтобы вызвать анестезию глаза при местном введении перед выполнением различных медицинских манипуляций, включая хирургические операции. Композиция особенно подходит для обеспечения анестезии глаза, позволяющей осуществлять инъекции в или через плоскую часть ресничного тела глаза с минимальной болью или без боли для пациента.
Примеры вариантов осуществления настоящего раскрытия включают препараты и/или их модификации и/или их применение, содержащие артикаин, который может являться амидсодержащим местным анестезирующим средством короткого действия со средней эффективностью. Артикаин может быстро метаболизироваться из-за наличия в молекулярной структуре сложноэфирной группы. Прежде артикаин вводили путем инъекции при блокаде периферических нервов, спинномозговой, эпидуральной, периокулярной или регионарной анестезии.
Согласно одному из вариантов осуществления, офтальмологическая анестезирующая композиция для местного применения содержит артикаин в количестве, эффективном для обеспечения анестезирующего эффекта для глаза пациента без необходимости повторного нанесения или инъекции в глаз анестезирующего средства. Артикаин может быть включен в анестезирующую композицию для местного применения в количествах и концентрациях, обеспечивающих требуемые анестезирующие свойства с помощью контролируемой дозировки. Композиция может содержать артикаин в количестве приблизительно до 13% мас./об. в расчете на общий объем композиции. Согласно некоторым вариантам осуществления, композиция может содержать артикаин в количестве приблизительно от 4% мас./об. до 12% мас./об. в расчете на общий объем композиции. Офтальмологические композиции с более высокой концентрацией артикаина можно вводить в меньших дозах, обеспечивая при этом требуемое анестезирующее действие для глаза.
Согласно одному из вариантов осуществления, офтальмологическая анестезирующая композиция для местного применения представляет собой водную композицию, содержащую приблизительно от 7,0% мас./об. до 8,5% мас./об. артикаина и буфер, не вступающий в реакцию с артикаином или/и не способствующий разложению артикаина. Буфер согласно варианту осуществления может обеспечивать величину рН приблизительно от рН 3,5 до рН 7,0 и осмоляльность приблизительно от 280 до 320 мосмоль/кг. Согласно одному из вариантов осуществления, офтальмологическая анестезирующая композиция имеет величину рН приблизительно от рН 4,5 до рН 5,0. Буфер согласно варианту осуществления представляет собой комплекс, полученный из кислоты и сахароспирта. Кислота может быть выбрана из группы, состоящей из борной кислоты, лимонной кислоты и их смесей. Согласно одному из частных вариантов осуществления, кислота является борной кислотой. Сахароспирт может быть D-маннитом, сорбитом и их смесью. Особенно подходящим буфером является комплекс борат/маннит, полученный из борной кислоты или ее соли, бората, и D-маннита. Буфер может представлять собой комплекс, полученный из приблизительно от 13 мас. % до 17 мас. % борной кислоты и приблизительно от 83 мас. % до 88 мас. % D-маннита, в расчете на общую массу борной кислоты и D-маннита. Анестезирующая композиция согласно варианту осуществления может содержать тригидрат ацетата натрия, уксусную кислоту и дигидрат эдетата динатрия. Анестезирующая композиция может иметь величину рН в диапазоне приблизительно от рН 4,5 до рН 7,0.
Офтальмологическая анестезирующая композиция для местного применения согласно одному из вариантов осуществления представляет собой водную смесь, содержащую по меньшей мере приблизительно 7,5% мас./об. артикаина, буфер, включающий в себя комплекс, полученный из борной кислоты и D-маннита, ацетат натрия, уксусную кислоту, эдетат динатрия и остальное - вода, где композиция имеет величину рН от рН 4,5 до рН 5,0. Было обнаружено, что величина рН менее приблизительно рН 5,0 улучшает долгосрочную стабильность композиции артикаина.
Согласно другому варианту осуществления, офтальмологическая анестезирующая композиция для местного применения представляет собой стабильную водную композицию, содержащую артикаин в количестве по меньшей мере приблизительно 8% мас./об. при величине рН приблизительно от рН 4,5 до рН 5,5, буфер и вспомогательные вещества, не вступающие в реакцию с артикаином и не способствующие разложению артикаина в водной композиции. Композиция может содержать артикаин в качестве единственного анестезирующего агента или соединения и, как правило, в отсутствие сосудосуживащего средства, такого как адреналин. Согласно одному из вариантов осуществления, композиция не содержит метабисульфита натрия и/или бисульфита натрия. Буфер в таком варианте осуществления представляет собой комплекс борат/маннит.
Отличительные признаки водной офтальмологической анестезирующей композиции для местного применения включают приблизительно от 4,0% мас./об. до 12,0% мас./об. артикаина и буфер в количестве, обеспечивающем величину рН приблизительно от рН 3,5 до рН 7,0, где буфер не вступает в реакцию с артикаином и стабилизирует его. Буфер может быть комплексом, полученным из борной кислоты и D-маннита.
Согласно одному из вариантов осуществления, водная офтальмологическая анестезирующая композиция содержит приблизительно 4% мас./об. артикаина, буфер, содержащий NaOH и HCl, имеет величину рН приблизительно рН 5,5, рКа приблизительно 7,8, вязкость приблизительно от 20 до 25 спз, осмоляльность приблизительно от 275 до 1171 мосмоль/кг и тоничность приблизительно от 0,5 до 5,0%.
Согласно другому варианту осуществления, водная анестезирующая композиция для местного применения содержит 80 мг/г артикаина-HCl, 1,373 мг/г моногидрата дигидрофосфата натрия, 1,413 мг/г безводного двухосновного фосфата натрия, 8,1 мг/г гидроксипропилметилцеллюлозы, 4 мг/г PEG400 (англ. polyethylenglycol - полиэтиленгликоль), где указанная композиция имеет величину рН от рН 6,0 до рН 7,0, вязкость от 743 до 803 спз и осмоляльность 517 мосмоль/кг.
Другим отличительным признаком данного раскрытия является способ предотвращения боли или дискомфорта в глазу пациента во время различных хирургических процедур на глазу и/или инъекции в глаз иглой. Согласно этому способу, анестезирующую композицию для местного применения вводят в глаз в количестве, вызывающем анестезию глаза, где анестезирующая композиция содержит количество артикаина, эффективное для обработки поверхности глаза и ткани под поверхностью глаза, включая плоскую часть ресничного тела. Способ особенно подходит для процедур введения вещества или лекарственного препарата в глаз, где поверхность глаза обрабатывают композицией для местного применения, содержащей по меньшей мере 4,0% мас./об. артикаина и нереакционноспособный буфер для получения величины рН приблизительно от рН 4,5 до рН 7,0 и, как правило, приблизительно от рН 4,5 до рН 5,5. Согласно другим вариантам осуществления, композиция для местного применения имеет величину рН от 4,5 до рН 5,0.
Эти и другие отличительные признаки станут очевидными из следующего подробного описания.
ПОДРОБНОЕ ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Объекты, рассмотренные в качестве примеров в данном описании, приведены, чтобы помочь общему пониманию примеров вариантов осуществления раскрытия. Соответственно, специалистам в данной области техники будет очевидно, что возможны различные изменения и модификации описанных в данном документе вариантов осуществления без отклонения от объема и сущности раскрытия. При этом описания хорошо известных функций и конструкций опущены для ясности и краткости. В раскрытии диапазоны различных компонентов и отличительных признаков композиции могут быть объединены с диапазонами или отличительными признаками других вариантов осуществления. Описанные варианты осуществления не предназначены для ограничения, так что отличительные признаки одного варианта осуществления могут быть объединены с другими вариантами осуществления.
Фразеология и терминология, использованные в данном документе, предназначены для описания и их не следует рассматривать, как ограничивающие. Использование в настоящем документе слов "включающий", "содержащий" или "имеющий" и их вариантов должно охватывать перечисленные после них элементы и их эквиваленты, а также дополнительные элементы. Варианты осуществления не предназначены для того, чтобы быть взаимоисключающими, так что отличительные признаки одного варианта осуществления могут быть объединены с другими вариантами осуществления до тех пор, пока они не противоречат друг другу. Термины, характеризующие количество, такие как "по существу", "приблизительно" и "примерно" понимаются специалистами в данной области как относящиеся к разумным диапазонам вблизи данной величины и включая ее, а также к диапазонам за пределами данной величины, например, общие допуски, связанные с изготовлением, сборкой и применением вариантов осуществления. Термин "по существу", относящийся к структуре или характеристике, включает в себя характеристику, которая в основном или полностью присутствует в характеристике или структуре.
В примерах вариантов осуществления настоящего раскрытия предложены методики, использующие анестезирующую композицию или препарат для местного применения, содержащий артикаин, с улучшенным анестезирующим действием на глаз и с пониженным риском инфицирования глаза. При использовании в данном контексте термины "композиция" и "препарат" используются взаимозаменяемо для обозначения смеси или комбинации соединений, включающей активные соединения и вспомогательные вещества. В описанных вариантах осуществления композиция представляет собой водную смесь, содержащую артикаин, буферы и другие вспомогательные вещества, для получения стабильной композиции с величиной рН, осмоляльностью и концентрацией артикаина, подходящими для местного нанесения на глаз.
Офтальмологическая анестезирующая композиция для местного применения представляет собой анестезирующую композицию, содержащую эффективное количество анестезирующего агента, для анестезии поверхности и внутренних сторон глаза пациента путем местного применения для выполнения различных медицинских манипуляций, таких как инъекции в стекловидное тело. Согласно одному из вариантов осуществления, офтальмологическую анестезирующую композицию для местного применения готовят в виде композиции для местного применения и наносят непосредственно на поверхность глаза для анестезии поверхности глаза и внутренней стороны глаза. Офтальмологическая анестезирующая композиция для местного применения содержит артикаин в количестве, эффективном для обеспечения анестезирующего действия на глаз для уменьшения или предотвращения боли и/или дискомфорта у пациента во время медицинской манипуляции на глазу, такой как инъекция в стекловидное тело или другая хирургическая операция.
Офтальмологическая анестезирующая композиция для местного применения, содержащая артикаин, может иметь различные диапазоны значений рН и содержать разные количества артикаина в зависимости от буфера и стабилизирующих агентов, включенных в анестезирующую композицию. В вариантах осуществления анестезирующей композиции буферы и стабилизирующие агенты обеспечивают эффективную анестезирующую композицию для местного применения, в которой буферы и стабилизирующие агенты позволяют получать различные диапазоны рН для стабилизации композиции и поддержания подходящей осмоляльности композиции.
Офтальмологическая анестезирующая композиция для местного применения в различных вариантах осуществления содержит приблизительно от 4,0% мас./об. до 13% мас./об. артикаина при величине рН, приемлемой для стабилизации артикаина, и при величине рН, приемлемой для сведения к минимуму дискомфорта пациента. Также могут быть приготовлены подходящие анестезирующие композиции, содержащие по меньшей мере 6% мас./об. артикаина. Композиция в описанных вариантах осуществления представляет собой водную офтальмологическую анестезирующую композицию. Согласно одному из вариантов осуществления, офтальмологическая анестезирующая композиция для местного применения содержит артикаин в количестве по меньшей мере приблизительно 7,0% мас./об. и, как правило, по меньшей мере приблизительно 8,0% мас./об. артикаина, в расчете на общий объем композиции. Согласно другому варианту осуществления, офтальмологическая анестезирующая композиция для местного применения содержит артикаин в количестве по меньшей мере приблизительно 8,5% мас./об. артикаина. При использовании в данном контексте мас./об. относится к граммам на 100 мл композиции. Офтальмологическая композиция обычно содержит по меньшей мере приблизительно 4% мас./об. артикаина и приблизительно до 8,5% мас./об. артикаина. Согласно одному из вариантов осуществления, композиция для местного применения содержит по меньшей мере приблизительно 7,0% и, как правило, по меньшей мере приблизительно 8,0% мас./об. артикаина. Артикаин, используемый в композиции для местного применения, обычно получают из его хлористоводородной соли.
Офтальмологическая композиция для местного применения согласно одному из вариантов осуществления содержит артикаин в количестве по меньшей мере приблизительно 4% мас./об. и буфер для регулирования величины рН в требуемом диапазоне. Согласно одному из вариантов осуществления, композиция для местного применения имеет величину рН в диапазоне от рН 4,5 до рН 7,0. Согласно другим вариантам осуществления, композиция может иметь величину рН приблизительно от рН 6,0 до рН 7,0. Согласно другим вариантам осуществления, композиция для местного применения может иметь величину рН менее рН 5,0. Буфер не вступает в реакцию с артикаином при величине рН от 4,0 до рН 7,0, ингибируя разложение артикаина, что обеспечивает стабильную при хранении композицию. Офтальмологическая композиция для местного применения может содержать артикаин в количестве более приблизительно 4,0% мас./об. и буфер для обеспечения стабильной смеси при величине рН приблизительно рН 6,0 или ниже, где буфер не вступает в реакцию с артикаином.
Величину рН офтальмологической композиции для местного применения обычно регулируют для поддержания требуемой долгосрочной стабильности артикаина и сведения к минимуму дискомфорта для пациента при местном нанесении на поверхность глаза. Величина рН обычно находится в диапазоне приблизительно от рН 4,5 до рН 7,0. Особенно предпочтительная величина рН композиции, содержащей артикаин, составляет приблизительно от рН 4,5 до рН 5,5 для композиции, содержащей артикаин в количестве более приблизительно 4,0% и, как правило, более приблизительно 6,0% мас./об. Например, подходящая композиция, содержащая по меньшей мере 7,0% мас./об. или выше, имеет диапазон рН приблизительно от рН 4,5 до рН 5,5 и, как было установлено, демонстрирует длительное хранение артикаина в составе композиции в течение нескольких месяцев при комнатной температуре. Композиции с величиной рН 5,0 или ниже обеспечивают длительное хранение артикаина, ингибируя разложение артикаина во время хранения. Композиции с величиной рН приблизительно от рН 4,5 до рН 5,0 обеспечивают очень хорошее длительное хранение, не сопровождающееся дискомфортом для пациента при местном нанесении.
Офтальмологическая анестезирующая композиция для местного применения, содержащая артикаин, включает буфер для регулирования, модифицирования и/или поддержания величины рН и осмоляльности в пределах требуемого диапазона для стабилизации артикаина, не вступающий в реакцию с артикаином или не вызывающий разложения артикаина в композиции во время хранения. Буфер и другие вспомогательные вещества, входящие в состав офтальмологической анестезирующей композиции для местного применения, обеспечивают более высокие концентрации артикаина 7,5% мас./об. и до 8,5% мас./об. или выше без разложения артикаина при сохранении артикаина в растворе или суспензии с минимальным дискомфортом для пациента при местном применении композиции на поверхность глаза. Буфер в соответствии с вариантами осуществления композиции обеспечивает стабильную композицию при более высоких концентрациях артикаина, отсутствующих в композициях предшествующего уровня техники.
Артикаин способен ингибировать рост некоторых бактерий, таких как Pseudomonas aeruginosa, Proteus mirabilis, Staphylococcus aureus и Escherichia coli. Считается, что механизм антибактериального действия опосредован ингибированием синтеза клеточной стенки или искажением цитоплазматической мембраны.
Описанная офтальмологическая анестезирующая композиция для местного применения представляет собой стабильную композицию, которую можно наносить локально на поверхность глаза. Офтальмологическую анестезирующую композицию для местного применения можно наносить в форме капель непосредственно на поверхность глаза. Офтальмологическая анестезирующая композиция для местного применения содержит количество артикаина, которое может оказывать анестезирующее действие на глаз при однократном дозировании на поверхность глаза. Для обеспечения требуемого анестезирующего действия дозировку выбирают с учетом конечной концентрации артикаина и других буферов, агентов для регулирования величины рН и прочих вспомогательных веществ в композиции. Согласно одному из вариантов осуществления, композицию для местного применения применяют в виде однократного дозирования одной капли объемом приблизительно от 2 мкп до 30 мкл при концентрации артикаина приблизительно 8,0 мг/г анестезирующей композиции. Например, размер капли составляет приблизительно 15 мкп. Согласно одному из вариантов осуществления, для офтальмологической композиции, содержащей приблизительно 8% мас./об. артикаина, подходящая дозировка составляет приблизительно 0,5 мкл. Согласно другим вариантам осуществления, композицию, содержащую артикаин, можно применять в виде приблизительно от 3 до 5 капель на поверхность глаза, что обеспечивает дозировку приблизительно от 20 мкл или единиц до 100 мкл. Согласно другому варианту осуществления, офтальмологическую анестезирующую композицию для местного применения наносят в дозировке от 3 до 8 капель, обычно приблизительно от 3 до 5 капель на поверхность глаза, что обеспечивает дозировку приблизительно от 40 мкл до 80 мкл композиции, содержащей приблизительно 8% мас./об. артикаина.
Согласно первому варианту осуществления анестезирующей композиции для местного применения, композиция представляет собой водную смесь, содержащую буфер, и имеет диапазон рН приблизительно от рН 3,5 до рН 7,0. Композиция может содержать менее 2 м.д. растворенного кислорода для стабилизации композиции и ингибирования окисления артикаина и/или других соединений в композиции. Особенно подходящий диапазон рН составляет приблизительно от рН 4,5 до рН 5,0, а осмоляльности - приблизительно от 580 до 630 мосмоль/кг. Подходящее количество артикаина в композиции составляет приблизительно от 7,0% до 8,5% мас./об. артикаина. Буфер в таком варианте осуществления может представлять собой комплекс, полученный из смеси борной кислоты и D-маннита. Было обнаружено, что комплекс борат/маннит, полученный из борной кислоты и D-маннита, стабилизирует артикаин и обеспечивает стабильность при длительном хранении артикаина в составе композиции при концентрациях артикаина выше приблизительно 4% мас./об. и выше 7% мас./об., при величине рН в диапазоне от рН 4,5 до рН 5,0, не вызывая раздражения глаза при местном нанесении на поверхность глаза. Не желая быть связанными соответствием какой-либо конкретной теории, авторы полагают, что боратный компонент комплекса борат/маннит обеспечивает подходящее стабилизирующее действие в отношении артикаина, что поддерживает постоянную концентрацию артикаина по меньшей мере 7% мас./об. при величине рН менее приблизительно рН 5,5. Буфер обеспечивает для артикаина стабильный диапазон рН приблизительно от рН 4,5 до рН 5,0, поддерживая концентрации артикаина выше 4% мас./об. без раздражения глаза.
Согласно другим вариантам осуществления, буфер может быть получен с использованием другого источника борат-аниона, такого как борнокислая соль (борат). Примеры борнокислых солей включают борат натрия, борат кальция, борат магния, борат марганца и другие. Буферный комплекс может быть получен из реакционной смеси, содержащей борную кислоту, лимонную кислоту или их смеси и сахароспирт, такой как D-маннит, сорбит и их смеси. Было установлено, что комплекс борат/маннит особенно подходит для стабилизации высоких концентраций артикаина, таких как 8% мас./об. артикаина или выше. В качестве источника бората и/или цитрата в реакционной смеси для образования комплекса борат/маннит, комплекса цитрат/маннит и/или комплекса борат/цитрат/маннит могут быть использованы борнокислая соль (борат) и/или лимоннокислая соль (цитрат).
Анестезирующая композиция согласно одному из вариантов осуществления содержит буферный комплекс, полученный из борной кислоты и сахароспирта, такого как D-маннит, где буферный комплекс представляет собой комплекс борат/маннит. Соотношение или относительные количества борной кислоты и сахароспирта выбирают с учетом требуемых рН, осмоляльности, совместимости с артикаином и концентрации артикаина в анестезирующей композиции. Буфер может быть получен из смеси борной кислоты в количестве приблизительно от 13 мас. % до 15 мас. % и D-маннита в количестве приблизительно от 85 мас. % до 87 мас. % в расчете на общую массу смеси борной кислоты и D-маннита. Буфер согласно одному из вариантов осуществления может быть получен из смеси приблизительно 14 мас. % борной кислоты и приблизительно 86 мас. % D-маннита в расчете на общую массу борной кислоты и D-маннита. Борная кислота, образующая комплекс борат/маннит, может присутствовать в офтальмологической анестезирующей композиции для местного применения в количестве приблизительно от 0,08% мас./об. до 0,10% мас./об., а D-маннит - в количестве от 0,50% мас./об. до приблизительно 0,60% мас./об. в расчете на общий объем офтальмологической анестезирующей композиции для местного применения.
Количество комплекса борат/маннит, включенного в офтальмологическую анестезирующую композицию для местного применения, зависит от количества артикаина в конечной композиции, что позволяет стабилизировать артикаин и обеспечивать длительное хранение офтальмологической композиции. Количество комплекса борат/маннит может составлять приблизительно от 0,4% мас./об. до 0,75% мас./об. в расчете на общий объем офтальмологической композиции. Согласно одному из вариантов осуществления, количество комплекса борат/маннит может составлять приблизительно от 0,5% мас./об. до 0,75% мас./об. в расчете на общий объем офтальмологической композиции. Согласно другим вариантам осуществления, комплекс борат/маннит включен в конечную офтальмологическую композицию в количестве приблизительно от 6,5 массовых частей до 7,5 массовых частей в расчете на 100 массовых частей артикаина в офтальмологической композиции.
Согласно другим вариантам осуществления, буферный комплекс получают из кислоты, такой как борная кислота, лимонная кислота и их смеси, и сахароспирта, такого как маннит, сорбит и их смеси, где соотношение кислоты и сахароспирта может варьироваться приблизительно от 1:10 до 10:1. Согласно описанному варианту осуществления, количество сахароспирта превышает количество кислоты, т.е. соотношение кислоты и сахароспирта составляет от 1:3 до 1:10. Соотношение борной кислоты и маннита может составлять приблизительно от 1:3 до 1:7 по массе. Согласно одному из вариантов осуществления, массовое соотношение борной кислоты и маннита может составлять приблизительно от 1:4 до 1:6. В качестве еще одного примера, приемлемое массовое соотношение борной кислоты и маннита может составлять приблизительно от 1:4,5 до 1:5,5. Другим примером подходящего буферного комплекса является комплекс борат/цитрат/маннит, полученный из смеси борной кислоты, лимонной кислоты и маннита.
Согласно варианту осуществления, дополнительно к борной кислоте и D-манниту могут быть включены и другие буферные и антиокислительные компоненты. Пример дополнительного буферного и/или антиокислительного соединения включает ацетат-анион, такой как тригидрат ацетата натрия. Дополнительное буферное и/или антиокислительное соединение может быть включено в количестве приблизительно от 0,3% до 0,5% мас./об. в расчете на общий объем офтальмологической анестезирующей композиции для местного применения. Согласно такому варианту осуществления, тригидрат ацетата натрия включен в количестве 0,33% мас./об. в расчете на общий объем офтальмологической анестезирующей композиции для местного применения. Ацетат натрия может быть включен вместе с комплексом борной кислоты и D-маннита в количестве приблизительно от 33 мас. % до 35 мас. % и, как правило, приблизительно 34 мас. %, в расчете на общую массу буфера, содержащего борную кислоту, D-маннит и ацетат натрия.
Другие вспомогательные вещества, входящие в офтальмологическую анестезирующую композицию для местного применения, включают агенты для регулирования величины рН или антисептические соединения. Примером кислоты, подходящей для регулирования величины рН, обладающей антисептическими свойствами и совместимой с офтальмологической анестезирующей композицией для местного применения, содержащей артикаин, является уксусная кислота, такая как ледяная уксусная кислота. Уксусная кислота, обычно добавляемая в виде ледяной уксусной кислоты, включена в количестве приблизительно от 0,05% мас./об. до 0,07% мас./об. в расчете на общий объем анестезирующей композиции. Другие вспомогательные вещества могут включать хелатирующий агент, такой как дигидрат эдетата динатрия.
Офтальмологическая анестезирующая композиция для местного применения согласно одному из вариантов осуществления содержит артикаин в количестве приблизительно 4,5% до 8,5% мас./об., комплекс, полученный из борной кислоты и D-маннита, в качестве буфера, ацетат натрия, уксусную кислоту, эдетат динатрия и остальное - вода. Согласно подходящему варианту осуществления, офтальмологическая анестезирующая композиция для местного применения содержит приблизительно от 7,5% до 8,5% мас./об. артикаина, комплекс, полученный из приблизительно от 0,08% мас./об. до 0,10% мас./об. борной кислоты и приблизительно от 0,5% мас./об. до 0,6% мас./об. D-маннита, приблизительно от 0,30 до 0,36% мас./об. ацетата натрия, приблизительно от 0,05% мас./об. до 0,07% мас./об. ледяной уксусной кислоты, приблизительно от 0,05% мас./об. до 0,07% мас./об. дигидрата эдетата динатрия в расчете на общий объем композиции. Композиция для местного применения может иметь осмоляльность приблизительно от 580 до 630 мосмоль/кг. Согласно другому варианту осуществления, композиция состоит по существу из артикаина, буфера, полученного из борной кислоты и D-маннита, диацетата натрия, уксусной кислоты, эдетата динатрия и воды.
Другим приемлемым примером подходящей офтальмологической композиции для местного применения является композиция, содержащая приблизительно от 7,5% до 8,5% мас./об. артикаина в расчете на общий объем композиции, буферный комплекс борат/маннит и соединение, стабилизирующее артикаин, где композиция имеет величину рН приблизительно от рН 4,5 до рН 7,0, осмоляльность приблизительно от 500 до 700 мосмоль/кг и вязкость приблизительно от 700 до 850 спз.
Согласно другому варианту осуществления, офтальмологическая анестезирующая композиция для местного применения представляет собой водную композицию, содержащую по меньшей мере 4% мас./об. артикаина и буфер, не вступающий в реакцию с артикаином, для обеспечения стабильной композиции без разложения артикаина и с минимальным раздражением глаза. Согласно другим вариантам осуществления, офтальмологическая анестезирующая композиция для местного применения содержит артикаин в количестве приблизительно от 5,0% до 8,5% мас./об. в расчете на общий объем композиции. Согласно другим вариантам осуществления, офтальмологическая анестезирующая композиция для местного применения содержит артикаин в количестве по меньшей мере приблизительно 8,0% мас./об. в расчете на общий объем композиции.
Буфер выбирают таким образом, чтобы он был совместим с артикаином во избежание реакций с артикаином, ингибировал разложение артикаина во время хранения и обеспечивал величину рН для стабилизации артикаина и обеспечения требуемой концентрации артикаина в композиции при минимальном раздражении глаза. Буфер стабилизирует артикаин за счет стабилизации реакционноспособных групп, таких как аминогруппа. Стабилизаторы включает в себя соединения, ингибирующие окисление реакционноспособных групп артикаина кислородом и/или оксо-радикалами. В некоторых вариантах осуществления примером стабилизатора для ингибирования окисления является сульфит натрия. Другие антиокислители включают натриевую соль EDTA (англ. Ethylene Diamine Tetraacetic Acid - этилендиаминтетрауксусная кислота), метасульфит натрия и аскорбиновую кислоту. Офтальмологическая анестезирующая композиция для местного применения по одному из вариантов осуществления имеет величину рН приблизительно от рН 4,5 до рН 7,0 и осмоляльность от 280 до 320 мосмоль/кг. Согласно другим вариантам осуществления, буфер содержит соединения для подержания величины рН офтальмологической анестезирующей композиции для местного применения в диапазоне приблизительно от рН 5,0 до рН 7,0. Буфер также позволяет получить композицию, имеющую величину рН приблизительно от рН 4,7 до рН 5,5 в зависимости от композиции и буфера. Согласно другому варианту осуществления, офтальмологическая анестезирующая композиция для местного применения может иметь величину рН по меньшей мере рН 5,4. Величина рН может зависеть от буферов и концентрации артикаина в офтальмологической анестезирующей композиции для местного применения.
Офтальмологическая анестезирующая композиция для местного применения может быть приготовлена с использованием способов или методик получения композиции, подходящей для местного нанесения на глаз. В вариантах осуществления, содержащих буферный комплекс, комплекс обычно готовят перед смешиванием или объединением с артикаином для обеспечения стабилизирующего воздействия на артикаин. Согласно одному из вариантов осуществления, способ получения композиции предполагает сначала приготовление комплекса в водной среде путем добавления кислотного компонента в воду с образованием раствора кислоты. Кислотным соединением может быть борная кислота, лимонная кислота или их смеси. Затем в раствор кислоты добавляют сахароспирт, такой как маннит, сорбит или их смеси, и оставляют реагировать в течение времени, достаточного для образования комплекса, такого как комплекс борат/маннит. После этого в раствор комплекса борат/маннит добавляют вспомогательные вещества для получения требуемого значения рН и образования конечной композиции. Примеры вспомогательных веществ включают добавление в раствор комплекса борат/маннит тригидрата ацетата натрия до растворения. Для подкисления раствора добавляют уксусную кислоту, такую как ледяная уксусная кислота. Затем добавляют дигидрат EDTA для получения требуемого значения рН. Добавляют соль артикаин HCl и растворяют, получая композицию, содержащую артикаин, для приготовления офтальмологической композиции, имеющей требуемую концентрацию артикаина.
Могут быть использованы различные способы введения и анестезирования глаза пациента с помощью содержащей артикаин офтальмологической анестезирующей композиции для местного применения. Согласно одному из вариантов осуществления, водную анестезирующую композицию для местного применения наносят непосредственно на поверхность глаза в количестве, эффективном для обеспечения достаточной анестезии глаза. Для обеспечения достаточной анестезии глаза офтальмологическую анестезирующую композицию для местного применения, содержащую 7% мас./об. или более, можно вводить на поверхность глаза по каплям. Для композиции, содержащей по меньшей мере приблизительно 7% мас./об. артикаина, подходящая дозировка обычно составляет приблизительно 30 мкл. В случае композиций, содержащих менее 7% мас./об. артикаина, для введения на поверхность глаза количества артикаина, эффективного для достижения требуемого анестезирующего действия, может потребоваться большая дозировка или повторное дозирование.
Согласно другому варианту осуществления, буфер может представлять собой борат/маннит (рН 6,0), цитрат (рН 5,5), ацетат (рН 5,5) или фосфат (рН 6,5, 7,0, 7,5). Буфер может быть включен в количестве не более 25 мМ и обеспечивать величину рН менее рН 7,0, как правило, менее рН 5,5. Согласно другим вариантам осуществления, буфер может включать в себя смесь гидроксида натрия и соляной кислоты. Другие подходящие буферы включают одноосновный фосфат натрия и двухосновный фосфат натрия.
Анестезирующая композиция для местного применения также может содержать необязательные смазывающие вещества и модификаторы вязкости. Примеры других добавок и вспомогательных веществ могут включать полиэтиленгликоль, глицерин, сульфит натрия, метасульфит натрия, цетиловый спирт, гидроксипропил-В-циклодекстрин, полоксамер, тилоксапол и аскорбат.
Примеры вариантов осуществления настоящего раскрытия предлагают офтальмологическое анестезирующее средство для местного применения, имеющее уникальный состав с требуемыми концентрацией артикаина, величиной рН, вязкостью, константой диссоциации и добавками, такими как антиокислители, буферы, загустители, такие как метил целлюлоза, для достижения эффективности и безопасности. Примеры реализации настоящего раскрытия включают препараты, являющиеся жидкостью, гелем, мазью или выполненные в капсулированной форме.
Другие примеры реализации настоящего раскрытия могут учитывать практические вопросы изготовления препаратов в соответствии с примерами вариантов осуществления. Например, в случае примеров реализации, включающих в себя офтальмологический раствор, могут быть добавлены различные количества метилцеллюлозы для повышения вязкости и увеличения посредством этого времени контакта с внешней поверхностью глаза, что повышает эффективность артикаина. Подходящие модификаторы вязкости не вступают в нежелательные реакции с артикаином и не дестабиллизируют его. Другие модификаторы вязкости включают поливиниловые спирты и гидроксипропилметилцеллюлозу.
Еще один примерный вариант реализации офтальмологической анестезирующей композиции для местного применения содержит артикаин в количестве приблизительно от 4% до 8,0% мас./об. в сочетании с адреналином, 1:100000, в виде стерильной композиции для местного применения в виде офтальмологических капель. Композицию можно применять локально для обработки глаза при подготовке к инъекции в стекловидное тело. Для получения требуемого анестезирующего воздействия на глаз композицию для местного применения можно наносить в виде одной капли либо использовать несколько аппликаций. Местную офтальмологическую композицию можно применять в виде капли, используя от 3 до 6 аппликаций с интервалами от 3 до 5 минут между аппликациями. Согласно другому варианту осуществления, композицию для местного применения можно наносить или вводить в виде одной капли и повторно наносить через от 2 до 5 минут от 3 до 5 раз.
Другой пример варианта осуществления предлагает местную офтальмологическую анестезирующую композицию, содержащую артикаин, в качестве офтальмологического анестезирующего средства для местного применения, содержащего от 4% до 8,0% мас./об. артикаина, имеющего величину рН приблизительно от рН 4,5 до рН 5,5 и значение рКа приблизительно от 7,0 до 8,5. Пример водной анестезирующей композиции включает в себя композицию, содержащую приблизительно от 4% мас./об. до 5 мас./об. артикаина, имеющую величину рН 5,5, рКа 7,8, вязкость от 20 до 25 спз (сантипуаз), осмоляльность от 275 до 1171 мосмоль/кг, тоничность от 0,5% до 5,0%, содержащую NaOH буфер и HCl буфер.
Еще один пример подходящей водной офтальмологической композиции для местного применения включает в себя композицию, содержащую приблизительно от 4% мас./об. до 13% мас./об. артикаина, как правило, по меньшей мере приблизительно 7% мас./об. артикаина, моногидрат дигидрофосфата натрия, двухосновный фосфат натрия, усилитель вязкости, такой как гидроксипропилметилцеллюлоза и полиэтиленгликоль, имеющую величину рН приблизительно от рН 6,0 до рН 7,0. Пример анестезирующей композиции включает композицию, содержащую 80 мг/г артикаина HCl, 1,373 мг/г моногидрата дигидрофосфата натрия, 1,413 мг/г безводного двухосновного фосфата натрия, 8,1 мг/г гидроксипропилметилцеллюлозы, 4 мг/г PEG400, где композиция имеет величину рН от рН 6,0 до рН 7,0, вязкость от 743 до 803 спз и осмоляльность 517 мосмоль/кг.
Композиция для местного применения, содержащая 4% мас./об. артикаина, применяемая в виде одной или двух доз, не обеспечивала полного анестезирующего действия. Однако было отмечено, что использование 3 или более доз по одной капле за одно применение с интервалами от 3 до 5 минут приводили к эффективной анестезии. Кроме того, пациенты не жаловались на жжение, зуд, покраснение или другие проявления раздражения глазной поверхности, обычно наблюдающиеся при применении принятых в настоящее время местных офтальмологических анестезирующих средств.
Отличительным признаком раскрытия является способ обеспечения анестезии глаза путем местного применения или доставки в глаз анестезирующей офтальмологической композиции для местного применения. Анестезирующее средство вводят местно перед хирургическим вмешательством, например, перед внутриглазными инъекциями, витрэктомией в плоской части ресничного тела и тому подобным.
Обычно врач вводит инъекционное анестезирующее средство для анестезии глаза, после чего он должен выждать требуемый период времени, чтобы анестезирующее средство подействовало, прежде чем начинать процедуру. Преимущество местного применения в соответствии с примерами реализации настоящего раскрытия заключается в простоте введения анестезирующего средства путем местного нанесения композиции без необходимости инъекции анестезирующего средства в глаз.
Хорошо известно об эффективности и безопасности артикаина при использовании его в качестве анестезирующего средства путем инъекции, например, в стоматологической отрасли. Артикаин HCl имеет молекулярную формулу, соответствующую гидрохлориду метилового эфира 4-метил-3-(2-[пропиламино]пропионамидо)-2-тиофенкарбоновой кислоты, молекулярную массу 320,84 г/моль, высокую степень связывания с белками и величину рКа 7,8. Артикаин представляет собой амидсодержащее анестезирующее средство, содержащее тиофеновое кольцо и дополнительную сложноэфирную группу. Тиофеновое кольцо обеспечивает лучшую растворимость артикаина в липидах по сравнению с другими амидсодержащими анестезирующими средствами. Артикаин обладает высокой диффузионной способностью и эффективно проникает в ткани и кости при введении путем инъекции. Наличие амидной группы и сложноэфирной связи сводит к минимуму токсическую реакцию, поскольку биотрансформация происходит как в плазме (гидролиз плазменной эстеразой), так и в печени (микросомальными ферментами). Метаболизм инициируется гидролизом сложноэфирных групп с образованием свободной карбоксильной группы. Основным метаболитом является артикаиновая кислота. Дополнительные неактивные метаболиты обнаружены в небольших количествах. От 5 до 10% выводится почками в неизмененном виде, а 89% выводится в виде метаболитов. Инъекционную форму артикаина обычно применяют в качестве анестезирующего средства в стоматологии.
Артикаин действует путем ингибирования нервной проводимости за счет блокады натриевых каналов в ткани. Артикаин действует путем обратимого связывания с альфа-субъединицей потенциалзависимых натриевых каналов внутри нерва. Это уменьшает приток натрия, в результате чего пороговый потенциал действия нерва не достигается, что приводит к угнетению проводимости импульса. Артикаин представляет собой проникающее в ткани местное анестезирующее средство короткого действия с быстрым началом действия. Артикаин применяют в составе инъекционных композиций в комбинации с адреналином для того, чтобы вызвать местное сужение сосудов, повышая абсорбцию и увеличивая продолжительность действия. В виде инъекций артикаин обычно используют в концентрации 4% мас./об. Коммерчески доступные инъекционные препараты включают гидрохлорид артикаина (4%) с адреналином в количестве 1:1000000 (0,01 мг/мл).
О каких-либо серьезных побочных реакциях на коммерчески доступные инъекционные формы артикаина не сообщалось. Аллергические реакции возникают редко, хотя бисульфит натрия, используемый в некоторых коммерческих препаратах в качестве консерванта, может вызывать у отдельных пациентов аллергические реакции, такие как отек, крапивница, покраснение кожи и анафилактический шок. Артикаин не приводит к повышению уровня метгемоглобина. Артикаин противопоказан пациентам с аллергией на амидсодержащие анестезирующие средства и метабисульфиты. Артикаин не противопоказан пациентам с аллергией на сульфаниламиды, поскольку отсутствует перекрестная аллергенность между тиольной группой тиофенового кольца артикаина и сульфаниламидами.
Следующем примеры представлены для иллюстрации подходящих композиций и способов и не предназначены для ограничения объема данного описания.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Пример 1
Две части одного из исследований проводили на голландских кроликах (Dutch Belted rabbit), а именно, исследование офтальмологической переносимости и последующее исследование биораспределения в глазу.
При изучении офтальмологической переносимости в общей сложности двенадцати самцам голландских кроликов, случайным образом распределенным в четыре группы, вводили плацебо, фосфатно-солевой буфер (англ. PBS) или артикаин в концентрации 4%, 8% или 12%, соответственно. Дозы вводили путем двустороннего местного введения (две капли по 35 мкл/глаз). При изучении переносимости дозы за кроликами наблюдали в течение 24 ч после обработки на предмет выявления любых признаков/симптомов нежелательных реакций на лекарственное средство. Офтальмологические исследования проводили на животных с переносимостью дозы (группы с 1 по 4) до применения препарата и через 5, 10 и 20 минут, а также через 1, 2, 4 и 24 часа после второго введения глазных капель в каждый глаз с использованием модифицированной системы оценки Хакетта-Макдональда. Следуя модифицированной шкале Хакетта-Макдональда, контролировали местное анестезирующее действие в каждом глазу с помощью эстезиометрии Кочета-Боннета до использования препарата и приблизительно через 5, 10, 20 минут и 1 час после введения второй глазной капли в каждый глаз. Глазные капли, содержащие артикаин, хорошо переносились всеми животными в концентрациях до 12% мас./об., при этом не отмечалось никаких нежелательных явлений, связанных с лечением. Местное офтальмологическое введение артикаина обеспечивало анестезирующее действие в течение 20 минут после дозирования без каких-либо заметных проблем с переносимостью.
При изучении биораспределения в глазу через, как минимум, 72 часа после завершения исследования офтальмологической переносимости двенадцать кроликов перераспределяли в группу 5 для изучения биораспределения в глазу. Добавляли группу 6, в которую вошли 3 интактных кролика. Группа 6 была включена для оценки потенциального влияния предшествующей терапии артикаином в течение 72 часов после обработки. Животным групп 5 и 6 вводили артикаин в дозах 8% и 12% мас./об., соответственно. Дозы вводили путем двустороннего местного введения (две капли по 35 мкл/глаз). Животных группы 5 умерщвляли через 10 минут и через 1, 4 и 8 часов после обработки (N=3 в каждый момент времени). Кроликов группы 6 умерщвляли через 24, 48 и 72 часа после обработки (N=1 в каждый момент времени). Непосредственно перед умерщвлением у каждого животного брали образцы крови. Затем животных подвергали эвтаназии и забирали внутриглазную жидкость, конъюктивы (палпебральную и бульбарную части), хрусталик, роговицу, жидкую часть стекловидного тела, иридо-цилиарную зону [англ. ICB], зрительный нерв, слезную железу, сетчатку и хороид. Ткани плазмы, внутриглазной жидкости, конъюктив (палпебральной и бульбарной частей), хрусталика, роговицы, ICB, хороида и слезной железы анализировали в отношении концентраций артикаина (активного исходного соединения) и артикаиновой кислоты (неактивного метаболита), остальные ткани хранили в замороженном состоянии для возможного последующего анализа. Концентрации артикаина после местного введения в глаз 8% препарата имели типичный профиль; с максимумом в самый ранний исследуемый момент времени (0,167 часов) и затем снижающийся в более поздние моменты времени (1, 4 и 8 часов). Концентрации артикаиновой кислоты следовали аналогичному профилю во всех матриксах, за исключением внутриглазной жидкости, в которой концентрация возрастала с 0,167 часа до 1 часа, а затем снижалась в более поздние моменты времени (4 и 8 часов). Низкие остаточные концентрации артикаина и артикаиновой кислоты после местного введения в глаз 12% артикаина были обнаружены во всех матриксах глаза, исследованных через 24, 48 и 72 часа после дозирования (за исключением артикаиновой кислоты в хороиде). При этом концентрации артикаина была выше, чем концентрация артикаиновой кислоты во всех матриксах глаза, за исключением роговицы. Как и ожидалось, Tmax после местного введения в глаз артикаина отмечался в первый исследованный момент времени (0,167 часов) во всех матриксах глаза и плазме. Cmax артикаина была самой высокой в иридо-цилиарной зоне (294000 нг/г), затем в палпебральной части конъюктивы (131000 нг/г), хороиде (103000 нг/г), бульбарной части конъюктивы (94000 нг/г) и роговице (53,500 нг/г). Cmax в плазме составляла 457 нг/мл, что является самым низким показателем из всех исследованных матриц. Значения AUC (англ. Area under the curve - площадь под фармакокинетической кривой), выражающие воздействие артикаина на матриксы, обычно следовали тому же порядку от наивысшего (т.е. иридо-цилиарной зоны) до самого низкого (т.е. плазмы), как видно из значений Cmax. Т1/2 (период полувыведения) артикаина в матриксах глаза варьировался от 1,95 до 3,83 часа за исключением палпебральной части конъюктивы, где Т1/2 составлял 6,31 часа, что, вероятно, связано с накоплением местной дозы на нижнем веке после дозирования. Т1/2 артикаина в плазме составлял приблизительно 0,5 часов. Cmax артикаиновой кислоты была самой высокой в палпебральной части конъюктивы (71,100 нг/г), роговице (53,500 нг/г), бульбарной части конъюктивы (29,100 нг/г) и иридо-цилиарной зоне (12,600 нг/г). Cmax в плазме составляла 217 нг/мл, что является самым низким показателем из всех исследованных матриц. Значения AUC, выражающие воздействие на матриксы артикаиновой кислоты, обычно следовали тому же порядку от высокого к низкому, что и в случае артикаина, но были существенно ниже, чем для артикаина, за исключением роговицы и плазмы. Как было отмечено для соотношения AUC0-последнее артикаиновой кислоты и AUC0-последнее артикаина, это соотношение составляло приблизительно 2 как для роговицы, так и для плазмы, что указывает на большее воздействие артикаиновой кислоты, чем артикаина в этих двух матриксах. Во всех других матриксах соотношение составляло <0,7. Т1/2 (период полувыведения) артикаиновой кислоты в большинстве матриксов глаза варьировался от 1,70 до 3,29 часа. Т1/2 артикаиновой кислоты в плазме составлял приблизительно 1,5 часа.
Таким образом, местное введение артикаина в глаз обеспечивало анестезирующее действие в течение 20 минут после введения дозы без каких-либо заметных проблем с переносимостью. Артикаин и артикаиновая кислота были обнаружены во всех исследованных матриксах глаза, при этом наибольшее воздействие было отмечено в иридо-цилиарной зоне, бульбарной и палпебральной частях конъюктивы и роговице. Учитывая наличие активности эстеразы в тканях глаза, ожидается быстрый метаболизм артикаина до артикаиновой кислоты. Системное воздействие является минимальным, на что указывает AUC плазмы.
Целями данного исследования было определение переносимости плацебо и офтальмологических растворов артикаина HCl в концентрациях 4, 8 и 12% (мас./об.) после местного применения глазных капель, а также определение офтальмологической фармакокинетики и биораспределения артикаина и артикаиновой кислоты после местного применения глазных капель, содержащих 8% офтальмологический раствор артикаина-HCl. Кролик является стандартным видом, не относящимся к грызунам, используемым в доклинических фармакокинетических исследованиях, включая офтальмологическую фармакокинетику, новых химических соединений и различных испытываемых образцов препарата. Количество животных соответствует количеству, необходимому для надлежащего выполнения такого исследования переносимости и биораспределения в глазу, с учетом изменчивости среди животных, и позволяющему проводить описательный статистический анализ. Был выбран местный способ введения, поскольку это является предполагаемым способом введения человеку. Уровни дозировки офтальмологического препарата, выбранные заказчиком исследования, были разработаны с учетом достижения терапевтических концентраций исследуемого препарата в ткани глаза. Разовая доза исследуемого препарата является обычной для определения фармакокинетики.
Исследование с использованием разрешенной к медицинскому применению водного препарата артикаина проводили на людях, полученные благоприятные первоначальные результаты подтверждают результаты исследования на кроликах.
Пример 2
Готовили офтальмологическую анестезирующую композицию для местного применения, содержащую артикаин-HCl в концентрации 8,0% мас./об., как показано в Таблице 1.
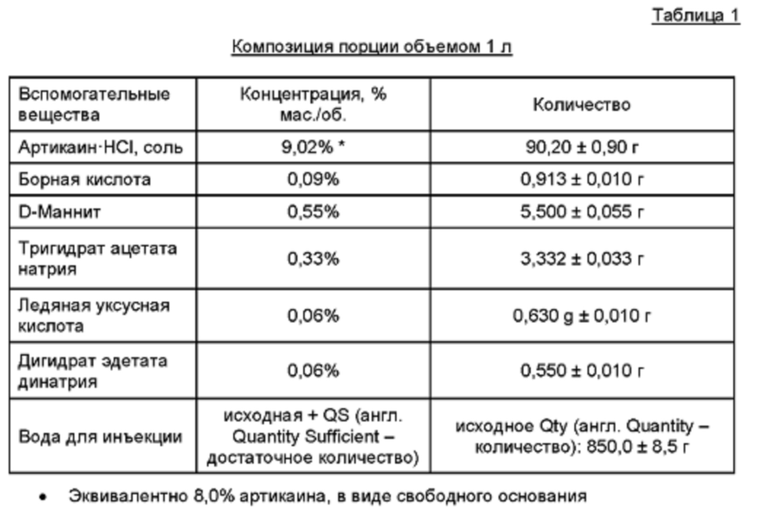
Размер серии (л) - 40
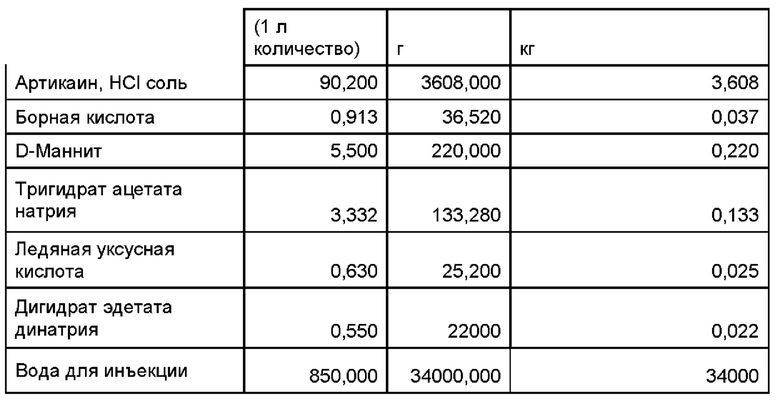
Композицию готовили добавлением борной кислоты в смеситель, содержащий некоторый объем воды, до достижения растворения. Затем добавляли маннит, размешивали до растворения и перемешивали с образованием буферного комплекса борат/маннит. После этого добавляли тригидрат ацетата натрия и перемешивали до растворения, после чего добавляли ледяную уксусную кислоту. Добавляли дигидрат EDTA для получения величины рН приблизительно от рН 4,5 до рН 5,2. Добавляли артикаин HCl и перемешивали до растворения. Полученная композиция имела величину рН от рН 4,7 до рН 4,9 и осмоляльность от 580 до 630 мосмоль/кг.
Пример 3
Готовили офтальмологические композиции для местного применения, имеющие составы, представленные в Таблице 2 ниже. Систейн и «Систейн + 8% артикаин⋅HCl» включены здесь исключительно потому, что их использовали для сравнения вязкости, в других отношениях они не являются частью исследования препараты.
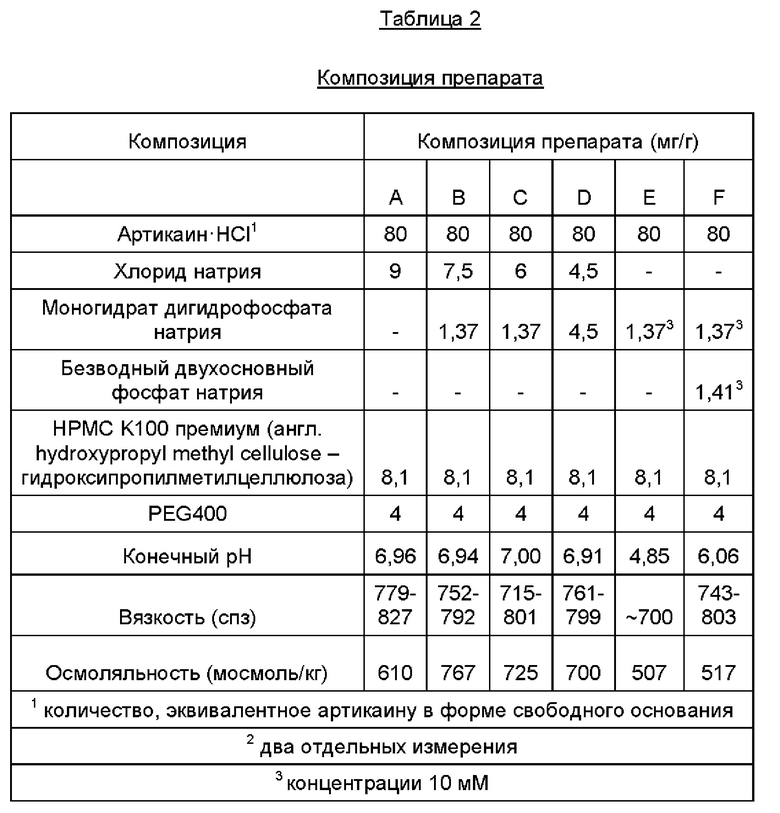
Препараты С и F оценивали с точки зрения стабильности препаратов в течение 8 недель в контейнерах, хранящихся при температурах 5°С, 25°С и 45°С.
Результаты хранения при температурах 5°С, 25°С и 45°С показали приемлемые уровни примесей, стабильные величину рН, вязкость и осмоляльность. На основании уровней разложения было показано, что препарат F является приемлемым. PEG400, по-видимому, обладает высокой реактивностью в отношении артикаина. Был выявлен буфер с наиболее низким возможным значением рН, переносимый пациентом. Буфер борная кислота/маннит обеспечивал необходимую стабильность.
Согласно одному из вариантов осуществления, композиция включала в себя 35 мМ ацетата, рН 4,8 с помощью 15 мМ комплекса борат-маннит и 0,055% EDTA (дигидрата динатриевой соли). Ацетат может быть получен из уксусной кислоты, ацетата натрия или их смесей. Данный препарат показал стабильное значение рН, а также продемонстрировал низкую скорость гидролиза, соответствующую образованию - 0,04% артикаиновой кислоты в неделю, в течение 4-недельного периода при температуре 40°С (всего - 1,53% в течение 8 недель) и гидролиз со скоростью 0,061% в неделю при температуре 25°С (всего - 0,49% в течение 8 недель). Это более чем в 4 раза медленнее, чем для известного препарата.
Некоторые аспекты способа были определены в ходе экспериментов в объеме 100 г, а затем увеличены до 500 г для подтверждения.
Комплекс борат-маннит, являющийся значительно более кислым, чем одна борная кислота (рКа 9,14), легко образуется при объединении этих двух вспомогательных вещества в отсутствие других вспомогательных веществ или буферов, приводя к величине рН около 4,2. Что касается порядка добавления, эти два вспомогательных вещества добавляют первыми, после чего смесь перемешивают, чтобы комплекс полностью сформировался.
Подходящее молярное соотношение ацетата натрия и уксусной кислоты составляет 70:30 (24,5 мМ к 10,5 мМ) во избежание необходимости регулирования величины рН после растворения артикаина HCl. При использовании такого соотношения конечное значение рН после добавления 90,2 мг/мл артикаина-HCl (что соответствует 80 мг/мл артикаина в форме свободного основания) воспроизводимо составляло около рН 4,80±0,05.
Способ легко масштабировался до 500 мл с конечным значением рН 4,80 и конечной осмоляльностью 622 мосмоль/кг. Позже его также масштабировали до 1 л, при этом конечный препарат после фильтрации имел величину рН 4,85 и осмоляльность 597 мосмоль/кг.
Затем лекарственные продукты, полученные в ходе экспериментов по разработке способа, использовали при изучении фильтрации, чтобы выяснить, является ли PVDF (англ. polyvinildenftoride - поливинилиденфторид) подходящим фильтрующим материалом для данного препарата, и определить подходящий размер фильтра.
Какие-либо признаки связывания API (англ. Active Pharmaceutical Ingredient -активный фармацевтический ингредиент) с фильтрующим материалом PVDF отсутствовали, поскольку концентрация лекарственного средства до и после фильтрации была постоянной, без потери концентрации в начальных аликвотах. Следовательно, учитывать объем отбрасываемого не требуется.
Исследование Vmax выявило незначительное снижение скорости потока с течением времени, указывая на то, что для данного состава засорение фильтра не является проблемой и для фильтрации порции лекарственного продукта объемом 1 л может использоваться относительно небольшая площадь фильтрации. Следовательно, размер фильтра может быть выбран, руководствуясь главным образом требуемой скоростью потока, которая может быть скорректирована использованием более высокого давления.
Хотя настоящее раскрытие было показано и описано со ссылкой на некоторые примеры вариантов его осуществления, специалистам в данной области техники будет понятно, что в него могут быть внесены различные изменения в форме и деталях без отступления от сущности и объема настоящего раскрытия.
Публикации, цитируемые в настоящем документе, полностью включены в него посредством ссылки. Каждый из признаков, описанных в данном документе, и каждая комбинация двух или более таких признаков включены в объем настоящего раскрытия при условии, что признаки, включенные в такую комбинацию, не являются взаимоисключающими.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВОДНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ КОМПЛЕКСЫ БОРАТПОЛИОЛ | 2010 |
|
RU2563125C2 |
| ВОДНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ БОРАТ-ПОЛИОЛЬНЫЕ КОМПЛЕКСЫ | 2009 |
|
RU2477631C2 |
| САМОКОНСЕРВИРУЮЩИЕСЯ ВОДНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2007 |
|
RU2436568C2 |
| КОНСЕРВИРУЮЩАЯ КОМПОЗИЦИЯ ДЛЯ ОФТАЛЬМОЛОГИЧЕСКОГО ПРИМЕНЕНИЯ | 2006 |
|
RU2413534C2 |
| Фармацевтическая композиция на основе трамадола для офтальмологического применения | 2016 |
|
RU2744570C2 |
| ОФТАЛЬМОЛОГИЧЕСКАЯ КОМПОЗИЦИЯ С ВЫСОКОЙ КОНЦЕНТРАЦИЕЙ ОЛОПАТАДИНА | 2012 |
|
RU2613715C2 |
| ПРИМЕНЕНИЕ В ТЕРАПИИ СТЕРИЛЬНОГО ВОДНОГО ОФТАЛЬМОЛОГИЧЕСКОГО РАСТВОРА | 2016 |
|
RU2741912C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ТАФЛУПРОСТА | 2021 |
|
RU2761625C2 |
| СУСПЕНЗИИ НАНОЧАСТИЦ, СОДЕРЖАЩИЕ КАРБОКСИВИНИЛОВЫЙ ПОЛИМЕР | 2010 |
|
RU2571078C2 |
| ВОДНЫЙ ОФТАЛЬМОЛОГИЧЕСКИЙ РАСТВОР И СПОСОБ ЛЕЧЕНИЯ СИНДРОМА СУХИХ ГЛАЗ | 2015 |
|
RU2688935C2 |
Группа изобретений относится к области медицины и фармацевтики, а именно к водным офтальмологическим анестезирующим композициям и способу их получения. Водная офтальмологическая анестезирующая композиция для местного применения содержит артикаин в количестве от 4,0 до 12,0% мас./об. в расчете на объем композиции и буфер в количестве, обеспечивающем рН от 3,5 до 7,0 и осмоляльность от 275 до 1171 мосмоль/кг для облегчения местного применения для офтальмологической анестезии, где указанный буфер не вступает в реакцию с артикаином и стабилизирует его и ингибирует разложение указанного артикаина при хранении. Способ получения указанной композиции включает стадии, на которых смешивают кислоту или ее соль с сахароспиртом в растворе с образованием комплекса, доводят рН до величины от 3,5 до 7,0 и добавляют в полученный раствор артикаин в количестве, достаточном для получения композиции, содержащей от 4,0 до 12,0% мас./об. в расчете на объем композиции. Водная офтальмологическая композиция содержит 80 мг/г артикаина HCl, 1,373 мг/г моногидрата дигидрофосфата натрия, 1,413 мг/г безводного двухосновного фосфата натрия, 8,1 мг/г гидроксипропилметилцеллюлозы, 4 мг/г PEG400 и при этом указанная композиция имеет рН от 6,0 до 7,0, вязкость от 0,743 до 0,803 Па⋅с (от 743 до 803 сПз) и осмоляльность 517 мосмоль/кг, и где указанный буфер не вступает в реакцию с артикаином и стабилизирует указанный артикаин с ингибированием разложения указанного артикаина при хранении. Водная офтальмологическая анестезирующая композиция содержит артикаин в количестве по меньшей мере 7,0% мас./об. в расчете на объем композиции и буфер в количестве, обеспечивающем рН от 4,0 до 5,5 и стабилизацию артикаина, при этом указанный буфер представляет собой комплекс, полученный из борной кислоты или соли борной кислоты и сахароспирта, в количестве, которое сохраняет указанный артикаин в растворе или суспензии и ингибирует разложение указанного артикаина при хранении. Вышеуказанная группа изобретений позволяет обеспечить стабильность артикаина при длительном хранении полученных композиций. 4 н. и 26 з.п. ф-лы, 2 табл., 2 пр.
1. Водная офтальмологическая анестезирующая композиция для местного применения, содержащая:
артикаин в количестве от 4,0 до 12,0% мас./об. в расчете на объем композиции; и буфер в количестве, обеспечивающем рН от 3,5 до 7,0, и осмоляльность от 275 до 1171 мосмоль/кг для облегчения местного применения для офтальмологической анестезии, где указанный буфер не вступает в реакцию с артикаином и стабилизирует его и ингибирует разложение указанного артикаина при хранении.
2. Композиция по п. 1, где указанная композиция имеет рН от 4,5 до 5,5, и при этом указанный буфер содержит комплекс, полученный из цитрата, ацетата или их смеси и сахароспирта, выбранного из группы, состоящей из маннита, сорбита и их смесей.
3. Композиция по п. 1, где указанная композиция содержит от 7,5 до 8,5% мас./об. артикаина, при этом указанная композиция имеет рН от 4,5 до 5,0.
4. Композиция по п. 1, где указанная композиция содержит по меньшей мере 7,0% мас./об. артикаина и имеет рН от 4,5 до 5,0.
5. Композиция по п. 1, где буфер содержит комплекс борат/маннит, полученный из бората и D-маннита, и где указанный комплекс борат/маннит содержится в количестве, которое обеспечивает концентрацию артикаина для анестезии поверхности глаза и внутренней стороны глаза путем местного применения, и указанная композиция имеет осмоляльность от 500 до 700 мосмоль/кг.
6. Композиция по п. 5, где указанный комплекс борат/маннит включен в количестве от 0,5 до 0,75% мас./об. в расчете на объем композиции.
7. Композиция по п. 5, где указанный комплекс борат/маннит включен в количестве от 6,5 до 7,5 массовых частей в расчете на 100 массовых частей артикаина в композиции.
8. Композиция по п. 5, где указанный комплекс борат/маннит получен при массовом соотношении борат/маннит от 1:3 до 1:7, при этом указанный комплекс борат/маннит включен в количестве, которое сохраняет указанный артикаин в растворе или суспензии в указанной анестезирующей композиции для местного применения, ингибирует разложение указанного артикаина при длительном хранении и обеспечивает осмоляльность от 500 до 700 мосмоль/кг и рН от 3,5 до 7,0 и тоничность от 0,5 до 5,0%.
9. Композиция по п. 5, где указанная композиция дополнительно включает ацетат натрия, уксусную кислоту и эдетат динатрия.
10. Композиция по п. 1, где указанная композиция содержит по меньшей мере 7,0% мас./об. артикаина, при этом указанный буфер содержит комплекс борной кислоты и D-маннита в количестве, обеспечивающем рН от 4,5 до 5,0, причем указанная композиция дополнительно содержит ацетат натрия, уксусную кислоту и эдетат динатрия, где указанная композиция имеет осмоляльность для местного применения для офтальмологической анестезии и указанный буфер включен в количестве, которое обеспечивает стабилизацию и ингибирование разложения артикаина при хранении.
11. Композиция по п. 5, где указанный артикаин присутствует в количестве по меньшей мере 7,0% мас./об., а указанный комплекс борной кислоты и D-маннита получен из от 0,08 до 0,10% мас./об. борной кислоты и от 0,50 до 0,6% мас./об. D-маннита в расчете на общий объем композиции.
12. Композиция по п. 1, где указанная композиция содержит по меньшей мере 8,0% мас./об. артикаина, буферный комплекс, полученный из от 0,08 до 0,10% мас./об. борной кислоты и от 0,5 до 0,60% мас./об. D-маннита, от 0,3 до 0,36% мас./об. ацетата натрия, от 0,05 до 0,07% мас./об. эдетата динатрия и остальное - вода, и при этом указанная композиция имеет осмоляльность от 280 до 320 мосмоль/кг, причем количества даны в расчете на общий объем композиции.
13. Композиция по п. 1, где указанная композиция содержит 4% мас./об. артикаина, а указанный буфер содержит NaOH и HCl, при этом указанная композиция имеет рН 5,5, рКа 7,8, вязкость от 0,02 до 0,025 Па⋅с (от 20 до 25 сПз), осмоляльность от 275 до 1171 мосмоль/кг и тоничность от 0,5 до 5,0%.
14. Водная офтальмологическая композиция, содержащая 80 мг/г артикаина HCI, 1,373 мг/г моногидрата дигидрофосфата натрия, 1,413 мг/г безводного двухосновного фосфата натрия, 8,1 мг/г гидроксипропилметилцеллюлозы, 4 мг/г PEG400 и при этом указанная композиция имеет рН от 6,0 до 7,0, вязкость от 0,743 до 0,803 Па⋅с (от 743 до 803 сПз) и осмоляльность 517 мосмоль/кг, и где указанный буфер не вступает в реакцию с и стабилизирует указанный артикаин с ингибированием разложения указанного артикаина при хранении.
15. Водная офтальмологическая анестезирующая композиция, содержащая: артикаин в количестве по меньшей мере 7,0% мас./об. в расчете на объем композиции; и буфер в количестве, обеспечивающем рН от 4,0 до 5,5 и стабилизацию артикаина, при этом указанный буфер представляет собой комплекс, полученный из борной кислоты или соли борной кислоты и сахароспирта, в количестве, которое сохраняет указанный артикаин в растворе или суспензии и ингибирует разложение указанного артикаина при хранении.
16. Водная офтальмологическая анестезирующая композиция по п. 15, где указанный буфер представляет собой комплекс борат/маннит в количестве от 6,5 до 7,5 массовых частей в расчете на 100 массовых частей артикаина в композиции.
17. Водная офтальмологическая анестезирующая композиция по п. 16, где указанный комплекс борат/маннит получен при массовом соотношении борат/маннит от 1:3 до 1:7.
18. Водная офтальмологическая анестезирующая композиция по п. 17, дополнительно содержащая диацетат натрия, уксусную кислоту и эдетат динатрия.
19. Композиция по п. 1 для местного применения на поверхность глаза пациента в количестве, эффективном для анестезии поверхности глаза и внутренней стороны у пациента.
20. Композиция по п. 19, где указанная композиция содержит артикаин в количестве по меньшей мере 5,0%, буферный комплекс, полученный из от 0,08 до 0,10% мас./об. борной кислоты и от 0,50 до 0,6% мас./об. D-маннита, в расчете на общий объем композиции.
21. Композиция по п. 19, где указанная композиция содержит по меньшей мере 7,5% мас./об. артикаина; буфер, включающий комплекс, полученный из борной кислоты и D-маннита, в количестве, не вступающем в реакцию с артикаином; ацетат натрия; уксусную кислоту; эдетат динатрия и остальное - вода, и где указанная композиция имеет рН от 4,5 до 5,5.
22. Композиция по п. 19, где указанная композиция содержит по меньшей мере 7% мас./об. артикаина.
23. Композиция по п. 22, где композиция имеет рН от 4,5 до 5,0.
24. Композиция по п. 19, где указанная композиция содержит 4% мас./об. артикаина, имеет рН 5,5, рКа 7,8, вязкость от 0,02 до 0,025 Па⋅с (от 20 до 25 сПз), осмоляльность от 275 до 1171 мосмоль/кг, тоничность от 0,5 до 5,0%, содержит буфер NaOH и буфер HCl.
25. Композиция по п. 19, где указанная композиция содержит 80 мг/г артикаина HCl, 1,373 мг/г моногидрата дигидрофосфата натрия, 1,413 мг/г безводного двухосновного фосфата натрия, 8,1 мг/г гидроксипропилметилцеллюлозы, 4 мг/г PEG400, и где указанная композиция имеет рН от 6,0 до 7,0, вязкость от 0,743 до 0,803 Па⋅с (от 743 до 803 сПз) и осмоляльность 517 мосмоль/кг.
26. Способ получения композиции по п. 1, включающий стадии, на которых: смешивают кислоту или ее соль с сахароспиртом в растворе с образованием комплекса;
доводят рН до величины от 3,5 до 7,0; и
добавляют в полученный раствор артикаин в количестве, достаточном для получения композиции, содержащей от 4,0 до 12,0% мас./об. в расчете на объем композиции.
27. Способ по п. 26, где указанную кислоту выбирают из группы, состоящей из уксусной кислоты, лимонной кислоты и их смесей, а сахароспирт выбирают из группы, состоящей из D-маннита, сорбита и их смесей.
28. Способ по п. 26, где указанная кислота или ее соль представляет собой борнокислую соль (борат), сахароспирт представляет собой D-маннит, а комплекс представляет собой комплекс борат/маннит, и где композиция содержит по меньшей мере 7,0% артикаина и имеет величину рН от 6,0 до 7,0.
29. Способ по п. 28, где комплекс борат/маннит получают при массовом соотношении борат/маннит от 1:3 до 1:7.
30. Водная анестезирующая композиция для местного применения по п. 1, где указанный буфер обеспечивает рН от 4,5 до 7,0, и где указанная композиция имеет осмоляльность от 280 до 320 мосмоль/кг.
| WO 2018220288 A1, 06.12.2018 | |||
| WO 2015103450 A1, 09.07.2015 | |||
| WO 2017066787 A1, 20.04.2017 | |||
| US 2009318882 A1, 24.12.2009 | |||
| US 6503497 B2, 07.01.2003 | |||
| US 2017348199 A1, 07.12.2017 | |||
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНЕСТЕЗИРУЮЩЕЙ АКТИВНОСТЬЮ | 2004 |
|
RU2261092C1 |
Авторы
Даты
2024-02-05—Публикация
2020-03-16—Подача