Предлагаемое изобретение относится к органической химии, а точнее к способам получения новых гетероциклических соединений фуранового ряда. Фурилсодержащие карбоновые кислоты и их производные представляют интерес как лиганды для получения металлокомплексов, обладающих каталитической активностью, значимыми спектрально-люминесцентными характеристиками, аналитические реагенты для определения металлов, экстрагенты, полупродукты для синтеза биологически активных соединений.
Известен способ получения структурно близкой фурилсодержащей кислоты 5, осуществляющийся взаимодействием фурана 1 с метилтрифторпируватом 2 в среде Хладона-113 при комнатной температуре, последующее метилирование образовавшегося гидроксиэфира 3 диметилсульфатом и щелочной гидролиз метоксипроизводного 4:
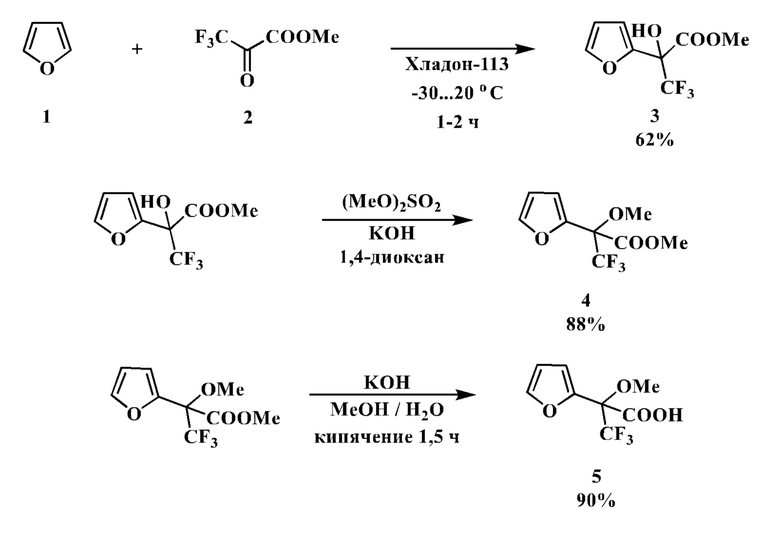
Общий выход кислоты 5 в расчете на исходный фуран составляет 49%.
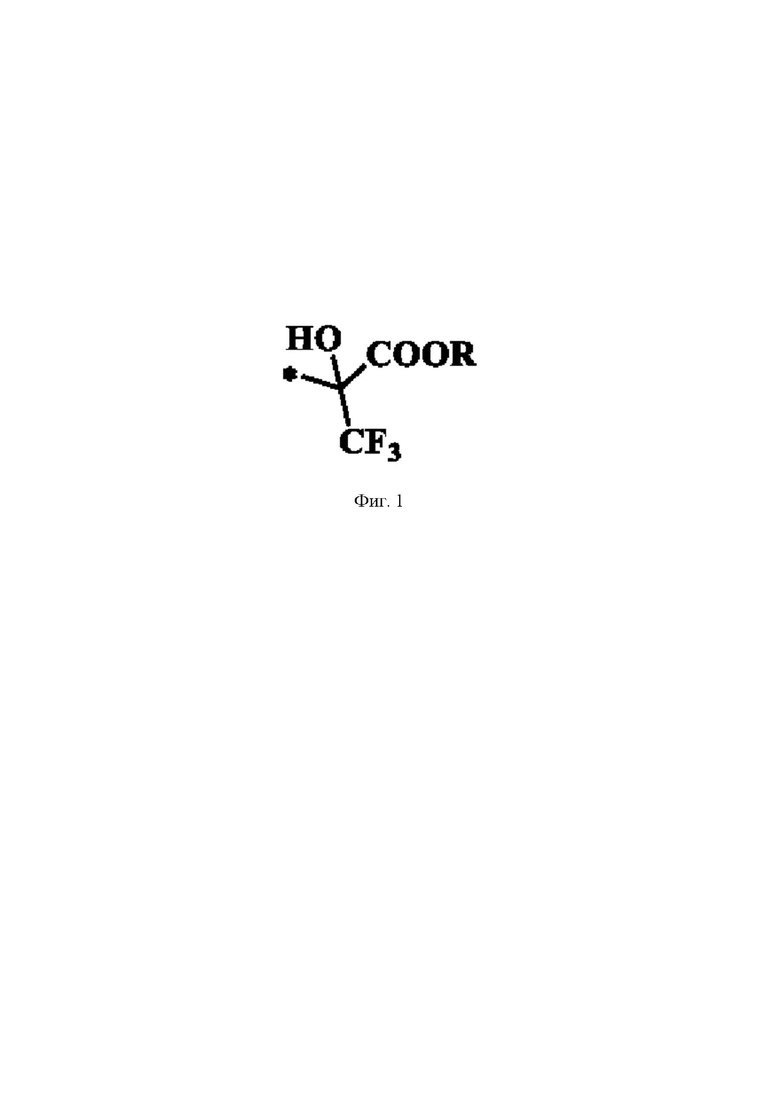
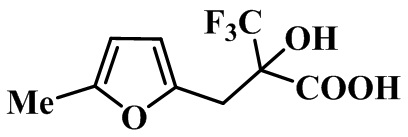
В представленном примере реакция протекает по фурановому кольцу и в молекуле продукта 3 четвертичный атом углерода, имеющий связи с трифторметильной, гидрокси- и карбалкоксильной группами (фиг.1), непосредственно связан с кольцом.
(Т.П. Васильева, Д.В. Воробьева. Синтез фуранил- и-триазолилсодержащих α-CF3-α-гидроксикислот и их производных. Известия Академии наук. Серия химическая, 2020, №2, с. 300-304).
Аналогичные способы получения полупродукта 3 и родственных соединений различаются используемыми условиями взаимодействия: реакцию осуществляли в среде четыреххлористого углерода при комнатной температуре, получая 3 С выходом 85% (АС. Голубев, А.Ф. Коломиец, А.В. Фокин. Метиловый эфир трифторпировиноградной кислоты в реакциях с пятичленными электроноизбыточными гетероциклами. Известия Академии наук СССР. Серия химическая, 1989, №10, с. 2369-2371), в присутствии трифторметансульфоновой кислоты (G.K. Surya Prakash, P. Yan, В. Torok, G.A. Olah. Superacid catalyzed hydroxyalkylation of aaromatics with ethyl trifluoropyruvate: a new synthetic route to Mosher's acid analogs. Synlett 2003, №4, p. 527-531.), энантиоселективные варианты С дикатионным палладиевым комплексом (Aikawa, К., Asai, Y., Hioki, Y., Mikami, К. Catalytic and highly enantioselective Friedel-Crafts type reactions of heteroaromatic compounds with trifluoropyruvate and glyoxylate by a dicationic palladium complex. Tetrahedron: Asymmetry 2014, 25(15), 1104 1115. doi: 10.1016/j.tetasy.2014.06.013) И бисоксазолиновым комплексом трифлата меди (Zhuang, W., Gather good, К, Hazell, R. G., Jorgensen, K. A.. Catalytic, Highly Enantioselective Friedel-Crafts Reactions of Aromatic and Heteroaromatic Compounds to Trifluoropyruvate. A Simple Approach for the Formation of Optically Active Aromatic and Heteroaromatic Hydroxy Trifluoromethyl Esters. The Journal of Organic Chemistry 2001, 66(3), 1009 1013. doi: 10.1021/jo001176m). Во всех случаях реакция протекает по фурановому кольцу.
Учитывая важность структурного фрагмента (фиг.1) для разработки физиологически активных соединений, в частности ингибиторов амилоидного фибриллогенеза (Torok, М., Abid, М., Mhadgut, S. С, & Torok, В. Organofluorine Inhibitors of Amyloid Fibrillogenesis. Biochemistry 2006, 45(16), 5377-5383. doi:10.l021/bi0601104), а также его поли функциональность, открывающую путь к различным классам потенциально практически значимых соединений, разработка способов получения соединений, включающий такой фрагмент является актуальной.
Производные фурана, в которых фрагмент с четвертичным атомом углерода, имеющим связи с трифторметильной, гидрокси- и карбалкоксильной / карбоксильной группами, отделен от гетероциклического ядра метиленовой группой, не описаны.
Задачей предлагаемого изобретения является создание способа получения фурилсодержащей карбоновой кислоты, которая содержит карбоксильную группу в составе фрагмента с четвертичным атомом углерода, дополнительно связанного с трифторметильной и гидроксильными группами и отделенного от гетероциклического кольца метиленовым фрагментом, представляющей собой перспективный полупродукт для получения металлокомплексов, биологически активных соединений и др.
Техническим результатом настоящего изобретения является расширение ассортимента способов получения фурилсодержащих карбоновых кислот, используемых в качестве многоцелевых органических соединений, например лигандов для синтеза люминесцирующих комплексных соединений.
Технический результат достигается проведением реакции 2,5-диметилфурана 6 с этилтрифторпируватом 7 в течение 2 часов при 25°С, последующим щелочным гидролизом в водно-этанольной среде образовавшегося эфира 8 и подкислением раствором соляной кислоты:
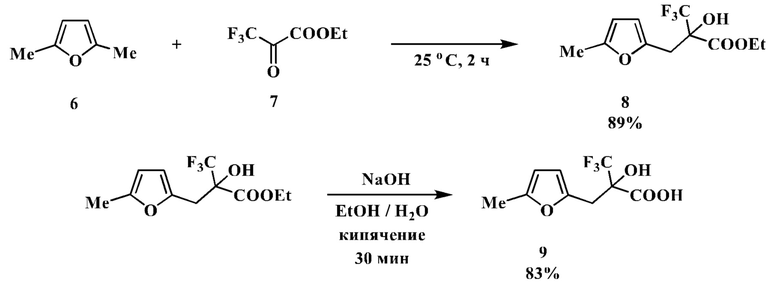
Реакция между 2,5-диметилфураном и этилтрифторпируватом гладко протекает при комнатной температуре без использования растворителя. Мониторинг реакционной массы с использованием хромато-масс-спектрометрии показывает, что максимальная конверсия достигается через 2 часа, препаративный выход гидроксиэфира 8 составил 89%. Гидролиз в целевую кислоту 9 проходит за 30 мин кипячения в водно-этанольном растворе гидроксида натрия. Выход 9 на две стадии в расчете на исходный 2,5-диметилфуран 74%.
Предложенный двухстадийный способ получения 2-гидрокси-2-((5-метилфуран-2-ил)метил)-3,3,3-трифторпропановой кислоты 9 обеспечивает высокий выход целевого соединения при использовании коммерчески доступных реагентов, не требует применения растворителя, катализатора и сложных приемов выделения и очистки. Реализуемый способ позволяет получать перспективный продукт на основе важного возобновляемого сырья, получаемого переработкой растительной биомассы - 2,5-диметилфурана, рассматриваемого в настоящее время как альтернатива ископаемым углеводородам.
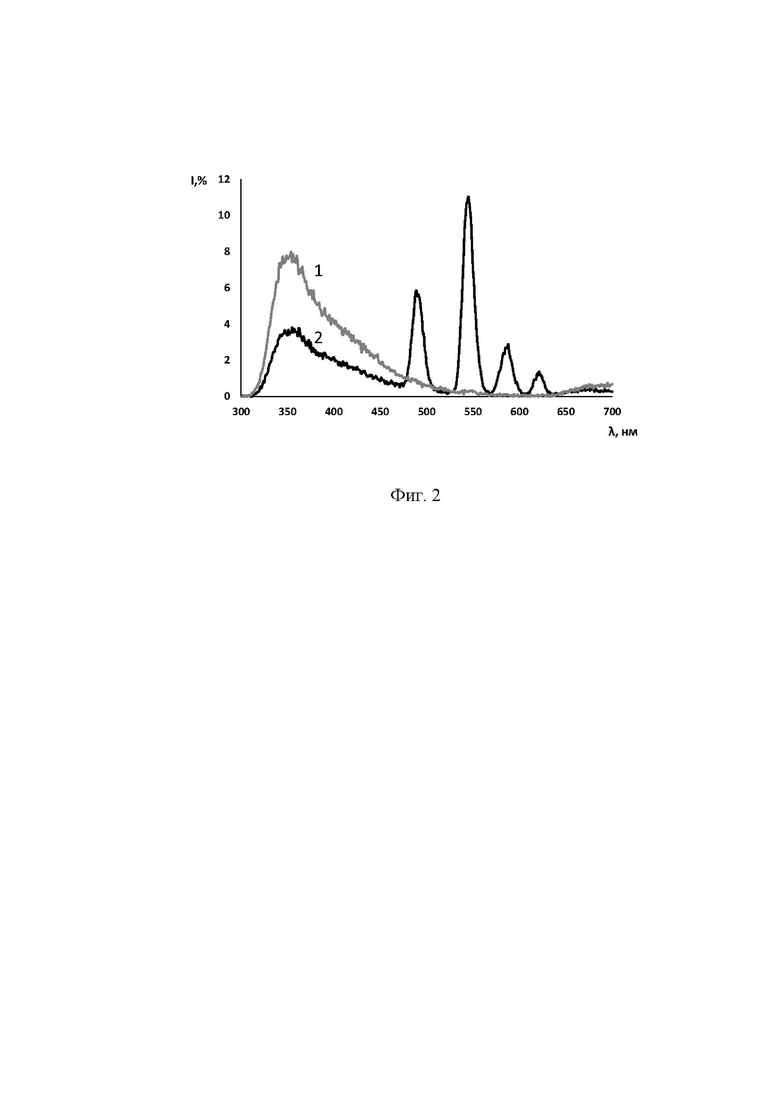
Применимость полученной 2-гидрокси-2-((5-метилфуран-2-ил)метил)-3,3,3-трифторпропановой кислоты 9 продемонстрирована на примере получения люминесцирующего комплекса с тербием (III), образующегося в водной среде (рН 5.5) при мольном соотношении п(кислоты): n(Tb3+) 3:1. На фиг.2 представлены спектры люминесценции водных растворов рН 5.5 (С =9.373⋅10-5 М) при возбуждении на длине волны 220 нм, где 1 - раствор лиганда 9; 2 - комплекс лиганда 9 - Tb (3:1), демонстрирующий люминесценцию при λ = 495, 545, 585, 623 нм.
Пример получения 2-гидрокси-2-((5-метилфуран-2-ил)метил)-3,3,3-трифторпропановой кислоты
Стадия 1. В реакционную виалу помещают 0,500 мл (0,00469 моль) 2,5-диметилфурана, осторожно приливают 0,623 мл (0,00469 моль) этилтрифторпирувата. Реакционную массу выдерживают 2 часа при комнатной температуре. Затем количественно переносят в колонку с силикагелем (высота столба 150 мм, диаметр 20 мм) и элюируют (петролейный эфир - хлороформ 10: 3). Выход 1,11 г (89%). Бесцветное подвижное масло.
ПК (KBr), v/см-1: 3485 (ОН), 3109 (Csp2-H), 2987, 2943, 2926 (Csp3-H), 1743 (С=О).
1Н ЯМР (399.78 МГц, CDCl3, δ, м.д.): 1.34 т (7.7 Гц, 3Н, СН3), 2.20 с (3Н, СН3), 3.14 д (15.1 Гц, 1H, СН2), 3.37 д (14.6 Гц, 1H, СН2), 3.87 уш.с (1H, ОН), 4.29 - 4.40 м (1H, СН2), 5.85 д (2.3 Гц, 1H, СН), 6.04 д (3.2 Гц, 1H, СН).
13СЯМР (100.5 МГц, CDCl3, δ, м.д.): 13.4 (СН3), 13.9 (СН3), 31.3 (СН2), 63.8 (СН2), 76.4 (С), 106.4 (СН), 110.1 (СН), 123.2 квадр. (CF3, JC-F 286 Гц), 145.5 (С), 151.8 (С), 168.9 (С=O).
19F ЯМР (376.17 МГц, CDCl3, δ, м.д.): -78.31 s (CF3).
Масс-спектр (ЭУ, 70 eV), m/z (Iотн., %): 266 (6) М+, 248 (5), 220 (3), 193 (4), 95 (100).
Стадия 2. В колбу помещают 0,5 г (0,0019 моль) этил 2-гидрокси-2-((5-метилфуран-2-ил)метил)-3,3,3-трифторпропаноат, 10 мл этанола и вносят раствор 0,306 г (0,0077 моль) гидроксида натрия в 5 мл воды. Реакционную массу выдерживают при кипении растворителя 30 минут. После остывания до комнатной температуры реакционную массу нейтрализуют, прибавляя 2М раствор соляной кислоты. Продукт экстрагируют этилацетатом, подсушивают экстракт над сульфатом натрия, затем выпаривают досуха на ротационном испарителе и остаток возгоняют в вакууме. Выход 83%. Бесцветное кристаллическое вещество. Тпл 87-890С.
ПК (KBr), v/см-1: 3412, 3010 уш. (ОН), 3107 (Csp2-H), 2931 (Csp3-H), 1753 (С=О).
1Н ЯМР (399.78 МГц, (CD3)2SO, δ, м.д.): 2.17 с (3Н, СН3), 3.02 д (14.9 Гц, 1Н, СН2), 3.22 д (14.9 Гц, 1Н, СН2), 5.94 - 5.95 м (1Н, СН), 6.04 д (3 Гц, 1Н, СН), 6.53 уш.с (1Н, ОН).
13С ЯМР (100.5 МГц, (CD3)2SO, δ, м.д.): 13.2 (СН3), 31.5 (СН2), 76.5 квадр. (С, JC-F 27 Гц), 106.5 (СН), 109.4 (СН), 124.2 квадр. (CF3, JC-F 286 Гц), 146.4 (С), 150.6 (С), 169.0 (С=O).
Масс-спектр (ЭУ, 70 eV), m/z (Iотн., %): 238 (7) М+, 193 (1), 95 (100).
Бис Me3Si-производное: Масс-спектр (ЭУ, 70 eV), m/z (Ioтн., %): 382 (0.5) М+, 367 (3), 339 (1), 319 (1), 292 (10), 200 (1), 147 (15), 131 (3), 95 (100), 73 (25).
Масс-спектр высокого разрешения (ESI): найдено 237,0383 [М-Н]-, рассчитано для C9H9F3O4 237,0380.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФТОРСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ ТЕВИНОЛА И ОРВИНОЛА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2012 |
|
RU2506265C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФУРИЛГЕТАРИЛМЕТАНОВ, СОДЕРЖАЩИХ ТИЕНО[2,3-B]ПИРИДИНОВЫЙ ФРАГМЕНТ | 2007 |
|
RU2346947C1 |
| 7α-(1-ГИДРОКСИ-2,2,2-ТРИФТОРЭТИЛ)-17-МЕТИЛ-3,6-ДИМЕТОКСИ-4,5α-ЭПОКСИ-6α,14αЭТЕНОИЗОМОРФИНАН И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2503678C1 |
| Способ получения 1,3-диоксациклоалкилсодержащих азоокисей | 2021 |
|
RU2767880C1 |
| 5-АМИНО-3-(2-АМИНОПРОПИЛ)-[1,2,4]ТИАДИАЗОЛЫ | 2011 |
|
RU2449997C1 |
| ЛИГАНДЫ, ТРОПНЫЕ К ПРОСТАТИЧЕСКОМУ СПЕЦИФИЧЕСКОМУ МЕМБРАННОМУ АНТИГЕНУ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ДВОЙНЫХ КОНЪЮГАТОВ С ТЕРАПЕВТИЧЕСКИМИ АГЕНТАМИ НА ИХ ОСНОВЕ ДЛЯ КОМБИНИРОВАННОЙ ТЕРАПИИ ПСМА ЭКСПРЕССИРУЮЩИХ ОПУХОЛЕЙ | 2023 |
|
RU2841078C1 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 1-ОКСА-2,8-ДИАЗАСПИРО[4.5]ДЕЦ-2-ЕНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ АНАЛЬГЕТИЧЕСКИМ ДЕЙСТВИЕМ | 2002 |
|
RU2296128C2 |
| ПРОИЗВОДНЫЕ 1-(4-ИЗОКСАЗОЛ-5-ИЛ)-1Н-ПИРАЗОЛ-1-ИЛ)-2-МЕТИЛПРОПАН-2-ОЛА И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИРОРОВ ИЛ-17 И ИФН-ГАММА ДЛЯ ЛЕЧЕНИЯ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ И ХРОНИЧЕСКОГО ВОСПАЛЕНИЯ | 2018 |
|
RU2785342C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(1Н-БЕНЗОХРОМЕН-2-ИЛ)-2,2,2-ТРИФТОРЭТАНОНОВ | 2016 |
|
RU2662439C2 |
| Способ получения (1-адамантил)фуранов | 2017 |
|
RU2661482C1 |
Предлагаемое изобретение относится к органической химии, а именно к способу получения 2-гидрокси-2-((5-метилфуран-2-ил)метил)-3,3,3-трифторпропановой кислоты формулы
I
Фурилсодержащие карбоновые кислоты и их производные представляют интерес как лиганды для получения металлокомплексов, обладающих каталитической активностью, значимыми спектрально-люминесцентными характеристиками, аналитические реагенты для определения металлов, экстрагенты, полупродукты для синтеза биологически активных соединений. Предлагаемый способ включает взаимодействие 2,5-диметилфурана с этилтрифторпируватом в течение 2 часов. Далее образующийся продукт подвергается гидролизу в водно-этанольной среде под действием гидроксида натрия при кипячении в течение 30 минут, с последующим подкисление раствором соляной кислоты. Технический результат - расширение ассортимента способов получения фурилсодержащих карбоновых кислот. 2 ил., 1 пр.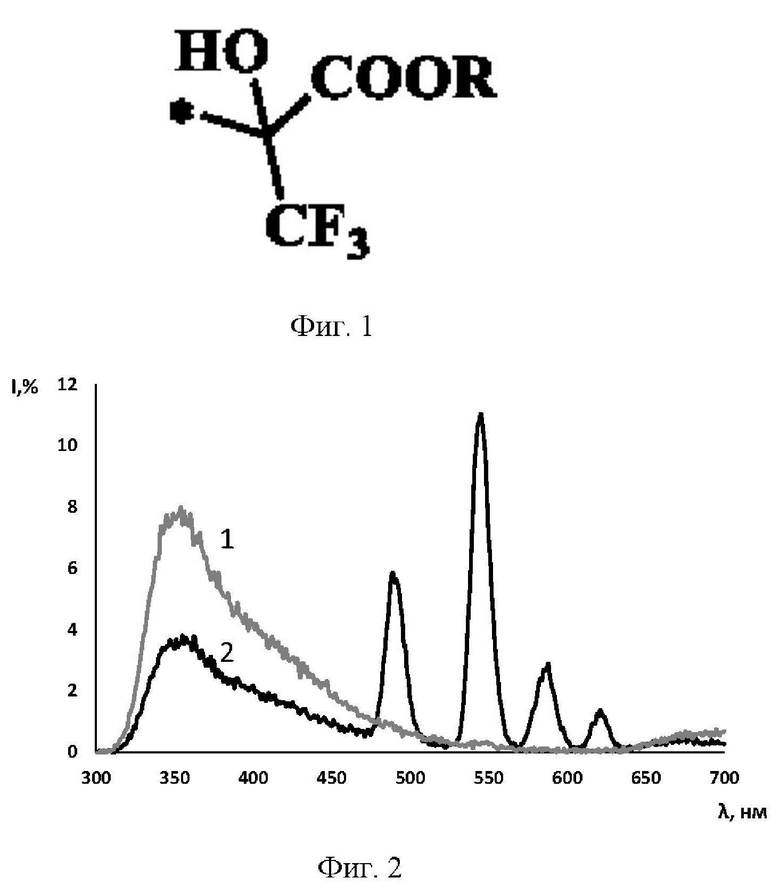
Способ получения 2-гидрокси-2-((5-метилфуран-2-ил)метил)-3,3,3-трифторпропановой кислоты формулы
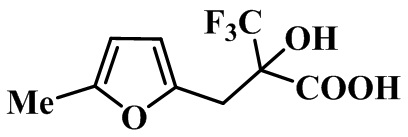
I
включающий взаимодействие 2,5-диметилфурана с этилтрифторпируватом в течение 2 часов, гидролиз образующегося продукта, протекающий в водно-этанольной среде под действием гидроксида натрия при кипячении в течение 30 минут и последующее подкисление раствором соляной кислоты.
| Васильева Т.П | |||
| и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Известия Академии наук | |||
| Серия химическая, 2020, N 2, 300-304 | |||
| Kohsuke Aikawa et al | |||
| Catalytic and highly enantioselective Friedel-Crafts type reactions of heteroaromatic compounds with trifluoropyruvate and glyoxylate by a dicationic palladium | |||
Авторы
Даты
2024-02-07—Публикация
2023-11-08—Подача