Область техники
Группа изобретений относится к биотехнологии, биохимии, молекулярной биологии, микробиологи и может быть использована при создании антибактериальных препаратов для профилактики и лечения инфекций, вызванных, бактериями Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli.
Уровень техники
Востребованность новых подходов к лечению и профилактике бактериальных инфекций возрастает с распространением проблемы приобретенной устойчивости к антибиотикам среди микроорганизмов по всему миру. Особенно это актуально при борьбе с инфекциями, связанными с оказанием медицинской помощи, поскольку в их случае, наблюдается значительное давление отбора замкнутой системы госпитальных организаций и предрасположенности к передаче факторов резистентности среди патогенов. В свете распространения проблемы антибиотикоустойчивости, поиск и разработка новых классов антибиотиков с новыми мишенями и механизмами действия, не обладающими перекрестной устойчивостью к существующим классам антибиотиков, имеет первостепенное значение [1,2]. Среди них, активно изучаемым классом являются антибактериальные препараты на основе ферментов (энзибиотики), представляющие собой литические ферменты из различных источников, способные разрушать компоненты клеточных стенок бактериальных клеток и приводить к их лизису. К таким ферментам относят эндолизины бактериофагов, разрушающие бактерии за счет гидролиза пептдогликанового слоя и последующего осмотического лизиса клеток патогенов, которые активно исследуются в свете перспектив борьбы с инфекциями, связанными с оказанием медицинской помощи, склонными к распространению и приобретению множественной лекарственной устойчивости [3,4]. Так, например, показана высокая активность эндолизинов против грамотрицательных и грамположительных бактерий, независимо от их статуса устойчивости к антибиотическим препаратам [5]. Кроме того, они обладают значительной противобиопленочной активностью [6-8] и, по всей видимости, не провоцируют бактерии к быстрому развитию устойчивости, поскольку действуют на высококонсервативные участки клеточной стенки [9,10].
В литературе описаны примеры использования эндолизинов в качестве противомикробных средств. Кроме того, проводятся клинические исследования эндолизинов CF-301 и N-Rephasin® SAL200 у пациентов с бактериемией, вызванной золотистым стафилококком (ClinicalTrials.gov Identifiers: NCT03089697; NCT03163446).
Из уровня техники известны несколько примеров решений на основе эндолизинов.
Известна заявка на изобретение (RU 202128276 A, опубликовано: 20.03.2022), в котором разработаны модифицированные варианты эндолизина PlySs2 ингибирующие рост, уменьшающие популяцию или приводящие к уничтожению по меньшей мере одного вида грамположительных бактерий, а также соответствующий вектор экспрессии, антибактериальная композиция и способ предотвращения или лечения бактериальной инфекции, вызванной по меньшей мере одним видом грамположительных бактерий, в том числе, в комбинации с антибиотиками.
Известен патент на изобретение (RU 2715694 C1, опубликовано: 02.03.2020), в котором представлена фармацевтическая композиция для лечения глазных инфекций, вызванных метициллин-устойчивыми штаммами Staphylococcus aureus, включающей в качестве активного начала N-концевой СНАР-домен эндолизина бактериофага K Staphylococcus aureus. Заявляемая фармацевтическая композиция не токсична и более эффективна, чем антибиотик ванкомицин.
Известен патент на группу изобретений (RU 2735103 C2, опубликовано: 28.10.2020), относящийся к способам предотвращения образования, а также разрушения или эрадикации биопленок грамположительных бактерий. Предложены способ предотвращения, разрушения или эрадикации биопленки, включающей одну или более из бактерий Staphylococcus и Streptococcus, и способ профилактики или лечения инфекции, ассоциированной с биопленкой.
Предполагается, что данные изобретения позволяют устранять зрелые стрептококковые или стафилококковые биопленки, и предотвращать образование биопленок de novo на поверхности устройств, имплантатов, разделительных мембран.
Все вышеуказанные решения предназначены для лечения инфекций, вызванных грамположительными видами патогенов, а результаты клинических исследований неоднозначны. Так, для производного эндолизина LSVT-1701 (tonabacase), были досрочно завершены КИ 2 фазы, без оглашения результатов, по причине спонсорского решения об отзыве, не связанного с какими-либо проблемами безопасности препарата. При этом, из литературы известно, что лизины, активные в отношении грамположительных бактерий часто не обладают широким спектром действия, и способны эффективно действовать только на бактерии в пределах рода, а иногда даже вида или определенных штаммов.
В то же время, для лизинов, выделенных из бактериофагов, действующих против грамотрицательных видов бактерий, показан широкий спектр активности [11]. Однако, в случае грамотрицательных патогенов взаимодействие лизина с его субстратом пептидогликаном может быть затруднено из-за наличия внешней мембраны и часто требует дополнительных пермеабилизующих соединений в составе лекарственной формы.
Эту проблему позволяют решать модификации нативных полипептидов эндолизинов путем введения в последовательность рекомбинантного белка пермеабилизующих пептидов.
Для грамотрицательных бактерий известен патент на изобретение (RU 2725809 C2, опубликовано 06.07.2020), в котором полипептид F307 и его производные, в том числе, конъюгированные с антимикробными пептидами используют в качестве противомикробной композиция для лечения бактериальной инфекции, вызванной A. baumannii и других видов грамотрицательных бактерий (A. baumannii, E. coli, P. aeruginosa, S. aureus, B. anthracis и K. pneumoniae). Раскрыты способы лечения субъекта, дезинфекции предмета, ингибирования образования или разрушения бактериальной биопленки. Однако, в испытаниях in vitro для бактерий видов A. baumannii и B. anthracis снижение в высевах после применения данных полипептидов составляло не более 4 порядков, а в случае E. coli, P. aeruginosa и S. aureus полипептиды были практически неэффективны (снижение КОЕ менее 1,5 порядков). Испытания in vivo были проведены только для инфекционных моделей с использованием A. baumannii, поэтому, определить реальную эффективность в отношении широкого спектра грамотрицательных патогенов невозможно.
Известен патент на изобретение (RU 2703043 C1, опубликовано 15.10.2019), относящееся к модификации нативного эндолизина антисинегнойного бактериофага КРР10 модифицированным фрагментом миелоидного антимикробного пептида овцы SMAP-29 [K2,7,13]-SMAP-29(1-17), с целью использования в качестве антибактериальной композиции, проявляющей активность в отношении грамотрицательных бактерий Pseudomonas aeruginosa. Его активность в отношении широкого спектра бактерий так же не установлена.
Известна заявка на изобретение (RU 2020118691 A, дата публикации 13.01.2022), где описано применение для элиминации P. aeruginosa фармацевтической композиции по п. 1 или 2, которая представляет собой раствор, суспензию, эмульсию, ингалируемый порошок, аэрозоль или спрей. Его применение ограничено действием в отношении P. aeruginosa.
В заявке на изобретение (RU 2015122812 A, дата публикации 10.01.2017) описан рекомбинантный эндолизин rEPA в качестве антибактериального средства против инфекционных заболеваний, вызываемых P. aeruginosa и фармацевтическая композиция на его основе для лечения инфекции глаз, вызванных этой бактерией. Его применение ограничено действием в отношении инфекций, вызванных P. aeruginosa.
Известна заявка на изобретение (RU 2020129467 A, дата публикации 04.05.2022), в которой приведены последовательности 34 различных эндолизинов, в том числе модифицированных различными пептидами. Для данных белков были определены минимальные ингибирующие концентрации на одном штамме P. aeruginosa. Шесть из них были оценены в комбинациях с широко применяемыми в терапии антибиотиками в эксперименте in vitro. Однако, не показано получение данных эндолизинов, их эффективность не была оценена на моделях экспериментальных инфекций, а также не приведены составы фармацевтических композиций с данными белками.
Известен патент на изобретение (RU 2730613 C1, опубликовано 24.08.2020), в котором разработано антибактериальное средство на основе эндолизина LysAm24. Предложено использование белка рекомбинантного эндолизина бактериофага, в том числе в комбинации с фармацевтически приемлемыми носителями и/или веществами, увеличивающими проницаемость мембран, в качестве антимикробного средства, направленного против бактерий Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Salmonella typhi и Staphylococcus haemolyticus. На основе указанного белка, в том числе слитого с 8-гистидиновой меткой, получены антибактериальные композиции. Изобретение обеспечивает эффективное проникновение эндолизина без добавления различных пермеабилизаторов или ковалентно связанных пенетрирующих пептидов через наружную мембрану указанных бактерий и расщепление пептидогликана, что в конечном итоге приводит к гибели бактерий. Тем не менее, данный белок значительно теряет активность в отношении бактерий в стационарной фазе роста, а также в сложных смесях, в присутствии высоких концентраций солей, а, значит, может быть менее эффективен при системном введении препаратов на его основе.
В настоящее время отсутствуют препараты на основе эндолизинов бактериофагов, разрешенные к применению для лечения инфекционных заболеваний. Заявленное техническое решение более эффективно, чем исходный немодифицированный белок, так как сохраняет свои антибактериальные свойства в присутствии физиологических концентраций соли, что позволяет повысить эффективность антибактериальной терапии в отношении бактерий A. baumannii, P. aeruginosa, K. pneumoniae, E. coli, в том числе для применения в качестве инъекционной формы препарата.
Известен патент на изобретение (RU 2781050 C1, опубликовано 04.10.2022), в котором разработана бактерицидная композиция определенного состава в форме геля для местного применения на основе модифицированного эндолизина LysECD7-SMAP, гидроксиэтилцеллюлозы и полиэтиленгликоля, обладающая активностью в отношении грамотрицательных бактерий при местном применении. Данная композиция предназначена для применения в качестве антимикробного средства при раневых и ожоговых инфекциях. Однако, для действующего вещества данной композиции не показано действие на бактериальные пленки, что является важной составляющей терапии раневых инфекций, а также не установлен антибактериальный эффект в комбинации с антибиотиками.
Раскрытие сущности изобретения
Технической задачей заявленного изобретения является расширение арсенала противомикробных средств литического действия в отношении грамотрицательных бактерий, в том числе, с множественной лекарственной устойчивостью к используемым в терапии антибактериальным средствам.
Технический результат заключается в создании эффективного противомикробного средства, обладающего бактерицидным действием в отношении грамотрицательных бактерий видов K. pneumoniae, P. aeruginosa, A. baumannii и E. coli, в том числе обладающих множественной устойчивостью к антибиотикам. Данное средство может быть использовано в виде антибактериальной композиции, применяемой индивидуально или в комбинации с другими лекарственными средствами, где комбинации с другими лекарственными препаратами обладают синергетическим или аддитивным эффектом. Кроме того, данное средство может быть использовано для профилактики и лечения инфекционных заболеваний, вызванных грамотрицательными бактериями, а также для элиминации и предотвращения образования бактериальных биопленок.
Указанный технический результат достигается тем, что получен рекомбинантный полипептид модифицированного эндолизина (GRC-ML07), содержащий полипептид эндолизина LysAm24 дикого типа и антимикробный пептид RKLRRLKRKIAHKVKKY, при этом полипептид модифицированного эндолизина имеет аминокислотную последовательность SEQ ID NO:1.
Кроме того, были получены антибактериальные композиции, содержащие указанный полипептид в различных концентрациях (от 0,001 мг/мл до 10 мг/мл). Также антибактериальные композиции помимо полипептида могут содержать различные фармацевтически приемлемые вспомогательные вещества, пермеабилизаторы (трис(гидроксиметил)аминометан, этилендиаминтетрауксусная кислота (ЭДТА) и/или ее соли), противомикробными препаратами (антибиотики и синтетические антибактериальные средства - полимиксины, пенициллины, хлорамфеникол и другие; антимикробные пептиды - SMAP-29 (и его варианты), LL37, грамицидин, магаинин, протегрин, колицин, цекропин и другие) и другими литическими ферментами (нативные или модифицированные лизины бактериофагов AM24, AP22, ECD7, SI3 или других бактериофагов, лизостафин, лизоцим) для улучшения терапевтических свойств.
Также разработано лекарственное средство в виде раствора, лиофилизата или геля, содержащее указанную антибактериальную композицию.
Кроме того, раскрыто применение модифицированного полипептида лизина в качестве антимикробного средства, направленного против бактерий Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli.
Также разработан способ лечения заболеваний, вызванных бактериями Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, заключающийся в введении субъекту, нуждающемуся в этом, эффективного количества индивидуальной антибактериальной композиции, содержащей полипептид модифицированного эндолизина, или эффективного количества антибактериальной композиции в составе комбинированной терапии с антибиотиками классов полимиксинов, пенициллинов, цефалоспоринов или хлорамфениколом.
Краткое описание чертежей
На фиг.1 представлен график, отображающий бактерицидную активность различных концентраций 1 мкг/мл, 10 мкг/мл и 100 мкг/мл полипептида GRC-ML07 против штаммов A. baumannii Ts 50-16, P. aeruginosa Ts 38-16 и E. coli ATCC 25922. Антибактериальная активность (%) исследуемого полипептида рассчитана по отношению к количеству бактерий в контроле, инкубированном с буфером вместо белка. Для всех экспериментов показаны средние значения по стандартным отклонением после трех независимых экспериментов.
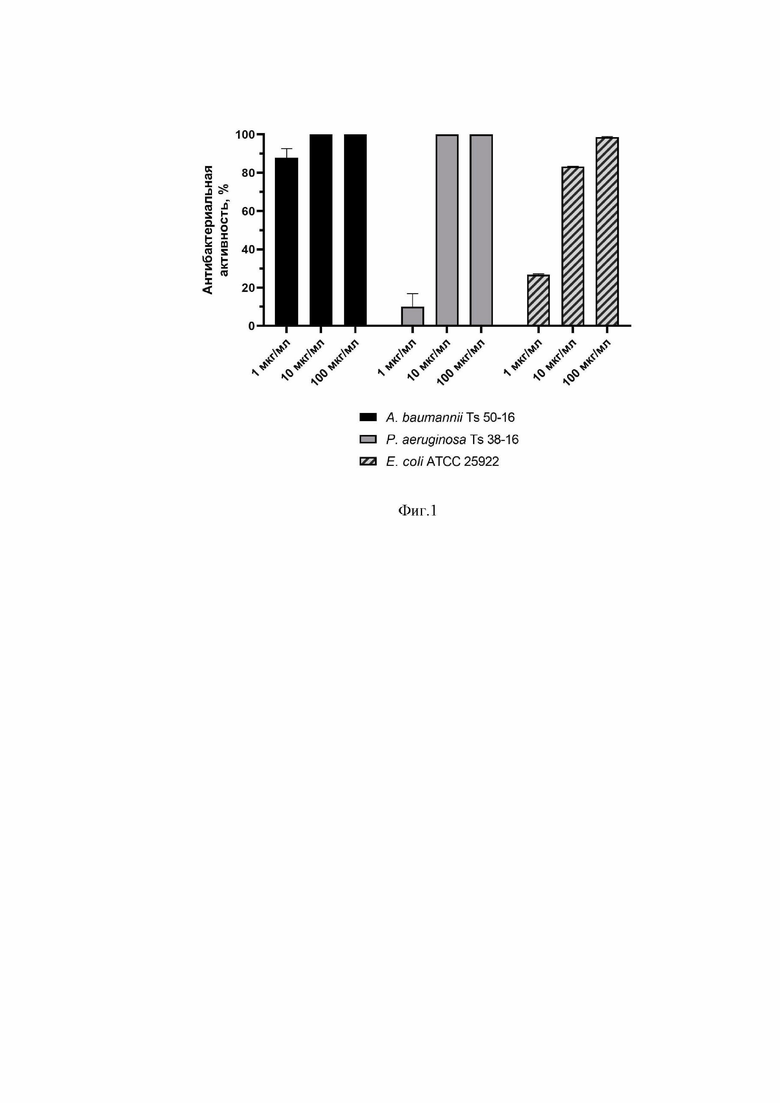
На фиг.2 представлен график, отображающий бактерицидную активность полипептида GRC-ML07 в концентрации 100 мкг/мл против различных штаммов грамотрицательных бактерий. Приведена антибактериальная активность (%) по сравнению с контролем. Результаты представлены диаграммами размаха: линии - медианы; ящики - интерквартильный диапазон; усы - мин-макс.
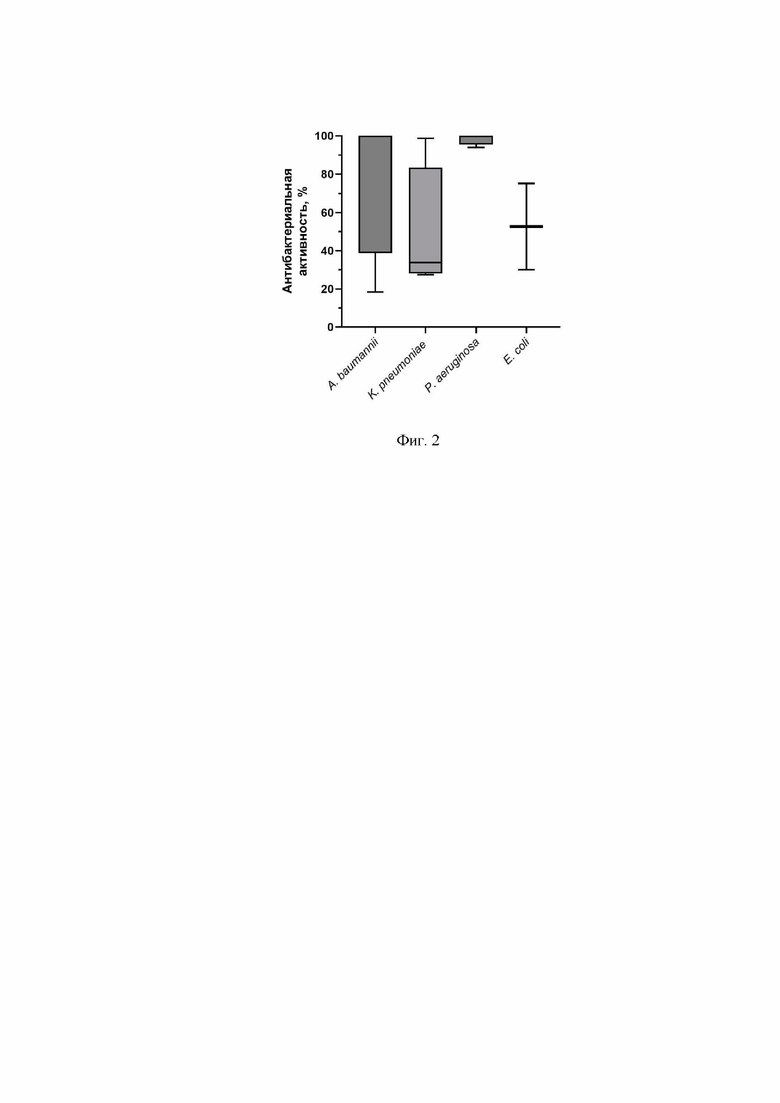
На фиг. 3 приведены микрофотографии суспензии бактерий A. baumannii Ts 50-16 после инкубации с полипептидом GRC-ML07 в концентрации 100 мкг/мл или с контрольным буфером PBS в течении 30 минут. Общее увеличение 16000.
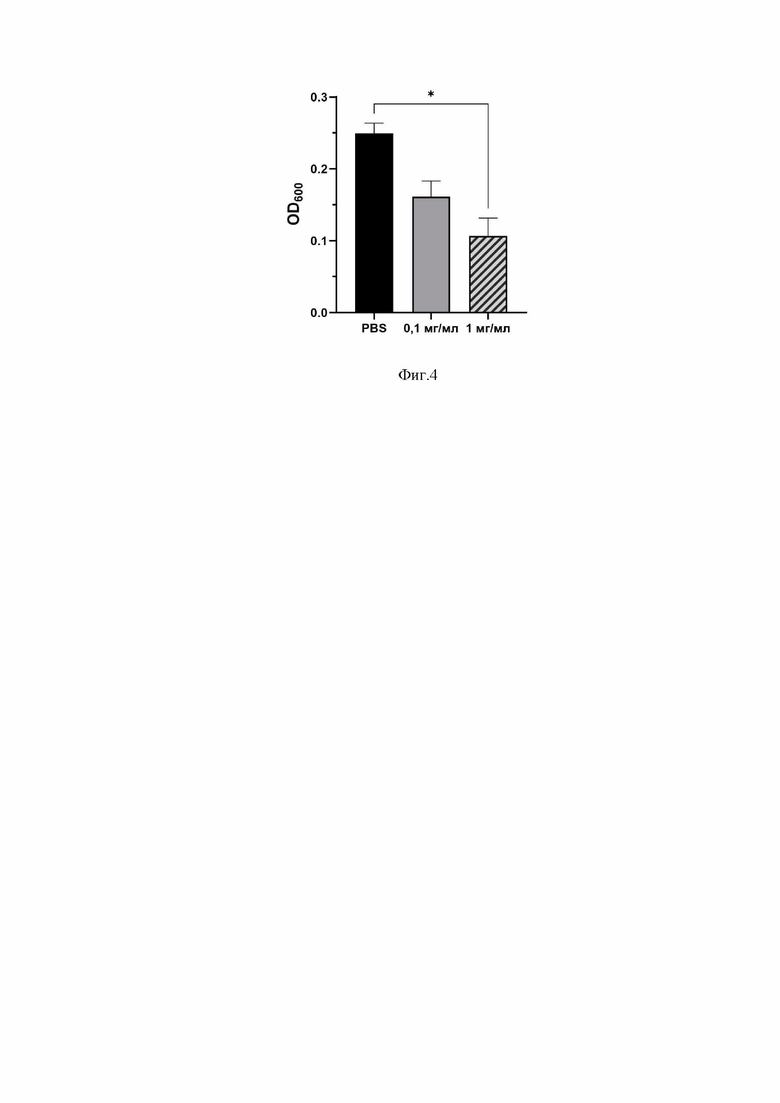
На фиг.4 представлен график активности GRC-ML07 в различных концентрациях (0,1 и 1 мг/мл) в отношении сформированных 24-часовых биопленок K. pneumoniae Ts 104-14 после инкубации с полипептидом или контрольным буфером в течение 2 часов. Активность выражена в снижении оптической плотности (OD600) биопленок, окрашенных кристаллическим фиолетовым красителем. Для всех экспериментов показаны средние значения с SD после трех независимых экспериментов. * - значимый бактерицидный эффект относительно контроля (p<0,05), критерий Краскела-Уоллиса.
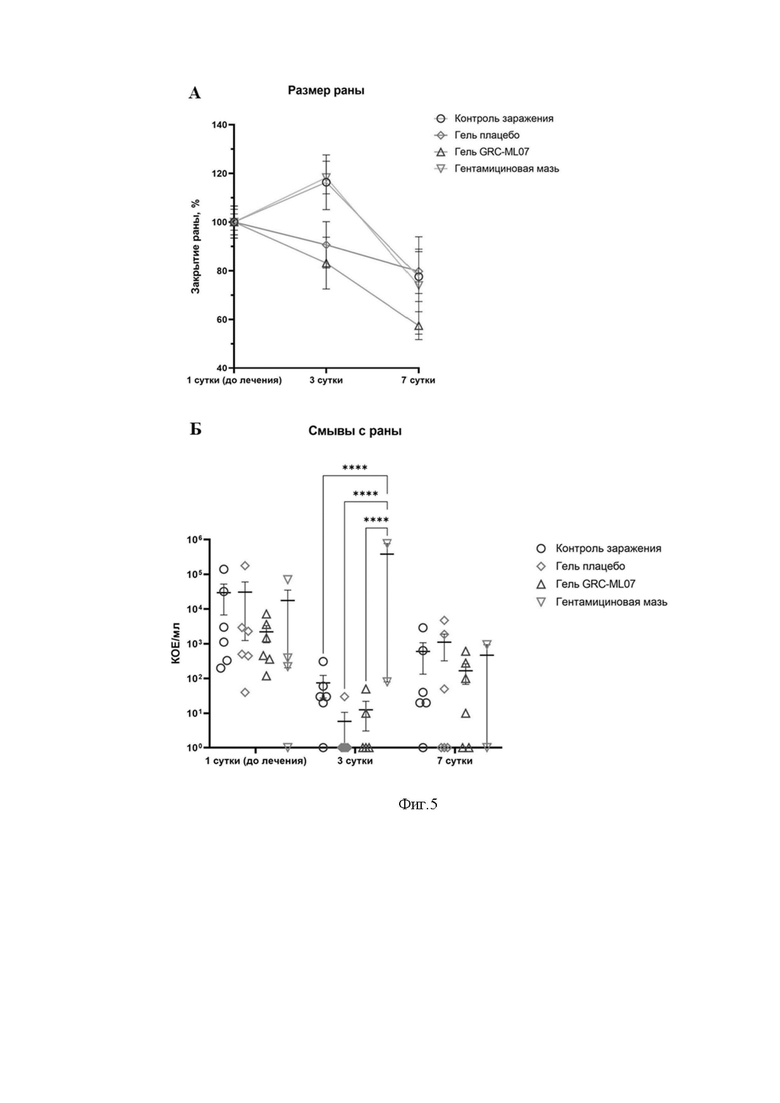
На фиг.5 представлены результаты экспериментального изучения антибактериального эффекта GRC-ML07 на модели инфекции (инфицированная рана). А. Динамика ранозаживления, представленная в виде изменения площади раны, выраженной в процентах от значения на 1 сутки до начала лечения. Для всех экспериментов показаны средние значения с SEM. Значимый эффект относительно контроля наблюдается на 3 сутки в группе гель GRC-ML07 (p=0,033), двухфакторный дисперсионный анализ. Б. Бактериальная нагрузка смывов с раневой поверхности. Для всех экспериментов показаны средние значения с SD. **** - значимый бактерицидный эффект относительно контроля (p<0,0001), двухфакторный дисперсионный анализ.
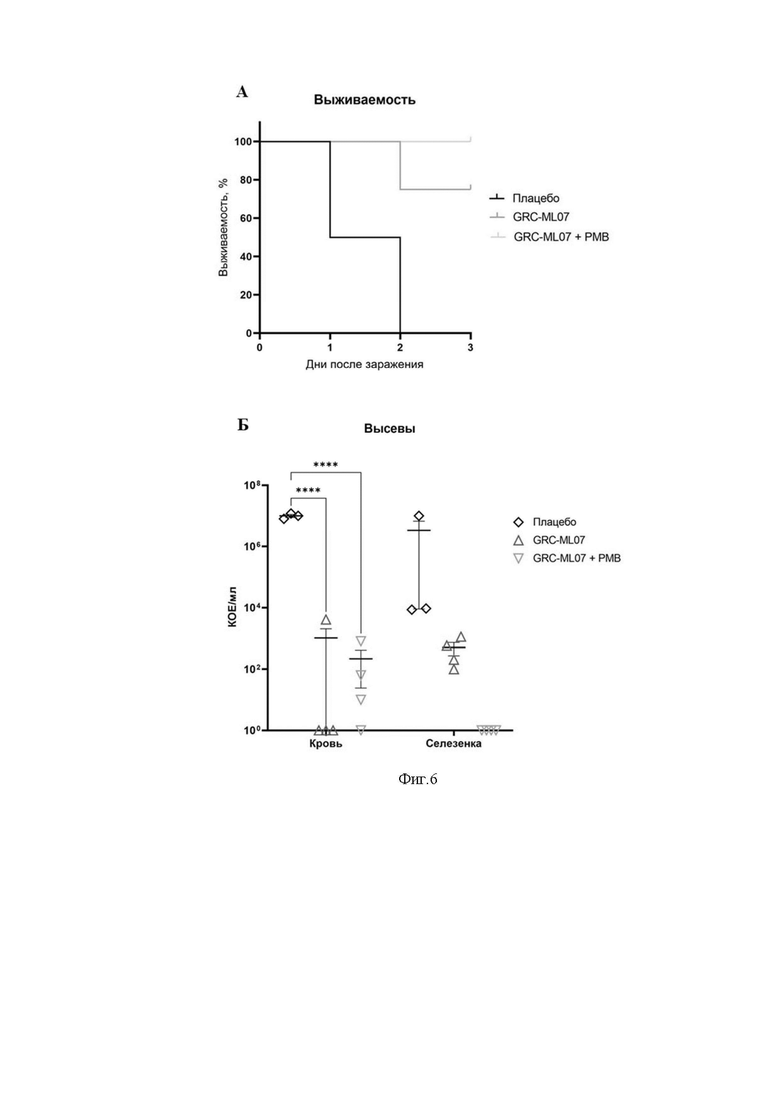
На фиг.6 представлены результаты экспериментального изучения антибактериального эффекта GRC-ML07 на модели инфекции (сепсис) при монотерапии и в комбинации с антибиотиком. А. Выживаемость мышей в ходе эксперимента (в каждой группе n=4). Б. Высевы из крови и селезенок животных в ходе эксперимента. Для всех экспериментов показаны средние значения с SEM. **** - значимый эффект относительно контроля (p<0,0001), двухфакторный дисперсионный анализ.
Осуществление изобретения
Средство представляет собой полипептид модифицированного эндолизина GRC-ML07, рекомбинантный фермент, полученный биотехнологическим путем. Получение полипептида состоит из нескольких этапов. Исходная кодирующая последовательность GRC-ML07 была искусственно синтезирована в векторе pALTA-GRC-ML07 и интегрирована в экспрессионный вектор pET-42b (+), в результате чего была получена плазмида pET42b-GRC-ML07. Корректность сборки векторной конструкций проверяли методом секвенирования по Сэнгеру.
Субстанцию белка получали по следующей технологии: трансформация клеток штамма продуцента плазмидой методом heat-shock, культивирование полученных клеток-продуцентов E. coli Bl21(DE3)pLysS в колбах Эрленмейера с индукцией экспрессии белка с помощью изопропил-β-D-1-тиогалактопиранозида, осветление культуральной жидкости центрифугированием, получение растворимых фракций лизатов биомассы клеток продуцента, их двухстадийная хроматографическая очистка (катионообменная хроматография на носителе SP-sepharose, с последующей гель-эксклюзионной хроматографией на носителе Superdex 75).
Таким образом была получена фармакологически активная субстанция полипептида GRC-ML07 в виде раствора в стерильном фосфатно-солевом буфере, pH 7,4 в диапазоне концентраций от 1 до 30 мг/мл. Чистоту и подлинность полученного рекомбинантного полипептида подтверждали методом вертикального электрофореза в полиакриламидном геле в денатурирующих условиях, а концентрацию измеряли спектрофотометрически с учетом теоретического коэффициента экстинкции.
Авторами изобретения были получены антибактериальные композиции на основе указанной выше субстанции, содержащие указанный полипептид в различных концентрациях (от 0,001 мг/мл до 10 мг/мл).
Были разработаны образцы композиций, дополненные различными фармацевтически приемлемыми носителями (например, вода, физиологический раствор, фосфатно-солевой буфер, трис(гидроксиметил)аминометан гидрохлорид). Данные композиции были включены в образцы лекарственных средств в виде раствора, в виде лиофилизата, а также в виде геля (гидроксиэтилцеллюлоза, натрий-карбоксиметилцеллюлоза, альгинаты натрия). Было показано, что они оказывают выраженный антибактериальный эффект в отношении различных видов бактерий.
Данные композиции могут быть дополнены пермеабилизаторами (трис(гидроксиметил)аминометан, этилендиаминтетрауксусная кислота и/или ее соли), противомикробными препаратами (антибиотики и синтетические антибактериальные средства - полимиксины, пенициллины, хлорамфеникол и другие; антимикробные пептиды - SMAP-29 (и его варианты), LL37, грамицидин, магаинин, протегрин, колицин, цекропин и другие) и другими литическими ферментами (нативные или модифицированные лизины бактериофагов AM24, AP22, ECD7, SI3 или других бактериофагов, лизостафин, лизоцим) для улучшения терапевтических свойств.
Осуществление изобретения подтверждается следующими примерами.
Пример 1. Изучение антибактериальной активности GRC-ML07
Оценка спектра действия и степени антибактериальной активности GRC-ML07 проводилась в экспериментах in vitro в отношении различных представителей грамотрицательных бактерий с различной степенью устойчивости к антибиотикам. Для этого суспензию бактерий в экспоненциальной фазе роста в PBS, pH 7,4 смешивали с эндолизином и инкубировали в течение 30 минут при 37°С с дальнейшим высевом на чашки Петри с агаризованной питательной средой и подсчетом колоний после инкубации в термостате. Полипептид проявлял дозозависимый антибактериальный эффект на штаммах P. aeruginosa, A. baumannii и E. coli (фиг. 1), значительно снижая количество бактерий в концентрации от 1 мкг/мл до 10 мг/мл. В концентрации 100 мкг/мл эндолизин проявлял значимую бактерицидную активность (более 30%) в отношении представителей грамотрицательных бактерий видов K. pneumoniae (n=4), P. aeruginosa (n=4), A. baumannii (n=4) и E. coli (n=2) (фиг. 2). Таким образом, в спектр антибактериальной активности модифицированного эндолизина входят практически все представители социально значимой группы патогенных бактерий ESKAPE, а также другие важные возбудители инфекционных заболеваний различной этиологии.
Пример 2. Бактерицидное действие фермента
Антибактериальная активность полипептида заключается в бактерицидном типе действия на бактериальные клетки, что было показано с помощью сканирующей электронной микроскопии.
После инкубации полипептида в концентрации 100 мкг/мл с суспензией бактерий модельного штамма A. baumannii в течение 30 минут и приготовления микропрепаратов, был показан лизис бактерий под действием GRC-ML07, в отличии от бактерий, инкубированных с PBS буфером (фиг.3).
Пример 3. Преимущества полипептида GRC-ML07 в сравнении с немодифицированным эндолизином
Показано, что полипептид GRC-ML07 в концентрации 10 мкг/мл оказывает 100% антибактериальную активность на клетки бактерий модельного штамма A. baumannii в буфере с концентрацией натрия хлорида 150 мМ (фосфатно-солевой буфер, рН 7,4), в отличие от немодифицированного эндолизина, чья активность полностью ингибируется добавлением NaCl в концентрации от 50 мМ. Данное преимущество полипептида GRC-ML07 позволяет использовать его для создания фармацевтических композиций для парентерального применения.
Пример 4. Действие GRC-ML07 в отношении сформированных бактериальных биопленок.
Противобиопленочную активность эндолизина оценивали на 24-часовых биопленках различных видов бактерий (K. pneumoniae, P. aeruginosa, A. baumannii). Для этого биопленки были выращены в лунках 96-луночного планшета, отмыты от планктонных клеток и подвержены воздействию раствора эндолизина в концентрациях 100 и 1000 мкг/мл в течение 2 часов. Дальнейшая окраска с помощью раствора кристаллического фиолетового показала, что эндолизин GRC-ML07 значительно снижал плотность биопленок относительно контроля в дозозависимой манере, разрушая до 100% биопленки. Пример действия полипептида на сформированные 24-часовые биопленки K. pneumoniae представлен на фиг. 4.
Пример 5. Синергизм действия полипептида GRC-ML07 и антибактериальных препаратов.
В ходе работы был оценен in vitro потенциал применения подхода комбинированной терапии на основе классических антибиотиков и модифицированного эндолизина бактериофага GRC-ML07, в отношении грамотрицательных патогенов.
Синергизм действия различных концентраций GRC-ML07 и антибиотиков полимиксина В, хлорамфеникола, ампициллина и цефотаксима был показан методом шахматной доски на различных представителях грамотрицательных бактерий (по два штамма видов K. pneumoniae, P. aeruginosa, A. baumannii), в том числе, обладающих множественной лекарственной устойчивостью.
Для этого двукратные разведения раствора эндолизина были инкубированы в лунках 96-луночного планшета с двукратными разведениями антибиотика в течение 16-20 часов и были оценены ингибирующие бактериальный рост комбинации. Для каждой комбинации рассчитывали ∑ФИК (индекс фракционной ингибирующей концентрации).
∑ФИК = МИКАБ / МИКА + МИКБА / МИКБ,
где МИКА - МИК антибиотика А;
МИКБ - МИК антибиотика Б;
МИКАБ - МИК антибиотика A в присутствии антибиотика Б;
МИКБА - МИК антибиотика Б в присутствии антибиотика А.
Полученные результаты интерпретировали следующим образом:
В диапазоне доз GRC-ML07 от 512 мкг/мл до 64 мкг/мл и антибиотиков от 16 мкг/мл до 0,015 мкг/мл наблюдался выраженный синергетический или аддитивный эффект на всех трех видах бактерий (Таблица 1). Более того, ни для одной комбинации не было показано случаев антагонизма.
Мы показали, что комбинации могут не только обладать синергетическим действием (в случае комбинации лизина и полимиксина), но и возвращать чувствительность микроорганизма к антибиотику. Например, для трех штаммов удалось показать аддитивный эффект в комбинации лизина с ампициллином, к которому все штаммы были исходно устойчивы. Аналогичные результаты были показаны для хлорамфеникола, причем следует отметить, что A. baumannii и P. aeruginosa обладают природной к нему устойчивостью, в то время как мы показали выраженный синергизм или аддитивный эффект. При этом, механизм противомикробного действия эндолизинов предполагает отсутствие развития устойчивости к нему бактерий, а значит такая терапевтическая схема безопасна при курсовом применении. Эти исследования могут послужить основой для разработки новых схем лечения с тяжелыми и хроническими инфекциями, вызванными антибиотико-устойчивыми возбудителями.
Пример 6. Получение образцов антибактериальных композиций на основе GRC-ML07
Были получены образцы композиций со следующим составом:
1. Растворы были получены путем разведения концентрата (субстанции) полипептида в соответствующем буфере до необходимой концентрации.
Растворы полипептида с концентрацией 0,001 мг/мл, 0,01 мг/мл, 0,1 мг/мл, 1 мг/мл, 10 мг/мл в фосфатно-солевом буфере с рН 5,0, 6,0, 7,0, 7,5, 8,0, 9,0.
Растворы полипептида с концентрацией 0,001 мг/мл, 0,01 мг/мл, 0,1 мг/мл, 1 мг/мл, 10 мг/мл 20 мМ растворе трис гидрохлорида с рН 5,0, 6,0, 7,5, 8,0, 9,0.
Растворы полипептида с концентрацией 0,001 мг/мл, 0,01 мг/мл, 0,1 мг/мл, 1 мг/мл, 10 мг/мл в физиологическом растворе.
Растворы были дополнены веществами, улучшающими проницаемость бактериальных мембран (пермеабилизаторами) - трис(гидроксиметил)аминометаном в концентрации 40-100 мМ, этилендиаминтетрауксусной кислотой (ЭДТА) или ее натриевой солью в концентрации 1-100 мМ.
2. Лиофилизаты с полипептидом были получены из вышеуказанных растворов путем сублимационного высушивания.
3. Гели с полипептидом были получены путем введения вышеуказанных растворов полипептида в предварительно подготовленный 0,5% - 1% раствор альгината натрия, 1 - 3% раствор гидроксиэтилцеллюлозы и 1 - 3% раствор натрий-карбоксиметилцеллюлозы.
Антибактериальная активность образцов оценивалась в экспериментах in vitro на модельном штамме A. baumannii. Например, растворы полипептида в PBS, Трис-HCl в диапазоне рН 5,0 - 9,0, а также физрастворе в концентрации 1 мкг/мл обладают активностью 80 - 100%. Добавление пермеабилизаторов приводит к увеличению активности до 100% во всех случаях. Заявленные композиции могут быть получены специалистами на практике и их использование обеспечивает реализацию заявленного назначения.
Пример 7. Экспериментальное изучение антибактериального эффекта GRC-ML07 на модели инфекции (инфицированная рана).
Для эксперимента готовили гель на основе водорослевого альгината (1%), содержащего 1 мг/мл эндолизина GRC-ML07. Мышам BALB/c (самки, 18-20 г) за сутки до начала эксперимента удаляли шерстный покров машинкой для стрижки. Раневой дефект наносили на спинах животных под наркозом (золетил-ксилазин) специальным инструментом для биопсии (d=8 мм, Medax, Italy). Через 5 минут на поверхность раны наносили суспензию полирезистентного штамма P. aeruginosa Ts 38-16 в концентрации 5×108 КОЕ/рану. Спустя 24 ч начинали лечение накожным нанесением препарата (n = 6), плацебо (гель без полипептида, n = 6) или стандартным препаратом (гентамициновая мазь, n = 6) в соответствии с планом эксперимента. Для этого, препараты в объеме 100 мкл наносили на раневую поверхность ежедневно два раза в сутки в течение 5 дней. На 1, 3 и 7 сутки изучали патоморфологические изменения раневой поверхности и измеряли ее площадь (планиметрия), а также оценивали микробную нагрузку путем смывов с поверхности раны. Полученные смывы в PBS высевали разведения на плотную питательную среду с дальнейшим культивированием в течение 18 ч при температуре 37°С для оценки их обсемененности.
При оценке результатов исследования, с учетом динамики изменения площади ран и бактериальной нагрузки смывов, был выявлен непосредственный эффект исследуемой антибактериальной композиции на ранозаживление при образовании инфицированных ран. Показано изменение в обсемененности раны и достоверное снижение бактериальной нагрузки под действием геля с GRC-ML07. При лечении гелем GRC-ML07 было показано достоверное снижение площади ран по сравнению с контролем. Более того, после окончания лечения терапевтический эффект в группе GRC-ML07 сохранялся гораздо лучше, чем в группе плацебо. Лечение гентамициновой мазью значительно ухудшало течение инфекции, ранозаживление и обсемененность раневых поверхностей. Результаты эксперимента представлены на фиг. 5.
Пример 8. Экспериментальное изучение антибактериального эффекта GRC-ML07 на модели инфекции (сепсис) при монотерапии и в комбинации с антибиотиком.
Самкам мышей линии BALB/c (18-20 г) внутрибрюшинно вводили взвесь клеток штамма K. pneumoniae М9 в дозе 1×105 КОЕ/животное. Спустя 2 часа после заражения внутривенно вводили исследуемый препарат GRC-ML07 в PBS рН=7,5 (12,5 мг/кг, n = 4), комбинацию GRC-ML07 и полимиксина В (0,05 мг/кг, n = 4) или плацебо (PBS, n = 4) в объеме 100 мкл. Лечение проводили ежедневно, 5 дней, 2 раза в сутки. В течение 3 суток за животными проводили наблюдение, учитывали их гибель, строили кривые выживаемости.
У павших животных отбирали образцы крови и извлекали селезенку, выживших животных подвергали эвтаназии методом цервикальной дислокации и отбирали те же образцы в последний день эксперимента. Проводили оценку обсемененности крови и гомогенатов селезенки методом бактериологического посева различных разведений на плотную питательную среду с дальнейшим культивированием в течение 18 ч при температуре 37°С, проводя подсчет выросших бактериальных колоний.
При оценке результатов исследования, был выявлен значительный антибактериальный эффект исследуемого препарата GRC-ML07 как при монотерапии, так и в комбинации с антибиотиком в дозировке, составляющей 0,5 МИК. Выживаемость в контрольной группе составила 0% (все пали на вторые сутки эксперимента), при этом в группе GRC-ML07 выживаемость на 3 сутки составила 75%, а в группе с добавлением субтерапевтической дозы полимиксина В достигала 100%. Также показано достоверное снижение бактериальной нагрузки в крови под действием GRC-ML07. В селезёнке не было показано достоверных различий, тем не менее тенденция снижения высевов выражена. Результаты эксперимента представлены на фиг. 6.
Список литературы
1. 2021 antibacterial agents in clinical and preclinical development: an overview and analysis [Internet]. [cited 2022 Jun 26]. Available from: https://www.who.int/publications/i/item/9789240047655;
2. Antibacterial agents in preclinical development: an open access database [Internet]. [cited 2022 Jun 26]. Available from: https://apps.who.int/iris/handle/10665/330290).
3. 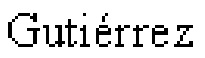 D, Briers Y. Lysins breaking down the walls of Gram-negative bacteria, no longer a no-go. Current Opinion in Biotechnology. 2021 Apr 1;68:15-22.
D, Briers Y. Lysins breaking down the walls of Gram-negative bacteria, no longer a no-go. Current Opinion in Biotechnology. 2021 Apr 1;68:15-22.
4. Choi YJ, Kim S, Bae S, Kim Y, Chang HH, Kim J. Antibacterial Effects of Recombinant Endolysins in Disinfecting Medical Equipment: A Pilot Study. Frontiers in Microbiology. 2022 Mar 2;12:4380.
5. Schmelcher M, Loessner MJ. Bacteriophage endolysins - extending their application to tissues and the bloodstream. Current Opinion in Biotechnology. 2021 Apr 1;68:51-9.
6. Fursov M v., Abdrakhmanova RO, Antonova NP, Vasina D v., Kolchanova AD, Bashkina OA, et al. Antibiofilm activity of a broad-range recombinant endolysin LysECD7: In vitro and in vivo study. Viruses. 2020 May 1;12(5).
7. Vasina D v., Antonova NP, Grigoriev I v., Yakimakha VS, Lendel AM, Nikiforova MA, et al. Discovering the Potentials of Four Phage Endolysins to Combat Gram-Negative Infections. Frontiers in Microbiology. 2021 Oct 13;12:3033.
8. Kim S, Jin JS, Lee DW, Kim J. Antibacterial activities of and biofilm removal by Ablysin, an endogenous lysozyme-like protein originated from Acinetobacter baumannii 1656-2. Journal of Global Antimicrobial Resistance. 2020 Dec 1;23:297-302.
9. Love MJ, Abeysekera GS, Muscroft-Taylor AC, Billington C, Dobson RCJ. On the catalytic mechanism of bacteriophage endolysins: Opportunities for engineering. Biochim Biophys Acta Proteins Proteom [Internet]. 2020 Jan 1 [cited 2022 Jun 26];1868(1). Available from: https://pubmed.ncbi.nlm.nih.gov/31678195/
10. Grishin A v., Karyagina AS, Vasina D v., Vasina I v., Gushchin VA, Lunin VG. Resistance to peptidoglycan-degrading enzymes. Critical Reviews in Microbiology. 2020 Nov 1;46(6):703-26.
11. Gontijo MTP, Jorge GP, Brocchi M. Current Status of Endolysin-Based Treatments against Gram-Negative Bacteria. Antibiotics (Basel). 2021 Sep 22;10(10):1143.
--->
Перечень последовательностей
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing originalFreeTextLanguageCode="ru"
dtdVersion="V1_3" fileName="Эндолизин GRC-ML07.xml"
softwareName="WIPO Sequence" softwareVersion="2.2.0"
productionDate="2023-04-06">
<ApplicantFileReference>1</ApplicantFileReference>
<ApplicantName languageCode="ru">федеральное государственное
бюджетное учреждение «Национальный исследовательский центр
эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи»
Министерства здравоохранения Российской Федерации</ApplicantName>
<ApplicantNameLatin>federalnoe gosudarstvennoe biudzhetnoe
uchrezhdenie Natsionalnyi issledovatelskii tsentr epidemiologii i
mikrobiologii imeni pochetnogo akademika N F Gamalei Ministerstva
zdravookhraneniia Rossiiskoi Federatsii</ApplicantNameLatin>
<InventionTitle languageCode="ru">Модифицированный эндолизин и
антибактериальные композиции на его основе для лечения инфекций,
вызванных бактериями Acinetobacter baumannii, Pseudomonas aeruginosa,
Klebsiella pneumoniae, Escherichia coli</InventionTitle>
<SequenceTotalQuantity>1</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>243</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..243</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>MDILKFNSRGDLVVHLQKKLASLGYKLNPDGIFGKATQEAVIHFQRQNG
LTSDGIVGKLTWSMLDSKTSSIGKTRTISQNGINFIKSFEGLRLRAYDDGVGVITIGYGTTRYPNGHKVQ
LGDTCTEKQAEQYLSNDLVKFEKAVNELVKVPVNQNQYDALVSFTYNVGVGALSTSKALKLLNAGDYTGC
AKAMLSWNKGRVGGKLVEIGGLTRRRNAEKDLFLKLERKLRRLKRKIAHKVKKY</INSDSeq_sequen
ce>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против бактерий Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Salmonella typhi и Staphylococcus haemolyticus (варианты) | 2019 |
|
RU2730614C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против грамотрицательных бактерий: Pseudomonas aeruginosa, Acinetobacter baumannii, Klebsiella pneumoniae и Salmonella typhi (варианты) | 2019 |
|
RU2730615C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против бактерий Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Salmonella typhi и Staphylococcus haemolyticus (варианты) | 2019 |
|
RU2730613C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против бактерий Acinetobacter baumannii, (варианты) | 2019 |
|
RU2730616C1 |
| БАКТЕРИЦИДНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПАРЕНТЕРАЛЬНОГО ПРИМЕНЕНИЯ В ФОРМЕ ЛИОФИЛИЗАТА С ЭНДОЛИЗИНОМ | 2021 |
|
RU2792679C1 |
| БАКТЕРИЦИДНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ В ФОРМЕ ГЕЛЯ БАКТЕРИЦИДНОГО С ЭНДОЛИЗИНОМ | 2021 |
|
RU2781050C1 |
| БАКТЕРИОФАГИ, ФАГОВЫЕ ПЕПТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2614114C2 |
| ПОЛИПЕПТИДЫ ЛИЗИНА, АКТИВНЫЕ ПРОТИВ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ | 2016 |
|
RU2724545C2 |
| Бета-шпилечный пептид, обладающий антимикробной активностью в отношении бактерий с множественной лекарственной устойчивостью | 2023 |
|
RU2812977C1 |
| КОМПОЗИЦИЯ АНТИБАКТЕРИАЛЬНАЯ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ГОСПИТАЛЬНЫХ ИНФЕКЦИЙ (ВАРИАНТЫ), ШТАММЫ БАКТЕРИОФАГОВ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ПОЛУЧЕНИЯ ТАКОЙ КОМПОЗИЦИИ | 2015 |
|
RU2628312C2 |
Группа изобретений относится к биотехнологии, биохимии, молекулярной биологии, микробиологии. Предложен полипептид модифицированного эндолизина, имеющий аминокислотную последовательность SEQ ID NO:1, обладающий противомикробной активностью в отношении Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli. Также созданы антибактериальная композиция, лекарственное средство и способ для лечения заболеваний, вызванных бактериями Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, с использованием полипептида модифицированного эндолизина. Группа изобретений обеспечивает создание эффективного средства, обладающего бактерицидным действием в отношении грамотрицательных бактерий видов K. pneumoniae, P. aeruginosa, A. baumannii и E. coli, в том числе обладающих множественной устойчивостью к антибиотикам. 5 н. и 6 з.п. ф-лы, 6 ил., 1 табл., 8 пр.
1. Полипептид модифицированного эндолизина, имеющий аминокислотную последовательность SEQ ID NO:1 и обладающий противомикробной активностью в отношении Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli.
2. Полипептид модифицированного эндолизина по п. 1, где указанная последовательность содержит линкер между полипептидом эндолизина и антимикробным пептидом, состоящий как минимум из одного аминокислотного остатка.
3. Антибактериальная композиция против бактерий Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, включающая полипептид модифицированного эндолизина по любому из пп. 1, 2, в количестве от 0,001 до 10 мг/мл.
4. Антибактериальная композиция по п. 3, дополнительно включающая фармацевтически приемлемый носитель.
5. Антибактериальная композиция по любому из пп. 3, 4, дополнительно включающая пермеабилизаторы, выбранные из трис(гидроксиметил)аминометана, этилендиаминтетрауксусной кислоты (ЭДТА) и/или ее солей.
6. Антибактериальная композиция по любому из пп. 3-5, дополнительно включающая антибиотики, в частности полимиксины, пенициллины, хлорамфеникол и/или цефалоспорины.
7. Антибактериальная композиция по любому из пп. 3-6, дополнительно включающая SMAP-29 или его варианты, LL37, грамицидин, магаинин, протегрин, колицин или цекропин.
8. Антибактериальная композиция по любому из пп. 3-7, дополнительно включающая нативные или модифицированные лизины бактериофагов AM24, AP22, ECD7, SI3, лизостафин, лизоцим.
9. Лекарственное средство, содержащее антибактериальную композицию по любому из пп. 3-8, в виде раствора, лиофилизата или геля.
10. Применение полипептида модифицированного эндолизина по любому из пп. 1, 2 в качестве антимикробного средства, направленного против бактерий Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli.
11. Способ лечения заболеваний, вызванных бактериями Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, заключающийся во введении субъекту, нуждающемуся в этом, эффективного количества индивидуальной антибактериальной композиции по любому из пп. 3-8, содержащей полипептид модифицированного эндолизина по любому из пп. 1, 2, или эффективного количества антибактериальной композиции в составе комбинированной терапии с антибиотиками классов полимиксинов, пенициллинов, цефалоспоринов и/или хлорамфениколом.
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против бактерий Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Salmonella typhi и Staphylococcus haemolyticus (варианты) | 2019 |
|
RU2730613C1 |
| БАКТЕРИЦИДНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ В ФОРМЕ ГЕЛЯ БАКТЕРИЦИДНОГО С ЭНДОЛИЗИНОМ | 2021 |
|
RU2781050C1 |
| ЛИТИЧЕСКИЙ ФЕРМЕНТ БАКТЕРИОФАГА И АНТИБАКТЕРИАЛЬНАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2018 |
|
RU2703043C1 |
| Приспособление для ионизации воздуха | 1933 |
|
SU37202A1 |
| АНТИБАКТЕРИАЛЬНАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ЭНДОЛИЗИНОВ И ЛЕКАРСТВЕННЫЕ СРЕДСТВА В ФОРМЕ ГЕЛЯ ИЛИ СПРЕЯ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2021 |
|
RU2790481C1 |
| Приспособление для оплавливания стеклянных бус в электрической печи | 1928 |
|
SU20282A1 |
| CARRATALA J | |||
| V | |||
| et al | |||
| Design strategies for positively charged endolysins: Insights into Artilysin | |||
Авторы
Даты
2024-02-14—Публикация
2023-10-02—Подача