Изобретение относится к области биотехнологии и может быть использовано в медицине и ветеринарии. Пептид абареницин, обладающий антимикробным действием в отношении бактерий с множественной лекарственной устойчивостью, имеет следующую аминокислотную последовательность: Gly1-Tyr2-Cys3-Phe4-Thr5-Ala6-Cys7-Ala8-Arg9-Arg10-Asn11-Gly12-Val13-Arg14-Ile15-Cys16-Tyr17-Arg18-Arg19-Cys20-Asn21 (SEQ ID No: 1).
Мультирезистентные внутрибольничные бактериальные инфекции (ВБИ) все чаще становятся причиной смерти пациентов, подвергающихся инвазивным процедурам при лечении в стационарах. В условиях глобальной пандемии (например, COVID-19) критически возрастает нагрузка на систему здравоохранения, что может привести к резкому росту смертности от вторичных ВБИ, в первую очередь, вызванных патогенами группы «ESKAPE» (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa и Enterobacter spp.). В сложившейся ситуации снижения эффективности антибиотиков критически важной задачей для системы здравоохранения является создание резервных антимикробных препаратов, для которых минимален риск развития бактериальной резистентности. В последние годы значительное внимание ведущих мировых научных групп и фармацевтических компаний уделяется исследованию катионных антимикробных пептидов (АМП) - ключевых молекулярных факторов врожденного иммунитета живых организмов [Lazzaro, B.P.; Zasloff, M.; Rolff, J. Antimicrobial Peptides: Application Informed by Evolution. Science 2020, 368, eaau5480, doi:10.1126/science.aau5480.]. Принципиальными преимуществами коротких (16-22 а.о.) бета-шпилечных АМП являются сочетание быстрого бактерицидного эффекта за счет действия на мембрану патогена и, как следствие, низкая вероятность возникновения антибиотикорезистентности, а также высокой устойчивости к протеолизу [Panteleev, P.V.; Balandin, S.V.; Ivanov, V.T.; Ovchinnikova, T.V. A Therapeutic Potential of Animal β-Hairpin Antimicrobial Peptides. Curr Med Chem 2017, 24, 1724-1746, doi:10.2174/0929867324666170424124416]. Эти качества позволяют рассматривать бета-шпилечные АМП как прототипы индивидуальных антибиотиков для системного применения. Меньшие размеры молекулы и более простая пространственная организация, чем у большинства других цистеинсодержащих АМП (таких как дефенсины), упрощают задачу биотехнологического получения этих пептидов. Однако сравнительно высокая цитотоксичность (в т.ч. гемолитическая активность) многих природных пептидов ограничивает их применение в медицине. Недостатки АМП могут быть устранены, полностью или частично, путем модификации структуры природных соединений [Panteleev, P.V.; Bolosov, I.A.; Balandin, S.V.; Ovchinnikova, T.V. Design of Antimicrobial Peptide Arenicin Analogs with Improved Therapeutic Indices. J Pept Sci 2015, 21, 105-113, doi:10.1002/psc.2732].
Наиболее близким аналогом заявляемого изобретения являются ранее открытые представители семейства бета-шпилечных АМП ареницинов, а также их модифицированные аналоги, например, АА139 (Фиг. 1) - пептид с доказанной высокой эффективностью антибактериального действия на мышиных моделях инфекции, разработкой и клиническими испытаниями которого занимается компания Adenium Biotech Pty Ltd. [Elliott, A.G.; Huang, J.X.; Neve, S.; Zuegg, J.; Edwards, I.A.; Cain, A.K.; Boinett, C.J.; Barquist, L.; Lundberg, C.V.; Steen, J.; et al. An Amphipathic Peptide with Antibiotic Activity against Multidrug-Resistant Gram-Negative Bacteria. Nat Commun 2020, 11, 3184, doi:10.1038/s41467-020-16950-x]. Заявляемый пептид аналогично препарату АА139 действует на мембраны бактериальных клеток-мишеней и не проявляет существенных цитотоксических эффектов в отношении клеток человека в диапазоне концентраций до 64-128 мкМ, при этом обладает сравнительно более высокой антибактериальной активностью в отношении грамотрицательных микроорганизмов: среднее геометрическое значений минимальных ингибирующих концентраций (МИК) для абареницина составило 0,29 мкМ против 0,5 мкМ для АА139. Таким образом, в большинстве случаев ингибирующий антибактериальный эффект достигается при действии в субмикромолярных концентрациях, что указывает на высокую селективность действия заявляемого пептида. Техническим результатом изобретения является высокая антибактериальная активность заявляемого пептида в отношении грамотрицательных бактерий, в том числе в отношении штаммов с множественной лекарственной устойчивостью, а также при лечении инфицированных животных. Заявляемый пептид абареницин имеет катионную природу, состоит из 21 аминокислотного остатка, содержит две дисульфидные связи и не требуют осуществления ферментативных посттрансляционных модификаций, что делает предпочтительным его биотехнологическое получение в бактериальной системе. Заявляемый пептид может быть получен путем гетерологической экспрессии в бактериальной системе на основе Еscherichia coli, а также с помощью химического синтеза.
Изобретение иллюстрируют графические материалы
Фиг. 1. Выравнивание аминокислотных последовательностей АМП. Квадратными скобками отмечен характер замыкания дисульфидных мостиков.
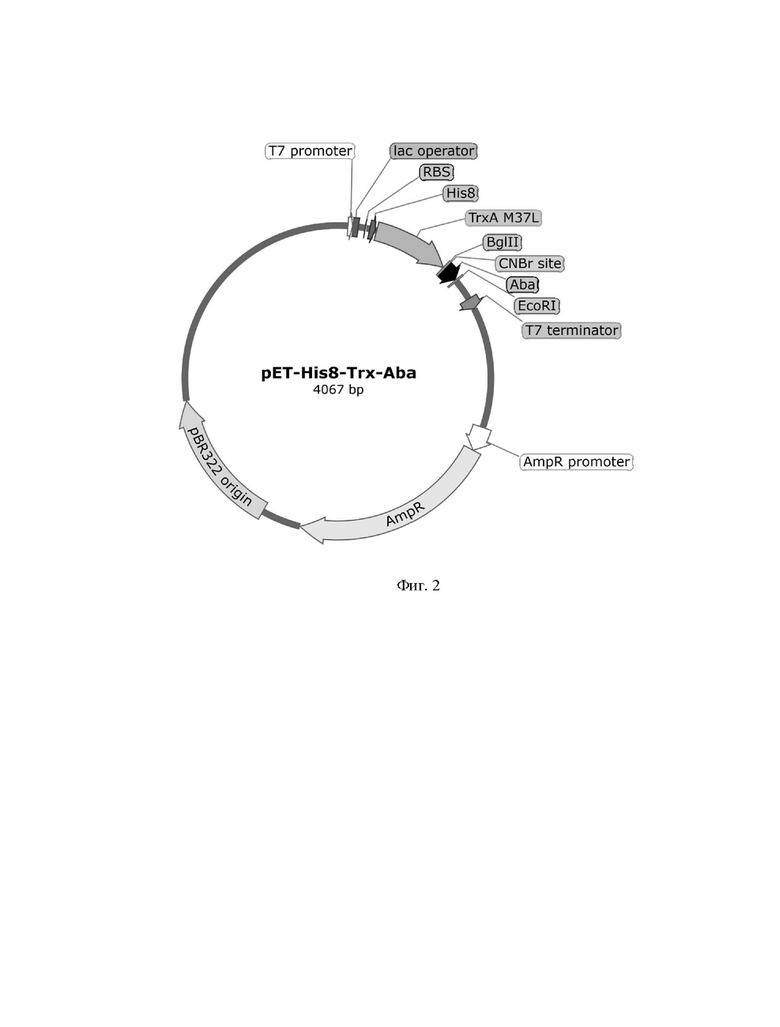
Фиг. 2. Физическая карта плазмидного вектора для экспрессии бета-шпилечных полипептидов: pBR322 origin - участок инициации репликации плазмиды; AmpR - ген устойчивости к β-лактамным антибиотикам; T7 promoter - промотор транскрипции; T7 terminator - терминатор транскрипции; RBS - сайт связывания рибосомы; TrxA M37L - последовательность, кодирующая модифицированный тиоредоксин; His8 - последовательность, кодирующая восемь остатков гистидина; Aba - последовательность, кодирующая заявляемый пептид.
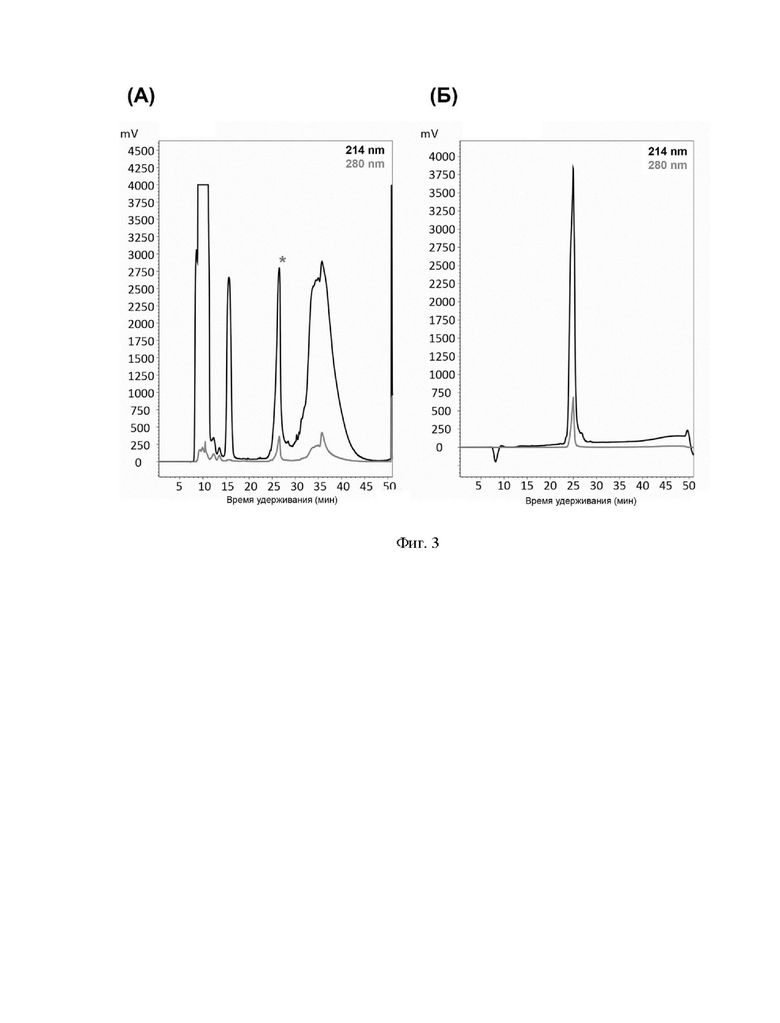
Фиг. 3. (А) Хроматограмма первичной очистки рекомбинантного пептида абареницина (SEQ ID No.1) методом обращенно-фазовой ВЭЖХ (* - пик, соответствующий целевому пептиду). (Б) Хроматограмма повторной очистки рекомбинантного пептида абареницина (SEQ ID No.1) методом обращенно-фазовой ВЭЖХ.
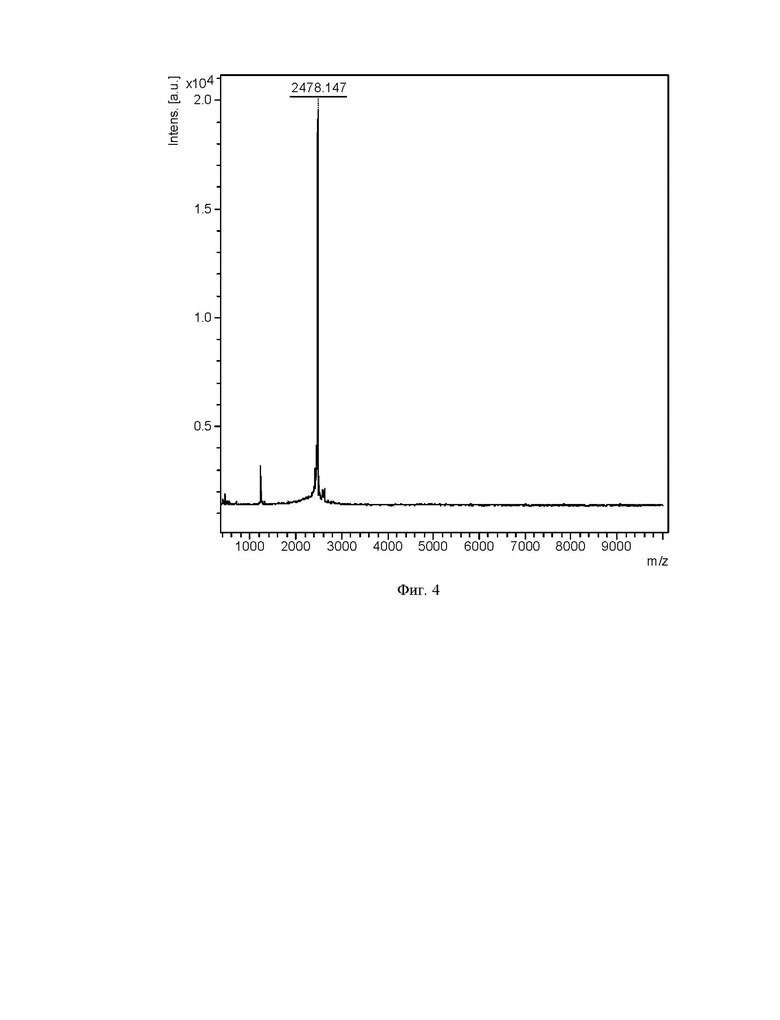
Фиг. 4. МАЛДИ масс-спектр рекомбинантного пептида абареницина (SEQ ID No.1), полученного генно-инженерным способом.
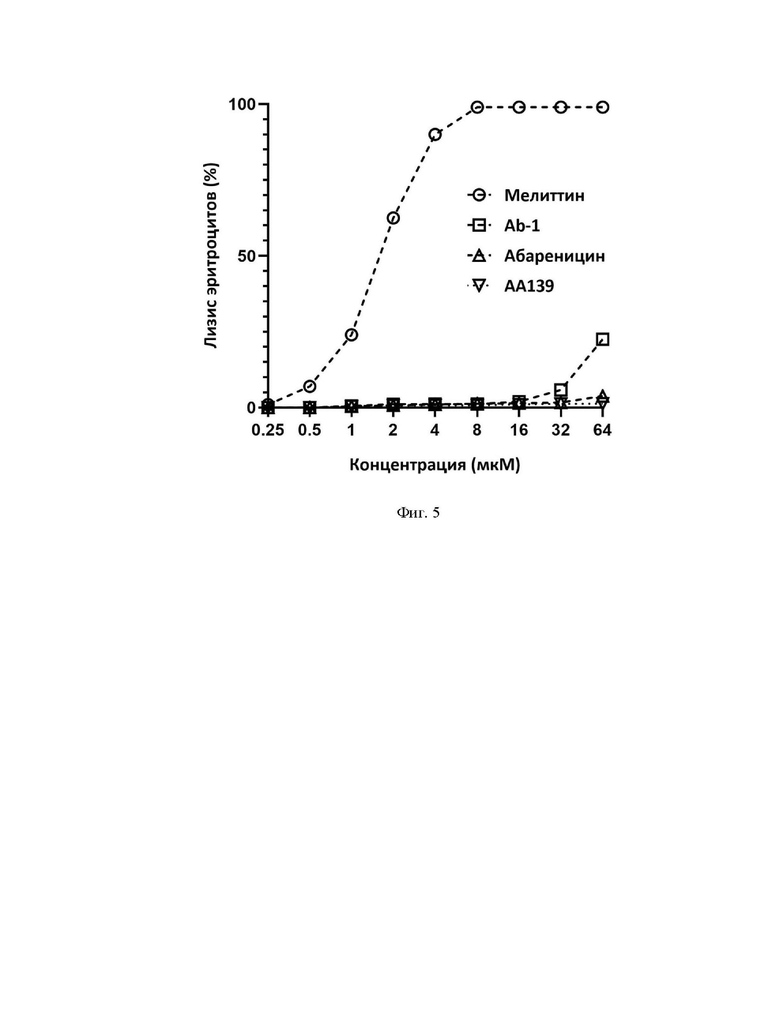
Фиг. 5. Цитотоксическое действие АМП на человеческие эритроциты.
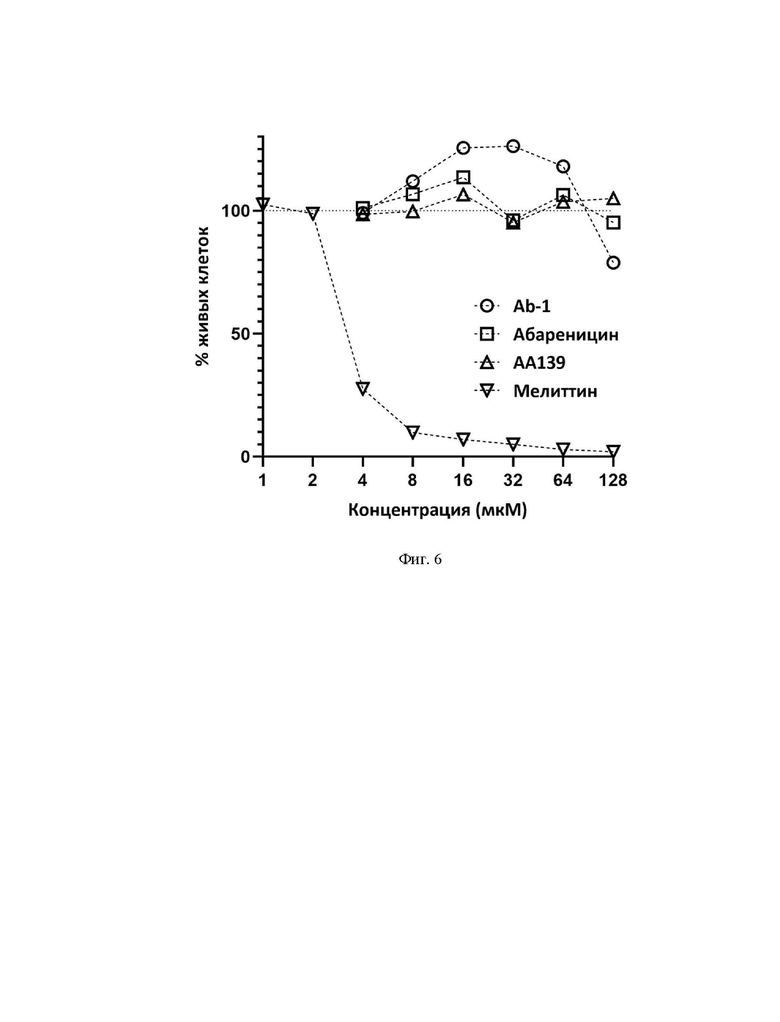
Фиг. 6. Цитотоксическое действие АМП на адгезионные клетки человека HEK293T.
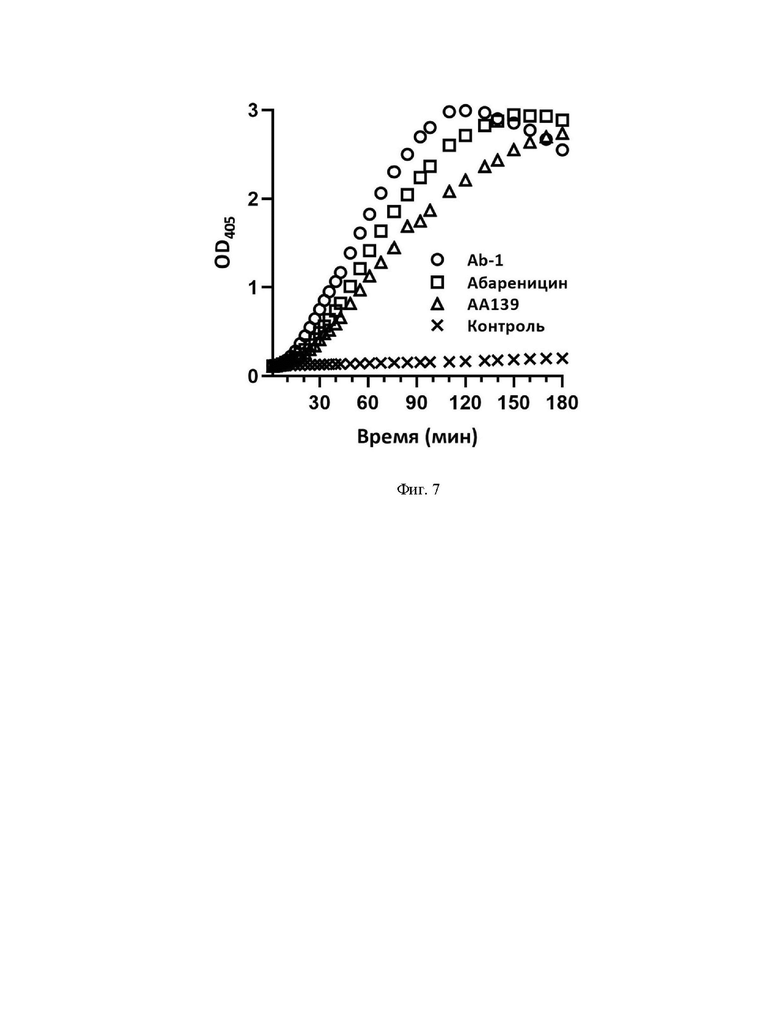
Фиг. 7. Фотометрическая оценка повышения проницаемости цитоплазматической мембраны бактерий E. coli ML-35p, вызванной АМП.
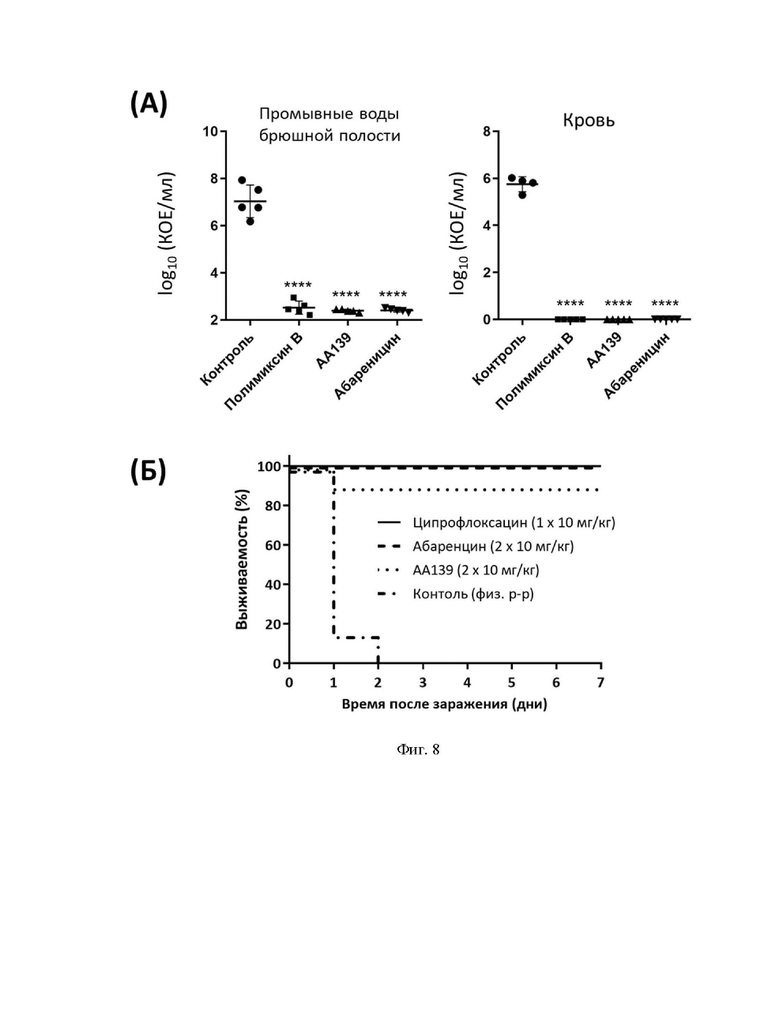
Фиг. 8. Эффективность антибиотического действия новых рекомбинантных АМП на мышиных моделях эшерихиозного перитонита. (А) Среднее количество бактерий E. coli 3421 E/19 в крови и промывных водах брюшной полости мышей линии BALB/c через 6 ч после заражения и через 5 ч после однократного внутривенного введения АМП и полимиксина B. Данные приведены в виде средних значений с учетом стандартного отклонения (**** достоверные различия с контролем без лечения, p ≤ 0,0001). (Б) Выживаемость мышей линии BALB/c при лечении летальной инфекции, вызываемой E. coli ATCC 25922, с использованием АМП или полимиксина B в присутствии муцина.
Осуществление изобретения
Задача изобретения заключается в расширении спектра пептидных антибиотиков, обладающих антибактериальным действием, в том числе против бактерий с множественной лекарственной устойчивостью, при низком уровне цитотоксического и гемолитического действия, то есть обладающих высокой антибактериальной селективностью. Для ее достижения был проведен рациональный дизайн модифицированных аналогов природного β-шпилечного пептида Ab-1, который был обнаружен по результатам биоинформатического анализа транскриптома морской полихеты Abarenicola pacifica [Safronova, V.N.; Bolosov, I.A.; Kruglikov, R.N.; Korobova, O.V.; Pereskokova, E.S.; Borzilov, A.I.; Panteleev, P.V.; Ovchinnikova, T.V. Novel β-Hairpin Peptide from Marine Polychaeta with a High Efficacy against Gram-Negative Pathogens. Marine Drugs 2022, 20, 517, doi:10.3390/md20080517]. Пептид Ab-1 обладает высокой антибактериальной активностью и широким спектром антимикробного действия, однако, вместе с тем, обладает умеренным гемолитическим действием в отношении эритроцитов человека. Ранее было показано, что аминокислотные замены гидрофобных остатков на аланин, аргинин или серин в области β-поворота схожих по структуре АМП зачастую приводят к повышению селективности антибактериального действия за счет снижения цитотоксических свойств молекулы [anteleev, P.V.; Bolosov, I.A.; Balandin, S.V.; Ovchinnikova, T.V. Design of Antimicrobial Peptide Arenicin Analogs with Improved Therapeutic Indices. J Pept Sci 2015, 21, 105-113, doi:10.1002/psc.2732; Panteleev, P.V.; Myshkin, M.Y.; Shenkarev, Z.O.; Ovchinnikova, T.V. Dimerization of the Antimicrobial Peptide Arenicin Plays a Key Role in the Cytotoxicity but Not in the Antibacterial Activity. Biochem Biophys Res Commun 2017, 482, 1320-1326, doi:10.1016/j.bbrc.2016.12.035; Panteleev, P.V.; Ovchinnikova, T.V. Improved Strategy for Recombinant Production and Purification of Antimicrobial Peptide Tachyplesin I and Its Analogs with High Cell Selectivity. Biotechnol Appl Biochem 2017, 64, 35-42, doi:10.1002/bab.1456]. Аналогичный подход был использован при введении аминокислотных замен в одном, двух или трех положениях полипептидной цепи Ab-1. Остатки цистеина, участвующие в образовании дисульфидных связей, не подвергались мутациям, чтобы сохранить целостность пептидного остова и вторичную структуру, необходимые для проявления антимикробной активности. Результаты испытаний биологической активности панели аналогов показали, что вариант с заменами двух аминокислотных остатков (Фиг. 1, выделены жирным шрифтом), названный абареницином (SEQ ID No: 1), по сравнению с пептидом дикого типа обладает как увеличенной антибактериальной активностью в отношении целого ряда грамотрицательных бактерий, так и сниженной цитотоксичностью в отношении нормальных клеток млекопитающих.
Получение плазмидной конструкции для гетерологической экспрессии абареницина в составе гибридного белка
Нуклеотидную последовательность SEQ ID No. 2, кодирующую целевой пептид (включающий N-концевой остаток метионина - сайт расщепления бромцианом), получают химико-ферментативным синтезом с помощью ПЦР и праймеров, несущих на 5’-концах сайты узнавания рестриктаз BglII и EcoRI. Олигонуклеотиды, используемые в ПЦР, синтезируют твердофазным фосфорамидитным методом с наращиванием олигонуклеотидной цепи в направлении от 3’-конца к 5’-концу с помощью защищенных фосфорамидитов - 5’-диметокситритил-N-ацил-2’-дезоксинуклеозид-3’-O-(β-цианэтилдиизопропиламино)-фосфитов, активированных тетразолом. Продукт амплификации гидролизуют указанными рестриктазами, очищают электрофорезом в 1,5% агарозном геле, целевую полосу ДНК выделяют из геля с помощью колонки с силикагелем и лигируют в экспрессионный вектор серии pET для дальнейшего биосинтеза целевого пептида в составе гибридного белка с модифицированным тиоредоксином А. С целью осуществления металлохелатной очистки гибридного белка от других компонентов клеточного лизата в его структуре был предусмотрен N-концевой фрагмент из восьми остатков гистидина. В результате лигазной реакции получают кольцевую ковалентно замкнутую ДНК размером 4067 п.н. (Фиг. 2). Продуктами лигазной реакции трансформируют компетентные клетки E. coli DH10B, приготовленные с помощью 0,1 М хлорида кальция. После трансформации суспензию бактерий смешивают с питательной средой LB, растят 60 мин при 37°C и высевают на чашки Петри с LB-агаром, содержащим 100 мкг/мл ампициллина.
Первичный отбор клонов, содержащих нужную плазмиду, осуществляют методом «ПЦР с клонов». Отобранные клоны подращивают в жидкой питательной среде и выделяют плазмидную ДНК, которую анализируют на наличие вставки с помощью секвенирования по Сэнгеру. По данным секвенирования отбирают плазмиду со вставкой, нуклеотидная последовательность которой полностью соответствует запланированной (SEQ ID No. 2).
Получение рекомбинантного абареницина
Проводят трансформацию компетентных клеток E. coli ClearColi® BL21(DE3), приготовленных с помощью 0,1 М хлорида кальция, плазмидным вектором, сборка которого описана в примере 1. Использование данного штамма сводит к минимуму риск контаминации препарата бактериальным эндотоксином, что позволяет использовать рекомбинантный пептид в биологических испытаниях на животных. После трансформации суспензию бактерий смешивают с питательной средой LB, растят 1 ч при 37°C и высевают на чашки Петри с LB-агаром, содержащим 100 мкг/мл ампициллина и 0,02 М глюкозы. Чашки инкубируют при 37°C в течение 18 ч.
Бактериологической петлей переносят выросшие колонии в 10 мл жидкой среды LB, содержащей 100 мкг/мл ампициллина, растят в течение 18 ч на термостатируемой качалке со скоростью вращения 220 об•мин-1 при температуре 37°C. Полученную культуру засевают в жидкую забуференную питательную среду LB, содержащую 0,02 М глюкозы, 100 мкг/мл ампициллина, 1 мМ MgSO4 и 0,1 мМ CaCl2. При этом начальная OD600 составляет 0,05. Индукцию биосинтеза гибридного белка осуществляют путем добавления изопропилтио-β-D-галактопиранозида (IPTG) к культуре клеток с оптической плотностью 1,0 до конечной концентрации 0,3 мМ. Культуру растят в течение 16 ч при температуре 30°С на термостатируемой качалке со скоростью вращения 220 об•мин-1. После экспрессии клетки осаждают центрифугированием, ресуспендируют в фосфатном буфере (pH 7,8) с добавлением 6М гуанидина гидрохлорида и 20 мМ имидазола при помощи стеклянного гомогенизатора Поттера и разрушают путем ультразвуковой обработки. Лизат клеток центрифугируют при 25000 g в течение 40 мин. Все работы по получению осветленного лизата проводят при температуре 4°С. Очистку гибридного белка, содержащего в качестве аффинной метки октагистидиновую последовательность, осуществляют с помощью металлохелатной хроматографии на препаративной колонке с Ni-NTA агарозой в денатурирующих условиях. Элюцию проводят повышением концентрации имидазола в буфере до 0,5 М. Собранную после очистки с помощью металлохелатной хроматографии фракцию, содержащую гибридный белок, титруют концентрированной соляной кислотой до значения pH 1,0, после чего добавляют бромциан (1 г бромциана на 1 г белка) и выдерживают при температуре 25°С в защищенном от света месте в течение 20 ч. Реакцию останавливают добавлением пятикратного объема деионизированной воды, после чего упаривают образцы на вакуумной центрифуге до исходного объема раствора и титруют до нейтральных значений pH. Финальную стадию очистки пептида проводят методом обращенно-фазовой ВЭЖХ (ОФ-ВЭЖХ) на колонке Reprosil-Pur C18-AQ в системе водных буферов, содержащих ацетонитрил и 0,1% ТФУ. Разделение происходит в линейном градиенте ацетонитрила от 5% до 80% за 60 мин. Выход полипептидов детектируют по изменению оптического поглощения при двух длинах волн: 214 и 280 нм (Фиг. 3А). Далее проводят повторную очистку с помощью ОФ-ВЭЖХ в аналогичной системе (Фиг. 3Б). Концентрацию водного раствора очищенного рекомбинантного абареницина определяют методом спектрофотометрии по поглощению при 280 нм на основе расчетного коэффициента экстинкции.
Определение молекулярной массы рекомбинантного пептида
Соответствие относительной молекулярной массы полученного рекомбинантного полипептида расчетному значению, а также индивидуальность очищенного вещества подтверждают с помощью масс-спектрометрического анализа на приборе Reflex III (Bruker Daltonics), оснащенном УФ-лазером с длиной волны 336 нм, с регистрацией положительных ионов в рефлекторном режиме. В качестве матрицы используют 2,5-дигидроксибензойную кислоту в смеси, содержащей 20% ацетонитрил и 0,1% трифторуксусную кислоту. Пик с m/z 2478,147 (Фиг. 4) соответствует молекулярному иону абареницина (расчетная молекулярная масса 2478,15), что свидетельствует об образовании двух дисульфидных связей.
Установление антибактериальных свойств
Антибактериальную активность АМП определяют методом двукратных серийных разведений в 96-луночных планшетах в жидкой питательной среде Мюллера-Хинтона с добавлением 0,9% NaCl (далее - среда МНВ) и инкубации с грамположительными или грамотрицательными бактериальными тестовыми культурами. Характеристика тест-штаммов приводят в Таблице 1.
* Штаммы, продуцирующие металло-бета-лактамазы (МβЛ)
В качестве антибактериальных соединений сравнения используют бета-шпилечные антимикробные пептиды Ab-1 и АА139, а также липопептидный антибиотик полимиксин В. Тест-культуры высевают из консерва в 10 мл среды МНВ без антибиотика и растят в течение 18 ч при 37°С и 220 об⋅мин-1. После этого аликвоту культуры объемом 300 мкл добавляют к 6 мл среды МНВ и инкубируют в термостатируемой качалке при 37°С до достижения культурой оптической плотности OD600 1,0. Далее методом последовательных разведений в 2× питательной среде МНВ доводят тестовые культуры до концентрации 106 КОЕ/мл. Аликвоты тест-культуры объемом 50 мкл добавляют к 50 мкл растворов пептидов, предварительно разведенных 0,1% раствором бычьего сывороточного альбумина (БСА) от 64 до 0,031 мкМ в пересчете на конечную концентрацию в лунке. После добавления культуры планшет инкубируют в течение 24 ч при 37°С и интенсивном перемешивании (1000 об⋅мин-1). Значения минимальных ингибирующих концентраций (МИК) определяются визуально и спектрофотометрически как минимальные концентрации пептидов, при которых отсутствует рост культуры. Эксперименты проводятся трижды в трехкратной повторности, причем итоговый МИК рассчитывается как медиана девяти полученных значений. Результаты, представленные в Таблице 2, показывают, что абареницин (SEQ ID No. 1) проявлял более высокую антибактериальную активность в отношении грамотрицательных микроорганизмов по сравнению с другими АМП и была сопоставима с таковой для полимиксина В: среднее геометрическое значений МИК для абареницина - 0,29 мкМ против 0,5 мкМ для АА139 и 0,52 мкМ для Ab-1. Среднее геометрическое значений МИК для полимиксина В составило 0,31 мкМ.
* - абареницин (SEQ ID No. 1)
** - полимиксин В
*** - среднее геометрическое значений МИК в отношении грамотрицательных штаммов
Тестирование гемолитической активности
Для тестирования гемолитической активности пептида используют свежевыделенные человеческие эритроциты. Для предотвращения свертывания к цельной крови добавляют цитратный буфер (pH 5,6). Кровь центрифугируют в растворе фиколла и урографина плотностью 1,077 г/мл в течение 15 мин при 1500 об•мин-1. Фракцию эритроцитов отбирают со дна и трижды промывают двадцатью объемами изотонического натрий-фосфатного буфера (pH 7,4), последовательно осаждая эритроциты путем центрифугирования при 2000 об•мин-1 в течение 10 мин. После отмывки готовят 8% суспензию эритроцитов в изотоническом натрий-фосфатном буфере.
Для теста в 96-луночном планшете готовят серии двойных разведений исследуемого пептида от 64 до 0,25 мкМ (в пересчете на конечную концентрацию) объемом 50 мкл. После этого к раствору пептида добавляют по 50 мкл 8% суспензии эритроцитов. Планшет инкубируют в течение 1,5 ч при 37°С и перемешивании при 1000 об•мин-1. После инкубации планшеты центрифугируют в течение 15 мин при 3000 об•мин-1 для осаждения интактных эритроцитов. Далее аликвоты супернатанта переносят в другой планшет для измерения количества свободного гемоглобина. Определение количества гемоглобина в растворе осуществляют по поглощению раствора при 405 нм. В качестве отрицательного контроля (K-) используют супернатант, полученный после центрифугирования эритроцитов, инкубировавшихся в растворе натрий-фосфатного буфера без добавления пептидов. В качестве положительного контроля (K+) используют супернатант, полученный после центрифугирования эритроцитов, инкубировавшихся в 0,1% водном растворе неионогенного детергента Triton X-100, вызывающего их полный лизис. В качестве препарата сравнения используют α-спиральный известный цитолитический пептид мелиттин из яда медоносной пчелы Apis mellifera. Эксперименты проводят дважды с кровью одного и того же человека в трехкратной повторности. Процент гемолиза рассчитывают по формуле: Гемолиз (%) = (OD405 пробы - OD405 «K-»)×100%/(OD405 «K+» - OD405 «K-»). Результаты, представленные на Фиг. 5, показывают, что абареницин (SEQ ID No. 1) не обладает гемолитичекой активностью при концентрациях до 64 мкМ, а пептид дикого типа Ab-1 вызывал лизис около 20% эритроцитов при данной концентрации.
Тестирование цитотоксического действия
Тестирование проводят с помощью МТТ-метода, который основан на способности дегидрогеназ живых клеток восстанавливать 3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-2H-тетразолий бромид (МТТ-реагент) до нерастворимого в воде фиолетового кристаллического формазана. Для оценки цитотоксического эффекта АМП используют клеточную линию почек эмбриона человека (HEK293T). Клеточную линию высаживают в 96-луночные планшеты (по 10000 клеток в каждую лунку) и растят в среде DMEM/F-12 в течение 24 ч при 37°С в CO2-инкубаторе (5% CO2 в воздухе). Далее культуральную жидкость заменяют свежей средой, в которой предварительно растворяют тестируемый пептид. После инкубации в течение 24 ч в приведенных выше условиях в каждую лунку добавляют по 20 мкл раствора МТТ в ЗФР (5 г/л), после чего продолжают инкубацию в течение 4 ч. Аккуратно удаляют среду, добавляют в лунки по 100 мкл смеси диметилсульфоксида и этилового спирта (1:1) для растворения кристаллов формазана и измеряют оптическую плотность растворов при 570 нм с помощью планшетного спектрофотометра. Долю живых клеток определяют по формуле:
Выживаемость (%) = [(OD570 пробы - OD570 «K-»)×100%/(OD570 клетки без пептида - OD570 «K- »)],
где «K-» - фоновое поглощение лунки с растворителем. Эксперименты проводят дважды в трехкратной повторности. В отличие от контрольного пептида мелиттина, который является сильным цитолитиком, исследуемые АМП, включая абареницин (SEQ ID No. 1), не проявляли существенных цитотоксических эффектов в исследуемом диапазоне концентрации до 128 мкМ (Фиг. 6).
Измерение проницаемости цитоплазматической мембраны E. coli в реальном времени
Используемый в данном методе штамм E. coli ML-35p отличается отсутствием пермеазы лактозы и конститутивным синтезом β-галактозидазы в цитоплазме. О состоянии цитоплазматической мембраны бактерий судили по ее проницаемости в присутствии АМП для хромогенного маркера - о-нитрофенил-β-D-галактопиранозида (ONPG). Состав смеси в каждой лунке (200 мкл) планшета был следующим: 2,5 мМ ONPG, забуференный физиологический раствор (ЗФР, рН 7,4), 2,5×107 КОЕ/мл отмытых в ЗФР бактерий, АМП (4 мкМ). Контрольные пробы содержали вместо препаратов равные объемы воды. Для снижения неспецифической сорбции пептидов на низких концентрациях в лунки планшета предварительно добавляли по 200 мкл 0,1% БСА, инкубировали 60 мин и удаляли перед внесением тестируемых смесей. Пробы вносили в лунки 96-луночного планшета, инкубировали в течение 180 мин при 37°С и перемешивании. Оптическую плотность раствора измеряли с помощью планшетного спектрофотометра. Результаты, представленные на Фиг. 7, показывают, что абареницин (SEQ ID No. 1) обладает схожим с пептидом дикого типа Ab-1, а также АА139 механизмом антибактериального действия: все АМП в течение 100-150 мин нарушали целостность цитоплазматической мембраны клеток-мишеней. Полученные данные наряду с результатами, приведенными в Примере 5, также свидетельствуют о высокой селективности действия абареницина в отношении бактериальных мембран.
Изучение эффективности препаратов на инфицированных мышиных моделях
Изучение антибактериальной активности АМП в условиях in vivo проводили с помощью двух моделей острого эшерихиозного перитонита у мышей. В качестве модельных животных использовались мыши линии BALB/c (самки/самцы, 6-8 недель, вес 22-24 г). Первая модель была использована для выявления бактерицидного эффекта АМП (анализ снижения обсемененности тканей) при лечении инфекционного заболевания, вызванного внутрибрюшинным (в/бр) введением культуры штамма E. coli 3421 E/19, в сравнении с эффектом полимиксина В. Вирулентный штамм 3421 E/19 является клиническим изолятом и обладает гемолитической активностью. С целью повышения восприимчивости животных к инфекции у них вызывали индуцированный иммунодефицит. Для этого внутрибрюшинно в «-4-й» день животным вводили циклофосфамид в дозе 200 мг/кг, а в «-1-й» день - в дозе 100 мг/кг. Схема эксперимента приведена в таблице 3.
Животных подвергали эвтаназии методом декапитации. Для получения промывных вод брюшной полости мышам внутрибрюшинно вводили 2 мл стерильного физиологического раствора. Кровь на бактериологический анализ брали у мышей посмертно после декапитации. После этого готовили последовательные десятикратные разведения отобранных образцов и высевали по 0,1 мл на плотную питательную среду - агар «Эндо-ГРМ» - для определения концентрации бактериальных клеток.
Вторая модель была использована для изучения выживаемости животных при курсовом лечении с помощью АМП (2 введения) перитонита у мышей, вызванного внутрибрюшинным введением культуры штамма E. coli АТСС 25922 в присутствии 2,5% муцина в сравнении с ципрофлоксацином. В ходе эксперимента наблюдали за самочувствием животных и регистрировали их гибель. Умершие мыши были исследованы на наличие специфического возбудителя. На 7-й день всех выживших мышей эвтаназировали, вскрывали, высевали гомогенаты селезенки на плотную среду «Эндо-ГРМ» методом мазков-отпечатков для подтверждения эрадикации клеток патогена. Схема эксперимента приведена в таблице 4.
Полученные результаты по сравнительной эффективности пептидов абареницина и АА139 приведены на рисунке 8. Была показана высокая эффективность абареницина на обоих моделях: пептид в дозе 10 мг/кг вызывал достоверное снижение обсемененности крови и промывных вод брюшной полости в 105 раз, а также способствовал выживаемости 100% мышей. Лечение препаратом АА139 способствовало выживанию 7 из 8 животных в группе. Бактериологическое исследование выживших животных показало отсутствие у них возбудителя инфекции - бактерий E. coli. Таким образом, эффективность заявляемого пептида абареницина (SEQ ID No. 1) сопоставима с таковой для референсного пептида АА139, а также известных антибиотиков полимиксина В и ципрофлоксацина.
--->
Перечень последовательностей
<110> ИБХ РАН
<120> БЕТА-ШПИЛЕЧНЫЙ ПЕПТИД, ОБЛАДАЮЩИЙ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ В
ОТНОШЕНИИ БАКТЕРИЙ С МНОЖЕСТВННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ
<130> (Reference Number)
<160> 2
<170> PatentIn version 3.5
<210> 1
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Artificial Sequence
<400> 1
Gly Tyr Cys Phe Thr Ala Cys Ala Arg Arg Asn Gly Val Arg Ile Cys
1 5 10 15
Tyr Arg Arg Cys Asn
20
<210> 2
<211> 81
<212> DNA
<213> Artificial Sequence
<220>
<223> Artificial Sequence
<400> 2
AGATCTATGG GGTACTGCTT TACGGCATGT GCTCGTCGTA ATGGAGTCCG CATTTGCTAT 60
CGCCGCTGCA ATTAAGAATT C 81
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| БЕТА-ШПИЛЕЧНЫЙ ПОЛИПЕПТИД, ОБЛАДАЮЩИЙ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2624020C2 |
| ПЕПТИД НИКОМИЦИН ИЗ МОРСКОГО КОЛЬЧАТОГО ЧЕРВЯ NICOMACHE MINOR, ОБЛАДАЮЩИЙ АНТИМИКРОБНЫМ И ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ. | 2019 |
|
RU2721273C1 |
| Катионный пептид, проявляющий антибактериальные свойства | 2021 |
|
RU2778856C1 |
| ИДЕНТИФИКАЦИЯ ЛИЗИНОВ И ИХ ПРОИЗВОДНЫХ, ОБЛАДАЮЩИХ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ ПРОТИВ PSEUDOMONAS AERUGINOSA | 2018 |
|
RU2807688C2 |
| ПОЛИПЕПТИДЫ ЛИЗИНА, АКТИВНЫЕ ПРОТИВ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ | 2016 |
|
RU2724545C2 |
| Пептид, проявляющий антибактериальные и противоопухолевые свойства | 2019 |
|
RU2702661C1 |
| Модифицированный эндолизин и антибактериальные композиции на его основе для лечения инфекций, вызванных бактериями Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli | 2023 |
|
RU2813626C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против бактерий Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Salmonella typhi и Staphylococcus haemolyticus (варианты) | 2019 |
|
RU2730613C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против бактерий Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Salmonella typhi и Staphylococcus haemolyticus (варианты) | 2019 |
|
RU2730614C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против грамотрицательных бактерий: Pseudomonas aeruginosa, Acinetobacter baumannii, Klebsiella pneumoniae и Salmonella typhi (варианты) | 2019 |
|
RU2730615C1 |

Изобретение относится к области биотехнологии и может быть использовано в медицине и ветеринарии. Предложен новый бета-шпилечный антимикробный пептид абареницин, который был сконструирован путем введения двух аминокислотных замен в структуру природного пептида из морской полихеты Abarenicola pacifica. Абареницин обладает высокой антибактериальной активностью в отношении ключевых возбудителей внутрибольничных инфекций, в том числе штаммов с множественной лекарственной устойчивостью, а также эффективен при лечении острой эшерихиозной инфекции у мышей. Изобретение позволяет расширить спектр пептидных антибиотиков, обладающих антибактериальным действием, в том числе против бактерий с множественной лекарственной устойчивостью, при низком уровне цитотоксического и гемолитического действия, то есть обладающих высокой антибактериальной селективностью. 8 ил., 4 табл.
Бета-шпилечный пептид, обладающий антимикробной активностью в отношении грамотрицательных бактерий - возбудителей внутрибольничных инфекций, обладающих множественной лекарственной устойчивостью, а именно: Pseudomonas aeruginosa, Klebsiella pneumoniae, Acinetobacter baumanii, Escherichia coli, Enterobacter cloacae, Proteus mirabilis, имеющий аминокислотную последовательность SEQ ID NО: 1.
| SAFRONOVA V | |||
| N | |||
| et al., Novel β-Hairpin Peptide from Marine Polychaeta with a High Efficacy against Gram-Negative Pathogens, Mar Drugs, 2022, vol | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| ORLOV D | |||
| S | |||
| et al., Redesigning Arenicin-1, an Antimicrobial Peptide from the Marine Polychaeta Arenicola marina, by Strand Rearrangement or Branching, Substitution of Specific Residues, | |||
Авторы
Даты
2024-02-06—Публикация
2023-02-07—Подача