Изобретение относится к медицине, а именно к кардиохирургии, и может быть использовано для прогнозирования острой сердечной недостаточности после операций коронарного шунтирования (КШ).
Известен способ прогнозирования исходов операций коронарного шунтирования (RU 2719914 С1 опубл, 23.04.2020 Бюл. №12), включающий интраоперационное определение концентрации активной миелопероксидазы (МРО) в плазме крови. Рассчитывают показатель Р по формуле 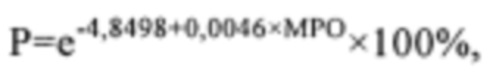 где МРО - концентрация активной миелопероксидазы, нг/мл и при значении Р более 1,2% прогнозируют неблагоприятный исход операции КШ. Способ обеспечивает возможность интраоперационного прогнозирования исходов КШ за счет интраоперационного определения концентрации активной МРО, являющейся маркером ишемически-реперфузионного изменения миокарда при операциях КШ, что позволяет своевременно корректировать хирургическую тактику лечения раньше, чем проявятся очевидные признаки синдрома малого сердечного выброса.
где МРО - концентрация активной миелопероксидазы, нг/мл и при значении Р более 1,2% прогнозируют неблагоприятный исход операции КШ. Способ обеспечивает возможность интраоперационного прогнозирования исходов КШ за счет интраоперационного определения концентрации активной МРО, являющейся маркером ишемически-реперфузионного изменения миокарда при операциях КШ, что позволяет своевременно корректировать хирургическую тактику лечения раньше, чем проявятся очевидные признаки синдрома малого сердечного выброса.
Техническим результатом заявленного изобретения является расширение арсенала средств прогнозирования острой сердечной недостаточности после операций КШ.
Заявленный технический результат достигается в способе прогнозирования исходов операций коронарного шунтирования, включающем интраоперационный забор венозной крови для лабораторного исследования сразу после завершения наложения шунтов, согласно которому определяют концентрацию лактоферрина в плазме крови, рассчитывают показатель Р по формуле
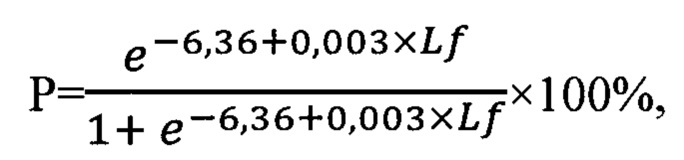
где Lf - концентрация лактоферрина, нг/мл; е - основание натурального логарифма, и при значении Р более 36% прогнозируют развитие синдрома малого сердечного выброса.
Способ обеспечивает возможность интраоперационного прогнозирования исходов КШ за счет интраоперационного определения концентрации лактоферрина, являющегося белком острой фазы, что позволяет своевременно корректировать хирургическую тактику лечения раньше, чем проявятся очевидные признаки синдрома малого сердечного выброса.
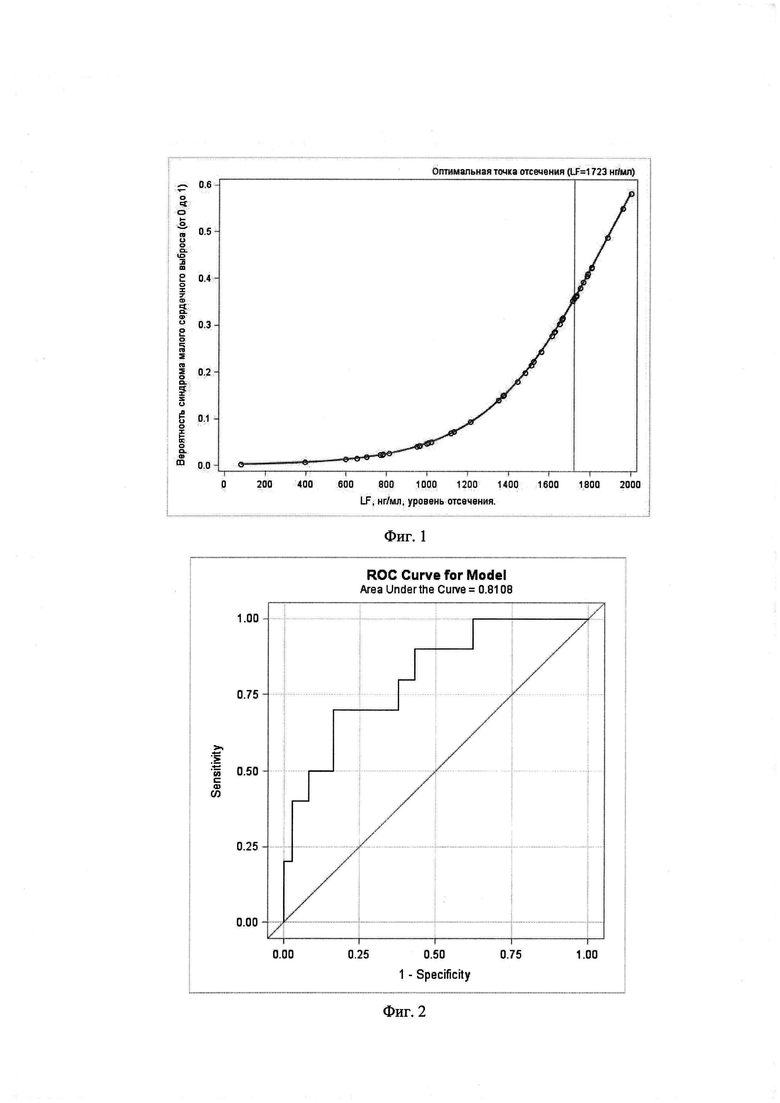
Изобретение поясняется следующими фигурами: фиг. 1 - кривая риска летального исхода в зависимости от концентрации лактоферрина (LF); фиг. 2 - ROC-кривая регрессионной модели: Sensitivity - чувствительность, Specifity - специфичность.
Способ был разработан в рамках проспективного нерандомизированного одноцентрового исследования Evaluating of Role of Myeloperoxidase in Prediction of Outcomes of Cardiac Surgery Procedures (ClinicalTrials.gov Identifier: NCT03786965), в которое было включено 128 пациентов. Выполнена оценка связи между интраоперационным уровнем лактоферрина и развитием синдрома малого сердечного выброса - сердечный индекс, измеренный инвазивным способом, в послеоперационном периоде менее 2,2, при плановых операциях коронарного шунтирования с искусственным кровообращением.
Критерии включения в исследование: возраст от 25 до 80 лет, наличие ишемической болезни сердца - стенокардия напряжения 3-4 ф.к., с доказанным многососудистым поражением коронарных артерий. Критерии исключения: отказ пациента, наличие патологии клапанов сердца, острый коронарный синдром.
Операции выполняли в плановом порядке по стандартной методике. Аппарат искусственного кровообращения Maquet HL-20, оксигенатор Affinity. Подключение экстракорпорального контура ИК производили по схеме аорта-правое предсердие - одна двухсекционная канюля. Заполнение аппарата: маннитол 15% -200 мл, гелофузин - 500 мл, стерофундин - 500 мл, NaHCO3 5% - 50 мл, транексам - 20 мл, антибиотик 2 г, гепарин 2 мл, инсулин - 10 Ед, дексаметазон 24 мг.Полная перфузия выполнялась с пережатием аорты при температуре 32 С. Кардиоплегия: раствор глюкозы 5% - 250 мл, MgSO4 25%» -20 мл, KCl 10%) - 30 мл, лидокаин 10% - 2 мл. Режим перфузии сердца кардиоплегией: антеградно в корень аорты (2/3) и ретроградно (1/3) - каждые 15 минут, после наложения дистальных анастомозов - дополнительно по шунтам.
Инструментальные исследования.
Электрокардиография (ЭКГ) до и после операции каждые 3-5 дней или чаще в зависимости от клинической ситуации. Критерии ишемии или инфаркта миокарда: вновь выявленное повышение сегмента ST в 2-х смежных отведениях или более, наличие нового зубца Q или впервые выявленная блокада левой ножки пучка Гиса.
Эхокардиография (ЭхоКГ) выполнялась всем пациентам до и после операции в соответствии с актуальными рекомендациями. Критерии ишемии или инфаркта миокарда: новые зоны гипокинезии или акинезии.
Коронаро-шунтография выполнялась при прогрессировании нестабильности гемодинамики, рефрактерной к вазопрессорной и инотропной поддержке.
Лабораторные исследования.
Забор венозной крови для лабораторного исследования лактоферрина в плазме крови осуществляли дважды: первичный - исследование до начала оперативного вмешательства, повторно - после завершения наложения шунтов. Методика определения концентрации лактоферрина в плазме переферической крови (Milstein С.(1975) Continuous cultures of fused cells secreting antibody of predefined specificity. Nature, 256 (5517), 495-497)
На первой стадии анализа проводили сорбцию лактоферрина из 10 мкл исследуемых образцов плазмы крови и серии образцов объемом 10 мкл с известной концентрацией лактоферрина (0; 31,3; 62,5; 125; 250; 500; 1000; 2000 нг/мл) на твердую фазу 96-луночного полистирольного планшета, поверхность которого предварительно покрывали специфическими моноклональными антителами против лактоферрина (клон ЗЕ11, 500 нг антител в лунке). После часа инкубации при перемешивании 350 об/мин в течение 1 часа при 37°С и промывки лунок 150 мМ NaCl, содержащим 0,05% твин-20 и 10 мМ натрий-боратного буфера (рН 8,0), переходили ко второй стадии. На второй стадии во все лунки добавляли 100 мкл меченных пероксидазой моноклональных антител против лактоферрина (10 нг/мл, 3B7-HRP). После часа инкубации при перемешивании 350 об/мин в течение 1 часа при 37°С и промывки лунок 150 мМ NaCl, содержащим 0,05% твин-20 и 10 мМ натрий-боратного буфера (рН 8,0), переходили к третьей стадии. На третьей стадии во все лунки планшета добавляли 100 мкл 0,5 мМ тетраметилбензидина и 2 мМ пероксида водорода в 100 мМ натрий-ацетатном буфере (рН 5,5), содержащем 8% ацетонитрила. Спустя 8 минут развития окраски пероксидазной метки реакцию останавливали, добавляя в лунки по 50 мкл 1 М серной кислоты. После регистрации поглощения при 450 нм в лунках планшета с помощью аппарата «CLARIOstar» (BMG LABTECH) по градуировочному графику определяли концентрацию лактоферрина в исследуемых образцах плазмы крови.
Расчетная формула получена в результате построения логистической регрессионной модели синдром малого сердечного выброса = концентрация лактоферрина (фиг. 1) на основании наблюдения 128 пациентов. Длительность послеоперационного наблюдения составила до 30 дней с момента операции. За период наблюдения из 128 пациентов синдром малого сердечного выброса развился у 15 человек. Статистическая обработка данных выполнялась в программе SAS Enterprise Guide 9.4.
Точность и специфичность рассчитаны с использованием индекса Юдена на основании ROC-анализа, выполненного по результатам построения логистической регрессии.
Точность способа определена по площади под ROC-кривой (фиг. 2) и составила 0,81.
Чувствительность и специфичность способа для выбранного порогового значения расчетного показателя Р более 36% составили 0,7 и 0,8 соответственно. Способ осуществляют, например, следующим образом.
Сразу после завершения наложения шунтов у пациента в операционной берут кровь из периферической вены.
Для достижения наилучшей воспроизводимости результатов иммуноферментного анализа при сорбции лактоферрина из образца плазмы и возможности выявления пероксидазной метки применяются моноклональные антитела против лактоферрина человека (клонов 3Е11 и 3В7), полученные из асцитной жидкости мышей после инокуляции гибридомами, продуцирующими данные антитела. Гибридомы получают по методу Милыптейна-Келера [Milstein С. (1975) Continuous cultures of fused cells secreting antibody of predefined specificity. Nature, 256 (5517), 495-497] путем слияния в присутствии полиэтиленгликоля клеток миеломы и лимфоцитов мыши, иммунизированной препаратом очищенного лактоферрина человека. Селекцию гибридом проводят на основе способности к продукции антител, связывающих лактоферрин при проведении иммуноферментного анализа. После проверки отсутствия конкуренции между антителами клонов 3Е11 и 3В7, первый используют для сорбции на твердую фазу, а второй - конъюгируют с пероксидазой, предварительно окисленной периодатом натрия. Применяемый для иммунизации мышей препарат очищенного лактоферрина человека получают в соответствии с описанным ранее методом хроматографии с использованием карбоксиметил-сефарозы и сефадекса G-75 Superfine (Sokolov A.V., Zakahrova Е.Т., Kostevich V.A., Samygina V.R., Vasilyev V.B. (2014) Lactoferrin, myeloperoxidase, and ceruloplasmin: complementary gearwheels cranking physiological and pathological processes. Biometals. 2014. V. 27. P. 815-828. DOI: 10.1007/s10534-014-9755-2)
Концентрацию лактоферрина в образцах плазмы крови оценивают по поглощению при 450 нм продукта окисления тетраметилбензидина в кислой среде, сравнивая его с градуировочной зависимостью, построенной для серии образцов, содержащих 0; 31,3; 62,5; 125; 250; 500; 1000; 2000 нг лактоферрина в мл. Концентрацию лактоферрина в образцах плазмы с учетом разведения выражают в нг/мл.
Рассчитывают показатель Р по формуле 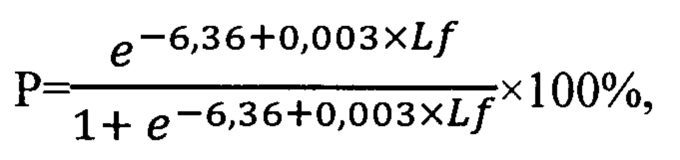 при значении Р более 36% прогнозируют синдром малого сердечного выброса после коронарного шунтирования.
при значении Р более 36% прогнозируют синдром малого сердечного выброса после коронарного шунтирования.
Способ подтверждается следующими клиническими примерами.
1. Пациент Э., 47 лет. Поступил с диагнозом ИБС. Стенокардия напряжения 3 ф.к. для оперативного лечения ИБС. Подтверждено многососудистое поражение коронарного русла, определены показания к операции коронарного шунтирования. Исходная тяжесть состояния пациента: Syntax Score II 29,5, Euroscore II 2,85, Index Charlson/Deyo 5. Выполнена операция аутовенозное аортокоронарное шунтирование правой коронарной артерии, ветви тупого края, диагональной ветви, маммарокоронарное шунтирование передней межжелудочковой ветви левой коронарной артерии в средней трети. Интраоперационная концентрация лактоферрина 1886 нг/мл, тропонин I 12,4 нг/мл, расчетный показатель Р=37,1% указывает на высокую вероятность развития синдрома малого сердечного выброса после операции. В послеоперационном периоде развился синдром малого сердечного выброса, потребовавший установки внутриаортальной баллонной контрпульсации. Длительность нахождения в реанимации 6 дней, длительность послеоперационной госпитализации 18 дней. Пациент благополучно выписан в удовлетворительном состоянии.
2. Пациент Т., 71 лет. Поступил с диагнозом ИБС. Стенокардия напряжения 3 ф.к. для оперативного лечения ИБС. Подтверждено многососудистое поражение коронарного русла, определены показания к операции коронарного шунтирования с искусственным кровообращением. Исходная тяжесть состояния пациента: Syntax Score II 36,3, Euroscore II 0,63, Index Charlson/Deyo 4.
Выполнена операция аутовенозное аорто-коронарное шунтирование правой коронарной артерии, огибающей ветви, маммарокоронарное шунтирование передней межжелудочковой ветви в условиях искусственного кровообращения и кровяной кардиоплегии. Интраоперационная концентрация лактоферрина 81,0 нг/мл, концентрация тропонина I 1,16 нг/мл, расчетный показатель Р=0,2%, что говорит о благоприятном прогнозе исхода операции. Операция успешно завершена. Длительность ИК 128 минут, время пережатия аорты 70 минут. Длительность нахождения в реанимации 2 дня, длительность послеоперационной госпитализации 8 дней. Послеоперационный период без осложнений. Пациент выписан в удовлетворительном состоянии.
3. Пациентка Ф., 63 года. Поступил с диагнозом ИБС. Стенокардия напряжения 3 ф.к. для оперативного лечения ИБС. Подтверждено многососудистое поражение коронарного русла, определены показания к операции КШ с ИК. Исходная тяжесть состояния пациента: Syntax Score II 21,9, Euroscore II 2,17, Index Charlson/Deyo 5. Выполнена операция аутовенозное аорто-коронарное шунтирование правой коронарной артерии, огибающей ветви и маммарокоронарное шунтирование передней межжелудочковой ветви в условиях искусственного кровообращения и кровяной кардиоплегии, время пережатия аорты 97 минут, время ИК 194 минут. Интраоперационная концентрация лактоферрина 2000 нг/мл, расчетный показатель Р=41,1%, что говорит о серьезном риске развития синдрома малого сердечного выброса. В послеоперационном периоде развились признаки инфаркта миокарда, кардиогенный шок, экстренно установлена внутриаортальная баллонная контрпульсация, выполнена рестернотомия, выявлен тромбоз шунта в бассейне правой коронарной артерии, выполнено коронарное шунтирование. Летальный исход на 2 сутки после операции, несмотря на проводимое лечение.
Способ позволяет интраоперационно прогнозировать развитие острой сердечной недостаточности после операции коронарного шунтирования за счет интраоперационного определения концентрации лактоферрина, являющегоcя белком острой фазы. Это позволяет своевременно корректировать хирургическую тактику лечения раньше, чем проявятся очевидные признаки синдрома малого сердечного выброса.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования исходов операций коронарного шунтирования | 2019 |
|
RU2719914C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА НЕБЛАГОПРИЯТНОГО ИСХОДА У ПАЦИЕНТОВ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА В ТЕЧЕНИЕ ГОДА ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ | 2019 |
|
RU2704956C1 |
| ТАКТИКА ЛЕЧЕНИЯ БОЛЬНЫХ С КРИТИЧЕСКОЙ ИШЕМИЕЙ НИЖНИХ КОНЕЧНОСТЕЙ И МНОГОСОСУДИСТЫМ ПОРАЖЕНИЕМ КОРОНАРНОГО РУСЛА | 2014 |
|
RU2553429C1 |
| Способ прогнозирования развития фибрилляции предсердий после операции коронарного шунтирования у пациентов низкого послеоперационного риска | 2023 |
|
RU2811647C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ НЕБЛАГОПРИЯТНЫХ СЕРДЕЧНО-СОСУДИСТЫХ СОБЫТИЙ В ТЕЧЕНИЕ 12 МЕСЯЦЕВ ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ | 2024 |
|
RU2830502C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ОСЛОЖНЕНИЙ В РАННЕМ ГОСПИТАЛЬНОМ ПЕРИОДЕ У ПАЦИЕНТОВ ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2017 |
|
RU2642238C1 |
| Способ прогнозирования неблагоприятных сердечно-сосудистых событий у больных с хронической сердечной недостаточностью ишемической этиологии в течение года после аортокоронарного шунтирования | 2022 |
|
RU2801160C1 |
| Способ определения вероятности окклюзий коронарных шунтов у мужчин с сахарным диабетом 2 типа | 2019 |
|
RU2702865C1 |
| Способ интраоперационного прогнозирования высокого риска ранней дисфункции коронарных шунтов по флоуметрической оценке резерва кровотока | 2023 |
|
RU2813797C1 |
| СПОСОБ ПОЛНОЙ МАЛОИНВАЗИВНОЙ ЭНДОСКОПИЧЕСКИ АССИСТИРОВАННОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА ПРИ МНОГОСОСУДИСТОМ АТЕРОСКЛЕРОТИЧЕСКОМ ПОРАЖЕНИИ КОРОНАРНОГО РУСЛА | 2019 |
|
RU2723751C1 |
Изобретение относится к медицине, а именно к кардиохирургии. Выполняют интраоперационный забор венозной крови для лабораторного исследования сразу после завершения наложения шунтов, определяют концентрацию лактоферрина в плазме крови, рассчитывают показатель Р по оригинальной формуле. И при значении Р более 36% прогнозируют развитие синдрома малого сердечного выброса. Способ позволяет интраоперационно прогнозировать развитие острой сердечной недостаточности после операции коронарного шунтирования за счет интраоперационного определения концентрации лактоферрина, являющегоя белком острой фазы. Это позволяет своевременно корректировать хирургическую тактику лечения раньше, чем проявятся очевидные признаки синдрома малого сердечного выброса. 2 ил., 3 пр.
Способ прогнозирования синдрома малого сердечного выброса после операций коронарного шунтирования, включающий интраоперационный забор венозной крови для лабораторного исследования сразу после завершения наложения шунтов, отличающийся тем, что определяют концентрацию лактоферрина в плазме крови, рассчитывают показатель P по формуле
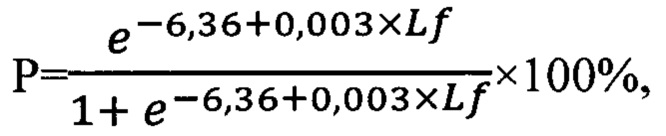
где Lƒ - концентрация лактоферрина, нг/мл; e - основание натурального логарифма, и при значении P более 36% прогнозируют развитие синдрома малого сердечного выброса.
| Белоконева К | |||
| П., Прогностическое значение лактоферрина и цитокинов в оценке неблагоприятных исходов у больных с Q-образующим инфарктом миокарда, умерших от острой сердечной недостаточности, Кардиология: Новости | |||
| Мнения | |||
| Обучение, 2016, 3 (10), pp | |||
| Фальцовая черепица | 0 |
|
SU75A1 |
| Транспортер | 1932 |
|
SU35661A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СНИЖЕНИЯ СОКРАТИТЕЛЬНОЙ СПОСОБНОСТИ ПРАВОГО ЖЕЛУДОЧКА В ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ У ПАЦИЕНТОВ ПЕРЕНЕСШИХ КОРОНАРНОЕ ШУНТИРОВАНИЕ В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2014 |
|
RU2563958C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ЖИЗНЕУГРОЖАЮЩИХ ОСЛОЖНЕНИЙ У ПАЦИЕНТОВ В ОСТРОМ ПЕРИОДЕ ИНФАРКТА МИОКАРДА | 2021 |
|
RU2767914C1 |
| Vengen IT, et | |||
Авторы
Даты
2024-03-11—Публикация
2023-06-26—Подача