ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[1] Данная заявка испрашивает приоритет по предварительной заявке США № 62/730471, поданной 12 сентября 2018 г., содержание которой полностью включено в данный документ.
Уровень техники
[2] Streptococcus pneumoniae остается основной причиной серьезных заболеваний, включая бактериемию, сепсис, менингит и пневмонию, среди детей и взрослых во всем мире. Заболеваемость и смертность среди младенцев, маленьких детей, пожилых людей и лиц с определенными основными заболеваниями высоки.
[3] S. pneumoniae представляет собой грамположительный инкапсулированный кокк, который колонизирует носоглотку примерно у 5-10% здоровых взрослых и 20-40% здоровых детей. Нормальная колонизация становится инфекционной, когда S. pneumoniae попадает в евстахиевы трубы, носовые пазухи, легкие, кровоток, оболочки головного мозга, суставные щели, кости и брюшную полость. Инфекция, вызванная S. pneumoniae, является наиболее частой причиной бактериемии, пневмонии, менингита, синусита и острого среднего отита [CDC, 2010].
[4] Пневмококковая инфекция может быть инвазивной или неинвазивной. Наиболее частая форма неинвазивного заболевания, небактериемическая пневмококковая пневмония, остается одной из наиболее частых причин госпитализации с пневмонией. Инвазивное пневмококковое заболевание (ИПЗ) определяют по S. pneumoniae, выделенной из обычно стерильного места (например, спинномозговой жидкости, крови, суставной жидкости, плевральной жидкости или перитонеальной жидкости). Самая высокая частота ИПЗ наблюдается в крайнем возрасте - у пожилых людей и у детей младше 2 лет. В США до появления первой пневмококковой вакцины S. pneumoniae ежегодно вызывала приблизительно 17000 случаев инвазивных заболеваний среди детей младше 5 лет, включая 700 случаев менингита и 200 случаев смерти [CDC, 2000]. Самые высокие показатели заболеваемости и смертности зарегистрированы в развивающихся странах, но бремя болезней также велико в промышленно развитых странах.
[5] S. pneumoniae имеет несколько факторов вирулентности, которые позволяют организму уклоняться от иммунной системы. Примеры включают полисахаридную капсулу, которая предотвращает фагоцитоз иммунными клетками хозяина, протеазы, которые ингибируют опсонизацию, опосредованную комплементом, и белки, вызывающие лизис клеток хозяина. В полисахаридной капсуле наличие сложных полисахаридов является основой для разделения пневмококков на разные серотипы. На сегодняшний день идентифицировано около 100 серотипов S. pneumoniae.
[6] В настоящее время в США доступны две вакцины против S. pneumoniae; PCV13 и PPSV23. PCV13 не может обеспечить защиту от большинства известных серотипов S. pneumoniae. Хотя PPSV23 содержит полисахаридные компоненты большего количества серотипов S. pneumoniae, чем PCV13, она индуцирует иммунный ответ, который не является ни длительным, ни анамнестическим при последующем заражении. PPSV23 защищает взрослых и пожилых людей от инвазивного пневмококкового заболевания; однако устойчивого эффекта в предотвращении пневмонии не наблюдалось [Gruber et al, 2008].
[7] Таким образом, существует медицинская потребность в вакцине, которая обеспечивает Т-клеточный иммунитет против широкого спектра серотипов S. pneumoniae.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[8] В настоящем изобретении рассматривается отсутствие подходящих технологий для предотвращения и/или лечения пневмококковой инфекции. Среди прочего, в настоящем изобретении рассматриваются проблемы, связанные с обеспечением вакцин с достаточной иммуногенностью для защиты от инвазивного пневмококкового заболевания и пневмонии путем индукции Т- и В-клеточного ответа, обеспечивающего иммунитет против широкого спектра серотипов S. pneumoniae, включая те серотипы, которые не включены в вакцине.
[9] Среди прочего, в настоящем изобретении предложены композиции и способы предотвращения и/или лечения пневмококковых инфекций у групп пациентов, которые в этом нуждаются.
[10] В некоторых вариантах осуществления вакцина содержит иммуногенный комплекс, причем иммуногенный комплекс содержит: (а) биотинилированный полисахаридный антиген; и (b) слитый белок, содержащий: (i) биотинсвязывающий фрагмент; и (ii) по меньшей мере один полипептидный антиген; где биотинилированный полисахаридный антиген нековалентно связан с биотинсвязывающим фрагментом слитого белка с образованием иммуногенного комплекса.
[11] В некоторых вариантах осуществления по меньшей мере один полипептидный антиген содержит: полипептид SP1500 или его антигенный фрагмент; или полипептид SP0785 или его антигенный фрагмент. В некоторых вариантах осуществления по меньшей мере один полипептидный антиген содержит: (а) первый полипептидный антиген, содержащий полипептид SP1500 или его антигенный фрагмент; и (b) второй полипептидный антиген, содержащий полипептид SP0785 или его антигенный фрагмент.
[12] В некоторых вариантах осуществления биотинилированный полисахаридный антиген содержит полисахарид Streptococcus pneumoniae. В некоторых вариантах осуществления биотинилированный полисахаридный антиген содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из следующих: 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48.
[13] В некоторых вариантах осуществления биотинилированный полисахаридный антиген содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F.
[14] В некоторых вариантах осуществления биотинилированный полисахаридный антиген содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F, и 33F.
[15] В некоторых вариантах осуществления биотинилированный полисахаридный антиген содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F и 20B.
[16] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: (а) множество биотинилированных полисахаридных антигенов, причем множество содержит полисахаридные антигены одного или более Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48; и (b) множество слитых белков, причем каждый слитый белок содержит (i) биотинсвязывающий фрагмент; (ii) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (iii) второй полипептидный антиген, содержащий аминокислотную последовательность, который на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент; причем каждый из первого множества биотинилированных полисахаридных антигенов нековалентно связан с биотинсвязывающим фрагментом одного или более из множества слитых белков с образованием иммуногенного комплекса.
[17] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: (а) множество биотинилированных полисахаридных антигенов, причем множество содержит полисахаридные антигены одного или более Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F; и (b) множество слитых белков, причем каждый слитый белок содержит (i) биотинсвязывающий фрагмент; (ii) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (iii) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент; причем каждый из первого множества биотинилированных полисахаридных антигенов нековалентно связан с биотинсвязывающим фрагментом одного или более из множества слитых белков с образованием иммуногенного комплекса.
[18] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: (а) множество биотинилированных полисахаридных антигенов, причем множество содержит полисахаридные антигены каждого из серотипов Streptococcus pneumoniae 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F; и (b) множество слитых белков, причем каждый слитый белок содержит (i) биотинсвязывающий фрагмент; (ii) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (iii) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент; причем каждый из первого множества биотинилированных полисахаридных антигенов нековалентно связан с биотинсвязывающим фрагментом одного или более из множества слитых белков с образованием иммуногенного комплекса.
[19] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: (а) множество биотинилированных полисахаридных антигенов, причем множество содержит полисахаридные антигены одного или более Streptococcus pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F, и 33F; и (b) множество слитых белков, причем каждый слитый белок содержит (i) биотинсвязывающий фрагмент; (ii) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (iii) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент; причем каждый из первого множества биотинилированных полисахаридных антигенов нековалентно связан с биотинсвязывающим фрагментом одного или более из множества слитых белков с образованием иммуногенного комплекса.
[20] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: (а) множество биотинилированных полисахаридных антигенов, причем множество содержит полисахаридные антигены каждого из серотипов Streptococcus pneumoniae 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F, и 33F; и (b) множество слитых белков, причем каждый слитый белок содержит (i) биотинсвязывающий фрагмент; (ii) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (iii) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент; причем каждый из первого множества биотинилированных полисахаридных антигенов нековалентно связан с биотинсвязывающим фрагментом одного или более из множества слитых белков с образованием иммуногенного комплекса.
[21] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: (а) множество биотинилированных полисахаридных антигенов, причем множество содержит полисахаридные антигены одного или более Streptococcus pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, и 20B; и (b) множество слитых белков, причем каждый слитый белок содержит (i) биотинсвязывающий фрагмент; (ii) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (iii) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент; причем каждый из первого множества биотинилированных полисахаридных антигенов нековалентно связан с биотинсвязывающим фрагментом одного или более из множества слитых белков с образованием иммуногенного комплекса.
[22] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: (а) множество биотинилированных полисахаридных антигенов, причем множество содержит полисахаридные антигены каждого из серотипов Streptococcus pneumoniae 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, и 20B; и (b) множество слитых белков, причем каждый слитый белок содержит (i) биотинсвязывающий фрагмент; (ii) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (iii) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент; причем каждый из первого множества биотинилированных полисахаридных антигенов нековалентно связан с биотинсвязывающим фрагментом одного или более из множества слитых белков с образованием иммуногенного комплекса.
[23] В некоторых вариантах осуществления вакцина содержит биотинсвязывающий фрагмент, причем биотинсвязывающий фрагмент представляет собой полипептид, который имеет или содержит аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 1, или его биотинсвязывающий фрагмент; или полипептид, который имеет или содержит аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере, 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 2, или его биотинсвязывающий фрагмент. В некоторых вариантах осуществления вакцина содержит слитый белок, который представляет собой или содержит аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 6. В некоторых вариантах осуществления вакцина содержит слитый белок CP1.
[24] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих один или более видов иммуногенных комплексов, причем вид относится к комплексам, содержащим полисахаридный антиген одного серотипа Streptococcus pneumoniae. В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих два или более видов иммуногенных комплексов, причем вид относится к комплексам, содержащим полисахаридный антиген одного серотипа Streptococcus pneumoniae. В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих девять или более видов иммуногенных комплексов, причем вид относится к комплексам, содержащим полисахаридный антиген одного серотипа Streptococcus pneumoniae.
[25] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих пятнадцать или более видов иммуногенных комплексов, причем вид относится к комплексам, содержащим полисахаридный антиген одного серотипа Streptococcus pneumoniae.
[26] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих двадцать четыре или более видов иммуногенных комплексов, причем вид относится к комплексам, содержащим полисахаридный антиген одного серотипа Streptococcus pneumoniae.
[27] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: первый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 1, нековалентно связанный в комплекс со слитым белком; второй вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 2, нековалентно связанный в комплекс со слитым белком; третий вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 3, нековалентно связанный в комплекс со слитым белком; четвертый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 4, нековалентно связанный в комплекс со слитым белком; пятый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 5, нековалентно связанный в комплекс со слитым белком; шестой вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 6A, нековалентно связанный в комплекс со слитым белком; седьмой вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 6B, нековалентно связанный в комплекс со слитым белком; восьмой вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 7F, нековалентно связанный в комплекс со слитым белком; девятый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 8, нековалентно связанный в комплекс со слитым белком; десятый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 9N, нековалентно связанный в комплекс со слитым белком; одиннадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 9V, нековалентно связанный в комплекс со слитым белком; двенадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 10A, нековалентно связанный в комплекс со слитым белком; тринадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 11A, нековалентно связанный в комплекс со слитым белком; четырнадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 12F, нековалентно связанный в комплекс со слитым белком; пятнадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 14, нековалентно связанный в комплекс со слитым белком; шестнадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae serotype 15B, нековалентно связанный в комплекс со слитым белком; семнадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 17F, нековалентно связанный в комплекс со слитым белком; восемнадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 18C, нековалентно связанный в комплекс со слитым белком; девятнадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 19A, нековалентно связанный в комплекс со слитым белком; двадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 19F, нековалентно связанный в комплекс со слитым белком; двадцать первый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 20B, нековалентно связанный в комплекс со слитым белком; двадцать второй вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 22F, нековалентно связанный в комплекс со слитым белком; двадцать третий вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 23F, нековалентно связанный в комплекс со слитым белком; двадцать четвертый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 33F, нековалентно связанный в комплекс со слитым белком; причем каждый слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94% по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентичную SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентичную SEQ ID NO: 4, или его антигенный фрагмент; и при этом каждый из биотинилированных полисахаридных антигенов с первого по двадцать четвертый нековалентно связан с биотинсвязывающим фрагментом по меньшей мере одного слитого белка с образованием иммуногенных комплексов.
[28] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: первый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 1, нековалентно связанный в комплекс со слитым белком; второй вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 3, нековалентно связанный в комплекс со слитым белком; a третий вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 4, нековалентно связанный в комплекс со слитым белком; четвертый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 5, нековалентно связанный в комплекс со слитым белком; пятый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 6A, нековалентно связанный в комплекс со слитым белком; шестой вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 6B, нековалентно связанный в комплекс со слитым белком; седьмой вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 7F, нековалентно связанный в комплекс со слитым белком; восьмой вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 9V, нековалентно связанный в комплекс со слитым белком; девятый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 14, нековалентно связанный в комплекс со слитым белком; десятый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 18C, нековалентно связанный в комплекс со слитым белком; одиннадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 19A, нековалентно связанный в комплекс со слитым белком; двенадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 19F, нековалентно связанный в комплекс со слитым белком; тринадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 22F, нековалентно связанный в комплекс со слитым белком; четырнадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 23F, нековалентно связанный в комплекс со слитым белком; пятнадцатый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 33F, нековалентно связанный в комплекс со слитым белком; причем каждый слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94% по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентичную SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентичную SEQ ID NO: 4, или его антигенный фрагмент; и при этом каждый из биотинилированных полисахаридных антигенов с первого по пятнадцатый нековалентно связан с биотинсвязывающим фрагментом по меньшей мере одного слитого белка с образованием иммуногенных комплексов.
[29] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих: первый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 2, нековалентно связанный в комплекс со слитым белком; второй вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 8, нековалентно связанный в комплекс со слитым белком; a третий вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 9N, нековалентно связанный в комплекс со слитым белком; четвертый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 10A, нековалентно связанный в комплекс со слитым белком; пятый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 11A, нековалентно связанный в комплекс со слитым белком; шестой вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 12F, нековалентно связанный в комплекс со слитым белком; седьмой вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 15B, нековалентно связанный в комплекс со слитым белком; восьмой вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 17F, нековалентно связанный в комплекс со слитым белком; и девятый вид иммуногенного комплекса, содержащий биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 20B, нековалентно связанный в комплекс со слитым белком; причем каждый слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94% по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентичную SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентичную SEQ ID NO: 4, или его антигенный фрагмент; и при этом каждый из биотинилированных полисахаридных антигенов с первого по девятый нековалентно связан с биотинсвязывающим фрагментом по меньшей мере одного слитого белка с образованием иммуногенных комплексов.
[30] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, содержащих два или более видов иммуногенных комплексов, при этом каждый вид иммуногенных комплексов вносит стехиометрически равное по массе соотношение полисахаридного антигена.
[31] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, включающих два или более видов иммуногенных комплексов, причем по меньшей мере один вид иммуногенного комплекса вносит стехиометрически различное соотношение по массе полисахаридного антигена.
[32] В некоторых вариантах осуществления вакцина содержит множество иммуногенных комплексов, включающих два или более видов иммуногенных комплексов, при этом разные виды иммуногенных комплексов вносят стехиометрически различное соотношение по массе полисахаридного антигена.
[33] В некоторых вариантах осуществления вакцина содержит слитый белок, содержащий биотинсвязывающий фрагмент, причем биотинсвязывающий фрагмент представляет собой полипептид, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 1, или его биотинсвязывающий фрагмент; или полипептид, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 2, или его биотинсвязывающий фрагмент.
[34] В некоторых вариантах осуществления иммуногенный комплекс содержит слитый белок, содержащий биотинсвязывающий фрагмент, причем биотинсвязывающий фрагмент представляет собой полипептид, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 1, или его биотинсвязывающий фрагмент; или полипептид, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 2, или его биотинсвязывающий фрагмент.
[35] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae, нековалентно связанный со слитым белком, причем слитый белок содержит биотинсвязывающий фрагмент и по меньшей мере один полипептидный антиген.
[36] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген, причем биотинилированный полисахаридный антиген содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48.
[37] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген, причем биотинилированный полисахаридный антиген содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F.
[38] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген, причем биотинилированный полисахаридный антиген содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F и 33F.
[39] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген, причем биотинилированный полисахаридный антиген содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F и 20B.
[40] В некоторых вариантах осуществления иммуногенный комплекс содержит по меньшей мере один пептидный антиген, причем по меньшей мере один полипептидный антиген содержит полипептид SP1500 или его антигенный фрагмент; полипептид SP0785 или его антигенный фрагмент; или их комбинацию.
[41] В некоторых вариантах осуществления иммуногенный комплекс содержит по меньшей мере один полипептидный антиген, причем по меньшей мере один полипептидный антиген содержит: (а) первый полипептидный антиген, содержащий полипептид SP1500 или его антигенный фрагмент; и (b) второй полипептидный антиген, содержащий полипептид SP0785 или его антигенный фрагмент.
[42] В некоторых вариантах осуществления иммуногенный комплекс содержит по меньшей мере один пептидный антиген, причем по меньшей мере один полипептидный антиген содержит: (а) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентичную SEQ ID NO: 5, или его антигенный фрагмент; и (b) второй полипептидный антиген, содержащий аминокислотную последовательность на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[43] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 1, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[44] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 2, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[45] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 3, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[46] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 4, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[47] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 5, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[48] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 6A, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[49] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 6B, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[50] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 7F, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[51] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 8, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[52] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 9N, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[53] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 9V, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[54] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 10A, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[55] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 11A, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[56] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 12F, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4 , или его антигенный фрагмент.
[57] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 14, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[58] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 15B, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[59] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 17F, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[60] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 18C, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[61] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 19A, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[62] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 19F, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[63] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 20B, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[64] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 22F, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[65] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 23F, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность , которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[66] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинилированный полисахаридный антиген Streptococcus pneumoniae серотипа 33F, нековалентно связанный со слитым белком, причем слитый белок содержит (а) биотинсвязывающий фрагмент; (b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по меньшей мере 99,5% идентична SEQ ID NO: 5, или его антигенный фрагмент; и (c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент.
[67] В некоторых вариантах осуществления иммуногенный комплекс содержит биотинсвязывающий фрагмент, причем биотинсвязывающий фрагмент представляет собой полипептид, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 1, или его биотинсвязывающий фрагмент; или полипептид, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 2, или его биотинсвязывающий фрагмент.
[68] В некоторых вариантах осуществления иммуногенный комплекс содержит слитый белок и полисахаридный антиген, причем соотношение слитого белка к полисахаридному антигену в комплексе составляет около 1:1, около 2:1, около 3:1, около 4:1, около 5:1, около 6:1, около 7:1, около 8:1, около 9:1 или около 10:1 по массе. В некоторых вариантах осуществления вакцина содержит один или более иммуногенных комплексов, описанных в данном документе.
[69] В некоторых вариантах осуществления фармацевтическая композиция содержит вакцину или вакцинную композицию, описанные в данном документе, и фармацевтически приемлемый носитель. В некоторых вариантах осуществления фармацевтическая композиция содержит иммуногенный комплекс, описанный в данном документе, и фармацевтически приемлемый носитель. В некоторых вариантах осуществления описанная в данном документе фармацевтическая композиция содержит один или более адъювантов. В некоторых вариантах осуществления один или более адъювантов представляют собой или содержат фактор костимуляции.
[70] В некоторых вариантах осуществления один или более адъювантов выбраны из группы, состоящей из фосфата алюминия, гидроксида алюминия и фосфатированного гидроксида алюминия. В некоторых вариантах осуществления изобретения один или более адъювантов представляют собой или содержат фосфат алюминия. В некоторых вариантах осуществления описанная в данном документе фармацевтическая композиция составлена для инъекции.
[71] В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, индуцирует иммунный ответ. В некоторых вариантах осуществления иммунный ответ включает врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ включает образование антител или ответ В-клеток. В некоторых вариантах осуществления иммунный ответ включает ответ CD4+ Т-клеток (например, ответ TH1, TH2, или TH17), ответ CD8+ T-клеток, ответ CD4+ и CD8+ T-клеток, или ответ CD4-/CD8- T-клеток. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток и (ii) ответ T-клеток. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток, (ii) ответ T-клеток и (iii) врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ направлен на по меньшей мере один полисахаридный антиген или на по меньшей мере один полипептидный антиген слитого белка. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток на по меньшей мере один полисахаридный антиген и (ii) ответ CD4+ T-клеток (например, TH1, TH2, или TH17), ответ CD8+ T-клеток, ответ CD4+ и CD8+ Т-клеток или ответ CD4-/CD8- Т-клеток на по меньшей мере один полипептид слитого белка. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток на по меньшей мере один полисахаридный антиген и (ii) образование антител или ответ B-клеток на по меньшей мере один полипептид слитого белка. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток на по меньшей мере один полисахаридный антиген и (ii) образование антител или ответ B-клеток и ответ CD4+ T-клеток, включая ответ TH1, TH2, или TH17, ответ CD8+ Т-клеток, ответ CD4+ и CD8+ Т-клеток или ответ CD4-/CD8- Т-клеток на по меньшей мере один полипептид слитого белка.
[72] В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, индуцирует опсонический/бактерицидный ответ против одного или более серотипов Streptococcus pneumoniae. В некоторых вариантах осуществления такой опсонический/бактерицидный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, при этом фармацевтическая композиция, описанная в данном документе, содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такой опсонический/бактерицидный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, при этом фармацевтическая композиция, описанная в данном документе, не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такой опсонический/бактерицидный ответ может быть направлен против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления опсонический/бактерицидный ответ может включать продукцию антител, опсонизирующих один или более серотипов Streptococcus pneumoniae, что приводит к уничтожению такого серотипа(-ов) одним или более иммунными путями. В некоторых вариантах осуществления такой опсонический/бактерицидный ответ можно определить с помощью анализа опсонофагоцитирующей активности (OPA) или анализа опсонофагоцитирующей активности в концентрированной смеси (COPA), известные в данной области техники и/или описанные в данном документе. В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, ингибирует трансмиссию одного или более серотипов Streptococcus pneumoniae от одного субъекта к другому субъекту. В некоторых вариантах осуществления такое ингибирование трансмиссии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование трансмиссии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование трансмиссии может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[73] В некоторых вариантах осуществления изобретения при введении субъекту фармацевтическая композиция, описанная в данном документе, ингибирует или снижает частоту возникновения инвазивного пневмококкового заболевания (ИПЗ), связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование ИПЗ или снижение частоты возникновения ИПЗ может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование ИПЗ или снижение частоты возникновения ИПЗ может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование ИПЗ или снижение частоты возникновения ИПЗ может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, снижает степень тяжести инвазивного пневмококкового заболевания (ИПЗ), связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести ИПЗ может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести ИПЗ может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести ИПЗ может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[74] В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, ингибирует или снижает частоту возникновения бактериемии, сепсиса и/или менингита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения бактериемии, сепсиса и/или менингита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения бактериемии, сепсиса и/или менингита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения бактериемии, сепсиса и/или менингита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, снижает степень тяжести бактериемии, сепсиса и/или менингита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести бактериемии, сепсиса и/или менингита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести бактериемии, сепсиса и/или менингита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени частоты бактериемии, сепсиса и/или менингита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[75] В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, ингибирует или снижает частоту возникновения поражения органов, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения поражения органов может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения поражения органов может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения поражения органов может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, снижает степень тяжести поражения органа, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести поражения органов может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести поражения органов может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести поражения органа может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[76] В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, ингибирует или снижает частоту возникновения пневмонии, связанной с или индуцированной одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения пневмонии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения пневмонии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения пневмонии может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, снижает степень тяжести пневмонии, связанной с или индуцированной одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести пневмонии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести пневмонии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести пневмонии может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[77] В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, ингибирует или снижает частоту возникновения среднего отита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения среднего отита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения среднего отита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения среднего отита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, снижает степень тяжести среднего отита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести среднего отита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести среднего отита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести среднего отита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[78] В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, ингибирует или снижает частоту возникновения синусита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения синусита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения синусита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения синусита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, снижает степень тяжести синусита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести синусита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести синусита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести синусита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[79] В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, ингибирует колонизацию поверхности(-ей) слизистой оболочки одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование колонизации поверхности(-ей) слизистой оболочки быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингбирование колонизации поверхности(-ей) слизистой оболочки быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингбирование колонизации поверхности(-ей) слизистой оболочки может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления при введении субъекту фармацевтическая композиция, описанная в данном документе, ингибирует колонизацию носоглотки одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование колонизации носоглотки быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингбирование колонизации носоглотки быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингбирование колонизации носоглотки может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе фармацевтическая композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[80] В некоторых вариантах осуществления предложен способ изготовления вакцины, включающий нековалентное образование комплекса множества биотинилированных полисахаридных антигенов с множеством слитых белков, содержащих по меньшей мере один полипептидный антиген, выбранный из: полипептида SP1500 или его антигенного фрагмента; полипептида SP0785 или его антигенного фрагмента; или их комбинации. В некоторых вариантах осуществления множество биотинилированных полисахаридных антигенов содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из следующих:1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48. В некоторых вариантах осуществления множество биотинилированных полисахаридных антигенов содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F. В некоторых вариантах осуществления множество биотинилированных полисахаридных антигенов содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из каждого из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F. В некоторых вариантах осуществления множество биотинилированных полисахаридных антигенов содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F и 33F. В некоторых вариантах осуществления множество биотинилированных полисахаридных антигенов содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из каждого из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F, и 33F. В некоторых вариантах осуществления множество биотинилированных полисахаридных антигенов содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из одного или более из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F и 20B. В некоторых вариантах осуществления множество биотинилированных полисахаридных антигенов содержит полисахарид Streptococcus pneumoniae, имеющий серотип, выбранный из каждого из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F и 20B.
[81] В некоторых вариантах осуществления предложен способ иммунизации субъекта против инфекции и/или колонизации Streptococcus pneumoniae, при этом способ включает введение субъекту иммунологически эффективного количества вакцины, описанной в данном документе. В некоторых вариантах осуществления способ иммунизации субъекта против инфекции и/или колонизации Streptococcus pneumoniae включает введение субъекту иммунологически эффективного количества иммуногенного комплекса, описанного в данном документе. В некоторых вариантах осуществления способ иммунизации субъекта против инфекции и/или колонизации Streptococcus pneumoniae включает введение субъекту иммунологически эффективного количества фармацевтической композиции, описанной в данном документе.
[82] В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции вызывает иммунный ответ. В некоторых вариантах осуществления иммунный ответ включает врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ включает образование антител или ответ В-клеток. В некоторых вариантах осуществления иммунный ответ включает ответ CD4+Т-клеток (например, ответ TH1, TH2, или TH17), ответ CD8+ T-клеток, ответ CD4+ и CD8+ T-клеток, или ответ CD4-/CD8- T-клеток. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток и (ii) ответ T-клеток. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток, (ii) ответ T-клеток и (iii) врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ направлен на по меньшей мере один полисахаридный антиген или на по меньшей мере один полипептид слитого белка. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток на по меньшей мере один полисахаридный антиген и (ii) ответ CD4+ T-клеток (например, TH1, TH2, или TH17), ответ CD8+ T-клеток, ответ CD4+ и CD8+ Т-клеток или ответ CD4-/CD8- Т-клеток на по меньшей мере один полипептид слитого белка. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток на по меньшей мере один полисахаридный антиген и (ii) образование антител или ответ B-клеток на по меньшей мере один полипептид слитого белка. В некоторых вариантах осуществления иммунный ответ включает (i) образование антител или ответ B-клеток на по меньшей мере на один полисахаридный антиген и (ii) образование антител или ответ B-клеток и ответ CD4+ T-клеток, включая ответ TH1, TH2, или TH17, или ответ CD8+ T-клеток, ответ CD4+ и CD8+ T-клеток, или ответ CD4-/CD8- T-клеток на по меньшей мере один полипептид слитого белка.
[83] В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) индуцирует опсонический/бактерицидный ответ против одного или более серотипов Streptococcus pneumoniae. В некоторых вариантах осуществления такой опсонический/бактерицидный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, при этом вакцина, иммуногенный комплекс или фармацевтическая композиция, описанные в данном документе, содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такой опсонический/бактерицидный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, при этом вакцина, иммуногенный комплекс или фармацевтическая композиция, описанные в данном документе, не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такой опсонический/бактерицидный ответ может быть направлен против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) ингибирует трансмиссию одного или более серотипов Streptococcus pneumoniae от одного субъекта к другому субъекту. В некоторых вариантах осуществления такое ингибирование трансмиссии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование трансмиссии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, при этом вакцина, иммуногенный комплекс или фармацевтическая композиция, описанные в данном документе, не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование трансмиссии может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[84] В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) ингибирует или снижает частоту возникновения инвазивного пневмококкового заболевания (ИПЗ), связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения ИПЗ может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения ИПЗ может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения ИПЗ может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) снижает степень тяжести инвазивного пневмококкового заболевания (ИПЗ), связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести ИПЗ может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести ИПЗ может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести ИПЗ может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[85] В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) снижает степень тяжести бактериемии, сепсиса и/или менингита, связанных с или индуцированных одним или несколькими серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения бактериемии, сепсиса и/или менингита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения бактериемии, сепсиса и/или менингита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения бактериемии, сепсиса и/или менингита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) снижает степень бактериемии, сепсиса и/или менингита, связанных с или индуцированных одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести бактериемии, сепсиса и/или менингита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести бактериемии, сепсиса и/или менингита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести бактериемии, сепсиса и/или менингита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[86] В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) ингибирует или снижает частоту возникновения поражения органа, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения поражения органов может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения поражения органов может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения поражения органов может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) снижает степень тяжести поражения органов, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести поражения органов может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести поражения органов может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести поражения органов может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[87] В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) ингибирует или снижает частоту возникновения пневмонии, связанной с или индуцированной одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения пневмонии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения пневмонии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения пневмонии может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) снижает степень тяжести пневмонии, связанной с или индуцированной одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести пневмонии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести пневмонии может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести пневмонии может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[88] В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) ингибирует или снижает частоту возникновения среднего отита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения среднего отита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения среднего отита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения среднего отита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) снижает степень тяжести среднего отита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести среднего отита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести среднего отита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести среднего отита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[89] В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) ингибирует или снижает частоту возникновения синусита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения синусита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения синусита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование или снижение частоты возникновения среднего отита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) снижает степень тяжести синусита, связанного с или индуцированного одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое снижение степени тяжести синусита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести синусита может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое снижение степени тяжести отита может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс, фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[90] В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) ингибирует колонизацию поверхности(-ей) слизистой оболочки одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование колонизации поверхности(-ей) слизистой оболочки быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование колонизации поверхности(-ей) слизистой оболочки может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, при этом вакцина, иммуногенный комплекс или фармацевтическая композиция, описанные в данном документе, не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование колонизации поверхности(-ей) слизистой оболочки может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления введение вакцины, иммуногенного комплекса или фармацевтической композиции (например, описанных и/или используемых в данном документе) ингибирует колонизацию носоглотки одним или более серотипами Streptococcus pneumoniae. В некоторых вариантах осуществления такое ингибирование колонизации носоглотки быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование колонизации носоглотки может быть направлено против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, при этом вакцина, иммуногенный комплекс или фармацевтическая композиция, описанные в данном документе, не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такое ингибирование колонизации носоглотки может быть направлено против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанные в данном документе вакцина, иммуногенный комплекс или фармацевтическая композиция (i) содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[91] В некоторых вариантах осуществления способов, описанных в данном документе, Streptococcus pneumoniae имеет серотип, выбранный из одного или более из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48. В некоторых вариантах осуществления Streptococcus pneumoniae имеет серотип, выбранный из одного или более из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления Streptococcus pneumoniae имеет серотип, выбранный из одного или более из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F, и 33F. В некоторых вариантах осуществления Streptococcus pneumoniae имеет серотип, выбранный из одного или более из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F и 20B.
[92] В некоторых вариантах осуществления субъекта подвергают иммунизации против инфекции и/или колонизации Streptococcus pneumoniae одной дозой вакцины. В некоторых вариантах осуществления субъекта подвергают иммунизации против инфекции и/или колонизации Streptococcus pneumoniae двумя дозами вакцины. В некоторых вариантах осуществления субъекта подвергают иммунизации против инфекции и/или колонизации Streptococcus pneumoniae тремя дозами вакцины.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[93] Настоящие идеи, описанные в данном документе, будут более полно понятны из следующего описания различных иллюстративных вариантов осуществления при чтении вместе с сопроводительными графическими материалами. Следует понимать, что графические материалы, описанные ниже, предназначены только для целей иллюстрации и никоим образом не предназначены для ограничения объема настоящих идей.
[94] На Фиг.1 представлено схематическое изображение иллюстративной системы презентации множественных антигенов (MAPS). В показанном иллюстративном варианте осуществления иммуногенные комплексы MAPS содержат один или более полипептидных антигенов, слитых с биотинсвязывающим белком ризавидином, или его биотинсвязывающим доменом или биотинсвязывающим фрагментом, и биотинилированный антигенный полисахарид. На этой фигуре каждый комплекс MAPS образуется между одним или более слитыми белками и биотинилированным полисахаридом путем нековалентного связывания усеченного ризавидина с биотином.
[95] На Фиг. 2 представлена схема иллюстративного слитого белка CP1. Такой иллюстративный слитый белок CP1 содержит биотинсвязывающий белок, такой как, например, усеченный белок ризавидин (например, аминокислоты 45-179 белка ризавидина дикого типа), первый линкер (например, линкер GGGGSSS), полипептид SP1500 (например, аминокислоты 27-278 полноразмерного полипептида SP1500 S. pneumoniae), второй линкер (например, аминокислотную последовательность AAA) и полипептид SP0785 (например, аминокислоты 33-399 полноразмерного полипептида S. pneumoniae SP0785). В некоторых вариантах осуществления слитый белок CP1 может дополнительно содержать детектируемую метку или метку для очистки (например, His-метку). Аминокислотная последовательность AAA может быть получена из сайта Not I плазмиды PET21/24b или может быть синтезированной. Для линкера GGGGSSS аминокислотная последовательность SSS может быть получена из сайта Sac I плазмиды PET21/24b с добавленной аминокислотной последовательностью GGGG для создания гибкого линкера с минимальными стерическими препятствиями. В качестве альтернативы можно синтезировать линкер GGGGSSS.
[96] На Фиг.3 представлена таблица, демонстрирующая иллюстративные структуры антигенных полисахаридов S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[97] На Фиг. 4 представлена схема иллюстративной конструкции pET24a(+) CP1.
[98] На Фиг. 5 представлена блок-схема, изображающая иллюстративный производственный процесс синтеза для слитого белка CP1. Иллюстративный полипептид CP1 представляет собой слитый белок, содержащий усеченный ризавидин [АК 45-179 полноразмерного белка ризавидина], первый линкер (например, линкер GGGGSSS), полипептид SP1500, второй линкер (например, аминокислотную последовательность AAA) и полипептид SP0785. ДСН-ПААГ-электрофорез: электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия.
[99] На Фиг. 6 представлена блок-схема, изображающая иллюстративный производственный процесс выделения для слитого белка CP1. Иллюстративный полипептид CP1 представляет собой слитый белок, содержащий усеченный ризавидин [АК 45-179 полноразмерного белка ризавидина], первый линкер (например, линкер GGGGSSS), полипептид SP1500, второй линкер (например, аминокислотную последовательность AAA) и полипептид SP0785. DS: лекарственная субстанция; ДСН-ПААГ-электрофорез: электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия; TFF: тангенциальная фильтрация потока.
[100] На Фиг. 7 представлена блок-схема, изображающая иллюстративный производственный процесс иммуногенных комплексов MAPS, включающий биотинилирование антигенных полисахаридов и сборку слитым белком CP1. MAPS: Система презентации множественных антигенов.
[101] Фиг. 8 включает панель A и панель B, которые представляют собой блок-схемы, изображающие иллюстративные производственные процессы для вакцины MAPS. Например, такие иллюстративные процессы могут быть использованы для производства вакцины MAPS24, содержащей иммуногенные комплексы MAPS, которые содержат капсульные полисахариды из 24 различных серотипов S. pneumoniae. DMAP: 4-диметиламинопиридин; MAPS: система презентации множественных антигенов; PS: полисахарид. † производственные анализы
[102] На Фиг. 9 показана иммуногенность иллюстративных составов 24-валентной вакцины MAPS24 по сравнению с 13-валентной вакциной Prevnar 13 после однократной дозы. На графике показаны титры серотипспецифических антител IgG к полисахаридам указанных серотипов S. pneumoniae, полученные из сывороток, собранных через две недели после первой иммунизации (P1) вакциной MAPS24 или Prevnar 13. Вакцина MAPS24, используемая для иммунизации, не имела адъюванта или была дополнена адъювантом пассивированным гидроксидом алюминия или фосфатом алюминия, как указано. Результаты выражены в виде соотношения средних геометрических титров антител IgG из сывороток MAPS24 к сывороткам Prevnar 13. Каждый кружок на графике представляет собой соотношение среднего геометрического титра указанной сыворотки MAPS24 против полисахарида(-ов) указанного серотипа S. pneumoniae (верхняя часть графика). Пунктирной линией представлено соотношение средних геометрических титров, равное 1. Планки погрешностей представляют собой ±95% доверительный интервал. Сокращения: 24v MAPS: 24-валентная вакцина MAPS24; AlPO4: фосфат алюминия; pAlOH: пассивированный гидроксид алюминия; соотношение GMT: среднее геометрическое соотношение титров.
[103] На Фиг. 10 показана иммуногенность иллюстративных составов 24-валентной вакцины MAPS24 по сравнению с 13-валентной вакциной Prevnar 13 после второй дозы. На графике показаны титры серотипспецифических антител IgG к полисахаридам указанных серотипов S. pneumoniae, полученные из сывороток, собранных через две недели после второй иммунизации (P2) вакциной MAPS24 или Prevnar 13. Вакцина MAPS24, используемая для иммунизации, не имела адъюванта или была дополнена адъювантом пассивированным гидроксидом алюминия или фосфатом алюминия, как указано. Результаты выражены в виде соотношения средних геометрических титров антител IgG из сывороток MAPS24 к сывороткам Prevnar 13. Каждый кружок на графике представляет собой соотношение средних геометрических титров указанной сыворотки MAPS24 против полисахарида(-ов) указанного серотипа S. pneumoniae (верхняя часть графика). Пунктирной линией представлено соотношение средних геометрических титров, равное 1. Планки погрешностей представляют собой ± 95% доверительный интервал. Сокращения: 24v MAPS: 24-валентная вакцина MAPS24; AlPO4: фосфат алюминия; pAlOH: пассивированный гидроксид алюминия; соотношение GMT: соотношение средних геометрических титров.
[104] На Фиг. 11 показана иммуногенность иллюстративных составов 15-валентной вакцины MAPS15 по сравнению с 13-валентной вакциной Prevnar 13 после однократной дозы. На графике показаны титры серотипспецифических антител IgG к полисахаридам указанных серотипов S. pneumoniae, полученные из сывороток, собранных через две недели после первой иммунизации (P1) вакциной MAPS15 или Prevnar 13. Вакцина MAPS15, используемая для иммунизации, не имела адъюванта или была дополнена адъювантом пассивированным гидроксидом алюминия или фосфатом алюминия, как указано. Результаты выражены в виде соотношения средних геометрических титров антител IgG из сывороток MAPS24 к сывороткам Prevnar 13. Каждый кружок на графике представляет собой соотношение средних геометрических титров указанной сыворотки MAPS24 против полисахарида(-ов) указанного серотипа S. pneumoniae (верхняя часть графика). Пунктирной линией представлено соотношение средних геометрических титров, равное 1. Планки погрешностей представляют собой ±95% доверительный интервал. Сокращения: 15v MAPS: 15-валентная вакцина MAPS15; AlPO4: фосфат алюминия; pAlOH: пассивированный гидроксид алюминия; соотношение GMT: среднее геометрическое соотношение титров.
[105] На Фиг. 12 показана иммуногенность иллюстративных составов 15-валентной вакцины MAPS15 по сравнению с 13-валентной вакциной Prevnar 13 после второй дозы. На графике показаны титры серотипспецифических антител IgG к полисахаридам указанных серотипов S. pneumoniae, полученные из сывороток, собранных через две недели после второй иммунизации (P2) вакциной MAPS15 или Prevnar 13. Вакцина MAPS15, используемая для иммунизации, не имела адъюванта или была дополнена адъювантом пассивированным гидроксидом алюминия или фосфатом алюминия, как указано. Результаты выражены в виде соотношения средних геометрических титров антител IgG из сывороток MAPS24 к сывороткам Prevnar 13. Каждый кружок на графике представляет собой соотношение средних геометрических титров указанной сыворотки MAPS24 против полисахарида(-ов) указанного серотипа S. pneumoniae (верхняя часть графика). Пунктирной линией представлено соотношение средних геометрических титров, равное 1. Планки погрешностей представляют собой ± 95% доверительный интервал. Сокращения: 15v MAPS: 15-валентная вакцина MAPS15; AlPO4: фосфат алюминия; pAlOH: пассивированный гидроксид алюминия; соотношение GMT: соотношение средних геометрических титров.
[106] На Фиг. 13 показана иммуногенность иллюстративных составов 24-валентных вакцин MAPS24 и 15-валентных MAPS15 по сравнению с 13-валентной вакциной Prevnar 13. На графике показаны титры серотипспецифических антител IgG против капсульного полисахарида репрезентативного S. pneumoniae серотипа 1, полученные из сывороток, собранных до иммунизации (P0) и в два момента времени после иммунизации вакцинами MAPS24, MAPS15 или Prevnar 13: P1=две недели после первой иммунизации, а P2=две недели после второй иммунизации. Вакцины, используемые для иммунизации, не имели адъюванта или была дополнена адъювантом пассивированным гидроксидом алюминия или фосфатом алюминия, как указано. Результаты выражаются в условных единицах на мл. Каждая вертикальная планка на графике демонстрирует средний геометрический титр антител IgG против капсульного полисахарида S. pneumoniae серотипа 1 для указанных сывороток (верхняя часть графика) в указанный момент времени (нижняя часть графика). Планки погрешностей представляют собой 95% доверительный интервал. Сокращения: CPS: капсульный полисахарид; Non-Adj: без адъювантов; 24V MAPS: 24-валентная вакцина MAPS24; 15V MAPS: 15-валентная вакцина MAPS15; AlPO4: фосфат алюминия; p-AlOH: пассивированный гидроксид алюминия.
[107] На Фиг. 14 показана иммуногенность иллюстративного состава 24-валентной вакцины MAPS24 по сравнению с 13-валентной вакциной Prevnar 13 после одной и двух доз. На графике показано соотношение индукции (кратность изменения от исходного уровня) для серотипспецифических антител IgG против полисахаридов S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. Сыворотку собирали до иммунизации (P0) и в два момента времени после иммунизации вакцинами MAPS24 или Prevnar 13: P1 (14-й день) = две недели после первой иммунизации и P2 (28-й день) = две недели после второй иммунизации. Каждая вертикальная планка на графике представляет соотношение индукции для средних геометрических титров антител IgG (P1/P0 или P2/P0) для указанных сывороток против полисахарида(-ов) указанного серотипа S. Pneumoniae (нижняя часть графика). Планки погрешностей представляют собой ± 95% доверительный интервал. Сокращения: PCV13: 13-валентная вакцина Prevnar 13; MAPS24: 24-валентная вакцина MAPS24.
[108] На Фиг. 15 показана иммуногенность иллюстративного состава 24-валентной вакцины MAPS24 по сравнению с 13-валентной вакциной Prevnar 13 после одной и двух доз. На графике показано соотношение индукции (кратность изменения от исходного уровня) для серотипспецифических антител IgG против полисахаридов S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F, и 33F. Сыворотки собирали до иммунизации (P0) и в два момента времени после иммунизации вакцинами MAPS24 или Prevnar 13: P1 (14-й день) = две недели после первой иммунизации, а P2 (28-й день) = две недели после второй иммунизации. Каждая вертикальная планка на графике представляет соотношение индукции для средних геометрических титров антител IgG (P1/P0 или P2/P0) для указанных сывороток против полисахарида(-ов) указанного серотипа S. pneumoniae (нижняя часть графика). Планки погрешностей представляют собой 95% доверительный интервал. Сокращения: PCV13: 13-валентная вакцина Prevnar 13; MAPS24: 24-валентная вакцина MAPS24.
[109] На Фиг. 16 показаны ответы TH17 на иллюстративные вакцины, содержащие иммуногенные комплексы MAPS. Вакцины, используемые для иммунизации, представляли собой 12-валентную вакцину MAPS12 на CP1, 6-валентную вакцину MAPS6 на CP1, 6-валентную вакцину MAPS6 на альтернативном слитом белке в комбинации с предыдущей 6-валентной вакциной MAPS6 на CP1 и инактивированную цельноклеточную вакцину против S. pneumoniae (WCB). Образцы периферической крови иммунизированных мышей стимулировали цельноклеточным антигеном S. pneumoniae (WCA; левая панель) или комбинацией белков SP1500 и SP0785 (правая панель). Ответы TH17 для стимулированных клеток проявляются секрецией ИЛ-17A в среде. Каждая точка на графике демонстрирует концентрацию секретируемого ИЛ-17A для одной мыши. Горизонтальные планки демонстрируют среднюю геометрическую концентрацию секретируемого ИЛ-17A для каждой группы. Данные были проанализированы с использованием U-критерия Манна-Уитни (***: p <0,001). Сокращения: BPL: бетапропиолактон; CP1: ризавидин [аминокислотные остатки 45-179] -GGGGSSS-SP1500-AAA-SP0785; CP2a: альтернативный слитый белок; MAPS: система презентации множественных антигенов; 12V CP1: 12-валентная вакцина MAPS12 на CP1; 6V CP1: 6-валентная вакцина MAPS6 на CP1; 6V CP2a: 6-валентная вакцина MAPS6 на CP2a; p-AlOH: пассивированный гидроксид алюминия.
[110] На Фиг. 17 показаны защитные эффекты иллюстративных вакцин, содержащих иммуногенные комплексы MAPS. На графике показана защита от колонизации S. pneumoniae после иммунизации указанными вакцинами и интраназального заражения S. pneumoniae серотипа 6B (полисахарид(-ы) которого(-ых) включены/не включены в вакцины). Вакцины, используемые для иммунизации, представляли собой 12-валентную вакцину MAPS12 на CP1, 6-валентную вакцину MAPS6 на CP1, 6-валентную вакцину MAPS6 на альтернативном слитом белке в комбинации с предыдущей 6-валентной вакциной MAPS6 на CP1 и инактивированную цельноклеточную вакцину против S. pneumoniae (WCB). Каждая точка на графике представляет КОЕ S. pneumoniae на назальный смыв для одной мыши. Горизонтальные планки представляют собой среднюю геометрическую величину КОЕ S. pneumoniae на назальный смыв для каждой группы. Данные были проанализированы с использованием U-критерия Манна-Уитни. Сокращения: BPL: бетапропиолактон; КОЕ: колониеобразующая единица; CP1: ризавидин [аминокислотные остатки 45-179] -GGGGSSS-SP1500-AAA-SP0785; CP2a: альтернативный слитый белок; MAPS: система презентации множественных антигенов; 12V CP1: 12-валентная вакцина MAPS12 на CP1; 6V CP1: 6-валентная вакцина MAPS6 на CP1; 6V CP2a: 6-валентная вакцина MAPS6 на CP2a; p-AlOH: пассивированный гидроксид алюминия.
[111] На Фиг. 18 показаны ответы TH17 на иллюстративные вакцины, содержащие иммуногенные комплексы MAPS. Вакцины, используемые для иммунизации, представляли собой (i) 24-валентную вакцину MAPS24 на CP1 (24V) в комбинации с адъювантом фосфатом алюминия (AlPO4) и (ii) 24-валентную вакцину MAPS на CP1 (24V) в комбинации с адъювантом пассивированным гидроксидом алюминия (p-AlOH). Спленоциты иммунизированных мышей стимулировали гибридом белков SP1500 и SP0785. Ответы TH17 для стимулированных клеток проявляются секрецией ИЛ-17A в среде. Каждая точка на графике демонстрирует концентрацию секретируемого ИЛ-17A для одной мыши. Горизонтальные планки демонстрируют среднюю геометрическую концентрацию секретируемого ИЛ-17A для каждой группы. Статистический анализ проводили по сравнению с контрольной группой p-AlOH с использованием U-критерия Манна-Уитни (***: p <0,001).
[112] На Фиг. 19 показаны защитные эффекты иллюстративных вакцин, содержащих иммуногенные комплексы MAPS. На графике показана защита от колонизации S. pneumoniae после иммунизации указанными вакцинами и интраназального заражения S. pneumoniae серотипа 6B (полисахарид(-ы) которого(-ых) включены/не включены в вакцины). Вакцины, используемые для иммунизации, представляли собой (i) 23-валентную вакцину MAPS23 (без серотипа 6B) с CP1 (23V) в комбинации с адъювантом фосфатом алюминия (AlPO4) и (ii) 23-валентную вакцину MAPS23 (без серотипа 6B) с CP1 (23V) в комбинации с адъювантом пассивированным гидроксидом алюминия (p-AlOH). Каждая точка на графике представляет собой количество колониеобразующих единиц (КОЕ) S. pneumoniae на назальный смыв для одной мыши. Горизонтальные планки представляют собой среднюю геометрическую величину КОЕ S. pneumoniae на назальный смыв для каждой группы. Статистический анализ проводили по сравнению с контрольной группой p-AlOH с использованием U-критерия Манна-Уитни (*: p=0,2, **: p=0,02).
[113] На Фиг. 20 показана иммуногенность иллюстративного состава 24-валентной вакцины MAPS24 по сравнению с 13-валентной вакциной Prevnar 13. На графике показаны титры антител IgG против цельноклеточного S. pneumoniae указанных серотипов, полисахариды которых не включены в вакцину MAPS24 или Prevnar 13 (невакцинные типы, NVT). Сыворотку собирали до иммунизации (P0) и через две недели после второй иммунизации (P2) вакциной MAPS24 или Prevnar 13. Результаты выражаются в условных единицах на мл. Каждая вертикальная планка на графике обозначает средний геометрический титр связывающих цельные клетки антител IgG для указанных сывороток против цельноклеточного S. pneumoniae указанного серотипа (нижняя часть графика). Планки погрешностей представляют собой ± 95% доверительный интервал. Сокращения: AU: условные единицы; Prevnar: 13-валентная вакцина Prevnar 13; MAPS24: 24-валентная вакцина MAPS24; *p <0,05 и **p <0,01 для теста согласованных пар Уилкоксона; н.з: статистически не значимо.
[114] На Фиг. 21 показана иммуногенность иллюстративного состава 24-валентной вакцины MAPS24 по сравнению с 13-валентной вакциной Prevnar 13 после двух доз. На графике соотношение индукции (кратность изменения от исходного уровня) антител IgG против цельноклеточного S. pneumoniae указанных серотипов, полисахариды которых не включены в вакцину MAPS24 или Prevnar 13 (невакцинные типы, NVT). Сыворотку собирали до иммунизации (P0) и через две недели после второй иммунизации (P2) вакциной MAPS24 или Prevnar 13. Каждая вертикальная полоса на графике представляет соотношение индукции для средних геометрических титров антител IgG (P2/P0) для указанных сывороток против цельноклеточного S. pneumoniae указанного серотипа (нижняя часть графика). Планки погрешностей представляет собой ± 95% доверительный интервал. Сокращения: Prevnar: 13-валентная вакцина Prevnar 13; MAPS24: 24-валентная вакцина MAPS24; P2/P0: титр IgG после второй иммунизации (P2), деленный на предиммунный титр (P0) IgG; **p<0,01 и ***p<0,001 для теста Манна-Уитни.
[115] На Фиг. 22 показано присутствие функциональных антител против репрезентативных невакцинных серотипов S. pneumoniae в иммунных сыворотках MAPS24 с использованием анализа опсонофагоцитарного уничтожения. S. pneumoniae серотипов 15A, 16F, 23A, 31, 35B и 35F, полисахариды которых не включены в вакцину MAPS24 или Prevnar 13, инкубировали отдельно в модифицированном анализе опсонофагоцитирующей активности в концентрированной смеси (COPA) с инактивированной нагреванием сывороткой иммунизированных кроликов с иллюстративным составом 24-валентной вакцины MAPS24. Присутствие функциональных антител подтверждается уничтожением инкубированных S. pneumoniae. Сыворотку собирали перед иммунизацией (P0) и через две недели после второй иммунизации (P2). Результаты выражены как процент уничтожающей активности, то есть процент снижения количества колониеобразующих единиц (КОЕ) S. pneumoniae после инкубации с иммунной (P2) сывороткой по сравнению с инкубацией с подобранной предиммунной (P0) сывороткой. Каждая вертикальная планка на панелях A-F представляет процент уничтожающей активности, наблюдаемой с указанным разведением иммунных сывороток MAPS24 (нижняя часть каждой панели) против указанного серотипа S. pneumoniae (верхняя часть каждой панели).
[116] На Фиг. 23 показано присутствие функциональных антител против репрезентативного невакцинного серотипа S. pneumoniae (например, серотипа 16F) в иммунных сыворотках MAPS24 по сравнению с иммунными сыворотками Prevnar 13 с использованием анализа опсонофагоцитарного уничтожения. S. pneumoniae серотипа 16F, полисахарид(-ы) которого включен/не включен в вакцину MAPS24 или Prevnar 13, инкубировали в модифицированном анализе опсонофагоцитирующей активности в концентрированной смеси (COPA) с инактивированной нагреванием сывороткой кроликов, иммунизированных иллюстративным составом 24-валентной вакцины MAPS24 или с Prevnar 13. Присутствие функциональных антител было показано путем уничтожения инкубированных S. pneumoniae. Сыворотку собирали перед иммунизацией (P0) и через две недели после второй иммунизации (P2). Результаты выражены как процент выживаемости, то есть процент снижения количества колониеобразующих единиц (КОЕ) S. pneumoniae после инкубации с иммунной (P2) сывороткой по сравнению с инкубацией с подобранной предиммунной (P0) сывороткой. Каждая вертикальная планка графиков представляет процент выживаемости S. pneumoniae серотипа 16F, наблюдаемый с иммунными сыворотками MAPS24 (панель A) или иммунными сыворотками Prevnar 13 (панель B) при указанном разведении (внизу каждого графика). Планки погрешностей представляют собой ± 95% доверительный интервал. Сокращения: Prevnar: 13-валентная вакцина Prevnar 13; MAPS24: 24-валентная вакцина MAPS24; *p <0,05 и **p <0,01 для теста согласованных пар Уилкоксона; н.з: статистически не значимо.
[117] На Фиг. 24 показано присутствие функциональных антител против репрезентативного невакцинного серотипа S. pneumoniae (например, серотипа 15А) в иммунных сыворотках MAPS24 по сравнению с иммунными сыворотками Prevnar 13 с использованием анализа опсонофагоцитарного уничтожения. S. pneumoniae серотипа 15А, полисахарид(-ы) которого включен/не включен в вакцину MAPS24 или Prevnar 13, инкубировали в модифицированном анализе опсонофагоцитирующей активности в концентрированной смеси (COPA) с инактивированной нагреванием сывороткой кроликов, иммунизированных иллюстративным составом 24 -валентной вакцины MAPS24 или с Prevnar 13. Присутствие функциональных антител было показано путем уничтожения инкубированных S. pneumoniae. Сыворотку собирали перед иммунизацией (P0) и через две недели после второй иммунизации (P2). Результаты выражены как процент выживаемости, то есть процент снижения количества колониеобразующих единиц (КОЕ) S. pneumoniae после инкубации с иммунной (P2) сывороткой по сравнению с инкубацией с подобранной предиммунной (P0) сывороткой. Каждая вертикальная планка графиков представляет процент выживаемости S. pneumoniae серотипа 15А, наблюдаемый с иммунными сыворотками MAPS24 (панель A) или иммунными сыворотками Prevnar 13 (панель B) при указанном разведении (внизу каждого графика). Планки погрешностей представляют собой ± 95% доверительный интервал. Сокращения: Prevnar: 13-валентная вакцина Prevnar 13; MAPS24: 24-валентная вакцина MAPS24; * p <0,05 и ** p <0,01 для теста согласованных пар Уилкоксона; нс: статистически не значимо.
[118] На Фиг. 25 показана специфичность функциональных антител против репрезентативного невакцинного серотипа S. pneumoniae (например, серотипа 16F), полисахарид(-ы) которого(-ых) включен/не включен в вакцину MAPS24. Специфичность функциональных антител оценивали с использованием варианта ингибирования модифицированном анализе опсонофагоцитирующей активности в концентрированной смеси (iCOPA), в котором иммунные сыворотки предварительно инкубируют со специфическим ингибирующим реагентом (например, очищенным слитым белком CP1), который ингибирует или конкурирует со связыванием функционального антитела к целевому антигену. Затем предварительно инкубированные сыворотки инкубируют с S. pneumoniae, чтобы определить, ингибируется ли гибель функциональными антителами. Кроликов иммунизировали иллюстративным составом 24-валентной вакцины MAPS24. Сыворотку собирали перед иммунизацией (P0) и через две недели после второй иммунизации (P2). Результаты выражены как процент уничтожающей активности, то есть процент снижения количества колониеобразующих единиц (КОЕ) S. pneumoniae после инкубации с иммунной (P2) сывороткой по сравнению с инкубацией с подобранной предиммунной (P0) сывороткой. Каждая вертикальная планка на графике представляет процент убивающей активности против S. pneumoniae серотипа 16F, наблюдаемой с иммунными сыворотками MAPS24, предварительно инкубированными, как указано, с очищенным слитым белком CP1 (+ CP1) или без ингибитора при указанном разведении (нижняя часть графика).
[119] На Фиг. 26 показано присутствие функциональных антител против репрезентативного невакцинного серотипа S. pneumoniae (например, серотипа 16F) в иммунных сыворотках SP1500 и SP0785 с использованием анализа опсонофагоцитарного уничтожения. S. pneumoniae серотипа 16F, полисахарид(-ы) которого включен/не включен в вакцину MAPS24 или Prevnar 13, инкубировали в модифицированном концентрированном опсонофагоцитарном анализе (COPA) с инактивированной нагреванием сывороткой кроликов, иммунизированных белками SP1500 или SP0785. Присутствие функциональных антител было показано путем уничтожения инкубированных S. pneumoniae. Сыворотку собирали перед иммунизацией (P0) и через две недели после третьей иммунизации (P3). Результаты выражены как процент уничтожающей активности, то есть процент снижения количества колониеобразующих единиц (КОЕ) S. pneumoniae после инкубации с иммунной (P3) сывороткой по сравнению с инкубацией с подобранной предиммунной (P0) сывороткой. Каждая вертикальная планка на графике представляет процент уничтожающей активности против S. pneumoniae серотипа 16F, наблюдаемой с указанными иммунными сыворотками SP1500 или SP0785 при указанном разведении.
Определения
[120] В этой заявке, если иное не ясно из контекста, (i) термин в единственном числе может быть подразумеваться «по меньшей мере один»; (ii) под термином «или» может подразумеваться «и/или»; (iii) термины «содержащий» и «включающий» можно понимать как включающие перечисленные компоненты или этапы, представленные сами по себе или вместе с одним или более дополнительными компонентами или этапами; и (iv) термины «около» и «приблизительно» можно понимать как допускающие стандартное отклонение, которое понятно специалистам в данной области; и (v) в случае приведения диапазонов, в них включены конечные точки.
[121] Около: Термин «около», когда он используется в данном документе по отношению к значению, относится к значению, которое в контексте аналогично значению, на которое имеется ссылка. В общем, специалисты в данной области техники, знакомые с контекстом, оценят соответствующую степень вариации, заключенную в слове «около» в этом контексте. Например, в некоторых вариантах осуществления термин «около» может охватывать диапазон значений, который находится в пределах 25%, 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1% или меньше указанного значения.
[122] Введение: Используемый в данном документе термин «введение» обычно относится к введению композиции субъекту или к системе для достижения доставки агента, который является или включен в композицию. Специалистам в данной области техники известно множество путей, которые при соответствующих обстоятельствах могут быть использованы для введения субъекту, например, человеку. Например, в некоторых вариантах осуществления введение может быть глазным, пероральным, парентеральным, местным и т.д. В некоторых конкретных вариантах осуществления введение может быть бронхиальным (например, путем инстилляции в бронхи), буккальным, кожным (что может быть или включать, например, один или более из местного для дермы, внутрикожного, межкожного, трансдермального и т. д.), энтеральным, внутриартериальным, внутрикожным, внутрижелудочным, интрамедуллярным, внутримышечным, интраназальным, внутрибрюшинным, интратекальным, внутривенным, внутрижелудочковым, введением в конкретный орган (например, внутрипеченочным), слизистым, назальным, пероральным, ректальным, подкожным, подъязычным, местным, трахеальным (например, путем интратрахеальной инстилляции), вагинальным, витреальным введением и т.д. В некоторых вариантах осуществления введение может включать только разовую дозу. В некоторых вариантах осуществления введение может включать применение фиксированного количества доз. В некоторых вариантах осуществления введение может включать прерывистое (например, множество доз, разделенных во времени) и/или периодическое (например, отдельные дозы, разделенные общим периодом времени) дозирование. В некоторых вариантах осуществления введение может включать непрерывное дозирование (например, перфузию) в течение по меньшей мере выбранного периода времени.
[123] Агент: В общем, термин «агент», используемый в данном документе, может использоваться для обозначения соединения или объекта любого химического класса, включая, например, полипептид, нуклеиновую кислоту, сахарид, липид, небольшую молекулу, металл или комбинацию или их комплекс. В соответствующих обстоятельствах, как будет ясно из контекста специалистам в данной области техники, этот термин может использоваться для обозначения объекта, который представляет собой или включает клетку или организм, или их фракцию, экстракт или компонент. Альтернативно или дополнительно, как станет ясно из контекста, этот термин может использоваться для обозначения продукта природного происхождения в том смысле, что он обнаружен в природе и/или получен из природы. В некоторых случаях, опять же, как будет ясно из контекста, этот термин может использоваться для обозначения одного или более объектов, созданных человеком в том смысле, что он разработан, сконструирован и/или произведен посредством действий человека и/или не встречается в природе. В некоторых вариантах осуществления агент можно использовать в выделенном или чистом виде; в некоторых вариантах осуществления агент можно использовать в исходной форме. В некоторых вариантах осуществления потенциальные агенты могут быть предложены в виде коллекций или библиотек, например, которые могут быть подвергнуты скринингу для идентификации или характеристики активных агентов в них. В некоторых случаях термин «агент» может относиться к соединению или объекту, который является или включает полимер; в некоторых случаях термин может относиться к соединению или объекту, который содержит один или более полимерных фрагментов. В некоторых вариантах осуществления термин «агент» может относиться к соединению или объекту, который не является полимером и/или практически не содержит какого-либо полимера и/или одного или более конкретных полимерных фрагментов. В некоторых вариантах осуществления термин может относиться к соединению или объекту, в котором отсутствует или практически отсутствует какой-либо полимерный фрагмент.
[124] Аминокислота: в самом широком смысле термин «аминокислота» в контексте данного документа относится к любому соединению и/или субстанции, которые могут быть включены в полипептидную цепь, например, посредством образования одной или более пептидных связей. В некоторых вариантах осуществления аминокислота имеет общую структуру H2N-C(H)(R)-COOH. В некоторых вариантах осуществления аминокислота представляет собой природную аминокислоту. В некоторых вариантах осуществления аминокислота представляет собой неприродную аминокислоту; в некоторых вариантах осуществления аминокислота представляет собой D-аминокислоту; в некоторых вариантах осуществления аминокислота представляет собой L-аминокислоту. «Стандартная аминокислота» относится к любой из двадцати стандартных L-аминокислот, обычно встречающихся в природных пептидах. «Нестандартная аминокислота» относится к любой аминокислоте, отличной от стандартных аминокислот, независимо от того, получена ли она синтетическим путем или из природного источника. В некоторых вариантах осуществления аминокислота, включая С- и/или N-концевую аминокислоту в полипептиде, может содержать структурную модификацию по сравнению с общей структурой, приведенной выше. Например, в некоторых вариантах осуществления аминокислота может быть модифицирована метилированием, амидированием, ацетилированием, пегилированием, гликозилированием, фосфорилированием и/или замещением (например, аминогруппы, группы карбоновой кислоты, одного или более протонов и/или гидроксильная группа) по сравнению с общей структурой. В некоторых вариантах осуществления такая модификация может, например, изменить период полужизни в кровотоке полипептида, содержащего модифицированную аминокислоту, по сравнению с полипептидом, содержащим в остальном идентичную немодифицированную аминокислоту. В некоторых вариантах осуществления такая модификация существенно не изменяет релевантную активность полипептида, содержащего модифицированную аминокислоту, по сравнению с полипептидом, содержащим в остальном идентичную немодифицированную аминокислоту. Как будет ясно из контекста, в некоторых вариантах осуществления термин «аминокислота» может использоваться для обозначения свободной аминокислоты; в некоторых вариантах осуществления он может использоваться для обозначения аминокислотного остатка полипептида.
[125] Антитело: Используемый в данном документе термин «антитело» относится к полипептиду, который включает элементы канонических последовательностей иммуноглобулина, достаточные для обеспечения специфического связывания с конкретным антигеном-мишенью. Как известно в данной области техники, интактные антитела, продуцируемые в природе, представляют собой тетрамерные агенты приблизительно 150 кДа, состоящие из двух идентичных полипептидов тяжелой цепи (приблизительно 50 кДа каждый) и двух идентичных полипептидов легкой цепи (приблизительно 25 кДа каждый), которые связываются друг с другом в то, что обычно называют «Y-образной» структурой. Каждая тяжелая цепь состоит по меньшей мере из четырех доменов (каждый длиной около 110 аминокислот) - N-концевого вариабельного (VH) домена (расположенного на концах структуры Y), за которым следуют три константных домена: CH1, CH2 и С-концевой СН3 (расположенный в основании стержня Y). Короткая область, известная как «переключатель», соединяет вариабельную и константную области тяжелой цепи. «Шарнир» соединяет домены CH2 и CH3 с остальной частью антитела. Две дисульфидные связи в этой шарнирной области соединяют два полипептида тяжелой цепи друг с другом в интактном антителе. Каждая легкая цепь состоит из двух доменов - N-концевого вариабельного (VL) домена, за которым следует C-концевой константный (CL) домен, отделенных друг от друга другим «переключателем». Тетрамеры интактных антител состоят из двух димеров тяжелая цепь-легкая цепь, в которых тяжелая и легкая цепи связаны друг с другом одной дисульфидной связью; две другие дисульфидные связи соединяют шарнирные области тяжелой цепи друг с другом, так что димеры соединяются друг с другом и образуется тетрамер. Антитела, продуцируемые естественным путем, также гликозилируются, как правило, по домену CH2. Каждый домен в природном антителе имеет структуру, характеризующуюся «иммуноглобулиновой складкой», образованной двумя бета-складками (например, 3-, 4- или 5-цепочечными складками), упакованными друг против друга в сжатую антипараллельную бета-бочку. Каждый вариабельный домен содержит три гипервариабельные петли, известные как «определяющие комплемент области» (CDR1, CDR2 и CDR3), и четыре в некоторой степени инвариантные «каркасные» области (FR1, FR2, FR3 и FR4). Когда натуральные антитела складываются, области FR образуют бета-складки, которые обеспечивают структурную основу для доменов, а петлевые области CDR как тяжелой, так и легкой цепей объединяются в трехмерном пространстве, так что они создают единый гипервариабельный антигенсвязывающий сайт, расположенный на вершине Y-структуры. Область Fc природных антител связывается с элементами системы комплемента, а также с рецепторами на эффекторных клетках, включая, например, эффекторные клетки, которые опосредуют цитотоксичность. Как известно в данной области техники, аффиность и/или другие атрибуты связывания областей Fc с рецепторами Fc можно модулировать посредством гликозилирования или другой модификации. В некоторых вариантах осуществления антитела, продуцируемые и/или используемые в соответствии с настоящим изобретением, включают гликозилированные домены Fc, включая домены Fc с модифицированным или сконструированным таким гликозилированием. Для целей настоящего изобретения в определенных вариантах осуществления любой полипептид или комплекс полипептидов, который включает в себя достаточные последовательности иммуноглобулиновых доменов, которые обнаруживаются в природных антителах, можно назвать и/или использовать как «антитело», независимо от того, продуцируется ли такой полипептид в естественных условиях (например, образуется организмом, реагирующим на антиген), или получен путем рекомбинантной инженерии, химического синтеза или при помощи другой искусственной системы или методологии. В некоторых вариантах осуществления антитело является поликлональным; в некоторых вариантах осуществления антитело является моноклональным. В некоторых вариантах осуществления антитело имеет последовательности константной области, которые характерны для антител мыши, кролика, приматов или человека. В некоторых вариантах осуществления элементы последовательности антитела являются гуманизированными, приматизированными, химерными и т.д., как известно в данной области техники. Более того, используемый в данном документе термин «антитело» может относиться в соответствующих вариантах (если не указано иное или ясно из контекста) к любой из известных или разработанных конструкций или форматов для использования структурных и функциональных особенностей антитела в альтернативном представлении. Например, в вариантах осуществления антитело, используемое в соответствии с настоящим изобретением, находится в формате, выбранном, но не ограничиваясь, из следующего: интактные антитела IgA, IgG, IgE или IgM; би- или полиспецифические антитела (например, Zybodies® и т. д.); фрагменты антител, такие как фрагменты Fab, фрагменты Fab ’, фрагменты F(ab’)2, фрагменты Fd ’, фрагменты Fd и выделенные CDR или их наборы; одноцепочечные Fv; слитые молекулы полипептид-Fc; однодоменные антитела (например, однодоменные антитела акулы, такие как IgNAR или его фрагменты); верблюжьи антитела; замаскированные антитела (например, Probody®); Малые модульные иммунофармацевтические средства (“SMIPTM”); одноцепочечные или тандемные диатела (TandAb®); VHH; Антикалины®; Наноантитела®, миниантитела; BiTE®; белки с анкириновым повтором или DARPIN®; Авимеры®; DART; TCR-подобные антитела; Аднектины®; Аффилины®; Trans-bodies®; Аффитела®; TrimerX®; микропротеины; Финомеры®, Центирины®; и KALBITOR®s. В некоторых вариантах осуществления антитело может не иметь ковалентную модификацию (например, присоединение гликана), которую оно имело бы, если бы было получено естественным образом. В некоторых вариантах осуществления антитело может содержать ковалентную модификацию (например, присоединение гликана, полезную нагрузку [например, детектируемый фрагмент, терапевтический фрагмент, каталитический фрагмент и т.д.] или другую боковую группу [например, полиэтиленгликоль и др.]).
[126] Антиген: Используемый в данном документе термин «антиген» относится к (i) агенту, который индуцирует иммунный ответ; и/или (ii) агент, который связывается с Т-клеточным рецептором (например, когда он презентован молекулой ГКГС) или с антителом. В некоторых вариантах осуществления антиген индуцирует гуморальный ответ (например, включая продукцию антигенспецифических антител); в некоторых вариантах осуществления антиген индуцирует клеточный ответ (например, с участием Т-клеток, рецепторы которых специфически взаимодействуют с антигеном). В некоторых вариантах осуществления антиген индуцирует гуморальный ответ и клеточный ответ. В некоторых вариантах осуществления антиген связывается с антителом и может индуцировать или не индуцировать конкретный физиологический ответ в организме. В общем, антиген может представлять собой или включать любое химическое соединение, такое как, например, небольшая молекула, нуклеиновая кислота, полипептид, углевод, липид, полимер (в некоторых вариантах осуществления, отличный от биологического полимера (например, отличный от полимер нуклеиновой кислоты или аминокислотного полимера)) и т.д. В некоторых вариантах осуществления антиген представляет собой или содержит полипептид. В некоторых вариантах осуществления антиген представляет собой полисахарид или содержит его. Специалисты в данной области техники поймут, что, как правило, антиген может быть предоставлен в выделенной или чистой форме или, альтернативно, может быть предоставлен в неочищенной форме (например, вместе с другими материалами, например, в экстракте, таком как клеточный экстракт или другой относительно неочищенный препарат антигенсодержащего источника). В некоторых вариантах осуществления антигены, используемые в соответствии с настоящим изобретением, представлены в неочищенной форме. В некоторых вариантах осуществления антиген представляет собой рекомбинантный антиген. В некоторых вариантах осуществления антиген представляет собой полипептид или полисахарид, который при введении субъекту индуцирует специфический и/или клинически значимый иммунный ответ на такой полипептид или полисахарид. В некоторых вариантах осуществления антиген выбран для индукции специфического и/или клинически значимого иммунного ответа на такой полипептид или полисахарид.
[127] Связаны с: два объекта «связаны» друг с другом, как этот термин используется в данном документе, если присутствие, уровень и/или форма одного коррелируют с таковым другого. В некоторых вариантах осуществления два или более объекта физически «связаны» друг с другом, если они взаимодействуют, прямо или косвенно, так что они находятся и/или остаются в физической близости друг с другом. В некоторых вариантах осуществления два или более объекта, которые физически связаны друг с другом, ковалентно связаны друг с другом. В некоторых вариантах осуществления два или более объекта, которые физически связаны друг с другом, не связаны друг с другом ковалентно, но нековалентно связаны, например, посредством аффинных взаимодействий, электростатических взаимодействий, водородных связей, взаимодействия Ван-дер-Ваальса, гидрофобных взаимодействий, магнетизма и их комбинации.
[128] Связывание: следует понимать, что используемый в данном документе термин «связывание» обычно относится к нековалентной ассоциации между двумя или более объектами или между ними. «Прямое» связывание включает физический контакт между объектами или группами; косвенное связывание включает физическое взаимодействие посредством физического контакта с одним или более промежуточными объектами. Связывание между двумя или более объектами, как правило, можно оценить в любом из множества контекстов, в том числе в тех случаях, когда взаимодействующие объекты или группы изучаются по отдельности или в контексте более сложных систем (например, будучи ковалентно или иным образом связаны с субъектом-носителем и/или в биологической системе или клетке).
[129] Белок-носитель: используемый в данном документе термин «белок-носитель» относится к белку или пептиду, который связан, образует комплекс или иным образом связан с гаптеном (например, небольшой пептид или липид) или менее иммуногенным антигеном (например, полисахаридом) и который индуцирует или улучшает иммунный ответ на такой связанный, или комплексный, или иным образом связанный гаптен (например, небольшой пептид или липид) или менее иммуногенный антиген (например, полисахарид). В некоторых вариантах осуществления такой иммунный ответ представляет собой или включает ответ на гаптен или менее иммуногенный антиген, который связан, входит в комплекс или иным образом связан с таким белком-носителем. В некоторых вариантах осуществления такой иммунный ответ представляет собой или включает ответ как на белок-носитель, так и на гаптен или менее иммуногенный антиген, который связан, входит в комплекс или иным образом связан с таким белком-носителем. В некоторых вариантах осуществления не возникает значительного иммунного ответа на сам белок-носитель. В некоторых вариантах осуществления может быть обнаружен иммунный ответ на белок-носитель; в некоторых вариантах осуществления иммунный ответ на такой белок-носитель является сильным. В некоторых вариантах осуществления белок-носитель связан, образует комплекс или иным образом связан с одной или более другими молекулами.
[130] Колонизация: Используемый в данном документе термин «колонизация», как правило, относится к способности микроба расти на целевом участке или на поверхности. Например, термин «колонизация» относится к способности микроба (например, бактерии) расти на анатомическом участке (например, слизистой оболочке, желудочно-кишечном тракте, участке поражения, органе и т.д.) хозяина.
[131] Комбинированная терапия: Используемый в данном документе термин «комбинированная терапия» относится к тем ситуациям, в которых субъект подвергается воздействию двух или более терапевтических схем (например, двух или более терапевтических агентов). В некоторых вариантах осуществления две или более схемы можно применять одновременно; в некоторых вариантах осуществления такие схемы можно применять последовательно (например, все «дозы» первой схемы вводятся до введения любых доз второй схемы); в некоторых вариантах осуществления такие агенты вводят в перекрывающихся схемах дозирования. В некоторых вариантах осуществления «введение» комбинированной терапии может включать применение одного или более агентов или методов субъекту, применяющему другой(-ие) агент(-ы) или метод(-ы) в комбинации. Для ясности, комбинированная терапия не требует введения отдельных агентов вместе в одной композиции (или даже обязательно в одно время), хотя в некоторых вариантах осуществления два или более активных агентов, или их активных фрагментов можно вводить вместе в комбинированной композиции или даже в комбинированном соединении (например, в виде части одного химического комплекса или ковалентного соединения).
[132] Производное: Используемый в данном документе термин «производное» или его грамматические эквиваленты относится к структурному аналогу эталонной субстанции. То есть «производное» представляет собой субстанцию, которое демонстрирует значительное структурное сходство с эталонной субстанцией, например, разделяет основную или консенсусную структуру, но также отличается некоторыми дискретными способами. О такой субстанции можно сказать, что оно «получено из» указанной эталонной субстанции. В некоторых вариантах осуществления производное представляет собой субстанцию, которое может быть получено из эталонной субстанции с помощью химических манипуляций. В некоторых вариантах осуществления производное представляет собой субстанцию, которая может быть получена посредством выполнения синтетического процесса, по существу аналогичного (например, совместного использования множества стадий) с тем, который генерирует эталонную субстанцию.
[133] Домен: Используемый в данном документе термин «домен» относится к участку или части объекта. В некоторых вариантах осуществления «домен» связан с конкретным структурным и/или функциональным признаком объекта, так что, когда домен физически отделен от остальной части его исходного объекта, он по существу или полностью сохраняет конкретный структурный и/или функциональный признак. Альтернативно или дополнительно, домен может быть или включать в себя часть объекта, который, будучи отделенным от этого (исходного) объекта и связан с другим (получателем) объектом, по существу сохраняет и/или передает объекту-получателю один или более структурных и/или функциональных признаков, которые характеризовали его в исходном объекте. В некоторых вариантах осуществления домен представляет собой участок или часть молекулы (например, небольшую молекулу, углевод, липид, нуклеиновую кислоту или полипептид). В некоторых вариантах осуществления домен представляет собой часть полипептида; в некоторых таких вариантах осуществления домен характеризуется конкретным структурным элементом (например, конкретной аминокислотной последовательностью или мотивом последовательности, α-спиралью, β-складкой, суперспиралью, случайной спиралью и т. д.) и/или конкретным функциональным признаком (например, связывающей активностью, ферментативной активностью, активностью фолдинга, сигнальной активностью и т.д.).
[134] Дозированная форма или единичная дозированная форма: Специалисты в данной области техники поймут, что термин «дозированная форма» может использоваться для обозначения физически дискретной единицы активного агента (например, терапевтического или диагностического агента) для введения субъекту. Как правило, каждая такая единица содержит предопределенное количество активного агента. В некоторых вариантах осуществления такое количество представляет собой единичное дозированное количество (или его целую долю), подходящее для введения в соответствии со схемой дозирования, которая согласно предварительному определению коррелирует с желаемым или благоприятным результатом при введении релевантной популяции (т. е. с терапевтической схемой дозирования). Для специалистов в данной области техники очевидно, что общее количество терапевтической композиции или агента, вводимое конкретному субъекту, определяется одним или более лечащими врачами и может включать введение нескольких дозированных форм.
[135] Схема дозирования: Специалисты в данной области техники поймут, что термин «схема дозирования» может использоваться для обозначения набора стандартных доз (обычно более одной), которые вводятся индивидуально субъекту, как правило, через определенные периоды времени. В некоторых вариантах осуществления заданный терапевтический агент имеет рекомендуемую схему дозирования, которая может включать применение одной или более доз. В некоторых вариантах осуществления схема дозирования включает применение некоторого количества доз, при этом каждая из них отделена по времени от других доз. В некоторых вариантах осуществления приемы отдельных доз отделены друг от друга периодом времени одинаковой длины; в некоторых вариантах осуществления схема дозирования включает применение некоторого количества доз и по меньшей мере два разных периода времени, разделяющих прием отдельных доз. В некоторых вариантах осуществления все дозы в рамках схемы дозирования составляют одинаковое количество однократной дозы. В некоторых вариантах осуществления разные дозы в рамках схемы дозирования составляют разное количество. В некоторых вариантах осуществления схема дозирования включает применение первой дозы в количестве первой дозы с последующим применением одной или более дополнительных доз в количестве второй дозы, отличном от количества первой дозы. В некоторых вариантах осуществления схема дозирования включает применение первой дозы в количестве первой дозы с последующим применением одной или более дополнительных доз в количестве второй дозе, таком же, как и количество первой дозы. В некоторых вариантах осуществления схема дозирования коррелирует с желаемым или благоприятным результатом при введении в рамках релевантной популяции (т. е. представляет собой терапевтическую схему дозирования).
[136] Фрагмент: «Фрагмент» материала или объекта, как описано в данном документе, имеет структуру, которая включает дискретную часть целого, но не имеет одной или более составляющих, встречающихся в целом. В некоторых вариантах осуществления фрагмент состоит из такой дискретной части. В некоторых вариантах осуществления фрагмент включает дискретную часть целого, причем эта дискретная часть имеет одну или более функциональных характеристик, присущих целому. В некоторых вариантах осуществления фрагмент состоит из такой дискретной части. В некоторых вариантах осуществления фрагмент состоит из или включает характерный структурный элемент или фрагмент, присутствующий в целом. В некоторых вариантах осуществления фрагмент полимера, например, полипептид или полисахарид, содержит или состоит из по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 210, 220, 230, 240, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500 или более мономерных единиц (например, остатков), обнаруженных во всем полимере. В некоторых вариантах осуществления фрагмент полимера содержит или состоит из, по меньшей мере, около 5%, 10%, 15%, 20%, 25%, 30%, 25%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или более мономерных единиц (например, остатков), присутствующих во всем полимере. В некоторых вариантах осуществления весь материал или объект может называться «исходными» для целого.
[137] Гомология: Используемые в данном документе термин «гомология» относится к общему сходству между полимерными молекулами, например, между молекулами нуклеиновой кислоты (например, молекулами ДНК и/или молекулами РНК) и/или между молекулами полипептидов. В некоторых вариантах осуществления полимерные молекулы считаются «гомологичными» друг другу, если их последовательности на по меньшей мере 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, или 99% идентичны. В некоторых вариантах осуществления полимерные молекулы считаются «гомологичными» друг другу, если их последовательности на по меньшей мере 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, или 99% сходны (например, содержащие остатки со связанными химическими свойствами в соответствующих положениях). Например, как хорошо известно специалистам в данной области техники, определенные аминокислоты обычно классифицируют как сходные друг с другом как «гидрофобные» или «гидрофильные» аминокислоты и/или как имеющие «полярные» или «неполярные» боковые цепи. Замена одной аминокислоты на другую того же типа часто может считаться «гомологичной» заменой.
[138] Идентичность: Используемые в данном документе термин «гомология» относится к общему сходству между полимерными молекулами, например, между молекулами нуклеиновой кислоты (например, молекулами ДНК и/или молекулами РНК) и/или между молекулами полипептидов. В некоторых вариантах осуществления полимерные молекулы считаются «практически идентичными» друг другу, если их последовательности на по меньшей мере 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичны. Например, вычисление процента идентичности двух последовательностей нуклеиновой кислоты или полипептида может быть выполнено путем выравнивания двух последовательностей с целью оптимального сравнения (например, гэпы могут быть введены в одну или обе из первой и второй последовательностей для оптимального выравнивания и неидентичные последовательности могут игнорироваться с целью сравнения). В определенных вариантах осуществления длина последовательности, выровненной с целью сравнения, составляет по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или по существу 100% длины эталонной последовательности. Затем в соответствующих положениях сравнивают нуклеотиды. Когда положение в первой последовательности занято тем же остатком (аминокислотным или нуклеотидным), что и соответствующее положение во второй последовательности, то молекулы в этом положении идентичны. Процент идентичности между двумя последовательностями является функцией от числа совпадающих положений в последовательностях с учетом числа гэпов и длины каждого гэпа, которые необходимо вносить для оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процента идентичности между двумя последовательностями можно осуществлять с помощью математического алгоритма. Например, процент идентичности между двумя нуклеотидными последовательностями можно определить с помощью алгоритма Майерса и Миллера, 1989, который был включен в программу ALIGN (версия 2.0). В некоторых иллюстративных вариантах осуществления сравнения последовательностей нуклеиновых кислот, выполненные с помощью программы ALIGN, используют таблицу весов замен остатков PAM120, штраф за продолжение гэпа, равный 12, и штраф за открытие гэпа, равный 4. Процент идентичности между двумя нуклеотидными последовательностями, в качестве альтернативы, может быть определен с использованием программы GAP из пакета программного обеспечения GCG с использованием матрицы NWSgapdna.CMP.
[139] Улучшить, увеличить, ингибировать или уменьшить: Используемые в данном документе термины «улучшить», «увеличить», «ингибировать», «уменьшить» или их грамматические эквиваленты указывают на значения, которые относятся к базовому уровню или другому эталонному измерению. В некоторых вариантах осуществления соответствующее сравнительное измерение может представлять собой или включать измерение в конкретной системе (например, у одного субъекта) в других сопоставимых условиях при отсутствии (например, до и/или после) конкретного агента или лечения, или в присутствии соответствующего сопоставимого эталонного агента. В некоторых вариантах осуществления подходящее сравнительное измерение может представлять собой или включать измерение в сопоставимой системе, о которой известно или ожидается, что она будет реагировать определенным образом в присутствии соответствующего агента или лечения.
[140] Иммунологически эффективное количество или иммунологически эффективная доза: Используемый в данном документе термин «иммунологически эффективное количество» или «иммунологически эффективная доза» относится к количеству антигенного или иммуногенного вещества, например, антигена, иммуногена, иммуногенного комплекса, иммуногенной композиции, вакцины или фармацевтической композиции, которую при введении субъекту либо в виде разовой дозы, либо в составе серии доз достаточно для усиления собственного иммунного ответа субъекта против последующего воздействия патогена. В некоторых вариантах патоген представляет собой S. pneumoniae. В некоторых вариантах осуществления иммунный ответ направлен против одного или более различных серотипов S. pneumoniae. В некоторых вариантах осуществления иммунный ответ направлен против двух или более различных серотипов S. pneumoniae. В некоторых вариантах осуществления иммунный ответ направлен против девяти или более различных серотипов S. pneumoniae. В некоторых вариантах осуществления иммунный ответ направлен против тринадцати или более различных серотипов S. pneumoniae. В некоторых вариантах осуществления иммунный ответ направлен против пятнадцати или более различных серотипов S. pneumoniae. В некоторых вариантах осуществления иммунный ответ направлен против двадцати трех или более различных серотипов S. pneumoniae. В некоторых вариантах осуществления иммунный ответ направлен против двадцати четырех или более различных серотипов S. pneumoniae. Иммунологически эффективное количество может варьироваться в зависимости от субъекта, которого лечат, вида субъекта, степени иммунного ответа, который необходимо вызвать, и т.д. В некоторых вариантах осуществления иммунологически эффективное количество является достаточным для лечения или защиты субъекта, имеющего или есть риск заболеть. В некоторых вариантах осуществления иммунологически эффективное количество относится к нетоксичному, но достаточному количеству, которое может представлять собой количество для лечения, ослабления или предотвращения инфекции и/или заболевания (например, бактериальной инфекции, пневмококковой инфекции, бактериальной колонизации, пневмококковой колонизации, осложнений, связанных с бактериальной инфекцией, осложнений, связанных с пневмококковой инфекцией и т. д.) у любого субъекта. В некоторых вариантах осуществления иммунологически эффективное количество достаточно для индукции иммунопротективного ответа при введении субъекту.
[141] Иммунопротективный ответ или защитный ответ: Используемый в данном документе «иммунопротективный ответ» или «защитный ответ» относится к иммунному ответу, который опосредует антиген- или иммуноген-индуцированную иммунологическую память. В некоторых вариантах осуществления иммунопротективный ответ индуцируется введением субъекту субстанции, например, антигена, иммуногена, иммуногенного комплекса, иммуногенной композиции, вакцины или фармацевтической композиции. В некоторых вариантах осуществления иммунная защита включает одно или более из следующего: активный иммунный надзор, более быстрый и эффективный ответ на активацию иммунной системы по сравнению с ответом, наблюдаемым у не получавшего лечения субъекта, эффективный клиренс активирующего агента или патогена с последующим быстрым исчезновением воспаления. В некоторых вариантах осуществления иммунопротективный ответ представляет собой адаптивный иммунный ответ. В некоторых вариантах осуществления иммунопротективный ответ достаточен для защиты иммунизированного субъекта от продуктивной инфекции конкретным патогеном или патогенами, на которые направлена вакцина (например, инфекция, вызванная S. pneumoniae).
[142] Иммунизация: Используемый в данном документе термин «иммунизация» или его грамматические эквиваленты относится к процессу индукции иммунного ответа на инфекционный организм или агент у субъекта («активная иммунизация») или, альтернативно, обеспечения компонентов иммунной системы против инфекционного организма или агента субъекту («пассивная иммунизация»). В некоторых вариантах осуществления иммунизация включает введение субъекту одного или более антигенов, иммуногенов, иммуногенных комплексов, вакцин, иммунных молекул, таких как антитела, иммунные сыворотки, иммунные клетки, такие как Т-клетки или В-клетки, или фармацевтических композиций. В некоторых вариантах осуществления иммунизацию проводят путем введения субъекту иммунологически эффективного количества вещества, например, антигена, иммуногена, иммуногенного комплекса, иммуногенной композиции, вакцины, иммунной молекулы, такой как антитело, иммунной сыворотки, иммунной клетки, такой как Т-клетка или В-клетка, или фармацевтической композиции. В некоторых вариантах осуществления иммунизация приводит к иммунопротективному ответу у субъекта. В некоторых вариантах осуществления активную иммунизацию проводят путем введения субъекту антигенной или иммуногенной субстанции, например, антигена, иммуногена, иммуногенного комплекса, вакцины или фармацевтической композиции. В некоторых вариантах осуществления пассивную иммунизацию проводят путем введения субъекту компонента иммунной системы, например, иммунной молекулы, такой как антитело, иммунной сыворотки, или иммунной клетки, такой как Т-клетка или В-клетка.
[143] Выделенный: Используемый в данном документе термин «выделенный» или его грамматические эквиваленты относится к субстанции и/или объекту, который (1) отделен по меньшей мере от некоторых компонентов, с которыми он был связан при первоначальной выработке (природе и/или в экспериментальных условиях), и/или (2) разработан, приготовлен, подготовлен и/или изготовлен вручную. Выделенные вещества и/или объекты могут быть отделены от около 10%, около 20%, около 30%, около 40%, около 50%, около 60%, около 70%, около 80%, около 90%, около 91%, около 92%, около 93%, около 94%, около 95%, около 96%, около 97%, около 98%, около 99% или более чем около 99% других компонентов, с которыми они были первоначально связаны. В некоторых вариантах осуществления изобретения выделенные агенты имеют чистоту около 80%, около 85%, около 90%, около 91%, около 92%, около 93%, около 94%, около 95%, около 96%, около 97%, около 98%, около 99% или более чем около 99%. Как используется в данном документе, субстанция является «чистым», если оно по существу не содержит других компонентов. В некоторых вариантах осуществления, как будет понятно специалистам в данной области техники, субстанция может все еще считаться «выделенным» или даже «чистым» после объединения с некоторыми другими компонентами, такими как, например, один или более носителей или наполнителей (например, буфер, растворитель, вода и т. д.); в таких вариантах осуществления процент выделения или чистоты вещества рассчитывают без учета таких носителей или эксципиентов. Например, в некоторых вариантах осуществления биологический полимер, такой как полипептид или полисахарид, который встречается в природе, считается «выделенным», когда: а) в силу своего происхождения или источника деривации не связан с некоторыми или всеми из компонентов, которые сопровождают его в его естественном состоянии в природе; b) он по существу не содержит других полипептидов или нуклеиновых кислот того же вида из видов, которые его вырабатывают в природе; c) экспрессируется или иным образом ассоциируется с компонентами клетки или другой системы экспрессии, которая не относится к виду, производящему его в природе. Так, например, в некоторых вариантах осуществления полипептид или полисахарид, который синтезируется химически или синтезируется в клеточной системе, отличной от той, которая вырабатывает его в природе считается «выделенным» полипептидом или полисахаридом. Альтернативно или дополнительно, в некоторых вариантах осуществления полипептид или полисахарид, который был подвергнут одному или более способам очистки, может рассматриваться как «выделенный» полипептид или полисахарид в той степени, в которой он был отделен от других компонентов: а) с которыми он связан в природе; и/или b) с которым он был связан при первоначальной выработке.
[144] Линкер: Используемый в данном документе термин «линкер» используется для обозначения объекта, который соединяет два или более элементов, чтобы сформировать многоэлементный агент. Например, специалисты в данной области техники понимают, что полипептид, структура которого включает два или более функциональных или организационных домена, часто включает участок аминокислот между такими доменами, который связывает их друг с другом. В некоторых вариантах осуществления полипептид, содержащий линкерный элемент, имеет общую структуру общей формы S1-L-S2, где S1 и S2 могут быть одинаковыми или разными и представлять два домена, связанные друг с другом линкером (L). В некоторых вариантах осуществления полипептидный линкер представляет собой по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или более аминокислот в длину. В некоторых вариантах осуществления линкер отличается тем, что он не принимает жесткую трехмерную структуру, а, скорее, обеспечивает гибкость полипептида. В данной области техники известен ряд различных линкерных элементов, которые можно соответствующим образом использовать при конструировании полипептидов (например, слитых полипептидов) (Holliger et al, 1993; Poljak, 1994).
[145] Не меньший, не уступающий: используемые в данном документе термины «не меньший, не уступающий» в контексте оценки тестируемой фармацевтической композиции относится к тестируемой фармацевтической композиции, которая (например, с точки зрения иммуногенности и/или функционального титра антител, генерируемых тестируемой композицией) по меньшей мере так же эффективен, как эталонная композиция. В некоторых вариантах осуществления не меньшая эффективность демонстрируется, когда нижняя граница 95% доверительного интервала (ДИ) для соотношения средних геометрических титров (GMT) исследуемой фармацевтической композиции к контрольной композиции, по меньшей мере, больше или равна 0,4 или выше, включая, например, по меньшей мере 0,5, по меньшей мере 0,6, по меньшей мере 0,7, по меньшей мере 0,8, по меньшей мере 0,9, по меньшей мере 0,95, по меньшей мере 0,98, по меньшей мере 1,0 или выше. Например, в некоторых вариантах осуществления иммуногенная композиция или вакцина, описанные в данном документе, не уступают эталонной вакцине (например, PCV13 или PPSV23), когда нижняя граница 95% доверительного интервала (ДИ) для соотношения средних геометрических титров (GMT) для иммуногенной композиции или вакцины по сравнению с эталонной вакциной по меньшей мере больше или равно 0,4 или выше, включая, например, по меньшей мере 0,5, по меньшей мере 0,6, по меньшей мере 0,7, по меньшей мере 0,8, по меньшей мере 0,9, по меньшей мере 0,95, по меньшей мере 0,98, по меньшей мере 1,0 или выше. В некоторых вариантах осуществления иммуногенная композиция или вакцина, описанные в данном документе, не уступают эталонной вакцине (например, PCV13 или PPSV23), когда нижняя граница 95% доверительного интервала (ДИ) для соотношения средних геометрических титров (GMT) для иммуногенной композиции или вакцины по сравнению с эталонной вакциной по меньшей мере больше или равна 0,95 или выше, включая, например, по меньшей мере 0,96, по меньшей мере 0,97, по меньшей мере 0,98, по меньшей мере 0,99, по меньшей мере 1,0, по меньшей мере 1,1, по меньшей мере 1,3, по меньшей мере 1,5 или выше. В некоторых вариантах осуществления иммуногенная композиция или вакцина, описанные в данном документе, не уступают эталонной вакцине (например, PCV13 или PPSV23), когда показатели сероконверсии или процент реципиентов вакцины с иммунными ответами выше предопределенного порога, например, нижней границы 95% доверительного интервала для разницы между процентом субъектов, у которых произошла сероконверсия после иммунизации иммуногенной композицией или вакциной, описанной в данном документе, или иммунизации эталонной вакциной (например, PCV13 или PPSV23), превышает -0,10.
[146] Фармацевтическая композиция: Используемый в данном документе термин «фармацевтическая композиция» относится к композиции, в которой активный агент составлен вместе с одним или более фармацевтически приемлемыми носителями. В некоторых вариантах осуществления активный агент присутствует в количестве однократной дозы, подходящем для введения в терапевтической схеме, которая демонстрируют статистически значимую вероятность достижения заданного терапевтического эффекта при введении соответствующей популяции. В некоторых вариантах осуществления фармацевтическая композиция может быть специально составлена для введения в твердой или жидкой форме, включая те, которые адаптированы для следующего: пероральное введение, например, вливания (водные или неводные растворы или суспензии), таблетки, например, предназначенные для буккального, сублингвального и системного всасывания, болюсы, порошки, гранулы, пасты для нанесения на язык; парентеральное введение, например, путем подкожной, внутримышечной, внутривенной или эпидуральной инъекции в виде, например, стерильного раствора или суспензии, или состава с замедленным высвобождением; местное применение, например, в виде крема, мази или пластыря, или спрея с контролируемым высвобождением, наносимых на кожу, легкие или полость рта; интравагинально или интраректально, например, в виде пессария, крема или пены; сублингвально; окулярно; трансдермально; или интраназально, ингаляционно и наносимых на другие поверхности слизистой оболочки.
[147] Фармацевтически приемлемый: Используемый в данном документе термин «фармацевтически приемлемый», применяемый к носителю, разбавителю или эксципиенту, используемому для составления композиции, как раскрыто в данном документе, означает, что носитель, разбавитель или эксципиент должны быть совместимы с другими ингредиентами композиции и не вредны для реципиента.
[148] Полисахарид: Используемый в данном документе термин «полисахарид» относится к полимерной углеводной молекуле, состоящей из длинных цепей моносахаридных звеньев, связанных вместе гликозидными, фосфодиэфирными или другими связями, и при гидролизе образующей моносахариды или олигосахариды. Структура полисахаридов варьируется от линейной до сильно разветвленной. Примеры включают запасные полисахариды, такие как крахмал и гликоген, структурные полисахариды, такие как целлюлоза и хитин, и микробные полисахариды, и антигенные полисахариды, обнаруженные в микроорганизмах, включая, помимо прочего, капсульные полисахариды (CPS), O-полисахариды (OPS), основные O-полисахариды (COPS) и липополисахариды (LPS).
[149] Полипептид: Используемый в данном документе термин «полипептид», как правило, имеет общепризнанное значение полимера, состоящего по меньшей мере из трех аминокислот, например, связанных друг с другом пептидными связями. Специалисты в данной области техники поймут, что термин «полипептид» предназначен для того, чтобы быть достаточно общим, чтобы охватывать не только полипептиды, имеющие полную последовательность, приведенную в данном документе, но также охватывать полипептиды, которые представляют собой функциональные фрагменты (т. е. фрагменты, сохраняющие по меньшей мере одну активность) таких полных полипептидов. Более того, специалисты в данной области техники понимают, что белковые последовательности, как правило, допускают некоторую замену без нарушения активности. Таким образом, любой полипептид, который сохраняет активность и имеет по меньшей мере около 30-40% общей идентичности последовательностей, часто более около 50%, 60%, 70% или 80% и, кроме того, как правило, содержащий по меньшей мере одну область с гораздо более высокой идентичностью, часто более 90% или даже 95%, 96%, 97%, 98% или 99% в одной или более высококонсервативных областях, как правило, содержащих по меньшей мере 3-4, а часто до 20 или более аминокислот с другим полипептидом того же класса, охватывается соответствующим термином «полипептид», используемым в данном документе. Полипептиды могут содержать L-аминокислоты, D-аминокислоты или и то, и другое и могут содержать любые из множества модификаций аминокислот или аналогов, известных в данной области техники. Полезные модификации включают, например, концевое ацетилирование, амидирование, метилирование и т.д. В некоторых вариантах осуществления белки могут содержать природные аминокислоты, неприродные аминокислоты, синтетические аминокислоты и их комбинации.
[150] Предотвращение: Термин «предотвращать» или «предотвращение», используемые в данном документе в связи с заболеванием, расстройством и/или медицинским состоянием, относится к снижению риска развития заболевания, расстройства и/или патологического состояния и/или отсрочке начала заболевания, и/или снижения частоты и/или тяжести одной или более характеристик или симптомов конкретного заболевания, расстройства или патологического состояния. В некоторых вариантах осуществления предотвращение оценивается на основе популяции, так что считается, что агент «предотвращает» конкретное заболевание, расстройство или патологическое состояние, если статистически значимое снижение развития, частоты и/или интенсивности одного или более симптомов заболевания, расстройства или патологического состояния наблюдается в популяции, предрасположенной к заболеванию, расстройству или патологическому состоянию. В некоторых вариантах осуществления профилактика может считаться завершенной, если начало заболевания, расстройства или патологического состояния было отложено на предопределенный период времени.
[151] Белок: Используемый в данном документе термин «белок» включает полипептид. Белки могут включать фрагменты, отличные от аминокислот (например, могут быть гликопротеины, протеогликаны и т. д.), и/или могут быть процессированы или модифицированы иным образом. Специалисты в данной области техники поймут, что «белок» может быть полной полипептидной цепью, продуцируемой клеткой (с сигнальной последовательностью или без нее), или может быть ее характерной частью. Обычным специалистам будет понятно, что белок иногда может включать более одной полипептидной цепи, например, связанных одной или более дисульфидными связями или связанных другими способами. Полипептиды могут содержать L-аминокислоты, D-аминокислоты или и то, и другое и могут содержать любые из множества модификаций аминокислот или аналогов, известных в данной области техники. Полезные модификации включают, например, концевое ацетилирование, амидирование, метилирование и т.д. В некоторых вариантах осуществления белки могут содержать природные аминокислоты, неприродные аминокислоты, синтетические аминокислоты и их комбинации. Термин «пептид» обычно используется для обозначения полипептида, имеющего длину менее около 100 аминокислот, менее около 50 аминокислот, менее 20 аминокислот или менее 10 аминокислот. В некоторых вариантах осуществления белки представляют собой антитела, фрагменты антител, их биологически активные части и/или их характерные части.
[152] Рекомбинантный: Используемый в данном документе термин «рекомбинантный» предназначен для обозначения полипептидов, которые разработаны, сконструированы, получены, экспрессированы, созданы, произведены и/или выделены с помощью рекомбинантных способов, таких как полипептиды, экспрессируемые с использованием рекомбинантного вектора экспрессии, трансфицированного в клетку-хозяин; полипептиды, выделенные из рекомбинантной комбинаторной библиотеки полипептидов человека; полипептиды, выделенные из животного (например, мыши, кролика, овцы, рыбы и т. д.), которое является трансгенным или иным образом подвергается манипуляциям для экспрессии гена или генов или компонентов гена, которые кодируют и/или направляют экспрессию полипептида или одного или более компонентов, частей, элементов или доменов из них; и/или полипептиды, полученные, экспрессированные, созданные или выделенные любыми другими способами, которые включают сплайсинг или лигирование выбранных элементов последовательности нуклеиновых кислот друг с другом, химический синтез выбранных элементов последовательности и/или получение иным образом нуклеиновой кислоты, которая кодирует и/или направляет экспрессию полипептида или одного или более его компонентов, частей, элементов или доменов. В некоторых вариантах осуществления один или более таких выбранных элементов последовательности встречаются в природе. В некоторых вариантах осуществления один или более таких выбранных элементов последовательности сконструированы in silico. В некоторых вариантах осуществления один или более таких выбранных элементов последовательности являются результатом мутагенеза (например, in vivo или in vitro) известного элемента последовательности, например, из природного или синтетического источника, такого как, например, в зародышевой линии представляющего интереса исходного организма (например, человека, мыши и т. д.).
[153] Эталон: Используемый в данном документе термин «эталон» описывает стандарт или контроль, относительно которого выполняется сравнение. Например, в некоторых вариантах осуществления представляющие интерес агент, животное, субъект, популяцию, образец, последовательность или значение сравнивают с эталонными или контрольными агентом, животным, субъектом, популяцией, образцом, последовательностью или значением. В некоторых вариантах осуществления исследование и/или определение для эталона или контроля проводят практически одновременно с представляющим интерес исследованием или определением. В некоторых вариантах осуществления эталон или контроль представляет собой ретроспективный эталон или контроль, необязательно, отображенный на материальном носителе. Как правило, как очевидно для специалистов в данной области техники, определение или получение характеристик эталона или контроля проводят в условиях или при обстоятельствах, сравнимых с теми, для которых проводится оценка. Для специалистов в данной области техники очевиден факт присутствия достаточного сходства для подтверждения достоверности и/или сравнения с конкретным возможным эталоном или контролем.
[154] Ответ: Используемый в данном документе термин «ответ» на лечение может относиться к любому полезному изменению патологического состояния у субъекта, которое происходит в результате лечения или коррелирует с ним. Такое изменение может включать стабилизацию патологического состояния (например, предотвращение ухудшения, которое произошло бы в отсутствие лечения), снижение интенсивности симптомов патологического состояния и/или улучшение перспектив излечения патологического состояния и т. д. Это может относиться к ответу субъекта или к ответу опухоли на лечение. Ответ субъекта или опухоли можно измерить в соответствии с широким спектром критериев, включая клинические критерии и объективные критерии. Методы оценки ответа включают, помимо прочего, клиническое обследование, позитронно-эмиссионную томографию, рентгеновскую компьютерную томографию грудной клетки, МРТ, ультразвук, эндоскопию, лапароскопию, наличие или уровень биомаркеров в образце, полученном от субъекта, цитологию и/или гистологию. Точные критерии ответа могут быть выбраны любым подходящим способом при условии, что при сравнении групп субъектов и/или опухолей сравниваемые группы оцениваются на основе тех же или сопоставимых критериев для определения частоты ответа. Специалист в данной области техники сможет выбрать подходящие критерии.
[155] Риск: Как будет понятно из контекста, «риск» заболевания, расстройства и/или патологического состояния относится к вероятности того, что у конкретного субъекта разовьется заболевание, расстройство и/или патологическое состояние. В некоторых вариантах осуществления риск выражается в процентах. В некоторых вариантах осуществления составляет от 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90 и вплоть до 100%. В некоторых вариантах осуществления риск выражается как риск относительно риска, связанного с эталонным образцом или группой эталонных образцов. В некоторых вариантах осуществления эталонный образец или группа эталонных образцов имеют известный риск заболевания, расстройства, патологического состояния и/или явления. В некоторых вариантах осуществления эталонный образец или группа эталонных образцов взяты от субъектов, сравнимых с конкретным субъектом. В некоторых вариантах осуществления относительный риск составляет 0,1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более.
[156] Серотип: Используемый в данном документе термин «серотип», также называемый сероваром, относится к отдельной вариации внутри одного вида бактерий или вируса или среди иммунных клеток разных субъектов. Эти микроорганизмы, вирусы или клетки классифицируются вместе на основе антигенов их клеточной поверхности, что позволяет проводить эпидемиологическую классификацию организмов на уровне подвидов. Группа сероваров с общими антигенами может называться серогруппой или иногда серокомплексом.
[157] Субъект: Используемый в данном документе термин «субъект» относится к организму, обычно млекопитающему (например, человеку, в некоторых вариантах осуществления, включая пренатальные человеческие формы). В некоторых вариантах осуществления субъект страдает соответствующим заболеванием, расстройством или патологическим состоянием. В некоторых вариантах осуществления субъект предрасположен к заболеванию, расстройству или патологическому состоянию. В некоторых вариантах осуществления у субъекта проявляется один или более симптомов или характеристик заболевания, расстройства или патологического состояния. В некоторых вариантах осуществления субъект не проявляет никаких симптомов или характеристик заболевания, расстройства или патологического состояния. В некоторых вариантах осуществления субъект представляет собой субъекта с одной или более признаками, характерными для предрасположенности к или риска развития заболевания, расстройства или патологического состояния. В некоторых вариантах осуществления субъект представляет собой пациента. В некоторых вариантах осуществления субъект представляет собой субъект, которому поставлен диагноз и/или назначена терапия.
[158] Превосходящая Используемый в данном документе термин «превосходящая» в контексте оценки исследуемой фармацевтической композиции относится к исследуемой фармацевтической композиции, которая работает (например, с точки зрения иммуногенности и/или функционального титра антител, генерируемых исследуемой композицией) лучше, чем эталонная композиция. В некоторых вариантах осуществления большая эффективность демонстрируется, когда верхняя граница 95% доверительного интервала (ДИ) для соотношения средних геометрических титров (GMT) для исследуемой фармацевтической композиции к контрольной композиции составляет по меньшей мере 1,3 или выше, включая, например, по меньшей мере 1,4, по меньшей мере 1,5, по меньшей мере 2, по меньшей мере 2,5, по меньшей мере 3, по меньшей мере 4 или выше. Например, в некоторых вариантах осуществления иммуногенная композиция или вакцина, описанная в данном документе, превосходит эталонную вакцину (например, PCV13 или PPSV23), когда верхняя граница 95% доверительного интервала (ДИ) для соотношения средних геометрических титров (GMT) для иммуногенной композиции или вакцины по сравнению с эталонной вакциной составляет по меньшей мере 1,3 или выше, включая, например, по меньшей мере 1,4, по меньшей мере 1,5, по меньшей мере 2, по меньшей мере 2,5, по меньшей мере 3, по меньшей мере 4 или выше. В некоторых вариантах осуществления иммуногенная композиция или вакцина, описанная в данном документе, превосходит эталонную вакцину (например, PCV13 или PPSV23), когда двусторонний 95% доверительный интервал (ДИ) для соотношения средних геометрических титров (GMT) для иммуногенной композиции или вакцины по сравнению с эталонной вакциной исключает ноль.
[159] Предрасположенность к: Субъект, который «предрасположен к» заболеванию, расстройству или патологическому состоянию, находится в группе риска развития заболевания, расстройства или патологического состояния. В некоторых вариантах осуществления субъект, который является предрасположенным к заболеванию, расстройству или патологическому состоянию, не проявляет никаких симптомов заболевания, расстройства или патологического состояния. В некоторых вариантах осуществления у субъекта, который является предрасположенным к заболеванию, расстройству или патологическому состоянию, не диагностировано заболевание, расстройство и/или патологическое состояние. В некоторых вариантах осуществления субъект, который предрасположен заболеванию, расстройству или патологическому состоянию, представляет собой субъекта, который подвергался воздействию условий, связанных с развитием заболевания, расстройства или патологического состояния. В некоторых вариантах осуществления риск развития заболевания, расстройства и/или патологического состояния представляет собой популяционный риск (например, члены семей субъектов, страдающих этим заболеванием, расстройством или патологическим состоянием).
[160] Симптомы уменьшаются: в данном контексте «симптомы уменьшаются», когда один или более симптомов конкретного заболевания, расстройства или патологического состояния уменьшаются по величине (например, интенсивности, степени тяжести и т. д.) и/или частоте, например, до статистически значимого и/или клинически значимого или релевантного уровня. Для ясности, задержка появления определенного симптома считается одной из форм уменьшения частоты этого симптома.
[161] Лечение: Используемый в данном документе термин «лечение» (также «лечить» или «процесс лечения») относится к любому применению терапии, которая частично или полностью снимает, уменьшает интенсивность, облегчает, ингибирует, задерживает начало, снижает степень тяжести и/или уменьшает частоту возникновения одного или более симптомов, признаков и/или причин конкретного заболевания, расстройства и/или патологического состояния. В некоторых вариантах осуществления такое лечение может проводиться для субъекта, который не проявляет признаков соответствующего заболевания, расстройства и/или патологического состояния, и/или субъекта, у которого проявляются только ранние признаки заболевания, расстройства и/или патологического состояния. Альтернативно или дополнительно, такое лечение может относиться к субъекту, у которого проявляется один или более установленных признаков соответствующего заболевания, расстройства и/или патологического состояния. В некоторых вариантах осуществления лечение может проводиться для субъекта, которому был поставлен диагноз соответствующего заболевания, расстройства и/или патологического состояния. В некоторых вариантах осуществления лечение может проводиться у субъекта, о котором известно, что он имеет один или более факторов предрасположенности, которые статистически коррелируют с повышенным риском развития соответствующего заболевания, расстройства и/или патологического состояния.
[162] Вакцинация: Используемый в данном документе термин «вакцинация» относится к введению композиции, предназначенной для генерации иммунного ответа, например, против болезнетворного агента. Для целей настоящего изобретения вакцинацию можно проводить до, во время и/или после воздействия болезнетворного агента, а в некоторых вариантах осуществления до, во время и/или вскоре после воздействия агента. В некоторых вариантах осуществления вакцинация включает многократные введения вакцинной композиции через соответствующие промежутки времени. В некоторых вариантах осуществления вакцинация инициирует иммунизацию.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[163] Настоящее изобретение, в общем, относится к композициям, системам и способам, которые включают новые комплексные белки и полисахариды, например, вакцины из комплексных белков и полисахаридов. Такие комплексы можно использовать, например, для индукции и/или повышения иммунопротективного ответа у субъектов, подверженных риску пневмококковой инфекции или страдающих от нее.
[164] Предыдущие попытки создания вакцины для защиты от пневмококковой инфекции имели ограниченную эффективность.
[165] Первая поливалентная полисахаридная конъюгированная вакцина Prevnar 7 (PCV7) от Wyeth была лицензирована в 2000 году в США и Европе. 10-валентная полисахаридная конъюгированная вакцина Synflorix (PCV10) от GlaxoSmithKline была лицензирована в Европе, но не в США, в 2009 году. Synflorix не был лицензирован в Соединенных Штатах Америки, потому что клинические исследования не продемонстрировали не меньшей эффективности у младенцев по сравнению с Prevnar 7; кроме того, несмотря на охват трех дополнительных серотипов по сравнению с Prevnar 7, Synflorix формально не охватывал клинически важный S. pneumoniae серотипа 19A. Кроме того, Synflorix изначально был разработан как 11-валентная полисахаридная конъюгированная вакцина (PCV11), но один серотип S. pneumoniae (серотип 3) был удален, когда клинические исследования показали отсутствие эффективности против этого серотипа, несмотря на иммуногенность.
[166] Поливалентная полисахаридная конъюгированная вакцина PCV-15 от Merck все еще проходит клинические исследования. PCV15 прошел клиническую оценку у взрослых, причем, по-видимому, она не уступает Prevnar 13 у взрослых. PCV15 также оказался не менее эффективной у детей раннего возраста, но затем не смогла соответствовать уровню неполноценности у младенцев, поэтому был возвращен в состав. Новый состав PCV15 в настоящее время исследуется у взрослых и младенцев.
[167] Компания Sanofi Pasteur провела оценку первой белковой вакцины на основе PspA. Раннее клиническое испытание (опубликованное в 2000 г., PMID: 10699322) представляло собой исследование фазы 1 с 5-125 мкг рекомбинантного PspA (rPspA), которое было связано с явным повышением уровней антител, антител, которые были реактивными с гетерологичными молекулами rPspA, и повышенное связывание постиммунных сывороток с 37 штаммами пневмококков, экспрессирующими различные клады PspA, и капсульными серотипами. Некоторые опасения были высказаны по поводу области PspA, которая имеет гомологию с сердечным миозином, и программа была прекращена Sanofi Pasteur.
[168] Еще одну белковую вакцину, основанную на комбинации трех белков, PhtD, пневмолизоида и PcpA, оценивала компания Sanofi Pasteur с 2011 по 2014 год. Вакцина прошла фазу 1 у взрослых, а затем была протестирована на детях раннего возраста (12-13 месяцев) и младенцах (6 недель). Исследование в Бангладеш показало иммуногенность; однако не было зарегистрировано никаких доказательств воздействия на носительство S. pneumoniae (представлено на ISPPD 2014; исследование не позволяло выявить небольшую разницу в распространенности носительства). Программа была прекращена компаний Sanofi Pasteur.
[169] Белковую вакцину на основе комбинации PhtD и пневмолизоида оценивали компанией GlaxoSmithKline с 2012 по 2016 год. Вакцина была признана безопасной и иммуногенной для всех возрастов (взрослые, дети раннего возраста, младенцы). Однако в двух дальнейших исследованиях младенцев, проведенных в Гамбии и нации навахо в Соединенных Штатах Америки, не было доказательств клинической эффективности (отсутствие воздействия на носительство S. pneumoniae в Гамбии или на средний отит в нации навахо). Программа была прекращена GlaxoSmithKline.
[170] Белковая вакцина GEN-004, основанная на комбинации трех белков, SP0148, SP1912 и SP2108 с адъювантом гидроксидом алюминия, была разработана и оценена компанией Genocea Biosciences. Было показано, что GEN-004 безопасен и иммуногенен у взрослых в фазе 1. Однако исследование фазы 2 преднамеренной пневмококковой инфекции, проведенное в Великобритании, не показало значительного влияния на носительство S. pneumoniae. Программа разработки GEN-004 была приостановлена в 2015 году.
[171] Живая аттенуированная сконструированная вакцина против Salmonella была разработана в Университете штата Аризона. Мутантные штаммы Salmonella typhi, сконструированные для экспрессии PspA, оценивались в клинических исследованиях фазе 1 у взрослых (PMID: 23916987) с 2009 по 2011 годы. Оценивали три разных штамма. О серьезных нежелательных явлениях не сообщали, но у одного пациента посев крови на Salmonella typhi был положительным. Ни один субъект не выделял вакцину с калом. Различий в результатах ИФА или ELISPOT между группами до и после вакцинации между группами не было. Вакцина была признана безопасной, но неиммуногенной, поэтому неэффективной, и разработка была остановлена.
[172] В настоящее время в США доступны две вакцины против S. pneumoniae. Вторая поливалентная полисахаридная конъюгированная вакцина компании Wyeth-Pfizer, Prevnar 13 (PCV13), была лицензирована в 2010 году в США и Европе. PCV13 был одобрен для предотвращения ИПЗ, вызванного 13 серотипами, содержащимися в вакцине, у детей, а также для профилактики пневмонии и ИПЗ у взрослых. В этой вакцине ковалентная конъюгация сахаридов из 13 серотипов пневмококка с белком мутантного дифтерийного анатоксина (CRM197) образует конъюгаты сахарид-белок, которые способны индуцировать Т-клеточный иммунный ответ против одного или более из 13 серотипов пневмококка, представленных сахаридами. [PREVNAR 13, инструкция по применению препарата, 2017].
[173] PCV13 формально не отвечала критериям «не меньшей эффективности» по сравнению с PCV7 и не была иммуногенной против нескольких серотипов. Однако включение S. pneumoniae серотипа 19A способствовало лицензированию PCV13, поскольку серотип 19A возник в период с 2000 по 2010 год как основная причина заболеваемости и смертности и был связан с устойчивостью к антибиотикам. В то время как инфекции, вызванные S. pneumoniae с множественной лекарственной устойчивостью серотипов, содержащихся в PCV13, по-видимому, уменьшились после утверждения этой вакцины, было отмечено увеличение числа инфекций, вызванных серотипами 35B, 23A, 23B и 15B с множественной лекарственной устойчивостью, которые являются лишь некоторыми из почти 100 известных серотипов S. pneumoniae, не включенных в PCV13. Также сообщалось, что PCV13 обладает минимальной активностью в отношении серотипа 3, поскольку его распространенность сохраняется в популяции [Richter et al, 2014].
[174] Вторая вакцина, PPSV23, представляет собой 23-валентную полисахаридную вакцину, разработанную Merck, и показана для предотвращения пневмококковой инфекции у взрослых старше 50 лет или у лиц старше 2 лет с повышенным риском пневмококковой инфекции. Он состоит из очищенных капсульных полисахаридов 23 серотипов пневмококков. Хотя эта вакцина обладает потенциалом защиты от большего числа серотипов по сравнению с PCV13, она не обеспечивает защиты от новых серотипов 35B, 23A и 23B. Кроме того, PPSV23 вызывает Т-независимый полисахаридный иммунный ответ, который стимулирует зрелые В-лимфоциты, но не Т-лимфоциты. Таким образом, эта вакцина индуцирует иммунный ответ, который не является ни длительным, ни анамнестическим при последующем заражении. PPSV23 не эффективен против колонизации. Кроме того, вакцины полисахаридного типа не используются у младенцев и детей младше 2 лет, потому что эти дети плохо реагируют на Т-независимые антигены [PNEUMOVAX 23, инструкция по применению препарата, 2017; CDC, 2010]. Данные демонстрируют, что PPSV23 может защищать взрослых и пожилых людей от ИПЗ; однако устойчивого эффекта в предотвращении пневмонии не наблюдалось [Gruber et al, 2008].
[175] Описанные в настоящее время новые комплексные белки и полисахариды, например, вакцины из комплексных белков и полисахаридов и их комбинации, отражают существенный прогресс по сравнению с предыдущими попытками разработки вакцины против S. pneumoniae и по сравнению с доступными в настоящее время вариантами иммунизации пациентов против пневмококковой инфекции. Такие новые комплексы и вакцины можно использовать, например, для индукции и/или повышения иммунопротективного ответа у субъектов, например, у субъектов, подверженных риску пневмококковой инфекции или страдающих от нее.
Иммуногенные комплексы
[176] Настоящее изобретение охватывает иммуногенные комплексы, которые содержат один или более полисахаридов и/или полипептидов S. pneumoniae.
[177] В некоторых вариантах осуществления иммуногенные комплексы представляют собой системы презентации множественных антигенов (MAPS) или основаны на них. Аспекты платформы MAPS были ранее описаны в WO2012/155007, содержание которой полностью включено в данный документ посредством ссылки и схематично показано на Фиг. 1. См. также Zhang et al, 2013.
[178] Как описано в данном документе, иммуногенные комплексы по изобретению включают один или более антигенных полипептидов, нековалентно связанных в комплекс с одним или более антигенными полисахаридами. В некоторых вариантах осуществления один или более антигенных полипептидов образуют комплекс посредством аффинного взаимодействия с одним или более антигенными полисахаридами. В некоторых вариантах осуществления иммуногенные комплексы по изобретению содержат один или более антигенных полипептидов, нековалентно связанных с одним или более антигенными полисахаридами с использованием одной или более пар аффинная молекула/комплементарная аффинная молекула. В некоторых вариантах осуществления иммуногенный комплекс содержит (i) первую аффинную молекулу, описанную в данном документе, конъюгированную с одним или более антигенными полисахаридами, и (ii) слитый белок, который представляет собой или содержит комплементарную аффинную молекулу, описанную в данном документе, и полипептид. В некоторых вариантах осуществления иммуногенный комплекс включает (i) множество первых аффинных молекул, описанных в данном документе, конъюгированных с одним или более антигенными полисахаридами, и (ii) слитый белок, который представляет собой или содержит комплементарную аффинную молекулу, описанную в данном документе, и полипептид. После ассоциации первой аффинной молекулы и комплементарной аффинной молекулы один или более антигенных полипептидов нековалентно связываются в комплекс с одним или более антигенными полисахаридами.
[179] В некоторых вариантах осуществления один или более антигенных полипептидов образуют комплекс посредством аффинного взаимодействия с одним антигенным полисахаридом. В некоторых вариантах осуществления иммуногенные комплексы по изобретению содержат один или более антигенных полипептидов, нековалентно связанных в комплекс с одним антигенным полисахаридом с использованием одной пары аффинная молекула/комплементарная аффинная молекула. В некоторых вариантах осуществления иммуногенные комплексы по изобретению содержат один или более антигенных полипептидов, нековалентно связанных в комплекс с одним антигенным полисахаридом с использованием одной или более пар аффинная молекула/комплементарная аффинная молекула. В некоторых вариантах осуществления каждая из пар аффинная молекула/комплементарная аффинная молекула является одинаковой, например, пары биотин/биотинсвязывающий фрагмент. В некоторых вариантах осуществления иммуногенный комплекс содержит (i) первую аффинную молекулу, описанную в данном документе, конъюгированную с одним антигенным полисахаридом, и (ii) слитый белок, который представляет собой или содержит комплементарную аффинную молекулу, описанную в данном документе, и полипептид. В некоторых вариантах осуществления иммуногенный комплекс содержит (i) множество первых аффинных молекул, описанных в данном документе, конъюгированных с одним антигенным полисахаридом, и (ii) слитый белок, который представляет собой или содержит комплементарную аффинную молекулу, описанную в данном документе, и полипептид. После ассоциации первой аффинной молекулы и комплементарной аффинной молекулы один или более антигенных полипептидов нековалентно связываются в комплекс с одним антигенным полисахаридом.
[180] В некоторых вариантах осуществления пара аффинная молекула/комплементарная аффинная молекула выбрана из одного или более из следующих: биотин/биотинсвязывающий фрагмент, антитело/антиген, фермент/субстрат, рецептор/лиганд, металл/металлсвязывающий белок, углевод/углеводсвязывающий белок, липид/липидсвязывающий белок и His-метка/связывающая His-метку молекула.
[181] В некоторых вариантах осуществления первая аффинная молекула представляет собой биотин (или его производное или фрагмент), а комплементарная аффинная молекула представляет собой фрагмент, например, биотинсвязывающий белок, или его биотинсвязывающий домен, или биотинсвязывающий фрагмент. В некоторых вариантах осуществления биотинсвязывающий фрагмент представляет собой ризавидин, авидин, стрептавидин, брадавидин, тамавидин, лентиавидин, зебавидин, нейтравидин, CaptAvidin™, или биотинсвязывающий домен, или их биотинсвязывающий фрагмент, или их комбинацию. В некоторых вариантах осуществления биотинсвязывающий фрагмент представляет собой ризавидин, или его биотинсвязывающий домен, или биотинсвязывающий фрагмент. В некоторых вариантах осуществления биотинсвязывающий фрагмент представляет собой или содержит полипептид SEQ ID NO: 1, или его биотинсвязывающий домен, или биотинсвязывающий фрагмент. В некоторых вариантах осуществления биотинсвязывающий фрагмент представляет собой или содержит полипептид SEQ ID NO: 2, или его биотинсвязывающий домен, или биотинсвязывающий фрагмент.
[182] В некоторых вариантах осуществления один или более антигенных полисахаридов представляют собой или получены из грамотрицательных бактерий и/или грамположительных бактерий. В некоторых вариантах осуществления один или более бактериальных антигенных полисахаридов представляют собой или получены из S. pneumoniae. В некоторых вариантах осуществления один или более антигенных полисахаридов представляют собой или получены из одного или более патогенов. В некоторых вариантах осуществления один или более антигенных полисахаридов представляют собой или получены из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 серотипов или штаммов патогена. В некоторых вариантах осуществления один или более антигенных полисахаридов представляют собой или получены из более чем 25 серотипов или штаммов патогена, например, 26, 27, 28, 29, 30, 35, 40, 45, или 50 серотипов или штаммов. В некоторых вариантах осуществления один или более антигенных полисахаридов представляют собой или получены из более чем 60, 70, 80, 90 или 100 серотипов или штаммов патогена.
[183] В некоторых вариантах осуществления один или более антигенных полисахаридов содержат одну или более аффинных молекул, конъюгированных с антигенными полисахаридами. В некоторых вариантах осуществления одна или более аффинных молекул содержат биотин или производные биотина.
[184] В некоторых вариантах осуществления антигенные полисахариды содержат множество аффинных молекул, конъюгированных с антигенными полисахаридами. В некоторых вариантах осуществления аффинные молекулы содержат биотин или производные биотина.
[185] В некоторых вариантах осуществления один или более антигенных полипептидов ковалентно связаны (например, слиты) с комплементарной аффинной молекулой, описанной в данном документе. В некоторых вариантах осуществления слитый белок содержит один или более антигенных полипептидов и комплементарную аффинную молекулу, описанные в данном документе. В некоторых вариантах осуществления комплементарная аффинная молекула представляет собой или содержит биотинсвязывающий фрагмент. В некоторых вариантах осуществления биотинсвязывающий фрагмент содержит ризавидин или его биотинсвязывающую часть.
[186] В некоторых вариантах осуществления антигенные полисахариды и/или антигенные полипептиды, которые могут быть включены в иммуногенные комплексы, получают рекомбинантно или синтетически. В некоторых вариантах осуществления антигенные полисахариды и/или антигенные полипептиды, которые могут быть включены в иммуногенные комплексы, выделены и/или получены из природных источников. В некоторых вариантах осуществления антигенные полисахариды и/или антигенные полипептиды, которые могут быть включены в иммуногенные комплексы, выделены из бактериальных клеток. Иллюстративные полисахариды и/или полипептиды описаны ниже.
Антигенные полипептиды
[187] В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс содержит один или более полипептидных антигенов. В некоторых вариантах осуществления полипептидный антиген представляет собой бактериальный полипептид, грибной полипептид и/или вирусный полипептид. В некоторых вариантах осуществления полипептидный антиген представляет собой полипептид S. pneumoniae или полипептид, полученный из него. В некоторых вариантах осуществления один или более полипептидных антигенов представляют собой полипептид патогена, отличного от S. pneumoniae, или полипептид, полученный из него. В некоторых вариантах осуществления один или более полипептидных антигенов содержат (i) полипептид из, или полученный от S. pneumoniae, и (ii) полипептид из, или полученный от патогена, отличного от S. pneumoniae. В некоторых вариантах осуществления иммуногенный комплекс содержит один или более из следующих антигенных полипептидов S. pneumoniae или их частей.
Полипептиды SP0785
[188] SP0785 представляет собой консервативный гипотетический белок S. pneumoniae, описанный в WO 2014/124228. В некоторых вариантах осуществления полипептид SP0785 представляет собой эффлюксный белок-транспортер, консервативный в штаммах S. pneumoniae. В некоторых вариантах осуществления полипептид SP0785 представляет собой или содержит полноразмерный полипептид SP0785. Например, в некоторых вариантах осуществления полноразмерный полипептид SP0785 имеет 399 аминокислот (38 кДа) и представлен аминокислотной последовательностью, указанной в SEQ ID NO: 10. Предполагается, что аминокислоты 1-32 из SEQ ID NO: 10 представляют собой сигнальную последовательность и трансмембранный домен полипептида SP0785 (аминокислоты 1-32 полноразмерного белка). В некоторых вариантах осуществления полипептид SP0785 содержит часть полипептида SP0785 (например, часть полипептида SP0785 SEQ ID NO: 10, которая содержит по меньшей мере 7, 8, 9, 10, 11, 12, 13, 14 , 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350 или более смежных аминокислот SEQ ID NO: 10). В некоторых вариантах осуществления часть полипептида SP0785 соответствует белку, имеющему аминокислоты 33-399 аминокислотной последовательности, указанной в SEQ ID NO: 10. В некоторых вариантах осуществления полипептид SP0785 содержит одно или более аминокислотных изменений (например, делецию, замену и/или вставку) из природной последовательности полипептида SP0785 дикого типа. Например, полипептид SP0785 может содержать аминокислотную последовательность, которая на по меньшей мере 60% или более (например, по меньшей мере 65%, 70%, 75%, 80%, 85%, 90%, 95% или 98%) идентична SEQ ID NO: 10 или его части (например, по меньшей мере 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 45, 50, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350 или более последовательных аминокислот последовательности, показанной в SEQ ID NO: 10). В качестве альтернативы полипептид SP0785 может содержать часть (например, по меньшей мере 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 45, 50, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350 или 400 последовательных аминокислот) последовательности, которая на по меньшей мере 60% или более (например, по меньшей мере 65%, 70%, 75%, 80%, 85%, 90%, 95% или 98%) идентична SEQ ID NO: 10. Нуклеотидная последовательность, кодирующая полипептид SP0785, предложена в данном документе как SEQ ID NO: 11.
Полипептиды SP1500
[189] SP1500 представляет собой белок S. pneumoniae, описанный в WO 2014/124228. В некоторых вариантах осуществления полипептид SP1500 представляет собой аминокислотный ABC-транспортер, полипептид, связывающий аминокислоты, консервативный во всех штаммах S. pneumoniae. В некоторых вариантах осуществления полипептид SP1500 представляет собой или содержит полноразмерный полипептид SP1500. Например, в некоторых вариантах осуществления полноразмерный полипептид SP1500 имеет 278 аминокислот (28 кДа) и представлен аминокислотной последовательностью, указанной в SEQ ID NO: 12. Предполагается, что аминокислоты 1-26 из SEQ ID NO: 12 являются сигнальной последовательностью полипептида SP1500 (аминокислоты 1-26 полноразмерного белка). В некоторых вариантах осуществления полипептид SP1500 содержит часть полипептида SP1500 (например, часть полипептида SP1500 SEQ ID NO: 12, которая содержит по меньшей мере 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, или более смежных аминокислот SEQ ID NO: 12). В некоторых вариантах осуществления часть полипептида SP1500 соответствует белку, имеющему аминокислоты 27-278 аминокислотной последовательности, указанной в SEQ ID NO: 12. В некоторых вариантах осуществления полипептид SP1500 содержит одно или более аминокислотных изменений (например, делецию, замену и/или вставку) из природной последовательности полипептида SP1500 дикого типа. Например, полипептид SP1500 может содержать аминокислотную последовательность, которая на по меньшей мере 60% или более (например, по меньшей мере 65%, 70%, 75%, 80%, 85%, 90%, 95% или 98%) идентична SEQ ID NO: 12 или его части (например, по меньшей мере 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 45, 50, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250 или более последовательных аминокислот последовательности, показанной в SEQ ID NO: 12). В качестве альтернативы полипептид SP1500 может содержать часть (например, по меньшей мере 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 45, 50, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250 или более последовательных аминокислот) последовательности, которая на по меньшей мере 60% или более (например, по меньшей мере 65%, 70%, 75%, 80%, 85%, 90%, 95% или 98%) идентична SEQ ID NO: 12. Нуклеотидная последовательность, кодирующая полипептид SP1500, предложена в данном документе как SEQ ID NO: 13.
[190] В некоторых вариантах осуществления последовательности нуклеиновых кислот, кодирующие полипептид SP0785 (SEQ ID NO: 10), полипептид SP1500 (SEQ ID NO: 12) и полипептид CP1 (SEQ ID NO: 6), представлены как SEQ ID NO: 11, 13 и 9, соответственно. Из-за вырожденности генетического кода специалисты в данной области техники поймут, что другие последовательности ДНК (включая последовательности с оптимизированными кодонами) могут кодировать эти полипептиды, а также другие, описанные в данном документе.
Слитые белки, содержащие антигенные полипептиды
[191] Описанные в данном документе антигенные полипептиды могут быть частью слитого белка. Например, в некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс содержит слитый белок, который представляет собой или содержит комплементарную аффинную молекулу и один или более антигенных полипептидов, описанных в данном документе. В некоторых вариантах осуществления слитый белок иммуногенного комплекса обладает свойствами носителя. В некоторых вариантах осуществления слитый белок иммуногенного комплекса обладает антигенными свойствами. В некоторых вариантах осуществления слитый белок иммуногенного комплекса обладает свойствами носителя и антигенными свойствами.
[192] В некоторых вариантах осуществления слитый белок иммуногенного комплекса содержит один или более линкеров и/или меток, например, гистидиновую метку. В некоторых вариантах осуществления линкер содержит полипептид, содержащий аминокислотную последовательность SEQ ID NO: 3 (GGGGSSS). В некоторых вариантах осуществления линкер содержит полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с последовательностью SEQ ID NO: 3. В некоторых вариантах осуществления линкер содержит аминокислотную последовательность AAA. В некоторых вариантах осуществления слитый белок иммуногенного комплекса содержит первый линкер, содержащий полипептид, содержащий аминокислотную последовательность SEQ ID NO: 3 (GGGGSSS), и второй линкер, содержащий аминокислотную последовательность AAA. В некоторых вариантах осуществления такой линкер может быть синтезирован или получен из аминокислотных остатков сайта рестрикции (например, сайта рестрикции Not I).
Комплементарные аффинные молекулы
[193] В некоторых вариантах осуществления комплементарная аффинная молекула содержит биотинсвязывающий фрагмент. В некоторых вариантах осуществления слитый белок иммуногенного комплекса содержит биотинсвязывающий фрагмент и один или более полипептидных антигенов. В некоторых вариантах осуществления слитый белок содержит биотинсвязывающий фрагмент и два или более полипептидных антигена. Используемый в данном документе термин «биотинсвязывающий фрагмент» относится к биотинсвязывающему белку, его биотинсвязывающему фрагменту или биотинсвязывающему домену.
[194] В некоторых вариантах осуществления в комплексах MAPS, описанных в данном документе, используется нековалентное связывание с высокой аффинностью (константа диссоциации [KD] ≈ 10-15M) между биотином и ризавидином, биотинсвязывающим белком, который не имеет значительной предсказанной гомологии с человеческими белками. Ризавидин, встречающийся в природе димерный белок из семейства белков авидина, был впервые обнаружен у Rhizobium etli, симбиотической бактерии фасоли. Ризавидин имеет только 22% аминокислотную идентичность с куриным авидином, белком, обычно обнаруживаемым в яйцах, но с высоким уровнем сохранения аминокислотных остатков, участвующих в связывании биотина. В образцах сыворотки человека, полученных от субъектов, подвергшихся действию авидина, перекрестной реактивности с ризавидином не наблюдается [Helppolainen et al, 2007], что позволяет предположить, что антитела к ризавидину не могут перекрестно реагировать с куриным авидином. Конъюгаты биотина использовали в нескольких клинических применениях без каких-либо нежелательных явлений [Buller et al, 2014; Paty et al, 2010; Lazzeri et al, 2004].
[195] В некоторых вариантах осуществления биотинсвязывающий фрагмент слитого белка содержит ризавидин или его биотинсвязывающий домен или биотинсвязывающий фрагмент, как дополнительно описано в WO 2012/155053, содержание которой полностью включено в данный документ посредством ссылки. В некоторых вариантах осуществления биотинсвязывающий фрагмент представляет собой полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с ризавидином, или его биотинсвязывающим доменом или биотинсвязывающим фрагментом. В некоторых вариантах осуществления биотинсвязывающий фрагмент содержит полипептид SEQ ID NO: 1 или его биотинсвязывающий домен или биотинсвязывающий фрагмент. В некоторых вариантах осуществления биотинсвязывающий фрагмент представляет собой или содержит полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с последовательностью SEQ ID NO: 1, или его биотинсвязывающий домен, или его биотинсвязывающий фрагмент. В некоторых вариантах осуществления биотинсвязывающий фрагмент содержит полипептид SEQ ID NO: 2 или его биотинсвязывающий домен или биотинсвязывающий фрагмент. В некоторых вариантах осуществления биотинсвязывающий фрагмент представляет собой или содержит полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с последовательностью SEQ ID NO: 2, или его биотинсвязывающий домен, или биотинсвязывающий фрагмент.
[196] В некоторых вариантах осуществления слитый белок представляет собой или содержит комплементарную аффинную молекулу, описанную в данном документе (например, биотинсвязывающий фрагмент, описанный в данном документе), и один или более полипептидов S. pneumoniae, или один или более полипептидов, полученных из него. В некоторых вариантах осуществления слитый белок иммуногенного комплекса представляет собой CP1, дополнительно описанный в предварительной заявке США № 62/730199, озаглавленной «Пневмококковые вакцины на основе слитого белка» и поданной 12 сентября 2018 г. («заявка 199»), а также в заявке РСТ, озаглавленной «Пневмококковые вакцины на основе слитого белка» и поданной 12 сентября 2019 г., в которой испрашивается приоритет по заявке 199, содержание каждой из которых полностью включено в данный документ посредством ссылки. В некоторых вариантах осуществления слитый белок содержит комплементарную аффинную молекулу, описанную в данном документе (например, биотинсвязывающий фрагмент, описанный в данном документе), и полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 4 (аминокислоты 33-399 S. pneumoniae SP0785), или его антигенный фрагмент, и полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 5 (аминокислоты 27-278 S. pneumoniae SP1500), или его антигенный фрагмент. В некоторых вариантах осуществления слитый белок содержит полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичность с последовательностью SEQ ID NO: 6. В некоторых вариантах осуществления слитый белок представляет собой или содержит комплементарную аффинную молекулу, описанную в данном документе (например, биотинсвязывающий фрагмент, описанный в данном документе), полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с SP0785, или его антигенный фрагмент, и полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с SP1500, или его антигенный фрагмент.
[197] В некоторых вариантах осуществления слитый белок иммуногенного комплекса содержит комплементарную аффинную молекулу, описанную в данном документе (например, биотинсвязывающий фрагмент, описанный в данном документе), и полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 4 (аминокислоты 33-399 S. pneumoniae SP0785), или его антигенный фрагмент. В некоторых вариантах осуществления слитый белок содержит комплементарную аффинную молекулу, описанную в данном документе (например, биотинсвязывающий фрагмент, описанный в данном документе), и полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 5 (аминокислоты 27-278 S. pneumoniae SP1500), или его антигенный фрагмент.
[198] В некоторых вариантах осуществления слитый белок иммуногенного комплекса содержит биотинсвязывающий фрагмент, который представляет собой или содержит полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с последовательностью SEQ ID NO: 1 (ризавидином), или его биотинсвязывающий фрагмент. В некоторых вариантах осуществления слитый белок содержит биотинсвязывающий фрагмент, который представляет собой полипептид или содержит полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с последовательностью SEQ ID NO: 2 (аминокислоты 45-179 ризавидина), или его биотинсвязывающий фрагмент. В некоторых вариантах осуществления слитый белок содержит полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 4 (аминокислоты 33-399 S. pneumoniae SP0785), или его антигенный фрагмент. В некоторых вариантах осуществления слитый белок содержит полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 5 (аминокислоты 27-278 S. pneumoniae SP1500), или его антигенный фрагмент.
[199] В некоторых вариантах осуществления слитый белок иммуногенного комплекса содержит каждое из следующего: (а) биотинсвязывающий фрагмент, который представляет собой или содержит полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с последовательностью SEQ ID NO: 1 (ризавидин), или его биотинсвязывающий фрагмент; (b) полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 4 (аминокислоты 33-399 S. pneumoniae SP0785), или его антигенный фрагмент; и (c) полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 5 (аминокислоты 27-278 S. pneumoniae SP1500), или его антигенный фрагмент. В некоторых вариантах осуществления слитый белок дополнительно содержит один или более линкеров.
[200] В некоторых вариантах осуществления слитый белок иммуногенного комплекса содержит каждое из следующего: (а) биотинсвязывающий фрагмент, который представляет собой или содержит полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности с последовательностью SEQ ID NO: 2 (аминокислоты 45-179 ризавидина), или его биотинсвязывающий фрагмент; (b) полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 4 (аминокислоты 33-399 S. pneumoniae SP0785), или его антигенный фрагмент; и (c) полипептид, содержащий аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 5 (аминокислоты 27-278 S. pneumoniae SP1500), или его антигенный фрагмент. В некоторых вариантах осуществления слитый белок дополнительно содержит один или более линкеров.
[201] В некоторых вариантах осуществления слитый белок иммуногенного комплекса представляет собой или содержит слитый белок CP1. В некоторых вариантах осуществления слитый белок CP1 содержит (а) биотинсвязывающий фрагмент, который представляет собой или содержит полипептид, имеющий по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99%. идентичности с последовательностью SEQ ID NO: 1 (ризавидин) или последовательностью SEQ ID NO: 2 (аминокислоты 45-179 ризавидина), или его биотинсвязывающий фрагмент; (b) первый полипептидный линкер, содержащий аминокислотную последовательность SEQ ID NO: 3 (GGGGSSS); (c) полипептид SP0785, описанный в данном документе; (d) второй полипептидный линкер, содержащий аминокислотную последовательность AAA; и (e) полипептид SP1500, описанный в данном документе. В некоторых вариантах осуществления такой слитый белок CP1 может дополнительно содержать метку обнаружения или очистки, например, His-метку. В некоторых таких вариантах осуществления слитый белок CP1 содержит полипептид SP1500 между биотинсвязывающим фрагментом и полипептидом SP0785. В некоторых вариантах осуществления слитый белок CP1 может содержать полипептид SP0785 между биотинсвязывающим фрагментом и полипептидом SP1500. В некоторых вариантах осуществления полипептид SP0785, включенный в слитый белок иммуногенного комплекса, представляет собой или содержит аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности с последовательностью SEQ ID NO: 4 (аминокислоты 33-399 S. pneumoniae SP0785), или его антигенный фрагмент. В некоторых вариантах осуществления полипептид SP1500, включенный в слитый белок иммуногенного комплекса, представляет собой или содержит аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности с последовательностью SEQ ID NO: 5 (аминокислоты 27-278 S. pneumoniae SP1500), или его антигенный фрагмент. В некоторых вариантах осуществления слитый белок содержит аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с последовательностью SEQ ID NO: 6. В некоторых вариантах осуществления слитый белок содержит аминокислотную последовательность SEQ ID NO: 6. В некоторых вариантах осуществления слитый белок состоит из аминокислотной последовательности SEQ ID NO: 6.
Антигенные полисахариды
[202] В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс содержит один или более полисахаридов S. pneumoniae. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс содержит один полисахарид S. pneumoniae. Капсульные полисахариды используются для различения серотипов S. pneumoniae. Существует не менее 97 полисахаридов различных серотипов S. pneumoniae, каждый из которых имеет различную химическую структуру. Обозначения серотипа, используемые в данном документе, являются обозначениями в соответствии с датской номенклатурой [Kauffmann et al, 1960; Geno et al, 2015]. (Примечание. Серотип 20 в номенклатуре США упоминается как серотип 20A в датской номенклатуре).
[203] В некоторых вариантах осуществления иммуногенный комплекс содержит один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48.
[204] В некоторых вариантах осуществления иммуногенный комплекс содержит один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F. В некоторых вариантах осуществления иммуногенный комплекс содержит один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенный комплекс содержит один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, и 20B.
[205] В некоторых вариантах осуществления иммуногенный комплекс содержит один капсульный полисахарид S. pneumoniae из, или полученный от, одного серотипа S. pneumoniae. В некоторых вариантах осуществления иммуногенный комплекс содержит один капсульный полисахарид S. pneumoniae из, или полученный от, одного серотипа S. pneumoniae, выбранного из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48. В некоторых вариантах осуществления иммуногенный комплекс содержит один капсульный полисахарид S. pneumoniae из, или полученный от, одного серотипа S. pneumoniae, выбранного из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенный комплекс содержит один капсульный полисахарид S. pneumoniae из, или полученный от, одного серотипа S. pneumoniae, выбранного из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенный комплекс содержит один капсульный полисахарид S. pneumoniae из, или полученный от, одного серотипа S. pneumoniae, выбранного из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F и 20B.
Способы выделения и очистки полисахаридов
[206] В некоторых вариантах осуществления изобретение обеспечивает способы очистки одного или более полисахаридов, описанных в данном документе, от одного или более клеточных компонентов бактерий. В некоторых вариантах осуществления способы включают очистку капсульных полисахаридов от одного или более клеточных компонентов бактерий.
[207] В некоторых вариантах осуществления бактерии являются грамотрицательными. В некоторых вариантах осуществления бактерии являются грамположительными. В некоторых вариантах осуществления бактерии представляют собой S. pneumoniae.
[208] В некоторых вариантах осуществления клеточные компоненты включают белок. В некоторых вариантах осуществления клеточные белки включают нуклеиновую кислоту. В некоторых вариантах осуществления клеточные компоненты включают липиды. В некоторых вариантах осуществления клеточные компоненты включают полисахариды. В некоторых вариантах осуществления клеточные компоненты являются частью лизата.
[209] В некоторых вариантах осуществления процессы очистки полисахаридов включают серию осаждения этанолом, отмывки неочищенных препаратов полисахаридов этанолом, диэтиловым эфиром и/или ацетоном и сушку в вакууме для получения очищенных продуктов. В некоторых вариантах осуществления стадия экстракции фенолом включена для очистки полисахаридов. В некоторых вариантах осуществления процесс очистки включает стадию осаждения CTAB (цетилтриметиламмоний бромид) в дополнение к стадиям осаждения этанолом и фенолом.
[210] На Фиг. 3 показаны иллюстративные структуры и химическая информация для капсульных полисахаридов S. pneumoniae, включенных в иммуногенные комплексы по изобретению. Все структуры взяты из Европейской Фармакопеи 9.0.
Способы биотинилирования полисахаридов
[211] В некоторых вариантах осуществления изобретение обеспечивает способы биотинилирования одного или более полисахаридов, описанных в данном документе. В некоторых вариантах осуществления способ включает взаимодействие очищенных полисахаридов с тетрафторборатом 1-циано-4-диметиламинопиридиния (CDAP) для активации гидроксильных групп в полисахаридах с последующим добавлением амин-ПЭГ-биотина, в условиях, которые приводят к ковалентному связыванию биотина с полисахаридами. В некоторых вариантах осуществления желаемый уровень биотинилирования достигается путем изменения соотношения CDAP и полисахарида. В некоторых вариантах осуществления биотинилированные полисахариды очищают фильтрованием для удаления остатков процесса, таких как непрореагировавший биотин, диметиламинопиридин, ацетонитрил, цианид и непрореагировавший глицин. В некоторых вариантах осуществления уровень биотинилирования полисахарида, описанный в данном документе, оптимизирован для уменьшения количества доступного биотина после комплексообразования MAPS.
Производство иммуногенных комплексов
[212] Настоящее изобретение включает способы производства иммуногенных комплексов, описанных в данном документе. В некоторых вариантах осуществления способ производства иммуногенных комплексов включает комплексообразование по меньшей мере одного биотинилированного полисахарида с по меньшей мере одним биотинсвязывающим слитым белком. В некоторых вариантах осуществления слитый белок содержит аминокислотную последовательность, имеющую по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с SEQ ID NO: 6.
[213] В некоторых вариантах осуществления среднее (например, среднее арифметическое) соотношение белка (например, антигенного белка) к полисахариду для множества иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [масса/масса]). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка к полисахариду множества иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белок: PS выбрано для повышения потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или для ингибирования колонизации любым пневмококком (независимо от серотипа полисахарида) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[214] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 1. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из или полученного от S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1, 7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты от, или для ингибирования колонизации любым пневмококком (независимо от серотипа полисахарида) посредством специфического к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[215] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 2. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из или полученного от S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1, 7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты от, или для ингибирования колонизации любым пневмококком (независимо от серотипа полисахарида) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[216] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 3. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из или полученного от S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1, 7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты от, или для ингибирования колонизации любым пневмококком (независимо от серотипа полисахарида) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[217] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 4. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из или полученного от S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты от, или для ингибирования колонизации любым пневмококком (независимо от серотипа полисахарида) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[218] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 5. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из или полученного от S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1, 7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты от, или для ингибирования колонизации любым пневмококком (независимо от серотипа полисахарида) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[219] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6A. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6A во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6A во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[220] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6B. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[221] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 7F. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[222] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 8. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из или полученного от S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты от, или для ингибирования колонизации любым пневмококком (независимо от серотипа полисахарида) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[223] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9N. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[224] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9V. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[225] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 10A. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10A во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10A во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[226] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 11A. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11A во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11A во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[227] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 12F. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[228] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 14. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты от, или для ингибирования колонизации любым пневмококком (независимо от серотипа полисахарида) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[229] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 15B. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[230] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 17F. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[231] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 18C. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[232] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19A. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19A во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19A во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[233] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19F. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[234] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 20B. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[235] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 22F. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[236] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 23F. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[237] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 33F. В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 1:1, 1,5:1, 2:1, 2,5:1, 3:1, 3,5:1, 4:1, 4,5:1, 5:1, 5,5:1, 6:1, 6,5:1, 7:1,7,5:1, 8:1, 8,5:1, 9:1, 9,5:1, или 10:1 (масса/масса [мас./мас.]). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 1:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 2:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 3:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 4:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 5:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 6:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 7:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 8:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 9:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 10:1 (мас./мас.). В некоторых вариантах осуществления среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов выбрано для усиления потенциала иммуногенности полисахарида (функции носителя) и/или для обеспечения защиты против, или ингибирования колонизации любым пневмококком (независимо от полисахарида серотипа) посредством специфичного к белку иммунного ответа. Иммуногенные композиции и вакцины по изобретению могут содержать смеси иммуногенных комплексов с различным средним соотношением белка к полисахариду.
[238] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 1, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 2, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 3, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 4, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 5, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 7F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 8, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(10) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9N, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(11) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9V, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(12) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 10А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(13) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 11А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляют от около 2,5:1 до около 3,5:1 (мас./мас.);
(14) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 12F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(15) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 14, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(16) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 15B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(17) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 17F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(18) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 18C, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(19) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляют от около 5,5:1 до около 6,5:1 (мас./мас.);
(20) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(21) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 20B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(22) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 22F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(23) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 23F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.); и
(24) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 33F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас).
[239] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 1, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 3, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 4, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 5, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 7F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9V, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 14, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(10) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 18C, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(11) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляют от около 5,5:1 до около 6,5:1 (мас./мас.);
(12) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(13) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 22F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(14) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 23F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.); и
(15) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 33F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас).
[240] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 2, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 8, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9N, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 10А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 11А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляют от около 2,5:1 до около 3,5:1 (мас./мас.);
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 12F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 15B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.);
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 17F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./мас.); и
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 20B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет от около 2,5:1 до около 3,5:1 (мас./маc).
[241] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 1, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 2, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 3, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет около 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 4, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 5, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 7F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 8, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(10) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9N, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(11) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9V, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(12) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 10А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(13) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 11A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11A во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(14) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 12F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(15) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 14, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(16) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 15B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(17) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 17F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(18) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 18C, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(19) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19A во множестве иммуногенных комплексов составляет приблизительно 5,5:1, 5,6:1, 5,7:1, 5,8:1, 5,9:1, 6:1, 6,1:1, 6,2:1, 6,3:1, 6,4:1, или 6,5:1 (мас./мас.);
(20) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(21) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 20B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(22) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 22F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(23) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 23F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.); и
(24) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 33F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.).
[242] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 1, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 3, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 4, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 5, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6A во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 7F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9V, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 14, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(10) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 18C, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(11) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19A во множестве иммуногенных комплексов составляет приблизительно 5,5:1, 5,6:1, 5,7:1, 5,8:1, 5,9:1, 6:1, 6,1:1, 6,2:1, 6,3:1, 6,4:1, или 6,5:1 (мас./мас.);
(12) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(13) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 22F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(14) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 23F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.); и
(15) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 33F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.).
[243] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 2, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 8, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9N, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 10A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10A во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 11A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11A во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 12F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 15B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.);
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 17F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.); и
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 20B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет приблизительно 2,5:1, 2,6:1, 2,7:1, 2,8:1, 2,9:1, 3:1, 3,1:1, 3,2:1, 3,3:1, 3,4:1, или 3,5:1 (мас./мас.).
[244] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 1, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 2, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 3, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 4, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 5, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 7F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 8, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(10) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9N, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(11) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9V, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(12) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 10А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(13) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 11А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляют от около 2,9:1 до около 3,1:1 (мас./мас.);
(14) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 12F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(15) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 14, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(16) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 15B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(17) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 17F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(18) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 18C, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(19) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляют от около 5,9:1 до около 6,1:1 (мас./мас.);
(20) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(21) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 20B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(22) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 22F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(23) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 23F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.); и
(24) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 33F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас).
[245] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 1, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 3, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 4, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 5, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 7F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9V, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 14, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(10) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 18C, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(11) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19А во множестве иммуногенных комплексов составляют от около 5,9:1 до около 6,1:1 (мас./мас.);
(12) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(13) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 22F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(14) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 23F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.); и
(15) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 33F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас).
[246] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 2, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 8, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9N, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 10А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10А во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 11А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11А во множестве иммуногенных комплексов составляют от около 2,9:1 до около 3,1:1 (мас./мас.);
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 12F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 15B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.);
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 17F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./мас.); и
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 20B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет от около 2,9:1 до около 3,1:1 (мас./маc).
[247] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 1, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет около 3:1;
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 2, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет около 3:1;
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 3, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет около 3:1;
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 4, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет около 3:1;
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 5, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет около 3:1;
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6А, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6А во множестве иммуногенных комплексов составляет около 3:1;
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет около 3:1;
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 7F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет около 3:1;
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 8, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет около 3:1;
(10) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9N, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет около 3:1;
(11) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9V, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет около 3:1;
(12) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 10A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10A во множестве иммуногенных комплексов составляет около 3:1;
(13) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 11A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11A во множестве иммуногенных комплексов составляет около 3:1;
(14) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 12F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет около 3:1;
(15) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 14, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет около 3:1;
(16) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 15B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет около 3:1;
(17) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 17F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет около 3:1;
(18) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 18C, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет около 3:1;
(19) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19A во множестве иммуногенных комплексов составляет около 6:1(мас./мас.);
(20) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет около 3:1;
(21) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 20B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет около 3:1;
(22) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 22F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет около 3:1;
(23) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 23F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет около 3:1; и
(24) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 33F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет около 3:1.
[248] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 1, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 1 во множестве иммуногенных комплексов составляет около 3:1;
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 3, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 3 во множестве иммуногенных комплексов составляет около 3:1;
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 4, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 4 во множестве иммуногенных комплексов составляет около 3:1;
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 5, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 5 во множестве иммуногенных комплексов составляет около 3:1;
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6A во множестве иммуногенных комплексов составляет около 3:1;
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 6B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 6B во множестве иммуногенных комплексов составляет около 3:1;
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 7F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 7F во множестве иммуногенных комплексов составляет около 3:1;
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9V, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9V во множестве иммуногенных комплексов составляет около 3:1;
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 14, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 14 во множестве иммуногенных комплексов составляет около 3:1;
(10) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 18C, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 18C во множестве иммуногенных комплексов составляет около 3:1;
(11) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19A во множестве иммуногенных комплексов составляет около 6:1(мас./мас.);
(12) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 19F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 19F во множестве иммуногенных комплексов составляет около 3:1;
(13) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 22F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 22F во множестве иммуногенных комплексов составляет около 3:1;
(14) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 23F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 23F во множестве иммуногенных комплексов составляет около 3:1; и
(15) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 33F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 33F во множестве иммуногенных комплексов составляет около 3:1.
[249] В некоторых вариантах осуществления вакцина или иммуногенная композиция содержит:
(1) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 2, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 2 во множестве иммуногенных комплексов составляет около 3:1;
(2) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 8, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 8 во множестве иммуногенных комплексов составляет около 3:1;
(3) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 9N, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 9N во множестве иммуногенных комплексов составляет около 3:1;
(4) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 10A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 10A во множестве иммуногенных комплексов составляет около 3:1;
(5) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 11A, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 11A во множестве иммуногенных комплексов составляет около 3:1;
(6) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 12F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 12F во множестве иммуногенных комплексов составляет около 3:1;
(7) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 15B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 15B во множестве иммуногенных комплексов составляет около 3:1;
(8) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 17F, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 17F во множестве иммуногенных комплексов составляет около 3:1; и
(9) множество иммуногенных комплексов, содержащих белок CP1 и капсульный полисахарид из, или полученный от, S. pneumoniae серотипа 20B, при этом среднее соотношение белка CP1 к капсульному полисахариду из, или полученному от, S. pneumoniae серотипа 20B во множестве иммуногенных комплексов составляет около 3:1.
Иммуногенные и вакцинные композиции
[250] Другой аспект изобретения относится к композициям, которые содержат один или более иммуногенных комплексов, описанных в данном документе. Например, иммуногенная композиция, например, вакцинная композиция, может содержать один или более иммуногенных комплексов, описанных в данном документе. В некоторых вариантах осуществления такие композиции могут содержать множество иммуногенных комплексов одного типа, описанных в данном документе. Например, композиция может содержать популяцию одного типа иммуногенного комплекса, где все иммуногенные комплексы содержат один и тот же антигенный полипептид и один и тот же антигенный полисахарид. Дополнительно или альтернативно такие композиции могут содержать множество иммуногенных комплексов более чем одного типа, описанных в данном документе. Например, композиция может содержать совокупность различных типов иммуногенных комплексов. В некоторых вариантах осуществления композиция может содержать совокупность иммуногенного комплекса первого типа и совокупность иммуногенного комплекса второго типа, где иммуногенный комплекс первого типа и второго типа имеют разные антигенные полипептиды и/или разные антигенные полисахариды. В некоторых вариантах осуществления композиция может содержать совокупность иммуногенного комплекса первого типа и совокупность иммуногенного комплекса второго типа, где первый и второй тип иммуногенного комплекса содержат один и тот же антигенный полипептид и разные антигенные полисахариды (например, полисахариды разных серотипов). В некоторых вариантах осуществления описанные в данном документе иммуногенные комплексы включены в фармацевтическую композицию. В некоторых вариантах осуществления фармацевтическая композиция может представлять собой вакцину. В некоторых вариантах осуществления фармацевтическая композиция содержит фармацевтически приемлемый носитель. В некоторых вариантах осуществления фармацевтическая композиция содержит адъювант.
[251] В некоторых вариантах осуществления иммуногенная композиция содержит один или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 40, 50 или более) видов иммуногенных комплексов, выбранных из следующего:
(1) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 1 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 2 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 3 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 4 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 5 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(9) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6D и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(10) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6E и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(11) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(12) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6G и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(13) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6H и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(14) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(15) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(16) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(17) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(18) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 8 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(19) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(20) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9L и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(21) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9N и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(22) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9V и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(23) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(24) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(25) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(26) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(27) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(28) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(29) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(30) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11D и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(31) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11E и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(32) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(33) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(34) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(35) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(36) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 13 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(37) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 14 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(38) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(39) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(40) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(41) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(42) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 16А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(43) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 16F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(44) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(45) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(46) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(47) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(48) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(49) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(50) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(51) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(52) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(53) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(54) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(55) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(56) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 21 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(57) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(58) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(59) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(60) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(61) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(62) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 24А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(63) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 24B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(64) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 24F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(65) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 25А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(66) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 25F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(67) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 27 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(68) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 28А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(69) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 28F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(70) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 29 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(71) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 31 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(72) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 32А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(73) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 32F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(74) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(75) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(76) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(77) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33D и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(78) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33E и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(79) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(80) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 34 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(81) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 35А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(82) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 35B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(83) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 35C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(84) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 35F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(85) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 36 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(86) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 37 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(87) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 38 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(88) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 39 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(89) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 40 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(90) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 41А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(91) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 41F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(92) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 42 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(93) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 43 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(94) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 44 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(95) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 45 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(96) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 46 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(97) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 47А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(98) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 47F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(99) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 48 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
[252] В некоторых вариантах осуществления иммуногенная композиция содержит один или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 21, 22, 23, или 24) видов иммуногенных комплексов, выбранных из следующего:
(1) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 1 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 2 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 3 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 4 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 5 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(9) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 8 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(10) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9N и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(11) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9V и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(12) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(13) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(14) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(15) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 14 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(16) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(17) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(18) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(19) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(20) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(21) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(22) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(23) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(24) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
[253] В некоторых вариантах осуществления вакцинная композиция содержит один или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15) видов выбранных иммуногенных комплексов из следующего:
(1) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 1 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 3 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 4 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 5 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9V и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(9) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 14 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(10) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(11) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(12) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(13) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(14) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(15) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
[254] В некоторых вариантах осуществления вакцинная композиция содержит один или более (например, 1, 2, 3, 4, 5, 6, 7, 8 или 9) видов иммуногенных комплексов, выбранных из следующего:
(1) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 2 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 8 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9N и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(9) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
Композиции вакцин
[255] В некоторых вариантах осуществления вакцинная композиция представляет собой поливалентную или поливалентную вакцину. В некоторых вариантах осуществления валентность вакцинной композиции относится к количеству видов иммуногенных комплексов, присутствующих в вакцинной композиции. Валентность вакцины, описанной в данном документе, не ограничена по отношению к общему количеству антигенов, присутствующих в указанной фармацевтической композиции, иммуногенном комплексе или вакцине, или к числу штаммов патогена, для которых введение указанной фармацевтической композиции, иммуногенного комплекса, иммуногенной композиции или вакцинной композиции может вызвать иммуннопротективный ответ. В неограничивающем примере композиция 24-валентной вакцины может содержать более 24 антигенных компонентов (например, пептидные и/или полисахаридные компоненты) и может индуцировать иммунопротективный ответ против более чем 24 патогенов или патогенных серотипов или штаммов.
[256] В некоторых вариантах осуществления вакцинная композиция содержит от 1 до 50 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит от 1 до 40 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит от 1 до 35 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит от 1 до 30 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит от 1 до 30 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит от 1 до 24 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит от 1 до 15 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит от 1 до 9 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит от 1 до 5 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцина представляет собой поливалентную вакцину.
[257] В некоторых вариантах осуществления вакцинная композиция содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, или 50 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит иммуногенный комплекс 1 типа. В некоторых вариантах осуществления вакцинная композиция содержит 2 вида иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 4 вида иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 6 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 7 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 8 вида иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 9 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 10 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 11 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 12 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 13 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 14 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 15 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 16 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 17 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 18 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 19 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 20 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 21 вид иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 22 вида иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 23 вида иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 24 вида иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 25 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 26 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 27 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 28 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 29 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 30 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 35 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 40 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 45 видов иммуногенных комплексов. В некоторых вариантах осуществления вакцинная композиция содержит 50 видов иммуногенных комплексов.
[258] В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахаридов в композиции вакцины от каждого иммуногенного комплекса примерно одинакова, например, присутствуют в массовом соотношении примерно 1:1. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 0,20 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 0,25 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 0,5 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 1 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 1,5 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 2 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 2,5 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 3 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 3,5 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 4 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 4,5 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 5 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 5,5 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 6 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 7 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 8 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 9 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 10 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 11 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 12 мкг. В некоторых вариантах осуществления масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, составляет более 12 мкг, например, 13 мкг, 14 мкг, 15 мкг, 16 мкг, 17 мкг, 18 мкг, 19 мкг, 20 мкг, 21 мкг, 22 мкг, 23 мкг, 24 мкг, 25 мкг или более.
[259] В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахаридов в композиции вакцины, вносимая каждым иммуногенным комплексом, различна, например, присутствуют в массовом соотношении отличном от около 1:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахарида в вакцинной композиции, вносимая первым иммуногенным комплексом и вторым иммуногенным комплексом, составляет 1:2. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахарида в вакцинной композиции, вносимая первым иммуногенным комплексом и вторым иммуногенным комплексом, составляет 1:3. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахарида в вакцинной композиции, вносимая первым иммуногенным комплексом и вторым иммуногенным комплексом, составляет 1:4. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахарида в вакцинной композиции, вносимая первым иммуногенным комплексом и вторым иммуногенным комплексом, составляет 1:5. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахарида в вакцинной композиции, вносимая первым иммуногенным комплексом и вторым иммуногенным комплексом, составляет 1:6. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахарида в вакцинной композиции, вносимая первым иммуногенным комплексом и вторым иммуногенным комплексом, составляет 1:7. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахарида в вакцинной композиции, вносимая первым иммуногенным комплексом и вторым иммуногенным комплексом, составляет 1:8. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахарида в вакцинной композиции, вносимая первым иммуногенным комплексом и вторым иммуногенным комплексом, составляет 1:9. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что масса полисахарида в вакцинной композиции, вносимая первым иммуногенным комплексом и вторым иммуногенным комплексом, составляет 1:10. В некоторых вариантах осуществления вакцинная композиция вакцины содержит смесь иммуногенных комплексов, так что масса полисахарида в вакцине, вносимая иммуногенным комплексом, находится в диапазоне от около 0,20 мкг до около 6 мкг. В некоторых вариантах осуществления вакцинная композиция вакцины содержит смесь иммуногенных комплексов, так что масса полисахарида в вакцине, вносимая иммуногенным комплексом, находится в диапазоне от около 0,20 мкг до около 12 мкг. В некоторых вариантах осуществления вакцинная композиция содержит смесь иммуногенных комплексов, так что масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, находится в диапазоне от около 0,20 мкг до около 20 мкг. В некоторых вариантах осуществления вакцинная композиция содержит смесь иммуногенных комплексов, так что масса полисахаридов в вакцине, вносимая каждым иммуногенным комплексом, находится в диапазоне от около 0,20 мкг до около 40 мкг.
[260] В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), примерно одинакова, например, присутствует в массовом соотношении белок: PS около 1:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), присутствует в массовом соотношении белок: PS около 2:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), присутствует в массовом соотношении белок: PS около 3:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), присутствует в массовом соотношении белок: PS около 4:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), присутствует в массовом соотношении белок: PS около 5:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), присутствует в массовом соотношении белок: PS около 6:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), присутствует в массовом соотношении белок: PS около 7:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), присутствует в массовом соотношении белок: PS около 8:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), присутствует в массовом соотношении белок: PS около 9:1. В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что совокупная масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом (например, в иммуногенной композиции), присутствует в массовом соотношении белок: PS около 10:1.
[261] В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 0,20 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 0,40 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 1 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждым иммуногенным комплексом, составляет около 2 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 3 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 4 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 5 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 6 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 7 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 8 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 9 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 10 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 11 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 12 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 14 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 16 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 18 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 20 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 21 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 22 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 23 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 24 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 25 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 30 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 40 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 50 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 60 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 70 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 80 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 90 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 100 мкг. В некоторых вариантах осуществления совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждой иммуногенной композицией, составляет около 110 мкг.
[262] В некоторых вариантах осуществления вакцинная композиция содержит два или более видов иммуногенных комплексов (например, в иммуногенных композициях) в таких количествах, что общая масса полисахаридов и полипептидов в вакцинной композиции, вносимая каждым иммуногенным комплексом, является различной, например, присутствуют в массовом соотношении белок: PS отличном от около 1:1, например, соотношение белок: PS составляет 2:1, 3:1, 4:1. 5:1. 6:1, 7:1, 8:1, 9:1, или 10:1. В некоторых вариантах осуществления вакцинная композиция содержит смесь иммуногенных комплексов, так что совокупная масса полисахаридов и полипептидов в вакцине, вносимая каждым иммуногенным комплексом, составляет от около 0,4 мкг до около 110 мкг.
[263] В некоторых вариантах осуществления вакцинная композиция содержит один или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 40, 50 или более) видов иммуногенных комплексов, выбранных из следующего:
(1) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 1 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 2 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 3 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 4 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 5 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(9) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6D и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(10) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6E и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(11) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(12) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6G и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(13) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6H и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(14) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(15) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(16) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(17) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(18) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 8 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(19) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(20) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9L и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(21) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9N и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(22) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9V и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(23) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(24) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(25) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(26) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(27) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(28) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(29) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(30) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11D и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(31) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11E и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(32) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(33) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(34) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(35) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(36) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 13 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(37) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 14 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(38) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(39) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(40) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(41) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(42) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 16А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(43) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 16F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(44) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(45) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(46) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(47) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(48) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(49) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(50) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(51) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(52) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(53) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(54) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(55) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(56) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 21 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(57) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(58) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(59) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(60) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(61) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(62) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 24А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(63) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 24B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(64) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 24F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(65) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 25А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(66) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 25F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(67) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 27 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(68) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 28А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(69) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 28F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(70) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 29 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(71) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 31 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(72) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 32А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(73) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 32F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(74) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(75) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(76) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(77) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33D и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(78) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33E и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(79) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(80) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 34 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(81) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 35А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(82) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 35B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(83) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 35C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(84) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 35F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(85) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 36 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(86) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 37 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(87) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 38 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(88) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 39 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(89) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 40 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(90) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 41А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(91) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 41F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(92) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 42 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(93) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 43 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(94) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 44 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(95) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 45 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(96) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 46 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(97) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 47А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(98) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 47F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(99) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 48 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
[264] В некоторых вариантах осуществления вакцинная композиция содержит два или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 21, 22, 23 или 24) видов выбранных иммуногенных комплексов из следующего:
(1) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 1 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 2 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 3 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 4 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 5 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(9) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 8 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(10) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9N и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(11) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9V и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(12) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(13) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(14) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(15) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 14 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(16) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(17) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(18) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(19) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(20) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(21) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(22) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(23) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(24) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
[265] В некоторых вариантах осуществления вакцинная композиция содержит два или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, или 15) видов выбранных иммуногенных комплексов из следующего:
(1) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 1 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 3 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 4 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 5 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9V и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(9) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 14 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(10) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(11) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(12) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(13) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(14) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(15) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
[266] В некоторых вариантах осуществления вакцинная композиция содержит два или более (например, 2, 3, 4, 5, 6, 7, 8, или 9) видов иммуногенных комплексов, выбранных из следующего:
(1) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 2 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 8 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9N и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(9) иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
[267] В некоторых вариантах осуществления вакцинная композиция содержит следующее:
(1) первый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 1 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) второй иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 2 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) третий иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 3 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) четвертый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 4 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) пятый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 5 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) шестой иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) седьмой иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) восьмой иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(9) девятый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 8 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(10) десятый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9N и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(11) одиннадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9V и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(12) двенадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10A и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(13) тринадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(14) четырнадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(15) пятнадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 14 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(16) шестнадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(17) семнадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(18) восемнадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(19) девятнадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19A и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(20) двадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(21) двадцать первый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(22) двадцать второй иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(23) двадцать третий иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(24) двадцать четвертый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
[268] В некоторых вариантах осуществления вакцинная композиция содержит следующее:
(1) первый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 1 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) второй иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 3 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) третий иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 4 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) четвертый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 5 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) пятый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) шестой иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 6B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) седьмой иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 7F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) восьмой иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 8 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(9) девятый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 14 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(10) десятый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 18C и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(11) одиннадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19A и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(12) двенадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 19F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(13) тринадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 22F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(14) четырнадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 23F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(15) пятнадцатый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 33F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
[269] В некоторых вариантах осуществления вакцинная композиция содержит следующее:
(1) первый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 2 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(2) второй иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 8 и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(3) третий иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 9N и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(4) четвертый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 10А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(5) пятый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 11А и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(6) шестой иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 12F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(7) седьмой иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 15B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом;
(8) восьмой иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 17F и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом; и
(9) девятый иммуногенный комплекс, содержащий биотинилированный капсульный полисахарид S. pneumoniae серотипа 20B и один или более слитых белков CP1, нековалентно связанных в комплекс с биотинилированным полисахаридом.
Конъюгированные иммуногенные комплексы; иммуногенные и вакцинные композиции, содержащие тоже самое
[270] В некоторых вариантах осуществления один или более полипептидов (например, антигенные полипептиды) иммуногенных комплексов конъюгированы с одним или более полисахаридами. В некоторых вариантах осуществления один или более конъюгированных полисахаридов содержат капсульный полисахарид S. pneumoniae. В некоторых вариантах осуществления один или более полипептидов конъюгированного иммуногенного комплекса содержат антигенный полипептид S. pneumoniae. В некоторых вариантах осуществления антигенный полипептид конъюгированного иммуногенного комплекса представляет собой или содержит слитый белок. В некоторых таких вариантах осуществления слитый белок конъюгированного иммуногенного комплекса представляет собой или содержит слитый белок CP1.
[271] В некоторых вариантах осуществления конъюгированный иммуногенный комплекс содержит один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48. В некоторых вариантах осуществления конъюгированный иммуногенный комплекс содержит один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F. В некоторых вариантах осуществления иммуногенный комплекс содержит один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенный комплекс содержит один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, и 20B.
[272] В некоторых вариантах осуществления конъюгированный иммуногенный комплекс содержит следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[273] В некоторых вариантах осуществления конъюгированный иммуногенный комплекс содержит следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[274] В некоторых вариантах осуществления конъюгированный иммуногенный комплекс содержит следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F и 33F, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[275] В некоторых вариантах осуществления конъюгированный иммуногенный комплекс содержит следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, и 20B, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[276] В некоторых вариантах осуществления иммуногенная композиция содержит один или более конъюгированных иммуногенных комплексов, содержащих следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48,
причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[277] В некоторых вариантах осуществления иммуногенная композиция содержит один или более конъюгированных иммуногенных комплексов, содержащих следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[278] В некоторых вариантах осуществления иммуногенная композиция содержит один или более конъюгированных иммуногенных комплексов, содержащих следующее:
(a) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F и 33F, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[279] В некоторых вариантах осуществления иммуногенная композиция содержит один или более конъюгированных иммуногенных комплексов, содержащих следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, и 20B, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[280] В некоторых вариантах осуществления вакцинная композиция содержит один или более конъюгированных иммуногенных комплексов, содержащих следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F, и 48,
причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[281] В некоторых вариантах осуществления вакцинная композиция содержит один или более конъюгированных иммуногенных комплексов, содержащих следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[282] В некоторых вариантах осуществления вакцинная композиция содержит один или более конъюгированных иммуногенных комплексов, содержащих следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F и 33F, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
[283] В некоторых вариантах осуществления вакцинная композиция содержит один или более конъюгированных иммуногенных комплексов, содержащих следующее:
(а) один или более белков CP1; и
(b) один или более капсульных полисахаридов S. pneumoniae из, или полученных от, одного или более серотипов S. pneumoniae, выбранных из 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, и 20B, причем один или более белков CP1 ковалентно присоединены к одному или более полисахаридам.
Применение иммуногенных и вакцинных композиций
[284] В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс, который содержит один или более антигенных полисахаридов, отличается тем, что один или более из потенциалов опсонизации или иммунного ответа на один или более антигенных полисахаридов увеличиваются по сравнению с предопределенным уровнем, как измерено с помощью ИФА и или с помощью функционального анализа антител. В некоторых вариантах осуществления один или более из потенциалов опсонизации, иммунного ответа на один или более антигенных полисахаридов увеличиваются по меньшей мере в 1, 2, 3, 4 или 5 раз относительно предопределенного уровня, как измерено с помощью ИФА и/или функционального анализа антител. В некоторых вариантах осуществления предопределенный уровень представляет собой предиммунный уровень. В некоторых вариантах осуществления предопределенный уровень представляет собой предиммунный уровень. В некоторых вариантах осуществления один или более полипептидных антигенов являются белками-носителями для одного или более антигенных полисахаридов.
[285] В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует иммунный ответ против одного или более патогенов у субъекта на уровне выше, чем композиция, содержащая только антигенный полисахарид. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует иммунный ответ против одного или более патогенов у субъекта на уровне выше, чем композиция, содержащая только полипептидный антиген. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует протективный иммунный ответ.
[286] В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует иммунный ответ против S. pneumoniae. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует иммунный ответ против одного или более серотипов S. pneumoniae. В некоторых вариантах осуществления такой иммунный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанный в данном документе иммуногенный комплекс содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такой иммунный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанный иммуногенный комплекс не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такой иммунный ответ может быть направлен против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанный в данном документе иммуногенный комплекс (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует протективный иммунный ответ против одного или более серотипов S. pneumoniae. В некоторых вариантах осуществления такой защитный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанный в данном документе иммуногенный комплекс содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такой протективный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанный в данном документе иммуногенный комплекс не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такой протективный ответ может быть направлен против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанный в данном документе иммуногенный комплекс (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах.
[287] В некоторых вариантах осуществления иммунный ответ представляет собой образование антител или ответ В-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой ответ Т-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ представляет собой ответ CD4+ T-клеток, включая ответ TH1, TH2, или TH17 или ответ CD8+ T-клеток, или ответ CD4+ и CD8+ T-клеток, или ответ CD4-/CD8- T-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой образование антител или ответ В-клеток и ответ Т-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой образование антител или ответ В-клеток, ответ Т-клеток и врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ представляет собой протективный иммунный ответ.
[288] В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует продукцию антител против одного или более патогенов у субъекта на уровне выше, чем композиция, содержащая только антигенный полисахарид. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует продукцию антител против одного или более патогенов у субъекта на уровне выше, чем композиция, содержащая только полипептидный антиген.
[289] В некоторых вариантах осуществления иммуногенная композиция или вакцина, описанная в данном документе, при введении субъекту индуцирует иммунный ответ против одного или более патогенов у субъекта на уровне выше, чем композиция, содержащая только антигенный полисахарид. В некоторых вариантах осуществления иммуногенная композиция или вакцина, описанная в данном документе, при введении субъекту индуцирует иммунный ответ против одного или более патогенов у субъекта на уровне выше, чем композиция, содержащая только полипептидный антиген. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует протективный иммунный ответ.
[290] Описанные в данном документе иммуногенные композиции и вакцины против S. pneumoniae могут быть использованы для профилактического и/или терапевтического лечения S. pneumoniae. Соответственно, в данной заявке предложен способ иммунизации субъекта, страдающего от инфекции, вызванной S. pneumoniae, или восприимчивого к ней, включающий введение иммунологически эффективного количества любой из иммуногенных композиций или вакцинных составов, описанных в данном документе. Субъект, получающий вакцинацию, может быть мужчиной или женщиной, а также младенцем, ребенком, подростком или взрослым. В некоторых вариантах осуществления субъектом, которого лечат, является человек. В других вариантах осуществления субъект не является человеком. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует протективный иммунный ответ против одного или более серотипов S. pneumoniae.
[291] В профилактических вариантах осуществления композицию вакцины (например, описанную и/или используемую в данном документе) вводят субъекту для индукции иммунного ответа, который может помочь защитить от инвазии S. pneumoniae, например, путем защиты от колонизации, первой и необходимой стадии развития болезни. В некоторых вариантах осуществления такой иммунный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, при этом описанная в данном документе вакцинная композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. В некоторых вариантах осуществления такой иммунный ответ может быть направлен против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, при этом описанная в данном документе вакцинная композиция содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах (невакцинных типах, NVT). В некоторых вариантах осуществления такой иммунный ответ может быть направлен против двух или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) серотипов Streptococcus pneumoniae, причем описанная в данном документе вакцинная композиция (i) содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах; и (ii) не содержит полисахарид(-ы), присутствующий по меньшей мере в одном или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) таких серотипах. Таким образом, в некоторых аспектах способ ингибирования инфицирования S. pneumoniae у неколонизированных или неинфицированных субъектов. В другом аспекте способ может сократить продолжительность колонизации у субъекта, который уже колонизирован.
[292] В терапевтических вариантах осуществления вакцина может вводиться субъекту, страдающему инфекцией, вызванной S. pneumoniae, в количестве, достаточном для лечения субъекта. В данном случае лечение субъекта относится к уменьшению симптомов S. pneumoniae и/или бактериальной нагрузки и/или осложнений у инфицированного субъекта. В некоторых вариантах осуществления лечение субъекта относится к уменьшению продолжительности симптомов или осложнений или снижению интенсивности симптомов или осложнений. В некоторых вариантах осуществления вакцина снижает трансмиссивность S. pneumoniae от вакцинированного субъекта. В определенных вариантах осуществления описанные выше уменьшения чего-либо составляют по меньшей мере 25%, 30%, 40%, 50%, 60%, 70%, 80% или 90%.
[293] В терапевтических вариантах осуществления вакцину вводят субъекту после инфицирования. Вакцину можно вводить вскоре после заражения, например, до проявления симптомов или осложнений, или можно вводить во время или после проявления симптомов или осложнений.
[294] В некоторых вариантах осуществления вакцинные композиции по изобретению обеспечивают защитный иммунитет, позволяя вакцинированному субъекту проявлять отсроченное начало симптомов или осложнений или сниженной степени тяжести выраженные симптомы или осложнения в результате воздействия вакцины на него. В определенных вариантах осуществления снижение степени тяжести симптомов или осложнений составляет по меньшей мере 25%, 40%, 50%, 60%, 70%, 80% или 90%. В конкретных вариантах осуществления вакцинированные субъекты могут не проявлять никаких симптомов или осложнений при контакте с S. pneumoniae, могут не колонизироваться S. pneumoniae или и то, и другое. Защитный иммунитет, как правило, достигается одним или более из следующих механизмов: мукозальным, гуморальным или клеточным иммунитетом. Мукозальный иммунитет в первую очередь обусловлен секреторными антителами IgA (sIGA) на поверхности слизистой оболочки дыхательных, желудочно-кишечных и мочеполовых путей. Антитела sIGA образуются после серии событий, опосредованных антигенпроцессирующими клетками, B- и T-лимфоцитами, которые приводят к продукции sIGA B-лимфоцитами на тканях тела, выстланных слизистой оболочкой. Гуморальный иммунитет, как правило, обусловлен антителами IgG и антителами IgM в сыворотке крови. Клеточный иммунитет может быть достигнут за счет цитотоксических Т-лимфоцитов или гиперчувствительности замедленного типа с участием макрофагов и Т-лимфоцитов, а также других механизмов с участием Т-клеток без необходимости в антителах. В частности, клеточный иммунитет может быть опосредован клетками TH1 или TH17.
[295] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцирует иммунный ответ против S. pneumoniae. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцирует иммунный ответ против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или более) серотипов S. pneumoniae. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцирует иммунный ответ против всех серотипов S. pneumoniae, содержащихся в такой иммуногенной композиции или вакцине. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует защитный иммунный ответ против одного или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или более) серотипов S. pneumoniae. В некоторых вариантах осуществления описанный в данном документе иммуногенный комплекс при введении субъекту индуцирует протективный иммунный ответ против всех серотипов S. pneumoniae, содержащихся в такой иммуногенной композиции или вакцине.
[296] В некоторых вариантах осуществления иммунный ответ представляет собой образование антител или ответ В-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой ответ Т-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ представляет собой ответ CD4+ T-клеток, включая ответ TH1, TH2, или TH17, или ответ CD8+ T-клеток, или ответ CD4+ и CD8+ T-клеток, или ответ CD4-/CD8- T-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой образование антител или ответ В-клеток и ответ Т-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой образование антител или ответ В-клеток, ответ Т-клеток и врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ представляет собой протективный иммунный ответ.
[297] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцирует у субъекта образование антител или В-клеточный ответ против одного или более патогенов на уровне выше, чем композиция, содержащая только антигенный полисахарид. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцирует у субъекта образование антител или В-клеточный ответ против одного или более патогенов на уровне выше, чем композиция, содержащая только полипептидный антиген. В некоторых вариантах осуществления иммунный ответ представляет собой протективный иммунный ответ.
[298] В некоторых вариантах осуществления иммуногенная композиция или вакцина, описанная в данном документе, при введении субъекту индуцирует ответ Т-клеток против одного или более патогенов у субъекта на уровне выше, чем композиция, содержащая только антигенный полисахарид. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцирует ответ Т-клеток против одного или более патогенов у субъекта на уровне выше, чем композиция, содержащая только полипептидный антиген. В некоторых вариантах осуществления иммунный ответ представляет собой протективный иммунный ответ.
[299] В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают инфекцию, вызванную S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают инвазивное пневмококковое заболевание (ИПЗ), связанное с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают бактериемию, связанную с инфекцией, вызванной S. pneumoniae.В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают сепсис, связанное с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают поражение органов, связанное с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают менингит, связанный с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают пневмонию, связанную с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают средний отит, связанную с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают синусит, связанный с инфекцией, вызванной S. pneumoniae.
[300] В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения инфекции, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения инвазивного пневмококкового заболевания (ИПЗ), связанного инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения бактериемии, связанной инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения сепсиса, связанного с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения поражение органов, связанной с инфекцией S. pneumoniae. В некоторых вариантах осуществления при введении субъекту иммуногенная композиция или вакцина, описанные в настоящем документе, ингибируют или снижают частоту возникновения менингита, связанного с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения пневмонии, связанной с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения среднего отита, связанного с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения синусита, связанного с инфекцией, вызванной S. pneumoniae.
[301] В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести инфекции, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести инвазивного пневмококкового заболевания (ИПЗ), связанного с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести бактериемии, связанной с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести сепсиса, связанной с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести поражения органов, связанного с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести менингита, связанного с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести пневмонии, связанной с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести среднего отита, связанного с инфекцией, вызванной S. pneumoniae. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести синусита, связанного с инфекцией, вызванной S. pneumoniae.
[302] В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют трансмиссию S. pneumoniae от одного субъекта к другому субъекту. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют колонизацию S. pneumoniae у субъекта. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют колонизацию S. pneumoniae в носоглотке субъекта.
[303] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцируют иммунный ответ против одного или более патогенов у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцируют протективный иммунный ответ против одного или более патогенов у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[304] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PCV13 против одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PCV13 против каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления иммуногенность определяют путем измерения количества антитела к капсульному полисахариду одного или более серотипов S. pneumoniae. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[305] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PCV13 против одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PCV13 против каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления иммуногенность определяют путем измерения количества антитела к капсульному полисахариду одного или более серотипов S. pneumoniae. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[306] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PPSV23 против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A , 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PPSV23 против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенность определяют путем измерения количества антитела к капсульному полисахариду одного или более серотипов S. pneumoniae. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[307] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PPSV23 против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PPSV23 против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенность определяют путем измерения количества антитела к капсульному полисахариду одного или более серотипов S. pneumoniae. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[308] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PCV13 в комбинации с PPSV23 против одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PCV13 в комбинации с PPSV23 против каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PCV13 в комбинации с PPSV23 против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, не уступающую (например, иммуногенность не менее эффективную, чем) иммуногенности, которая вызывается введением PCV13 в комбинации с PPSV23 против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенность определяют путем измерения количества антитела к капсульному полисахариду одного или более серотипов S. pneumoniae. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23.
[309] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PCV13 в комбинации с PPSV23 против одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PCV13 в комбинации с PPSV23, против каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PCV13 в комбинации с PPSV23 против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность, превосходящую иммуногенность, вызываемую введением PCV13 в комбинации с PPSV23 против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенность определяют путем измерения количества антитела к капсульному полисахариду одного или более серотипов S. pneumoniae. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23.
[310] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 против одного или более из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 против каждого из серотипов S. pneumoniae 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 против (i) одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[311] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 против одного или более из S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 против каждого из серотипов S. pneumoniae 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 против (i) одного или более S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[312] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PPSV23 против одного или более из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PPSV23 против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PPSV23 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PPSV23 против (i) одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[313] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PPSV23 против одного или более из S. pneumoniae серотипов 6A и 20B. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PPSV23 против каждого из S. pneumoniae серотипов 6А и 20В. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PPSV23 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PPSV23 против (i) одного или более S. pneumoniae серотипов 6A и 20B, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[314] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 против одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 против каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 против (i) одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[315] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 против одного или более S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 против каждого из серотипов S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 против (i) одного или более S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[316] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PPSV23 против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PPSV23 против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PPSV23 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PPSV23 против (i) одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[317] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PPSV23 против одного или более серотипов S. pneumoniae 6A и 20B. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PPSV23 против каждого из S. pneumoniae серотипов 6А и 20В. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PPSV23 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PPSV23 против (i) одного или более S. pneumoniae серотипов 6A и 20B, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[318] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против одного или более из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против каждого из серотипов S. pneumoniae 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против одного или более из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против (i) одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против (i) одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23.
[319] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против одного или более из S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против каждого из серотипов S. pneumoniae 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который не меньше (например, титр функциональных антител не менее эффективный, чем) титра функциональных антител, вызываемого введением PCV13 в комбинации с PPSV23 против (i) одного или более S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23.
[320] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23, против каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают титр функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против (i) одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против (i) одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23.
[321] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против одного или более S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против каждого из серотипов S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают образование титра функциональных антител, который превосходит титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против (i) одного или более S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23.
[322] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против (i) одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких дополнительных серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления иммуногенность определяется путем измерения количества антитела к капсульному полисахариду против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенность определяется путем измерения количества антитела к капсульному полисахариду против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления общее измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления предварительно определенное пороговое значение представляет собой концентрацию в сыворотке или плазме крови от около 0,20 мкг/мл до около 0,35 мкг/мл. В некоторых вариантах осуществления предварительно определенное пороговое значение составляет по меньшей мере около 0,35 мкг/мл. В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[323] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против (i) одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F, и (ii) один или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких дополнительных серотипов S. pneumoniae (невакцинные виды, NVT). В некоторых вариантах осуществления иммуногенность определяется путем измерения количества антитела к капсульному полисахариду против одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления иммуногенность определяется путем измерения количества антитела к капсульному полисахариду против каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F. В некоторых вариантах осуществления измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления общее измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления предварительно определенное пороговое значение представляет собой концентрацию в сыворотке или плазме крови от около 0,20 мкг/мл до около 0,35 мкг/мл. В некоторых вариантах осуществления предварительно определенное пороговое значение составляет по меньшей мере около 0,35 мкг/мл. В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[324] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммуногенность против (i) одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких дополнительных серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления иммуногенность определяется путем измерения количества антитела к капсульному полисахариду против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления иммуногенность определяется путем измерения количества антитела к капсульному полисахариду против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F. В некоторых вариантах осуществления измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления общее измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления предварительно определенное пороговое значение представляет собой концентрацию в сыворотке или плазме крови от около 0,20 мкг/мл до около 0,35 мкг/мл. В некоторых вариантах осуществления предварительно определенное пороговое значение составляет по меньшей мере около 0,35 мкг/мл. В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[325] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту (i) вызывают образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PCV13 против одного или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F; и (ii) вызывают иммуногенность против одного или более серотипов S. pneumoniae 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту (i) вызывают образование титр функциональных антител, который превышает титр функциональных антител, вызываемый введением PCV13 против каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F; и (ii) вызывают иммуногенность против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают (i) образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PCV13, и (ii) иммуногенность (например, врожденный иммунный ответ, образование антител или ответ B-клеток и/или ответ Т-клеток) против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают (i) образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PCV13, и (ii) иммуногенность (например, врожденный иммунный ответ, образование антител или ответ B-клеток и/или ответ Т-клеток) против одного или более серотипов S. pneumoniae 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14 , 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F, а также против одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких дополнительных серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления иммуногенность определяется путем измерения количества антитела к капсульному полисахариду против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления общее измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления предварительно определенное пороговое значение представляет собой концентрацию в сыворотке или плазме крови от около 0,20 мкг/мл до около 0,35 мкг/мл. В некоторых вариантах осуществления предварительно определенное пороговое значение составляет по меньшей мере около 0,35 мкг/мл. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[326] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту (i) вызывают образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PPSV23 против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F и 33F; и (ii) вызывают иммуногенность против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту (i) вызывают образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PPSV23 против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F и 33F; и (ii) вызывают иммуногенность против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают (i) образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PPSV23, и (ii) иммуногенность (например, врожденный иммунный ответ, образование антител или ответ B-клеток и/или ответ Т-клеток) против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают (i) образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PPSV23, и (ii) иммуногенность (например, врожденный иммунный ответ, образование антител или ответ B-клеток и/или ответ Т-клеток) против одного или более серотипов S. pneumoniae 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14 , 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F, а также против одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких дополнительных серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления иммуногенность определяется путем измерения количества антитела к капсульному полисахариду против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления общее измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления предварительно определенное пороговое значение представляет собой концентрацию в сыворотке или плазме крови от около 0,20 мкг/мл до около 0,35 мкг/мл. В некоторых вариантах осуществления предварительно определенное пороговое значение составляет по меньшей мере около 0,35 мкг/мл. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[327] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту (i) вызывают образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против одного или более S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F; и (ii) вызывают иммуногенность против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления описанная в настоящем документе иммуногенная композиция или вакцина при введении субъекту (i) вызывают образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23 против каждого из S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F; и (ii) вызывают иммуногенность против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают (i) образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23, и (ii) иммуногенность (например, врожденный иммунный ответ, образование антител или ответ B-клеток и/или ответ Т-клеток) против одного или более серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают (i) образование титра функциональных антител, который превышает титр функциональных антител, вызываемый введением PCV13 в комбинации с PPSV23, и (ii) иммуногенность (например, врожденный иммунный ответ, образование антител или ответ B-клеток и/или ответ Т-клеток) против одного или более серотипов S. pneumoniae 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14 , 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F, а также против одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких дополнительных серотипов S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления иммуногенность определяется путем измерения количества антитела к капсульному полисахариду против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления титр функциональных антител измеряют с помощью анализа опсонофагоцитирующей активности (например, описанного в данном документе). В некоторых вариантах осуществления измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления общее измеренное количество антитела к капсульному полисахариду представляет собой количество, которое соответствует предварительно определенному пороговому значению. В некоторых вариантах осуществления предварительно определенное пороговое значение представляет собой концентрацию в сыворотке или плазме крови от около 0,20 мкг/мл до около 0,35 мкг/мл. В некоторых вариантах осуществления предварительно определенное пороговое значение составляет по меньшей мере около 0,35 мкг/мл. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23.
[328] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммунопротективный ответ против одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммунопротективный ответ против каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту вызывают иммунопротективный ответ против (i) одного или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F, и (ii) одного или более дополнительных серотипов S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более из таких дополнительных серотипов S. pneumoniae (невакцинные типы, NVT).
[329] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию одним или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F в большей степени, чем введение PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию каждым из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F в большей степени, чем введение PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13 (i) по меньшей мере одним или более S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F, и (ii) одним или более дополнительными серотипами S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких дополнительных серотипах S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[330] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию одним или более S. pneumoniae серотипами 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F в большей степени, чем введение PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию каждым из S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F в большей степени, чем введение PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13 (i) по меньшей мере одним или более S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F, и (ii) одним или более дополнительными серотипами S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких дополнительных серотипах S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[331] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F в большей степени, чем введение PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию каждым из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F в большей степени, чем введение PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13 (i) по меньшей мере одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F, и (ii) одним или более дополнительными серотипами S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких дополнительных серотипах S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[332] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F в большей степени, чем введение PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию каждым из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F в большей степени, чем введение PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PPSV23 (i) по меньшей мере одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F и 33F, и (ii) одним или более дополнительными серотипами S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких дополнительных серотипах S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[333] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию одним или более S. pneumoniae серотипов 6А и 20В в большей степени, чем введение PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию каждым из S. pneumoniae серотипов 6А и 20В в большей степени, чем введение PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PPSV23, (i) по меньшей мере одним или более из S. pneumoniae серотипов 6A и 20B и ( ii) одним или более дополнительными серотипами S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких дополнительных серотипах S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[334] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F в большей степени, чем введение PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию каждым из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F в большей степени, чем введение PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PPSV23 (i) по меньшей мере одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F, и (ii) одним или более дополнительными серотипами S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких дополнительных серотипах S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше.
[335] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13 в комбинации с PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F в большей степени, чем введение PCV13 в комбинации с PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию каждым из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F, и 33F в большей степени, чем введение PCV13 в комбинации с PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13 в комбинации с PPSV23 (i) по меньшей мере одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20A, 22F, 23F и 33F, и (ii) одним или более дополнительными серотипами S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких дополнительных серотипах S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23.
[336] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13 в комбинации с PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию одним или более S. pneumoniae серотипами 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F в большей степени, чем введение PCV13 в комбинации с PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию каждым из S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F в большей степени, чем введение PCV13 в комбинации с PCV13. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13 в комбинации с PPSV23 (i) по меньшей мере одним или более S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F, и (ii) одним или более дополнительными серотипами S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких дополнительных серотипах S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23.
[337] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13 в комбинации с PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F в большей степени, чем введение PCV13 в комбинации с PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию каждым из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F в большей степени, чем введение PCV13 в комбинации с PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту снижают колонизацию S. pneumoniae в большей степени, чем введение PCV13 в комбинации с PPSV23 (i) по меньшей мере одним или более S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F, и 33F, и (ii) одним или более дополнительными серотипами S. pneumoniae, причем такая иммуногенная композиция или вакцина не содержат полисахарид(-ы), присутствующий по меньшей мере в одном или более таких дополнительных серотипах S. pneumoniae (невакцинные типы, NVT). В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления PCV13 вводят до PPSV23. В некоторых вариантах осуществления PCV13 вводят после PPSV23. В некоторых вариантах осуществления PCV13 вводят приблизительно в то же время, что и PPSV23. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцируют иммунный ответ, который может помочь защитить от инвазии S. pneumoniae на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина защищают от колонизации на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина ингибируют инфекцию, вызванной S. pneumoniae, у неколонизированного или неинфицированного субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина уменьшают продолжительность колонизации S. pneumoniae у субъекта, который уже колонизирован, на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[338] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцируют иммунный ответ против S. pneumoniae на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцируют иммунный ответ против одного или более серотипов S. pneumoniae на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления иммунный ответ представляет собой образование антител или ответ В-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой ответ Т-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ представляет собой ответ CD4+ T-клеток, включая ответ TH1, TH2, или TH17 или ответ CD8+ T-клеток, или ответ CD4+ и CD8+ T-клеток, или ответ CD4-/CD8- T-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой образование антител или ответ В-клеток и ответ Т-клеток. В некоторых вариантах осуществления иммунный ответ представляет собой образование антител или ответ В-клеток, ответ Т-клеток и врожденный иммунный ответ. В некоторых вариантах осуществления иммунный ответ представляет собой протективный иммунный ответ. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[339] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцируют у субъекта образование антител или ответ В-клеток против одного или более патогенов на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[340] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцируют образование антител или ответ B-клеток против одного или более патогенов у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[341] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцируют ответ Т-клеток против одного или более патогенов у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина при введении субъекту индуцируют ответ Т-клеток против одного или более патогенов у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[342] В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают инфекцию, вызванную S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают инвазивное пневмококковое заболевание (ИПЗ), связанное с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают бактериемию, связанную с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают сепсис, связанный с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают поражение органов, связанное с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают менингит, связанный с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают пневмонию, связанную с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают средний отит, связанный с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина лечат или предотвращают синусит, связанный с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[343] В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения инфекции, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения инвазивного пневмококкового заболевания (ИПЗ), связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения бактериемии, связанной с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения сепсиса, связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения поражения органов, связанной с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения менингита, связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения пневмонии, связанной с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения среднего отита, связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют или снижают частоту возникновения синусита, связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[344] В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести инфекции, вызванной S. pneumoniae у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести инвазивного пневмококкового заболевания (ИПЗ), связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести бактериемии, связанной с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести сепсиса, связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести поражения органов, связанной с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести менингита, связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести пневмонии, связанной с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести среднего отита, связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина снижают степень тяжести синусита, связанного с инфекцией, вызванной S. pneumoniae, у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[345] В некоторых вариантах осуществления изобретения при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют трансмиссию S. pneumoniae от одного субъекта к другому субъекту на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют колонизацию S. pneumoniae у субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления при введении субъекту описанные в данном документе иммуногенная композиция или вакцина ингибируют колонизацию S. pneumoniae в носоглотке субъекта на уровне, превышающем уровень для контрольной композиции. В некоторых вариантах осуществления уровень выше на около 1%, около 2%, около 3%, около 4%, около 5%, около 6%, около 7%, около 8%, около 9%, около 10%, около 11%. %, около 12%, около 13%, около 14%, около 15%, около 16%, около 17%, около 18%, около 19%, около 20%, около 21%, около 22%, около 23%, около 24%, около 25%, около 30%, около 35%, около 40%, около 45%, около 50%, около 55%, около 60%, около 65%, около 70%, около 75%, около 80%, около 85%, около 90% или около 95% для контрольной композиции. В некоторых вариантах осуществления контрольная композиция может представлять собой PCV13 или PPSV23.
[346] В некоторых вариантах осуществления описанные в данном документе иммуногенная композиция или вакцина вводят субъекту в период от около 6 недель до около 5 лет (например, до 6-летнего возраста) для активной иммунизации для предотвращения инвазивного заболевания, вызываемого Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[347] В некоторых вариантах осуществления вакцину MAPS24 вводят субъекту в период от около 6 недель до около 5 лет (например, до 6-летнего возраста) для активной иммунизации для предотвращения инвазивного заболевания, вызываемого Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[348] В некоторых вариантах осуществления описанные в данном документе иммуногенную композицию или вакцину вводят субъекту в возрасте от около 6 до около 17 лет (например, до 18-летнего возраста) для активной иммунизации для предотвращения инвазивного заболевания, вызываемого Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[349] В некоторых вариантах осуществления вакцину MAPS24 вводят субъекту в возрасте от около 6 до около 17 лет (например, до 18-летнего возраста) для активной иммунизации для предотвращения инвазивного заболевания, вызываемого Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[350] В некоторых вариантах осуществления описанные в данном документе иммуногенную композицию или вакцину вводят субъекту в возрасте 18 лет или старше для активной иммунизации для предотвращения инвазивного заболевания, вызываемого Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[351] В некоторых вариантах осуществления вакцину MAPS24 вводят субъекту в возрасте 18 лет или старше для активной иммунизации для предотвращения инвазивного заболевания, вызываемого Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[352] В некоторых вариантах осуществления описанные в данном документе иммуногенную композицию или вакцину вводят субъекту в возрасте 18 лет или старше для активной иммунизации для предотвращения пневмонии, вызываемой Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[353] В некоторых вариантах осуществления вакцину MAPS24 вводят субъекту в возрасте 18 лет или старше для активной иммунизации для предотвращения пневмонии, вызываемой Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[354] В некоторых вариантах осуществления описанные в данном документе иммуногенную композицию или вакцину вводят субъекту в возрасте 18 лет или старше для активной иммунизации для предотвращения инвазивного заболевания и пневмонии, вызываемых Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
[355] В некоторых вариантах осуществления вакцину MAPS24 вводят субъекту 18 лет или старше для активной иммунизации для предотвращения инвазивного заболевания и пневмонии, вызываемых Streptococcus pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
Композиции антител
[356] В некоторых вариантах осуществления предложена композиция антител, содержащая антитела, вырабатываемые у млекопитающего, иммунизированного иммуногенным комплексом по изобретению. В некоторых вариантах осуществления антитело содержит по меньшей мере одно антитело, выбранное из группы, состоящей из мкАт и антиидиотипических антител. В некоторых вариантах осуществления композиция антител содержит выделенную фракцию гамма-глобулина. В некоторых вариантах осуществления композиция антител содержит поликлональные антитела. В некоторых вариантах осуществления композицию антител вводят субъекту. В некоторых вариантах осуществления композиция антител, вводимая субъекту, обеспечивает пассивную иммунизацию.
Вакцинные составы
[357] Оптимальные количества компонентов для конкретной вакцины могут быть установлены стандартными исследованиями, включающими наблюдение соответствующих иммунных ответов у субъектов. После первоначальной вакцинации субъекты могут получить одну или более бустерных иммунизаций, разделенных соответствующими промежутками времени.
[358] Описанные в данном документе иммуногенные комплексы и/ или их препараты могут быть составлены в виде единичной дозированной формы для простоты введения и единообразия дозировки. Конкретный терапевтически эффективный уровень дозы для любого конкретного субъекта или организма может зависеть от множества факторов, включая следующее: серьезность или степень риска инфекции; активность конкретной применяемой вакцины или вакцинной композиции; другие характеристики конкретной применяемой вакцины или вакцинной композиции; возраст, масса тела, общее состояние здоровья, пол субъекта, диета субъекта, фармакокинетическое состояние субъекта, время введения (например, в отношении других видов деятельности субъекта, таких как прием пищи, сон, прием других лекарственных препаратов, включая другие дозы вакцины и т. д.), способ введения, скорость выведения конкретной используемой вакцины или вакцинной композиции; вакцины, используемые в комбинации или одновременно с применяемой вакцинной композицией; и подобные факторы, хорошо известные в области медицины.
[359] Иммуногенные комплексы для применения в соответствии с настоящим изобретением могут быть включены в композиции (например, фармацевтические композиции) в соответствии с известными методами. Приготовление вакцины, как правило, описано в Vaccine Design (Powell and Newman, 1995). Например, иммунологическое количество вакцинного препарата может быть составлено вместе с одним или более органическими или неорганическими, жидкими или твердыми фармацевтически подходящими материалами-носителями. Приготовление пневмококковых полисахаридных и конъюгированных вакцин описано, например, в USSN 11/395 593, поданном 31 марта 2006 г., содержание которого включено в данный документ посредством ссылки.
[360] Как правило, фармацевтически приемлемый носитель(-и) включает растворители, дисперсионные среды и т.п., которые совместимы с фармацевтическим введением. Например, материалы, которые могут служить фармацевтически приемлемыми носителями, включают, но не ограничиваются ими, сахара, такие как лактоза, глюкоза, декстроза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлоза и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетат целлюлозы; порошкообразный трагакант; солод; желатин; тальк; эксципиенты, такие как масло какао и воски для суппозиториев; масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; полиолы, такие как глицерин, пропиленгликоль и жидкий полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные агенты, такие как гидроксид магния; альгиновая кислота; апирогенная вода; изотонический физиологический раствор; раствор Рингера; этиловый спирт и фосфатные буферные растворы, а также другие нетоксичные совместимые смазывающие вещества, такие как лаурилсульфат натрия и стеарат магния, а также консерванты и антиоксиданты, также могут присутствовать в композиции, по мнению разработчика (Martin, 1975).
[361] Вакцины могут быть составлены путем объединения одного или более иммуногенных комплексов, описанных в данном документе, с носителями и/или другими необязательными компонентами любыми доступными способами, включая, например, обычное смешивание, гранулирование, растворение, лиофилизацию или аналогичные процессы.
[362] Вакцинные композиции, применимые в предлагаемых способах, могут быть лиофилизованы до момента их применения, после чего их сразу же восстанавливают разбавителем. В некоторых вариантах осуществления компоненты или вакцинные композиции лиофилизируют в присутствии одного или более других компонентов (например, адъювантов) и немедленно восстанавливают физиологическим раствором. Альтернативно, отдельные компоненты или наборы компонентов можно отдельно лиофилизировать и/или хранить (например, в наборе для вакцинации), при этом компоненты восстанавливают и либо смешивают перед применением, либо вводят субъекту отдельно.
[363] Лиофилизация позволяет получить более стабильную композицию (например, предотвращая или уменьшая разрушение полисахаридных антигенов). Лиофилизация вакцин или компонентов вакцины хорошо известна в данной области техники. Как правило, жидкую вакцину или компонент вакцины сушат сублимацией, часто в присутствии антислеживающего агента (такого как, например, сахара, такие как сахароза или лактоза). В некоторых вариантах осуществления антислеживающий агент присутствует, например, в начальной концентрации 10-200 мг/мл. Лиофилизация, как правило, происходит в несколько этапов, например, цикл начинается при -69 °C, постепенно повышается до -24°C в течение 3 часов, затем сохраняется эта температура в течение 18 часов, а затем постепенно устанавливается до -16°C в течение 1 часа, затем поддерживая эту температуру в течение 6 часов, затем постепенно доводя до +34°C в течение 3 часов и, наконец, сохраняя эту температуру в течение 9 часов.
[364] В некоторых вариантах осуществления вакцина представляет собой жидкость. В некоторых вариантах осуществления жидкость представляет собой восстановленный лиофилат. В некоторых вариантах осуществления вакцина имеет pH около 5, около 6, около 7 или около 8. В некоторых вариантах осуществления вакцина имеет pH от около 5 до около 7,5. В некоторых вариантах осуществления вакцина имеет pH от 5 до 7,5. В некоторых вариантах осуществления вакцина имеет pH от около 5,3 до около 6,3. В некоторых вариантах осуществления вакцина имеет pH от 5,3 до 6,3. В некоторых вариантах осуществления вакцина имеет pH около 5,0, около 5,1, около 5,2, около 5,3, около 5,4, около 5,5, около 5,6, около 5,7, около 5,8, около 5,9, около 6,0, около 6,1, около 6,2, около 6,3, около 6,4, около 6,5, около 6,6, около 6,7, около 6,8, около 6,9, около 7,0, около 7,1, около 7,2, около 7,3, около 7,4 или около 7,5.
[365] Вакцины или компоненты вакцины для применения в соответствии с настоящим изобретением могут быть включены в липосомы, кохлеаты, биоразлагаемые полимеры, такие как полилактид, полигликолид и сополимеры лактида с гликолидами, или иммуностимулирующие комплексы (ISCOM).
[366] В определенных ситуациях может быть желательно продлить действие вакцины или для применения в соответствии с настоящим изобретением, например, путем замедления абсорбции одного или более компонентов вакцины. Такая задержка абсорбции может быть достигнута, например, посредством применения жидкой суспензии кристаллического или аморфного материала с плохой растворимостью в воде. Скорость абсорбции препарата затем зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера и формы. Альтернативно или дополнительно отсроченная абсорбция может быть достигнута путем растворения или суспендирования одного или более компонентов вакцины в масляном носителе. Для задержки абсорбции также можно использовать инъекционные депо-формы. Такие депо-формы могут быть получены путем формирования матриц микрокапсул из одного или более компонентов вакцины в виде сети биоразлагаемых полимеров. В зависимости от соотношения полимера и компонента вакцины и природы конкретного используемого полимера(-ов) скорость высвобождения можно контролировать.
[367] Примеры биоразлагаемых полимеров, которые можно использовать в соответствии с данным изобретением, включают, например, поли(ортоэфиры) и поли(ангидриды). Одним из конкретных примеров полимеров является полилактид-полигликолид.
[368] Депо-инъекционные составы могут также готовить путем включения препарата в липосомы или микроэмульсии, которые совместимы с тканями организма.
[369] Полимерные системы доставки также могут быть использованы в отличных от депо составах, включая, например, составы для перорального применения. Например, в составах для перорального применения можно использовать биоразлагаемые, биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полилактидная кислота и т.д. Полисахаридные антигены или конъюгаты могут быть составлены с такими полимерами, например, для получения частиц, микрочастиц, экструдатов, твердых дисперсий, смесей или других комбинаций, чтобы облегчить приготовление полезных составов (например, для перорального применения).
[370] Вакцины для применения в соответствии с настоящим изобретением содержать иммуногенные композиции и могут дополнительно содержать один или более дополнительных активных агентов (то есть агентов, которые оказывают биологический эффект, а не инертных ингредиентов). Например, как правило, в состав вакцины содержат один или более адъювантов. Следует понимать, что такие дополнительные агенты могут быть составлены вместе с одним или более другими компонентами вакцины или могут сохраняться отдельно и объединяться при введении или непосредственно перед введением. В некоторых вариантах осуществления такие дополнительные компоненты можно вводить отдельно от некоторых или всех других компонентов вакцины в пределах подходящего временного окна для достижения соответствующего эффекта.
Адъюванты
[371] Описанные в данном документе вакцинные составы и иммуногенные композиции могут содержать адъювант. Адъюванты, как правило, представляют собой агенты, усиливающие иммунный ответ на антиген. Адъюванты можно в целом разделить на два класса в зависимости от их основных механизмов действия: системы доставки вакцины и иммуностимулирующие адъюванты (см., например, Singh et al, 2003). В большинстве вакцинных составов адъювант подает сигнал иммунной системе, так что она генерирует ответ на антиген, а антиген необходим для стимулирования специфичности ответа на патоген. Системы доставки вакцины часто представляют собой составы в виде частиц, например, эмульсии, микрочастицы, иммуностимулирующие комплексы (ISCOM), наночастицы, которые могут быть, например, частицами и/или матрицами, и липосомами. Напротив, иммуностимулирующие адъюванты иногда получены из патогенов или происходят от них и могут представлять патоген-ассоциированные молекулярные паттерны (PAMP), например, липополисахариды (LPS), монофосфориллипид A (MPL) или CpG-содержащую ДНК, которые активируют клетки врожденной иммунной системы.
[372] Альтернативно адъюванты можно разделить на органические и неорганические. Неорганические адъюванты включают соли алюминия, такие как фосфат алюминия, аморфный сульфат гидроксифосфата алюминия и гидроксид алюминия, которые, как правило, используются в вакцинах для человека. Органические адъюванты включают органические молекулы, включая макромолекулы. Неограничивающие примеры органических адъювантов включают холерный токсин/токсоиды, другие энтеротоксины/токсоиды или лабильные токсины/токсоиды грамотрицательных бактерий, интерлейкины (например, ИЛ-1, ИЛ-2, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7, ИЛ-12, ИЛ-15, ИЛ-18 и т. д.), интерфероны (например, гамма-интерферон), гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), макрофагальный колониестимулирующий фактор (М-КСФ) и фактор некроза опухоли (ФНО).
[373] Адъюванты также можно классифицировать по реакции, которую они вызывают. В некоторых вариантах осуществления адъювант индуцирует образование, пролиферацию или активацию клеток TH1 или клеток TH2. В других вариантах осуществления адъювант индуцирует образование, пролиферацию или активацию В-клеток. В еще других вариантах осуществления адъювант индуцирует активацию антигенпрезентирующих клеток. Эти категории не исключают друг друга; в некоторых случаях адъювант активирует более одного типа клеток.
[374] В некоторых вариантах осуществления адъювант индуцирует образование, пролиферацию или активацию клеток TH17. Адъювант может стимулировать CD4+ или CD8+ T-клетки к секреции ИЛ-17. В некоторых вариантах осуществления изобретения адъювант, который индуцирует образование, пролиферацию или активацию клеток TH17, представляет собой адъювант, который продуцирует по меньшей мере 2-кратное, а в некоторых случаях 10-кратное соотношение экспериментального образца и контроля в следующем анализе. В этом анализе экспериментатор сравнивает уровни ИЛ-17, секретируемые двумя популяциями клеток: (1) клетки животных, иммунизированных адъювантом, и полипептидом, который, как известно, индуцирует образование, пролиферацию или активацию TH17, и (2) клетки животных, обработанные адъювантом и нерелевантным (контрольным) полипептидом. Адъювант, который индуцирует образование, пролиферацию или активацию клеток TH17, может привести к тому, что клетки популяции (1) будут продуцировать более чем в 2 раза или более чем в 10 раз больше ИЛ-17, чем клетки популяции (2). ИЛ-17 можно измерить, например, с помощью ИФА или ELISPOT. Некоторые токсины, такие как холерный токсин и лабильный токсин (продуцируемый энтеротоксигенной E. coli или ETEC), активируют ответ TH17. Таким образом, в некоторых вариантах осуществления адъювант представляет собой токсин или анатоксин. Холерный токсин был успешно использован на мышиной модели для индукции защитного иммунитета в сочетании с некоторыми полипептидами из Таблицы 1 (см. Примеры 5-8). Компания Intercell производит одну из форм лабильных токсинов. Также можно использовать мутантные производные лабильного токсина (токсоиды), которые активны в качестве адъювантов, но значительно менее токсичны. Примеры детоксифицированных мутантных производных лабильного токсина включают мутанты, лишенные активности АДФ-рибозилтрансферазы. Конкретные детоксифицированные мутантные производные лабильного токсина включают LTK7 (Douce et al, 1995) и LTK63 (Williams et al, 2004), LT-G192 (Douce et al, 1999) и LTR72 (Giuliani et al, 1998).
[375] В некоторых вариантах осуществления адъювант содержит VLP (вирусоподобную частицу). Одна из таких адъювантных платформ, репликоны альфавируса, индуцирует активацию клеток TH17 с использованием альфавируса и производится компанией Alphavax. В определенных вариантах осуществления системы репликона альфавируса, альфавирус может быть сконструирован для экспрессии представляющего интерес антигена, представляющего интерес цитокина (например, ИЛ-17 или цитокина, который стимулирует продукцию ИЛ-17) или того и другого, и может быть продуцирован в линии Т-хелперов. Более подробную информацию можно найти в патентах США №№ 5643576 и 6783939. В некоторых вариантах осуществления вакцинный состав вводят субъекту в комбинации с нуклеиновой кислотой, кодирующей цитокин.
[376] Определенные классы адъювантов активируют Toll-подобные рецепторы (TLR), чтобы активировать ответ TH17. TLR представляют собой хорошо известные белки, которые могут быть обнаружены на мембранах лейкоцитов и распознают чужеродные антигены (включая микробные антигены). Введение известного лиганда TLR вместе с представляющим интерес антигеном (например, в виде слитого белка) может способствовать развитию иммунного ответа, специфичного для представляющего интерес антигена. Один иллюстративный адъювант, который активирует TLR, включает монофосфориллипид A (MPL). Традиционно MPL производился в виде детоксифицированного липополисахаридного (LPS) эндотоксина, полученного из грамотрицательных бактерий, таких как S. minnesota. В частности, последовательный кислотный и основной гидролиз LPS дает иммуноактивную фракцию липида A (которая представляет собой MPL), и в ней отсутствуют группы сахаров и все фосфаты, кроме одного, который присутствует в LPS. Ряд синтетических агонистов TLR (в частности, агонистов TLR-4) описан Evans et al, 2003. Подобно адъювантам MPL, эти синтетические соединения активируют врожденную иммунную систему через TLR. Другой тип агониста TLR представляет собой димер синтетического фосфолипида, например, E6020 (Ishizaka et al, 2007). Различные агонисты TLR (включая агонисты TLR-4) производятся и/или продаются, например, институтом исследования инфекционных заболеваний (IRDI), Corixa, Esai, Avanti Polar Lipids, Inc. и Sigma Aldrich. Другой иллюстративный адъювант, который активирует TLR, включает смесь MPL, дикоиномиколата трегалозы (TDM) и бромида диоктадецилдиметиламмония (DDA). Другой адъювант, активирующий TLR, представляет собой R848 (резиквимод).
[377] В некоторых вариантах осуществления адъювант представляет собой или содержит сапонин. Как правило, сапонин представляет собой тритерпеновый гликозид, такой как гликозид, выделенный из коры дерева Quillaja saponaria. Экстракт сапонина из биологического источника можно дополнительно фракционировать (например, с помощью хроматографии) для выделения частей экстракта с наилучшей адъювантной активностью и приемлемой токсичностью. Типичные фракции экстракта дерева Quillaja saponaria, используемые в качестве адъювантов, известны как фракции A и C.
[378] В определенных вариантах осуществления используются комбинации адъювантов. Три иллюстративных комбинации адъювантов: MPL и квасцы, E6020 и квасцы, а также MPL и ISCOM.
[379] Адъюванты могут быть ковалентно или нековалентно связаны с антигенами. В некоторых вариантах осуществления адъювант может содержать белок, который вызывает воспалительные реакции посредством активации антигенпрезентирующих клеток (АПК). В некоторых вариантах осуществления один или более из этих белков могут быть рекомбинантно слиты с выбранным антигеном, так что полученная слитая молекула способствует созреванию дендритных клеток, активирует дендритные клетки для продуцирования цитокинов и хемокинов и, в конечном итоге, усиливает презентацию антигена T-клетки и инициирование Т-клеточного ответа (например, см. Wu et al, 2005).
[380] В некоторых вариантах осуществления описанные в данном документе иммуногенные комплексы составляются и/или вводятся в комбинации с адъювантом. В некоторых вариантах осуществления адъювант выбран из группы, состоящей из фосфата алюминия, гидроксида алюминия и фосфат алюминий гидроксида. В некоторых вариантах осуществления адъювант содержит фосфат алюминия. В некоторых вариантах осуществления адъювант представляет собой фосфат алюминия.
[381] Как правило, один и тот же адъювант или смесь адъювантов присутствует в каждой дозе вакцины. Как правило, необязательно адъювант можно вводить с первой дозой вакцины, а не с последующими дозами (т.е. бустерными инъекциями). Альтернативно, сильный адъювант можно вводить с первой дозой вакцины, а более слабый адъювант или более низкую дозу сильного адъюванта можно вводить с последующими дозами. Адъювант можно вводить до введения антигена, одновременно с введением антигена или после введения антигена субъекту (иногда в течение 1, 2, 6 или 12 часов, а иногда в течение 1, 2 или 5 дней). Некоторые адъюванты подходят для людей, животных, не относящихся к человеку, или для того и другого.
[382] Вакцины для применения в соответствии с настоящим изобретением могут включать или вводиться одновременно с другой противомикробной терапией. Например, такие вакцины могут включать или вводиться с одним или более агентами, которые убивают или замедляют рост патогена. Такие агенты включают, например, пенициллин, ванкомицин, эритромицин, азитромицин и кларитромицин, цефотаксим, цефтриаксон, левофлаксин, гатифлоксацин.
[383] Альтернативно или дополнительно вакцины для применения в соответствии с настоящим изобретением могут включать одну или более других вакцин или видов терапий или вводиться вместе с ними. Например, один или более непневмококковых антигенов могут быть включены в вакцины или введены вместе с ними.
Дополнительные компоненты и эксципиенты
[384] В дополнение к антигенам и адъювантам, описанным выше, состав вакцины или иммуногенная композиция может содержать один или более эксципиентов.
[385] В некоторых вариантах осуществления вакцинный состав или иммуногенная композиция может содержать один или более стабилизаторов, таких как сахара (например, сахароза, глюкоза или фруктоза), фосфат (такой как двухосновный фосфат натрия, одноосновный фосфат калия, двухосновный фосфат калия или мононатрийфосфат), глутамат (например, L-глутамат натрия), желатин (например, обработанный желатин, гидролизованный желатин или свиной желатин), аминокислоты (такие как аргинин, аспарагин, гистидин, L-гистидин, аланин, валин, лейцин, изолейцин, серин, треонин, лизин, фенилаланин, тирозин и их сложные алкиловые эфиры), инозин или борат натрия.
[386] В определенных вариантах осуществления вакцинный состав или иммуногенная композиция содержит один или более буферов, таких как смесь бикарбоната натрия и аскорбиновой кислоты. В некоторых вариантах осуществления вакцинный состав можно вводить в солевом растворе, таком как фосфатно-солевой буфер (PBS), или дистиллированной воде.
[387] В некоторых вариантах осуществления вакцинный состав или иммуногенная композиция содержит одно или более поверхностно-активных веществ, например, но не ограничиваясь ими, полисорбат-80 (TWEEN-80), полисорбат-20 (TWEEN 20), полиэтиленгликоль п-(1,1,3,3 -тетраметилбутил)-фениловый эфир (TRITON X-100) и полимер 4-(1,1,3,3-тетраметилбутил)фенола с формальдегидом и оксираном (TYLOXAPOL). Поверхностно-активное вещество может быть ионным или неионным.
[388] В определенных вариантах осуществления вакцинный состав или иммуногенная композиция содержат одну или более солей, таких как хлорид натрия, хлорид аммония, хлорид кальция или хлорид калия.
[389] В определенных вариантах осуществления консервант включен в вакцину или иммуногенную композицию. В других вариантах осуществления консервант не используется. Консервант чаще всего используется во многодозовых флаконах с вакциной и реже требуется в однодозовых флаконах с вакциной. В определенных вариантах осуществления консервант представляет собой 2-феноксиэтанол, метил- и пропилпарабены, бензиловый спирт и/или сорбиновую кислоту.
Способы введения
[390] В некоторых вариантах осуществления иммуногенные комплексы вводят субъекту с риском развития пневмококкового заболевания, например, младенец, ребенок раннего возраста, несовершеннолетний или человек старшего возраста. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления возраст человека составляет от около 2 недель до около 6 недель. В некоторых вариантах осуществления возраст человека составляет от около 6 недель до около 6 лет. В некоторых вариантах осуществления возраст человека составляет от около 6 лет до около 18 лет. В некоторых вариантах осуществления возраст человека составляет от около 18 лет до около 50 лет. В некоторых вариантах осуществления возраст человека составляет около 50 лет или старше. В некоторых вариантах осуществления иммуногенные комплексы вводят субъекту с повышенным риском развития пневмококкового заболевания, например, субъектам с ослабленным иммунитетом, субъектам с серповидноклеточной анемией или другими гемоглобинопатиями, врожденной или приобретенной аспленией, дисфункцией селезенки, хронической почечной недостаточностью или нефротическим синдромом, заболеваниями, ассоциированными с лечением иммунодепрессантами или лучевой терапией (включая злокачественные новообразования, лейкоз, лимфомы, болезнь Ходжкина или трансплантацию твердых органов), врожденным или приобретенным иммунодефицитом, ВИЧ-инфекцией, цереброспинально-жидкостной отореей, кохлеарным имплантатом(-ами), хроническими заболевания сердца, хроническим заболеванием легких, сахарным диабетом, алкоголизмом, хроническим заболеванием печени, курением сигарет, астмой, генерализованной злокачественной опухолью, множественной миеломой или трансплантацией твердых органов. Следует принимать во внимание, что субъект может рассматриваться как подверженный риску развития заболевания, не имея диагноза каких-либо симптомов заболевания. Например, если известно, что субъект находился или должен находиться в ситуациях с относительно высоким риском инфицирования, этот субъект будет считаться подверженным риску развития заболевания.
[391] Может быть использован любой эффективный путь введения, такой как, например, пероральный, назальный, энтеральный, парентеральный внутримышечный или внутривенный, подкожный, трансдермальный, внутрикожный, ректальный, вагинальный, местный, окулярный, ингаляционный путь введения или контактное применение. В некоторых вариантах осуществления вакцинные композиции можно вводить (например, внутримышечно, внутрибрюшинно, внутрикожно и/или подкожно); или доставлять через слизистую оболочку (например, в ротовой канал/пищеварительные, дыхательные и/или мочеполовые пути). Интраназальное введение вакцин может быть особенно полезным в некоторых случаях, например, для лечения пневмонии или среднего отита (поскольку носоглоточное носительство пневмококков может быть более эффективно предотвращено, таким образом ослабляя инфекцию на самой ранней стадии). В некоторых вариантах осуществления изобретения может быть желательно вводить разные дозы вакцины разными путями; в некоторых вариантах осуществления может быть желательно вводить разные компоненты одной дозы разными путями. В некоторых вариантах осуществления иммуногенную композицию или вакцину, описанные в данном документе, вводят внутримышечно. В некоторых вариантах осуществления иммуногенную композицию или вакцину, описанные в настоящем документе, вводят подкожно.
[392] В некоторых вариантах осуществления настоящего изобретения фармацевтические композиции (например, вакцины) вводят внутрикожно. Традиционная техника внутрикожной инъекции, «проба Манту», включает этапы очистки кожи, а затем растягивания одной рукой, при этом, когда скос узкой иглы (размер 26-31) направлен вверх, игла вводят под углом 10-15°. Как только скос иглы введен, ствол иглы опускается и продвигается дальше, обеспечивая при этом небольшое давление, чтобы поднять его под кожей. Затем жидкость очень медленно вводят, образуя пузырек или шишку на поверхности кожи, после чего следует медленное извлечение иглы.
[393] Были описаны устройства, специально предназначенные для введения жидких агентов в кожу или через кожу, например устройства, описанные в WO 99/34850 и EP 1092444, а также устройства для струйных инъекций, описанные, например, в WO 01/13977; патент США №5480381, патент США №5599302, патент США № 5334144, патент США № 5993412, патент США № 5649912, патент США № 5569189, патент США № 5704911, патент США № 5383851, патент США № 5893397, патент США № 5466220, патент США № 5339163, патент США № 5312335, патент США № 5503627, патент США № 5064413, патент США № 5520639, патент США № 4596556, патент США № 4790824, патент США № 4941880, патент США № 4940460, WO 97/37705 и WO 97/13537. Другие способы внутрикожного введения вакцинных препаратов могут включать обычные шприцы и иглы или устройства, предназначенные для баллистической доставки твердых вакцин (WO 99/27961) или трансдермальные пластыри (WO 97/48440; WO 98/28037); или наносят на поверхность кожи (трансдермальная или чрескожная доставка WO 98/20734; WO 98/28037).
[394] Как описано выше, фармацевтические композиции (например, вакцины) можно вводить в виде однократной дозы или в виде множественных доз. Следует понимать, что введение представляет собой однократную «дозу» при условии, что все соответствующие компоненты вводятся субъекту в пределах временного окна; не обязательно, чтобы каждый компонент присутствовал в одной композиции. Например, введение двух разных иммуногенных композиций в течение периода менее 24 часов считается однократной дозой. Приведем лишь один пример: иммуногенные композиции, содержащие разные антигенные компоненты, можно вводить в отдельных композициях, но как часть однократной дозы. Как отмечалось выше, такие отдельные композиции можно вводить разными путями или одним и тем же путем. Альтернативно или дополнительно, в вариантах осуществления, где вакцина содержит комбинацию иммуногенных композиций и дополнительных типов активных агентов, иммуногенные композиции можно вводить одним путем, а второй активный агент можно вводить тем же путем или другим путем.
[395] Фармацевтические композиции (например, вакцины) вводят в таких количествах и в течение такого времени, которые необходимы для достижения желаемого результата. В определенных вариантах осуществления настоящего изобретения вакцинная композиция содержит иммунологически эффективное количество по меньшей мере иммуногенной композиции. Точное количество, необходимое для достижения иммунологически эффективного количества, может варьироваться в зависимости от иммуногенной композиции и от субъекта к субъекту, в зависимости от вида, возраста и общего состояния субъекта, стадии заболевания, конкретной фармацевтической смеси, его способа введения и тому подобного.
[396] Количество полипептидного антигена(-ов), полисахаридного антигена(-ов) или конъюгата(-ов) в каждой дозе фармацевтической композиции (например, вакцины) выбрано таким образом, чтобы вакцина при введении, как описано в данном документе, вызывала соответствующий иммунопротективный ответ без значительных побочных эффектов.
[397] В некоторых вариантах осуществления фармацевтическая композиция, содержащая описанный в данном документе иммуногенный комплекс, индуцирует ответ клеток TH1 и/или TH17 при введении субъекту. В некоторых вариантах осуществления фармацевтическая композиция, содержащая описанный в данном документе иммуногенный комплекс, индуцирует опсонический/бактерицидный ответ против S. pneumoniae при введении субъекту. В некоторых вариантах осуществления фармацевтическая композиция, содержащая описанный в данном документе иммуногенный комплекс, снижает скорость трансмиссии и/или колонизации поверхности слизистой оболочки S. pneumoniae при введении субъекту.
[398] В некоторых вариантах осуществления фармацевтическая композиция, содержащая описанный в данном документе иммуногенный комплекс, снижает скорость трансмиссии и/или колонизации носоглотки или легких S. pneumoniae при трансмиссии.
[399] Некоторые варианты осуществления обеспечивают способ иммунизации субъекта против инфекции, вызванной S. pneumoniae, включающий введение субъекту иммунологически эффективного количества иммуногенного комплекса, описанного в данном документе. Некоторые варианты осуществления обеспечивают способ иммунизации субъекта против инфекции, вызванной S. pneumoniae, включающий введение субъекту иммунологически эффективного количества иммуногенного комплекса, описанного в данном документе. Некоторые варианты осуществления обеспечивают способ иммунизации субъекта против инфекции, вызванной S. pneumoniae, включающий введение субъекту иммунологически эффективного количества композиции вакцины, описанной в данном документе. Некоторые варианты осуществления обеспечивают способ иммунизации субъекта против инфекции, вызванной S. pneumoniae, включающий введение субъекту иммунологически эффективного количества композиции вакцины, описанной в данном документе.
Комбинированная профилактика или комбинированная терапия
[400] В некоторых вариантах осуществления иммуногенный комплекс, иммуногенная композиция, вакцина или фармацевтическая композиция, описанные в данном документе, могут вводиться в комбинации с другим агентом. В некоторых вариантах осуществления агент представляет собой или содержит PCV13. В некоторых вариантах осуществления агент представляет собой или содержит PPSV23. В некоторых вариантах осуществления агент представляет собой или содержит антибиотик.
Дозирование
[401] В некоторых вариантах осуществления введение вакцины (например, вакцинной композиции), описанной в данном документе, может включать доставку однократной дозы. В некоторых вариантах осуществления введение может включать начальную дозу, за которой следует одна или более дополнительных доз иммунизации, разделенных соответствующими промежутками времени. Схема иммунизации представляет собой программу введения одной или более определенных доз одной или более указанных пневмококковых вакцин одним или более конкретными путями введения в одном или более определенных возрастах субъекта.
[402] В настоящем изобретении предложены способы иммунизации, которые включают введение по меньшей мере одной дозы вакцины младенцу. В некоторых вариантах осуществления субъекту-младенцу исполнилось 18 месяцев или меньше. В некоторых вариантах осуществления субъекту-младенцу исполнилось 12 месяцев или меньше. В некоторых вариантах осуществления субъект-младенец ранее получил одну или более доз конъюгированной пневмококковой полисахаридной вакцины; в других вариантах осуществления субъект-младенец не получал пневмококковыми вакцинами. В некоторых вариантах осуществления субъект-младенец ранее был инфицирован или подвергался инфицированию S. pneumoniae.
[403] В данном документе предложены способы иммунизации, которые включают введение по меньшей мере одной дозы вакцины субъекту-ребенку раннего возраста. В некоторых вариантах осуществления возраст субъекта-ребенка раннего возраста составляет 5 лет или меньше. В некоторых вариантах осуществления возраст субъекта-ребенка раннего возраста составляет 4 года или меньше. В некоторых вариантах осуществления субъект-ребенок ясельного возраста ранее получил одну или более доз конъюгированной пневмококковой полисахаридной вакцины; в других вариантах осуществления субъект-ребенок раннего возраста не получал пневмококковыми вакцинами. В некоторых вариантах осуществления субъект-ребенок раннего возраста ранее был инфицирован или подвергался инфицированию S. pneumoniae.
[404] В настоящем изобретении предложены способы иммунизации, которые включают введение по меньшей мере одной дозы вакцины несовершеннолетнему субъекту. В некоторых вариантах осуществления несовершеннолетнему субъекту исполнилось 18 лет или меньше. В некоторых вариантах осуществления несовершеннолетнему субъекту исполнилось 15 лет или меньше. В некоторых вариантах осуществления несовершеннолетний субъект ранее получил одну или более доз конъюгированной пневмококковой полисахаридной вакцины; в других вариантах осуществления несовершеннолетний субъект не получал пневмококковыми вакцинами. В некоторых вариантах осуществления несовершеннолетний субъект ранее был инфицирован или подвергался инфицированию S. pneumoniae.
[405] В настоящем изобретении предложены способы иммунизации, которые включают введение по меньшей мере одной дозы вакцины взрослому субъекту. В некоторых вариантах осуществления взрослый субъект старше около 50 лет. В некоторых вариантах осуществления взрослый субъект старше около 65 лет. В некоторых вариантах осуществления взрослый субъект ранее получил одну или более доз конъюгированной пневмококковой полисахаридной вакцины; в других вариантах осуществления взрослый субъект не получал пневмококковыми вакцинами. В некоторых вариантах осуществления взрослый субъект ранее был инфицирован или подвергался инфицированию S. pneumoniae.
[406] Схемы иммунизации настоящего изобретения предназначены для индукции иммунного ответа (например, иммунопротективного ответа) у субъекта, достаточного для снижения по меньшей мере одного показателя, выбранного из группы, состоящей из заболеваемости, распространенности, частоты и/или степени тяжести по меньшей мере одной инфекции, заболевания или расстройства, и/или по меньшей мере одного суррогатного маркера инфекции, заболевания или расстройства в популяции и/или субпопуляции субъектов(-а). Дополнительная схема иммунизации представляет собой схему, которая имеет такой эффект по сравнению со стандартной схемой, которую она дополняет. В дополнительной схеме может потребоваться дополнительные введения и/или супраиммуногенные дозы иммуногенных композиций, описанных в данном документе, которые есть в стандартной схеме, или для введения вакцин, не являющихся частью стандартной схемы. Полная схема иммунизации по настоящему изобретению может включать как стандартную, так и дополнительную схемы. Иллюстративные графики вакцинации приведены в иллюстративных целях. Подробные описания способов оценки иммуногенного ответа, обсуждаемые в данном документе, позволяют вносить изменения в схемах иммунизации образцов без излишнего экспериментирования.
[407] В некоторых вариантах осуществления настоящего изобретения первое введение пневмококковой вакцины осуществляют, когда субъекту исполняется более около 2 недель, более около 5 недель, более около 1 года, более около 2 лет, более около 15 лет или старше 18 лет.
[408] В некоторых вариантах осуществления первое введение пневмококковой вакцины осуществляют, когда субъекту исполняется около двух месяцев. В некоторых вариантах осуществления второе введение пневмококковой вакцины осуществляют, когда субъекту исполняется около четырех месяцев. В некоторых вариантах осуществления третье введение пневмококковой вакцины осуществляют, когда субъекту исполняется около шести месяцев. В некоторых вариантах осуществления четвертое введение пневмококковой вакцины осуществляют, когда субъекту исполняется от около двенадцати месяцев до около пятнадцати месяцев.
[409] В некоторых вариантах осуществления настоящего изобретения первое введение пневмококковой вакцины осуществляют, когда субъекту исполняется более около 50 лет, более около 55 лет, более около 60 лет, более около 65 лет или более около 70 лет.
[410] В некоторых вариантах осуществления изобретения применяется однократное введение вакцины. Возможно, что цели настоящего изобретения могут быть достигнуты при однократном введении, особенно когда один или более используемых вакцинных полипептидов, полисахаридов и/или иммуногенных комплексов или их комбинаций являются сильными, и в такой ситуации схемы однократной дозы достаточно, чтобы вызвать длительный иммунопротективный ответ.
[411] В определенных вариантах осуществления желательно ввести две или более доз вакцины для большей иммунопротективной эффективности и охвата. Таким образом, в некоторых вариантах осуществления количество доз составляет по меньшей мере две, по меньшей мере три или более доз. Не существует установленного максимального количества доз, однако хорошей клинической практикой является не проводить иммунизацию чаще, чем это необходимо для достижения желаемого эффекта.
[412] Не ограничиваясь теорией, первая доза вакцины, вводимая в соответствии с изобретением, может считаться «примирующей» дозой. В определенных вариантах осуществления в схему иммунизации включено более одной дозы. В таком случае последующая доза может считаться «бустерной» дозой.
[413] Начальная доза может быть введена наивному субъекту (субъекту, который ранее никогда не получал конъюгированную полисахаридную вакцину). В некоторых вариантах осуществления примирующая доза может быть введена субъекту, который ранее получал конъюгированную полисахаридную вакцину, по меньшей мере, за пять или более лет до введения начальной дозы вакцины согласно изобретению. В других вариантах осуществления примирующая доза может быть введена субъекту, который ранее получал конъюгированную полисахаридную вакцину по меньшей мере за двадцать или более лет до введения примирующей вакцины согласно изобретению.
[414] Если схема иммунизации предусматривает введение двух или более отдельных доз, учитывается интервал между дозами. Интервал между двумя последовательными дозами может быть одинаковым на протяжении всей схемы иммунизации или может меняться по мере с возрастом субъекта. В схемах иммунизации по настоящему изобретению после введения первой дозы вакцины существует первый интервал перед введением следующей дозы. Первый интервал, как правило, составляет по меньшей мере 2 недель, 1 месяц, 6 недель, 2 месяца, 3 месяца, 6 месяцев, 9 месяцев, 12 месяцев или дольше. Если вводят более одной последующей дозы, между такими последующими дозами могут быть предусмотрены вторые (или более продолжительные) интервалы. В некоторых вариантах осуществления все интервалы между последующими дозами имеют одинаковую продолжительность; в других вариантах осуществления вторые интервалы могут различаться по продолжительности. В некоторых вариантах осуществления интервал между последующими дозами может составлять по меньшей мере около 12 месяцев, по меньшей мере около 15 месяцев, по меньшей мере около 18 месяцев, по меньшей мере около 21 месяца или по меньшей мере около 2 лет. В определенных вариантах осуществления интервал между дозами может составлять до 3 лет, до около 4 лет или до около 5 лет, или 10 лет или более. В определенных вариантах осуществления интервалы между последующими дозами могут уменьшаться с возрастом субъекта.
[415] Специалистам в данной области техники будет понятно, что множество возможных комбинаций и подкомбинаций различных условий выбора времени первого введения, кратчайшего интервала, наибольшего интервала и общего количества введений (в абсолютном выражении или в пределах заявленного периода) существуют, и все эти комбинации и подкомбинации следует рассматривать как находящиеся в рамках задумки изобретателя, хотя и не перечисленные в данном документе явно.
Анализы для определения иммунного ответа
[416] В некоторых вариантах осуществления способ оценки иммуногенности иммуногенной композиции, описанной в данном документе, включает оценку, измерение и/или сравнение иммунного ответа с использованием одного или более биоанализов in vitro, включая ответы В-клеток и Т-клеток, такие как уровни антител по ИФА, мультиплексному ИФА, MSD, Luminex, проточной цитометрии, ответ клеток TH1/TH17, измерение уровня цитокинов и функциональные уровни антител, измеренные с помощью опсонофагоцитарного уничтожения (OPK), сывороточного бактерицидного теста (SBA), агглютинации, подвижности, цитотоксичности или адгезии; и анализы in vivo на животных моделях пневмококкового заболевания (например, пневмонии, бактериемии, менингита, сепсиса, среднего отита, колонизации носоглотки). Параметры анализов in vivo включают клиренс бактерий из поверхностей слизистых оболочек или кровотока, уменьшение или предотвращение бактериемии, менингита, сепсиса или среднего отита, уменьшение или предотвращение колонизации носоглотки, снижение смертности, а также пассивную и активную защиту после заражения пневмококковыми патогенами, которые являются мишенями иммуногенного состава. В некоторых вариантах осуществления иммунный ответ сравнивают с контрольной композицией. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полисахарид, присутствующий в иммуногенной композиции, и не содержать антигенный полипептид, который присутствует в иммуногенной композиции. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полипептид, присутствующий в иммуногенной композиции, и не содержать антигенный полисахарид, присутствующий в иммуногенной композиции. В некоторых вариантах осуществления контрольная композиция может содержать адъювант, присутствующий в иммуногенной композиции, и не содержать антигенный полисахарид и/или иммуногенный полипептид, присутствующий в иммуногенной композиции.
[417] В некоторых вариантах осуществления способ оценки эффективности иммуногенной композиции, описанной в данном документе, включает оценку, измерение и/или сравнение иммунного ответа с использованием одного или более биоанализов in vitro, включая ответы В-клеток и Т-клеток, такие как уровни антител по ИФА, мультиплексному ИФА, MSD, Luminex, проточной цитометрии, ответ клеток TH1/TH17, измерение уровня цитокинов и функциональные уровни антител, измеренные с помощью OPK, сывороточного бактерицидного теста (SBA), интернализации, нейтрализации активности, агглютинации, подвижности, цитотоксичности или адгезии; и анализы in vivo на животных моделях пневмококкового заболевания (например, пневмонии, бактериемии, менингита, сепсиса, среднего отита, колонизации носоглотки). Параметры анализов in vivo включают клиренс бактерий или уменьшение бактерий на поверхностях слизистых оболочек или в кровотоке, уменьшение или предотвращение бактериемии, менингита, сепсиса или среднего отита, уменьшение или предотвращение колонизации носоглотки, снижение смертности, а также пассивную и активную защиту после заражения пневмококковыми патогенами, которые являются мишенями иммуногенного состава. В некоторых вариантах осуществления иммунный ответ сравнивают с контрольной композицией. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полисахарид, присутствующий в иммуногенной композиции, и не содержать антигенный полипептид, который присутствует в иммуногенной композиции. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полипептид, присутствующий в иммуногенной композиции, и не содержать антигенный полисахарид, присутствующий в иммуногенной композиции. В некоторых вариантах осуществления контрольная композиция может содержать адъювант, присутствующий в иммуногенной композиции, и не содержать антигенный полисахарид и/или иммуногенный полипептид, присутствующий в иммуногенной композиции.
[418] В некоторых вариантах осуществления способ оценки иммуногенности вакцинной композиции, описанной в данном документе, включает оценку, измерение и/или сравнение иммунного ответа с использованием одного или более биоанализов in vitro, включая ответы В-клеток и Т-клеток, такие как уровни антител по ИФА, мультиплексному ИФА, MSD, Luminex, проточной цитометрии, ответ клеток TH1/TH17, измерение уровня цитокинов и функциональные уровни антител, измеренные с помощью OPK, сывороточного бактерицидного теста (SBA), агглютинации, подвижности, цитотоксичности или адгезии; и анализы in vivo на животных моделях пневмококкового заболевания (например, пневмонии, бактериемии, менингита, сепсиса, среднего отита, колонизации носоглотки). Параметры анализов in vivo включают клиренс бактерий из поверхностей слизистых оболочек или в кровотоке, уменьшение или предотвращение бактериемии, менингита, сепсиса или среднего отита, уменьшение или предотвращение колонизации носоглотки, снижение смертности, а также пассивную и активную защиту после заражения пневмококковыми патогенами, которые являются мишенями иммуногенного состава. В некоторых вариантах осуществления иммунный ответ сравнивают с контрольной композицией. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полисахарид, присутствующий в вакцинной композиции, и не содержать антигенный полипептид, присутствующий в вакцинной композиции. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полипептид, присутствующий в вакцинной композиции, и не содержать антигенный полисахарид, присутствующий в вакцинной композиции. В некоторых вариантах осуществления контрольная композиция может содержать адъювант, присутствующий в вакцинной композиции, и не содержать антигенный полисахарид и/или иммуногенный полипептид, присутствующий в вакцинной композиции.
[419] В некоторых вариантах осуществления способ оценки эффективности иммуногенной композиции, описанной в данном документе, включает оценку, измерение и/или сравнение иммунного ответа с использованием одного или более биоанализов in vitro, включая ответы В-клеток и Т-клеток, такие как уровни антител по ИФА, мультиплексному ИФА, MSD, Luminex, проточной цитометрии, ответ клеток TH1/TH17, измерение уровня цитокинов и функциональные уровни антител, измеренные с помощью OPK, сывороточного бактерицидного теста (SBA), агглютинации, подвижности, цитотоксичности или адгезии; и анализы in vivo на животных моделях пневмококкового заболевания (например, пневмонии, бактериемии, менингита, сепсиса, среднего отита, колонизации носоглотки). Параметры анализов in vivo включают клиренс бактерий из поверхностей слизистых оболочек или в кровотоке, уменьшение или предотвращение бактериемии, менингита, сепсиса или среднего отита, уменьшение или предотвращение колонизации носоглотки, снижение смертности, а также пассивную и активную защиту после заражения пневмококковыми патогенами, которые являются мишенями иммуногенного состава. В некоторых вариантах осуществления иммунный ответ сравнивают с контрольной композицией. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полисахарид, присутствующий в вакцинной композиции, и не содержать антигенный полипептид, присутствующий в вакцинной композиции. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полипептид, присутствующий в вакцинной композиции, и не содержать антигенный полисахарид, присутствующий в вакцинной композиции. В некоторых вариантах осуществления контрольная композиция может содержать адъювант, присутствующий в вакцинной композиции, и не содержать антигенный полисахарид и/или иммуногенный полипептид, присутствующий в вакцинной композиции.
[420] В некоторых вариантах осуществления способ оценки иммуногенности фармацевтической композиции, описанной в данном документе, включает оценку, измерение и/или сравнение иммунного ответа с использованием одного или более биоанализов in vitro, включая ответы В-клеток и Т-клеток, такие как уровни антител по ИФА, мультиплексному ИФА, MSD, Luminex, проточной цитометрии, ответ клеток TH1/TH17, измерение уровня цитокинов и функциональные уровни антител, измеренные с помощью OPK, сывороточного бактерицидного теста (SBA), агглютинации, подвижности, цитотоксичности или адгезии; и анализы in vivo на животных моделях пневмококкового заболевания (например, пневмонии, бактериемии, менингита, сепсиса, среднего отита, колонизации носоглотки). Параметры анализов in vivo включают клиренс бактерий из поверхностей слизистых оболочек или в кровотоке, уменьшение или предотвращение бактериемии, менингита, сепсиса или среднего отита, уменьшение или предотвращение колонизации носоглотки, снижение смертности, а также пассивную и активную защиту после заражения пневмококковыми патогенами, которые являются мишенями иммуногенного состава. В некоторых вариантах осуществления иммунный ответ сравнивают с контрольной композицией. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полисахарид, присутствующий в фармацевтической композиции, и не содержать антигенный полипептид, присутствующий в фармацевтической композиции. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полипептид, присутствующий в фармацевтической композиции, и не содержать антигенный полисахарид, присутствующий в фармацевтической композиции. В некоторых вариантах осуществления контрольная композиция может содержать адъювант, присутствующий в фармацевтической композиции, и не содержать антигенный полисахарид и/или иммуногенный полипептид, присутствующий в фармацевтической композиции.
[421] В некоторых вариантах осуществления способ оценки эффективности фармацевтической композиции, описанной в данном документе, включает оценку, измерение и/или сравнение иммунного ответа с использованием одного или более биоанализов in vitro, включая ответы В-клеток и Т-клеток, такие как уровни антител по ИФА, мультиплексному ИФА, MSD, Luminex, проточной цитометрии, ответ клеток TH1/TH17, измерение уровня цитокинов и функциональные уровни антител, измеренные с помощью OPK, сывороточного бактерицидного теста (SBA), агглютинации, подвижности, цитотоксичности или адгезии; и анализы in vivo на животных моделях пневмококкового заболевания (например, пневмонии, бактериемии, менингита, сепсиса, среднего отита, колонизации носоглотки). Параметры анализов in vivo включают клиренс бактерий из поверхностей слизистых оболочек или в кровотоке, уменьшение или предотвращение бактериемии, менингита, сепсиса или среднего отита, уменьшение или предотвращение колонизации носоглотки, снижение смертности, а также пассивную и активную защиту после заражения пневмококковыми патогенами, которые являются мишенями иммуногенного состава. В некоторых вариантах осуществления иммунный ответ сравнивают с контрольной композицией. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полисахарид, присутствующий в фармацевтической композиции, и не содержать антигенный полипептид, присутствующий в фармацевтической композиции. В некоторых вариантах осуществления контрольная композиция может содержать антигенный полипептид, присутствующий в фармацевтической композиции, и не содержать антигенный полисахарид, присутствующий в фармацевтической композиции. В некоторых вариантах осуществления контрольная композиция может содержать адъювант, присутствующий в фармацевтической композиции, и не содержать антигенный полисахарид и/или иммуногенный полипептид, присутствующий в фармацевтической композиции.
[422] В некоторых вариантах осуществления способ оценки иммуногенности и/или эффективности иммуногенного комплекса включает оценку иммунного ответа на иммуногенные или вакцинные композиции, содержащие один или более иммуногенных комплексов. В некоторых вариантах осуществления способ оценки иммуногенности и/или эффективности иммуногенного комплекса, описанного в данном документе, включает оценку, измерение и/или сравнение иммунного ответа с использованием одного или более биоанализов in vitro, включая ответы В-клеток и Т-клеток, такие как уровни антител по ИФА, мультиплексному ИФА, MSD, Luminex, проточной цитометрии, ответ клеток TH1/TH17, измерение уровня цитокинов и функциональные уровни антител, измеренные с помощью OPK, сывороточного бактерицидного теста (SBA), агглютинации, подвижности, цитотоксичности или адгезии; и анализы in vivo на животных моделях пневмококкового заболевания (например, пневмонии, бактериемии, менингита, сепсиса, среднего отита, колонизации носоглотки). Параметры анализов in vivo включают клиренс бактерий из поверхностей слизистых оболочек или в кровотоке, уменьшение или предотвращение бактериемии, менингита, сепсиса или среднего отита, уменьшение или предотвращение колонизации носоглотки, снижение в смертности, а также пассивную и активную защиту после заражения пневмококковыми патогенами, которые являются мишенями иммуногенного состава.
[423] Вообще говоря, может быть желательно оценить гуморальные ответы, клеточные ответы и/или взаимодействия между ними. При оценке гуморальных ответов титры и/или типы антител (например, общий IgG, IgG1, IgG2, IgM, IgA и т. д.), специфичные к полисахаридам или полипептидам конкретных патогенов (серотипспецифическими или консервативными для двух или более серотипов) могут быть определены, например, до и/или после введения примирующей или бустерной дозы вакцины (и/или по сравнению с уровнями антител в отсутствие антигенной стимуляции). Клеточные ответы можно оценивать путем мониторинга реакций, таких как реакции гиперчувствительности замедленного типа и т.д., на белок-носитель. Клеточные ответы также можно измерить непосредственно путем оценки ответа моноцитов из мононуклеарных клеток периферической крови (МКПК) на стимуляцию представляющими интерес антигенами. Популяции предшественников В клеток и В-клеток памяти можно оценивать с помощью иммуноферментных анализов (ELISpot), направленных против полисахаридов или полипептидов конкретных патогенов.
[424] Для определения уровней и/или активности антител в сыворотках субъектов можно использовать любой из множества анализов. Подходящие анализы включают, например, анализы связывания лиганда, такие как радиоиммуноанализ (РИА), ИФА и мультиплексные анализы (Luminex, Bioplex, MSD); функциональные анализы, такие как анализы опсонофагоцитирующей активности или анализы интернализации; и анализы in vivo на животных моделях пневмококкового заболевания (например, пневмонии, бактериемии, менингита, сепсиса, среднего отита, колонизации носоглотки). Параметры анализов in vivo включают клиренс бактерий из поверхностей слизистых оболочек или в кровотоке, уменьшение или предотвращение бактериемии, менингита, сепсиса или среднего отита, уменьшение или предотвращение колонизации носоглотки, снижение в смертности, а также пассивную и активную защиту после заражения пневмококковыми патогенами, которые являются мишенями иммуногенного состава.
[425] При помощи метода РИА выявляют специфические антитела путем инкубации сывороток с радиоактивно меченными полисахаридами или полипептидами в суспензии (например, Schiffiman et al, 1980). Затем комплексы антиген-антитело осаждают сульфатом аммония и радиоактивно меченые гранулы анализируют на количество импульсов в минуту (имп/мин).
[426] В методе обнаружения при помощи ИФА специфические антитела из сывороток вакцинированных субъектов количественно оценивают путем инкубации с полисахаридами или полипептидами (серотипспецифическими или консервативными для двух или более серотипов), которые были адсорбированы на твердой подложке (например, Koskela and Leinonen (1981); Kojima et al, 1990; Concepcion and Frasch, 2001). Связанное антитело обнаруживают с помощью конъюгированных с ферментом вторичных детектирующих антител. ИФА также позволяет изотипировать и разделить на подклассы иммунный ответ (например, IgM и IgG или IgG1 и IgG2) с использованием вторичных антител, специфичных для изотипа или подкласса, и может быть адаптирован для оценки авидности антител (Anttila et al, 1998; Romero-Steiner et al, 2005). Мультиплексные анализы (например, Luminex) облегчают одновременное обнаружение антител к нескольким антигенам. Капсульный полисахарид(-ы) или полипептиды конъюгированы со спектрально различными микрогранулами, которые смешиваются и инкубируются с сывороткой. Антитела, связанные с полисахаридами или полипептидами на покрытых микрогранулах, выявляют с использованием вторичных антител (например, конъюгированного с R-фикоэритрином козьего антитела к IgG человека).
[427] Подход к оценке функциональных антител в сыворотке представляет собой анализ опсонофагоцитирующей активности (OPA) или анализ опсонофагоцитирующей активности в концентрированной смеси (COPA), который определяет количественно только те антитела, которые могут опсонизировать бактерии, что приводит к поглощению и уничтожению бактерий. В стандартном анализе используются фагоцитарные эффекторные клетки человека, источник комплемента, бактерии и разбавленные сыворотки. Результатом анализа является сывороточный титр в конечной точке, при котором происходит уничтожение >50% по сравнению с бактериями, инкубированными только с комплементом и человеческими клетками (Romero-Steiner et al, 1997). Этот OPA в отношении уничтожения также может быть мультиплексирован за счет применения штаммов-мишеней патогена, которые несут различные маркеры устойчивости к антибиотикам (Kim et al, 2003). Другой тип мультиплексного опсонического анализа представляет собой неуничтожающий анализ, в котором поглощение фагоцитарными эффекторными клетками флуоресцентно окрашенного инкапсулированного патогена или флуоресцентных микрогранул, конъюгированных с антигенными полисахаридами или полипептидами целевого патогена в присутствии разбавленных сывороток плюс источник комплемента, оценивается в проточной цитометрии (Martinez et al, 1999). Опсоническая активность сывороточного антитела плюс комплемент также может быть оценена путем измерения окислительного ответа фагоцитирующих эффекторных клеток человека на поглощенный патоген (Munro et al. 1985; Ojo-Amaize et al. 1995).
[428] Некоторые модельные системы in vivo можно использовать для оценки защиты, обеспечиваемой сывороточными антителами, индуцированными вакцинами по настоящему изобретению. В таких системах пассивной защиты мышам или крысам вводят патоген плюс разбавленные сыворотки и определяют конечный сывороточный титр в конечной точке, который обеспечивает защиту от пневмонии, бактериемии, колонизации органов или тканей или смертности (Stack et al. 1998; Saeland et al. 2000).
[429] В некоторых вариантах осуществления эффективность вакцинации может быть определена путем анализа одного или более уровней цитокинов путем стимуляции Т-клеток субъекта после вакцинации. Один или более уровней цитокинов можно сравнить с одним или более уровнями цитокинов у одного и того же субъекта до вакцинации. Повышенные уровни одного или более цитокинов, например, 1,5-кратное, 2-кратное, 5-кратное, 10-кратное, 20-кратное, 50-кратное или 100-кратное или большее увеличение по сравнению с уровнями цитокинов до иммунизации, могут указывать на повышенный ответ на вакцину. В некоторых вариантах осуществления один или более цитокинов выбраны из GM-CSP; ИЛ-1α; ИЛ-1β; ИЛ-2; ИЛ-3; ИЛ-4; ИЛ-5; ИЛ-6; ИЛ-7; ИЛ-8; ИЛ-10; ИЛ-12; ИЛ-17A, ИЛ-17F или другие члены семейства ИЛ-17; ИЛ-22; ИЛ-23; ИФН-α; ИФН-β; ИФН-γ; MIP-1α; MIP-1β; ТФР-β; ФНО-α или ФНО-β. В неограничивающем примере эффективность вакцинации может быть определена путем анализа уровней ИЛ-17 (особенно ИЛ-17A) путем стимуляции Т-клеток субъекта после вакцинации. Уровни ИЛ-17 можно сравнить с уровнями ИЛ-17 у того же субъекта перед вакцинацией. Повышенные уровни ИЛ-17 (например, ИЛ-17A), например, 1,5-кратное, 2-кратное, 5-кратное, 10-кратное, 20-кратное, 50-кратное или 100-кратное или большее увеличение, будут указывать на повышенное ответ на вакцину.
[430] В некоторых вариантах осуществления можно анализировать нейтрофилы в присутствии Т-клеток или антител пациента на предмет уничтожения пневмококков. Повышенное уничтожение пневмококков, например, 1,5-красное, 2-красное, 5-кратное, 10-кратное, 20-кратное, 50-кратное или 100-кратное или большее увеличение, будет указывать на повышенный ответ на вакцину. Например, можно измерить активацию клеток TH17, причем повышенная активация клеток TH17, такая как 1,5-кратное, 2-кратное, 5-кратное, 10-кратное, 20-кратное, 50-кратное или 100-кратное или большее увеличение, коррелирует с повышенным ответом на вакцину. В другом неограничивающем примере можно измерить активацию клеток TH1, причем повышенная активация клеток TH1, такая как 1,5-кратное, 2-кратное, 5-кратное, 10-кратное, 20-кратное, 50-кратное или 100-кратное или большее увеличение, коррелирует с повышенным ответом на вакцину. Можно также измерить уровни антитела, специфичного к вакцине, причем повышенные уровни специфического антитела, например, 1,5-кратное, 2-кратное, 5-кратное, 10-кратное, 20-кратное, 50-кратное или 100-кратное или большее увеличение, коррелируют с повышенной эффективностью вакцины. В некоторых вариантах осуществления используются два или более из этих анализов. Например, можно измерить уровни ИЛ-17 и уровни специфических для вакцин антител. В качестве альтернативы можно следить за эпидемиологическими маркерами, такими как частота, тяжесть или продолжительность пневмококковой инфекции у вакцинированных лиц по сравнению с невакцинированными.
[431] Эффективность вакцины также можно анализировать в различных модельных системах, таких как модель заражения мышей. Например, можно использовать линии мышей BALB/c или C57BL/6. После введения исследуемой вакцины (однократной или многократной) экспериментатор вводит дозу для заражения S. pneumoniae. В некоторых случаях дозы для заражения, вводимой интраназально, достаточно, чтобы вызвать колонизацию S. pneumoniae (особенно назальную колонизацию) у невакцинированных животных, а в некоторых случаях дозы для заражения, вводимой посредством аспирации, достаточно, чтобы вызвать сепсис и высокий уровень летальности у невакцинированных животных. В некоторых случаях дозы для заражения, вводимой внутрибрюшинно, достаточно, чтобы вызвать сепсис и привести к высокой летальности у невакцинированных животных. В некоторых случаях дозы для заражения, вводимой посредством внутривенной инъекции, достаточно, чтобы вызвать сепсис и привести к высокой летальности у невакцинированных животных. Затем можно измерить снижение колонизации или снижение летальности у вакцинированных животных.
[432] Некоторые модельные системы in vivo можно использовать для оценки защиты, обеспечиваемой сывороточными антителами, индуцированными вакцинами по настоящему изобретению. В таких системах пассивной защиты мышам или крысам вводят патоген плюс разбавленные сыворотки и определяют конечный сывороточный титр в конечной точке, который обеспечивает защиту от бактериемии, колонизации органов или тканей или смертности (Stack et al. 1998; Saeland et al. 2000).
Наборы
[433] Настоящее изобретение также обеспечивает наборы для получения иммуногенного комплекса, как описано в данном документе, которые могут быть использованы исследователем для адаптации иммуногенного комплекса с их предпочтительными антигенами, например, в исследовательских целях для оценки действия антигена или комбинации антигенов в отношении иммунной реакции. Такие наборы можно приготовить из легкодоступных материалов и реагентов. Например, такие наборы могут содержать любой один или более из следующих материалов: контейнер, содержащий полисахарид, сшитый с множеством первых аффинных молекул; контейнер, содержащий комплементарную аффинную молекулу, которая ассоциируется с первой аффинной молекулой, причем комплементарная аффинная молекула ассоциируется с антигеном или белком-носителем; контейнер, содержащий антиген; контейнер, содержащий белок-носитель; контейнер, содержащий антиген, ассоциированный с комплементарной аффинной молекулой; контейнер, содержащий белок-носитель, ассоциированный с комплементарной аффинной молекулой.
[434] В еще одном варианте осуществления набор содержит контейнер, содержащий полисахарид; контейнер, содержащий множество первых аффинных молекул; и контейнер, содержащий сшивающий реагент для сшивания первых аффинных молекул с полисахаридом, например, но не ограничиваясь ими, CDAP (1-циано-4-диметиламинопиридиний тетрафторборат) и EDC (1-этил-3-[3-диметиламинопропил] карбодиимид гидрохлорид).
[435] В еще одном варианте осуществления набор содержит контейнер, содержащий антиген или белок-носитель, и контейнер, содержащий комплементарную аффинную молекулу, которая ассоциируется с первой аффинной молекулой. В некоторых вариантах осуществления набор дополнительно содержит средства для присоединения комплементарной аффинной молекулы к антигену или белку-носителю, где средство может быть сшивающим реагентом или каким-либо промежуточным слитым белком.
[436] В некоторых вариантах осуществления набор может содержать по меньшей мере один фактор костимуляции, который может быть добавлен к полимеру. В некоторых вариантах осуществления набор содержит сшивающий реагент, например, но не ограничиваясь ими, CDAP (1-циано-4-диметиламинопиридиний тетрафторборат); EDC (1-этил-3-[3-диметиламинопропил] карбодиимид гидрохлорид); натрий цианоборгидрид; бромид цианоген; и аммоний бикарбонат/йодуксусную кислоту для связывания кофактора с полимером.
[437] Для применения в описанных в данном документе способах можно приготовить множество наборов и компонентов, в зависимости от предполагаемого использования набора, конкретного антигена-мишени и потребностей пользователя.
ИЛЛЮСТРАТИВНЫЕ ПРИМЕРЫ
Пример 1. Капсульные полисахариды S. pneumoniae
Получение и очистка
[438] Способы культивирования пневмококков хорошо известны специалистам в данной области техники (например, Chase, 1967, Methods of Immunology and Immunochemistry 1:52). Способы получения капсульных полисахаридов пневмококка также хорошо известны в данной области техники (например, европейский патент № EP0497524). Изоляты пневмококковых серотипов доступны в АТСС или Национальной коллекции типовых культур Министерства здравоохранения Англии.
[439] S. pneumoniae идентифицируются как неподвижные грамположительные ланцетообразные диплококки, являющиеся альфа-гемолитическими на кровяном агаре. Большинство, но не все штаммы инкапсулированы. Серотипы дифференцируют на основе пробы Нейфельда (реакция набухания бактериальной капсулы) с использованием специфических антисывороток (например, патент США № 5847112), латексной агглютинации или мультилокусного типирования последовательностей.
[440] Замороженный флакон, в котором представлен каждый из серотипов S. pneumoniae, присутствующих в вакцине MAPS, размораживали и использовали для создания посевной культуры в подходящей предварительно стерилизованной питательной среде. Посевную культуру выращивали с контролем температуры и pH. Посевную культуру переносили в производственный ферментер, который содержал предварительно стерилизованную питательную среду. Культуру для продуцирования выращивали, контролируя температуру, pH и скорость перемешивания. Процесс роста прекращали добавлением инактивирующего агента с контролируемой температурой.
[441] Процесс очистки был инициирован удалением клеточного дебриса с использованием комбинации центрифугирования и фильтрации. Материал фильтровали с последующим фракционированием на основе растворителя для удаления примесей и извлечения PS.
Характеристики
[442] Все характеристики PS в Таблице 1 были получены из Европейской фармакопеи 9.0, таблица 0966-1, за исключением размера молекулы и серотипа 6A, которые получены из сертификата производителя для анализа.
Таблица 1. Иллюстративные характеристики полисахарида (PS)
Показанные значения представляют собой процентное содержание компонентов моновалентного суммарного PS.
† Различные типы указаны с использованием датской номенклатуры.
‡ Сшитая агароза для хроматографии R.
§ Сшитая агароза для хроматографии R1.
Пример 2. Получение слитого белка CP1
Конструкция вектора
[443] Слитый белок CP1 содержит биотинсвязывающую часть ризавидина, охватывающую аминокислоты с 45 по 179 полноразмерного белка, кодируемого геномом. Предсказанные сигнальные последовательности (аминокислоты 1-44) ризавидина не были включены. Для оптимизации уровня экспрессии CP1 в E.coli последовательность гена, кодирующего полипептид ризавидина (аминокислоты 45-179; SEQ ID NO: 2), была переработана с использованием кодонов экспрессии, предпочтительных для E.coli, синтезированных и клонированных в плазмиду pET24a(+). Этот синтетический ген ризавидина был обозначен как Rhavi.
[444] Для конструирования CP1 последовательность ДНК, кодирующую гибкую линкерную область, состоящую из семи аминокислот (GGGGSSS; SEQ ID NO: 3), непосредственно вставляли в 3'-конец синтетического гена Rhavi, чтобы обеспечить отделение от Rhavi и способствовать правильному фолдингу в последующем слитому белку. Гены, кодирующие желаемые части белка SP1500 и SP0785 (не включая предсказанные сигнальные последовательности; последовательности нуклеиновых кислот SEQ ID NO: 7 и SEQ ID NO: 8, соответственно), были синтезированы и вставлены в вектор экспрессии Rhavi сразу за линкерной областью. Три остаточные аминокислоты (AAA) из сайта рестрикции Not I pET24a(+) разделяют SP1500 и SP0785 и могут называться вторым линкером CP1.
[445] Схема слитого белка CP1 показана на Фиг. 2. Конструкция плазмиды pET24a(+)-CP1 показана на Фиг. 4, а карта признаков показана в Таблице 2. Последовательность ДНК, кодирующая слитый белок CP1 (Rhavi-GGGGSSS-SP1500- AAA-SP0785) клонировали в вектор pET-24a(+) с использованием сайтов рестрикции NdeI и XhoI. Стоп-кодоны вставляли на 3’-конце конструкции ДНК CP1. После завершения клонирования проводили секвенирование ДНК для подтверждения присутствия, ориентации и последовательности конструкции ДНК CP1, вставленной в вектор CP1/pET-24a(+).
Таблица 2. Карта признаков
п.о.: пара оснований; His: гистидиновая метка; Laci: ингибитор лактозного оперона r; LacO1: лактозный оператор; Ori_ColE1: точка начала репликации колицина E1; Ori_f1: точка начала репликации из фага F1; Term_T7: терминатор T7; ROP: репрессор праймера.
Создание Главного банка клеток (MCB)
[446] Для создания Исследовательского банка клеток (RCB) вектор CP1/pET-24a(+) трансформировали в экспрессионный штамм E. coli.
[447] Трансформированные клетки E. coli помещали в чашки Петри для культивирования, содержащие канамицин. Отбирали одиночную колонию из чашки Петри и использовали для инокуляции в жидкую среду во встряхиваемой колбе. Колбы помещали в шейкер-инкубатор для культивирования а течение ночи и выращивали до желаемой ОП. Затем бактериальную культуру смешивали с раствором глицерина. Смешанный раствор распределяли по флаконам для получения RCB.
[448] Для создания MCB, RCB инокулировали в жидкую среду во встряхиваемых колбах и выращивали до желаемой ОП. Затем бактериальную культуру доводили до 15% глицерина, смешивали и вносили аликвотами во флаконы. Затем флаконы MCB были помещены при -80 °C (от -70°C до -90 °C), и выбранные флаконы были взяты для проверки качества.
Общая схема производственного процесса
[449] Слитый белок CP1 экспрессировали в E. coli. Экспрессированный слитый белок CP1 был высвобожден из клеток E. coli и очищен с помощью ряда стадий хроматографии и фильтрации. В следующем разделе подробно описан процесс производства CP1 в условиях 300-х литровой культуры.
[450] Таким образом, процесс был инициирован размораживанием и инокуляцией клеток из флакона MCB в клеточную среду. Первоначальное размножение клеток проводили в колбе, а затем бактериальную культуру переносили в ферментер на 300 л.
[451] Бактерии собирали центрифугированием. Восстановленную клеточную пасту ресуспендировали в буфере для лизиса и псевдоожижали с помощью микрофлюидизатора. Суммарный слитый белок CP1 в псевдоожиженном клеточном лизате очищали стадиями осаждения и хроматографии. Конечный технологический поток представлял собой концентрацию и замену буфера на 20 мМ Трис, 150 мМ NaCl при pH 8,0 ± 0,1 через ультрафильтрационные мембраны. Наконец, слитый белок CP1 пропускали через фильтр с диаметром пор 0,22 мкм непосредственно перед розливом во флаконы и хранили при -80 °C.µ
[452] Никакое сырье не содержало компонентов животного или человеческого происхождения. Описание клетки см. выше.
Процесс синтеза
[453] Блок-схема процесса синтеза для CP1 представлена на Фиг. 5, а подробные сведения об отдельных стадиях приведены ниже.
[454] В культуре клеток использовали химически определенные среды и компоненты в зависимости от стадии производства. Используемые среды были средами для клеток, средами для продуцирования, подпитывающей средой 1 и подпитывающей средой 2. Эти среды использовали для размножения посевной культуры, выращивания и подпитки, соответственно.
Стадия 1-1. Размораживание клеток
Готовили достаточное количество клеточной среды и переносили в подходящую колбу для культивирования, а затем замороженные MCB оттаивали.
Стадия 1-2. Размножение в колбе
Размороженные MCB инокулировали и выращивали в колбе на 2,5 л. Рост клеток контролировали с помощью спектрофотометра при ОП600.
Стадия 1-3. Культура для продуцирования
Культивирование для продуцирования осуществляли в режиме периодического культивирования с подпиткой. Для поддержки получения продукта и продления периода продуцирования клеточной культуры, подпитывающую среду 1 и подпитывающую среду 2 добавляли после соответствующей фазы роста клеток. Как только температура ферментера достигла заданного значения, добавляли изопропил-β-D-1-тиогалактопиранозид для индукции экспрессии слитого белка CP1.
Примерно через 18 часов после индукции сбор начинали центрифугированием.
Стадия 1-4. Сбор
Бактериальную культуру собирали центрифугированием в непрерывном потоке.
Стадия 1-5. Лизис клеток и осветление
Восстановленную клеточную пасту ресуспендировали в буфере для лизиса и псевдоожижали с помощью микрофлюидизатора. Псевдоожиженный клеточный лизат, включая суммарный слитый белок CP1, центрифугировали и собирали супернатант.
Процесс выделения
[455] После сбора и лизиса клеток слитый белок CP1 очищали с помощью нескольких стадий хроматографии. Блок-схема процесса очистки CP1 представлена на Фиг. 6. Подробности для отдельных стадий приведены ниже.
Стадия 2-1. Осаждение сульфатом аммония/центрифугирование и фильтрация
К осветленному лизату добавляли раствор сульфата аммония и доводили его до конечной концентрации 0,8 М. После смешивания при комнатной температуре осветленный лизат с сульфатом аммония центрифугировали и собирали супернатант. Собранный супернатант фильтровали через фильтр с диаметром пор 0,22 мкм и собирали в соответствующий контейнер.µ
Стадия 2-2. Хроматография гидрофобных взаимодействий
Целью этой стадии является удаление загрязняющих веществ, связанных с процессом. Слитый белок CP1, связанный со смолой, промывали буфером с высокой концентрацией сульфата аммония, затем элюировали буфером для элюирования (концентрация NaCl в буфере постепенно снижалась). Анализ методом электрофореза в полиакриламидном геле с додецилсульфатом натрия (ДСН-ПААГ) проводили с каждой фракцией для подтверждения наличия слитого белка CP1.
Стадия 2-3. Концентрирование/Фильтрование с помощью тангенциальной поточной фильтрации
Пул для элюирования концентрировали, а затем заменяли буфер на несколько объемов трис-забуференного физиологического раствора с использованием фильтрующей мембраны на 30 кДа. Ретентат, отфильтрованный с помощью тангенциальной фильтрации (TFF), фильтровали через фильтр с диаметром пор 0,22 мкм.µ
Стадия 2-4. Анионообменная хроматография
Целью этой стадии является удаление загрязняющих веществ, связанных с процессом. Слитый белок CP1, связанный со смолой, промывали промывочным буфером NaCl, затем элюировали элюирующим буфером NaCl (концентрация NaCl в буфере постепенно увеличивалась). Анализ методом ДСН-ПААГ-электрофореза выполняли для каждой фракции, чтобы подтвердить наличие слитого белка CP1.
Стадия 2-5. Хроматография 1-го типа
Целью этой стадии является дополнительное удаление загрязняющих веществ, связанных с процессом. Слитый белок CP1, связанный со смолой, промывали фосфатным промывочным буфером, затем элюировали фосфатным элюирующим буфером (концентрация фосфата в буфере постепенно увеличивалась). Анализ методом ДСН-ПААГ-электрофореза выполняли для каждой фракции, чтобы подтвердить наличие слитого белка CP1.
Стадия 2-6. Состав TFF
Пул хроматографических фракций типа 1 концентрировали, а затем буфер заменяли на несколько объемов буфера для состава (20 мМ Трис, 150 мМ хлорид натрия, pH 8,0 ± 0,1) с использованием фильтрующей мембраны на 30 кДа. Составленный слитый белок CP1 пропускали через фильтр с диаметром пор 0,22 мкм.µ
Система контейнер/укупорочный элемент
[456] Слитый белок CP1 хранили при -80 °C (от -70°C до -90 °C) в стерильных флаконах из полиэтилентерефталата.
Пример 3. Получение иммуногенных комплексов MAPS
Обзор
[457] В платформе MAPS используется преимущества нековалентного связывания высокой аффинности (константа диссоциации
[KD] ≈ 10-15M) между биотином и ризавидином, биотинсвязывающим белком, который не имеет значительной предсказанной гомологии с человеческими белками. Ризавидин, встречающийся в природе димерный белок из семейства белков авидина, был впервые обнаружен у Rhizobium etli, симбиотической бактерии фасоли. Ризавидин имеет только 22% аминокислотную идентичность с куриным авидином, белком, обычно обнаруживаемым в яйцах, но с высоким уровнем сохранения аминокислотных остатков, участвующих в связывании биотина. В образцах сыворотки человека, полученных от субъектов, подвергшихся действию авидина, перекрестной реактивности с ризавидином не наблюдали [Helppolainen et al, 2007], что позволяет предположить, что антитела к ризавидину не могут перекрестно реагировать с куриным авидином. Конъюгаты биотина использовали в нескольких клинических применениях без каких-либо нежелательных явлений [Buller et al, 2014; Paty et al, 2010; Lazzeri et al, 2004]. Процесс биотинилирования PS и процесса иммуногенного комплексообразования MAPS в MAPS24 был оптимизирован для постоянного отсутствия свободного биотина, что снижает возможность образования антител к биотину.
[458] Вакцины-кандидаты MAPS включают генетически сконструированные слитые белки ризавидина или его биотинсвязывающего домена или биотинсвязывающего фрагмента, а также представляющие интерес белковые антигены, которые затем связываются в комплекс с представляющими интерес биотинилированными PS, что приводит к специфической сборке в интегрированные макромолекулярные иммуногенные комплексы, которые при обработке иммунной системой приводят к активации защитных B- и T-клеточных иммунных ответов, как схематично показано на Фиг. 1.
[459] MAPS24 представляет собой новую кандидатную пневмококковую вакцину, основанную на запатентованной платформе MAPS. MAPS24 представляет собой поливалентную вакцину MAPS, содержащую 24 капсульных пневмококковых полисахаридов серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F, индивидуально биотинилированных и связанных в комплекс со слитым белком CP1. MAPS15 представляет собой поливалентную вакцину MAPS, содержащую 15 капсульных пневмококковых PS серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F, и 33F), индивидуально биотинилированных и связанных с слитым белком CP1. MAPS9 представляет собой поливалентную вакцину MAPS, содержащую 9 капсульных пневмококковых PS серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F и 20B, индивидуально биотинилированных и связанных в комплекс со слитым белком CP1. CP1 содержит генетическую слитую конструкцию из усеченного ризавидина и 2 пневмококковых белков (SP1500 и SP0785), соединенных линкерами, как показано на Фиг. 2. Ни одна из доступных вакцин не содержит эту уникальную комбинацию PS и полипептидных антигенов, которые способны вызывать иммунный ответ против такого широкого спектра серотипов пневмококков.
Сборка иммуногенных комплексов MAPS
[460] Лекарственная субстанция (иммуногенный комплекс MAPS) состоит из PS и слитых белков CP1. Поскольку PS биотинилирован, а слитый белок CP1 имеет биотинсвязывающий домен ризавидина, они связаны посредством высокоаффинного взаимодействия биотин-ризавидин. Иммуногенное комплексообразование MAPS проводили по отдельности для каждого серотипа PS.
[461] Иммуногенный комплекс MAPS был сделан из 2 ключевых промежуточных продуктов: PS 24, 15 или 9 серотипов S. pneumoniae и слитого с ризавидином белка CP1. PS был активирован путем создания цианатного эфира, а затем биотинилирован. Биотинилированный PS смешивали со слитым белком CP1 для создания иммуногенного комплекса MAPS, который связан посредством высокоаффинного взаимодействия биотин-ризавидин.
[462] Иммуногенный комплекс MAPS составляли из 150 мМ хлорида натрия и буфера с поверхностно-активным веществом, затем пропускали через фильтр с диаметром пор 0,2 мкм непосредственно перед розливом во флаконы и хранением при 2-8 °C.µ Этот составленный иммуногенный комплекс MAPS называется лекарственной субстанцией MAPS.
[463] Никакое сырье не содержало компонентов животного или человеческого происхождения.
[464] Блок-схема процесса комплексирования MAPS представлена на Фиг. 7, а подробные сведения об отдельных стадиях приведены ниже.
Стадия 1: Очистка полисахаридов
[465] Целью этой стадии является удаление остаточных примесей в процессе. Растворенный PS очищали фильтрованием, затем заменяли
несколькими объемами воды для инъекций с последующей ультрафильтрацией для концентрирования PS. Очищенный PS фильтровали через фильтрующую мембрану с диаметром пор 0,22 мкм.µ
Стадия 2: Биотинилирование и очистка полисахарида
[466] Гидроксильная группа на PS была активирована 1-циано-4-диметиламинопиридиний тетрафторборатом (CDAP) для создания высокоактивного цианоэфира. Цианоэфиры реагировали с амин-ПЭГ3-биотином, а непрореагировавшие цианоэфиры блокировали глицином. Биотинилированный PS заменяли буфером на 1 мМ PBS, чтобы удалить непрореагировавший CDAP, амин-ПЭГ3-биотин, глицин и остаточные примеси. После замены буфера биотинилированный PS пропускали через фильтр с диаметром пор 0,22 мкм.µ
Стадия 3. Иммуногенное комплексообразование MAPS
[467] Биотинилированный PS смешивали со слитым белком CP1 для создания иммуногенного комплекса MAPS, который связан посредством высокоаффинного взаимодействия биотин-ризавидин. Иммуногенный комплекс MAPS очищали для удаления PS и белка, которые не образовали комплекс, с использованием фильтрующей мембраны. После очистки иммуногенный комплекс MAPS фильтровали через фильтр с диаметром пор 0,22 мкм и хранили при температуре от 2°C до 8 °C.µ
Характеристики
[468] Иллюстративные характеристики иммуногенного комплекса MAPS/лекарственной субстанции MAPS представлены в Таблице 3.
Таблица 3. Иллюстративные характеристики лекарственной субстанции MAPS
(1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F)
FIO: исключительно в информационных целях; MAPS: система презентации множественных антигенов; PS: полисахарид.
Пример 4. Вакцины MAPS24, MAPS15 и MAPS9
Лекарственный препарат
[469] MAPS24 представляет собой 24-валентную вакцину MAPS, содержащую 24 типа иммуногенных комплексов MAPS. Каждый тип комплекса содержит полисахарид одного из серотипов S. pneumoniae 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F. В иллюстративных составах вакцину MAPS24 составляют таким образом, чтобы каждая доза лекарственного препарата MAPS24 объемом 0,5 мл содержала 1, 2 или 5 мкг каждого PS (от каждого из S. pneumoniae серотипов 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F) вносятся каждым видом иммуногенного комплекса MAPS. MAPS24 был составлен для внутримышечного введения с адъювантом фосфатом алюминия. Общее количество алюминия на дозу составляло 0,625 мг, что ниже максимальной рекомендованной дозы FDA/ВОЗ от 0,85 до 1,25 мг. Этот приготовленный раствор имел pH около 5,8. Диапазон pH 5,3-6,3 считается приемлемым. MAPS15 и MAPS9 представляют собой 15-валентную и 9-валентную вакцины MAPS, соответственно. Иллюстративные вакцины MAPS15 и MAP9 были составлены таким же образом, как MAPS24, с соответствующим PS серотипа S. pneumoniae в качестве иммуногенных комплексов MAPS. Иллюстративные вакцины MAPS15 содержат 1, 2 или 5 мкг PS каждого из S. pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F и 33F в качестве иммуногенных комплексов MAPS. Иллюстративный MAPS9 содержал 1, 2 или 5 мкг PS каждого из S. pneumoniae серотипов 2, 8, 9N, 10A, 11A, 12F, 15B, 17F и 20B в виде иммуногенных комплексов MAPS.
Процесс производства вакцины
[470] Лекарственные препараты MAPS24, MAPS15 и MAPS9 были составлены путем смешивания лекарственных субстанций MAPS 24, 15 или 9, компаундирования путем смешивания эксципиентов и буферов, фильтрации через стерильный фильтр, добавления автоклавированного фосфата алюминия и хранения в стеклянных флаконах при 2 °C - 8 °С. Иллюстративные производственные процессы показаны на панели A и панели B на Фигуре 8. Технические характеристики лекарственного препарата представлены в Таблице 4.
Таблица 4. Иллюстративные технические характеристики лекарственного препарата (на PS)
суспензия
суспензия
суспензия
Конц.: концентрация; PS: полисахарид.
Пример 5. Иммуногенность поливалентных пневмококковых вакцин
Исследование 1. Оценка титров серотипспецифических антител к PS после иммунизации лекарственным препаратом на основе 24-валентного и 15-валентного MAPS
Способы
[471] Иммуногенные комплексы MAPS собирали путем объединения биотинилированного полисахарида со слитым белком CP1 в присутствии 20 мМ Трис, pH 8,0, 150 мМ хлорида натрия и инкубирования в условиях перемешивания при комнатной температуре в течение 16 ± 4 часов. Агрегаты, образовавшиеся в ходе реакции, удаляли фильтрованием через фильтр с диаметром пор 1,2 мкм.µ Затем иммуногенные комплексы MAPS очищали диафильтрацией в 150 мМ хлорида натрия и стерилизовали фильтрованием с использованием фильтра с диаметром пор 0,2 мкм.µ
[472] Отдельные иммуногенные комплексы MAPS объединяли для создания исходного материала в полной дозе для человека (2,2 мкг каждого PS на дозу) для 24-валентного (MAPS24) и 15-валентного (MAPS15) лекарственного препарата. 1,25 мг/мл (исходя из содержания элементарного алюминия) адъюванта, или p-Al(OH)3 или AlPO4, добавляли к этим смесям иммуногенных комплексов MAPS (24v или 15v) в буфере для композиции и инкубировали с вращением с донышка на крышку в течение 18 часов при 4 °C, чтобы позволить иммуногенным комплексам MAPS адсорбироваться на адъювантах.
[473] Шесть составов были приготовлены в полной дозе для человека с использованием 24-валентных и 15-валентных моновалентных MAPS. К ним относятся: MAPS24 без адъюванта (группа A), MAPS24 с адъювантом p-Al(OH)3 (группа B), MAPS24 с адъювантом AlPO4 (группа C), MAPS15 без адъюванта (группа E), MAPS15 с адъювантом p-Al(OH)3 (группа F) и MAPS15 с адъювантом AlPO4 (группа G). Prevnar 13 (группа D) использовали в качестве контроля в этом исследовании. Перед началом исследования указанные выше группы A-G разбавляли до 1/10 дозы для человека (0,22 мкг каждого PS на дозу, за исключением PS 6B с 0,44 мкг PS на дозу) соответствующими буферами для разведения.
[474] Шесть составов были приготовлены в полной дозе для человека с использованием 24-валентных и 15-валентных моновалентных MAPS. К ним относятся: MAPS24 без адъюванта (группа A), MAPS24 с адъювантом p-Al(OH)3 (группа B), MAPS24 с адъювантом AlPO4 (группа C), MAPS15 без адъюванта (группа E), MAPS15 с адъювантом p-Al(OH)3 (группа F) и MAPS15 с адъювантом AlPO4 (группа G). Prevnar 13 (группа D) использовали в качестве контроля в этом исследовании. Перед началом исследования группы A-G, указанные выше, были разбавлены до 1/10 человеческой дозы (0,22 мкг каждого PS на дозу, за исключением PS 6B в Prevnar 13 с 0,44 мкг PS на дозу) соответствующими буферами для разведения (Таблица 5).
Таблица 5. Разведения для создания доз, используемых в исследовании
доза
Н/П означает «не применимо»
Протокол иммунизации кроликов
[475] Как приведено в Таблице 6, новозеландских белых кроликов (NZW) (AFV1110-1162) иммунизировали внутримышечно в один участок (в бедро; 0,5 мл/участок) на 0-й день и в другое бедро на 14-й день с одной десятой дозы для человека (0,22 мкг) каждого PS для групп A-C, MAPS24; групп E-G, MAPS15 и группы D. Prevnar 13, (за исключением PS 6B с 0,44 мкг PS на дозу). Сыворотку собирали перед первой иммунизацией (обозначенной как P0), второй иммунизацией (обозначенной как P1) и через две недели после последней иммунизации на 28 день (обозначенной как P2).
Таблица 6. Исследуемые группы по иммунизации кроликов
введения
Иммунизации
Сыворотки
(0,22 мкг)
(0,22 мкг)
(0,22 мкг)
*(0,22 мкг)
(0,22 мкг)
(0,22 мкг)
(0,22 мкг)
*Доза 6B составляла 0,44 мкг для 1/10 дозы для человека.
Иммуногенность: оценка титров серотипспецифических полисахаридных антител
[476] Чтобы оценить титры серотипспецифических полисахаридных антител у иммунизированных кроликов, был проведен электрохемилюминесцентный иммуноанализ Meso Scale Discovery (MSD) с планшетами U-plex, покрытыми полисахаридами Streptococcus pneumoniae (PnPS) (серотипы 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9V, 9N, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 22F, 23F и 33F). Существующий 13v стандарт сыворотки (BCH14) и 13v сыворотка внутреннего контроля (BCH13) были дополнены антисыворотками, специфическими к 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20A, 22F и 33F, для получения модифицированного BCH14 и модифицированного BCH13, соответственно, (для облегчения количественного определения серотипов кроликов, иммунизированных вакциной MAPS). Вкратце, 5-кратные серийные разведения были созданы, начиная с разведения 1:200 для модифицированного BCH14 с использованием PBS-T, 1% BSA и 5 мкг/мл CWPS. Модифицированный BCH13 (сыворотка внутреннего контроля) и экспериментальные тестируемые образцы разбавляли в 1000, 5000 и 25000 раз PBS-T, 1% BSA и 5 мкг/мл CWPS, соответственно. Планшеты промывали 1X PBS-T перед добавлением эталонного стандарта, контрольной сыворотки и экспериментальных исследуемых сывороток. После инкубации при комнатной температуре в течение одного часа планшеты промывали PBS-T и добавляли вторичное сульфо-конъюгированное антикроличье антитело. Планшеты промывали PBS-T и добавляли 1X буфере считывания, и планшеты считывали с использованием MSD Meso QuickPlex SQ 120, модель № 1300.
[477] В этом исследовании в качестве контроля использовали сыворотку кроликов, иммунизированных Prevnar 13.
Результаты и заключение
[478] Результаты показаны на Фиг. 9-13. В целом, эквивалентные или более высокие ответы серотипспецифических полисахаридных антител наблюдали в группах, которые получали 24-валентные или 15-валентные композиции MAPS как на P1, так и на P2, по сравнению с группой Prevnar 13 (представлены пунктирной линией при соотношении GMT 1 на Фиг. 9-12). В целом, более высокие титры наблюдали в группах без адъюванта и с адъювантом AlPO4 по сравнению с группами с адъювантом p-Al(OH)3 для всех серотипов.
[479] На Фиг. 9-12 группы составов 24-валентных или 15-валентных MAPS сравнивали с группой Prevnar 13 (пунктирная линия при соотношении GMT, равном 1). Если соотношение GMT> 1, то титр антител к PS для групп составов MAPS выше. Если соотношение GMT <1, то титр антител к PS для групп составов MAPS ниже.
[480] На Фиг. 13 титр антител к PS репрезентативного отдельного серотипа S. pneumoniae (показан серотип 1) в группах составов 24-валентных или 15-валентных MAPS сравнивали с титром против соответствующего PS в группе Prevnar 13.
Исследование 2. Оценка титров серотипспецифических антител к PS после иммунизации лекарственным препаратом на основе 24-валентного MAPS в сравнении с PCV13
[481] Одно исследование фармакодинамики in vivo было выполнено для оценки профиля иммуногенности MAPS24 по сравнению с PCV13 при одной десятой дозы PCV13 для человека на кроликах. Оцениваемая исследуемая субстанция представляла собой MAPS24, составленное с адъювантом AlPO4. Исследуемая вакцина MAPS24, использованная в доклиническом фармакологическом исследовании, содержала 2,2 мкг каждого PS на дозу, что соответствует количеству каждого PS, обнаруженного в дозе PCV13 (за исключением 6B с 4,4 мкг в PCV13). MAPS24 и PCV13 разбавляли до одной десятой (0,22 мкг каждого PS, за исключением 6B с 0,44 мкг в PCV13) в буфере перед введением (0,5 мл/доза) кроликам. В целом, более высокий иммунный ответ наблюдали в группе MAPS24 по сравнению с группой PCV13 для большинства распространенных серотипов (1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F), как показано на Фиг. 14. Более того, устойчивый иммунный ответ наблюдали с группой MAPS24 для дополнительных серотипов (2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20B, 22F и 33F), как показано на Фиг. 15.
[482] Обратитесь к исследованию 1 выше для получения подробной информации.
Пример 6. Иммуногенность и защита от колонизации
Исследование 1. Иммуногенные ответы и защитный эффект 12V и 6V MAPS с иммуногенными комплексами на CP1
[483] Одно фармакодинамическое исследование проводили, чтобы увидеть, индуцируются ли ответы TH17 и защитный эффект против штамма пневмококков иммуногенными комплексами MAPS с CP1. В этом исследовании 12-валентная MAPS с CP1 (12V MAPS CP1; серотипы 1, 3, 4, 5, 6A, 7F, 9V, 14, 18C, 19A, 19F и 23F) и 6-валентная MAPS с CP1 (6V MAPS CP1; серотипы 1, 3, 4, 5, 14 и 23F). Также оценивали 6-валентную MAPS с альтернативным слитым белком (6V MAPS CP2a) и инактивированную цельноклеточную вакцину против S. pneumoniae (WCB). S. pneumoniae серотипа 6B использовали в исследованиях заражения мышей, поскольку серотип был исключен из иммуногенных комплексов MAPS.
[484] Ответы TH17 оценивали после трех иммунизаций. Образцы периферической крови брали через 2 недели после последней иммунизации для стимуляции ex vivo в присутствии антигенов в качестве стимулятора. Количество интерлейкина 17A (ИЛ-17A), секретируемого в среду, затем оценивали через 6 дней с помощью ИФА. Через 1-2 недели после забора крови мышам вводили 107 колониеобразующих единиц (КОЕ) пневмококков типа 6B (штамм 603). Носоглоточный смыв каждой мыши проводили через 10 дней после инфицирования и рассчитывали КОЕ пневмококков на основании роста на кровяном агаре.
[485] Иммунизация 12V MAPS CP1 и 6V MAPS CP1 индуцировала ответ TH17, который был обнаружен при стимуляции пневмококковым цельноклеточным антигеном (WCA), а также белками SP1500 и SP0785, как показано на Фиг. 16. Интересно, что, как показано на Фиг. 17, была продемонстрирована значительная защита от колонизации носоглотки S. pneumoniae серотипа 6B, серотипом, который не включен в компонент PS поливалентной MAPS с CP1, что позволяет предположить, что защита опосредуется через CP1-направленный иммунный ответ.
Исследование 2. Иммуногенные ответы и защитный эффект MAPS24 с иммуногенными комплексами на CP1
[486] Было проведено фармакодинамическое исследование, чтобы выяснить, индуцируются ли MAPS24 ответ Th17 к CP1 и защитный эффект против пневмококкового штамма. Мышей иммунизировали иллюстративным составом 24-валентной вакцины MAPS (MAPS24) с адъювантом (MAPS24: серотипы 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F), или иллюстративным составом 23-валентной вакцины MAPS (MAPS23) без серотипа контрольного заражения (S. pneumoniae серотипа 6B) с адъювантом (MAPS23: серотипы 1, 2, 3, 4, 5, 6A, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F). Мышей иммунизировали адъювантом только в качестве контроля.
[487] Ответы Th17 оценивали после двух иммунизаций. Спленоциты или периферическую кровь, собранные через 2 недели после последней иммунизации, подвергали стимуляции ex vivo в присутствии слитых белков CP1 SP1500 и SP0785 в качестве стимулятора. Количество интерлейкина 17A (ИЛ-17A), секретируемого в среду, оценивали через 3-6 дней после культивирования с помощью электрохемилюминесцентного иммуноанализа от Meso Scale (MSD). Статистически значимое увеличение ИЛ-17A было продемонстрировано для 24-валентной вакцины MAPS с адъювантом (например, пассивированным гидроксидом алюминия (p-AlOH) или фосфатом алюминия (AlPO4)) по сравнению с контрольной группой, иммунизированной только адъювантом (например, пассивированным гидроксидом алюминия) (Фиг. 18).
[488] Мышей, иммунизированных 23-валентной вакциной MAPS (без серотипа 6B) и адъювантным контролем, заражали 105 -107 колониеобразующими единицами (КОЕ) пневмококков серотипа 6B (штамм 603). Носоглоточный смыв каждой мыши проводили через 10 дней после инфицирования и рассчитывали КОЕ пневмококков на основании роста на кровяном агаре. Группа, иммунизированная 23-валентной вакциной MAPS и пассивированным гидроксидом алюминия (p-AlOH)), имела статистически значимое снижение колонизации носоглотки пневмококками, а группа, иммунизированная 23-валентной вакциной MAPS и фосфатом алюминия (AlPO4), продемонстрировала тенденцию к снижению колонизации носа пневмококками (Фиг. 19). Не желая быть связанными теориями, значительная защита от колонизации носоглотки S. pneumoniae серотипа 6B, полисахаридный компонент которого не включен в протестированную 23-валентную вакцину MAPS, указывает на то, что защита может быть опосредована иммунным ответом на белковый компонент CP1, или полисахаридные компоненты вакцины, обладающие перекрестной реактивностью со штаммами S. pneumoniae NVT, или с их комбинацией.
Пример 7. Антитела из сыворотки, полученной от животных, иммунизированных иллюстративным составом вакцины MAPS24, связываются с невакцинным типом S. pneumoniae
Способы
[489] Иллюстративные составы, содержащие MAPS24 и протокол иммунизации кроликов, использованные в этом примере, описаны в исследовании 1 примера 5. Новозеландских белых кроликов иммунизировали внутримышечно на 0-й и 14-й дни или иллюстративным составом 24-валентной вакцины MAPS24, или Prevnar 13, оба варианта с адъювантом фосфатом алюминия. Сыворотку собирали перед первой иммунизацией (P0) и через две недели после второй иммунизации (P2). Для оценки связывающей способности антител от MAPS24-иммунизированных кроликов к S. pneumoniae с серотипами с капсульным полисахаридом, не включенными в MAPS24 или Prevnar13 (невакцинные типы, NVT), использовали ИФА с цельноклеточным S. pneumoniae в качестве покрывающего антигена. При помощи такого иллюстративного анализа выявляют кроличий IgG, который связывается с цельноклеточными S. pneumoniae, нанесенными на планшет для ИФА, через поверхностные антигены, такие как белок или полисахарид. Для уменьшения связывания и сигнала от сыворотки неиммунизированных кроликов, планшет, покрытый S. pneumoniae, блокировали обезжиренным сухим молоком. Кроме того, кроличьи сыворотки предварительно инкубировали как обезжиренным сухим молоком, так и полисахаридом клеточной стенки S. pneumoniae для адсорбции любых полисахаридов клеточной стенки, специфических и любых неспецифических антител, которые могут давать сигнал в анализе. Сыворотки кроликов, иммунизированных MAPS24 (доза в 0,22 мкг на полисахарид) или Prevnar 13 (доза в 0,22 мкг на полисахарид, кроме 6B, доза 0,44 г), и соответствующие сыворотки перед иммунизацией были проанализированы на связывание с шестью различными серотипами S. pneumoniae с капсульным полисахаридом не включены ни в одну из вакцин.µµµ Титры связывающих все клетки IgG выражали в условных единицах/мл.
Результаты и выводы
[490] Как показано на Фиг. 20, статистически значимое увеличение между уровнями связывания IgG до иммунизации (P0) и после иммунизации (P2) для сывороток MAPS24 наблюдали для всех шести серотипов (p <0,01 для всех серотипов, двусторонний тест согласованных пар Уилкоксона). Статистически значимой разницы между уровнями связывания IgG для P0 и P2 для сывороток Prevnar 13 для четырех из шести проанализированных серотипов не было, и более низкая значимость, чем MAPS24 для двух серотипов.
[491] Были рассчитаны соотношения индукции (кратность изменения) титров P2 IgG по отношению к титрам P0 IgG для каждого образца сыворотки из обеих групп иммунизации, и соотношение индукции для средних геометрических титров, определенное для связывания антител с каждым цельноклеточным штаммом S. pneumoniae NVT. Как показано на Фиг. 21, соотношение индукции для всех шести серотипов был значительно выше для кроликов, иммунизированных MAPS24, чем для кроликов, иммунизированных Prevnar 13 (p <0,001 для пяти серотипов и p <0,01 для одного серотипа, двусторонний тест Манна-Уитни).
Пример 8. Опсонофагоцитарное уничтожение невакцинных типов S. pneumoniae: MAPS 24
Способы
[492] Иллюстративные составы, содержащие MAPS24, и протокол иммунизации кроликов, использованные в этом примере, описаны в исследовании 1 Примера 5. Новозеландских белых кроликов иммунизировали внутримышечно на 0-й и 14-й дни иллюстративным составом MAPS24 с адъювантом фосфатом алюминия. Сыворотку собирали перед первой иммунизацией (P0) и через две недели после второй иммунизации (P2).
[493] Для демонстрации присутствия функциональных антител против невакцинных типов (NVT) S. pneumoniae, полисахариды которых не включены в 24-валентную вакцину MAPS, был разработан модифицированный анализ опсонофагоцитирующей активности в концентрированной смеси (COPA) с последовательными стадиями инкубации. В таком иллюстративном анализе присутствие функциональных антител демонстрируется путем уничтожения штаммов S. pneumoniae NVT после инкубации с иммунными сыворотками. Вкратце, банк замороженных клеток S. pneumoniae оттаивали и ресуспендировали при 2 × 105 КОЕ/мл в буфере для анализа (забуференный физиологический раствор Хэнка с 10% инактивированной нагреванием FBS). В каждую лунку 96-луночного планшета добавляли 20 мкл инактивированной нагреванием кроличьей сыворотки, разведенной в буфере для анализа, а затем 10 мкл суспензии бактерий в буфере для анализа. Бактерии и кроличьи сыворотки инкубировали при комнатной температуре в течение 30 минут при встряхивании при 650 об/мин. В каждую лунку добавляли 10 мкл комплемента крольчат (Pel-Freeze Biologicals), в чистом виде или соответствующим образом разведенным в буфере для анализа, с последующей инкубацией при комнатной температуре в течение 30 минут при встряхивании при 650 об/мин. Дифференцированные клетки HL60 (ATCC) промывали буфером для анализа и ресуспендировали до 1×107 клеток/мл в буфере для анализа. В каждую лунку добавляли 40 мкл этой суспензии HL60 (200: 1, соотношение HL60 к бактериям) с последующей инкубацией при 37°C с 5% CO2 и встряхиванием при 650 об/мин в течение 1 часа. Каждый планшет переносили на лед и инкубировали в течение 20 минут. Содержимое каждой лунки разводили водой 1/5 и 1/25, и каждое разведение затем высевали на чашки Петри с 5% кровяным агаром. После инкубации в течение ночи при 37°C с 5% CO2 подсчитывали КОЕ для каждого образца и разведения, отбрасывая точки данных с количеством колоний более 250 КОЕ.
Результаты и выводы
[494] Сыворотки кроликов, иммунизированных MAPS24, анализировали в различных разведениях, например, в диапазоне от 1:2 до 1:54, по сравнению с подобранными сыворотками не получавших лечения кроликов, собранными до иммунизации (предиммунные сыворотки). Шесть различных штаммов S. pneumoniae NVT анализировали по отдельности (15A, 16F, 23A, 31, 35B и 35F). Колониеобразующие единицы (КОЕ) подсчитывали на чашках Петри с кровяным агаром. Уничтожающую активность выражали как процентное снижение КОЕ после инкубации с иммунными сыворотками по сравнению с инкубацией с подобранными предиммунными сыворотками, где процентное снижение определяется как [1 - (КОЕ/мл для иммунных сывороток/КОЕ/мл для предиммунных сывороток)] * 100. Не ограничиваясь теорией, в некоторых вариантах осуществления уничтожающая активность иммунных сывороток зависела как от клеток HL60, так и от активного комплемента. Как показано на Фиг. 22, снижение КОЕ для иммунных сывороток при различных разведениях по сравнению с подобранными предиммунными сыворотками наблюдали по меньшей мере для одного или более (например, 1, 2, 3, 4, 5 или 6) невакцинных серотипов. Например, снижение КОЕ для иммунных сывороток при разведении 1/18 или ниже по сравнению с подобранными предиммунными сыворотками наблюдали для всех шести невакцинных серотипов. Профили титрования для уничтожающей активности различаются в зависимости от серотипа бактерии. Не желая связывать себя теориями, в некоторых вариантах осуществления функциональные антитела против одного или более невакцинных серотипов (NVT) S. pneumoniae, генерируемые иммунизацией MAPS24, могут быть направлены на белковый компонент CP1 вакцины или на полисахаридные компоненты вакцины с перекрестной реактивностью к штаммам S. pneumoniae NVT или к их комбинации.
Пример 9. Опсонофагоцитарное уничтожение невакцинных типов S. pneumoniae: MAPS24 и Prevnar 13
Способы
[495] Иллюстративные составы, содержащие MAPS24, и протокол иммунизации кроликов, использованные в этом примере, описаны в исследовании 1 Примера 5. Новозеландских белых кроликов иммунизировали внутримышечно на 0-й и 14-й дни или иллюстративным составом MAPS24, или Prevnar 13, оба варианта с адъювантом фосфатом алюминия. Сыворотку собирали перед первой иммунизацией (P0) и через две недели после второй иммунизации (P2). Для демонстрации присутствия функциональных антител против NVT S. pneumoniae, полисахариды которых не включены в 24-валентную вакцину MAPS или Prevnar13, был проведен модифицированный анализ опсонофагоцитирующей активности в концентрированной смеси (COPA) с последовательными стадиями инкубации, как описано в Примере 8. В таком иллюстративном анализе присутствие функциональных антител демонстрируется путем уничтожения штаммов S. pneumoniae NVT после инкубации с иммунными сыворотками.
Результаты и выводы
[496] Сыворотки кроликов, иммунизированных или MAPS24, или Prevnar 13 анализировали в различных разведениях, например, в диапазоне от 1:2 до 1:54, по сравнению с подобранными сыворотками не получавших лечения кроликов, собранными до иммунизации (предиммунные сыворотки). Два разных штамма S. pneumoniae NVT (15A и 16F) анализировали по отдельности. Колониеобразующие единицы (КОЕ) подсчитывали на чашках Петри с кровяным агаром. Результаты выражали как процент выживаемости бактерий, инкубированных с иммунными сыворотками, по сравнению с инкубацией с подобранными предиммунными сыворотками.
[497] На Фиг. 23 показано, что NVT S. pneumoniae серотипа 16F, инкубированный с сывороткой от кроликов, иммунизированных MAPS24, продемонстрировал пониженную выживаемость по сравнению с бактериями, инкубированными с сывороткой от кроликов, иммунизированных Prevnar13. На панели А Фиг. 23 показано статистически значимое снижение выживаемости NVT S. pneumoniae серотипа 16F для трех из четырех протестированных разведений сывороток кроликов, иммунизированных MAPS24, по сравнению с предиммунными сыворотками. Напротив, на панели B Фиг. 23 показано, что сыворотка кроликов, иммунизированная Prevnar 13, не приводила к значительному снижению выживаемости бактерий при любом разведении.
[498] На Фиг. 24 показано, что NVT S. pneumoniae серотипа 15А, инкубированный с сывороткой от кроликов, иммунизированных MAPS24, продемонстрировал пониженную выживаемость по сравнению с бактериями, инкубированными с сывороткой от кроликов, иммунизированных Prevnar13. На панели А на Фиг. 24 показано статистически значимое снижение выживаемости NVT S. pneumoniae серотипа 15А для трех из четырех протестированных разведений сывороток кроликов, иммунизированных MAPS24, по сравнению с предиммунными сыворотками. Напротив, на панели B Фиг. 24 показано, что сыворотка кроликов, иммунизированная Prevnar 13, не приводила к значительному снижению выживаемости бактерий при любом разведении.
[499] Не желая связывать себя теориями, в некоторых вариантах осуществления функциональные антитела против одного или более невакцинных серотипов (NVT) S. pneumoniae, генерируемые иммунизацией MAPS24, могут быть направлены на белковый компонент CP1 вакцины или на полисахаридные компоненты вакцины с перекрестной реактивностью к штаммам S. pneumoniae NVT или к их комбинации.
Пример 10. Ингибирование опсонофагоцитарного уничтожения серотипа невакцинного типа S. pneumoniae с помощью CP1
[500] Примеры 8 и 9 демонстрируют присутствие функциональных антител путем опсонофагоцитарного уничтожения серотипа(-ов) невакцинного типа (NVT) S. pneumoniae с использованием иллюстративных составов MAPS (например, MAPS24). Для демонстрации специфичности функциональных антител против NVT S. pneumoniae, был разработан вариант ингибирования модифицированного анализа опсонофагоцитирующей активности в концентрированной смеси (iCOPA). В таком иллюстративном анализе присутствие функциональных антител демонстрируют путем уничтожения серотипов NVT S. pneumoniae после инкубации с иммунными сыворотками; специфичность этих функциональных антител оценивается путем предварительной инкубации иммунных сывороток со специфическим ингибирующим реагентом (например, очищенным белком, например, слитым белком CP1), который ингибирует связывание функциональных антител с антигеном-мишенью или конкурирует с ним, и последующей инкубацией с серотипами NVT S. pneumoniae, чтобы определить, было ли подавлено уничтожение. Сыворотки кроликов, иммунизированных MAPS24, анализировали в различных разведениях, например, в диапазоне от 1:2 до 1:54, по сравнению с подобранными сыворотками не получавших лечения кроликов, собранными до иммунизации (предиммунные сыворотки). Уничтожение штамма 16F S. pneumoniae NVT оценивали с использованием иммунных сывороток с предварительной инкубацией с очищенным компонентом CP1 MAPS24 и без него. Колониеобразующие единицы (КОЕ) подсчитывали на чашках Петри с кровяным агаром. Уничтожающую активность выражали как процентное снижение КОЕ после инкубации с иммунными сыворотками по сравнению с инкубацией с подобранными предиммунными сыворотками, где процентное снижение определяется как [1 - (КОЕ/мл для иммунных сывороток/КОЕ/мл для предиммунных сывороток)] * 100. Как показано на Фиг. 25, присутствие функциональных антител к штамму 16F S. pneumoniae NVT в иммунных сыворотках в отсутствие специфического ингибирующего реагента проявляется в процентах уничтожающей активности иммунных сывороток по сравнению с предиммунными сыворотками. Предварительная инкубация иммунных сывороток с очищенным белком CP1 в условиях, благоприятствующих конкурентному связыванию функциональных антител с белком CP1, приводила к более низкому проценту уничтожающей активности. Не желая быть связанными теорией, этот результат указывает на то, что функциональные антитела против серотипа невакцинного типа (например, серотипа 16F) S. pneumoniae, генерируемые иммунизацией MAPS24, могут быть направлены на белковый компонент CP1 вакцины.
Пример 11. Опсонофагоцитарное уничтожение невакцинного серотипа S. pneumoniae: полипептиды SP1500 и SP0785
[501] Этот пример демонстрирует присутствие функциональных антител против типичного NVT S. pneumoniae в сыворотках, собранных у животных, иммунизированных полипептидами SP1500 или SP0785 (иммунные сыворотки).
Способы
[502] Иллюстративные протоколы иммунизации кроликов, использованные в данном Примере, описаны в исследовании 1 из Примера 5. Новозеландских белых кроликов (n=3) иммунизировали внутримышечно по отдельности на 0-й, 14-й и 28-й дни 100 мкг полипептидов SP1500 или SP0785 с адъювантом фосфатом алюминия.µ Сыворотку собирали перед первой иммунизацией (P0) и через две недели после третьей иммунизации (P3). Сыворотки, собранные у 3 кроликов в каждый момент времени, объединяли, чтобы получить пул, и хранили при -80 °C. Для демонстрации наличия функциональных антител против штамма 16F S. pneumoniae NVT, полисахариды которых не включены в составы, содержащие SP1500 или SP0785, был проведен модифицированный анализ опсонофагоцитирующей активности в концентрированной смеси (COPA) с последовательными стадиями инкубации, как описано в Примере 8. В таком иллюстративном анализе присутствие функциональных антител демонстрируется путем уничтожения штамма 16F S. pneumoniae NVT после инкубации с иммунными сыворотками.
[503] Результаты. Сыворотки кроликов, иммунизированных или полипептиды SP1500, или полипептиды SP0785 анализировали в различных разведениях, например, в диапазоне от 1:2 до 1:54, по сравнению с подобранными сыворотками не получавших лечения кроликов, собранными до иммунизации (предиммунные сыворотки). Колониеобразующие единицы (КОЕ) подсчитывали на чашках Петри с кровяным агаром. Уничтожающую активность выражали как процентное снижение КОЕ после инкубации с иммунными сыворотками по сравнению с инкубацией с подобранными предиммунными сыворотками, где процентное снижение определяется как [1 - (КОЕ/мл для иммунных сывороток/КОЕ/мл для предиммунных сывороток)] * 100.
[504] На Фиг. 26 показано, что инкубация с иммунными сыворотками от кроликов, отдельно иммунизированных полипептидами SP1500 и SP0785, приводила к уничтожающей активности против NVT S. pneumoniae серотипа 16F для трех из четырех тестируемых разведений по сравнению с предиммунными сыворотками. Не ограничиваясь теорией, этот результат указывает на то, что функциональные антитела против одного или более невакцинных серотипов (NVT) S. pneumoniae могут быть получены иммунизацией полипептидами SP1500 или SP0785.
[505] Доклиническое исследование демонстрирует, что поливалентные вакцины MAPS, описанные в настоящем документе (например, вакцины MAPS24, MAPS15 и MAPS9), обладают высокой иммуногенностью в моделях на животных и вызывают серотипспецифические ответы. MAPS24 обеспечивает клинически значимые преимущества по сравнению с существующей вакциной PCV13, по меньшей мере, за счет значительного дополнительного охвата целевых популяций с помощью дополнительных 11 серотипов. Кроме того, MAPS24 генерировал функциональные антитела против одного или более невакцинных серотипов. Кроме того, вакцина MAPS24 упрощает нынешнюю сложную схему иммунизации против пневмококков у людей с высоким риском и у пожилых людей, обеспечивая защиту от всех включенных серотипов в одной дозе вместо двух доз двух разных вакцин, вводимых в соответствии со сложными схемами.
Перечень последовательностей
[506] SEQ ID NO:1, белок ризавидин, полноразмерный [аминокислоты 1-179]:
MIITSLYATFGTIADGRRTSGGKTMIRTNAVAALVFAVATSALAFDASNFKDFSSIASASSSWQNQSGSTMIIQVDSFGNVSGQYVNRAQGTGCQNSPYPLTGRVNGTFIAFSVGWNNSTENCNSATGWTGYAQVNGNNTEIVTSWNLAYEGGSGPAIEQGQDTFQYVPTTENKSLLKD
[507] SEQ ID NO:2, усеченный белок ризавидин, обозначаемый Rhavi [аминокислоты 45-179]:
FDASNFKDFSSIASASSSWQNQSGSTMIIQVDSFGNVSGQYVNRAQGTGCQNSPYPLTGRVNGTFIAFSVGWNNSTENCNSATGWTGYAQVNGNNTEIVTSWNLAYEGGSGPAIEQGQDTFQYVPTTENKSLLKD
[508] SEQ ID NO:3, линкерная последовательность [7 аминокислот]:
GGGGSSS
[509] SEQ ID NO:4, белок SP0785 без сигнальной последовательности и трансмембранного домена [аминокислот 33-399]:
Примечание: одно несоответствие T394A с последовательностями SP0785 NCBI ABJ54007.1 и YP816180
FRQPSQTALKDEPTHLVVAKEGSVASSVLLSGTVTAKNEQYVYFDASKGDLDEILVSVGDKVSEGQALVKYSSSEAQAAYDSASRAVARADRHINELNQARNEAASAPAPQLPAPVGGEDATVQSPTPVAGNSVASIDAQLGDARDARADAAAQLSKAQSQLDATTVLSTLEGTVVEVNSNVSKSPTGASQVMVHIVSNENLQVKGELSEYNLANLSVGQEVSFTSKVYPDKKWTGKLSYISDYPKNNGEAASPAAGNNTGSKYPYTIDVTGEVGDLKQGFSVNIEVKSKTKAILVPVSSLVMDDSKNYVWIVDEQQKAKKVEVSLGNADAENQEITSGLTNGAKVISNPTSSLEEGKEVKADEATN
[510] SEQ ID NO:5, белок SP1500 без сигнальной последовательности [аминокислоты 27-278]:
TSGDNWSKYQSNKSITIGFDSTFVPMGFAQKDGSYAGFDIDLATAVFEKYGITVNWQPIDWDLKEAELTKGTIDLIWNGYSATDERREKVAFSNSYMKNEQVLVTKKSSGITTAKDMTGKTLGAQAGSSGYADFEANPEILKNIVANKEANQYQTFNEALIDLKNDRIDGLLIDRVYANYYLEAEGVLNDYNVFTVGLETEAFAVGARKEDTNLVKKINEAFSSLYKDGKFQEISQKWFGEDVATKEVKEGQ
[511] SEQ ID NO:6, слитый белок CP1:
MFDASNFKDFSSIASASSSWQNQSGSTMIIQVDSFGNVSGQYVNRAQGTGCQNSPYP LTGRVNGTFIAFSVGWNNSTENCNSATGWTGYAQVNGNNTEIVTSWNLAYEGGSGP AIEQGQDTFQYVPTTENKSLLKDGGGGSSSTSGDNWSKYQSNKSITIGFDSTFVPMGF AQKDGSYAGFDIDLATAVFEKYGITVNWQPIDWDLKEAELTKGTIDLIWNGYSATDE RREKVAFSNSYMKNEQVLVTKKSSGITTAKDMTGKTLGAQAGSSGYADFEANPEILK NIVANKEANQYQTFNEALIDLKNDRIDGLLIDRVYANYYLEAEGVLNDYNVFTVGLE TEAFAVGARKEDTNLVKKINEAFSSLYKDGKFQEISQKWFGEDVATKEVKEGQAAAF RQPSQTALKDEPTHLVVAKEGSVASSVLLSGTVTAKNEQYVYFDASKGDLDEILVSV GDKVSEGQALVKYSSSEAQAAYDSASRAVARADRHINELNQARNEAASAPAPQLPAP VGGEDATVQSPTPVAGNSVASIDAQLGDARDARADAAAQLSKAQSQLDATTVLSTLE GTVVEVNSNVSKSPTGASQVMVHIVSNENLQVKGELSEYNLANLSVGQEVSFTSKV YPDKKWTGKLSYISDYPKNNGEAASPAAGNNTGSKYPYTIDVTGEVGDLKQGFSVN IEVKSKTKAILVPVSSLVMDDSKNYVWIVDEQQKAKKVEVSLGNADAENQEITSGLT NGAKVISNPTSSLEEGKEVKADEATN
[512] SEQ ID NO:7, ген SP0785, кодирующий белок SP0785, лишенный сигнальной последовательности [аминокислоты 33-399]:
TTTAGACAACCTTCTCAGACTGCTCTAAAAGATGAGCCTACTCATCTTGTTGTTGCCAAGGAAGGAAGCGTGGCCTCCTCTGTTTTATTGTCAGGGACAGTAACAGCAAAAAATGAACAATATGTTTATTTTGATGCTAGTAAGGGTGATTTAGATGAAATCCTTGTTTCTGTGGGCGATAAGGTCAGCGAAGGGCAGGCTTTAGTCAAGTACAGTAGTTCAGAAGCGCAGGCGGCCTATGATTCAGCTAGTCGAGCAGTAGCTAGGGCAGATCGTCATATCAATGAACTCAATCAAGCACGAAATGAAGCCGCTTCAGCTCCGGCTCCACAGTTACCAGCGCCAGTAGGAGGAGAAGATGCAACGGTGCAAAGCCCAACTCCAGTGGCTGGAAATTCTGTTGCTTCTATTGACGCTCAATTGGGTGATGCCCGTGATGCGCGTGCAGATGCTGCGGCGCAATTAAGCAAGGCTCAAAGTCAATTGGATGCAACAACTGTTCTCAGTACCCTAGAGGGAACTGTGGTCGAAGTCAATAGCAATGTTTCTAAATCTCCAACAGGGGCGAGTCAAGTTATGGTTCATATTGTCAGCAATGAAAATTTACAAGTCAAGGGAGAATTGTCTGAGTACAATCTAGCCAACCTTTCTGTAGGTCAAGAAGTAAGCTTTACTTCTAAAGTGTATCCTGATAAAAAATGGACTGGGAAATTAAGCTATATTTCTGACTATCCTAAAAACAATGGTGAAGCAGCTAGTCCAGCAGCCGGGAATAATACAGGTTCTAAATACCCTTATACTATTGATGTGACAGGCGAGGTTGGTGATTTGAAACAAGGTTTTTCTGTCAACATTGAGGTTAAAAGCAAAACTAAGGCTATTCTTGTTCCTGTTAGCAGTCTAGTAATGGATGATAGTAAAAATTATGTCTGGATTGTGGATGAACAACAAAAGGCTAAAAAAGTTGAGGTTTCATTGGGAAATGCTGACGCAGAAAATCAAGAAATCACTTCTGGTTTAACGAACGGTGCTAAGGTCATCAGTAATCCAACATCTTCCTTGGAAGAAGGAAAAGAGGTGAAGGCTGATGAAGCAACTAAT
[513] SEQ ID NO:8, ген SP1500, кодирующий белок SP1500, лишенный сигнальной последовательности [аминокислоты 27-278]:
ACTAGTGGAGATAATTGGTCAAAGTACCAGTCTAACAAGTCTATTACTATTGGATTTGATAGTACTTTTGTTCCAATGGGATTTGCTCAGAAAGATGGTTCTTATGCAGGATTTGATATTGATTTAGCTACAGCTGTTTTTGAAAAATACGGAATCACGGTAAATTGGCAACCGATTGATTGGGATTTGAAAGAAGCTGAATTGACAAAAGGAACGATTGATCTGATTTGGAATGGCTATTCCGCTACAGACGAACGCCGTGAAAAGGTGGCTTTCAGTAACTCATATATGAAGAATGAGCAGGTATTGGTTACGAAGAAATCATCTGGTATCACGACTGCAAAGGATATGACTGGAAAGACATTAGGAGCTCAAGCTGGTTCATCTGGTTATGCGGACTTTGAAGCAAATCCAGAAATTTTGAAGAATATTGTCGCTAATAAGGAAGCGAATCAATACCAAACCTTTAATGAAGCCTTGATTGATTTGAAAAACGATCGAATTGATGGTCTATTGATTGACCGTGTCTATGCAAACTATTATTTAGAAGCAGAAGGTGTTTTAAACGATTATAATGTCTTTACAGTTGGACTAGAAACAGAAGCTTTTGCGGTTGGAGCCCGTAAGGAAGATACAAACTTGGTTAAGAAGATAAATGAAGCTTTTTCTAGTCTTTACAAGGACGGCAAGTTCCAAGAAATCAGCCAAAAATGGTTTGGAGAAGATGTAGCAACCAAAGAAGTAAAAGAAGGACAG
[514] SEQ ID NO:9, кодон-оптимизированная последовательность, кодирующая слитый белок CP1 [нуклеиновая кислота]:
ATGTTCGACGCATCCAACTTTAAAGACTTTAGCAGCATCGCGTCCGCAAGCTCTAGCTGGCAGAATCAATCTGGTAGCACCATGATTATCCAAGTGGACAGCTTTGGTAACGTCAGCGGTCAATATGTTAATCGTGCACAGGGTACGGGTTGTCAGAATTCTCCGTACCCGCTGACCGGTCGTGTTAACGGCACGTTCATCGCTTTCAGCGTCGGTTGGAACAATTCTACTGAAAATTGCAACAGCGCGACCGGTTGGACGGGCTATGCACAAGTGAATGGCAATAACACCGAAATCGTCACGTCCTGGAATCTGGCGTATGAGGGTGGCAGCGGTCCGGCTATTGAACAGGGCCAGGATACCTTCCAATACGTCCCTACGACCGAGAATAAGTCCCTTCTGAAAGACGGCGGTGGCGGTTCGAGCTCGACCAGCGGCGACAATTGGTCCAAATACCAGAGCAACAAGAGCATCACGATCGGCTTCGACAGCACTTTTGTGCCGATGGGTTTCGCGCAAAAAGACGGTAGCTACGCGGGTTTCGATATTGACCTGGCGACCGCTGTCTTTGAGAAATACGGCATTACGGTTAATTGGCAGCCGATTGATTGGGACCTGAAAGAGGCCGAACTCACCAAAGGCACCATCGACCTGATCTGGAATGGTTACTCCGCAACCGATGAGCGTCGCGAAAAAGTTGCCTTCAGCAACAGCTATATGAAGAATGAACAAGTGTTGGTAACCAAGAAATCTAGCGGCATTACGACCGCGAAAGACATGACCGGTAAGACGCTGGGTGCGCAGGCCGGTAGCTCTGGCTATGCGGATTTCGAGGCGAATCCTGAGATTCTGAAAAACATCGTTGCGAATAAAGAGGCGAACCAGTACCAGACCTTTAACGAAGCACTGATCGACCTGAAAAACGATCGCATTGACGGTCTGCTGATCGATCGTGTGTACGCGAACTATTATCTGGAAGCCGAGGGCGTTCTGAACGATTATAATGTTTTTACCGTGGGTCTGGAGACTGAGGCATTCGCGGTTGGTGCGCGCAAGGAAGATACCAACCTGGTTAAAAAGATTAATGAGGCATTTAGCTCACTGTACAAGGACGGCAAGTTCCAAGAAATTAGCCAGAAGTGGTTCGGTGAAGATGTTGCGACGAAAGAGGTTAAAGAGGGCCAAGCGGCCGCATTTCGCCAACCGAGCCAGACTGCGTTGAAAGATGAGCCGACCCATCTGGTTGTTGCGAAAGAGGGCAGCGTGGCATCGAGCGTGCTGCTGAGCGGTACGGTTACTGCCAAAAACGAACAATACGTGTACTTCGATGCTAGCAAGGGTGATCTGGATGAAATTCTGGTGAGCGTGGGTGACAAAGTTAGCGAAGGCCAGGCACTGGTGAAGTATTCATCCTCCGAGGCACAGGCAGCGTACGACAGCGCAAGCCGCGCAGTGGCGCGTGCCGACCGTCACATTAACGAATTGAACCAAGCGCGTAACGAGGCCGCAAGCGCGCCAGCACCGCAGCTGCCGGCTCCGGTGGGTGGCGAAGATGCGACGGTGCAGAGCCCGACCCCGGTTGCGGGTAATTCGGTCGCCAGCATCGATGCGCAGCTGGGTGACGCGCGTGATGCCCGTGCGGATGCGGCTGCTCAACTGAGCAAGGCTCAGAGCCAACTGGACGCGACGACGGTGCTGAGCACCTTGGAGGGTACCGTTGTCGAAGTCAACAGCAATGTGAGCAAGAGCCCAACGGGTGCGAGCCAGGTTATGGTCCACATTGTGAGCAATGAAAACTTACAGGTCAAGGGTGAGCTGAGCGAGTATAACCTGGCGAATCTGAGCGTTGGTCAAGAGGTCAGCTTTACCAGCAAGGTCTACCCGGATAAGAAATGGACCGGCAAGTTGAGCTACATCAGCGACTACCCGAAGAACAATGGCGAGGCAGCCTCCCCGGCAGCCGGCAACAATACCGGCTCTAAGTATCCGTACACCATCGACGTAACCGGTGAGGTCGGCGACCTGAAACAGGGTTTTAGCGTGAATATCGAAGTGAAGTCCAAGACCAAGGCAATTTTGGTTCCGGTTAGCTCCCTGGTGATGGACGATAGCAAGAATTATGTGTGGATTGTCGACGAGCAACAGAAAGCGAAAAAAGTTGAAGTGAGCCTGGGCAATGCTGATGCCGAGAACCAAGAAATCACGTCTGGTCTGACCAACGGTGCGAAAGTTATTAGCAACCCGACCAGCAGCCTGGAAGAGGGTAAAGAGGTCAAAGCCGACGAAGCTACGAAC
[515] SEQ ID NO:10, белок SP0785, полноразмерный [аминокислоты 1-399], штамм TIGR4:
MKKKNGKAKKWQLYAAIGAASVVVLGAGGILLFRQPSQTALKDEPTHLVV
AKEGSVASSVLLSGTVTAKNEQYVYFDASKGDLDEILVSVGDKVSEGQAL
VKYSSSEAQAAYDSASRAVARADRHINELNQARNEAASAPAPQLPAPVGG
EDATVQSPTPVAGNSVASIDAQLGDARDARADAAAQLSKAQSQLDATTVL
STLEGTVVEVNSNVSKSPTGASQVMVHIVSNENLQVKGELSEYNLANLSV
GQEVSFTSKVYPDKKWTGKLSYISDYPKNNGEAASPAAGNNTGSKYPYTI
DVTGEVGDLKQGFSVNIEVKSKTKAILVPVSSLVMDDSKNYVWIVDEQQK
AKKVEVSLGNADAENQEITSGLTNGAKVISNPTSSLEEGKEVKADEATN
[516] SEQ ID NO:11, ген SP0785, кодирующий белок SP0785, полноразмерный [аминокислоты 1-399], штамм TIGR4: ATGAAGAAAAAGAATGGTAAAGCTAAAAAGTGGCAACTGTATGCAGCAAT
CGGTGCTGCGAGTGTAGTTGTATTGGGTGCTGGGGGGATTTTACTCTTTA
GACAACCTTCTCAGACTGCTCTAAAAGATGAGCCTACTCATCTTGTTGTT
GCCAAGGAAGGAAGCGTGGCCTCCTCTGTTTTATTGTCAGGGACAGTAAC
AGCAAAAAATGAACAATATGTTTATTTTGATGCTAGTAAGGGTGATTTAG
ATGAAATCCTTGTTTCTGTGGGCGATAAGGTCAGCGAAGGGCAGGCTTTA
GTCAAGTACAGTAGTTCAGAAGCGCAGGCGGCCTATGATTCAGCTAGTCG
AGCAGTAGCTAGGGCAGATCGTCATATCAATGAACTCAATCAAGCACGAA
ATGAAGCCGCTTCAGCTCCGGCTCCACAGTTACCAGCGCCAGTAGGAGGA
GAAGATGCAACGGTGCAAAGCCCAACTCCAGTGGCTGGAAATTCTGTTGC
TTCTATTGACGCTCAATTGGGTGATGCCCGTGATGCGCGTGCAGATGCTG
CGGCGCAATTAAGCAAGGCTCAAAGTCAATTGGATGCAACAACTGTTCTC
AGTACCCTAGAGGGAACTGTGGTCGAAGTCAATAGCAATGTTTCTAAATC
TCCAACAGGGGCGAGTCAAGTTATGGTTCATATTGTCAGCAATGAAAATT
TACAAGTCAAGGGAGAATTGTCTGAGTACAATCTAGCCAACCTTTCTGTA
GGTCAAGAAGTAAGCTTTACTTCTAAAGTGTATCCTGATAAAAAATGGAC
TGGGAAATTAAGCTATATTTCTGACTATCCTAAAAACAATGGTGAAGCAG
CTAGTCCAGCAGCCGGGAATAATACAGGTTCTAAATACCCTTATACTATT
GATGTGACAGGCGAGGTTGGTGATTTGAAACAAGGTTTTTCTGTCAACAT
TGAGGTTAAAAGCAAAACTAAGGCTATTCTTGTTCCTGTTAGCAGTCTAG
TAATGGATGATAGTAAAAATTATGTCTGGATTGTGGATGAACAACAAAAG
GCTAAAAAAGTTGAGGTTTCATTGGGAAATGCTGACGCAGAAAATCAAGA
AATCACTTCTGGTTTAACGAACGGTGCTAAGGTCATCAGTAATCCAACAT
CTTCCTTGGAAGAAGGAAAAGAGGTGAAGGCTGATGAAGCAACTAAT
[517] SEQ ID NO:12, белок SP1500, полноразмерный [аминокислоты 1-278], штамм TIGR4:
MKKWMLVLVSLMTALFLVACGKNSSETSGDNWSKYQSNKSITIGFDSTFV
PMGFAQKDGSYAGFDIDLATAVFEKYGITVNWQPIDWDLKEAELTKGTID
LIWNGYSATDERREKVAFSNSYMKNEQVLVTKKSSGITTAKDMTGKTLGA
QAGSSGYADFEANPEILKNIVANKEANQYQTFNEALIDLKNDRIDGLLID
RVYANYYLEAEGVLNDYNVFTVGLETEAFAVGARKEDTNLVKKINEAFSS
LYKDGKFQEISQKWFGEDVATKEVKEGQ
[518] SEQ ID NO:13, ген SP1500, кодирующий белок SP1500, полноразмерный [аминокислоты 1-278], штамм TIGR4:
ATGAAAAAATGGATGCTTGTATTAGTCAGTCTGATGACTGCTTTGTTCTT
AGTAGCTTGTGGGAAAAATTCTAGCGAAACTAGTGGAGATAATTGGTCAA
AGTACCAGTCTAACAAGTCTATTACTATTGGATTTGATAGTACTTTTGTT
CCAATGGGATTTGCTCAGAAAGATGGTTCTTATGCAGGATTTGATATTGA
TTTAGCTACAGCTGTTTTTGAAAAATACGGAATCACGGTAAATTGGCAAC
CGATTGATTGGGATTTGAAAGAAGCTGAATTGACAAAAGGAACGATTGAT
CTGATTTGGAATGGCTATTCCGCTACAGACGAACGCCGTGAAAAGGTGGC
TTTCAGTAACTCATATATGAAGAATGAGCAGGTATTGGTTACGAAGAAAT
CATCTGGTATCACGACTGCAAAGGATATGACTGGAAAGACATTAGGAGCT
CAAGCTGGTTCATCTGGTTATGCGGACTTTGAAGCAAATCCAGAAATTTT
GAAGAATATTGTCGCTAATAAGGAAGCGAATCAATACCAAACCTTTAATG
AAGCCTTGATTGATTTGAAAAACGATCGAATTGATGGTCTATTGATTGAC
CGTGTCTATGCAAACTATTATTTAGAAGCAGAAGGTGTTTTAAACGATTA
TAATGTCTTTACAGTTGGACTAGAAACAGAAGCTTTTGCGGTTGGAGCCC
GTAAGGAAGATACAAACTTGGTTAAGAAGATAAATGAAGCTTTTTCTAGT
CTTTACAAGGACGGCAAGTTCCAAGAAATCAGCCAAAAATGGTTTGGAGA
AGATGTAGCAACCAAAGAAGTAAAAGAAGGACAG
Ссылки
Anttila M, Eskola J, Ahman H, Käyhty H. Avidity of IgG for Streptococcus pneumoniae type 6B and 23F polysaccharides in infants primed with pneumococcal conjugates and boosted with polysaccharide or conjugate vaccines. J Infect Dis. 1998 Jun;177(6):1614-21.
Buller HR, Halperin J, Hankey GJ, Pillion G, Prins MH, Raskob GE. Comparison of idrabiotaparinux with vitamin K antagonists for prevention of thromboembolism in patients with atrial fibrillation: the Borsealis-Atrial Fibrillation study. J Throb Haemost. 2014;12:824-30.
[CDC] Centers for Disease Control and Prevention. Preventing pneumococcal disease among infants and young children. Morbidity and Mortality Weekly Report. 2000;49:1-55.
[CDC] Centers for Disease Control and Prevention. Prevention of pneumococcal disease among infants and children - use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine. Morbidity and Mortality Weekly Report. 2010;59:1-24.
Chase (1967). Perinatal and infant mortality in the United States and six West European countries. Am J Public Health Nations Health. 1967 Oct;57(10):1735-48.
Concepcion NF, Frasch CE. Pneumococcal type 22f polysaccharide absorption improves the specificity of a pneumococcal-polysaccharide enzyme-linked immunosorbent assay. Clin Diagn Lab Immunol. 2001 Mar;8(2):266-72.
Douce et al. Mutants of Escherichia coli heat-labile toxin lacking ADP-ribosyltransferase activity act as non-toxic, mucosal adjuvants. PNAS Vol. 92, pp. 1644-1648, February 1995.
Douce et al. Genetically detoxified mutants of heat-labile toxin from Escherichia coli are able to act as oral adjuvants” Infect Immun. 1999 Sep;67(9):4400-6)
Evans JT et al. Enhancement of antigen-specific immunity via the TLR-4 ligands MPL adjuvant and Ribi.529. Expert Rev Vaccines 2003 Apr;2(2):219-29.
Geno KA, Gilbert GL, Song JY, Skovsted IC, Klugman KP, Jones C et al. Pneumococcal Capsules and their types: past, present, and future. Clin Microbiol Rev 2015 Jul;28(3):871-899.
Giuliani MM et al. Mucosal adjuvanticity and immunogenicity of LTR72, a novel mutant of Escherichia coli heat-labile enterotoxin with partial knockout of ADP-ribosyltransferase activity. J Exp Med. 1998 Apr 6;187(7):1123-32.
Gruber MF, Pratt D, Haase M. Licensing of pneumococcal conjugate vaccines for children and adults: Regulatory perspective from the European Medicines Agency and the U.S. Food and Drug Administration. In: Siber GR, Klugman KP, Mäkelä PH, eds. Pneumococcal Vaccines: The Impact of Conjugate Vaccine. Washington, DC: ASM Press; 2008;183-96.
Helppolainen SH, Nurminen KP, Määttä JA, Halling KK, Slotte JP, Huhtala T, et al. Rhizavidin from Rhizobium etli: the first natural dimer in the avidin protein family. Biochem J. 2007;405:397- 405.
Holliger P, Prospero T, Winter G. "Diabodies": small bivalent and bispecific antibody fragments. Proc Natl Acad Sci U S A. 1993 Jul 15;90(14):6444-8.
Ishizaka ST et al. “E6020: a synthetic Toll-like receptor 4 agonist as a vaccine adjuvant.” Expert Rev. Vaccines. 2007 Oct; 6(5):773-84.
Kaufmann F, Lund E, Eddy B. Proposal for a change in the nomenclature of Diplococcus pneumoniae and a comparison of the Danish and American type designations. Intl Bulletin of Bacterial Nomenclature and Taxonomy 1960 Jan; 10(1):31-40.
Kim KH, Yu J, Nahm MH. Efficiency of a pneumococcal opsonophagocytic killing assay improved by multiplexing and by coloring colonies. Clin Diagn Lab Immunol. 2003 Jul; 10(4):616-21.
Lazzeri E, Pauwels EK, Erba PA, Volterrani D, Manca M, Bodei L, et al. Clinical feasibility of two- step streptavidin/111In-biotin scintigraphy in patients with suspected vertebral osteomyelitis. Eur J Nucl Med Mol Imaging. 2004;31:1505-11.
Kojima K, Ishizaka A, Oshika E, Taguchi Y, Tomizawa K, et al. Quantitation of IgG subclass antibodies to pneumococcal capsular polysaccharides by ELISA, using Pneumovax-specific antibodies as a reference. Tohoku J Exp Med. 1990 Jul;161(3):209-15.
Koskela M, Leinonen M. Comparison of ELISA and RIA for measurement of pneumococcal antibodies before and after vaccination with 14-valent pneumococcal capsular polysaccharide vaccine. J Clin Pathol. 1981 Jan;34(1):93-8.
Martin, EW, Ed. Remington’s Pharmaceutical Sciences. 15th ed. Easton, PA: Mack Publishing Company, 1975.
Martinez JE, Romero-Steiner S, Pilishvili T, Barnard S, Schinsky J, et al. A flow cytometric opsonophagocytic assay for measurement of functional antibodies elicited after vaccination with the 23-valent pneumococcal polysaccharide vaccine. Clin Diagn Lab Immunol. 1999 Jul;6(4):581-6.
Meyers and Miller. CABIOS, 1989, 4:11-17.
Munro CS, Stanley PJ, Cole PJ. Assessment of biological activity of immunoglobulin preparations by using opsonized micro-organisms to stimulate neutrophil chemiluminescence. Clin Exp Immunol. 1985 Jul;61(1):183-8.
Ojo-Amaize EA, Church JA, Barka NE, Agopian MS, Peter JB. A rapid and sensitive chemiluminescence assay for evaluation of functional opsonic activity of Haemophilus influenzae type b-specific antibodies. Clin Diagn Lab Immunol. 1995 May;2(3):286-90
Paty I, Trellu M, Destors JM, Cortez P, Boelle E, Sanderink G. Reversibility of the anti-FXa activity of idrabiotaparinux (biotinylated idraparinux) by intravenous avidin infusion. J Thromb Haemost. 2010;8:722-9.
PNEUMOVAX® 23 (prescribing information). Whitehouse Station, NJ: Merck & Co.; May 2015.
PREVNAR 13® (prescribing information). New York, NY: Pfizer; August 2017.
Poljak RJ. Production and structure of diabodies. Structure. 1994 Dec 15;2(12):1121-3.
Powell MF and Newman MJ, Eds. Vaccine Design: The Subunit and Adjuvant Approach. New York, NY: Plenum Press, 1995.
Richter SS, Diekema DJ, Heilmann KP, Dohrn CL, Riahi F, Doern GV. Changes in pneumococcal serotypes and antimicrobial resistance after introduction of the 13 valent conjugate vaccine in the United States. Antimicrob Agents Chemother. 2014;58:6484-9.
Romero-Steiner S, Libutti D, Pais LB, Dykes J, Anderson P, et al. Standardization of an opsonophagocytic assay for the measurement of functional antibody activity against Streptococcus pneumoniae using differentiated HL-60 cells. Clin Diagn Lab Immunol. 1997 Jul;4(4):415-22.
Romero-Steiner S, Holder PF, Gomez de Leon P, Spear W, Hennessy TW, et al. Avidity determinations for Haemophilus influenzae Type b anti-polyribosylribitol phosphate antibodies. Clin Diagn Lab Immunol. 2005 Sep;12(9):1029-35.
Saeland E, Vidarsson G, Jonsdottir I. Pneumococcal pneumonia and bacteremia model in mice for the analysis of protective antibodies. Microb Pathog. 2000 Aug;29(2):81-91.
Singh et al. Curr. HIV Res. 1:309-20, 2003.
Stack AM, Malley R, Thompson CM, Kobzik L, Siber GR, et al. Minimum protective serum concentrations of pneumococcal anti-capsular antibodies in infant rats. J Infect Dis. 1998 Apr;177(4):986-90.
Williams et al., Innate imprinting by the modified heat-labile toxin of Escherichia coli (LTK63) provides generic protection against lung infectious disease. The Journal of Immunology, 2004 173:7435-7443.
Wu W, Huang J, Duan B, Traficante DC, Hong H, et al. TH17-stimulating protein vaccines confer protection against Pseudomonas aeruginosa pneumonia. Am J Respir Crit Care Med. 2012 Sep 1;186(5):420-7.
Zhang F, Lu YJ, Malley R. Multiple antigen-presenting system (MAPS) to induce comprehensive B- and T-cell immunity. Proc Natl Acad Sci U S A. 2013;110:13564-9.
Эквиваленты
[519] Специалистам в данной области техники станет понятно или они смогут установить, используя не более чем рутинные эксперименты, существование многочисленных эквивалентов конкретных вариантов осуществления изобретения, описанных в данном документе. Объем настоящего изобретения не ограничивается приведенным выше описанием, а скорее соответствует изложенному в следующей формуле изобретения:
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> AFFINIVAX, INC.
<120> ПОЛИВАЛЕНТНЫЕ АНТИПНЕВМОКОККОВЫЕ ВАКЦИНЫ
<130> 2011588-0068
<140> PCT/US2019/050907
<141> 12.09.2019
<150> 62/730 471
<151> 12.09.2018
<160> 14
<170> PatentIn версия 3.5
<210> 1
<211> 179
<212> БЕЛОК
<213> Неизвестно
<220>
<223> Описание неизвестного:
последовательность белка ризавидин
<400> 1
Met Ile Ile Thr Ser Leu Tyr Ala Thr Phe Gly Thr Ile Ala Asp Gly
1 5 10 15
Arg Arg Thr Ser Gly Gly Lys Thr Met Ile Arg Thr Asn Ala Val Ala
20 25 30
Ala Leu Val Phe Ala Val Ala Thr Ser Ala Leu Ala Phe Asp Ala Ser
35 40 45
Asn Phe Lys Asp Phe Ser Ser Ile Ala Ser Ala Ser Ser Ser Trp Gln
50 55 60
Asn Gln Ser Gly Ser Thr Met Ile Ile Gln Val Asp Ser Phe Gly Asn
65 70 75 80
Val Ser Gly Gln Tyr Val Asn Arg Ala Gln Gly Thr Gly Cys Gln Asn
85 90 95
Ser Pro Tyr Pro Leu Thr Gly Arg Val Asn Gly Thr Phe Ile Ala Phe
100 105 110
Ser Val Gly Trp Asn Asn Ser Thr Glu Asn Cys Asn Ser Ala Thr Gly
115 120 125
Trp Thr Gly Tyr Ala Gln Val Asn Gly Asn Asn Thr Glu Ile Val Thr
130 135 140
Ser Trp Asn Leu Ala Tyr Glu Gly Gly Ser Gly Pro Ala Ile Glu Gln
145 150 155 160
Gly Gln Asp Thr Phe Gln Tyr Val Pro Thr Thr Glu Asn Lys Ser Leu
165 170 175
Leu Lys Asp
<210> 2
<211> 135
<212> БЕЛОК
<213> Неизвестно
<220>
<223> Описание неизвестного:
последовательность белка ризавидин
<400> 2
Phe Asp Ala Ser Asn Phe Lys Asp Phe Ser Ser Ile Ala Ser Ala Ser
1 5 10 15
Ser Ser Trp Gln Asn Gln Ser Gly Ser Thr Met Ile Ile Gln Val Asp
20 25 30
Ser Phe Gly Asn Val Ser Gly Gln Tyr Val Asn Arg Ala Gln Gly Thr
35 40 45
Gly Cys Gln Asn Ser Pro Tyr Pro Leu Thr Gly Arg Val Asn Gly Thr
50 55 60
Phe Ile Ala Phe Ser Val Gly Trp Asn Asn Ser Thr Glu Asn Cys Asn
65 70 75 80
Ser Ala Thr Gly Trp Thr Gly Tyr Ala Gln Val Asn Gly Asn Asn Thr
85 90 95
Glu Ile Val Thr Ser Trp Asn Leu Ala Tyr Glu Gly Gly Ser Gly Pro
100 105 110
Ala Ile Glu Gln Gly Gln Asp Thr Phe Gln Tyr Val Pro Thr Thr Glu
115 120 125
Asn Lys Ser Leu Leu Lys Asp
130 135
<210> 3
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3
Gly Gly Gly Gly Ser Ser Ser
1 5
<210> 4
<211> 367
<212> БЕЛОК
<213> Streptococcus pneumoniae
<400> 4
Phe Arg Gln Pro Ser Gln Thr Ala Leu Lys Asp Glu Pro Thr His Leu
1 5 10 15
Val Val Ala Lys Glu Gly Ser Val Ala Ser Ser Val Leu Leu Ser Gly
20 25 30
Thr Val Thr Ala Lys Asn Glu Gln Tyr Val Tyr Phe Asp Ala Ser Lys
35 40 45
Gly Asp Leu Asp Glu Ile Leu Val Ser Val Gly Asp Lys Val Ser Glu
50 55 60
Gly Gln Ala Leu Val Lys Tyr Ser Ser Ser Glu Ala Gln Ala Ala Tyr
65 70 75 80
Asp Ser Ala Ser Arg Ala Val Ala Arg Ala Asp Arg His Ile Asn Glu
85 90 95
Leu Asn Gln Ala Arg Asn Glu Ala Ala Ser Ala Pro Ala Pro Gln Leu
100 105 110
Pro Ala Pro Val Gly Gly Glu Asp Ala Thr Val Gln Ser Pro Thr Pro
115 120 125
Val Ala Gly Asn Ser Val Ala Ser Ile Asp Ala Gln Leu Gly Asp Ala
130 135 140
Arg Asp Ala Arg Ala Asp Ala Ala Ala Gln Leu Ser Lys Ala Gln Ser
145 150 155 160
Gln Leu Asp Ala Thr Thr Val Leu Ser Thr Leu Glu Gly Thr Val Val
165 170 175
Glu Val Asn Ser Asn Val Ser Lys Ser Pro Thr Gly Ala Ser Gln Val
180 185 190
Met Val His Ile Val Ser Asn Glu Asn Leu Gln Val Lys Gly Glu Leu
195 200 205
Ser Glu Tyr Asn Leu Ala Asn Leu Ser Val Gly Gln Glu Val Ser Phe
210 215 220
Thr Ser Lys Val Tyr Pro Asp Lys Lys Trp Thr Gly Lys Leu Ser Tyr
225 230 235 240
Ile Ser Asp Tyr Pro Lys Asn Asn Gly Glu Ala Ala Ser Pro Ala Ala
245 250 255
Gly Asn Asn Thr Gly Ser Lys Tyr Pro Tyr Thr Ile Asp Val Thr Gly
260 265 270
Glu Val Gly Asp Leu Lys Gln Gly Phe Ser Val Asn Ile Glu Val Lys
275 280 285
Ser Lys Thr Lys Ala Ile Leu Val Pro Val Ser Ser Leu Val Met Asp
290 295 300
Asp Ser Lys Asn Tyr Val Trp Ile Val Asp Glu Gln Gln Lys Ala Lys
305 310 315 320
Lys Val Glu Val Ser Leu Gly Asn Ala Asp Ala Glu Asn Gln Glu Ile
325 330 335
Thr Ser Gly Leu Thr Asn Gly Ala Lys Val Ile Ser Asn Pro Thr Ser
340 345 350
Ser Leu Glu Glu Gly Lys Glu Val Lys Ala Asp Glu Ala Thr Asn
355 360 365
<210> 5
<211> 252
<212> БЕЛОК
<213> Streptococcus pneumoniae
<400> 5
Thr Ser Gly Asp Asn Trp Ser Lys Tyr Gln Ser Asn Lys Ser Ile Thr
1 5 10 15
Ile Gly Phe Asp Ser Thr Phe Val Pro Met Gly Phe Ala Gln Lys Asp
20 25 30
Gly Ser Tyr Ala Gly Phe Asp Ile Asp Leu Ala Thr Ala Val Phe Glu
35 40 45
Lys Tyr Gly Ile Thr Val Asn Trp Gln Pro Ile Asp Trp Asp Leu Lys
50 55 60
Glu Ala Glu Leu Thr Lys Gly Thr Ile Asp Leu Ile Trp Asn Gly Tyr
65 70 75 80
Ser Ala Thr Asp Glu Arg Arg Glu Lys Val Ala Phe Ser Asn Ser Tyr
85 90 95
Met Lys Asn Glu Gln Val Leu Val Thr Lys Lys Ser Ser Gly Ile Thr
100 105 110
Thr Ala Lys Asp Met Thr Gly Lys Thr Leu Gly Ala Gln Ala Gly Ser
115 120 125
Ser Gly Tyr Ala Asp Phe Glu Ala Asn Pro Glu Ile Leu Lys Asn Ile
130 135 140
Val Ala Asn Lys Glu Ala Asn Gln Tyr Gln Thr Phe Asn Glu Ala Leu
145 150 155 160
Ile Asp Leu Lys Asn Asp Arg Ile Asp Gly Leu Leu Ile Asp Arg Val
165 170 175
Tyr Ala Asn Tyr Tyr Leu Glu Ala Glu Gly Val Leu Asn Asp Tyr Asn
180 185 190
Val Phe Thr Val Gly Leu Glu Thr Glu Ala Phe Ala Val Gly Ala Arg
195 200 205
Lys Glu Asp Thr Asn Leu Val Lys Lys Ile Asn Glu Ala Phe Ser Ser
210 215 220
Leu Tyr Lys Asp Gly Lys Phe Gln Glu Ile Ser Gln Lys Trp Phe Gly
225 230 235 240
Glu Asp Val Ala Thr Lys Glu Val Lys Glu Gly Gln
245 250
<210> 6
<211> 765
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 6
Met Phe Asp Ala Ser Asn Phe Lys Asp Phe Ser Ser Ile Ala Ser Ala
1 5 10 15
Ser Ser Ser Trp Gln Asn Gln Ser Gly Ser Thr Met Ile Ile Gln Val
20 25 30
Asp Ser Phe Gly Asn Val Ser Gly Gln Tyr Val Asn Arg Ala Gln Gly
35 40 45
Thr Gly Cys Gln Asn Ser Pro Tyr Pro Leu Thr Gly Arg Val Asn Gly
50 55 60
Thr Phe Ile Ala Phe Ser Val Gly Trp Asn Asn Ser Thr Glu Asn Cys
65 70 75 80
Asn Ser Ala Thr Gly Trp Thr Gly Tyr Ala Gln Val Asn Gly Asn Asn
85 90 95
Thr Glu Ile Val Thr Ser Trp Asn Leu Ala Tyr Glu Gly Gly Ser Gly
100 105 110
Pro Ala Ile Glu Gln Gly Gln Asp Thr Phe Gln Tyr Val Pro Thr Thr
115 120 125
Glu Asn Lys Ser Leu Leu Lys Asp Gly Gly Gly Gly Ser Ser Ser Thr
130 135 140
Ser Gly Asp Asn Trp Ser Lys Tyr Gln Ser Asn Lys Ser Ile Thr Ile
145 150 155 160
Gly Phe Asp Ser Thr Phe Val Pro Met Gly Phe Ala Gln Lys Asp Gly
165 170 175
Ser Tyr Ala Gly Phe Asp Ile Asp Leu Ala Thr Ala Val Phe Glu Lys
180 185 190
Tyr Gly Ile Thr Val Asn Trp Gln Pro Ile Asp Trp Asp Leu Lys Glu
195 200 205
Ala Glu Leu Thr Lys Gly Thr Ile Asp Leu Ile Trp Asn Gly Tyr Ser
210 215 220
Ala Thr Asp Glu Arg Arg Glu Lys Val Ala Phe Ser Asn Ser Tyr Met
225 230 235 240
Lys Asn Glu Gln Val Leu Val Thr Lys Lys Ser Ser Gly Ile Thr Thr
245 250 255
Ala Lys Asp Met Thr Gly Lys Thr Leu Gly Ala Gln Ala Gly Ser Ser
260 265 270
Gly Tyr Ala Asp Phe Glu Ala Asn Pro Glu Ile Leu Lys Asn Ile Val
275 280 285
Ala Asn Lys Glu Ala Asn Gln Tyr Gln Thr Phe Asn Glu Ala Leu Ile
290 295 300
Asp Leu Lys Asn Asp Arg Ile Asp Gly Leu Leu Ile Asp Arg Val Tyr
305 310 315 320
Ala Asn Tyr Tyr Leu Glu Ala Glu Gly Val Leu Asn Asp Tyr Asn Val
325 330 335
Phe Thr Val Gly Leu Glu Thr Glu Ala Phe Ala Val Gly Ala Arg Lys
340 345 350
Glu Asp Thr Asn Leu Val Lys Lys Ile Asn Glu Ala Phe Ser Ser Leu
355 360 365
Tyr Lys Asp Gly Lys Phe Gln Glu Ile Ser Gln Lys Trp Phe Gly Glu
370 375 380
Asp Val Ala Thr Lys Glu Val Lys Glu Gly Gln Ala Ala Ala Phe Arg
385 390 395 400
Gln Pro Ser Gln Thr Ala Leu Lys Asp Glu Pro Thr His Leu Val Val
405 410 415
Ala Lys Glu Gly Ser Val Ala Ser Ser Val Leu Leu Ser Gly Thr Val
420 425 430
Thr Ala Lys Asn Glu Gln Tyr Val Tyr Phe Asp Ala Ser Lys Gly Asp
435 440 445
Leu Asp Glu Ile Leu Val Ser Val Gly Asp Lys Val Ser Glu Gly Gln
450 455 460
Ala Leu Val Lys Tyr Ser Ser Ser Glu Ala Gln Ala Ala Tyr Asp Ser
465 470 475 480
Ala Ser Arg Ala Val Ala Arg Ala Asp Arg His Ile Asn Glu Leu Asn
485 490 495
Gln Ala Arg Asn Glu Ala Ala Ser Ala Pro Ala Pro Gln Leu Pro Ala
500 505 510
Pro Val Gly Gly Glu Asp Ala Thr Val Gln Ser Pro Thr Pro Val Ala
515 520 525
Gly Asn Ser Val Ala Ser Ile Asp Ala Gln Leu Gly Asp Ala Arg Asp
530 535 540
Ala Arg Ala Asp Ala Ala Ala Gln Leu Ser Lys Ala Gln Ser Gln Leu
545 550 555 560
Asp Ala Thr Thr Val Leu Ser Thr Leu Glu Gly Thr Val Val Glu Val
565 570 575
Asn Ser Asn Val Ser Lys Ser Pro Thr Gly Ala Ser Gln Val Met Val
580 585 590
His Ile Val Ser Asn Glu Asn Leu Gln Val Lys Gly Glu Leu Ser Glu
595 600 605
Tyr Asn Leu Ala Asn Leu Ser Val Gly Gln Glu Val Ser Phe Thr Ser
610 615 620
Lys Val Tyr Pro Asp Lys Lys Trp Thr Gly Lys Leu Ser Tyr Ile Ser
625 630 635 640
Asp Tyr Pro Lys Asn Asn Gly Glu Ala Ala Ser Pro Ala Ala Gly Asn
645 650 655
Asn Thr Gly Ser Lys Tyr Pro Tyr Thr Ile Asp Val Thr Gly Glu Val
660 665 670
Gly Asp Leu Lys Gln Gly Phe Ser Val Asn Ile Glu Val Lys Ser Lys
675 680 685
Thr Lys Ala Ile Leu Val Pro Val Ser Ser Leu Val Met Asp Asp Ser
690 695 700
Lys Asn Tyr Val Trp Ile Val Asp Glu Gln Gln Lys Ala Lys Lys Val
705 710 715 720
Glu Val Ser Leu Gly Asn Ala Asp Ala Glu Asn Gln Glu Ile Thr Ser
725 730 735
Gly Leu Thr Asn Gly Ala Lys Val Ile Ser Asn Pro Thr Ser Ser Leu
740 745 750
Glu Glu Gly Lys Glu Val Lys Ala Asp Glu Ala Thr Asn
755 760 765
<210> 7
<211> 1101
<212> ДНК
<213> Streptococcus pneumoniae
<400> 7
tttagacaac cttctcagac tgctctaaaa gatgagccta ctcatcttgt tgttgccaag 60
gaaggaagcg tggcctcctc tgttttattg tcagggacag taacagcaaa aaatgaacaa 120
tatgtttatt ttgatgctag taagggtgat ttagatgaaa tccttgtttc tgtgggcgat 180
aaggtcagcg aagggcaggc tttagtcaag tacagtagtt cagaagcgca ggcggcctat 240
gattcagcta gtcgagcagt agctagggca gatcgtcata tcaatgaact caatcaagca 300
cgaaatgaag ccgcttcagc tccggctcca cagttaccag cgccagtagg aggagaagat 360
gcaacggtgc aaagcccaac tccagtggct ggaaattctg ttgcttctat tgacgctcaa 420
ttgggtgatg cccgtgatgc gcgtgcagat gctgcggcgc aattaagcaa ggctcaaagt 480
caattggatg caacaactgt tctcagtacc ctagagggaa ctgtggtcga agtcaatagc 540
aatgtttcta aatctccaac aggggcgagt caagttatgg ttcatattgt cagcaatgaa 600
aatttacaag tcaagggaga attgtctgag tacaatctag ccaacctttc tgtaggtcaa 660
gaagtaagct ttacttctaa agtgtatcct gataaaaaat ggactgggaa attaagctat 720
atttctgact atcctaaaaa caatggtgaa gcagctagtc cagcagccgg gaataataca 780
ggttctaaat acccttatac tattgatgtg acaggcgagg ttggtgattt gaaacaaggt 840
ttttctgtca acattgaggt taaaagcaaa actaaggcta ttcttgttcc tgttagcagt 900
ctagtaatgg atgatagtaa aaattatgtc tggattgtgg atgaacaaca aaaggctaaa 960
aaagttgagg tttcattggg aaatgctgac gcagaaaatc aagaaatcac ttctggttta 1020
acgaacggtg ctaaggtcat cagtaatcca acatcttcct tggaagaagg aaaagaggtg 1080
aaggctgatg aagcaactaa t 1101
<210> 8
<211> 756
<212> ДНК
<213> Streptococcus pneumoniae
<400> 8
actagtggag ataattggtc aaagtaccag tctaacaagt ctattactat tggatttgat 60
agtacttttg ttccaatggg atttgctcag aaagatggtt cttatgcagg atttgatatt 120
gatttagcta cagctgtttt tgaaaaatac ggaatcacgg taaattggca accgattgat 180
tgggatttga aagaagctga attgacaaaa ggaacgattg atctgatttg gaatggctat 240
tccgctacag acgaacgccg tgaaaaggtg gctttcagta actcatatat gaagaatgag 300
caggtattgg ttacgaagaa atcatctggt atcacgactg caaaggatat gactggaaag 360
acattaggag ctcaagctgg ttcatctggt tatgcggact ttgaagcaaa tccagaaatt 420
ttgaagaata ttgtcgctaa taaggaagcg aatcaatacc aaacctttaa tgaagccttg 480
attgatttga aaaacgatcg aattgatggt ctattgattg accgtgtcta tgcaaactat 540
tatttagaag cagaaggtgt tttaaacgat tataatgtct ttacagttgg actagaaaca 600
gaagcttttg cggttggagc ccgtaaggaa gatacaaact tggttaagaa gataaatgaa 660
gctttttcta gtctttacaa ggacggcaag ttccaagaaa tcagccaaaa atggtttgga 720
gaagatgtag caaccaaaga agtaaaagaa ggacag 756
<210> 9
<211> 2295
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 9
atgttcgacg catccaactt taaagacttt agcagcatcg cgtccgcaag ctctagctgg 60
cagaatcaat ctggtagcac catgattatc caagtggaca gctttggtaa cgtcagcggt 120
caatatgtta atcgtgcaca gggtacgggt tgtcagaatt ctccgtaccc gctgaccggt 180
cgtgttaacg gcacgttcat cgctttcagc gtcggttgga acaattctac tgaaaattgc 240
aacagcgcga ccggttggac gggctatgca caagtgaatg gcaataacac cgaaatcgtc 300
acgtcctgga atctggcgta tgagggtggc agcggtccgg ctattgaaca gggccaggat 360
accttccaat acgtccctac gaccgagaat aagtcccttc tgaaagacgg cggtggcggt 420
tcgagctcga ccagcggcga caattggtcc aaataccaga gcaacaagag catcacgatc 480
ggcttcgaca gcacttttgt gccgatgggt ttcgcgcaaa aagacggtag ctacgcgggt 540
ttcgatattg acctggcgac cgctgtcttt gagaaatacg gcattacggt taattggcag 600
ccgattgatt gggacctgaa agaggccgaa ctcaccaaag gcaccatcga cctgatctgg 660
aatggttact ccgcaaccga tgagcgtcgc gaaaaagttg ccttcagcaa cagctatatg 720
aagaatgaac aagtgttggt aaccaagaaa tctagcggca ttacgaccgc gaaagacatg 780
accggtaaga cgctgggtgc gcaggccggt agctctggct atgcggattt cgaggcgaat 840
cctgagattc tgaaaaacat cgttgcgaat aaagaggcga accagtacca gacctttaac 900
gaagcactga tcgacctgaa aaacgatcgc attgacggtc tgctgatcga tcgtgtgtac 960
gcgaactatt atctggaagc cgagggcgtt ctgaacgatt ataatgtttt taccgtgggt 1020
ctggagactg aggcattcgc ggttggtgcg cgcaaggaag ataccaacct ggttaaaaag 1080
attaatgagg catttagctc actgtacaag gacggcaagt tccaagaaat tagccagaag 1140
tggttcggtg aagatgttgc gacgaaagag gttaaagagg gccaagcggc cgcatttcgc 1200
caaccgagcc agactgcgtt gaaagatgag ccgacccatc tggttgttgc gaaagagggc 1260
agcgtggcat cgagcgtgct gctgagcggt acggttactg ccaaaaacga acaatacgtg 1320
tacttcgatg ctagcaaggg tgatctggat gaaattctgg tgagcgtggg tgacaaagtt 1380
agcgaaggcc aggcactggt gaagtattca tcctccgagg cacaggcagc gtacgacagc 1440
gcaagccgcg cagtggcgcg tgccgaccgt cacattaacg aattgaacca agcgcgtaac 1500
gaggccgcaa gcgcgccagc accgcagctg ccggctccgg tgggtggcga agatgcgacg 1560
gtgcagagcc cgaccccggt tgcgggtaat tcggtcgcca gcatcgatgc gcagctgggt 1620
gacgcgcgtg atgcccgtgc ggatgcggct gctcaactga gcaaggctca gagccaactg 1680
gacgcgacga cggtgctgag caccttggag ggtaccgttg tcgaagtcaa cagcaatgtg 1740
agcaagagcc caacgggtgc gagccaggtt atggtccaca ttgtgagcaa tgaaaactta 1800
caggtcaagg gtgagctgag cgagtataac ctggcgaatc tgagcgttgg tcaagaggtc 1860
agctttacca gcaaggtcta cccggataag aaatggaccg gcaagttgag ctacatcagc 1920
gactacccga agaacaatgg cgaggcagcc tccccggcag ccggcaacaa taccggctct 1980
aagtatccgt acaccatcga cgtaaccggt gaggtcggcg acctgaaaca gggttttagc 2040
gtgaatatcg aagtgaagtc caagaccaag gcaattttgg ttccggttag ctccctggtg 2100
atggacgata gcaagaatta tgtgtggatt gtcgacgagc aacagaaagc gaaaaaagtt 2160
gaagtgagcc tgggcaatgc tgatgccgag aaccaagaaa tcacgtctgg tctgaccaac 2220
ggtgcgaaag ttattagcaa cccgaccagc agcctggaag agggtaaaga ggtcaaagcc 2280
gacgaagcta cgaac 2295
<210> 10
<211> 399
<212> БЕЛОК
<213> Streptococcus pneumoniae
<400> 10
Met Lys Lys Lys Asn Gly Lys Ala Lys Lys Trp Gln Leu Tyr Ala Ala
1 5 10 15
Ile Gly Ala Ala Ser Val Val Val Leu Gly Ala Gly Gly Ile Leu Leu
20 25 30
Phe Arg Gln Pro Ser Gln Thr Ala Leu Lys Asp Glu Pro Thr His Leu
35 40 45
Val Val Ala Lys Glu Gly Ser Val Ala Ser Ser Val Leu Leu Ser Gly
50 55 60
Thr Val Thr Ala Lys Asn Glu Gln Tyr Val Tyr Phe Asp Ala Ser Lys
65 70 75 80
Gly Asp Leu Asp Glu Ile Leu Val Ser Val Gly Asp Lys Val Ser Glu
85 90 95
Gly Gln Ala Leu Val Lys Tyr Ser Ser Ser Glu Ala Gln Ala Ala Tyr
100 105 110
Asp Ser Ala Ser Arg Ala Val Ala Arg Ala Asp Arg His Ile Asn Glu
115 120 125
Leu Asn Gln Ala Arg Asn Glu Ala Ala Ser Ala Pro Ala Pro Gln Leu
130 135 140
Pro Ala Pro Val Gly Gly Glu Asp Ala Thr Val Gln Ser Pro Thr Pro
145 150 155 160
Val Ala Gly Asn Ser Val Ala Ser Ile Asp Ala Gln Leu Gly Asp Ala
165 170 175
Arg Asp Ala Arg Ala Asp Ala Ala Ala Gln Leu Ser Lys Ala Gln Ser
180 185 190
Gln Leu Asp Ala Thr Thr Val Leu Ser Thr Leu Glu Gly Thr Val Val
195 200 205
Glu Val Asn Ser Asn Val Ser Lys Ser Pro Thr Gly Ala Ser Gln Val
210 215 220
Met Val His Ile Val Ser Asn Glu Asn Leu Gln Val Lys Gly Glu Leu
225 230 235 240
Ser Glu Tyr Asn Leu Ala Asn Leu Ser Val Gly Gln Glu Val Ser Phe
245 250 255
Thr Ser Lys Val Tyr Pro Asp Lys Lys Trp Thr Gly Lys Leu Ser Tyr
260 265 270
Ile Ser Asp Tyr Pro Lys Asn Asn Gly Glu Ala Ala Ser Pro Ala Ala
275 280 285
Gly Asn Asn Thr Gly Ser Lys Tyr Pro Tyr Thr Ile Asp Val Thr Gly
290 295 300
Glu Val Gly Asp Leu Lys Gln Gly Phe Ser Val Asn Ile Glu Val Lys
305 310 315 320
Ser Lys Thr Lys Ala Ile Leu Val Pro Val Ser Ser Leu Val Met Asp
325 330 335
Asp Ser Lys Asn Tyr Val Trp Ile Val Asp Glu Gln Gln Lys Ala Lys
340 345 350
Lys Val Glu Val Ser Leu Gly Asn Ala Asp Ala Glu Asn Gln Glu Ile
355 360 365
Thr Ser Gly Leu Thr Asn Gly Ala Lys Val Ile Ser Asn Pro Thr Ser
370 375 380
Ser Leu Glu Glu Gly Lys Glu Val Lys Ala Asp Glu Ala Thr Asn
385 390 395
<210> 11
<211> 1197
<212> ДНК
<213> Streptococcus pneumoniae
<400> 11
atgaagaaaa agaatggtaa agctaaaaag tggcaactgt atgcagcaat cggtgctgcg 60
agtgtagttg tattgggtgc tggggggatt ttactcttta gacaaccttc tcagactgct 120
ctaaaagatg agcctactca tcttgttgtt gccaaggaag gaagcgtggc ctcctctgtt 180
ttattgtcag ggacagtaac agcaaaaaat gaacaatatg tttattttga tgctagtaag 240
ggtgatttag atgaaatcct tgtttctgtg ggcgataagg tcagcgaagg gcaggcttta 300
gtcaagtaca gtagttcaga agcgcaggcg gcctatgatt cagctagtcg agcagtagct 360
agggcagatc gtcatatcaa tgaactcaat caagcacgaa atgaagccgc ttcagctccg 420
gctccacagt taccagcgcc agtaggagga gaagatgcaa cggtgcaaag cccaactcca 480
gtggctggaa attctgttgc ttctattgac gctcaattgg gtgatgcccg tgatgcgcgt 540
gcagatgctg cggcgcaatt aagcaaggct caaagtcaat tggatgcaac aactgttctc 600
agtaccctag agggaactgt ggtcgaagtc aatagcaatg tttctaaatc tccaacaggg 660
gcgagtcaag ttatggttca tattgtcagc aatgaaaatt tacaagtcaa gggagaattg 720
tctgagtaca atctagccaa cctttctgta ggtcaagaag taagctttac ttctaaagtg 780
tatcctgata aaaaatggac tgggaaatta agctatattt ctgactatcc taaaaacaat 840
ggtgaagcag ctagtccagc agccgggaat aatacaggtt ctaaataccc ttatactatt 900
gatgtgacag gcgaggttgg tgatttgaaa caaggttttt ctgtcaacat tgaggttaaa 960
agcaaaacta aggctattct tgttcctgtt agcagtctag taatggatga tagtaaaaat 1020
tatgtctgga ttgtggatga acaacaaaag gctaaaaaag ttgaggtttc attgggaaat 1080
gctgacgcag aaaatcaaga aatcacttct ggtttaacga acggtgctaa ggtcatcagt 1140
aatccaacat cttccttgga agaaggaaaa gaggtgaagg ctgatgaagc aactaat 1197
<210> 12
<211> 278
<212> БЕЛОК
<213> Streptococcus pneumoniae
<400> 12
Met Lys Lys Trp Met Leu Val Leu Val Ser Leu Met Thr Ala Leu Phe
1 5 10 15
Leu Val Ala Cys Gly Lys Asn Ser Ser Glu Thr Ser Gly Asp Asn Trp
20 25 30
Ser Lys Tyr Gln Ser Asn Lys Ser Ile Thr Ile Gly Phe Asp Ser Thr
35 40 45
Phe Val Pro Met Gly Phe Ala Gln Lys Asp Gly Ser Tyr Ala Gly Phe
50 55 60
Asp Ile Asp Leu Ala Thr Ala Val Phe Glu Lys Tyr Gly Ile Thr Val
65 70 75 80
Asn Trp Gln Pro Ile Asp Trp Asp Leu Lys Glu Ala Glu Leu Thr Lys
85 90 95
Gly Thr Ile Asp Leu Ile Trp Asn Gly Tyr Ser Ala Thr Asp Glu Arg
100 105 110
Arg Glu Lys Val Ala Phe Ser Asn Ser Tyr Met Lys Asn Glu Gln Val
115 120 125
Leu Val Thr Lys Lys Ser Ser Gly Ile Thr Thr Ala Lys Asp Met Thr
130 135 140
Gly Lys Thr Leu Gly Ala Gln Ala Gly Ser Ser Gly Tyr Ala Asp Phe
145 150 155 160
Glu Ala Asn Pro Glu Ile Leu Lys Asn Ile Val Ala Asn Lys Glu Ala
165 170 175
Asn Gln Tyr Gln Thr Phe Asn Glu Ala Leu Ile Asp Leu Lys Asn Asp
180 185 190
Arg Ile Asp Gly Leu Leu Ile Asp Arg Val Tyr Ala Asn Tyr Tyr Leu
195 200 205
Glu Ala Glu Gly Val Leu Asn Asp Tyr Asn Val Phe Thr Val Gly Leu
210 215 220
Glu Thr Glu Ala Phe Ala Val Gly Ala Arg Lys Glu Asp Thr Asn Leu
225 230 235 240
Val Lys Lys Ile Asn Glu Ala Phe Ser Ser Leu Tyr Lys Asp Gly Lys
245 250 255
Phe Gln Glu Ile Ser Gln Lys Trp Phe Gly Glu Asp Val Ala Thr Lys
260 265 270
Glu Val Lys Glu Gly Gln
275
<210> 13
<211> 834
<212> ДНК
<213> Streptococcus pneumoniae
<400> 13
atgaaaaaat ggatgcttgt attagtcagt ctgatgactg ctttgttctt agtagcttgt 60
gggaaaaatt ctagcgaaac tagtggagat aattggtcaa agtaccagtc taacaagtct 120
attactattg gatttgatag tacttttgtt ccaatgggat ttgctcagaa agatggttct 180
tatgcaggat ttgatattga tttagctaca gctgtttttg aaaaatacgg aatcacggta 240
aattggcaac cgattgattg ggatttgaaa gaagctgaat tgacaaaagg aacgattgat 300
ctgatttgga atggctattc cgctacagac gaacgccgtg aaaaggtggc tttcagtaac 360
tcatatatga agaatgagca ggtattggtt acgaagaaat catctggtat cacgactgca 420
aaggatatga ctggaaagac attaggagct caagctggtt catctggtta tgcggacttt 480
gaagcaaatc cagaaatttt gaagaatatt gtcgctaata aggaagcgaa tcaataccaa 540
acctttaatg aagccttgat tgatttgaaa aacgatcgaa ttgatggtct attgattgac 600
cgtgtctatg caaactatta tttagaagca gaaggtgttt taaacgatta taatgtcttt 660
acagttggac tagaaacaga agcttttgcg gttggagccc gtaaggaaga tacaaacttg 720
gttaagaaga taaatgaagc tttttctagt ctttacaagg acggcaagtt ccaagaaatc 780
agccaaaaat ggtttggaga agatgtagca accaaagaag taaaagaagg acag 834
<210> 14
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический пептид
<400> 14
Gly Gly Gly Gly
1
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОГЕННЫЕ КОМПОЗИЦИИ | 2018 |
|
RU2791256C2 |
| ПНЕВМОКОККОВЫЕ ПОЛИСАХАРИДЫ И ИХ ПРИМЕНЕНИЕ В ИММУНОГЕННЫХ КОНЪЮГАТАХ ПОЛИСАХАРИД-БЕЛОК-НОСИТЕЛЬ | 2018 |
|
RU2785429C2 |
| ИММУНОГЕННАЯ КОМПОЗИЦИЯ ПРЕЗЕНТАЦИИ МНОЖЕСТВЕННЫХ АНТИГЕНОВ, ОТНОСЯЩИЕСЯ К НЕЙ СПОСОБЫ И ПРИМЕНЕНИЯ | 2012 |
|
RU2619176C2 |
| ПНЕВМОКОККОВЫЕ ПОЛИСАХАРИДЫ И ИХ ПРИМЕНЕНИЕ В ИММУНОГЕННЫХ КОНЪЮГАТАХ ПОЛИСАХАРИД-БЕЛОК-НОСИТЕЛЬ | 2018 |
|
RU2801304C2 |
| ИММУНОГЕННЫЕ КОМПОЗИЦИИ ДЛЯ ПРИМЕНЕНИЯ В ПНЕВМОКОККОВЫХ ВАКЦИНАХ | 2021 |
|
RU2827429C1 |
| ПНЕВМОКОККОВЫЕ ПОЛИСАХАРИДЫ И ИХ ПРИМЕНЕНИЕ В ИММУНОГЕННЫХ КОНЪЮГАТАХ ПОЛИСАХАРИД-БЕЛОК-НОСИТЕЛЬ | 2018 |
|
RU2784449C2 |
| ИММУНОГЕННЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ КОНЪЮГИРОВАННЫЕ КАПСУЛЬНЫЕ САХАРИДНЫЕ АНТИГЕНЫ, И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2774075C1 |
| ПНЕВМОКОККОВЫЕ ПОЛИСАХАРИДЫ И ИХ ПРИМЕНЕНИЕ В ИММУНОГЕННЫХ КОНЪЮГАТАХ ПОЛИСАХАРИД-БЕЛОК-НОСИТЕЛЬ | 2018 |
|
RU2801288C2 |
| Капсульные полисахариды Streptococcus pneumoniae и их конъюгаты | 2015 |
|
RU2688831C2 |
| Капсульные полисахариды Streptococcus pneumoniae и их конъюгаты | 2015 |
|
RU2743793C1 |
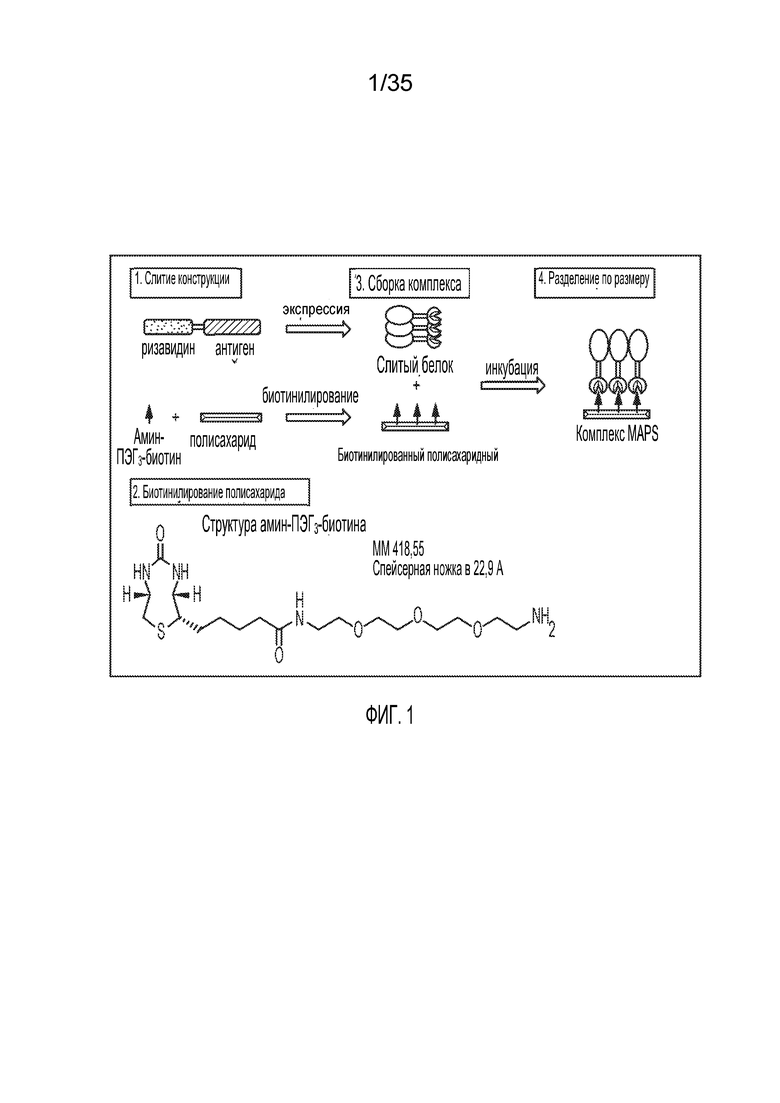
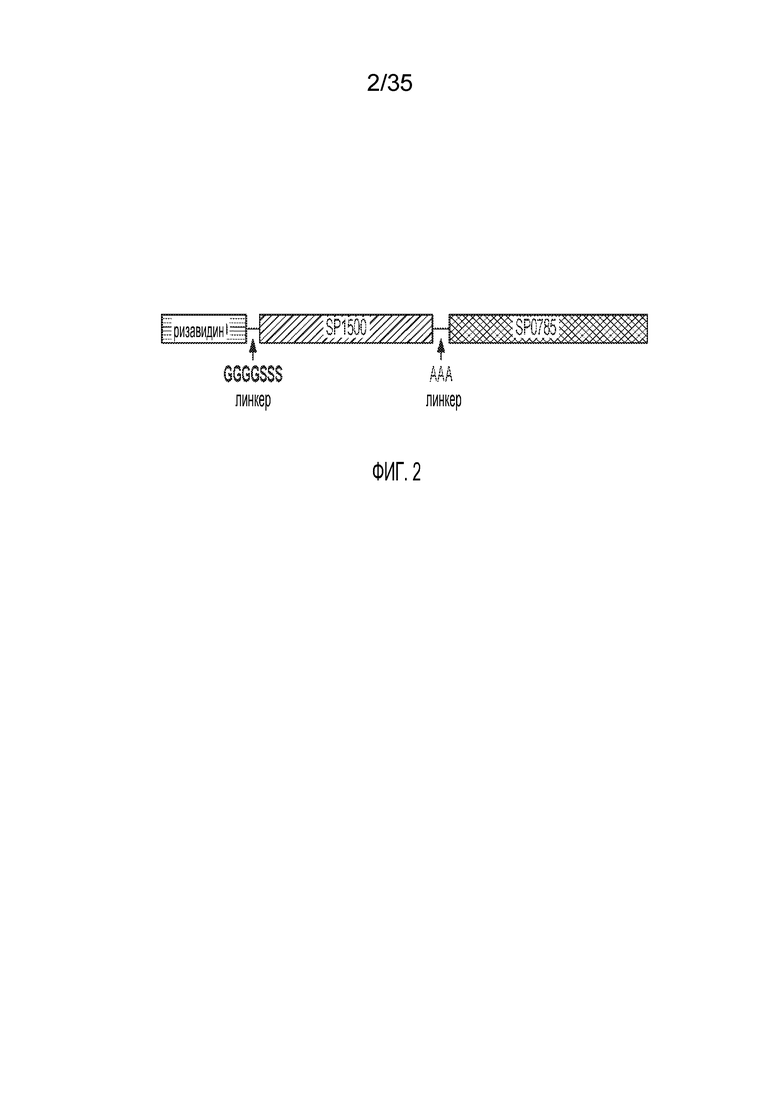

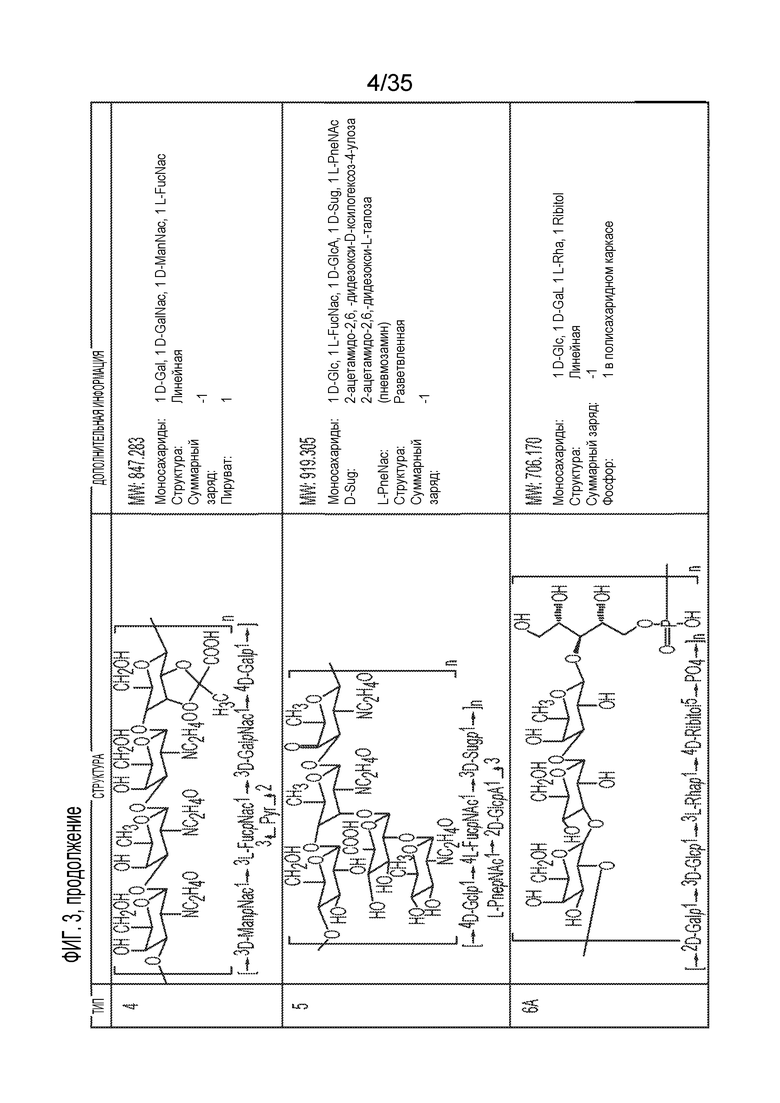
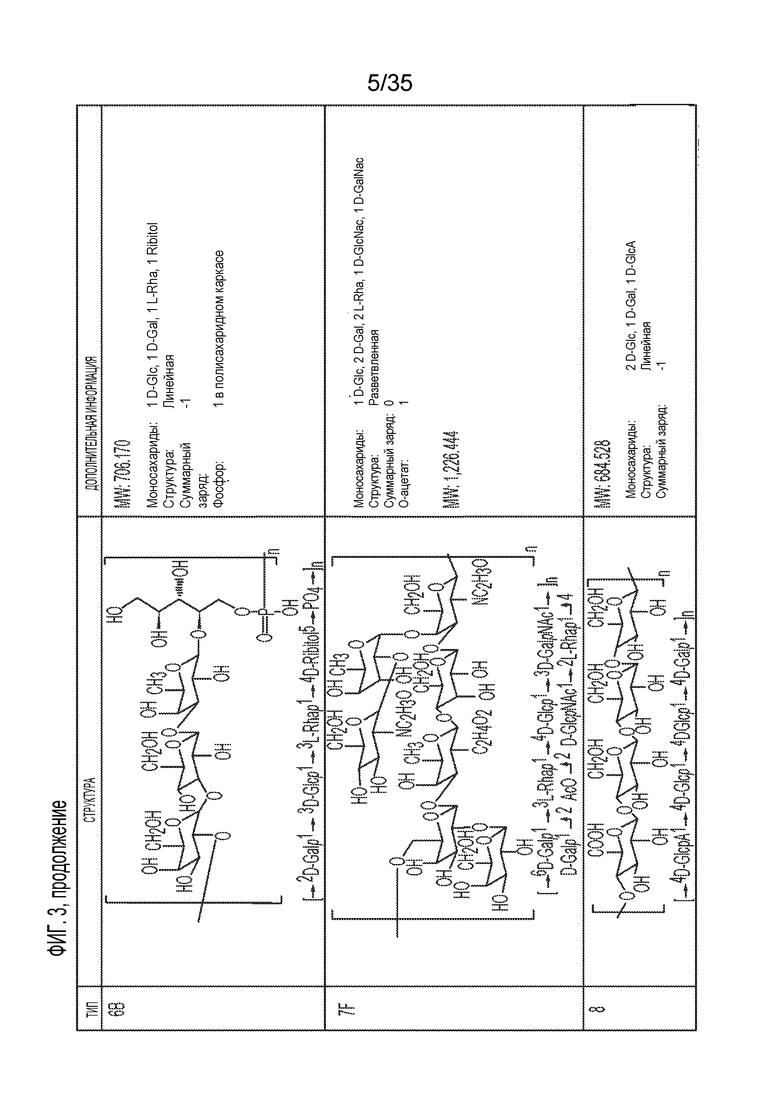
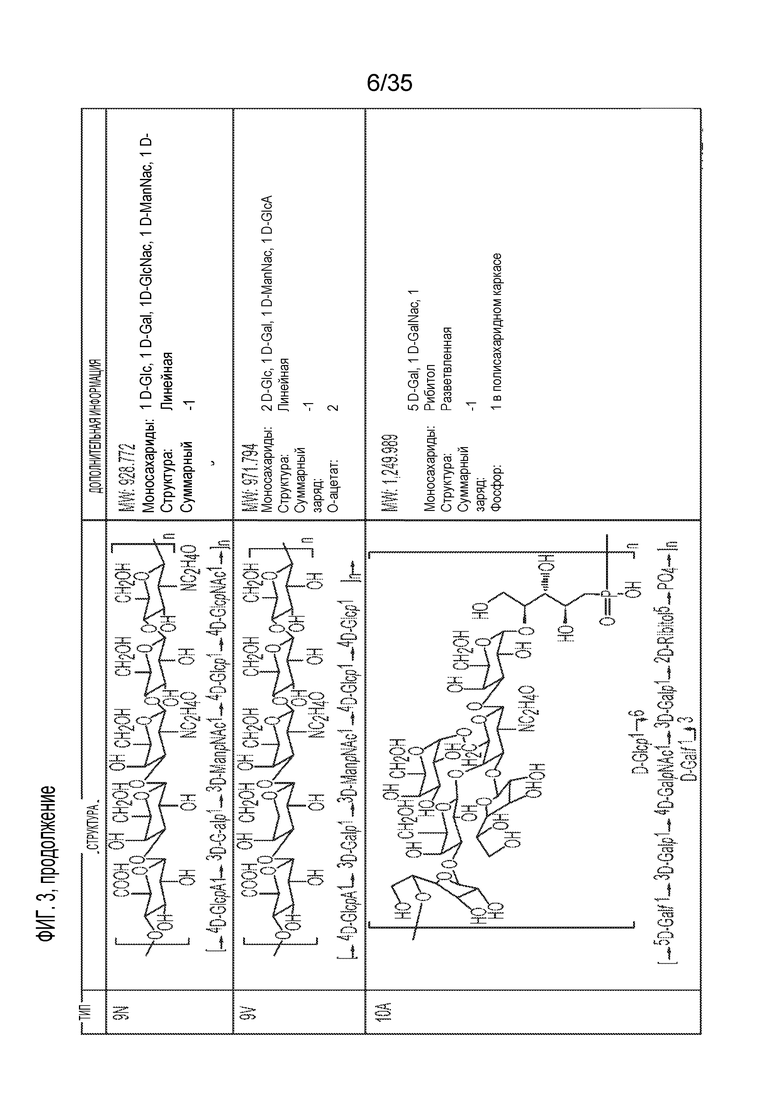
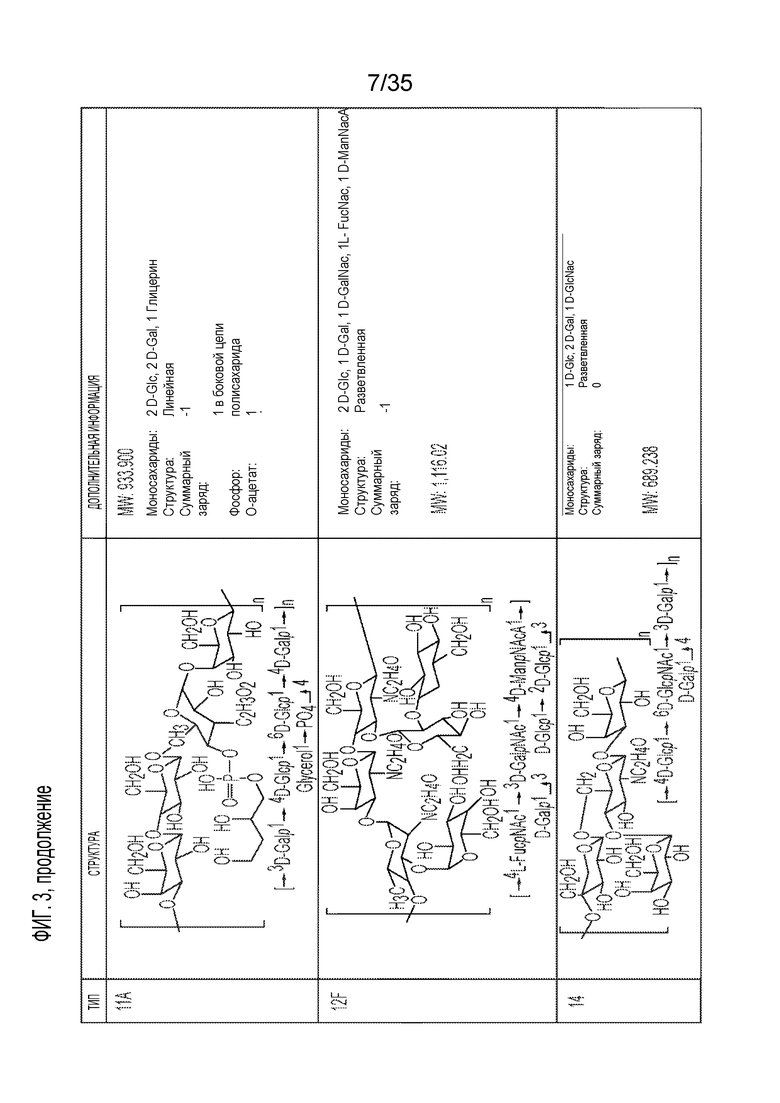


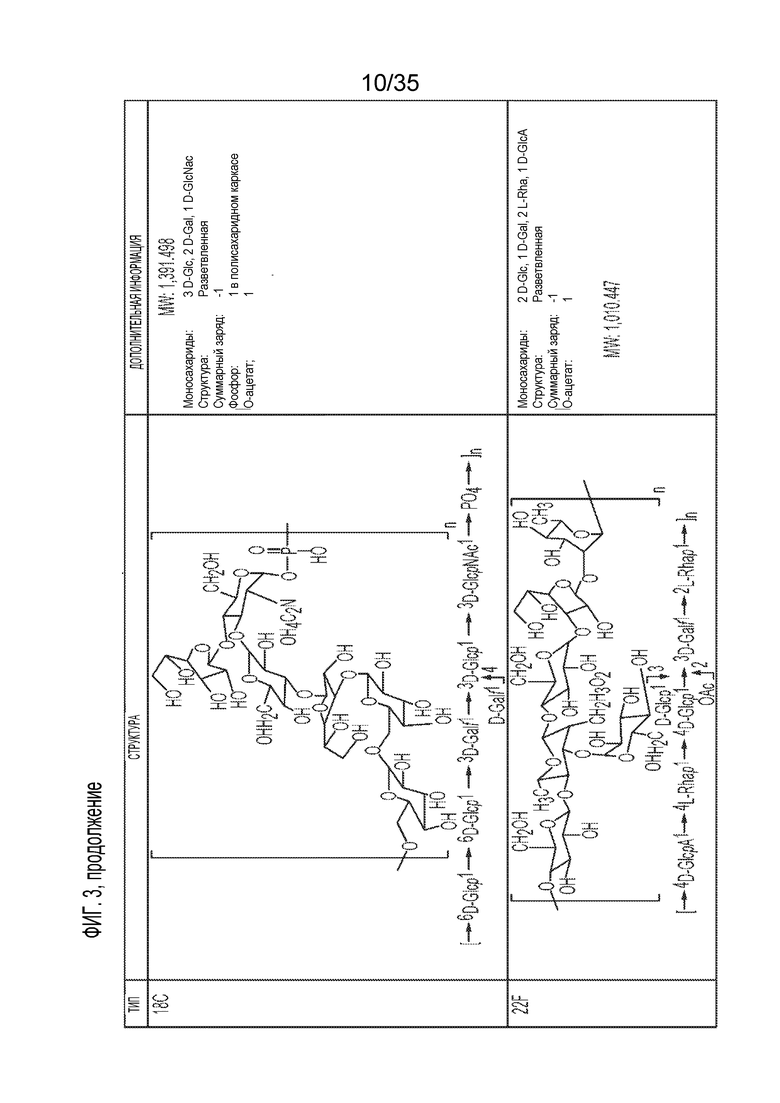
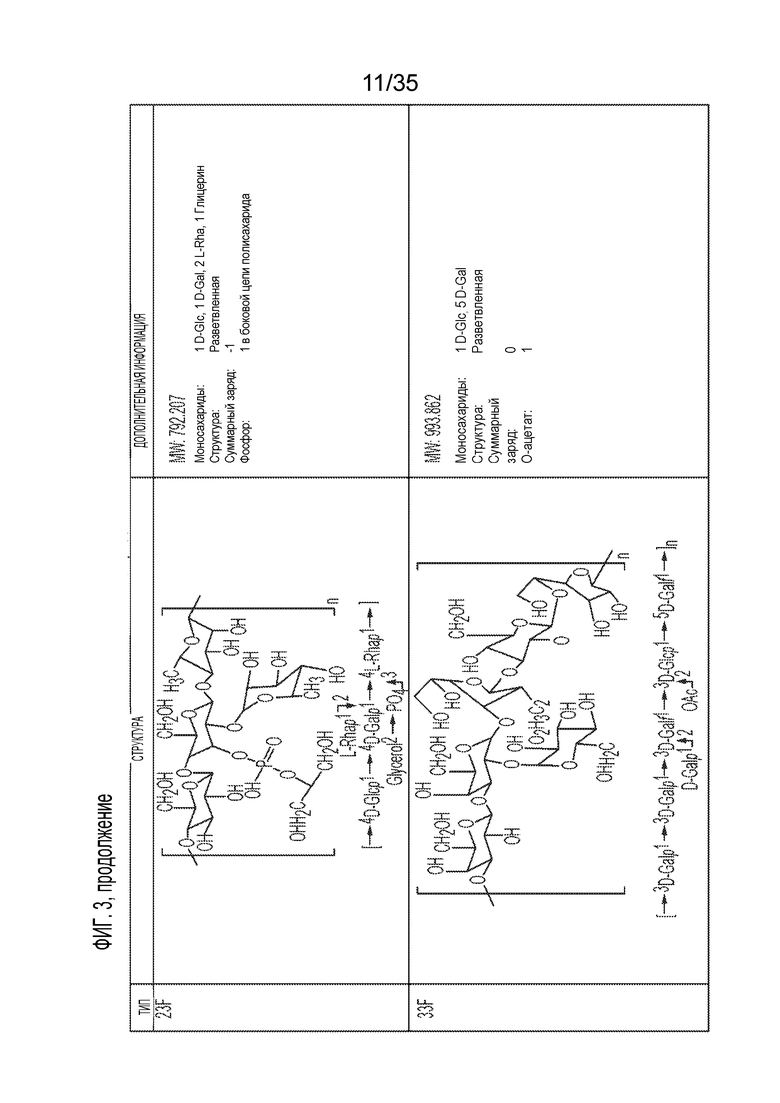
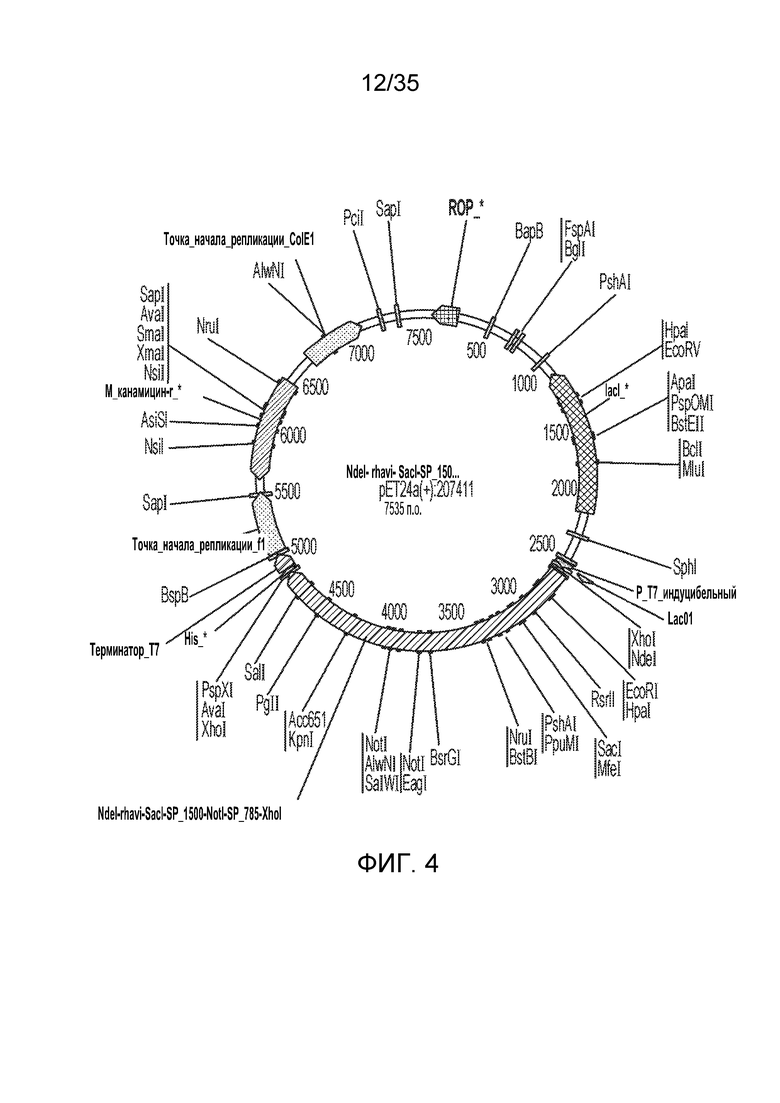
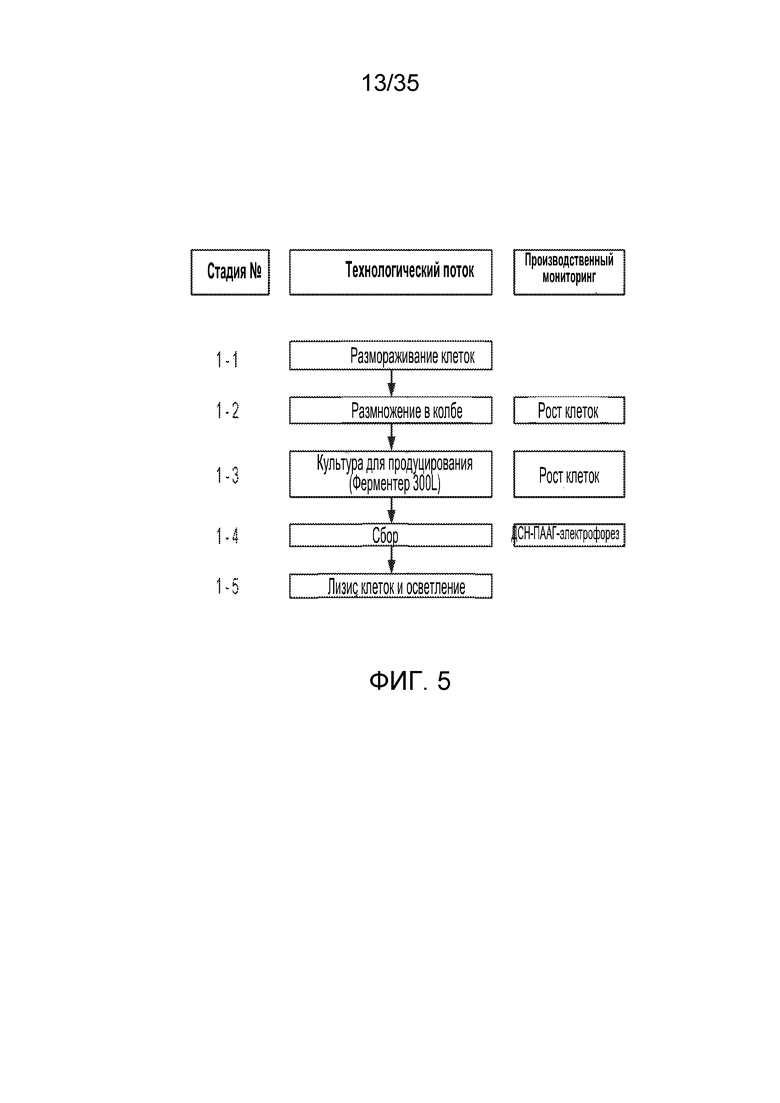
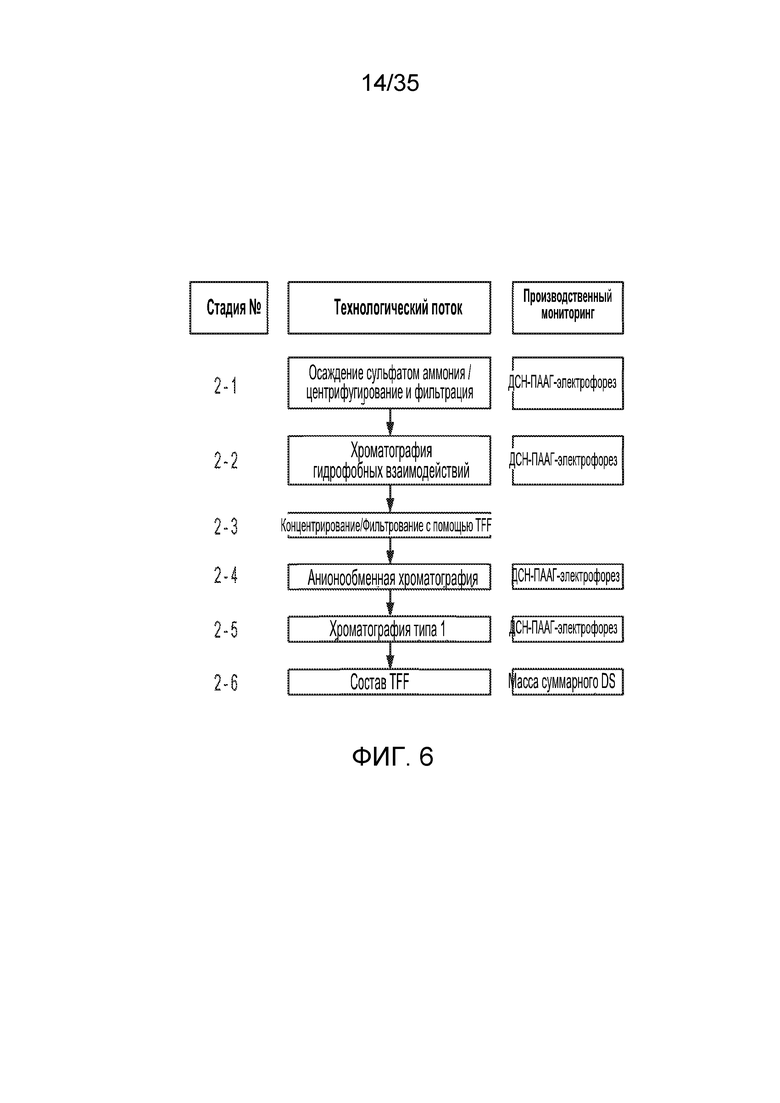
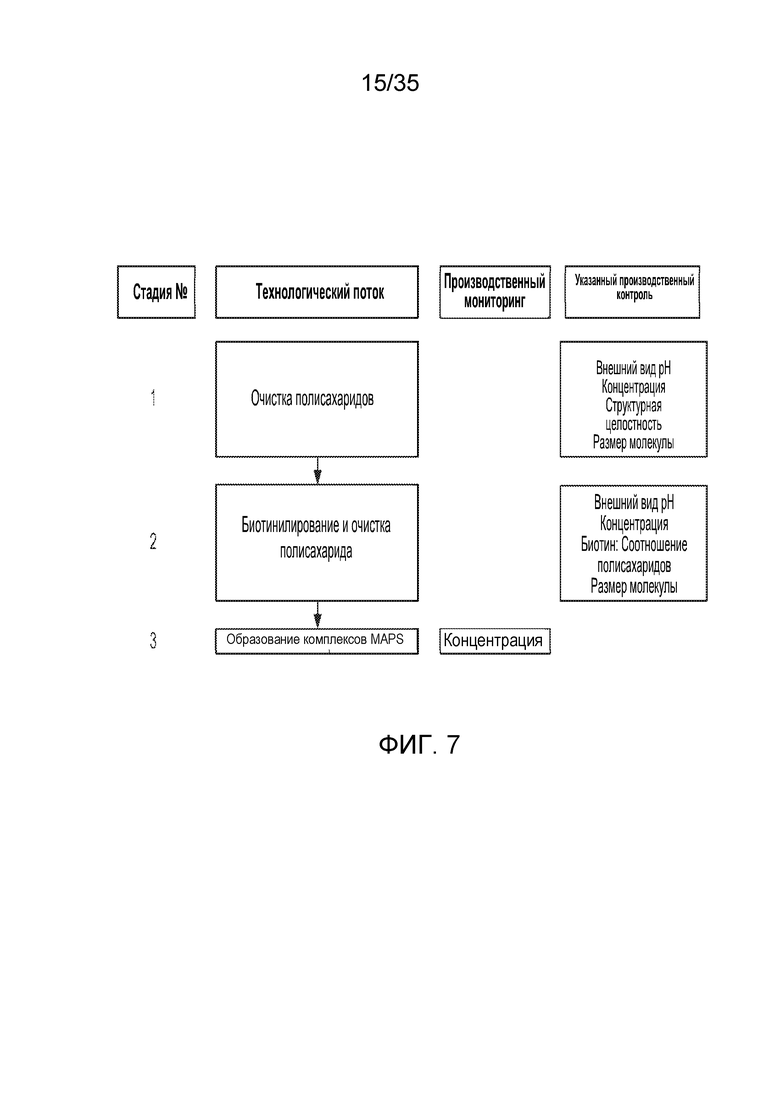
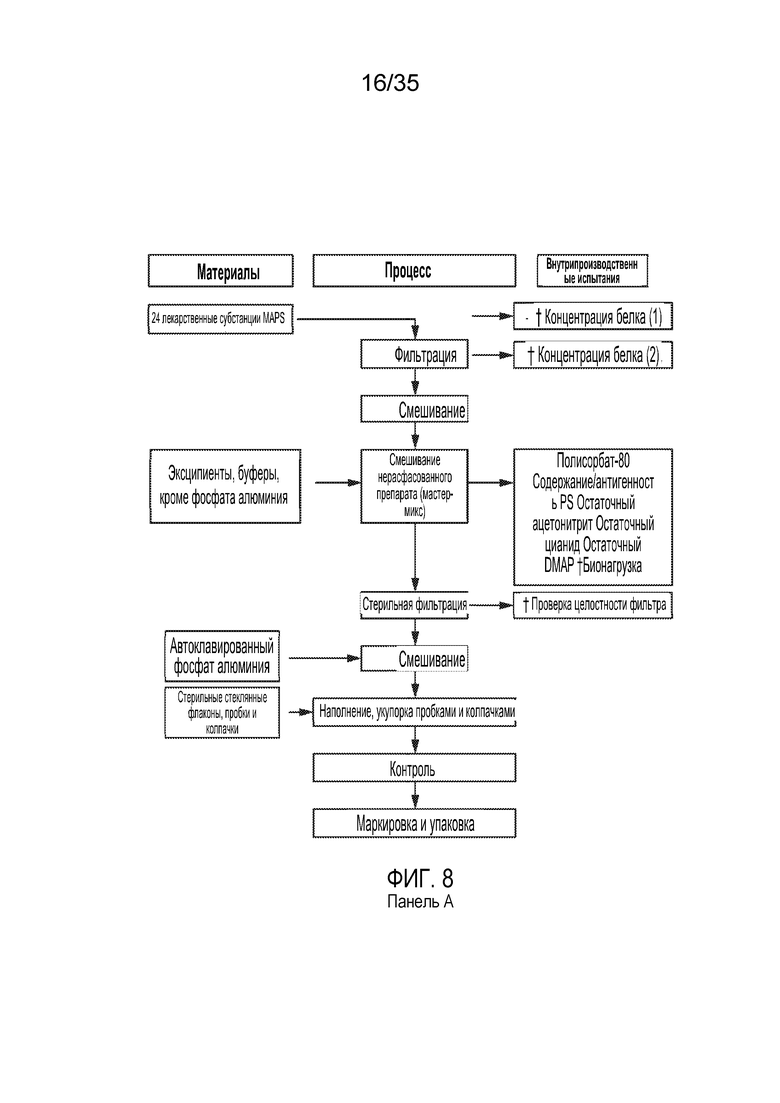
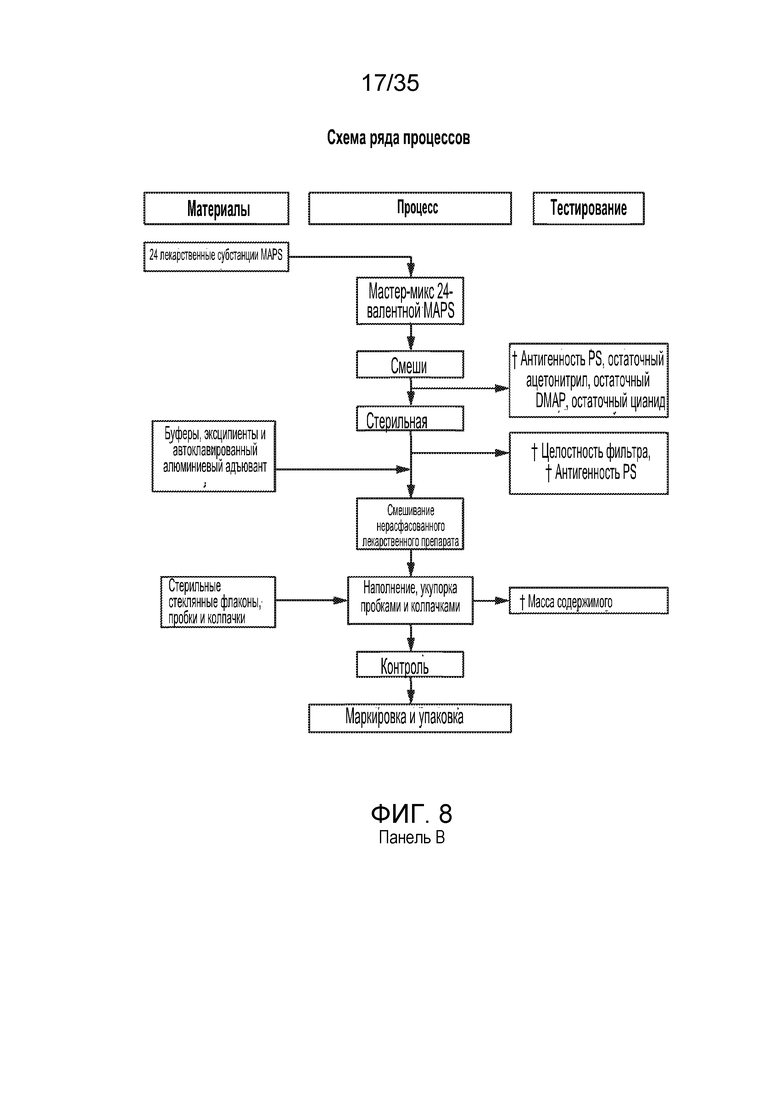

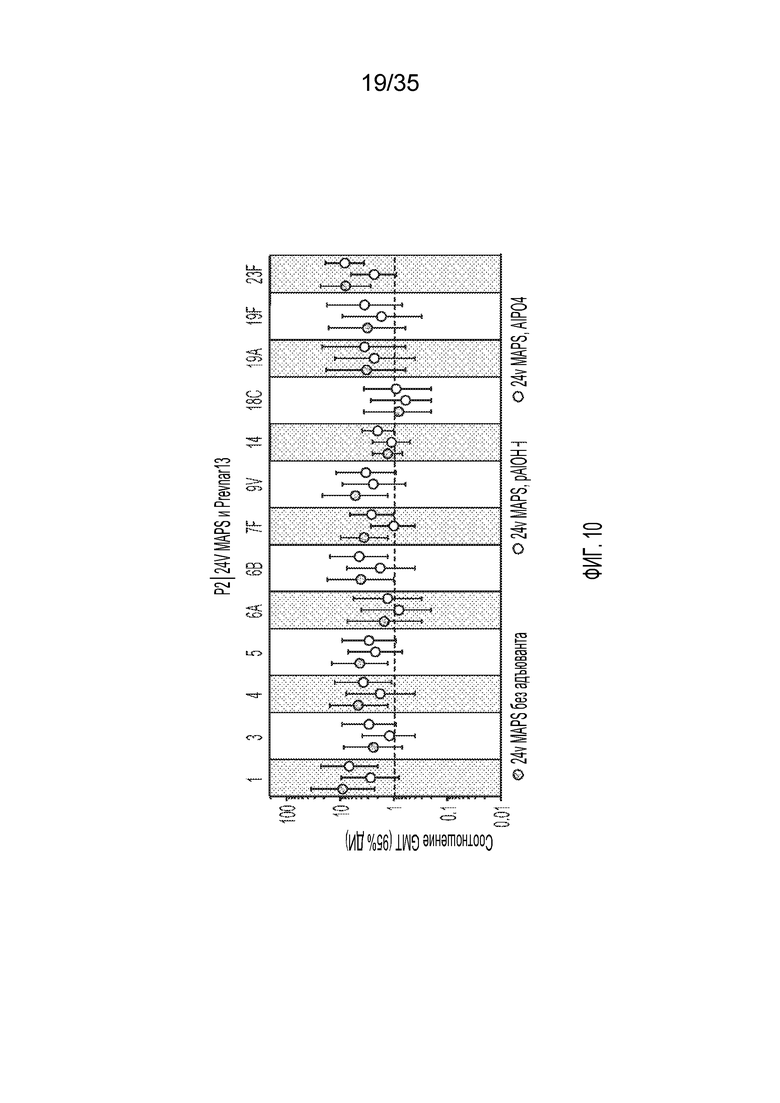
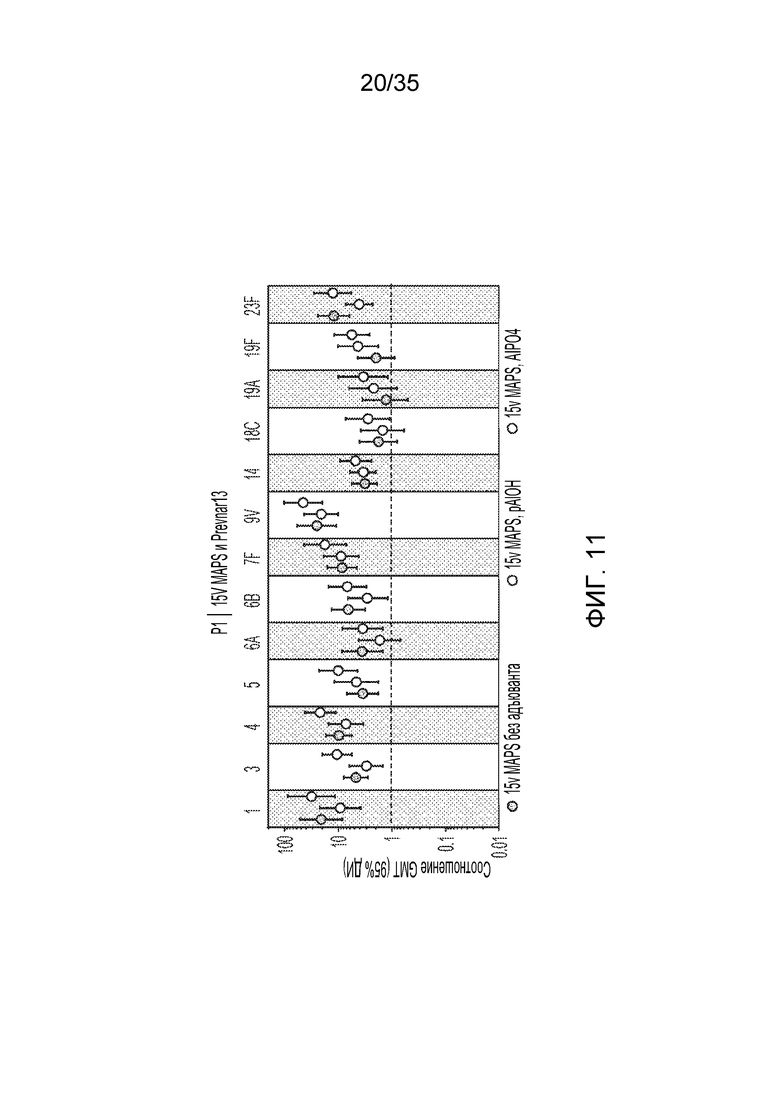

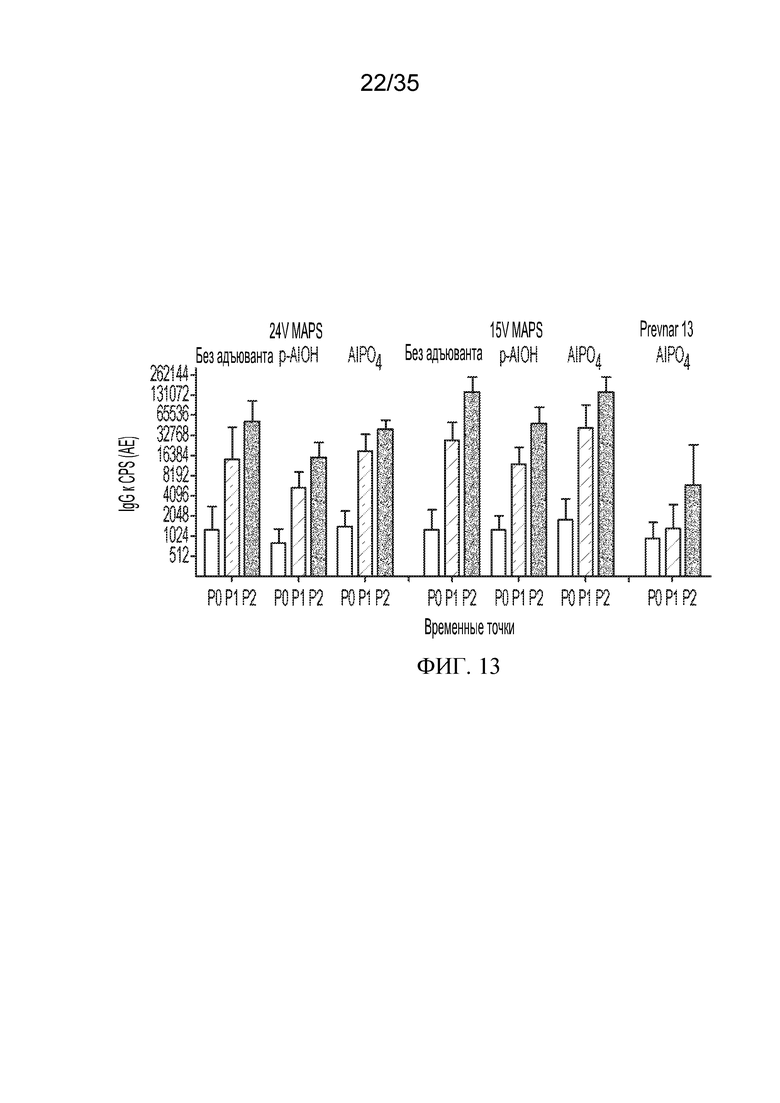
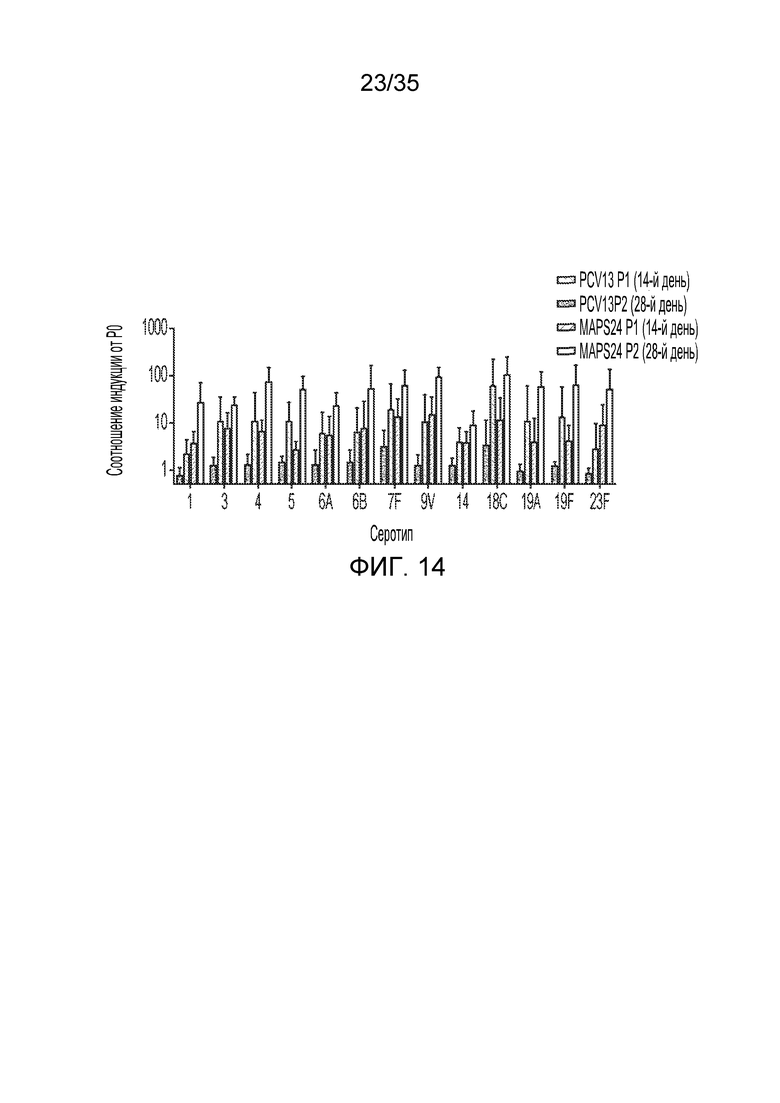
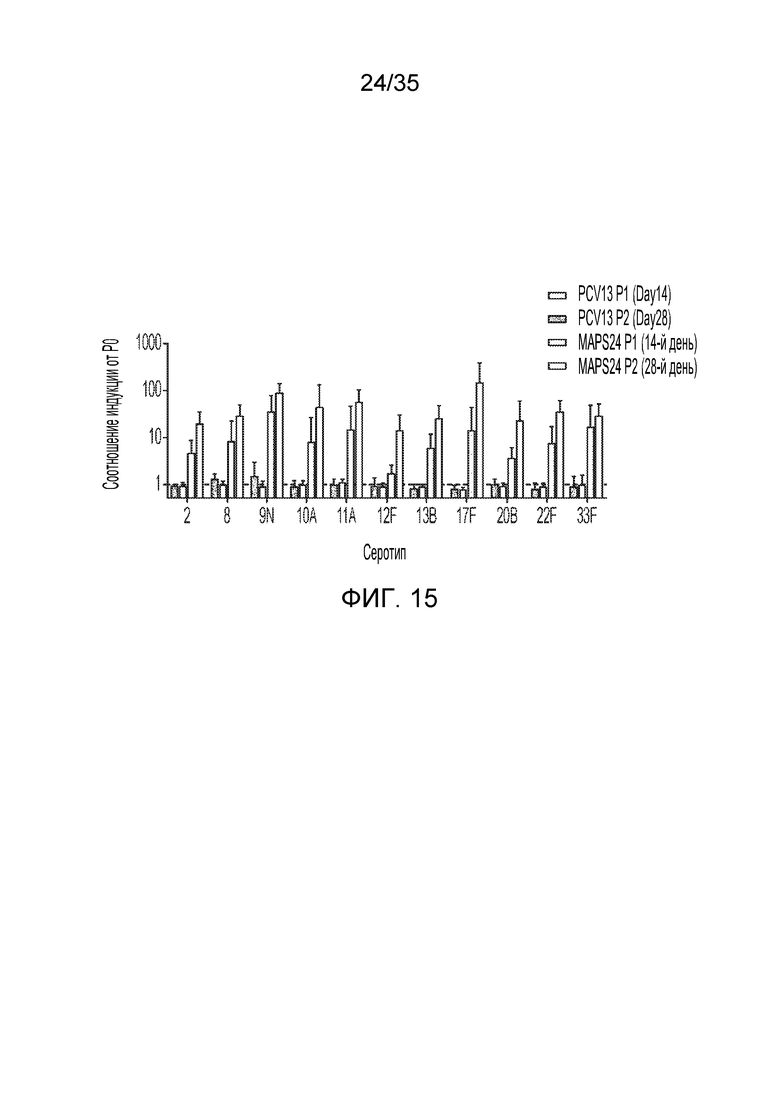
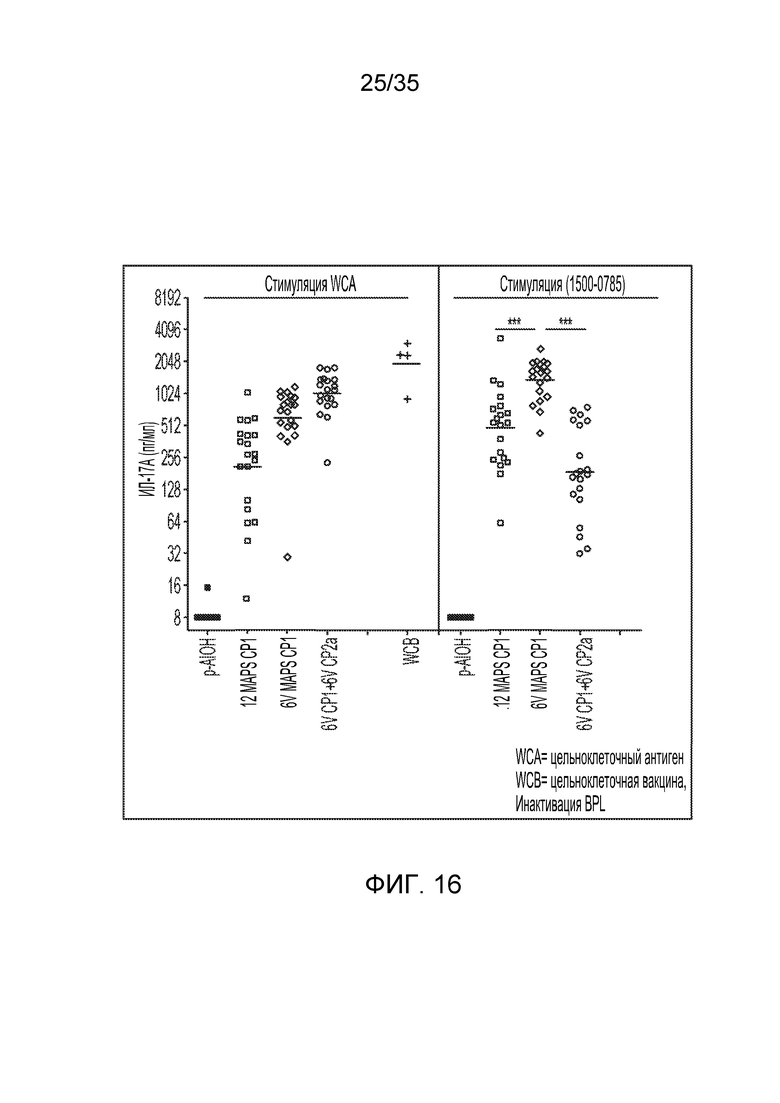
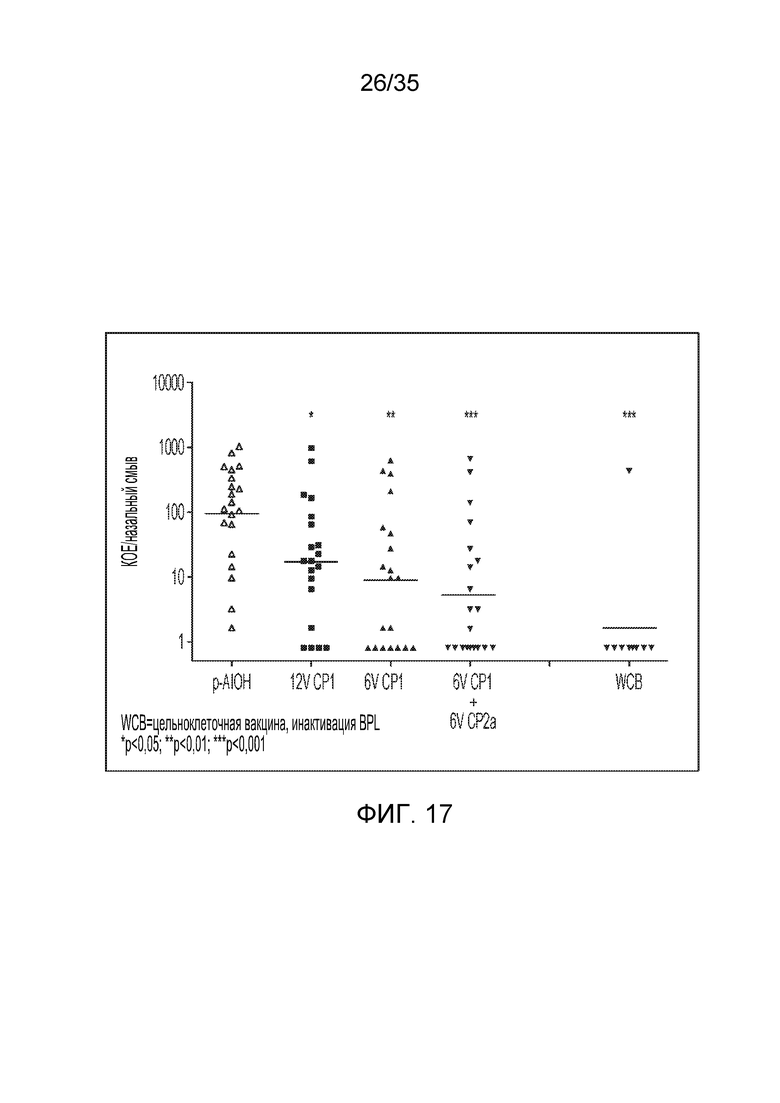
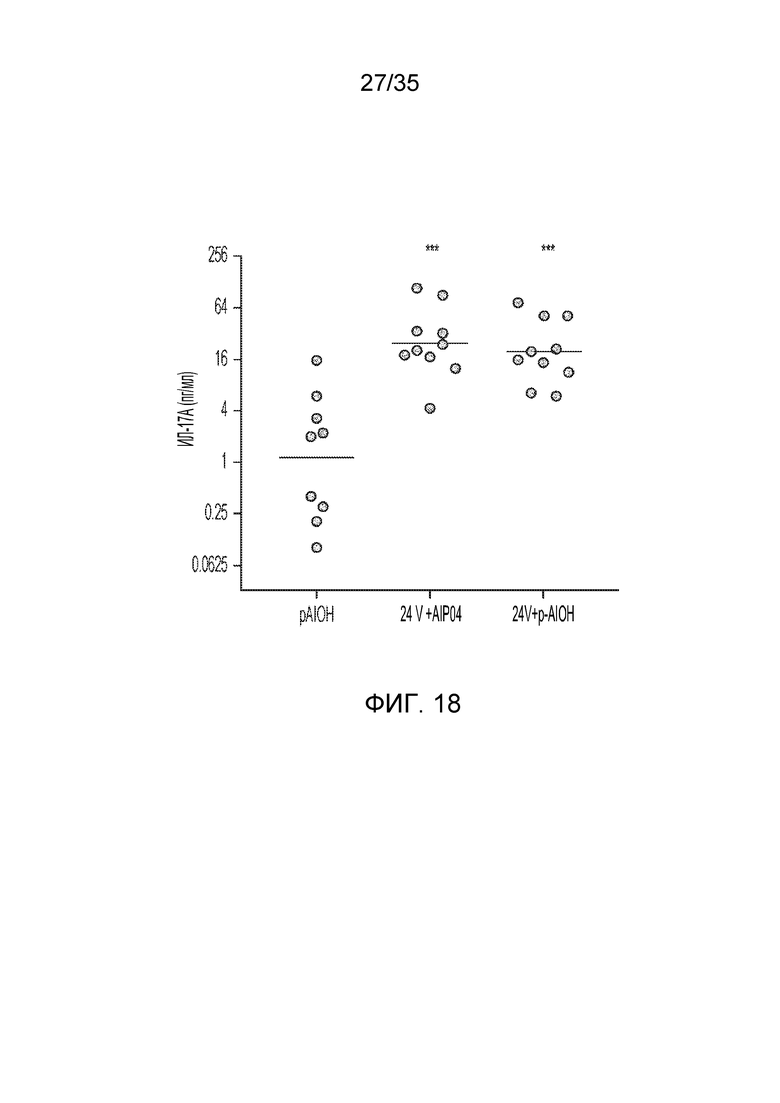
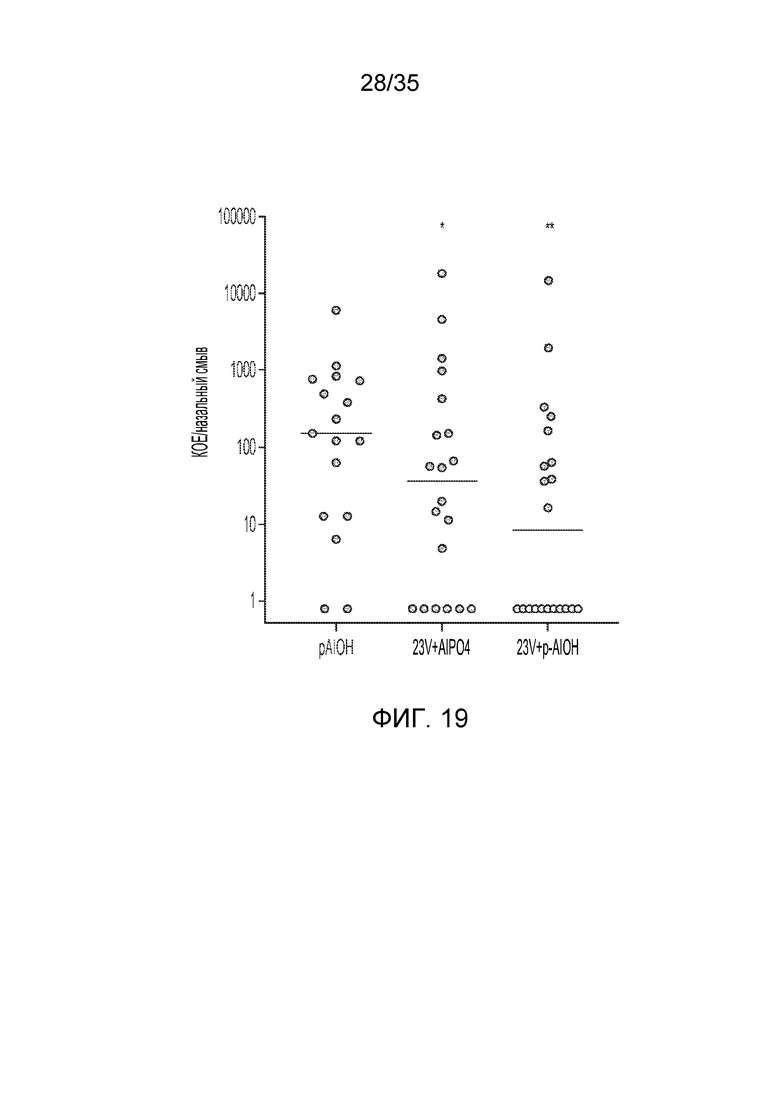
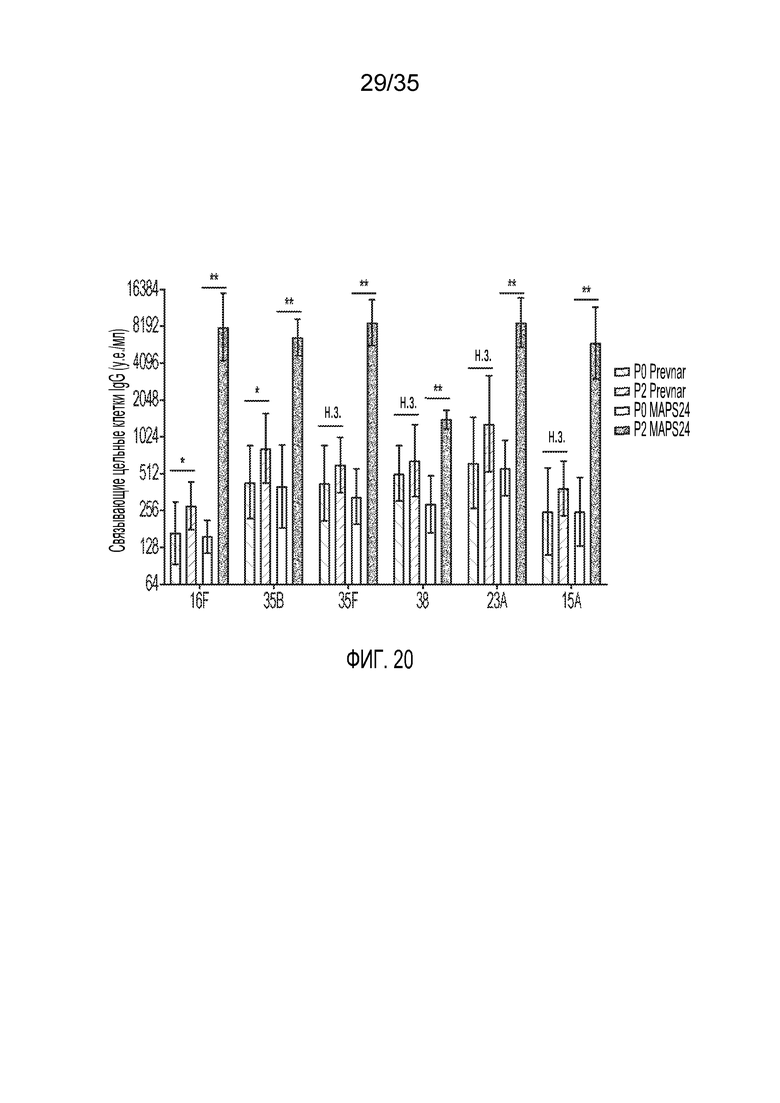
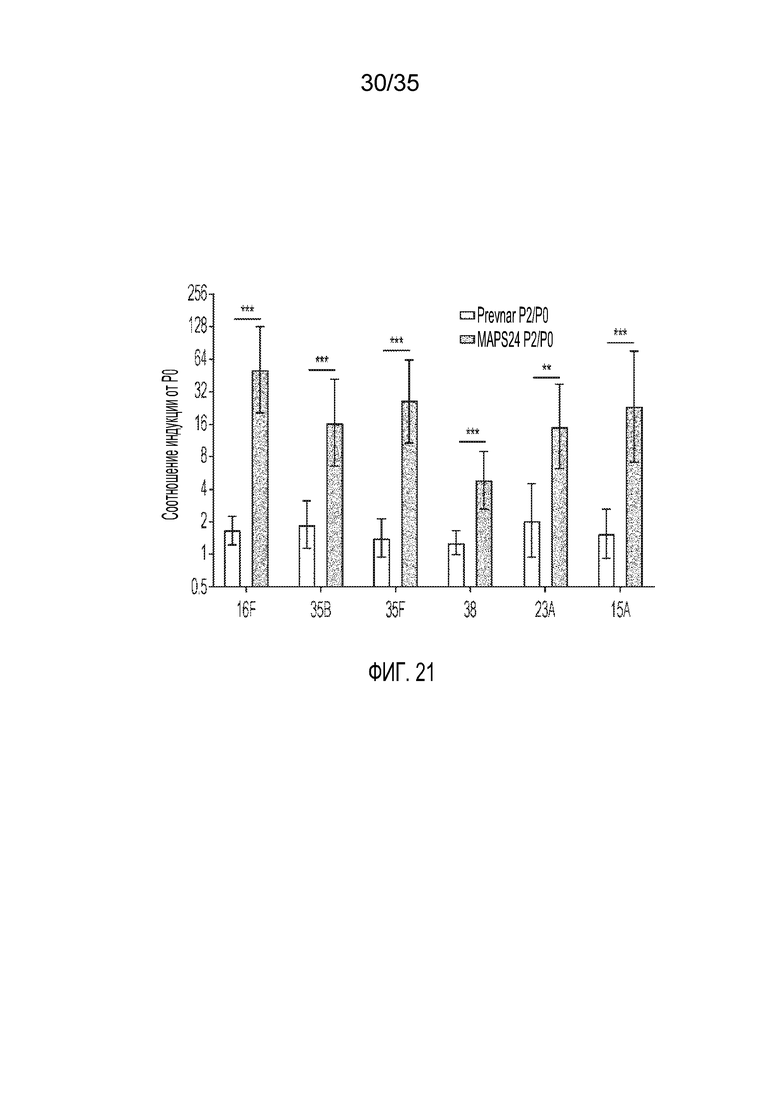
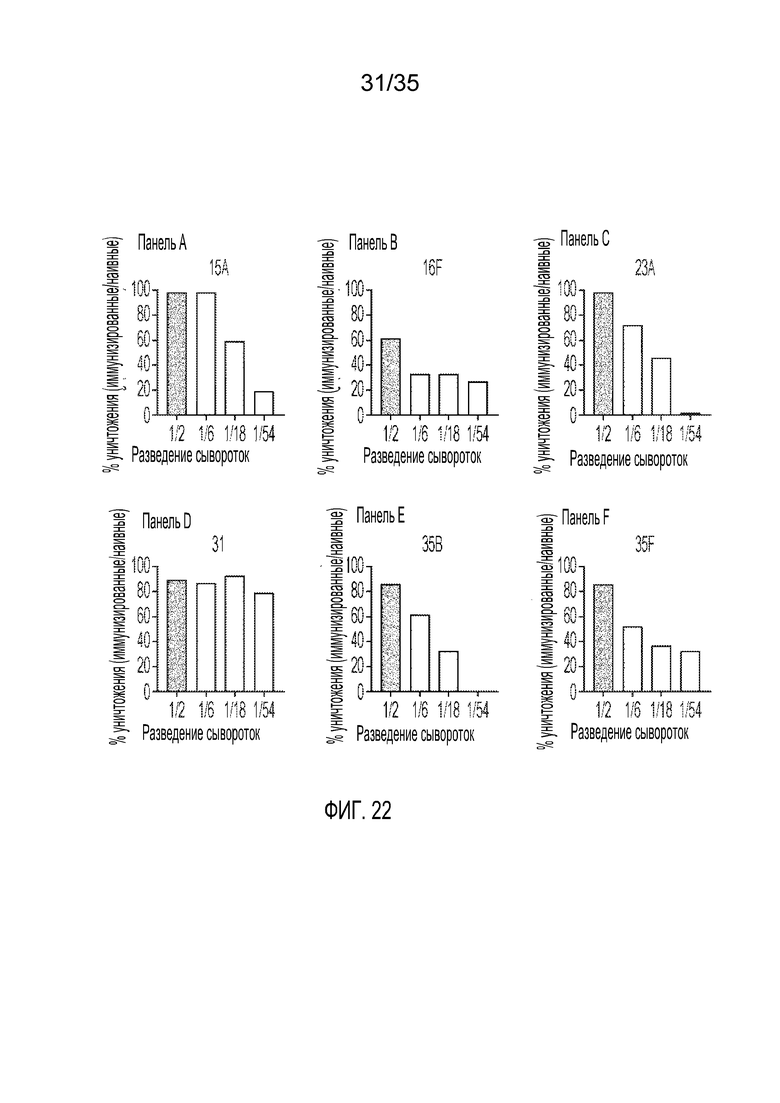


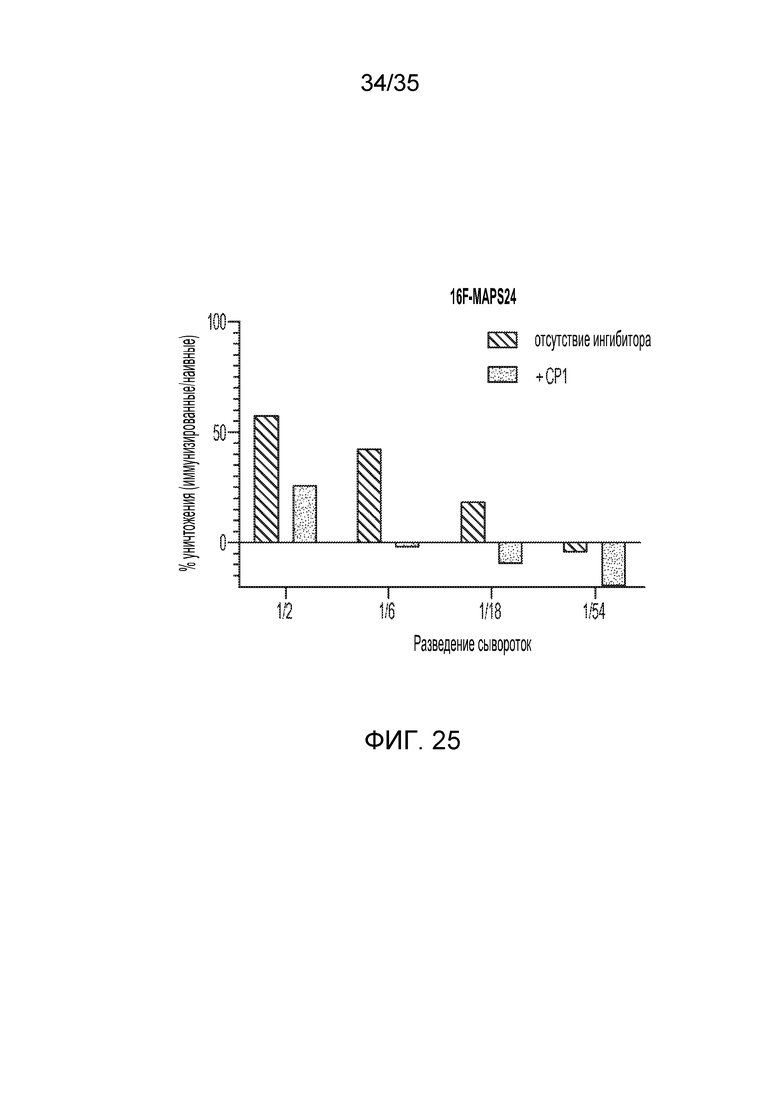
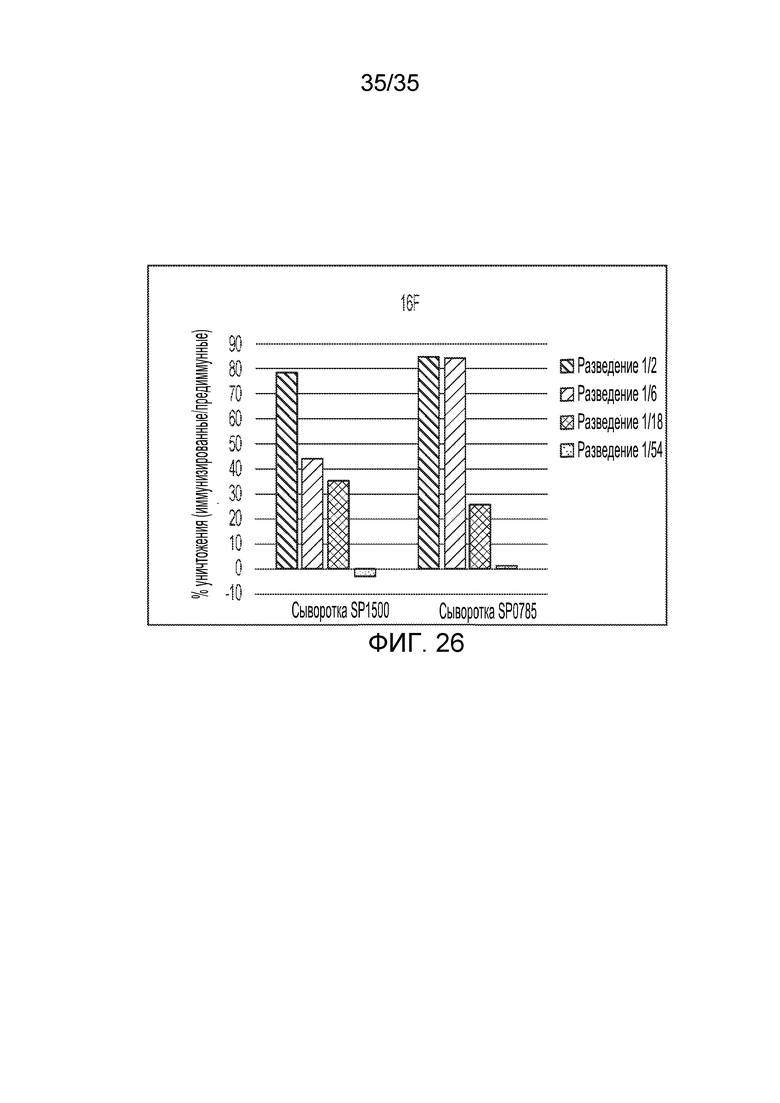
Изобретение относится к биотехнологии. Описана поливалентная вакцина, содержащая пятнадцать или более видов иммуногенных комплексов. Причем каждый из видов иммуногенных комплексов содержит: (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из отдельного серотипа Streptococcus pneumoniae; и (b) слитый белок. При этом слитый белок содержит:(i) биотинсвязывающий фрагмент; (ii) первый полипептидный антиген, содержащий полипептид SP1500 или его антигенный фрагмент; и (iii) второй полипептидный антиген, содержащий полипептид SP0785 или его антигенный фрагмент. В каждом из видов иммуногенных комплексов биотинилированный полисахаридный антиген нековалентно связан с биотинсвязывающим фрагментом слитого белка. Вакцина характеризуется тем, что после введения субъекту она вызывает иммунный ответ против Streptococcus pneumoniae. Также описана фармацевтическая композиция, содержащая указанную поливалентную вакцину и фармацевтически приемлемый носитель. Причем фармацевтическая композиция характеризуется тем, что после введения субъекту она вызывает иммунный ответ против Streptococcus pneumoniae. Раскрыт способ получения поливалентной вакцины. Способ включает смешивание пятнадцати или более видов иммуногенных комплексов в одном составе. При этом каждый вид иммуногенных комплексов включает: (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из отдельного серотипа Streptococcus pneumoniae; и (b) слитый белок. Слитый белок содержит: (i) биотинсвязывающий фрагмент; и (ii) первый полипептидный антиген, содержащий полипептид SP1500 или его антигенный фрагмент; и (iii) второй полипептидный антиген, содержащий полипептид SP0785 или его антигенный фрагмент. Причем в каждом из видов иммуногенных комплексов биотинилированный полисахаридный антиген нековалентно связан с биотинсвязывающим фрагментом слитого белка, а вакцина характеризуется тем, что после введения субъекту она вызывает иммунный ответ против Streptococcus pneumoniae. Также раскрыт способ иммунизации субъекта против инфекции и/или колонизации Streptococcus pneumoniae, включающий введение субъекту иммунологически эффективного количества поливалентной вакцины или фармацевтической композиции. Изобретение расширяет арсенал средств для борьбы с Streptococcus pneumoniae. 4 н. и 12 з.п. ф-лы, 26 ил., 6 табл., 11 пр.
1. Поливалентная вакцина, содержащая пятнадцать или более видов иммуногенных комплексов, причем каждый из видов иммуногенных комплексов содержит:
(a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из отдельного серотипа Streptococcus pneumoniae; и
(b) слитый белок, содержащий:
(i) биотинсвязывающий фрагмент;
(ii) первый полипептидный антиген, содержащий полипептид SP1500 или его антигенный фрагмент; и
(iii) второй полипептидный антиген, содержащий полипептид SP0785 или его антигенный фрагмент;
причем в каждом из видов иммуногенных комплексов биотинилированный полисахаридный антиген нековалентно связан с биотинсвязывающим фрагментом слитого белка;
причем вакцина характеризуется тем, что после введения субъекту она вызывает иммунный ответ против Streptococcus pneumoniae.
2. Поливалентная вакцина по п. 1, в которой серотип Streptococcus pneumoniae полисахаридного антигена для каждого из видов иммуногенных комплексов независимо выбран из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F и 48.
3. Поливалентная вакцина по п. 1 или 2, в которой серотип Streptococcus pneumoniae полисахаридного антигена для каждого из видов иммуногенных комплексов независимо выбран из 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20B, 22F, 23F и 33F.
4. Поливалентная вакцина по любому из пп. 1-3, отличающаяся тем, что (i) полипептид SP1500 или его антигенный фрагмент каждого из видов иммуногенных комплексов представляет собой или содержит аминокислотную последовательность по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или по меньшей мере на 99,5% идентичную SEQ ID NO: 5; или (ii) полипептид SP1500 или его антигенный фрагмент каждого из видов иммуногенных комплексов представляет собой или содержит аминокислотную последовательность SEQ ID NO: 5.
5. Поливалентная вакцина по любому из пп. 1-4, отличающаяся тем, что (i) полипептид SP0785 или его антигенный фрагмент каждого из видов иммуногенных комплексов представляет собой или содержит аминокислотную последовательность по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или по меньшей мере на 99,5% идентичную SEQ ID NO: 4; или (ii) полипептид SP0785 или его антигенный фрагмент каждого из видов иммуногенных комплексов представляет собой или содержит аминокислотную последовательность SEQ ID NO: 4.
6. Поливалентная вакцина по любому из пп. 1-5, содержащая двадцать четыре или более видов иммуногенных комплексов.
7. Поливалентная вакцина по п. 6, содержащая:
первый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 1, и (b) слитый белок;
второй иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 2, и (b) слитый белок;
третий иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 3, и (b) слитый белок;
четвертый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 4, и (b) слитый белок;
пятый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 5, и (b) слитый белок;
шестой иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 6А, и (b) слитый белок;
седьмой иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 6B, и (b) слитый белок;
восьмой иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 7F, и (b) слитый белок;
девятый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 8, и (b) слитый белок;
десятый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 9N, и (b) слитый белок;
одиннадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 9V, и (b) слитый белок;
двенадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 10A, и (b) слитый белок;
тринадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 11A, и (b) слитый белок;
четырнадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 12F, и (b) слитый белок;
пятнадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 14, и (b) слитый белок;
шестнадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 15B, и (b) слитый белок;
семнадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 17F, и (b) слитый белок;
восемнадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 18C, и (b) слитый белок;
девятнадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 19A, и (b) слитый белок;
двадцатый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 19F, и (b) слитый белок;
двадцать первый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 20B, и (b) слитый белок;
двадцать второй иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 22F, и (b) слитый белок;
двадцать третий иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 23F, и (b) слитый белок; и
двадцать четвертый иммуногенный комплекс, содержащий (a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из Streptococcus pneumoniae серотипа 33F, и (b) слитый белок;
причем каждый слитый белок содержит
(a) биотинсвязывающий фрагмент;
(b) первый полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 5 или его антигенному фрагменту; и
(c) второй полипептидный антиген, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 4, или его антигенный фрагмент;
и причем в каждом из иммуногенных комплексов, биотинилированный полисахаридный антиген нековалентно связан с биотинсвязывающим фрагментом слитого белка.
8. Поливалентная вакцина по любому из пп. 1-7, в которой биотинсвязывающий фрагмент каждого из видов иммуногенных комплексов представляет собой (i) полипептид, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 1 или его биотинсвязывающему фрагменту; (ii) или полипептид, содержащий аминокислотную последовательность, которая на по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на по меньшей мере 99,5% идентична SEQ ID NO: 2 или его биотинсвязывающему фрагменту; или (iii) полипептид, содержащий аминокислотную последовательность SEQ ID NO: 1 или аминокислотную последовательность SEQ ID NO: 2.
9. Поливалентная вакцина по любому из пп. 1-8, в которой слитый белок каждого из видов иммуногенных комплексов представляет собой или содержит аминокислотную последовательность по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или по меньшей мере на 99,5% идентичную SEQ ID NO: 6; или (ii) слитый белок каждого из видов иммуногенных комплексов представляет собой или содержит аминокислотную последовательность SEQ ID NO: 6.
10. Фармацевтическая композиция, содержащая поливалентную вакцину по любому из пп. 1-9 и фармацевтически приемлемый носитель, причем фармацевтическая композиция характеризуется тем, что после введения субъекту она вызывает иммунный ответ против Streptococcus pneumoniae.
11. Фармацевтическая композиция по п. 10, дополнительно содержащая один или более адъювантов.
12. Фармацевтическая композиция по п. 11, в которой один или более адъювантов выбраны из группы, состоящей из фосфата алюминия, гидроксида алюминия и фосфатированного гидроксида алюминия.
13. Способ получения поливалентной вакцины, включающий смешивание пятнадцати или более видов иммуногенных комплексов в одном составе, где каждый вид иммуногенных комплексов включает:
(a) биотинилированный полисахаридный антиген, содержащий биотин и полисахаридный антиген из отдельного серотипа Streptococcus pneumoniae; и
(b) слитый белок, содержащий:
(i) биотинсвязывающий фрагмент; и
(ii) первый полипептидный антиген, содержащий полипептид SP1500 или его антигенный фрагмент; и
(iii) второй полипептидный антиген, содержащий полипептид SP0785 или его антигенный фрагмент;
причем в каждом из видов иммуногенных комплексов биотинилированный полисахаридный антиген нековалентно связан с биотинсвязывающим фрагментом слитого белка; и
причем вакцина характеризуется тем, что после введения субъекту она вызывает иммунный ответ против Streptococcus pneumoniae.
14. Способ по п. 13, в котором серотип Streptococcus pneumoniae полисахаридного антигена для каждого из видов иммуногенных комплексов независимо выбран из 1, 2, 3, 4, 5, 6A, 6B, 6C, 6D, 6E, 6F, 6G, 6H, 7A, 7B, 7C, 7F, 8, 9A, 9L, 9N, 9V, 10A, 10B, 10C, 10F, 11A, 11B, 11C, 11D, 11E, 11F, 12A, 12B, 12F, 13, 14, 15A, 15B, 15C, 15F, 16A, 16F, 17A, 17F, 18A, 18B, 18C, 18F, 19A, 19B, 19C, 19F, 20A, 20B, 21, 22A, 22F, 23A, 23B, 23F, 24A, 24B, 24F, 25A, 25F, 27, 28A, 28F, 29, 31, 32A, 32F, 33A, 33B, 33C, 33D, 33E, 33F, 34, 35A, 35B, 35C, 35F, 36, 37, 38, 39, 40, 41A, 41F, 42, 43, 44, 45, 46, 47A, 47F и 48.
15. Способ иммунизации субъекта против инфекции и/или колонизации Streptococcus pneumoniae, включающий введение субъекту иммунологически эффективного количества поливалентной вакцины по любому из пп. 1-9 или фармацевтической композиции по любому из пп. 10-12.
16. Способ по п. 15, включающий введение субъекту одной или более доз поливалентной вакины, необязательно, включающий две или три дозы поливалентной вакцины.
| WO 2014124228 A1, 14.08.2014 | |||
| Машина для резки лоскута, бумажных обрезков и т.п. | 1927 |
|
SU19907A1 |
| Прибор для изготовления халвы | 1928 |
|
SU19904A1 |
Авторы
Даты
2024-03-14—Публикация
2019-09-12—Подача