Изобретение относится к области химических источников тока к экологичным способам получения функциональных композитных материалов, в частности к способу нанесения наночастиц платины на углеродные или композитные носители, и может быть использовано в качестве электрокатализаторов на аноде и катоде топливных элементов с протонообменной мембраной и электролизеров.
Токообразующие реакции в топливных элементах и электролизерах протекают на поверхности наночастиц металлов - электрокатализаторов. Наилучшими электрокатализаторами для анода и катода топливных элементов с протонообменной мембраной и катода электролизеров являются композиционные материалы, состоящие из наночастиц платины (НЧ), нанесенных на поверхность электропроводного графитизированного материала-носителя, обладающего развитой поверхностью. Электрокатализатор должен сочетать высокую площадь активной поверхности, повышенную активность в токообразующих реакциях, таких как восстановление кислорода, окисление метанола, окисления водорода и достаточную коррозионно-морфологическую стабильность в процессе работы.
Увеличение удельной площади поверхности катализатора и увеличение мощностных характеристик может быть достигнуто путем уменьшения размеров наночастиц платины и повышения равномерного распределения их по поверхности носителя (равноудаленность друг от друга). Равномерное распределение и закрепление наночастиц платины на поверхности носителя снижает эффект деградации, а также благоприятно сказывается на кинетике процесса, облегчая эффективный подвод реагентов и отвод продуктов реакции из реакционной зоны.
Известно, что увеличение удельной площади поверхности платины может привести к понижению удельной каталитической активности катализатора, поэтому существование оптимального размера наночастиц является дискуссионным вопросом (Hubert A. Gasteiger, Shyam S. Kocha, Bhaskar Sompalli, Frederick T. Wagner, Activitybenchmarksandrequirements for Pt, Pt-alloy, andnon -Ptoxygenreductioncatalysts for PEMFCs, Applied Catalysis B: Environmental 56, 2005, 9-35). Исследование ряда литературных источников демонстрирует наличие оптимального размерного диапазона наноастиц от 1.5 до 5 нм (Garlyyev, В., Kratzl, K.,  Fichtner, J., Macak, J., Fischer, R. (2019). Optimizing the size of platinum nanoparticles for enhanced oxygen electro-reduction mass activity. Angewandte Chemie International Edition, doi:10.1002/anie. 201904492). Также известно, что активность и стабильность антибатно зависят от размера наночастиц платины (Гутерман В.Е., Беленое С.В., Алексеенко А.А., Табачкова Н.Ю., Волочаев В.А., О связи активности и стабильности нанесенных платиноуглеродных электрокатализаторов, Электрохимия, 2017, т. 53, №5, с. 602-610), а катализаторы с размером наночастиц около 2 нм и их упорядоченным распределением по поверхности углеродного носителя такие же стабильные, как и материалы с размером наночастиц около 3 и 4 нм (Paperzh, K. О.; Alekseenko, A. A.; Volochaev, V. A.; Pankov, I. V.; Safronenko, О. A.; Guterman, V. Е. Beilstein J. Nanotechnol. 2021, 12, 593-606. doi: 10.3762/bjnano. 12.49). Таким образом, создание электрокатализаторов с заданными структурно-морфологическими характеристиками для оптимального сочетания стабильности и активности является актуальной задачей водородной энергетики.
Fichtner, J., Macak, J., Fischer, R. (2019). Optimizing the size of platinum nanoparticles for enhanced oxygen electro-reduction mass activity. Angewandte Chemie International Edition, doi:10.1002/anie. 201904492). Также известно, что активность и стабильность антибатно зависят от размера наночастиц платины (Гутерман В.Е., Беленое С.В., Алексеенко А.А., Табачкова Н.Ю., Волочаев В.А., О связи активности и стабильности нанесенных платиноуглеродных электрокатализаторов, Электрохимия, 2017, т. 53, №5, с. 602-610), а катализаторы с размером наночастиц около 2 нм и их упорядоченным распределением по поверхности углеродного носителя такие же стабильные, как и материалы с размером наночастиц около 3 и 4 нм (Paperzh, K. О.; Alekseenko, A. A.; Volochaev, V. A.; Pankov, I. V.; Safronenko, О. A.; Guterman, V. Е. Beilstein J. Nanotechnol. 2021, 12, 593-606. doi: 10.3762/bjnano. 12.49). Таким образом, создание электрокатализаторов с заданными структурно-морфологическими характеристиками для оптимального сочетания стабильности и активности является актуальной задачей водородной энергетики.
В качестве материалов-носителей НЧ платины часто применяются порошки мелкодисперсного углеродного (сажа, нанотрубки, нановолокна, графен и др.) или неуглеродного электронопроводящего носителя, которые обладают удельной площадью поверхности более 60 м2/г и высокой электронной проводимостью (Thompsett D. // Catalysts for the Proton Exchange Membrane Fuel Cell, in: Handbook of Fuel Cells. Fundamentals, Technology and Applications. Editors: Vielstich W., Lamm A., Gasteiger H.A. Sohn, Wiley & Sons Ltd., New York, USA, 2003. Vol. 3. P. 6-1-6-23).
Существуют два принципиальных подхода к формированию наноструктур. Первый подход - «сверху-вниз» заключается в разрушении крупных частиц и реализуется, например, в процессах механохимического измельчения, ультразвуковой обработки, высокодозных облучений, электрохимического диспергирования (Смирнова, Н.В. Структурные и электрокаталитические свойства катализаторов Pt/C и Pt-Ni/C, полученных методом электрохимического диспергирования / Н.В. Смирнова, А.Б. Куриганова, Д.В. Леонтьева, И.Н. Леонтьев, А.С. Михейкин // Кинетика и катализ. - 2013. - Т. 54. -№2. - С. 262-275).
Недостатком данных способов, а также способов, описанных в патентах RU 2424850, 2678438, 2660900, является получение материалов, содержащих разноразмерные и зачастую крупные частицы (в одном образе содержание наночастиц размером от 5 до 25 нм), что свидетельствует о нерациональном использовании дорогостоящей платины в электрокатализаторе.
Второй путь - получение наноструктурных катализаторов реализуется «снизу-вверх» и заключается в «сборке» наночастиц из отдельных атомов и молекул (Schroder, J.; Neumann, S.; Quinson, J.; Arenz, M.; Kunz, S. Anion Dependent Particle Size Controlof Platinum Nanoparticles Synthesizedin Ethylene Glycol. Na-nomateri als 2021, 11, 2092. https://doi.ore/10.3390/nano 11082092). К такому способу получения наночастиц платины (металлов) относятся методы химического осаждения, карботермическое восстановление прекурсоров (метод пропитки), коллоидный способ (микроэмульсионный) и др. (Coutanceau, С., Baranton, S., & Nappor, Т. W. (2012). Platinum Fuel Cell Nanoparticle Syntheses: Effect on Morphology, Structure and Electrocatalytic Behavior. The Delivery of Nanoparticles. doi:10.5772/18179; Quinson, J., & Jensen, K. M. ∅. (2020). From platinum atoms in molecules to colloidal nanoparticles: A review on reduction, nucleation and growth mechanisms. Advancesin Colloidand Interface Science, 102300. doi:10.1016/j.cis.2020.102300). Большинство из этих методов синтеза позволяют получать материалы на основе наночастиц размером менее 5 нм и узкой дисперсией по размеру.
Наиболее широко для получения Pt/C электрокатализаторов применяются химические способы синтеза в жидкой фазе, каждый из которых имеет свои достоинства и недостатки (Quinson, J., &Jensen, K. М. ∅. (2020). From platinum atoms in molecules to colloidal nanoparticles: A review on reduction, nucleation and growth mechanisms. Advances in Colloid and Interface Science, 102300. doi: 10.1016/j.cis.2020.102300).
Оптимальный способ (условия) жидкофазного синтеза подбирают в зависимости от требований к структуре получаемого материала, в первую очередь - к размеру наночастиц платины. К сожалению, многие способы дают результат, конкретный с точки зрения достижения определенных структурных характеристик (форма, размер и размерное распределение наночастиц), но не позволяющий управлять этими характеристиками.
Для регулирования размера частиц в процессе жидкофазного восстановления платиносодержащих соединений в реакционную смесь добавляют поверхностно-активные вещества (ПАВ), которые сорбируются на поверхности частиц платины и предотвращают их дальнейший рост и агрегацию (JIANG, Q., PENG, Z., XIE, X., DU, K., HU, G., & LIU, Y. (2011). Preparation of high active Pt/C cathode electrocatalyst for direct methanol fuel cell by citrate-stabilized method. Transactions of Nonferrous Metals Society of China, 21(1), 127-132. doi:10.1016/sl003-6326(11)60688-2; Coutanceau, C., Baranton, S., &Nappor, T. W. (2012). Platinum Fuel Cell Nanoparticle Syntheses: Effect on Morphology, Structure and Electrocatalytic Behavior. TheDeliveryofNanoparticles. doi:10.5772/18179). В ряде случаев такими веществом может служить сам растворитель, например, этиленгликоль или глицерин - «полиольный» метод (Qi J., Jiang L.H., Jing M. Y. etal. Preparation of Pt/C via a polyol process - Investigation on carbon support adding sequence//Int. J. of hydrogen energy. 2011. V. 36. P. 10490-10501; Fang, В., Chaudhari, N. K, Kim, M.S., Kim, J. H, & Yu, J.-S. (2009). Homogeneous Deposition of Platinum Nanoparticles on Carbon Black for Proton Exchange Membrane Fuel Cell. JournaloftheAmericanChemicalSociety, 131(42), 15330-15338. doi: 10.1021/ja905749e). Так, в процессе полиольного синтеза, ионы, содержащие платину, восстанавливаются, образуя наночастицы, а этиленгликоль, окисляясь, превращается в гликолевую кислоту, находящуюся в растворе в депро-тонированной форме. Адсорбируясь на поверхности частиц металла, она действует как стабилизирующий агент, предотвращающий коалесценцию наночастиц (Fang, В., Chaudhari, N. K., Kim, M.S., Kim, J. H, &Yu, J.S. (2009). Homogeneous Deposition of Platinum Nanoparticles on Carbon Black for Proton Exchange Membrane Fuel Cell. Journal of the American Chemical Society, 131(42), 15330-15338. doi:10.1021/ja905749e). Вработе Quinson, J., Inaba, M., Neumann, S., Swane, A. A., Bucher, J., Simonsen, S. В., Arenz, M. (2018). Investigating Particle Size Effects in Catalysis by Applying a Size-Controlled and Surfactant-Free Synthesis of Colloidal Nanoparticles in Alkaline Ethylene Glycol: Case Study of the Oxygen Reduction Reaction on Pt. ACS Catalysis, 8(7), 6627-6635. doi:10.1021/acscatal. 8b00694 отмечено, что, изменяя pH раствора перед началом полиольного синтеза (соотношение количеств щелочи и прекурсора платины), можно регулировать размер получаемых наночастиц металла.
Известным классическим методом получения платиносодержащих катализаторов с использованием ПАВ является метод Беннемана, в котором используется набор органических веществ и необходимой стадией для удаления стабилизирующего агента является термическая обработка в инертной атмосфере при 300-400°С, в процессе которой может произойти укрупнение наночастиц, приводящее к снижению площади активной поверхности (Coutanceau, С, Baranton, S., &Nappor, Т. W. (2012). Platinum Fuel Cell Nanoparticle Syntheses: Effect on Morphology, Structure and Electrocatalytic Behavior. The Delivery of Nanoparticles. doi:10.5772/18179).
Недостатком вышеописанных способов, а также способов, описанных в патентах JP 2021073379А, US 2006188772, является использование органических растворителей и стабилизирующих агентов - поверхностно-активных веществ, адсорбция которых происходит на поверхности и в порах углеродного носителя, обладающего высокой сорбционной способностью. Загрязнение носителя добавками, с трудом, поддающимся десорбции, приводит к снижению каталитической активности конечного продукта. Кроме того, массовая доля благородного металла в катализаторе может снижаться вследствие возникновения дополнительных затруднений при адсорбции наночастиц на поверхности углеродного носителя в процессе синтеза. Стабилизирующие агенты загрязняют конечный продукт, а проведение дополнительной многократной отмывки или нагревания платиноуглеродного материала от таких веществ является низкоэффективной и сложно реализуемой стадией в промышленном масштабе.
Представленные способы синтеза наноструктурных материалов с использованием монооксида углерода в качестве стабилизирующего и восстановительного агента, позволяющего оказывать влияние на форму образующихся наночастиц платины и ее сплавов, реализуются в среде органических растворителей (олеиламин, этиленгликоль) и при температуре более 150°С (Kang, Y., Руо, J. В., Ye, X., Diaz, R. Е., Gordon, Т. R., Stack, E. A., &Murray, С.B. (2012). Shape-Controlled Synthesis of Pt Nanocrystals: The Role of Metal Carbonyls. ACS Nano, 7(1), 645-653. doi:10.1021/nn3048439;A.A. Alekseenko, E.A. Ashihina, S.P. Shpanko, V.A. Volochaev, O.I. Safronenko, V.E. Guterman Application of CO atmosphere in the liquid phase synthesis as a universal way to control the microstructure and electrochemical performance of Pt/C electrocatalysts, Appl. Catal. B: Environ. 226 (2018) 608-615. https://doi.org/10.1016/j.apcatb.2018.01.013), а также с применением дополнительных восстановителей (Chang, S.-H., Yeh, M.-H., Pan, С.-J., Chen, K.-J., Ishii, H., Liu, D.-G., … Hwang, B.-J. (2011). СО-assisted synthesis of finely size-controlled platinum nanoparticles. Chemical Communications, 47(13), 3864. doi:10.1039/clcc00018g; A.A. Alekseenko, E.A. Ashihina, S.P. Shpanko, V.A. Volochaev, O.I. Safronenko, V.E. Guterman Application of CO atmosphere in the liquid phase synthesis as a universal way to control the microstructure and electrochemical performance of Pt/C electrocatalysts, Appl. Catal. B: Environ. 226 (2018) 608-615. https://doi.org/10.1016/j.apcatb.2018.01.13).
В ряде работ предпринята попытка использования растворов на основе двухкомпонентных органических или водно-органических растворителей при получении платиноуглеродных электрокатализаторов (Ye, F., Liu, H., Feng, Y., Li, J., Wang, X, &Yang, J. (2014). A solvent approach to the size-controllable synthesis of ultrafine Pt catalysts for methanol oxidation in direct methanol fuel cells. ElectrochimicaActa, 117, 480-485. doi:10.1016/j.electacta.2013.11.01). Вариация состава двухкомпонентного растворителя в некоторых случаях позволяет управлять структурой катализатора, что в значительной степени обусловлено изменением условий адсорбции компонентов растворителя на поверхности растущих наночастиц (Guterman, V. Е., Belenov, S. V., Dymnikova, О. V., Lastovina, Т. A., Konstantinova, Y. В., & Prutsakova, N. V. (2009). Influence of water-organic solvent composition on composition and structure of Pt/C and Pt x Ni/C electrocatalysts in borohydride synthesis. Inorganic Materials, 45(5), 498-505. doi:10.1134/s0020168509050082).
Проблемным вопросом при использовании таких способов также является необходимость удаления остатков весьма специфических органических растворителей из готового продукта.
Недостатком способа, описанного в патенте US 6815391, является необходимость длительного промывания продукта большим количеством воды (3 раза по 3000 мл) в процессе фильтрования, в результате чего остается значительный объем водно-органического фильтрата, загрязняющим компонентом сточных вод с точки зрения экологической безопасности.
Известен способ получения катализатора для топливного элемента, отличительной особенностью которого является отсутствие ПАВ (патент RU 2646761) Однако, реализация способа получения катализатора является длительным и многостадийным процессом, включающим стадии кислотного гидролиза, осаждение коллоида H2Pt(OH)6 (сорбция) на поверхности носителя, закрепление частиц платины (оксидов платины) на поверхности носителя с помощью термической обработки, окончательная восстановительная обработка.
Наиболее близким техническим решением к заявляемому является выбранный в качестве прототипа способ, описанный в патенте RU 2695999, в котором предлагается проводить осаждение платины или ее сплавов с другими металлами в водно-органической среде с обязательным присутствием восстанавливающего агента (муравьиной кислоты, боргидрида натрия, боргидрида калия, формальдегида, этиленгликоля, гидразина, гидроксиламина и др.) и газообразного адсорбата (NO, NO2, СО, SO2) для торможения роста наночастиц.
Однако рассматриваемый способ обладает рядом недостатков. Использование реагентов для формирования водно-органической среды усложняет технологический процесс и требует дополнительной операции для их удаления -тщательной отмывки электрокатализатора и большого расхода промывных вод. Используемые органические вещества, присутствующие в фильтрате, являются загрязняющими с точки зрения экологической безопасности, а применение большого числа реагентов оказывают влияние на конечную стоимость продукта.
Технической задачей предполагаемого изобретения является разработка дешевого и экологичного способа получения платиносодержащих электрокатализаторов за счет создания композитных материалов (платиноуглеродных катализаторов) с заданными структурными характеристиками, возможностью контроля среднего размера кристаллитов Pt от 1.0-13 нм и заданными функциональными параметрами при минимальном использовании реагентов и отсутствии агрессивных для окружающей среды органических растворителей и стабилизаторов (ПАВ).
Указанный технический результат достигается предложенным способом получения платиносодержащих электрокатализаторов в безорганических средах, включающим получение раствора платинохлороводородной кислоты, смешение с порошком дисперсных углеродных или неуглеродных носителей, их смесей и композиций с удельной поверхностью более 60 м2/г, диспергирование полученной смеси и химическое восстановление соединений платины с последующим осаждением наночастиц металлической платины на дисперсный носитель при пропускании монооксида углерода через раствор. При этом используются в качестве восстановителя монооксид углерода, в качестве щелочного агента - водные растворы гидроксида натрия или гидроксида калия, или гидроксида лития. Синтез проводят в одну стадию при температуре раствора от 10÷98°С, а растворителем для всех используемых реактивов и создания жидкой среды является бидистиллированная или деионизированная вода.
Суть и новизна предлагаемого способа состоит в получении в безорганических средах платиносодержащих электрокатализаторов для топливных элементов с заданными структурными характеристиками и функциональными параметрами, основанного на восстановлении прекурсора металла в водной среде, не содержащей органических растворителей и органических поверхностно активных веществ, не требующего стадии очистки спиртами и другими органическими смесями продукта. Отличительными признаками способа являются: отсутствие в качестве растворителей, восстановителей органических соединений в процессе синтеза; сокращение стадий технологического процесса за счет отсутствия необходимости удаления загрязняющих органических соединений, попадающих в поры углеродного носителя, тщательного и длительного промывания продукта спиртами и водой; обеспечение экологической безопасности процесса за счет отсутствия в фильтрате загрязняющих компонентов.
Технический результат данного изобретения заключается в создании дешевого и экологичного способа получения композитных материалов (платино-углеродных катализаторов) улучшенного качества с заданными структурными характеристиками (равномерным распределением наночастиц платины по поверхности углеродного носителя, возможностью контроля среднего размера кристаллитов Pt 1.0-13 нм и с заданными функциональными параметрами (повышенные значения площади электрохимически активной поверхности от 10 до 117 м2/г(Pt), что подтверждается примерами реализации способа.
Указанный технический результат достигается тем, что в процессе получения платиноуглеродных композитных материалов в системе отсутствуют органические растворители, стабилизаторы для управления средним размером наночастиц платины, что обеспечивает чистоту полученного материала. В качестве стабилизирующего компонента выступает двойное действие гидроксид ионов и молекул СО, одновременно находящихся в реакционной смеси. При приготовлении всех растворов и в качестве растворителя в синтезе используется бидистиллированная или деионизированная вода. При этом исключается необходимость в длительном промывании продукта спиртами и водой для удаления загрязняющих органических соединений и необходимость в дополнительной термической обработке продукта для удаления следов органических стабилизаторов, а также необходимость в проведении синтеза при температуре более 100°С.
Предложенный способ получения платиносодержащих электрокатализаторов в безорганических средах позволяет устранить вредное влияние на качество продукта органических стабилизирующих агентов за счет использования водного раствора щелочи различной концентрации для управления средним размером кристаллитов платины; упростить процесс получения электрокатализатора - использовать одностадийный метод синтеза с малым количеством реагентов и снизить в 10-50 раз количество промывных вод; устранить загрязнение сточных вод органическими веществами; получить Pt/C катализаторы, характеризующиеся значением ЭХАП превышающим таковое для коммерческих аналогов с близкой загрузкой платины. С прикладной точки зрения важнейшую роль играют технологичность и экологичность способа получения платиносодержащих наноструктурных электрокатализаторов, а также возможность масштабирования процесса.
Сущность изобретения поясняется следующими примерами, таблицами и иллюстрациями.
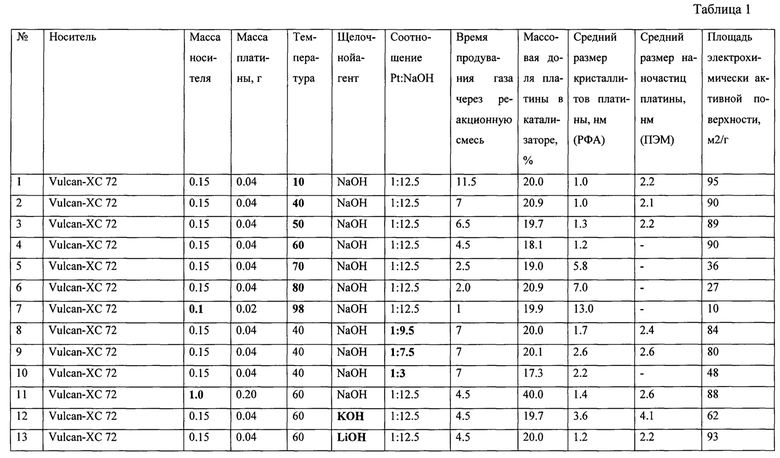
Табл. 1: Условия проведения синтеза, структурные и электрохимические характеристики катализаторов.
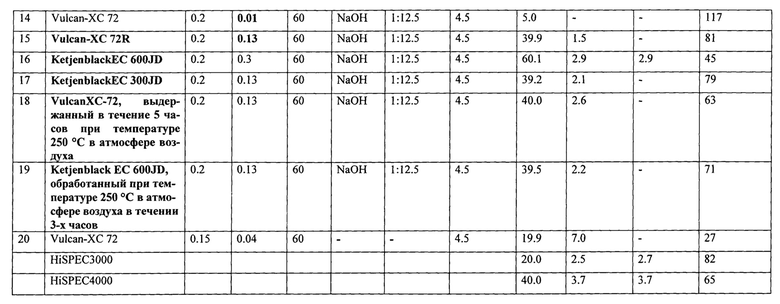
Фиг. 1а: Рентгеновские дифрактограммы Pt/C образцов, полученных в примерах 1-7.
Фиг.1б: Рентгеновские дифрактограммы Pt/C образцов, полученных в примерах 8-10.
Фиг. 1в: Рентгеновские дифрактограммы Pt/C образцов, полученных в примерах 14-19 на различных углеродных носителях: 1 - VulcanXC-72R; 2 -KetjenblackEC 600JD; 3 - KetjenblackEC 300JD; 4 - VulcanXC-72, выдержанный в течение 5 часов при температуре 250°С в атмосфере воздуха; 5 - KetjenblackEC 600JD, обработанный при температуре 250°С в атмосфере воздуха в течении 3-х часов;
Фиг. 1г: Рентгеновские дифрактограммы коммерческих Pt/C катализаторов HiSPEC3000 (массовая доля Pt 20%) и HiSPEC4000 (массовая доля Pt 40%); Pt/C образцов, полученных в примерах 13 и 11 с массовой долей платины 20 и 40% соответственно.
Фиг. 2: Фотографии просвечивающей электронной микроскопии (ПЭМ) высокого разрешения для образцов, соответствующих примерам 1, 2, 3, 9, 11, 13, 16 и коммерческие аналоги Pt/C катализаторов HiSPEC3000 (массовая доля Pt 20%) и HiSPEC4000 (массовая доля Pt 40%).
Фиг. 3: Микрофотографии (ПЭМ) образцов из примеров 3, 8, 12 и соответствующие гистограммы размерного распределения наночастиц.
Фиг. 4: Циклические вольтамперограммы Pt/C образцов, представленных в примерах 1 (кривая 1), 3 (кривая 2), 7 (кривая 3), 11 (кривая 4), HiSPEC3000 (кривая 5), HiSPEC4000 (кривая 6). Скорость развертки потенциала 20 мВ/с. 2-й цикл. Электролит - 0.1 М раствор HClO4, насыщенный аргоном.
Фиг. 5: Зависимость длительности синтеза от температуры в процессе получения катализаторов для примеров 1-7.
Фиг. 6: Зависимость среднего размера кристаллитов платины и площади электрохимически активной поверхности от температуры синтеза 1-7.
Ниже приведены примеры реализации экологичного способа получения платиносодержащих катализаторов.
Основными параметрами, определяющими функциональные характеристики получаемых материалов, являются: массовая доля платины (%), средний размер кристаллитов платины (нм), средний размер наночастиц (нм), площадь электрохимически активной поверхности (м2/г(Pt)).
Используемые реактивы
Синтез катализаторов проводили химическим восстановлением водных растворов прекурсоров платины (H2PtCl6⋅6H2O (Aurat, Russia)).
В приведенных примерах в качестве материала-носителя использовали углеродную сажу различных марок (Vulcan ХС-72 (CabotCorp.),VulcanXC-72R (CabotCorp.), KetjenblackEC 600JD, Ketjenblack EC 300JD) в том числе подвергнутых предварительной обработке VulcanXC-72, выдержанный в течение 5 часов при температуре 250°С в атмосфере воздуха; Ketjenblack ЕС 600JD, обработанный при температуре 250°С в атмосфере воздуха в течении 3-х часов. Однако могут быть использованы и другие дисперсные материалы с удельной поверхностью от 60 до 1000 м2/г, включая сажи, углеродные нановолокна и нанотрубки, графен, фуллерены, допированные и недопированные оксиды олова, титана, циркония, церия и др. металлов, нитриды и оксинитриды титана, циркония, молибдена и др. металлов, карбиды и карбонитриды вольфрама, тантала, циркония и других металлов, а также другие типы дисперсных материалов. Может использоваться комбинация материалов-носителей.
В качестве растворителя для всех используемых реактивов и создания жидкой среды использована бидистиллированная и/или деионизированная вода.
В качестве восстановителя использованы газы монооксида углерода (СО), а в качестве щелочного агента - водные растворы гидроксида натрия NaOH, гидроксида калия KOH, гидроксида лития LiOH.
В качестве стабилизирующего компонента выступает двойное действие гидроксид ионов и молекул СО, одновременно находящихся в реакционной смеси.
Синтез проводили при температуре суспензии от 10 до 98°С.
Пример 1. Высокодисперсный углеродный носитель Vulcan ХС-72 (удельная площадь поверхности 250-280 м2/г) в количестве 0.15 г помещали в раствор, содержащий 30 мл воды и 0.04 г платины в виде прекурсора платины (гексагидратплатино-хлороводородной кислоты (H2PtCl6⋅6H2O)) и проводили диспергирование углеродной смеси в течение 1 минуты при 50% амплитуде. Затем добавляли объем 1 М раствора NaOH, необходимый для соотношения Pt:NaOH 1:12.5. Реакционную смесь нагревали до 10°С и продували потоком СО. При постоянном барботировании монооксидом углерода реакционной смеси проводили синтез и постоянном перемешивании на магнитной мешалке в течение 11.5 часов при температуре 10°С. Далее отделяли продукт фильтрованием, промывая 4-5 раз бидистиллированной водой, и сушили продукт в вакуумном сушильном шкафу 4 часа при температуре 60°С.
В результате получен Pt/C катализатор, массовая доля платины в котором 20.0%, средний размер кристаллитов платины 1.0 нанометра, определенный с помощью РФА, а средний размер наночастиц платины 2.2 нанометра, определенный по фотографиям ПЭМ, площадь электрохимически активной поверхности 95 м2/г(Pt).
Пример 2. Аналогично примеру 1, но при нагревании реакционной смеси до 40°С при постоянной продувке газа СО. Синтез проводили в течение 7 часов: 6.5 часов при температуре 40°С и 0.5 часа без нагревания.
Получили Pt/C катализатор, массовая доля платины в котором 20.9%, средний размер кристаллитов платины 1.0 нанометра, средний размер наночастиц платины 2.1 нанометра, площадь электрохимически активной поверхности 90 м2/г(Pt).
Пример 3. Аналогично примеру 1, но при нагревании реакционной смеси до 50°С при постоянной продувке газа СО. Синтез проводили в течение 6.5 часов: 6 часов при температуре 50°С и 0.5 часа без нагревания.
Получили Pt/C катализатор, массовая доля платины в котором 19.7%, средний размер кристаллитов платины 1.3 нанометра, средний размер наночастиц платины 2.2 нанометра, площадь электрохимически активной поверхности 89 м2/г(Pt).
Пример 4. Аналогично примеру 1, но при нагревании реакционной смеси до 60°С при постоянной продувке газа СО. Синтез проводили в течение 4.5 часов: 4 часа при температуре 60°С и 0.5 часа без нагревания.
Получили Pt/C катализатор, массовая доля платины в котором 18.1%, средний размер кристаллитов платины 1.2 нанометра, площадь электрохимически активной поверхности 90 м2/г(Pt).
Пример 5. Аналогично примеру 1, но при нагревании реакционной смеси до 70°С при постоянной продувке газа СО. Синтез проводили в течение 2.5 часов: 2 часа при температуре 70°С и 0.5 часа без нагревания.
Получили Pt/C катализатор, массовая доля платины в котором 19%, средний размер кристаллитов платины 5.8 нанометра, площадь электрохимически активной поверхности 36 м2/г(Pt).
Пример 6. Аналогично примеру 1, но при нагревании реакционной смеси до 80°С при постоянной продувке газа СО. Синтез проводили в течение 2 часов: 1.5 часа при температуре 80°С и 0.5 часа без нагревания.
Получили Pt/C катализатор, массовая доля платины в котором 20.9%, средний размер кристаллитов платины 7 нанометров, площадь электрохимически активной поверхности 27 м2/г(Pt).
Пример 7. Аналогично примеру 1, но использовали навеску углеродного носителя массой 0.1 г, массу платины 0.02 г, выполняли синтез при нагревании реакционной смеси до 98°С при постоянной продувке газа СО. Синтез проводили в течение1 часа: 0.5 часа при температуре 98°С и 0.5 часа без нагревания.
Получили Pt/C катализатор, массовая доля платины в котором 19.9%, средний размер кристаллитов платины 13.0 нанометров, площадь электрохимически активной поверхности 10 м2/г(Pt).
Пример 8. Аналогично примеру 2, но добавляли раствор NaOH в объеме необходимом для соотношения Pt:NaOH 1:9.5.
Получили Pt/C катализатор, массовая доля платины в котором 20%, средний размер кристаллитов платины 1.7 нанометра, а средний размер наночастиц платины 2.4 нанометра, площадь электрохимически активной поверхности 84 м2/г(Pt).
Пример 9. Аналогично примеру 2, но добавляли раствор NaOH в объеме необходимом для соотношения Pt:NaOH 1:7.5.
Получили Pt/C катализатор, массовая доля платины в котором 20.1%, средний размер кристаллитов платины 2.6 нанометра, средний размер наночастиц платины 2.6 нанометра, площадь электрохимически активной поверхности 80 м2/г(Pt).
Пример 10. Аналогично примеру 2, но добавляли раствор NaOH в объеме необходимом для соотношения Pt:NaOH 1:3.
Получили Pt/C катализатор, массовая доля платины в котором 17.3%, средний размер кристаллитов платины 2.2 нанометра, площадь электрохимически активной поверхности 48 м2/г(Pt).
Пример 11. Аналогично примеру 4, но использовали навеску углеродного носителя массой 1.0 г, массу платины 0.20 г, выполняли синтез при постоянной продувке газа СО.
Получили Pt/C катализатор, массовая доля платины в котором 40.0%, средний размер кристаллитов платины 1.4 нанометра, средний размер наночастиц платины 2.6 нанометра, площадь электрохимически активной поверхности 88 м2/г(Pt).
Пример 12. Аналогично примеру 4, но использовали в качестве щелочи -раствор гидроксида калия.
Получили Pt/C катализатор, массовая доля платины в котором 19.7%, средний размер кристаллитов платины 3.6 нанометра, средний размер наночастиц платины 4.1 нм, площадь электрохимически активной поверхности 62 м2/г(Pt).
Пример 13.Аналогично примеру 4, но использовали в качестве щелочи -раствор гидроксида лития.
Получили Pt/C катализатор, массовая доля платины в котором 20.0%, средний размер кристаллитов платины 1.2 нанометра, средний размер наночастиц платины 2.2 нм, площадь электрохимически активной поверхности 93 м2/г(Pt).
Пример 14. Аналогично примеру 4, но использовали навеску углеродного носителя массой 0.2 г, массу платины 0.01 г.
Получили Pt/C катализатор, массовая доля платины в котором 5.0%, площадь электрохимически активной поверхности 117 м2/г(Pt).
Пример 15. Аналогично примеру 14, но использовали углеродный носитель Vulcan XC-72R, а массу платины 0.13 г.
Получили Pt/C катализатор, массовая доля платины в котором 39.9%, средний размер кристаллитов платины 1.5 нанометра, площадь электрохимически активной поверхности 81 м2/г(Pt).
Пример 16. Аналогично примеру 15, но использовали углеродный носитель Ketjenblack ЕС 600JD, а массу платины 0.3 г.
Получили Pt/C катализатор, массовая доля платины в котором 60.1%, средний размер кристаллитов платины 2.9 нанометра, средний размер наночастиц платины 2.9 нанометра, площадь электрохимически активной поверхности 45 м2/г(Pt).
Пример 17. Аналогично примеру 15, но использовали углеродный носитель Ketjenblack ЕС 300JD.
Получили Pt/C катализатор, массовая доля платины в котором 39.2%, средний размер кристаллитов платины 2.1 нанометра, площадь электрохимически активной поверхности 79 м2/г(Pt).
Пример 18. Аналогично примеру 15, но использовали углеродный носитель VulcanXC-72, выдержанный в течение 5 часов при температуре 250°С в атмосфере воздуха.
Получили Pt/C катализатор, массовая доля платины в котором 40.0%, средний размер кристаллитов платины 2.6 нанометра, площадь электрохимически активной поверхности 63 м2/г(Pt).
Пример 19. Аналогично примеру 15, но использовали углеродный носитель Ketjenblack ЕС 600JD, обработанный при температуре 250°С в атмосфере воздуха в течении 3-х часов.
Получили Pt/C катализатор, массовая доля платины в котором 39.4%, средний размер кристаллитов платины 2.2 нанометра, площадь электрохимически активной поверхности 71 м2/г(Pt).
Пример 20. Аналогично примеру 4, но без добавления раствора щелочи.
Получили Pt/C катализатор, массовая доля платины в котором 19.9%, средний размер кристаллитов платины 7.0 нанометра, площадь электрохимически активной поверхности 27 м2/г(Pt).
Все результаты экспериментов сведены в Табл. 1., где приведены условия проведения синтеза, структурные и электрохимические характеристики полученных катализаторов. Для сравнительной характеристики активности Pt/C катализаторов, представлены данные относительно коммерческого Pt/C катализатора HiSPEC3000 (Johnson-Matthey, 20% Pt) и HiSPEC4000 (Johnson-Matthey, 40% Pt).
Приведенные выше примеры реализации предложенного способа подтверждают возможность получения катализаторов на основе наночастиц платины, распределенных на поверхности углеродного носителя с заявленными характеристиками, а именно с массовой долей Ртот 5 до 60%; малым размером металлических наночастиц и возможностью его управления (по данным РФА от 1.0 до 13.0 нанометров); высокими значениями электрохимически активной площади поверхности от 10 до 117 м2/г(Pt). Примеры свидетельствует о высоком качестве получаемых катализаторов, которые характеризуются более ЭХАП по сравнению с аналогами, что подтверждает эффективность предлагаемого подхода.
Массовую долю платины в исследуемых образцах определяли методом гравиметрии. Керамические тигли прокаливали до постоянной массы при 800-850°С и взвешивали после полного остывания (mт). Затем помещали в тигли 0.02 г Pt/C материала (mзагр.), сжигали навески в муфельной печи при 800-850°С в течение 40 минут. Взвешивали тигли с несгораемым остатком после полного остывания (mт+ост). По изменению массы определяли содержание металлов в образце, используя формулу:
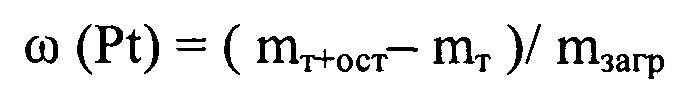
Для съемки рентгенограмм применялся порошковый дифрактометр ARL X'TRA с геометрией по Бреггу-Брентано (θ-θ), CuKα - излучение (λ=0.154056 нм) при комнатной температуре. Рентгенограммы исследуемых образцов записаны в интервале углов 5° ≤ 20 ≥ 55° методом пошагового сканирования с шагом перемещения детектора 0.02°.
Рентгенограммы обрабатывались программой SciDavis для корректного извлечения параметров пиков, что важно при их перекрывании в случае малого размера частиц. Исходя из уравнения Вульфа-Брегга, формула:

d - межплоскостное расстояние (hkl), (Å)
можно вывести формулу, в литературе известную как формулу Шеррера:
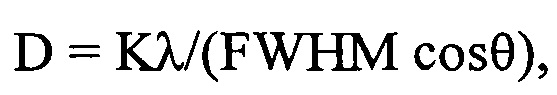
где λ - длина волны монохроматического излучения (Å),
FWHM - полуширина рефлекса на половине высоты (в радианах);
K=0.89 - постоянная Шеррера;
D - средняя толщина «стопки» отражающих плоскостей в области когерентного рассеяния, (Å);
θ - угол падения пучка рентгеновского излучения (в радианах).
Размер наночастиц платины определяли методом просвечивающей электронной микроскопии (ПЭМ) с помощью микроскопов JEM-2100 (JEOL, Japan) и FEI Tecnai G2 F20c (FEI, США). Пробоподготовку образца выполняли следующим образом: 0.5 мг катализатора помещали в 1 мл изопропанола и диспергировали ультразвуком в течение 10 минут. Каплю полученной суспензии наносили на стандартную медную сетку диаметром 3 мм, покрытую слоем аморфного углерода толщиной 5-7 нм, после чего образец сушили на воздухе при комнатной температуре в течение 30 минут. Гистограммы размерного распределения наночастиц в катализаторах строили по результатам определения размеров не менее 400 частиц, случайно выбранных на изображениях ПЭМ различных участках образца. Точность определения среднего размера наночастиц составляла ±5%.
Для приготовления суспензии катализаторов (каталитических «чернил») массу образца рассчитывали таким образом, чтобы при последующем нанесении катализатора на электрод масса платины составляла 20 мкг(Pt)/см2. Затем добавляли 1% водную эмульсию полимера Nafion®, деионизированной воды и изопропилового спирта. Затем суспензию диспергировали ультразвуком в течение 15 минут. При непрерывном перемешивании с помощью микродозатора отбирали аликвоту «чернил» объемом 6 мкл и наносили на торец отполированного и обезжиренного стеклоуглеродного диска площадью 0.196 см2, регистрируя точный вес капли. Электрод высушивали на воздухе в течение 20 минут при вращении 700 об/мин [K.О. Paperzh, A.A. Alekseenko, V.A. Volochaev, I.V. Pankov, О.A. Safronenko, V.E. GutermanStabilityandactivityofplatinumnanoparticle-sintheoxygenelectroreductionreaction: issizeoruniformityofprimaryimportance? BeilsteinJ. Nanotechnol. 2021, 12, 593-606. https://doi.org/10.3762/bjnano.12.49].
Электрохимические измерения катализаторов проводили в трехэлектрод-ной ячейке на потенциостате Versostat с использованием вращающегося дискового электрода (Pine Research Instruments) при температуре 23°С. В качестве электрода сравнения использовали хлорид серебряный, в качестве вспомогательного - платиновую проволоку. Все потенциалы в работе приведены относительно обратимого водородного электрода. Перед проведением электрохимических измерений подвергали электрод электрохимической стандартизации, задавая 100 вольтамперных циклов в диапазоне потенциалов 0.04-1.2 В со скоростью развертки потенциала 200 мВ/с в растворе 0.1 М HClO4 в атмосфере аргона. Далее регистрировали две ЦВА в диапазоне потенциалов 0.04-1.2 В со скоростью сканирования 20 мВ/с для дальнейшего расчета значения ЭХАП по количеству электричества, затраченному на адсорбцию/десорбцию водорода (K.О. Paperzh, A.A. Alekseenko, V.A. Volochaev, I.V. Pankov, O.A. Safronenko, V.E. GutermanStabilityandactivityofplatinumnanoparticlesintheoxyge-nelectroreductionreaction: issizeoruniformityofprimaryimportance? BeilsteinJ. Nanotechnol. 2021, 12, 593-606. https://doi.org/10.3762/bjnano.12.49).
Как следует из сравнения рентгеновских дифрактограмм, чем выше температура в процессе синтеза, тем быстрее осуществляется его протекание и тем больше средний размер кристаллитов и средний размер наночастиц платины в полученных катализаторах (Примеры 1-7, Фиг. 1а).
В процессе синтеза возможно использование различного соотношения Pt:OH от 1:3 до 1:12.5, при повышении которого наблюдается увеличение среднего размера кристаллитов платины в полученных катализаторах (Примеры 1, 8-10, Фиг. 1б). Синтез катализаторов может быть выполнен с использованием различных углеродных носителей (Примеры 14-19, Фиг. 1в).
С помощью описанного метода синтеза могут быть получены катализаторы с различной массовой долей платины (Примеры 4, 11, 14, 16).
Как следует из сравнения рентгеновских дифрактограмм, представленных на Фиг. 1г, и результатов просвечивающей электронной микроскопии, представленных на Фиг. 2, средний размер наночастиц платины в полученных Pt/C материалах (Примеры 1, 2, 3, 8, 9, 13) меньше, чем в коммерческих аналогах HiSPEC3000 и HiSPEC4000 (Табл. 1).
Как следует из результатов расчетов, проведенных для циклических вольтамперограмм, измеренных на Pt/C катализаторах и представленных на Фиг. 4, площадь электрохимически активной поверхности платины в Pt/C материалах, полученных при температуре 10-60°С выше (Примеры 1, 3, 11), чем в коммерческих катализаторах HiSPEC3000 и HiSPEC4000 с близкой загрузкой платины и в аналоге, синтезированном при температуре 70°С (Пример 5, Таблица 1, Примеры 6, 7).
Предлагаемая методика путем варьирования температуры в процессе синтеза дает возможность управлять временем реакции (Фиг. 5), средним размером образующихся кристаллитов платины, и, как следствие площадью электрохимически активной поверхности (Фиг. 6).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения платиносодержащих катализаторов для топливных элементов и электролизеров | 2022 |
|
RU2775979C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРОВ С НАНОРАЗМЕРНЫМИ ЧАСТИЦАМИ ПЛАТИНЫ И ЕЕ СПЛАВОВ С МЕТАЛЛАМИ | 2018 |
|
RU2695999C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИМЕТАЛЛИЧЕСКИХ КАТАЛИЗАТОРОВ С ГРАДИЕНТНОЙ СТРУКТУРОЙ НА ОСНОВЕ ПЛАТИНЫ | 2018 |
|
RU2677283C1 |
| Способ получения биметаллического электрокатализатора на основе платиновых ядер | 2021 |
|
RU2778126C1 |
| Способ получения электрокатализатора платина на углероде | 2016 |
|
RU2646761C2 |
| Способ изготовления самоувлажняющегося электрокатализатора для водородно-воздушных топливных элементов | 2020 |
|
RU2744103C1 |
| Способ получения катализатора с наноразмерными частицами платины | 2016 |
|
RU2616190C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ ТОПЛИВНОГО ЭЛЕМЕНТА | 2008 |
|
RU2367520C1 |
| КАТАЛИТИЧЕСКИЙ ЭЛЕКТРОД ДЛЯ СПИРТОВЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 2012 |
|
RU2507640C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПЛАТИНОВЫХ КАТАЛИЗАТОРОВ | 2009 |
|
RU2415707C2 |



Изобретение относится к способу получения функциональных композитных материалов. Предложен способ получения платиносодержащих электрокатализаторов в безорганических средах, включающий получение раствора платинохлороводородной кислоты, смешение с порошком дисперсных углеродных или неуглеродных носителей, их смесей и композиций с удельной поверхностью более 60 м2/г, диспергирование полученной смеси и химическое восстановление соединений платины с последующим осаждением наночастиц металлической платины на дисперсный носитель при пропускании монооксида углерода через раствор, отличающийся тем, что в качестве щелочного агента используются водные растворы гидроксида натрия, или гидроксида калия, или гидроксида лития, при этом синтез проводят в одну стадию при температуре раствора от 10÷98°С, а растворителем для всех используемых реактивов и создания жидкой среды является бидистиллированная или деионизированная вода. Технический результат - создание экологичного способа получения композитных материалов улучшенного качества с заданными структурными характеристиками и с заданными функциональными параметрами. 6 ил., 1 табл., 20 пр.
Способ получения платиносодержащих электрокатализаторов в безорганических средах, включающий получение раствора платинохлороводородной кислоты, смешение с порошком дисперсных углеродных или неуглеродных носителей, их смесей и композиций с удельной поверхностью более 60 м2/г, диспергирование полученной смеси и химическое восстановление соединений платины с последующим осаждением наночастиц металлической платины на дисперсный носитель при пропускании монооксида углерода через раствор, отличающийся тем, что в качестве щелочного агента используются водные растворы гидроксида натрия, или гидроксида калия, или гидроксида лития, при этом синтез проводят в одну стадию при температуре раствора от 10÷98°С, а растворителем для всех используемых реактивов и создания жидкой среды является бидистиллированная или деионизированная вода.
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРОВ С НАНОРАЗМЕРНЫМИ ЧАСТИЦАМИ ПЛАТИНЫ И ЕЕ СПЛАВОВ С МЕТАЛЛАМИ | 2018 |
|
RU2695999C1 |
| Способ получения платиносодержащих катализаторов для топливных элементов и электролизеров | 2022 |
|
RU2775979C1 |
| RU 2013102769 А, 20.10.2014 | |||
| RU 2016115797 А, 26.10.2017 | |||
| CN 0101152627 В, 18.07.2012. | |||
Авторы
Даты
2024-03-18—Публикация
2023-08-04—Подача