Область техники
Изобретение относится к гель-полимерным электролитам. Гель-полимеры на основе сополимеров триазина (меламина) оптически прозрачны и подходят для применения в электрохромных устройствах или иных оптико-электрохимических устройствах. Кроме того, такие электролиты могут применяться в устройствах для хранения электрической энергии (аккумуляторах, суперконденсаторах и гибридных накопителях) вместо традиционных электролитов на водной основе.
Уровень техники
Существует целый ряд электрохимических устройств, нуждающихся в оптически прозрачных электролитах. В первую очередь к таким устройствам относятся электрохромные ячейки. В последние годы стремительно растет количество компаний, производящих «умные стекла» для фасадов зданий и для автомобильной промышленности, принцип работы которых основан именно на электрохимических изменениях, происходящих с электрохромными материалами [1], [2]. Традиционные жидкие электролиты, имеют очень большую ионную проводимость. Тем не менее, их применение в «умных» стеклах весьма затруднительно по многим причинам. Во-первых, это вызывает технические сложности, связанные с надежной герметизацией больших по массе и площади устройств, а во-вторых, жидкие электролиты, как правило, являются химически агрессивными и могут нанести вред не только окружающей среде, но и людям, эксплуатирующим или изготавливающим «умное» стекло.
Поэтому в электрохромных стеклах предпочитают использовать безопасные композиции электролитов, находящихся не в жидком состоянии, а в виде густых гелей или гель-полимеров, а также в виде полностью полимерных или специальных твердых неорганических материалов, обладающих ионной проводимостью (т.н. твердотельные электролиты) [3]-[6].
Оптически прозрачные электролиты обычно представляют собой гель-электролиты. В таком электролите полимерный гель составляет некое подобие «каркаса» для обычных жидких электролитов на основе кислот, щелочей, солей металлов или органических ионных жидкостей. Известны гели на основе полистиролов, полиакрилатов, поливинилхлоридов, поливинилфторидов, поливинилацетатов, поливиниловых спиртов, полиэтиленоксида, поливинилиденхлорида, различных их производных, содержащих эпокси-группу и силоксановых полимеров [7]-[9]. Кроме того, в качестве гелирующей добавки применяются неорганические или гибридные материалы [10]. Например, в качестве гелевой основы применяется жидкое стекло и сополимеры ортосиликатов и полиольных спиртов [11]. В гелевых электролитах химическое взаимодействие между электролитом и полимерным составом отсутствует. В то же время существуют полимерные или гель-полимерные электролиты, в которых химическое взаимодействие между электролитом и полимерным каркасом существует и сам полимерный «каркас» является частью электролита. Такое взаимодействие становится возможным из-за наличия в составе полимера органических функциональных групп (например -COO-, -SO3- и т.д.). Соответственно, полимер, входящий в состав таких композиций является полиэлектролитом и сам обладает некоторой величиной ионной проводимости. В простейшем случае полимерные электролиты обладают протонной проводимостью, так как образуют такие группы с протонами, например, -COO-H+ и -SO3-H+, а также могут обладать ионной проводимостью за счет образования солей металлов (обычно одновалентных), например, -COO-M+, -SO3-M+ (где M = Li, Na, K и т.д.). Одновременно гель-полимерные электролиты содержат и некоторую часть низкомолекулярных растворителей (вода или органические растворители), которые, в основном, и обеспечивают подвижность ионов, а следовательно, ионную проводимость гель-полимерных электролитов в целом.
Кроме того, существуют истинно полимерные (твердотельные) электролиты, способные проводить протоны или ионы одновалентных металлов [12]. Обычно они содержат те же функциональные группы, что и гель-полимерные электролиты, либо представляют собой полимерные четвертичные соли аммония или соли с азот-содержащими гетероциклами [13], [14].
Упомянутые три группы электролитов имеют свои преимущества и недостатки. В частности, гелевые и гель-полимерные электролиты, как правило, имеют высокую электрическую проводимость (порядка 10-2…10-4 См·см-1), но их применение требует особой осторожности, так как при утечке или частичном испарении растворителя они дают сильную усадку, что приводит к появлению видимых дефектов в виде пузырьков, полостей, трещин и т.д. и, в конечном счете, существенно ухудшает или полностью нарушает работу электрохимической ячейки. Очевидно, возникновение дефектов подобного рода неприемлемо при использовании электролита в оптических системах.
Полностью полимерные электролиты практически не дают усадки, но их электрическая проводимость невелика (10-4…10-6 См·см-1) и, как правило, сильно зависит от температуры окружающей среды. Проводимость полимерных электролитов может падать при снижении температуры ниже 0°С на несколько порядков.
Технология получения прозрачных гель-полимерных электролитов на основе меламина, формальдегида и полиолов или сахаридов в той или иной степени описана в нескольких документах из уровня техники.
Из патентного документа US7931964B2 (Microporous layers, an article comprising a microporous layer, and a method of manufacture thereof) известен гель-полимерный электролит, получаемый сополимеризацией (а) меламина, (б) формальдегида или глиоксаля и (в) одного или нескольких полиолов и/или одного или нескольких моносахаридов, олигосахаридов или полисахаридов. Тем не менее, из этого документа не известно добавление концентрированной кислоты к продукту сополимеризации для образования оптически прозрачного гель-полимера с протонной проводимостью.
Из патентного документа EP2983186A1 (Electrode composition for supercapacitor, cured product of said composition, electrode comprising said cured product, capacitor comprising said electrode, and manufacturing method for said supercapacitor) известен прозрачный электрод, получаемый сополимеризацией (а) меламина, (б) формальдегида или глиоксаля и (в) одного или нескольких полиолов и/или одного или нескольких моносахаридов, олигосахаридов или полисахаридов. Тем не менее, из этого документа не известно получение оптически прозрачного гель-полимера с протонной проводимостью.
Из патентного документа US7842637B2 (Electroactivated film with polymer gel electrolyte) известен гель-полимерный электролит, получаемый сополимеризацией (а) меламина, (б) формальдегида или глиоксаля и (в) одного или нескольких полиолов и/или одного или нескольких моносахаридов, олигосахаридов или полисахаридов. Тем не менее, из этого документа не известно добавление концентрированной кислоты к продукту сополимеризации для образования оптически прозрачного гель-полимера с протонной проводимостью.
Из патентного документа US6280881B1 (Lithium secondary battery) известен гель-полимерный электролит, получаемый сополимеризацией (а) меламина, (б) формальдегида или глиоксаля и (в) одного или нескольких полиолов и/или одного или нескольких моносахаридов, олигосахаридов или полисахаридов. Тем не менее, из этого документа не известно добавление концентрированной кислоты к продукту сополимеризации для образования оптически прозрачного гель-полимера с протонной проводимостью.
Из патентного документа US8642895B2 (Substrate with transparent conductive layer and method for producing the same, and touch panel using the same) известен прозрачный несущий субстрат для электрода, получаемый сополимеризацией (а) меламина, (б) формальдегида или глиоксаля и (в) одного или нескольких полиолов и/или одного или нескольких моносахаридов, олигосахаридов или полисахаридов. Упоминается возможность наличия в субстрате кислот. Тем не менее, из этого документа не известно добавление концентрированной кислоты к продукту сополимеризации для образования оптически прозрачного гель-полимера с протонной проводимостью.
Из патентного документа US8968928B2 (Primer for battery electrode) известен материал подслоя для слоя токоотвода, получаемый сополимеризацией (а) меламина, (б) формальдегида или глиоксаля и (в) одного или нескольких полиолов и/или одного или нескольких моносахаридов, олигосахаридов или полисахаридов. Тем не менее, из этого документа не известно добавление концентрированной кислоты к продукту сополимеризации для образования оптически прозрачного гель-полимера с протонной проводимостью.
Из патентного документа US7238451B2 (Conductive polyamine-based electrolyte) известен гель-полимерный электролит, получаемый сополимеризацией (а) меламина, (б) формальдегида или глиоксаля и (в) одного или нескольких полиолов и/или одного или нескольких моносахаридов, олигосахаридов или полисахаридов. Обсуждается влияние сильных кислот на реакцию полимеризации и проводимость электролита. Тем не менее, из этого документа не известно добавление концентрированной кислоты к продукту сополимеризации для образования оптически прозрачного гель-полимера с протонной проводимостью.
Анализ документов из уровня техники показывает, что в данной области техники не известно получение оптически прозрачных гель-полимерных электролитов с протонной проводимостью на основе меламина, получаемых реакцией сополимеризации меламина и формальдегида или меламина и глиоксаля с одним или несколькими полиолами и/или с одним или несколькими моносахаридами, олигосахаридами или полисахаридами и/или их производными с последующим добавлением концентрированной кислоты для образования оптически прозрачного гель-полимера, и пригодных для применения в электрохромных и иных оптико-электрохимических устройствах или в устройствах для хранения электрической энергии (аккумуляторах, суперконденсаторах и гибридных накопителях) вместо традиционных электролитов на водной основе.
Гель-полимерные электролиты на основе сополимеров меламина обладают выдающейся оптической прозрачностью, высокой ионной проводимостью, стойкостью к механическим воздействиям, хорошей адгезией к материалам разной природы и пластичностью, а также имеют весьма незначительную усадку. Их применение в электрохимических устройствах вместо обычных электролитов на водной основе позволяет расширить диапазон рабочих температур устройств, увеличить их сроки эксплуатации, снизить пожарную опасность и придать существенную механическую прочность конечным изделиям.
Раскрытие изобретения
Гель-полимерные электролиты являются компромиссным решением для многих электрохимических устройств. Они обладают приемлемой проводимостью и не сильно подвержены физико-химическим изменениям в процессе эксплуатации.
Автором данного изобретения были разработаны гель-полимерные протонные электролиты на основе триазиновых соединений (сополимеров меламина) с различными многоатомными спиртами, моносахаридами, олигосахаридами, полисахаридами, а также с их производными, содержащими более одной гидроксильной группы (фиг. 1-2). В ходе экспериментов было выяснено, что такие сополимеры обладают достаточно высокой электрической проводимостью (приблизительно 1,2⋅10-1…2,5⋅10-1 См·см-1), оптической прозрачностью, механической прочностью и малой усадкой при условии должной герметизации электрохимической ячейки.
Электролиты согласно изобретению были разработаны, прежде всего, для применения в электрохромных устройствах. Тем не менее, ввиду их высокой ионной проводимости, химической стабильности, удобства применения и дешевизны, они, несомненно, могут применяться в качестве электролитов в электрохимических устройствах других типов, например, в свинцово-кислотных аккумуляторах или в суперконденсаторах.
Образование прозрачных гель-полимеров на основе простых меламинформальдегидных производных описано в источниках [15]-[18]. Синтез модифицированных меламиновых сополимеров с полиолами, органическими двухосновными кислотами и альдегидами также описан в источниках [19], [20]. Тем не менее, по данным автора данного изобретения, полученные таким образом гели использовались для других целей. В частности, они применялись в качестве клеев по дереву или бумаге, для улучшения свойств бетонов или для изготовления углеродных аэрогелей, допированных другими элементами (в частности, азотом), методом пиролиза в инертной атмосфере [21]. По данным автора данного изобретения, сополимеры меламина с полиолами, моносахаридами, олигосахаридами и полисахаридами, а также и их производными, не использовались ранее в качестве базы для образования прозрачных проводящих гель-полимерных электролитов для электрохромных устройств.
Возможно, это связано с тем, что при добавлении кислот к меламинформальдегидным полимерам происходит их дальнейшая глубокая полимеризация с образованием непрозрачных полимеров белого цвета. Лишь при использовании заведомо большего количества одноосновных кислот таких, как HF, HCl, HBr и СCl3COOH, происходит образование прозрачных гель-полимеров. При использовании же двух- и трехосновных кислот (например, H2SO4 и H3PO4) получаются, как правило, только непрозрачные или полупрозрачные гель-полимеры с большим коэффициентом оптического рассеяния. Кроме того, такие гель-полимеры дают очень большую усадку при твердении и высыхании. Все это препятствует их использованию в фотогальванических устройствах на основе электрохромных материалов.
В результате исследований автором были разработаны сополимеры на основе сочетания меламинформальдегида с многоатомными спиртами (полиолами), сахарами и полисахаридами. В отличие от обычных меламиновых сополимеров, они образуют прозрачные гель-полимеры при добавлении любых кислот (одноосновных и многоосновных) в нескольких диапазонах концентраций. Кроме того, в виду достаточной пластичности структуры таких гель-полимеров, они практически не дают усадки при гелеобразовании. Помимо вышесказанного, они обладают высокими клеящими свойствами и большой механической прочностью, что открывает дорогу для их применения в составе электрохромных устройств или в качестве протонных электролитов в источниках тока [22], [23].
Краткое описание чертежей
На фиг. 1 представлена схема первой стадии синтеза гель-полимерных электролитов - образование триметилолмеламина.
На фиг. 2 представлена схема второй стадии синтеза оптически прозрачных меламинформальдегидных гель-полимерных электролитов путем реакции триметилоламина с полиолами, моносахаридами, олигосахаридами, полисахаридами и любыми их производными, содержащими более одной свободной OH- группы.
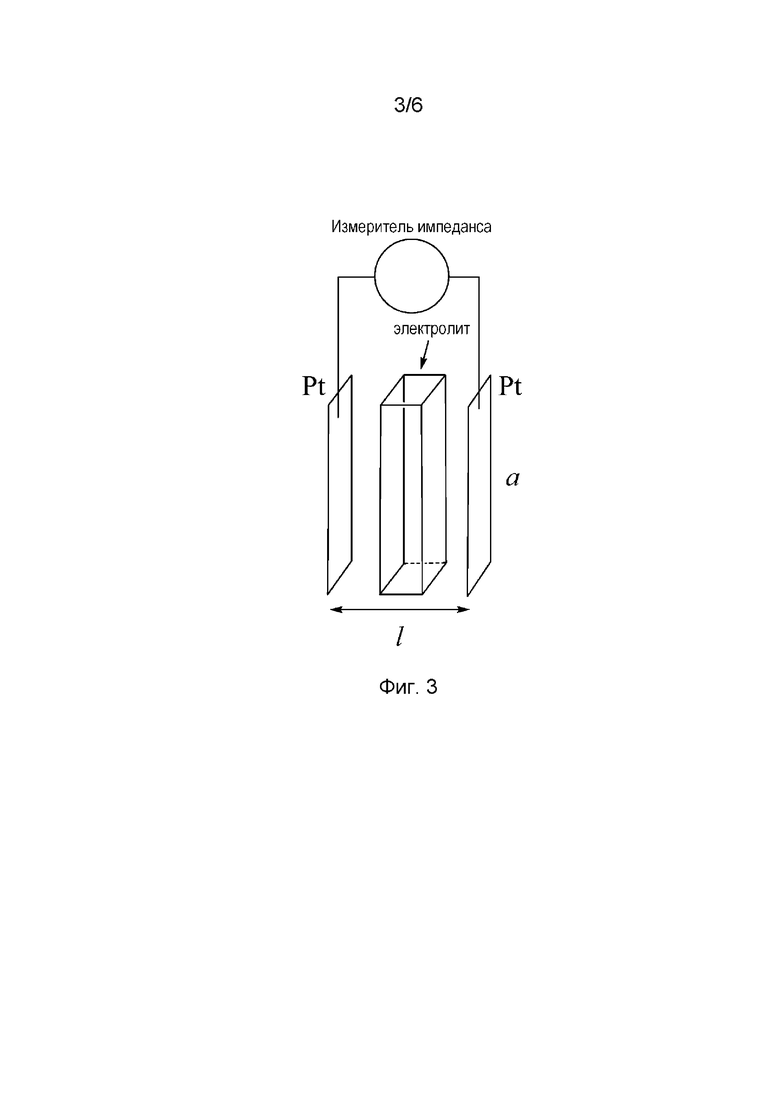
На фиг. 3 представлена схема измерения ионной проводимости гелевого электролита методом импедансной спектроскопии между двумя платиновыми электродами.
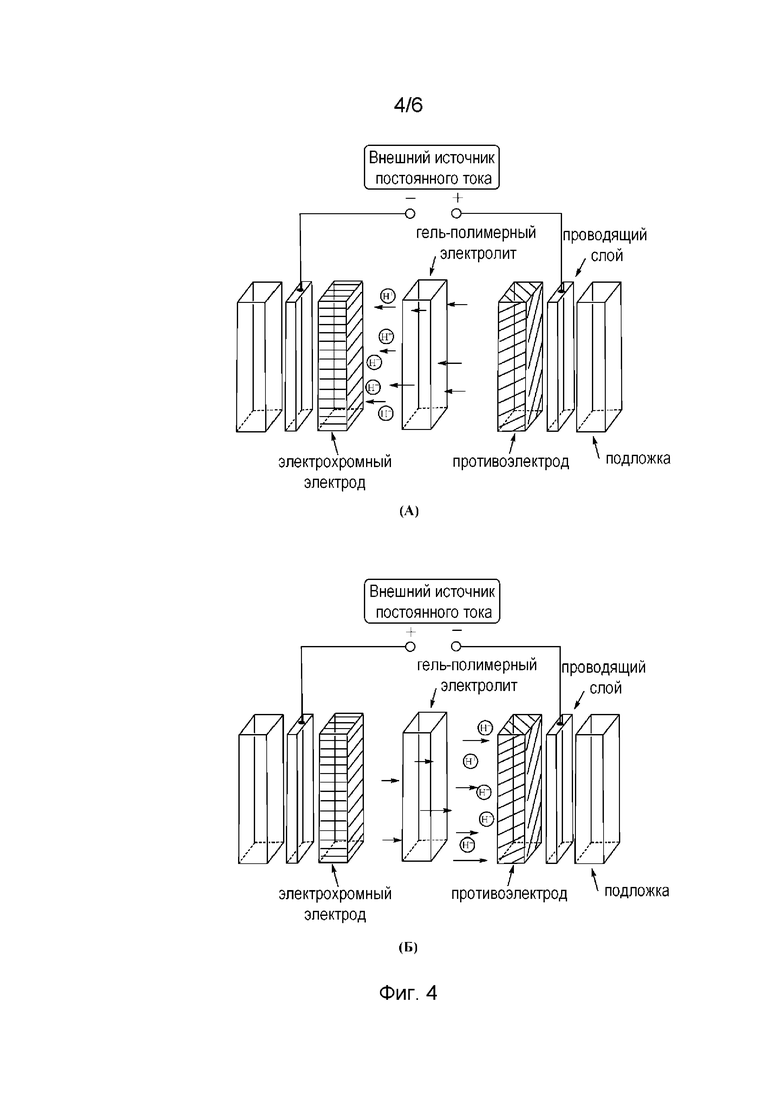
На фиг. 4 представлена схема электрохромного устройства. Процесс окрашивания (а) происходит, когда протоны движутся в направлении электрохромного электрода, а процесс обесцвечивания (б) происходит после смены полярности.
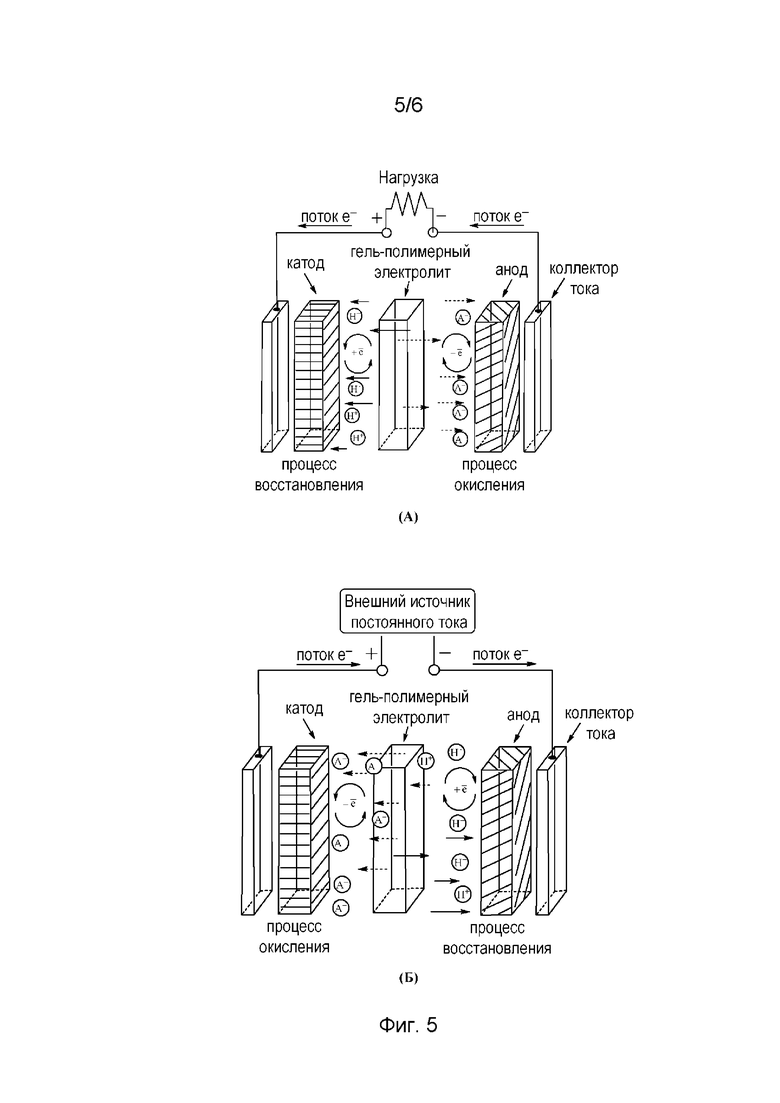
На фиг. 5 представлена схема вторичной электрохимической ячейки. Показано движение протонов и анионов в процессе разряда (а) и в процессе заряда (б), а также схематически изображены фарадеевские процессы, происходящие на электродах.
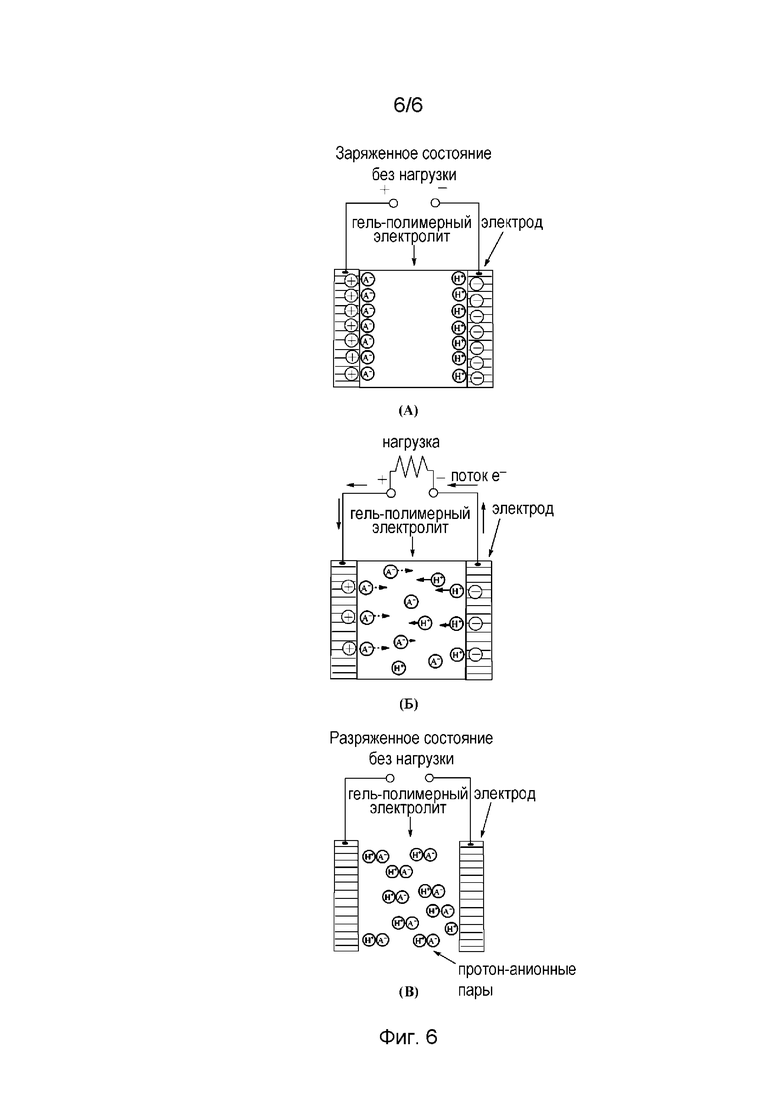
На фиг. 6 представлена схема симметричного суперконденсатора с двойным электрическим слоем и гель-полимерным электролитом с протонной проводимостью.
Осуществление изобретения
Основными недостатками полимеров на основе меламина является их хрупкость и склонность к усадке, для преодоления которых автором данного изобретения разработан способ получения более пластичных производных меламина путем сополимеризации триметилолмеламина (фиг. 1) с полиолами, сахарами, крахмалом и производными целлюлозы. Сополимеризация возникает со сравнительно длинными полимерными цепочками и концевыми гидроксильными группами (фиг. 2), что способствует пластичности результирующего полимера. Кроме того, гидроксил-содержащие группы, присутствующие в конечных меламиновых сополимерах, довольно объемны и заметно снижают усадку этих сополимеров.
Следует отметить, что получаемые таким образом сополимеры представляют собой прозрачные или полупрозрачные жидкости различной вязкости. Некоторые из них могут храниться до 12 месяцев (обычно от 30 дней до 8 месяцев) без существенного изменения их физических свойств. Далее путем добавления к меламиновым сополимерам сильных минеральных или органических кислот получаются протон-проводящие гели.
Сразу после добавления сильной кислоты раствор остается жидким и сохраняет прозрачность, но через некоторое время начинается процесс более глубокой полимеризации и полимерный раствор превращается в ион-проводящий гелевый электролит. При этом процесс превращения раствора в гель может занимать довольно продолжительное время и его длительность зависит как от концентрации кислоты, так и от наличия гидрофобных групп в полиольной цепи. Чем сильнее кислота и чем выше ее концентрация, тем медленней идет процесс образования геля. Гидрофобные группы в полиолах так же заметно снижают скорость образования геля. Например, при использовании пропиленгликоля и его производных, в частности, полоксамеров [24] процесс образования геля может занимать до 72 часов и более.
Оказалось неожиданным, что при добавлении к растворам сополимеров даже очень больших количеств сильных концентрированных кислот (например, концентрированной серной кислоты) - в отношении 1:1 или даже 1,5:1 (в пересчете на полимер) не происходит мгновенной полимеризации с образованием твердой фазы (гель-полимера), а происходит медленное (до 10 часов) загустевание исходного сополимера с образованием весьма пластичных и совершенно прозрачных гель-полимеров без отделения жидкой фазы.
Кроме того, следует отметить, что зависимость прозрачности протон-проводящего геля от концентрации кислоты не является линейной. С увеличением содержания кислоты наблюдаются по меньшей мере два значения отношения содержания кислоты и меламинового сополимера, при которых гелевый электролит становится прозрачным. Образование прозрачных гель-полимерных электролитов происходит при концентрации кислоты от 3,0% до 7,5% и от 10,0% до 40,0% в растворе сополимера. Между этими значениями гель может быть сильно замутненным и опалесцирующим или даже совершенно белым и непрозрачным.
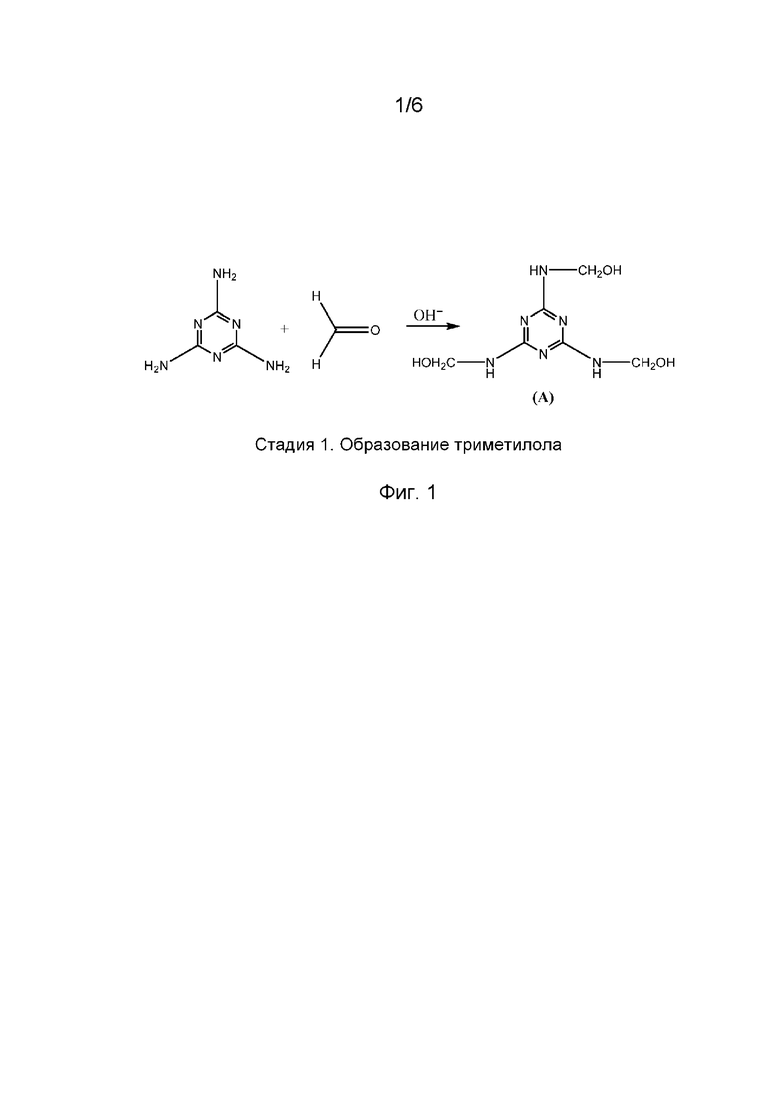
Измерение ионной проводимости меламиновых электролитов выполнялось в ячейке, содержащей два платиновых электрода с площадью рабочей поверхности (а) 17,2 см2. Расстояние между электродами (l) составляло 1 мм (см. фиг. 3). Импеданс ячейки измерялся методом электрохимической импедансной спектроскопии (EIS, Electrochemical Impedance Spectroscopy) в частотном диапазоне 1 кГц - 0,5 МГц при амплитуде напряжения от 50 мВ до 150 мВ. В результате для каждого гель-полимерного электролита была получена частотная характеристика (диаграмма Найквиста). Для получения значения импеданса (Z) выбиралась минимальная величина по оси ReZ (Ом) и по оси -ImZ (Ом). Проводимость определялась по формуле (1) [25].
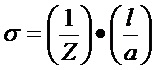 (1)
(1)
Ионная проводимость всех гель-полимерных электролитов, полученных описанным здесь способом, оказалась в диапазоне 1,2⋅10-1…2,5⋅10-1 См·см-1. Такая высокая проводимость позволяет достичь хороших характеристик электрохромных и других гальванических устройств.
Электрохромные устройства с применением предложенных гель-полимерных электролитов были изготовлены автором данного изобретения с целью экспериментальной проверки их работоспособности. Обобщенная схема этих устройств приведена на фиг. 4. Для электрохромного электрода использовался материал на основе оксида вольфрама, а для противоэлектрода использовался допированный оксид церия CeO2:M (M - переходный металл). Оба материала наносились магнетронным напылением на стекло со слоем допированного фтором оксида олова (FTO, Fluorine doped Tin Oxide). Рабочее напряжение в такой электрохимической ячейке, приводящее к смене окрашивания, не превышало 1,0 В. Эту величину потенциала следует признать приемлемой в силу ограниченного вольтамперомметрического окна водных электролитов при котором не происходит их преждевременной деградации ( ≤ 1,23 В).
Благодаря высокой проводимости электролита скорость переключения из обесцвеченного в окрашенное состояние в такой ячейке весьма высока - обычно от 5 до 20 секунд при расстоянии между электродами 1 мм. При этом с уменьшением расстояния между электродами существенного увеличения скорости не наблюдается. По всей видимости, работа электрохимической ячейки в таких условиях ограничивается уже не проводимостью гель-полимерного электролита, а скоростью электрохимических процессов, протекающих непосредственно на электродах.
Схема электрохромного устройства на фиг. 4 предполагает использование неорганических материалов для электрохромного электрода и противоэлектрода. Тем не менее, должно быть очевидно, что разработанные автором данного изобретения гель-полимерные электролиты могут с успехом использоваться и в устройствах на основе подходящих органических электрохромных материалов.
Электрохимические источники тока (аккумуляторы) с применением гель-полимерных электролитов на основе меламиновых сополимеров также были изготовлены автором данного изобретения с целью его экспериментальной проверки. Обобщенная схема этих устройств приведена на фиг. 5. В качестве примера использовалась электрохимическая система свинцово-кислотного аккумулятора. Раствор серной кислоты был заменен на гель-полимерный электролит, полученный путем формирования геля из исходного сополимера с добавлением H2SO4 близкой концентрации. Таким образом, все электрохимические процессы, происходящие в этом устройстве, были сходны с процессами в хорошо известном свинцово-кислотном аккумуляторе.
Из-за того, что ионная проводимость использованных гель-полимерных меламиновых электролитов не столь высока, как у обычного раствора серной кислоты, мощность, отдаваемая аккумулятором, была несколько ниже, чем у ячеек, собранных по классической схеме. Тем не менее, емкость аккумулятора оставалась неизменной, а его срок службы существенно вырос. Благодаря отсутствию жидкой фазы повышается стойкость аккумулятора к механическим воздействиям и растет безопасность его эксплуатации. Кроме того, такие аккумуляторы не требуют наличия сепаратора между электродами, поскольку эластичный гель-полимерный электролит идеально выполняет роль сепаратора и мембраны, исключая неправильную работу источника электрического тока.
Должно быть очевидно, что схема, подобная приведенной на фиг. 5, может использоваться для изготовления любых источников тока (включая первичные) с применением протон-проводящих электролитов.
Суперконденсаторы с применением гель-полимерных электролитов на основе меламиновых сополимеров также были изготовлены автором данного изобретения с целью его экспериментальной проверки. В качестве примера использовались простейшие симметричные суперконденсаторы с двойным электрическим слоем [24], [26], [27]. Обобщенная схема этих устройств приведена на фиг. 6. Электроды были выполнены из углеродной бумаги, а в качестве электролита был использован гель-полимер с концентрацией H2SO4, приблизительно равной 0,5-2,0 М. Применение сепаратора в этом случае также не требуется. Устройство нормально функционировало в диапазоне напряжений 0-1,2 В, а его характеристики оказались весьма близкими к характеристикам подобных устройств с применением кислотных электролитов. Удельная емкость полученных суперконденсаторов сильно зависела от пористости углеродной бумаги. Снижения емкости в течение 10000 циклов заряд-разряд зафиксировано не было.
Далее приведены примеры практической реализации изобретения.
Пример 1. Синтез этиленгликоль-меламин-формальдегидного концентрата ЭМФК-3-5 (50%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 15,52 г (0,25 моль) этиленгликоля, 4,86 г бутанола-1, 22,43 г воды и 5,00 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала совершенно прозрачной. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 50% раствор сополимера меламина с этиленгликолем смешивали с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,8-1,1 мл кислоты при охлаждении льдом и интенсивном перемешивании. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование прозрачного гель-полимера, обладающего протонной проводимостью, занимало от 7 до 24 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,56⋅10-1…1,5⋅10-1 См·cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,8% при толщине слоя полимера 1 мм.
Пример 2. Синтез глицерин-меламин-формальдегидного концентрата ГМФК-3-5 (50%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 23,02 г (0,25 моль) глицерина, 4,86 г бутанола-1, 29,93 г воды и 5,00 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала совершенно прозрачной. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 50% раствор сополимера меламина с глицерином смешивали с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,7-1,3 мл кислоты при охлаждении льдом и интенсивном перемешивании. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование прозрачного гель-полимера, обладающего протонной проводимостью, занимало от 7 до 48 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,56⋅10-1…1,48⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,9% при толщине слоя полимера 1 мм.
Пример 3. Синтез глицерин-меламин-формальдегидного концентрата ГМФК-3-5 (60%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 23,02 г (0,25 моль) глицерина, 4,86 г бутанола-1, 4,75 г воды и 5 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 0,5-2 минут и реакционная смесь стала совершенно прозрачной. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 60% раствор сополимера меламина с глицерином смешивали при охлаждении и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,7-1,3 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование прозрачного гель-полимерного электролита, обладающего протонной проводимостью, занимало от 5 до 48 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,55⋅10-1…1,59⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,8% при толщине слоя полимера 1 мм.
Пример 4. Синтез глицерин-меламин-формальдегидного концентрата ГМФК-3-5 (65%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 23,02 г (0,25 моль) глицерина, 4,86 г бутанола-1 и 0,20 г NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 0,5-2 минут и реакционная смесь стала совершенно прозрачной. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 65% раствор сополимера меламина с глицерином смешивали при охлаждении льдом и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,7-1,3 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование прозрачного гель-полимера, обладающего протонной проводимостью, занимало от 5 до 36 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,35⋅10-1…1,50⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,8% при толщине слоя полимера 1 мм.
Пример 5. Синтез полиэтиленгликоль (400)-глицерин-меламин-формальдегидного концентрата ПЭГ-ГМФК-3-5 (50%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 21,87 г (0,24 моль) глицерина, 5,00 г (0,05 моль) ПЭГ-400, 4,86 г бутанола-1, 33,78 г воды и 5,00 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала совершенно прозрачной. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 50% раствор сополимера меламина с глицерином и ПЭГ-400 смешивали при охлаждении льдом и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,7-1,3 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование прозрачного гель-полимера, обладающего протонной проводимостью, занимало от 5 до 72 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,64⋅10-1…2,00⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,5% при толщине слоя полимера 1 мм.
Пример 6. Синтез полипропиленгликоль-глицерин-меламин-формальдегидного концентрата ПГ-МФК-3-5 (50%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 19,02 г (0,25 моль) пропиленгликоля, 4,86 г бутанола-1, 26,94 г воды и 5,00 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала совершенно прозрачной. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 50% раствор сополимера меламина с пропиленгликолем смешивали при охлаждении льдом и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,7-1,4 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование прозрачного гель-полимера, обладающего протонной проводимостью, занимало от 12 до 120 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,2⋅10-1…1,7⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,5% при толщине слоя полимера 1 мм.
Пример 7. Синтез полиэтиленгликоль (400)-меламин-формальдегидного концентрата ПЭГ-МФК-3-7 (70%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 100 г (0,25 моль) ПЭГ-400, 4,86 г бутанола-1, 19,75 г воды и 5,00 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала совершенно прозрачной. Реакцию вели 7 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 50% раствор сополимера меламина с ПЭГ-400 смешивали при охлаждении льдом и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,8-1,2 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование прозрачного гель-полимера, обладающего протонной проводимостью, занимало от 48 до 120 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,51⋅10-1…1,62⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,3% при толщине слоя полимера 1 мм.
Пример 8. Синтез полиэтиленгликоль (400)-полипропиленгликоль-крахмал-формальдегидного концентрата ПЭГ-ППГ-крахмал-МФК-3-5 (61%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 32,46 г (0,26 моль) меламина, 13 г (0,03 моль) ПЭГ-400, 11,67 г (0,13 моль) пропиленгликоля, 1,19 г катионного крахмала, 4,86 г бутанола-1 и 0,10 г NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала прозрачной с небольшой опалесценцией. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 61% раствор сополимера смешивали при охлаждении льдом и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,5-2,0 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование гель-полимера, обладающего протонной проводимостью, занимало от 48 до 120 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,38⋅10-1…1,80⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 98,5% при толщине слоя полимера 1 мм. Образовавшийся гель обладал заметной опалесценцией.
Пример 9. Синтез сахароза-этиленгликоль-меламин-формальдегидного концентрата Сахар-ЭМФК-3-5 (60%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 11,15 г (0,2 моль) этиленгликоля, 17,1 г (0,05 моль) сахарозы, 4,86 г бутанола-1, 9,05 мл H2O и 5,00 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала прозрачной. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 60% раствор полимера смешивали при охлаждении льдом и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,7-1,5 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование гель-полимера, обладающего протонной проводимостью, занимало от 12 до 48 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,55⋅10-1…1,80⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,0% при толщине слоя полимера 1 мм.
Пример 10. Синтез карбоксиметилцеллюлоза-этиленгликоль-меламин-формальдегидного концентрата КМЦ-ЭМФК-3-3 (18%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 11,17 г (0,18 моль) этиленгликоля, 16,81 г (0,07 моль) натриевой соли карбоксиметилцеллюлозы (КМЦ), 4,86 г бутанола-1 и 453,90 мл воды. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 2-5 минут и реакционная смесь стала прозрачной. Реакцию вели 3 часа при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 18% раствор полимера смешивали при охлаждении льдом и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,7-3,5 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование гель-полимера, обладающего протонной проводимостью, занимало от 12 до 160 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,60⋅10-1…2,40⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,3% при толщине слоя полимера 1 мм.
Пример 11. Синтез сахароза-гидроксиэтилцеллюлоза-этиленгликоль-меламин-формальдегидного концентрата Сахароза-ГЭЦ-ЭМФК-3-3 (25%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 9,31 г (0,15 моль) этиленгликоля, 23,94 г (0,07 моль) сахарозы, 2,00 г гидроксиэтилцеллюлозы (ГЭЦ), 4,86 г бутанола-1, 217,69 мл H2O и 5,00 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала прозрачной. Реакцию вели 3 часа при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 25% раствор полимера смешивали при охлаждении льдом и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,5-3,5 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование прозрачного гель-полимера, обладающего протонной проводимостью, занимало от 12 до 160 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,35⋅10-1…2,50⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,6% при толщине слоя полимера 1 мм.
Пример 12. Синтез сахароза-поливиниловый спирт-этиленгликоль-меламин-формальдегидного концентрата Сахароза-ПВС-ЭМФК-3-5 (60%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 9,31 г (0,15 моль) этиленгликоля, 23,94 г (0,07 моль) сахарозы, 4,86 г бутанола-1, 3,50 г поливинилового спирта (ПВС), 217,69 мл воды и 5,00 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала прозрачной. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 60% раствор полимера смешивали при охлаждении льдом и интенсивном перемешивании с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,5-2,0 мл кислоты. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование гель-полимера, обладающего протонной проводимостью, занимало от 12 до 78 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,44⋅10-1…1,60⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,8% при толщине слоя полимера 1 мм.
Пример 13. Синтез глиоксаль-этиленгликоль-меламин-формальдегидного концентрата глиоксаль-ЭМФК-3-5 (50%)
В трехгорбую колбу, снабженную мешалкой, обратным холодильником и термометром, поместили 31,53 г (0,25 моль) меламина, 15,52 г (0,25 моль) этиленгликоля, 36,28 г (0,25 моль) глиоксаля, 4,86 г бутанола-1, 10,17 г воды и 10,00 г 2% раствора NaOH. Содержимое нагрели при перемешивании до 85-90°C, затем добавили 56,76 г (0,70 моль) предварительно нагретого до 50°С 37% раствора формалина, при этом следили за тем, чтобы температура реакционной смеси не опускалась ниже 70°С. Меламин растворился в течение 1-2 минут и реакционная смесь стала совершенно прозрачной. Реакцию вели 5 часов при температуре 80-85°C. Затем реакционную смесь быстро (менее чем за 10 минут) охладили до комнатной температуры. Полученный 50% раствор сополимера смешивали с концентрированной соляной кислотой в соотношении 5,0 мл раствора к 0,7-1,5 мл кислоты при охлаждении льдом и интенсивном перемешивании. Образовавшийся прозрачный раствор помещали в электрохромную ячейку в качестве электролита. Образование гель-полимера, обладающего протонной проводимостью, занимало от 7 до 48 ч.
Проводимость полученного гель-полимерного электролита находилась в диапазоне 1,53⋅10-1…1,55⋅10-1 См⋅cм-1, в зависимости от количества добавленной кислоты. Прозрачность в видимом диапазоне длин волн составляла T380-780 = 99,5% при толщине слоя полимера 1 мм.
Теоретический анализ и эксперименты, проведенные автором данного изобретения, показали, что для получения прозрачных протон-проводящих полимерных электролитов возможно использовать и другие сильные протонные кислоты, например, неорганические - H2SO4, H3PO4, HBr, HF, HBF4, CF3SO3H или органические - CH2ClCOOH, CCl3COOH, CF3COOH.
На первой стадии реакции образуется продукт взаимодействия меламина с тремя молями формалина - триметилол (A) (фиг. 1). Данный продукт является весьма реакционноспособным и поэтому легко вступает в реакцию с практически любыми соединениями, содержащими гидроксильные и аминогруппы (органическими аминами, спиртами, полиолами, моносахаридами, олигосахаридами и полисахаридами, а также с любыми многоосновными органическими кислотами или их ангидридами), образуя соответствующие сополимеры, графт-полимеры и их смеси, которые при взаимодействии с кислотами превращаются в гель-полимерные электролиты (Б) (фиг. 2).
В приведенных выше примерах полиолы представлены глицерином, этиленгликолем, полиэтиленгликолем и поливиниловым спиртом. При этом возможно применение и других многоатомных спиртов, например, пропиленгликоля, полипропиленгликоля, полиэтиленоксида и т.д. Физические возможности автора изобретения не позволяют провести эксперименты со всеми существующими в природе полиолами, тем не менее, возможность их применения в данном изобретении следует из общности химических свойств полиолов, как это должно быть очевидно специалисту.
В приведенных выше примерах моносахариды и олигосахариды обобщенно представлены сахарозой. Тем не менее, возможно применение и других коротких сахаридов - моносахаридов (например, глюкозы, фруктозы), дисахаридов (например, лактозы, мальтозы, изомальтозы), трисахаридов (например, глицеральдегида, мальтотриозы, рафинозы), тетрасахаридов (например, стахиозы, лихиозы, мальтотетраозы) и т.д. Как отмечено выше в отношении полиолов, физические возможности автора изобретения не позволяют провести эксперименты со всеми существующими в природе моносахаридами и олигосахаридами, тем не менее, возможность их применения в данном изобретении следует из общности химических свойств моносахаридов и олигосахаридов, как это должно быть очевидно специалисту.
В приведенных выше примерах полисахариды и их производные представлены натриевой солью карбоксиметилцеллюлозы (в качестве представителя карбоксилатных соединений) и гидроксиэтилцеллюлозой. При этом возможно применение и других производных полисахаридов, например, гидроксипропил-, гидроксиметил- и метилцеллюлозы. Как отмечено выше в отношении полиолов и сахаридов, физические возможности автора изобретения не позволяют провести эксперименты со всеми существующими в природе полисахаридами и их производными, в частности, получаемых из целлюлозы, крахмала или хитина, тем не менее, возможность их применения в данном изобретении следует из общности химических свойств полисахаридов и их производных, как это должно быть очевидно специалисту.
Пример 14. Электрохромное устройство с электродами на основе WO2,9:Al:C:N и СеO2:Zr
Материал электрохромного электрода толщиной 500 нм на основе WO2,9:Al:C:N толщиной 500 нм и материал противоэлектрода толщиной 300 нм на основе СеO2:Zr были нанесены на подложки из FTO-стекла методом магнетронного напыления. Свежеприготовленный раствор меламинового сополимера из примера 12 был смешан с концентрированной серной кислотой и помещен между электродами. В результате возникшей реакции дальнейшей полимеризации меламинового сополимера был получен эластичный прозрачный гель-полимерный электролит. Полученная таким образом электрохромная ячейка была работоспособна при потенциале ± 1,0 В. При приложении к электрохромному электроду отрицательного потенциала он окрашивался, а при смене полярности - обесцвечивался. Максимальная разность пропускной способности в видимом диапазоне длин волн для окрашенного и обесцвеченного состояний составила ΔT380-780 = 40%.
Пример 15. Свинцово-кислотный аккумулятор с гель-полимерным электролитом
Свежеприготовленный раствор меламинового сополимера из примера 9 был смешан с концентрированной серной кислотой и помещен в обычную свинцово-кислотную аккумуляторную батарею с номинальным напряжением 12 В без электролита. Концентрация H2SO4 составляла не менее 37%. Непосредственно в самой батарее протекала реакция более глубокой полимеризации первоначального сополимера, в результате которой был получен эластичный прозрачный гель-полимерный электролит, расположенный между электродами из свинца и оксида свинца PbO2. Процесс перехода в состояние проводящего геля занимал от 10 до 12 ч. Свинцово-кислотный аккумулятор был работоспособен в нормальных условиях с напряжением на ячейке от 1,80 В в разряженном состоянии до 2,25 В в полностью заряженном состоянии (непосредственно после зарядки). Емкость аккумулятора соответствовала его номинальной емкости по паспорту с изначально предназначенным для него обычным электролитом, содержащим 37-40% серной кислоты.
Пример 16. Симметричный суперконденсатор с протонным гель-полимерным электролитом
Свежеприготовленный раствор меламинового сополимера из примера 9 был смешан с концентрированной серной кислотой и помещен между двумя листами специальной углеродной бумаги с высокопористой поверхностью из активированного угля. Концентрация H2SO4 составляла 0,5-2,0 M. В результате запущенной таким образом реакции более глубокой полимеризации был получен эластичный прозрачный гель-полимерный электролит, расположенный между углеродными электродами. Сформированный таким образом симметричный суперконденсатор демонстрировал работоспособность в диапазоне 0-1,2 В и имел обычные значения емкости для этого типа конденсаторов с двойным электрическим слоем.
Список литературы
[1] Ayushi Choudhary, Eswara Prasad. Electrochromic glass market by application (windows, mirror, and display) and end-user industry (construction, automotive, aerospace, and others): Global Opportunity Analysis and Industry Forecast, 2020-2027, Allied Market Research, June 2020.
[2] Smart glass and smart window market report 2019-2029, Visiongain, July 2019.
[3] H. Iwahara. Oxide-ionic and protonic conductors based on perovskite-type oxides and their possible applications. Solid State Ionics, vol. 52, no. 1-3, pp. 99-104, May 1992.
[4] S. Oukassi, C. Giroud-Garampon, C. Dubarry, C. Ducros, R. Salot. All inorganic thin film electrochromic device using LiPON as the ion conductor. Solar Energy Materials and Solar Cells, vol. 145, pp. 2-7, July 2015.
[5] Y. Wang et al. Design principles for solid-state lithium superionic conductors. Nature Materials, vol. 14, no. 10, pp. 1026-1031, August 2015.
[6] F. Alloina, C. Iojoiu. Composite polymer electrolytes for electrochemical devices. Polymer Electrolytes. Fundamentals and Applications, 2010, pp. 129-175.
[7] N.A. Choudhury, A.K. Shukla, S. Sampath, S. Pitchumani. Cross-linked polymer hydrogel electrolytes for electrochemical capacitors. Journal of Electrochemical Society, vol. 153, no. 3, 2006.
[8] J.B. Kerr. Polymeric electrolytes: an overview. Lithium Batteries: Science and Technology, G.-A. Nazri, G. Pistoia, Eds. Boston, MA: Springer US, 2003, pp. 575-622.
[9] K.S. Ngai, S. Ramesh, K. Ramesh, J.C. Juan. A review of polymer electrolytes: fundamental, approaches and applications. Ionics, vol. 22, pp. 1259-1279, 2016.
[10] W. Wang, P. Alexandridis. Composite polymer electrolytes: nanoparticles affect structure and properties. Polymers, vol. 8, no. 11, 2016.
[11] P. Ghosh, C.K. Dhole, S. Ganguly, D. Banerjee, K. Kargupta. Portable smart highly proton conductive all inorganic gel paste electrolyte with optimum phosphorous to silicon ratio for enhanced durable operation of a fuel cell. Sustainable Energy & Fuels, 2018, no. 2, pp. 1737-1748.
[12] V.K. Thakur, G. Ding, J. Ma, P.S. Lee, X. Lu. Hybrid materials and polymer electrolytes for electrochromic device applications. Advanced Materials., vol. 24, no. 30, pp. 4071-4096, 2012.
[13] W. Ma et al. Cross-linked aromatic cationic polymer electrolytes with enhanced stability for high temperature fuel cell applications. Energy & Environmental Science, vol. 5, no. 6, pp. 7617-7625, 2012.
[14] G. Wang et al. Gel polymer electrolytes based on polyacrylonitrile and a novel quaternary ammonium salt for dye-sensitized solar cells. Materials Research Bulletin, vol. 39, no. 13, pp. 2113-2118, 2004.
[15] US2345543A Cationic melamine-formaldehyde resin solution, 1942.
[16] B. Bann, S.A. Miller. Melamine and Derivatives of Melamine. Chemical Reviews, vol. 58, no. 1, pp. 131-172, 1958.
[17] D.J. Merline, S. Vukusic, A.A. Abdala. Melamine formaldehyde: curing studies and reaction mechanism. Polymer Journal, vol. 45, no. 4, pp. 413-419, 2013.
[18] J. K. Fink. Melamine Resins. In: Reactive Polymers: Fundamentals and Applications. A Concise Guide to Industrial Polymers. Second edition, pp. 193-201, 2013.
[19] K. Bretterbauer, C. Schwarzinger. Melamine derivatives - a review on synthesis and application. Current Organic Synthesis, 9(3):342, pp. 342-356, 2012.
[20] C. Du Fresne Von Hohenesche, D.F. Schmidt, V. Schodler. Nanoporous melamine- formaldehyde gels by microemulsion templating. Chemical Materials, vol. 20, no. 19, pp. 6124-6129, 2008.
[21] K. Shijina et al. Melamine formaldehyde-metal organic gel interpenetrating polymer network derived intrinsic Fe-N-doped porous graphitic carbon electrocatalysts for oxygen reduction reaction. New Journal of Chemistry, vol. 42, no. 23, pp. 18690-18701, 2018.
[22] K. Mishra, S. A. Hashmi, D. K. Rai. Studies on a proton battery using gel polymer electrolyte. High Performance Polymers, vol. 26, no. 6, pp. 672-676, 2014.
[23] C. Zhong, Y. Deng, W. Hu, J. Qiao, L. Zhang, J. Zhang. A review of electrolyte materials and compositions for electrochemical supercapacitors. Chemical Society Reviews, vol. 44, no. 21, pp. 7484-7539, 2015.
[24] Abraham J. Domb, Joseph Kost, David M. Wiseman. Handbook of Biodegradable Polymers. First Edition. CRC Press, 2019.
[25] W. Chen et al. A novel ionically crosslinked gel polymer electrolyte as an ion transport layer for high-performance electrochromic devices. Journal of Materials Chemistry C, vol. 7, no. 13, pp. 3744-3750, 2019.
[26] L.N. Han, X. Wei, Q. C. Zhu, S. M. Xu, K. X. Wang, J. S. Chen. Nitrogen-doped carbon nets with micro/mesoporous structures as electrodes for high-performance supercapacitors. Journal of Materials Chemistry A, vol. 4, no. 42, pp. 16698-16705, 2016.
[27] J.A. Fernendez, T. Morishita, M. Toyoda, M. Inagaki, F. Stoeckli, T.A. Centeno. Performance of mesoporous carbons derived from poly(vinyl alcohol) in electrochemical capacitors. Journal of Power Sources, vol. 175, no. 1-3, pp. 675-679, 2008.
| название | год | авторы | номер документа |
|---|---|---|---|
| Электрохромное устройство | 1981 |
|
SU1126212A3 |
| ЭЛЕКТРОЛИТНЫЙ МАТЕРИАЛ ЭЛЕКТРОУПРАВЛЯЕМОГО УСТРОЙСТВА, СПОСОБ ЕГО ПОЛУЧЕНИЯ, СОДЕРЖАЩЕЕ ЕГО ЭЛЕКТРОУПРАВЛЯЕМОЕ УСТРОЙСТВО И СПОСОБ ПОЛУЧЕНИЯ УКАЗАННОГО УСТРОЙСТВА | 2007 |
|
RU2453883C2 |
| ПОЛИМЕРНОЕ ЭЛЕКТРОХРОМНОЕ УСТРОЙСТВО | 2012 |
|
RU2528841C2 |
| ЭЛЕКТРОПРОВОДЯЩИЙ АДГЕЗИВ ДЛЯ ЭЛЕКТРОХРОМНЫХ УСТРОЙСТВ | 2013 |
|
RU2524963C1 |
| Протонпроводящие полимерные мембраны и способ их получения | 2023 |
|
RU2797133C1 |
| СТАБИЛЬНЫЙ ЭЛЕКТРОХРОМНЫЙ МОДУЛЬ | 2012 |
|
RU2587079C2 |
| АМИНОПЛАСТОВАЯ ИЛИ ФЕНОПЛАСТОВАЯ СМОЛА НА ОСНОВЕ, ПО МЕНЬШЕЙ МЕРЕ, ОДНОГО МОНОАЦЕТАЛЯ ГЛИОКСАЛЯ И ГЛИОКСИЛОВОЙ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2434026C2 |
| ЭЛЕКТРОХРОМНОЕ УСТРОЙСТВО | 2019 |
|
RU2810917C1 |
| ПРОППАНТЫ ДЛЯ ПРИМЕНЕНИЯ В ГИДРАВЛИЧЕСКОМ РАЗРЫВЕ ПОДЗЕМНЫХ ПЛАСТОВ | 2011 |
|
RU2566347C2 |
| ПРИВИТЫЕ ПОЛИМЕРЫ НА ОСНОВЕ ПОЛИСАХАРИДОВ И/ИЛИ ПОЛИПЕПТИДОВ В КАЧЕСТВЕ СИНТЕТИЧЕСКИХ ТАНИНОВ | 2012 |
|
RU2603139C2 |

Изобретение относится к гель-полимерным электролитам. Предложен способ получения гель-полимерных оптически прозрачных электролитов, включающий в себя реакцию сополимеризации меламина и формальдегида или меламина и глиоксаля с одним или несколькими полиолами и добавление сильной протонной кислоты при концентрации кислоты от 3,0 до 7,5% или от 10,0 до 40,0% в растворе сополимера для образования оптически прозрачного гель-полимера. Предложены также варианты указанного способа. Предложенный способ позволяет получать гель-полимерные электролиты с отличной оптической прозрачностью, высокой ионной проводимостью, незначительной усадкой и хорошей адгезией к различным материалам. Электролит согласно изобретению может применяться в электрохромных устройствах и иных оптико-электрохимических устройствах, а также в устройствах для хранения электрической энергии (аккумуляторах, суперконденсаторах и гибридных накопителях) вместо традиционных электролитов на водной основе. 3 н. и 14 з.п. ф-лы, 6 ил., 16 пр.
1. Способ получения гель-полимерных электролитов с протонной проводимостью, включающий в себя следующие действия:
- проводят реакцию сополимеризации меламина и формальдегида или меламина и глиоксаля с одним или несколькими полиолами;
- добавляют сильную протонную кислоту при концентрации кислоты от 3,0 до 7,5% или от 10,0 до 40,0% в растворе сополимера для образования оптически прозрачного гель-полимера.
2. Способ по п. 1, в котором полиол представляет собой одно или несколько веществ из следующей группы: глицерин, этиленгликоль, пропиленгликоль, полиэтиленгликоль, полипропиленгликоль, полиэтиленоксид, поливиниловый спирт.
3. Способ по п. 1, в котором кислота представляет собой органическую кислоту.
4. Способ по п. 1, в котором кислота представляет собой неорганическую кислоту.
5. Способ получения гель-полимерных электролитов с протонной проводимостью, включающий в себя следующие действия:
- проводят реакцию сополимеризации меламина или формальдегида с одним или несколькими моносахаридами, олигосахаридами, полисахаридами и/или их производными;
- добавляют сильную протонную кислоту при концентрации кислоты от 3,0 до 7,5% или от 10,0 до 40,0% в растворе сополимера для образования оптически прозрачного гель-полимера.
6. Способ по п. 5, в котором полисахарид представляет собой одно или несколько веществ из следующей группы: крахмал, целлюлоза, хитин.
7. Способ по п. 6, в котором производные полисахарида представляют собой карбоксилатные соединения.
8. Способ по п. 6, в котором производные полисахарида представляют собой эфиры.
9. Способ по п. 5, в котором кислота представляет собой органическую кислоту.
10. Способ по п. 5, в котором кислота представляет собой неорганическую кислоту.
11. Способ получения гель-полимерных электролитов с протонной проводимостью, включающий в себя следующие действия:
- проводят реакцию сополимеризации меламина и формальдегида или меламина и глиоксаля с одним или несколькими полиолами и с одним или несколькими моносахаридами, олигосахаридами или полисахаридами и/или их производными;
- добавляют сильную протонную кислоту при концентрации кислоты от 3,0 до 7,5% или от 10,0 до 40,0% в растворе сополимера для образования оптически прозрачного гель-полимера.
12. Способ по п. 11, в котором полиол представляет собой одно или несколько веществ из следующей группы: глицерин, этиленгликоль, пропиленгликоль, полиэтиленгликоль, полипропиленгликоль, полиэтиленоксид, поливиниловый спирт.
13. Способ по п. 11, в котором полисахарид представляет собой одно или несколько веществ из следующей группы: крахмал, целлюлоза и хитин.
14. Способ по п. 13, в котором производные полисахаридов представляют собой карбоксилатные соединения.
15. Способ по п. 13, в котором производные полисахаридов представляют собой эфиры.
16. Способ по п. 11, в котором кислота представляет собой органическую кислоту.
17. Способ по п. 11, в котором кислота представляет собой неорганическую кислоту.
| US 7842637 B2, 30.11.2010 | |||
| ЛЮМИНОФОРНАЯ СМЕСЬ ДЛЯ НАНЕСЕНИЯ НА СТЕКЛЯННЫЕ КОЛБЫ ИСТОЧНИКОВ ОПТИЧЕСКОГО ИЗЛУЧЕНИЯ | 2000 |
|
RU2201636C2 |
| US 5081163 A1, 14.01.1992 | |||
| Pawlica A | |||
| et al | |||
| "Influence of Plasticizer Type on the Properties of Polymer Eletrolytes based on Chitosan", Journal of Physical Chemistry A, 2008, vol | |||
| Прялка для изготовления крученой нити | 1920 |
|
SU112A1 |
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| Штопальный прибор | 1925 |
|
SU8888A1 |
| KR 20120049748 A, 17.05.2012. | |||
Авторы
Даты
2024-05-03—Публикация
2020-10-23—Подача