Изобретение относится к медицине, к абдоминальной хирургии, а именно к хирургии печени и может быть использовано для подготовки операций по её безопасной резекции.
В настоящее время хирургическое лечение является методом выбора при первичных и метастатических злокачественных опухолях печени. В случае необходимости выполнения обширных резекций печени в ситуациях, когда поражение печени сочетается с патологически изменённой паренхимой на фоне стеатогепатоза или цирроза печени, последствий химиотерапии или же имеется недостаточный объем остающейся после резекции культи печени, существует высокий риск развития различных осложнений. Наиболее часто встречающимся, и тяжелым из которых является пострезекционная печеночная недостаточность.
К сегодняшнему дню разработано и апробировано в клинической практике множество хирургических методик профилактики развития пострезекционной печеночной недостаточности. Приведем в качестве примеров используемые наиболее часто:
1. С 2012 года известен способ двухэтапной резекции печени, получивший название по аббревиатуре ALPPS (от английского Associated Liver Partition and Portal vein ligation for Staged hepatectomy).
Методика ALPPS заключается в выполнении перевязки правой воротной вены и последующего разделения паренхимы печени по линии предполагаемой резекции до нижней полой вены с сохранением артериального кровотока и венозного оттока удаляемой доли печени.
Недостатком используемого способа является высокая травматичность проводимой операции и большое количество осложнений (основной причиной 90-дневной смертности была послеоперационная печеночная недостаточность у 75% пациентов [1]). Также в виду сохранения венозного оттока от пораженной доли печени сохраняется возможность системной диссеминации опухоли.
2. Другим способом профилактики развития пострезекционной печеночной недостаточности является предоперационная эмболизация воротной вены [2]. Эмболизация воротной вены - это процедура, в ходе которой блокируется ток воротной крови к доле печени. В результате та часть печени, в которой находятся опухоли, уменьшается. Ввиду перераспределения кровотока большее количество крови поступает в непораженную часть печени, что вызывает активизацию клеточной пролиферации и печень начинает увеличиваться в размерах, также функциональная активность её значительно возрастает, процессы при викарной гипертрофии печени вследствие перераспределения кровотока описаны в литературе [3, 4, 5].
Существенным недостатком этого способа является частое наличие ограничений по выявлению акустического доступа для ультразвуковой визуализации трассы пункции воротной вены и введения эмболизирующего агента, также аллергические и анафилактические реакции на эмболизат, содержащий контрастное вещество, на введение которого, в свою очередь, может развиваться тяжелая почечная дисфункция. Существенной и не редкой является ситуация неэффективности первой процедуры эмболизации за счет реканализации эмболизированной ветви воротной вены или если при первичной процедуре эмболизации не затронута эмболизатом ветвь воротной вены 4 сегмента печени. Эта ситуация требует повторных процедур эмболизации либо приводит к полному отказу от хирургического лечения основного заболевания.
При эмболизации воротной вены прекращение кровотока в пораженной области достигается не полным блоком магистрального венозного элемента, а, в основном, повреждающим воздействием химических агентов преимущественно на периферическую венозную систему печени (перисинусоидальные вены) [7]. Недостатком этого способа является и то, что сохраняется отток крови через печеночную вену в кавальных воротах в систему нижней полой вены, что способствует отдаленному гематогенному метастазированию и требует осуществлять второй этап хирургического лечения в сжатые сроки с позиций онкологической целесообразности (этапное хирургическое лечение в стандартном варианте осуществляется через 4 недели после эмболизации воротной вены.
Также сохраняется артериальной кровоснабжение пораженной доли печени и, тем самым, конверсия кровотока в контралатеральную долю печени является неполной, что замедляет процесс викарной гипертрофии.
3. Известен способ лигирования правой ветви воротной вены при лапаротомной операции с целью редукции кровотока и формирования викарной гипертрофии остающейся культи печени.
Техника операции заключается в нижеследующем: выполняется перевязка правой ветви воротной вены, которая не отличается от аналогичного этапа в ходе правосторонней гемигепатэктомии, когда при выполненной верхнесреднесрединной лапаротомии, дополненной поперечным разрезом в правой мезогастральной области, и после холецистэктомии производится выделение воротной вены правой доли печени путем отслойки глиссоновой капсулы печени от воротной пластинки гепатодуоденальной связки, далее вена перевязывается лигатурой. При этом суть лигирования вены состоит в полном прекращении кровотока в правой доле печени. В результате достигается полное прекращение кровотока к пораженной анатомической единице печени и преимущественное перераспределение кровотока в пользу контрлатеральной доли печени [6, 7].
Недостатком этого способа является то, что сохраняется отток крови через печеночную вену в кавальных воротах в систему нижней полой вены, что способствует отдаленному гематогенному метастазированию и требует осуществлять второй этап хирургического лечения в сжатые сроки с позиций онкологической целесообразности этапное хирургическое лечение в стандартном варианте осуществляется через 4 недели после лигирования воротной вены. Также сохраняется артериальной кровоснабжение пораженной доли печени и, тем самым, конверсия кровотока в контралатеральную долю печени является неполной, что замедляет процесс викарной гипертрофии.
Техническим результатом предлагаемого изобретения является минимизация риска развития пострезекционной печеночной недостаточности, уменьшение рисков отдаленного метастазирования, расширение допустимых сроков ожидания формирования викарной гипертрофии в случаях, когда прирост печени замедлен (стеатогепатоз, наличие последствий химиотерапии, цирротически измененная паренхима органа).
Предлагается способ воротно- кавального разобщения кровотока правой доли печени под эндотрахеальным наркозом с целью формирования условий для её резекции включающий проведение предоперационного клинико-лабораторного и рентгенологического обследования, расчета объема печени, предполагаемой к резекции и планируемого остатка печени путем КТ-волюмометрии.
Выполняется верхне-срединная лапаротомия с расширением доступа вправо, ревизия органов брюшной полости, мобилизация правой доли печени путем пересечения треугольной, венечной и серповидной связок, мобилизация элементов гепатодуоденальной связки: выделение по всей окружности правой ветви воротной вены, с обязательной дифференцировкой, визуализацией и выделением вены четвертого сегмента печени, а также правой печеночной артерии, лигированием правой ветви воротной вены проксимальнее отхождения вены четвертого сегмента с отдельным лигированием последней, без их пересечения, лигированием правой ветви печеночной артерии. Также способ отличается тем, что в области кавальных ворот печени путем прецизионной техники выделяется правая печеночная вена по всей окружности, затем лигируется путем наложения полимерной нити без пересечения.
Достигается технический результат за счет создания викарной гипертрофии интактной печени, то есть увеличения функционального и анатомического объема планируемого остатка печени, путем перераспределения кровотока в «остающуюся» долю печени и создания условий для последующего безопасного выполнения радикальной резекции печени. При этом значимо уменьшаются риски развития пострезекционной печеночной недостаточности, инкурабельная группа пациентов переводится в хирургически операбельную.
Отличительной особенностью способа является то, что за счет его осуществления снижаются риски отдаленного метастазирования опухоли гематогенным путем. Удается предупредить рост опухоли в отключенных сегментах печени, путем уменьшения артериального притока и, тем самым, расширяются возможные безопасные сроки выжидания формирования викарной гипертрофии.
Предлагаемый способ воротно-кавального разобщения кровотока правой доли печени с целью формирования условий для её резекции, включающий проведение предоперационного клинико-лабораторного и рентгенологического обследования, расчета объема печени методом компьютерной томографии (предполагаемой к резекции и планируемого остатка печени).
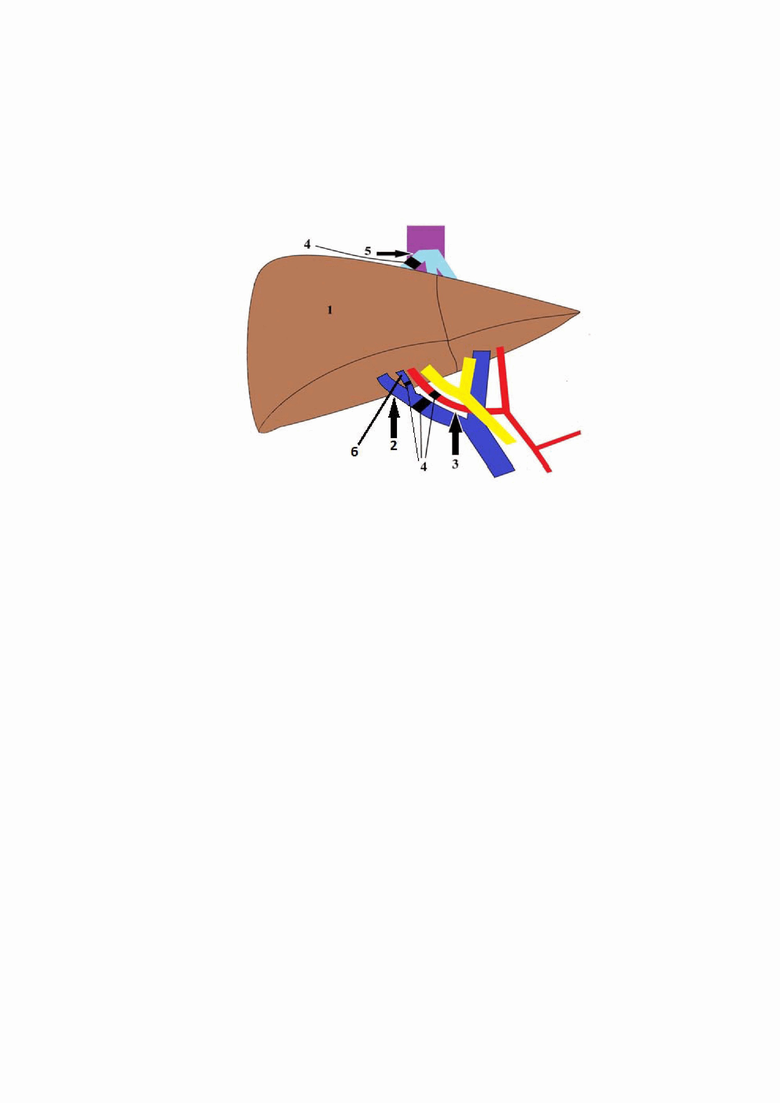
Осуществление способа: под эндотрахеальным наркозом выполняется верхне-срединная лапаротомия с расширением доступа вправо, ревизия органов брюшной полости, мобилизация правой доли печени (1) путем пересечения треугольной, венечной и серповидной связок, мобилизация элементов гепатодуоденальной связки: выделение по всей окружности правой ветви воротной вены (2), с обязательной дифференцировкой, визуализацией и выделением вены 4 сегмента печени (6), правой печеночной артерии (3) с последующим раздельным лигированием путем наложения полимерной нити правой печеночной артерии, правой ветви воротной вены проксимальнее отхождения вены 4 сегмента с отдельным лигированием последней (6), без их пересечения (для исключения риска соскальзывания лигатур и развития внутрибрюшного кровотечения), в области кавальных ворот путем прецизионной техники выделяется правая печеночная вена (5) по всей окружности, затем лигируется путем наложения полимерной нити без пересечения. На основании визуальных критериев (изменение окраски доли печени, формирование линии демаркации) подтверждается факт полного сосудистого выключения правой доли печени. Сущность предлагаемого изобретения показана на фиг. , где мобилизация правой доли печени показана 1, выделенная по всей окружности правая воротная вена показана 2, правая печеночная артерия показана 3, лигатуры показаны 4, выделение правой печеночной вены показано 5, ветвь воротной вены четвертого сегмента показано 6.
Предлагаемое изобретение отличается от указанных в тексте аналогов тем, что при проведении сосудистой изоляции собственным способом выполняется лапаротомия и лигируются все сосудистые элементы пораженной доли печени (тем самым достигается полная сосудистая изоляция пораженной доли печени), отсутствует этап разделения паренхимы печени по линии демаркации (что снижает травматичность процедуры за счет отсутствия существенной кровопотери и сокращения времени операции), который выполняется в дальнейшем при втором этапе хирургического лечения (этап резекции печени), нет строгой зависимости выполнения этапа резекции печени от временного промежутка в 4 недели с позиций онкологической целесообразности (за счет отсутствия магистрального венозного оттока в систему нижней полой вены от пораженной доли печени).
Таким образом, в случае цирроза печени или стеатоза паренхимы ожидание прироста остающейся после резекции доли печени продолжается и после достижения 4 недельного срока, что позволяет достичь больших объемов остатка печени ко второму этапу резекции печени в сравнении с другими способами без риска отдаленного метастазирования опухоли.
Преимущества предлагаемого изобретения заключаются в следующем:
1. Нет избыточной травматичности первого этапа хирургической операции как при ALLPS: не разделяем паренхиму за счет этого меньше кровопотеря, количество осложнений и летальность.
2. Задействованы 2 механизма гипертрофии печени (конверсия кровотока как венозного (воротная вена) так и артериального (печеночная артерия)).
3. Профилактируется диссеминация опухоли в системный кровоток за счет перевязки правой печеночной вены.
4. Возможны большие по времени безопасные сроки выжидания (относительно стандартных 4 недель) за счет окклюзии «кавальной» зоны оттока (правой печеночной вены).
5. Достигается уменьшение кровоточивости по линии резекции печени во время проведения второго этапа хирургического лечения, в области сформированной линии демаркации за счет обеднения кровотока резецируемой доли печени, что является следствием полной сосудистой изоляцией магистрального кровотока пораженной доли печени.
Заявленный технический результат, заключается в минимизации риска развития пострезекционной печеночной недостаточности, уменьшении риска отдаленного метастазирования, формирования условий для длительного выжидания викарной гипертрофии (более 4 недель). Достигается это за счет перераспределения кровотока печени, за счет лигирования всех магистральных сосудистых её элементов (долевой ветви воротной вены, долевой печеночной артерии, правой печеночной вены кавальных ворот), а также, за счет блока гематогенного компонента диссеминации опухоли печени, в силу полного прекращения тока венозной крови от пораженной доли печени в систему нижней полой вены.
Клинический пример
Пациент А, 33 года госпитализирован в Кузбасский гепатологический центр (КОГЦ) в 2015 году с диагнозом: эхинококкоз правой доли печени. В течение нескольких лет пациента беспокоила боль в правом подреберье давящего характера. Амбулаторно обследован. Выполнено УЗИ брюшной полости: в печени имеется очаговое образование до 16 см, занимающее практически всю правую долю печени. Выполнено МСКТ брюшной полости: в правой доле печени очаговое образование 19×16×17 см, с кальцинатами, не накапливающее контраст, объем левой доли печени 235 мл, что составляет 25% от общего объема печени, АФП крови повышен. Осмотрен хирургом-гепатологом в консультативной поликлинике, госпитализирован в КОГЦ для оперативного лечения. Учитывая объем поражения печени, пациенту показано выполнение правосторонней гемигепатэктомии, однако по данным МСКТ брюшной полости регистрируется малый объем левой доли печени (25 %), что может сказаться развитием тяжелой печеночной недостаточности в послеоперационном периоде в случае радикальной операции. По этой причине от выполнения расширенной резекции печени решено отказаться в пользу воротно-кавальной изоляции. Таким образом, с целью создания викарной гипертрофии левой доли печени первым этапом в июне 2015 года выполнена лапаротомия, сосудистая изоляция правой доли печени. Ход операции: верхне-срединная лапаротомия с расширением доступа вправо. В брюшной полости выпота нет. Признаков канцероматоза нет. Лимфоузлы паракавальной и парааортальной области не изменены. Печень увеличена правой долей за счет опухоли; в S4,5,6,7,8 печени тканевое образование с кальцинатами белесоватой окраски каменистой плотности; распространения на кавальные и портальные ворота печени нет. S1,2,3 печени небольших размеров, с признаками стеатоза. Выполнена биопсия из S3 сегмента печени, выполнена биопсия опухоли: ответ плановое патолого-гистологическое исследование - гепатоцеллярный рак. При ревизии: патологии желудка, тонкой и толстой кишки, органов малого таза и забрюшинного пространства не выявлено. Желчный пузырь обычной формы, размеров и окраски, пальпаторно - конкрементов не содержит. Холедох шириной 6 мм, не напряжен, пальпаторно - конкрементов в нем не определяется. Учитывая малые размеры левого латерального сектора печени, решено воздержаться от резекции печени. Мобилизация правой доли печени путем пересечения треугольной, венечной и серповидной связок, мобилизация элементов гепатодуоденальной связки: выделена по всей окружности правая ветвь воротной вены, вена четвертого сегмента печени, правая печеночная артерия, выполнена их лигирование путем перевязки полимерными нитями. В области кавальных ворот выделена правая печеночная вена по всей окружности, затем лигирована путем перевязки полимерной нитью. Отмечено появление линии демаркации на границе 4 сегмента печени. При дальнейшей ревизии патологии органов брюшной полости не выявлено. Санация брюшной полости. Страховой дренаж под печень. Счет материала и инструментария полный. Кровопотеря 100 мл. Послойное ушивание раны.
Список литературы
1. Schadde E, Raptis DA, Schnitzbauer AA, Ardiles V, Tschuor C, Lesurtel M, Abdalla EK, Hernandez-Alejandro R, Jovine E, Machado M, Malago M, Robles-Campos R, Petrowsky H, Santibanes ED, Clavien PA. Prediction of Mortality After ALPPS Stage-1: An Analysis of 320 Patients From the International ALPPS Registry. Ann Surg. 2015 Nov;262(5):780-5; discussion 785-6. doi: 10.1097/SLA.0000000000001450. PMID: 26583666.
2. П.Г. Тарасов, Д.А. Гранов, В.И. Сергеев, и др. Предоперационная эмболизация воротной вены при злокачественных опухолях печени. Анналы хирургической гепатологии, том 7, №1, 2002, стр.7-13.
3. Makuuchi M., Takayasu K., Takuma T. Preoperative transcatheter embolization of the portal venous branch for patients receiving extended lobectomy due to the bile duct carcinoma. J. Jap. Surg. Assoc. 1984; 45 (12): 1558–1564. doi: 10.3919/ringe1963.45.1558.
4. Takayasu K., Muramatsu Y., Shima Y., Moriyama N., Yamada T., Makuuchi M. Hepatic lobar atrophy following obstruction of the ipsilateral portal vein from hilar cholangiocarcinoma. Radiology. 1986; 160 (2): 389–393. doi: 10.1148/radiology.160.2.3014598.
5. Rous P., Larimore L. Relation of the portal blood to liver maintenance: a demonstration of liver atrophy conditional on compensation. J. Exp. Med. 1920; 31 (5): 609–637. PMID: 19868417.
6. Способ воротного доступа к сосудисто-секреторным элементам при анатомических сегментарных резекциях печени. Вишневский В.А. и соавт. Хирургия. 2008.-N 9.-С.33-40.
7. Л.О Полищук, О.Г. Скипенко. Окклюзия ветви воротной вены как метод наращивания объема левой доли печени: обзор литературы. Украинский журнал хирургии 1 (16), 2012.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ профилактики пострезекционной печеночной недостаточности | 2022 |
|
RU2798133C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПЕЧЕНОЧНОЙ НЕДОСТАТОЧНОСТИ ПОСЛЕ ОБШИРНЫХ РЕЗЕКЦИЙ ПЕЧЕНИ | 2013 |
|
RU2556514C2 |
| СПОСОБ ПАРЕНХИМОСОХРАНЯЮЩЕЙ ЛЕВОСТОРОННЕЙ ГЕМИГЕПАТЭКТОМИИ | 2019 |
|
RU2724205C1 |
| СПОСОБ ПАРЕНХИМОСОХРАНЯЮЩЕЙ ПРАВОСТОРОННЕЙ РАСШИРЕННОЙ ГЕМИГЕПАТЭКТОМИИ | 2017 |
|
RU2653637C1 |
| Способ лечения метастазов колоректального рака в печени | 2017 |
|
RU2663800C2 |
| СПОСОБ ЛЕВОСТОРОННЕЙ ГЕМИГЕПАТЭКТОМИИ | 2009 |
|
RU2416368C2 |
| СПОСОБ АНАТОМИЧЕСКОЙ РЕЗЕКЦИИ VIII СЕГМЕНТА ПЕЧЕНИ | 2009 |
|
RU2442539C2 |
| СПОСОБ АНАТОМИЧЕСКОЙ РЕЗЕКЦИИ IV СЕГМЕНТА ПЕЧЕНИ | 2009 |
|
RU2442541C2 |
| СПОСОБ АНАТОМИЧЕСКОЙ РЕЗЕКЦИИ V СЕГМЕНТА ПЕЧЕНИ | 2009 |
|
RU2442540C2 |
| СПОСОБ АНАТОМИЧЕСКОЙ РЕЗЕКЦИИ IV, V, VIII СЕГМЕНТОВ ПЕЧЕНИ | 2009 |
|
RU2444311C2 |
Изобретение относится к медицине, а именно к абдоминальной хирургии. Выполняют верхне-срединную лапаротомию с расширением доступа вправо. Выполняют ревизию органов брюшной полости. Мобилизуют правую долю печени путем пересечения треугольной, венечной и серповидной связок. Мобилизуют элементы гепатодуоденальной связки: выделяют по всей окружности правую ветвь воротной вены, с обязательной дифференцировкой, визуализацией и выделением вены четвертого сегмента печени, а также правую печеночную артерию. Выполняют лигирование правой ветви воротной вены проксимальнее отхождения вены четвертого сегмента с отдельным лигированием последней, без их пересечения. Лигируют правую ветвь печеночной артерии. В области кавальных ворот печени путем прецизионной техники выделяют правую печеночную вену по всей окружности, лигируют путем наложения полимерной нити без их пересечения. Способ позволяет выполнить воротно-кавальное разобщение кровотока правой доли печени, минимизировать риск развития пострезекционной печеночной недостаточности, уменьшить риск отдаленного метастазирования, расширить допустимые сроки ожидания формирования викарной гипертрофии в случаях, когда прирост печени замедлен при стеатогепатозе, наличии последствий химиотерапии, цирротически измененной паренхиме органа. 1 ил., 1 пр.
Способ воротно-кавального разобщения кровотока правой доли печени под эндотрахеальным наркозом с целью формирования условий для её резекции, включающий проведение предоперационного клинико-лабораторного и рентгенологического обследования, расчета объема печени, предполагаемой к резекции, и планируемого остатка печени путем КТ-волюмометрии, отличающийся тем, что выполняется верхне-срединная лапаротомия с расширением доступа вправо, ревизия органов брюшной полости, мобилизация правой доли печени путем пересечения треугольной, венечной и серповидной связок, мобилизация элементов гепатодуоденальной связки: выделение по всей окружности правой ветви воротной вены, с обязательной дифференцировкой, визуализацией и выделением вены четвертого сегмента печени, а также правой печеночной артерии, лигированием правой ветви воротной вены проксимальнее отхождения вены четвертого сегмента с отдельным лигированием последней, без их пересечения, лигированием правой ветви печеночной артерии, в области кавальных ворот печени путем прецизионной техники выделяется правая печеночная вена по всей окружности, затем лигируется путем наложения полимерной нити без пересечения.
| Способ профилактики пострезекционной печеночной недостаточности | 2022 |
|
RU2798133C1 |
| CN 109837300 A, 04.06.2019 | |||
| Загайнов Е.М | |||
| и др | |||
| Современные методы стимуляции викарной гипертрофии фрагмента печени перед обширной резекцией: оценка эффективности и пути улучшения результатов | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Schnitzbauer A.A | |||
| et al | |||
| / Right portal vein ligation combined with in situ | |||
Авторы
Даты
2024-05-21—Публикация
2023-10-06—Подача