Изобретение относится к области медицины, а именно к хирургической гепатологии, может быть использовано для лечения злокачественных опухолей печени и профилактики печеночной недостаточности после обширных резекций печени.
Печень является наиболее частым органом-мишенью для возможного метастазирования колоректального рака. Пятилетняя выживаемость у пациентов с колоректальным метастатическим поражением печени, не получавших специфического лечения, не превышает 2%, а медиана выживаемости колеблется от 6,6 до 10 месяцев. (Vigano L, Ferrero A, Lo Tesoriere R, Capussotti L. Liver surgery for colorectal metastases: results after 10 years of follow-up. Long-term survivors, late recurrences, and prognostic role of morbidity. Ann Surg Oncol. 2008 Sep; 15). В настоящее время смертность после резекции печени составляет менее 6%. Наиболее частая причина послеоперационной летальности - острая печеночная недостаточность (Wang X, Hershman DL, Abrams JA, Feingold D, Grann VR, Jacobson JS, Neugut AI. Predictors of survival after hepatic resection among patients with colorectal liver metastasis. Br J Cancer. 2007 Dec 17;97(12):1606-12. Epub 2007 Dec 11).
Известен способ профилактики и лечения острой печеночной недостаточности после гемигепатэктомий (С.Н. Бочаров. Печеночная недостаточность после гемигепатэктомий (патогенез, клиника, диагностика, профилактика и лечение): Автореф. дисс. д-ра мед. наук. - СПб., 1994. - 32 с.), включающий коррекцию реологических свойств крови и транскапиллярного обмена. Коррекция реологических свойств крови включает проведение ранней гепаринизации - использование гепарина через 6 часов после завершения операции. Стартовая доза составляет 100 ЕД/кг массы в сутки и в дальнейшем контролируется лабораторными показателями гемостаза. Коррекция транскапиллярного обмена включает нормализацию коллоидно-онкотического давления крови путем введения расчетных доз белковых препаратов с учетом их волемических коэффициентов.
К недостаткам данного способа следует отнести то, что последний основан только на послеоперационном мониторинге больных с учетом уже произошедших нарушений в системе гемостаза, транскапиллярного обмена и коллоидно-онкотического давления плазмы крови и при этом не учитывает некоторые причины, приводящие к этим нарушениям, такие как технические особенности выполнения операции, недостаточный объем остающейся после резекции паренхимы.
Предшественником предлагаемого способа по технической сущности является способ расширенной правосторонней гемигепатэктомии.
Пациенты с множественными билобарными метастазами рака толстой кишки в печени часто оказываются неоперабельными ввиду недостаточного предполагаемого объема остающейся паренхимы и, соответственно, высокого риска печеночной недостаточности в послеоперационном периоде, притом что техническое удаление метастазов выполнимо. Поэтому допустима эмболизация ветви воротной вены на стороне большего поражения для гипертрофии менее пораженной доли, как правило, это правая ветвь воротной вены. В последующем у части больных возможно удаление доли на стороне эмболизации и экономные резекции на контралатеральной стороне или выполнение расширенной гемигепатэктомии (Jaeck D, Oussoultzoglou Е, Rosso Е et al. A two-stage hepatectomy procedure combined with portal vein embolization to achieve curative resection for initially unresectable multiple and bilobar colorectal liver metastases. Ann Surg., 2004 Dec; vol. 240(6): 1037-49; discussion 1049-51).
Недостатком данного метода является высокий риск развития печеночной недостаточности при выполнении обширных резекций печени с недостаточным (менее 20%) объемом остающейся после резекции паренхимы, поскольку не всегда удается достичь гипертрофии левой доли печени путем дооперационной эмболизации правой ветви воротной вены. Риск развития печеночной недостаточности сохраняется и увеличивается при наличии цирроза печени, у пациентов старческого возраста, у пациентов с тяжелой сопутствующей патологией.
Задачей, на решение которой направлено изобретение, является разработка способа профилактики острой печеночной недостаточности после обширных резекций печени за счет увеличения функционального объема остающейся после резекции паренхимы.
Данная задача решается за счет того, что заявленный способ профилактики печеночной недостаточности после резекций печени, включающий эмболизацию правой воротной вены для гипертрофии левой доли печени за 2-3 недели до операции, отличается тем, что выполняют центральную бисекционэктомию S4, S5, S8, после которой вскрывают просвет правой ветви воротной вены и удаляют эмболизационный материал. Техническим результатом настоящего предложения является уменьшение количества пациентов с острой печеночной недостаточностью в послеоперационном периоде.
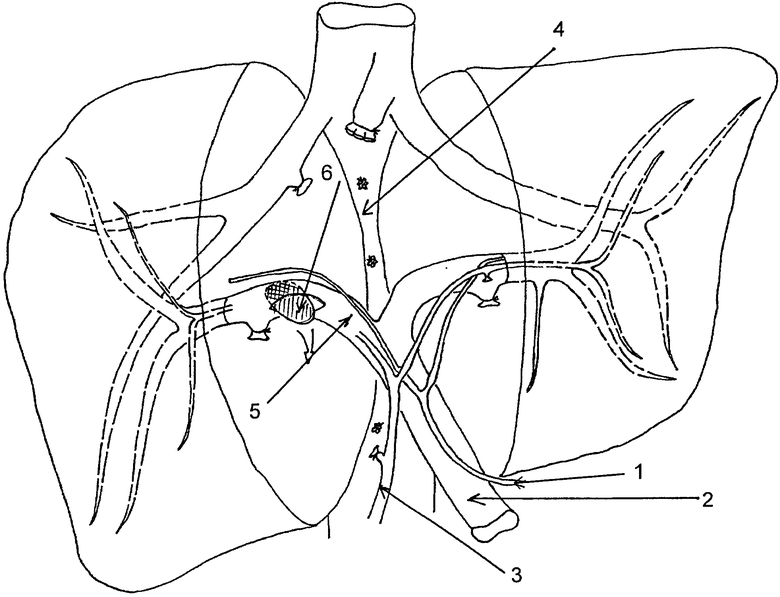
Предлагаемый способ осуществляют следующим образом. Под эндотрахеальным наркозом после обработки операционного поля раствором антисептика выполняется верхнесрединная лапаротомия с углообразным разрезом вправо до 12 ребра. Производят мобилизацию печени по задней поверхности до кавальных ворот с перевязкой и пересечением коммуникантных печеночных вен от правой доли. Выделяют, перевязывают и пересекают пузырный проток и пузырную артерию. Рассекают печеночно-желудочную связку. Выполняют лимфодиссекцию по ходу общей печеночной артерии и гепатодуоденальной связки. Мобилизуют воротные структуры печени. Отдельно выделяют собственную печеночную артерию 1 и ее долевые ветви, воротную вену 2, общий желчный проток 3, его конфлюэнс и долевые притоки. Мобилизуют, лигируют и последовательно пересекают артерии и вены четвертого, пятого и восьмого сегментов.
Отступя от определенных эхографически краев опухоли по 1 см в обе стороны, электроножом рассекают Глиссонову капсулу, при помощи водоструйного диссектора выполняют диссекцию паренхимы до передней поверхности нижней полой вены 4. Трубчатые структуры по линии резекции перевязывают, пересекают и коагулируют. Пересекают и ушивают циркулярным непрерывным сосудистым швом сагиттальную вену. Удаляют препарат. Рассекают в продольном направлении передне-боковую стенку правой ветви воротной вены 5 в проекции эмбола 6, при помощи диссектора из просвета извлекают эмбол, ушивают стенку правой ветви воротной вены обвивным непрерывным сосудистым швом. Перед ушиванием в просвет вены вводят гепарин. Гемостаз раневой поверхности культи печени электрокоагуляцией и прошиванием. Дополнительный гемостаз раневой поверхности культи печени аргоно-плазменной коагуляцией, установкой пластин «тахокомб». Дренируют брюшную полость. Послойно ушивают рану. Асептическая повязка.
Предлагаемый способ поясняется следующим примером.
Пациент И., 61 год. Диагноз: «Рак прямой кишки pT3N0M0G3 (03.12.2010 - передняя резекция прямой кишки. Лучевая терапия 40 Гр). Прогрессия в июле 2012 г. Солитарный метастаз в S4, 5, 6, 8 печени». 13.08.12 Эмболизация правой ветви воротной вены.
Общее состояние больного удовлетворительное. В биохимических анализах крови без видимых отклонений. На КТ: Печень в размерах не увеличена. Контуры ровные, четкие. Эхогенность обычная. Структура неоднородная: в правой доле и в четвертом сегменте определяется гиперэхогенное образование размерами 86×73 мм, с гипоэхогенным ободком. Сосудистый рисунок не изменен. Воротная вена, внутрипеченочные желчные протоки не расширены. Общий желчный проток не расширен.
Запланирована операция - расширенная правосторонняя гемигепатэктомия. Однако при ревизии выявлено плотное образование размерами 7×6 см в диаметре в S4, S5, S8 печени. S1, S2, S3, S6 и S7 визуально и пальпаторно не изменены, цвет и консистенция обычные. Эхографически других очагов в паренхиме не определяется. Принято решение выполнить центральную бисекционэктомию.
Выполнена мобилизация печени по задней поверхности до кавальных ворот с перевязкой и пересечением коммуникантных печеночных вен от правой доли. Выделены, перевязаны и пересечены пузырный проток и пузырная артерия. Рассечена печеночно-желудочная связка. Выполнена лимфодиссекция по ходу общей печеночной артерии и гепатодуоденальной связки. Мобилизованы воротные структуры печени. Отдельно выделена собственная печеночная артерия и ее ветви, воротная вена, общий печеночный проток. Мобилизованы, лигированы и последовательно пересечены артерии и вены четвертого, пятого и восьмого сегментов.
Отступя от определенных эхографически краев опухоли по 1 см в обе стороны, электроножом рассечена Глиссонова капсула, при помощи водоструйного диссектора выполнена диссекция паренхимы. Трубчатые структуры по линии резекции перевязаны и пересечены. Пережата, пересечена и ушита циркулярным непрерывным сосудистым швом сагиттальная вена. Препарат удален. Рассечена в продольном направлении стенка правой ветви воротной вены, при помощи диссектора из просвета извлечен эмбол, представленный организовавшимся инородным телом, произведено ушивание дефекта стенки правой ветви воротной вены обвивным непрерывным сосудистым швом. Гемостаз раневых поверхностей электрокоагуляцией и прошиванием. Дополнительный гемостаз раневых поверхностей печени аргоно-плазменной коагуляцией. Установка пластин «тахокомб».
Через контрапертуры в правой боковой области, брюшная полость дренирована четырьмя силиконовыми дренажами, два подведены в правое поддиафрагмальное пространство, два - к воротам печени. Послойное ушивание раны. Асептическая повязка.
Гистологическое исследование удаленной опухоли: метастаз аденокарциномы, хирургический край резекции 1,0 см. Эмбол - организовавшееся инородное тело, представленное синтетическим губчатым субстратом, волокнистой фиброзной тканью, с наложением нитей фибрина и форменных элементов крови.
Послеоперационный период протекал без осложнений.
Уровень билирубина до операции 11,1 мкмоль/л, АлАТ 22 Е/л, АсАТ 25 Е/л. В первые сутки после операции отмечено увеличение показателей: билирубин 25,6 мкмоль/л, АлАТ 350 Е/л, АсАТ 435 Е/л; на вторые сутки отмечено снижение показателей: билирубин 22,6 мкмоль/л, АлАТ 310 Е/л, АсАТ 380 Е/л; на третьи сутки: билирубин 18,1 мкмоль/л, АлАТ 210 Е/л, АсАТ 230 Е/л; на пятые сутки показатели крови нормализовались (билирубин 13,3 мкмоль/л, АлАТ 35 Е/л, АсАТ 45 Е/л).
Показатели коагулограммы. Первые сутки после операции ПТИ 60%, АЧТВ 65 сек, MHO 2,6; вторые сутки: ПТИ 65%, АЧТВ 49 сек, MHO 3,2; третьи сутки: ПТИ 70%, АЧТВ 49 сек, MHO 2,5; пятые сутки: ПТИ 90%, АЧТВ 35 сек, MHO 1,5.
Данные ЦДК сосудов печени в первые сутки после операции: Диаметр воротной вены 1,3 см. В просвете правой ветви воротной вены включений не выявлено. Кровоток фазный, гепатопетальный, связанный с фазами дыхания. Сегментарные вены SVI, SVII печени диаметр 0,9 см, кровоток фазный, связанный с фазами дыхания, линейная скорость кровотока 18 см/с. В просвете левой ветви воротной вены включений не выявлено. Кровоток фазный, гепатопетальный, связанный с фазами дыхания.
Выписан на 14 сутки после операции в удовлетворительном состоянии.
Данные КТ через 2 месяца после операции: На серии томограмм печень уменьшена в размерах после центральной бисекционэктомии S4, S5, S8. Участков патологической плотности не выявлено. Диаметр воротной вены 14,5 мм. Внутрипеченочные желчные протоки не расширены. Сосудистый рисунок не изменен. Желчный пузырь удален. Общий желчный проток не расширен.
Данные динамической сцинтиграфии через 1 месяц после операции: при гепатобилиосцинтиграфии с бромезидой-Тс99 м накопление РФП в SVI, SVII, SIII, SII хорошее, своевременное, практически равномерное. Очаги гипофиксации и дефекты накопления не определяются. Выведение РФП из печени своевременное, равномерное. Визуализируются долевые протоки и общий желчный проток. Внутрипеченочные и подпеченочные пути свободно проходимы. Заключение: Поглотительно-выделительная функция печени в пределах нормы.
Под наблюдением авторов заявляемого способа находилось 5 больных с объемными образованиями печени, которым была выполнена центральная бисекционэктомия по заявленному способу. Осложнений в виде печеночной недостаточности и летальности у этой группы пациентов не наблюдалось.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПАРЕНХИМОСОХРАНЯЮЩЕЙ ПРАВОСТОРОННЕЙ РАСШИРЕННОЙ ГЕМИГЕПАТЭКТОМИИ | 2017 |
|
RU2653637C1 |
| Способ профилактики пострезекционной печеночной недостаточности | 2022 |
|
RU2798133C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГИЛЮСНОЙ ХОЛАНГИОКАРЦИНОМЫ ПЕЧЕНИ | 2006 |
|
RU2314044C1 |
| Способ лечения метастазов колоректального рака в печени | 2017 |
|
RU2663800C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ И ПРОФИЛАКТИКИ ПОСТРЕЗЕКЦИОННОЙ ОСТРОЙ ПЕЧЕНОЧНОЙ НЕДОСТАТОЧНОСТИ У БОЛЬНЫХ ПЕРВИЧНЫМ И МЕТАСТАТИЧЕСКИМ РАКОМ ПЕЧЕНИ | 2017 |
|
RU2673667C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ОПУХОЛЕЙ ПЕЧЕНИ ЦЕНТРАЛЬНОЙ ЛОКАЛИЗАЦИИ С ИНВАЗИЕЙ В АРТЕРИИ ВОРОТ ПЕЧЕНИ И НЕРАВНОМЕРНОМ ПОРАЖЕНИИ ИХ ОБОЛОЧЕК, ОСЛОЖНЕННЫХ МЕХАНИЧЕСКОЙ ЖЕЛТУХОЙ | 2011 |
|
RU2456933C1 |
| СПОСОБ АНАТОМИЧЕСКОЙ СЕГМЕНТАРНОЙ (ДОЛЕВОЙ) РЕЗЕКЦИИ ПЕЧЕНИ С ИСПОЛЬЗОВАНИЕМ CO-ЛАЗЕРА И СПЕЦИАЛЬНОГО КОМПРЕССИРУЮЩЕГО ХИРУРГИЧЕСКОГО ИНСТРУМЕНТА | 2006 |
|
RU2328243C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ГЕТЕРОТОПИЧЕСКОЙ ТРАНСПЛАНТАЦИИ ПЕЧЕНИ | 2004 |
|
RU2258261C1 |
| Способ воротно-кавального разобщения кровотока правой доли печени с целью формирования условий для её резекции | 2023 |
|
RU2819517C1 |
| Способ радикального лечения больных с метастатическими опухолями печени | 2022 |
|
RU2804994C2 |
Изобретение относится к медицине, к хирургии. Проводят эмболизацию правой воротной вены для гипертрофии левой доли печени за 2-3 недели до операции. Выполняют центральную бисекционэктомию S4, S5, S8. После резекции вскрывают просвет правой ветви воротной вены и удаляют эмболизационный материал. Способ обеспечивает снижение количества пациентов с острой печеночной недостаточностью в послеоперационном периоде за счет профилактики печеночной недостаточности после обширных резекций печени за счет увеличения функционального объема остающейся после резекции паренхимы. 1 ил., 1 пр.
Способ профилактики печеночной недостаточности после резекций печени, включающий эмболизацию правой воротной вены для гипертрофии левой доли печени за 2-3 недели до операции, отличающийся тем, что выполняют центральную бисекционэктомию S4, S5, S8, после которой вскрывают просвет правой ветви воротной вены и удаляют эмболизационный материал.
| JAECK D, ROSSO Е et al | |||
| A two-stage hepatectomy procedure combined with portal vein embolization to achieve curative resection for initially unresectable multiple and bilobar colorectal liver metastases | |||
| Ann Surg., 2004 Dec; vol.240 (6):1037-49 | |||
| БОЧАРОВ С.Н | |||
| Печеночная недостаточность после гемигепатэктомии (патогенез, клиника, диагностика, |
Авторы
Даты
2015-07-10—Публикация
2013-03-12—Подача