Изобретение относится к области биотехнологии, а точнее к способам получения лиофилизированных белковых гидролизатов из морских двустворчатых моллюсков, которые могут быть использованы в качестве биологически активных добавок и продуктов лечебно-профилактического назначения или для изготовления функциональных продуктов в пищевой промышленности.
Большинство продуктов в их естественном состоянии плохо поддаются длительному хранению. Посредством лиофилизации биологические субстанции, лекарственные средства и пищевые продукты можно сохранять на длительный срок. Особенно это относится к таким термически нестабильным органическим веществам, как белки и пептиды. [1].
Оптимизация процесса лиофилизации требует решения наиболее частых технологических проблем, таких как разрушение первичной структуры лиофилизата (коллапс) и возникновение обратного плавления, и рационализации подходов к совершенствованию каждого этапа цикла лиофилизации (замораживанию, первичной и вторичной сушки, иногда перед первичной сушкой проводится дополнительный этап - отжиг, или термоциклирование) [2].
Известен способ получения лиофилизированного препарата кровь гемолизированная [Пат. 2455014, РФ, МПК A61K 35/14, G01N 33/48, 2012], где в дефибринированную кровь добавляют дистиллированную воду в соотношении 1:9 (одна часть крови + восемь частей дистиллированной воды) с последующим введением в качестве вещества-наполнителя раствора натрия хлорида в объеме, равном объему дефибринированной крови, до конечной концентрации 0,15 моль/л. Полученный полуфабрикат крови гемолизированной центрифугируют при 4000 g в центрифуге с бакет-ротором с охлаждением до 4-8°С в течение 30 мин и стерилизуют фильтрацией через мембранные или керамические фильтры с размером пор 0,2 мкм. Полученный фильтрат крови гемолизированной разливают по 2 мл в стерильные ампулы, охлаждают до температуры -(45±5)°С и промораживают. Затем препарат подвергают лиофилизации в течение 24 часов до конечной температуры материала 25°С, при этом стадия сублимации в среднем составляет - 14 часов, десорбции - 10 часов. Охлаждение возможно осуществлять в быстром или медленном режиме. При быстром режиме препарат охлаждают до -(45±5)°С в течение 3-4 часов, при медленном режиме - в течение 12 часов. Общее время криостабилизации крови гемолизированной, включающее охлаждение и промораживание, для обоих режимов составляет 18-20 часов. Недостатком способа является то, что он разработан для белков крови и содержания низкой концентрации натрия хлорида, которая не препятствуют стеклованию биопрепарата на этапе охлаждения и криостабилизации, а также не сталкивается с проблемой фазового расслоения препарата.
Известен способ лиофильной сушки биопрепаратов [Пат. 2111426 С1, РФ, МПК F26B 5/06, 1998]. Способ позволяет проводить лиофилизацию материалов с низкой температурой коллапса (-30°С и ниже) при более высоких температурах лиофильной сушки. Способ включает введение в раствор биопрепарата перед сушкой защитной среды с последующим замораживанием полученной смеси и вакуумной сушкой. В состав защитной среды дополнительно вводят вещество-наполнитель, кристаллизующееся при замораживании его разбавленного водного раствора, в концентрации, достаточной для формирования аморфно- кристаллической структуры в объеме жидкой фазы биопрепарата, остающейся после кристаллизации воды. Предварительно перед сушкой приготавливают пробные образцы биопрепарата с защитной средой или одну защитную среду с разной концентрацией вещества-наполнителя, с последующим проведением термического или рентгенофазового анализа, или пробной лиофилизации при температуре сушки, равной или выше температуры коллапса исходного биопрепарата, а концентрацию вещества-наполнителя выбирают равной или более концентрации вещества-наполнителя в пробном образце биопрепарата, кривая термического или рентгенофазового анализа которого содержит дополнительный пик по сравнению с аналогичной кривой термического или рентгенофазового анализа образца исходного биопрепарата, или равной или более концентрации вещества-наполнителя в пробном образце биопрепарата, показывающем наличие таблетки после лиофилизации. В качестве вещества-наполнителя используют хлорид натрия или хлорид калия, или глицин. Недостатком данного способа является необходимость введения дополнительных количеств солей или других стабилизирующих веществ в конечный продукт, а также использование сложных методов контроля структуры лиофилизата и процесса сушки.
Известен способ лиофильной сушки биопрепарата (см. пат. 2261623, Российская Федерация, МПК A23L 1/03, 2004 г.), предусматривающий введение в раствор гидролизата наполнителя для эффективного промерзания всего продукта в процессе замораживания. В качестве растворов биопрепаратов используют гидролизат из мидий «МИГИ-К ЛП», гидролизат из мяса рапаны «Рапанин», гидролизат из морского гребешка и другие. В качестве наполнителя используют нейтральные полисахариды - крахмал, метилцеллюлозу или пектины в количестве от 5-40% к массе гидролизатов из морских гидробионтов. Смесь перемешивают и разливают в емкости высотой слоя 8-10 мм, замораживание проводят при температуре -40-45°С и выдерживают при этих температурах в течение 4-10 ч. Сушку ведут до содержания сухих веществ 90-94%, а после сушки препарат измельчают.
Гидролизаты из морских гидробионтов содержат от 10-15% соли, это обстоятельство сдерживает процесс замораживания. При минус 40°С происходит фазовое расслоение, что затрудняет лиофильную сушку. Ведение в гидролизат нейтрального полисахарида повышает температуру замерзания раствора, продукт промерзает по всему объему. Нейтральные полисахариды являются сорбентом для солей хлористого натрия и хлористого калия. Недостатком способа является то, что в процессе получения требуется введение полисахаридов для криостабилизации гидролизатов гидробионтов, а также использованием кислотного и кислотно-ферментативного гидролиза, что приводит к высокому содержанию поваренной соли в конечном продукте.
Наиболее близким по технической сущности является способ получения биопрепаратов в сухой форме из гидролизатов гидробионтов [Пат. 2704829 С1, РФ, МПК A61K 35/618, 2019], включающей подготовку препарата, замораживание смеси при температуре минус 40°С и выдерживание полученной смеси, а также сушку и последующие таблетирование и капсулирование сухого препарата, предусматривающий получение композиций различных гидролизатов. Так, например, используют композицию гидролизатов, состоящую из мидийного щелочного гидролизата и кислотного гидролизата из рапаны. Указанную композицию разбавляют дистиллированной водой до содержания сухих веществ 5-10% и автоклавируют при температуре +114°С в течение 30 минут. Затем в камере сублимационной сушилки замораживают смесь в течение 2-3 часов и выдерживают, повышая температуру до минус 30°С в течение 16-20 часов. Для сушки продукта повышают температуру до +40°С при вакууме 9-11 мм рт.ст. в течение 20-24 часов, после чего досушивают продукт при указанной температуре в течение 8-12 ч. до содержания сухих веществ 92-94%. Недостатком способа является длительность процесса, как замораживания, так и отжига при достаточно низкой температуре - минус 30°С, а для преодоления фазового расслоения препарата используется дополнительно стадия разведения целевого продукта и его дополнительная термическая обработка для предотвращения бактериальной контаминации.
Задачей изобретения является разработка технологии получения лиофилизатов из белковых гидролизатов двустворчатых моллюсков, получаемых щелочным/кислотным гидролизом, без введения дополнительных веществ, с заменой на стадии гидролиза/нейтрализации реагента соляной кислоты на лимонную кислоту, и общим снижением концентрации солей в препарате до 4-12%.
Техническим результатом от решения поставленной задачи является то, что разработанная технология позволяет получить лиофилизат белковых гидролизатов из двустворчатых моллюсков без использования дополнительных компонентов, с содержанием соли в виде цитрата натрия не более 4-12%. Техническим результатом также является ускорение процесса сушки и увеличение срока хранения белковых гидролизатов из двустворчатых моллюсков с низким содержанием поваренной соли.
Для решения поставленной технической задачи изобретения предложен Способ получения лиофилизированного продукта из гидролизатов двустворчатых моллюсков, включающий подготовку сырья, измельчение моллюсков, фильтрование, упаривание, лиофильную сушку. В способе проводят гидролиз сырья из двустворчатых моллюсков, используя в качестве сырья анадар, гребешков или мидий, с дальнейшим упариванием полученного гидролизата под вакуумом при от минус 800 мбар до минус 900 мбар при температуре 80°С до содержания в гидролизате сухих растворенных веществ не более 15%. После этого полученные образцы гидролизатов замораживают в камере ледогенератора лиофильной сушилки при минус 60°С в течение 3-4 часов в поддонах для лиофилизации слоем 4-8 мм, выдерживают при температуре не выше минус 45°С в течение 12 часов. Отжиг проводят при температуре минус 20°С течение 3 часов, после чего снова охлаждают до минус 45°С в течение 2 часов и проводят сублимацию льда с подогревом полки от минус 35°С до 20°С в течение 14-16 часов при вакууме 1-5 Па. Затем проводят стадию десорбции при температуре полок от 30-40°С и вакууме 10-15 Па в течение 6-10 часов до получения препарата с остаточной влажностью не более 10%. Кроме того, в способе для получения гидролизата из мидий и анадар, взятых вместе с раковинами и интерстициальной жидкостью, применяют щелочной гидролиз путем добавления 40%-ного раствора NaOH при постоянном перемешивании в течение 180 мин с постепенным повышением температуры от 80°С до 95°С, после чего в отфильтрованный гидролизат добавляют 25%-ный раствор лимонной кислоты до рН 5,69 и содержания сухих растворенных веществ 5,2-5,9%. И наконец, что для получения гидролизата мягких тканей гребешка, отделенных от створки, применяют кислотный гидролиз путем добавления к массе мягких тканей в соотношении 1:1, нагретого до 60°С, 24%-ного раствора лимонной кислоты, который ведут в течение 16 часов при постепенном повышении температуры от 60°С до 95°С, затем полученный гидролизат отфильтровывают и охлаждают до комнатной температуры с последующей нейтрализацией 40%-ным раствором NaOH до рН 5,89 и содержания сухих веществ 4,8%.
Общим с прототипом является использование гидролизатов гидробионтов, упаривание, замораживание и сушка под вакуумом.
Новым является то, что лиофилизации подвергают гидролизаты из мидий и анадар, взятых вместе с раковинами и интерстициальной жидкостью, а также гидролизат из мягких тканей гребешка. Новым является то, что гидролизаты из мидий, анадар выполняют, применяя щелочной гидролиз, а для получения гидролизата из мягких тканей гребешка применяют кислотный гидролиз. Новым в заявляемом способе является упаривание гидролизатов до содержания сухих веществ 13-15% и содержания соли в пересчете на цитрат натрия не более 4-12%, замораживание проводят при температуре камеры минус 60°С до достижения образцом температуры не менее минус 45°С течение 3-4 часов выдерживании при этой температуре в течение 10-12 часов, проведении отжига в течение 3 часов при температуре минус 20°С и последующем охлаждении до минус 45°С в течение 2 часов, проведении сублимационной стадии сушки в течение 12-14 часов при вакууме 1-5 Па и температуре полки от минус 35°С до 20°С и стадии десорбции в течение 6-12 часов при повышении температуры полки от 30 до 40°С, что позволяет достичь остаточной влажности не более 10%.
В заявляемом способе авторами экспериментальным путем установлены последовательность операций, конкретные условия проведения каждой операции и средства, с помощью которых технология реализуется. Количественные значения являются оптимальными, позволяющими достигнуть заявленный технический результат.
Существенные признаки, характеризующие изобретение, включая отличительные от прототипа и совокупность признаков, обеспечивающих получение заявляемого технического результата, следующие:
- использование сырья из анадар, гребешков или мидий, добытых промысловым способом и/или при переборке мидийных или устричных коллекторов морских ферм из Черного и/или Азовского морей. Выбранное сырье широко распространено в указанных районах и не имеет количественных ограничений, препятствующих промышленному применению;
- проведение щелочного гидролиза моллюсков вместе со створкой способствует более полному использованию исходного сырья и упрощению отделения мягких тканей, а также снижению энерго-/трудо-/затрат на получение конечного продукта;
- применение лимонной кислоты для нейтрализации или гидролиза с целью замены минеральной кислоты, например, соляной кислоты, и снижения содержания в целевом продукте поваренной соли и образования в процессе нейтрализации цитрата натрия позволяет применить в технологии более экономичные режимы. Так как цитрат натрия имеет температуру стеклования минус 41°С, а криогидратная точка полученных гидролизатов лежит в пределах минус 35°С-минус 40°С, что позволяет проводить отжиг при температурах от минус 20 до минус 30°С, а сушку препарата при температуре сушки, равной или выше температуры коллапса исходного биопрепарата.
- проведение замораживания гидролизатов при температуре минус 60°С в течение 3-4 часов;
- снижение температуры отжига до минус 20°С, что выше температуры коллапса исходного препарата, с последующим охлаждением до минус 45°С, для увеличения размера кристаллов льда;
- проведение сублимационной стадии сушки при температурах равных или выше температуры коллапса исходного препарата при вакууме 1-5 Па;
- проведение стадии десорбции при температуре 30÷40°С.
Проведенный анализ уровня техники позволил установить, что по совокупности отличительных признаков описываемого способа не обнаружен источник, характеризующийся признаками, тождественными всем существенным признакам заявленного изобретения, что позволяет сделать вывод о соответствии изобретения критерию «новизна».
Патентные исследования и изучение научных публикаций по теме изобретения не обнаружили решений, имеющих сходства с заявляемым способом, что позволило сделать вывод о соответствии критерию «изобретательский уровень». Критерий патентоспособности «промышленная применимость» подтверждается тем, что изобретение может быть осуществлено с помощью средств и методов, приведенных в примерах реализации способа.
Сущность изобретения поясняется описанием.
Особенности химического состава двустворчатых моллюсков позволяют использовать их в качестве сырья для получения биологически активных добавок к пище на основе лиофилизатов из гидролизатов и/или их композиций и добавок лечебно-профилактического действия в пищевой промышленности. Переработка со створкой значительно сокращает время переработки исходного сырья, без потери таких компонентов, как гемолимфа и свободные аминокислоты в ней, особенно, у анадары с прочной створкой. В дополнение, в качестве сырья могут быть использованы мягкие ткани после отделения товарной части - ноги, т.е. будут утилизироваться отходы товарного производства. Аналогично и для гребешка, только у него более тонкая и легко отделяемая раковина, а поскольку мягкие ткани будут отделены от створки, то кислотный гидролиз даст более приятный по органолептическим показателям продукт. Содержание свободных аминокислот в двустворчатых моллюсках колеблется от наименьших значений у анадары - 818 до максимальных у гребешка - 1810,58 мг/100 г сырой ткани (Табл. 1.) [3, 4]. Содержание таурина колеблется от минимальных значений у мидии - 135 мг до максимальных у анадары - 405 мг/100 г сырой ткани. В состав свободных аминокислот двустворчатых моллюсков входят все заменимые и незаменимые аминокислоты.
Из свободных аминокислот особый интерес представляет производное аминокислоты метионина - таурин, которые не входит в состав белков. Он участвует в обмене холестерина, способствует детоксикационной функции печени, регуляции кровяного давления и улучшению светочувствительности сетчатки глаза [5]. Таурин обладает нейротропной активностью, кардиопротекторным действием, оказывает тонизирующее действие на сердечную мышцу [6]. Также установлено, что таурин способствует улучшению памяти и умственной работоспособности, повышению концентрации внимания, положительно влияет на высшие корковые функции головного мозга [7].
Гидролизаты, полученные из моллюсков, также способны корректировать различные патологические состояния у людей, вырабатывать адаптивный иммунитет у пожилых людей, обладают антиоксидантными и регенеративными свойствами [8]. Гидролизаты из мяса моллюсков благотворно влияют на функционально-биохимические и иммунологические показатели у пациентов с атеросклеротической дисциркуляторной энцефалопатией I ст.[9]
Примеры реализации способа.
Пример 1. 1,0 кг мидий вместе с раковинами и интерстициальной жидкостью, свежевыловленных промысловым способом в Черном или Азовском морях, или добытых при переборке мидийно-устричных коллекторов морских ферм, промытых водопроводной водой, измельчали на молотковой мельнице и помещали в химический реактор с мешалкой и 1 л предварительно нагретой до 60°С воды. Затем добавляли 26 мл 40%-го раствора NaOH. Нагретую массу гидролизовали при постоянном перемешивании в течение 180 мин при повышении температуры от 80°С до 95°С для отделения мяса от створок и растворения мягких тканей. К 0,95 л отфильтрованного через нутч-фильтр гидролизата добавляли 36,5 мл 25%-ного раствора лимонной кислоты до рН 5,65 и содержания сухих веществ 5,9%. Полученный гидролизат упаривали на роторном испарителе под вакуумом при от минус 800 мбар до минус 900 мбар при температуре 80°С до содержания сухих растворенных веществ 14,8% в объеме 384 мл.
Упаренный гидролизат разливали в металлические поддоны слоем до 8 мм (объем 120-130 мл) и замораживали при минус 60°С в камере ледогенератора лиофильной сушилки SCIENZ 12-ND/D (ЦКП «Спектрометрия и хроматография», ФИЦ ИнБЮМ), до температуры образца минус 45°С в течение 4 часов и выдерживали при этой температуре 12 часов. Затем поддоны с замороженными образцами помещали в морозильную камеру при минус 20°С на 3 часа. Потом поддоны вновь помещали в камеру ледогенератора лиофильной сушилки и в течение 2 часов охлаждали до минус 45°С. Затем поддоны размещали на полках лиофильной сушилки SCIENZ 12-ND/D и фаза сублимации протекала при температуре полки от минус 35°С до заданного значения 20°С при вакууме 1-5 Па в течение 14 часов. Затем температура полки повышалась до 30°С и десорбционная стадия протекала при вакууме 10-15 Па в течение 6 часов. По окончании сушки проводили определение остаточной влажности препарата, которое составляло - 6,60%.
Лиофилизат обладал приятным запахом морепродуктов и слабосоленым вкусом. Содержание соли составило 4% в пересчете на цитрат натрия. Полученный препарат весом 32 г в виде таблетки лиофилизации (далее ТЛ), показывающей что лиофилизат при высыхании, сохраняет первоначальную структуру, то есть не подвергся коллапсу, измельчали на шаровой мельнице и фасовали в твердые желатиновые капсулы размера 00.
Общее время собственно лиофилизации - составило 20 часов (сублимация - 14 ч; десорбция 6 ч). Стадия замораживания и криостабилизации с отжигом и приведением к исходной температуре для лиофилизации составило 21 ч. Срок хранения для лиофилизированных капсулированных препаратов устанавливают не менее трех лет.
Лиофилизированный продукт, полученный в соответствии с примером 1, может использоваться при изготовлении БАД, или получении смесей лиофилизатов из различных гидролизатов гидробионтов для получения БАД, сбалансированных по аминокислотному скору.
Пример 2. 0,6 кг анадар вместе с раковинами и интерстициальной жидкостью, свежевыловленных промысловым способом в Черном или Азовском морях, или добытых при переборке мидийно-устричных коллекторов морских ферм, промывали водопроводной водой, измельчали на молотковой мельнице и помещали в химический реактор с мешалкой и 0,6 л предварительно нагретой до 60°С воды. Затем добавляли 16 мл 40%-го раствора NaOH. Нагретую массу при постоянном перемешивании гидролизовали 180 минут при постепенном повышении температуры от 80°С до 95°С. Полученные 0,76 л гидролизата отфильтровывали через полипропиленовый фильтр с диаметром пор 100 мкм и охлаждали до комнатной температуры до 25°С. Затем добавляли 26 мл 25%-ного раствора лимонной кислоты до рН 5,69 и содержания сухих веществ 5,2%. Упаривали на роторном испарителе под вакуумом при от минус 800 мбар до минус 860 мбар при температуре 80°С до содержания сухих растворенных веществ 14,6% в объеме 370 мл.
Упаренный гидролизат разливали в металлические поддоны слоем до 8 мм (объем 120-130 мл) и замораживали при минус 60°С в камере ледогенератора лиофильной сушилки SCIENZ 12-ND/D (ЦКП «Спектрометрия и хроматография», ФИЦ ИнБЮМ), до температуры образца минус 45°С в течение 4 часов и выдерживали при этой температуре 12 часов. Затем поддоны с замороженными образцами помещали в морозильную камеру при минус 20°С на 3 часа. Потом поддоны вновь помещали в камеру ледогенератора лиофильной сушилки и в течение 2 часов охлаждали до минус 45°С. Затем поддоны размещали на полках лиофильной сушилки SCIENZ 12-ND/D и фаза сублимации протекала при температуре полки от минус 35°С до заданного значения 20°С при вакууме 1-5 Па в течение 14 часов. Затем температура полки повышалась до 30°С и десорбционная стадия протекала при вакууме 10-15 Па в течение 8 часов. По окончании сушки проводили определение остаточной влажности препарата, которое составляло - 6,82%.
Лиофилизат обладал приятным запахом морепродуктов и слабосоленым вкусом. Содержание соли составило 4% в пересчете на цитрат натрия. Полученный препарат весом 20,0 г в виде ТЛ измельчали на шаровой мельнице и фасовали в твердые желатиновые капсулы размера 00.
Общее время собственно лиофилизации - составило 22 часа (сублимация - 14 ч; десорбция 8 ч). Стадия замораживания и криостабилизации с отжигом и приведением к исходной температуре для лиофилизации составили 21 ч. Срок хранения для лиофилизированных капсулированных препаратов устанавливают не менее трех лет.
Лиофилизированный продукт, полученный в соответствии с примером 2, может использоваться при изготовлении БАД, или получении смесей лиофилизатов из различных гидролизатов гидробионтов для получения БАД, сбалансированных по аминокислотному скору.
Пример 3. 83 г отделенных от створки мягких тканей гребешка, свежевыловленного промысловым способом в Черном море, помещали в химический реактор с мешалкой и добавляли (в соотношении 1:1) 85 мл, предварительно нагретого до 60°С, 24%-ного раствора лимонной кислоты. Нагретую массу при постоянном перемешивании гидролизовали 16 часов при постепенном повышении температуры от 60°С до 95°С. Полученные 146 мл гидролизата отфильтровывали через полипропиленовый фильтр с диаметром пор 100 мкм и охлаждали до комнатной температуры. Затем нейтрализовали добавлением 21 мл 40%-ного раствора NaOH до рН 5,89 и содержания сухих веществ 4,8%. Упаривали на роторном испарителе под вакуумом при от минус 800 мбар до минус 840 мбар при температуре 80°С до содержания сухих растворенных веществ 13,7% в объеме 70 мл.
Упаренный гидролизат разливали в металлический поддон слоем до 4 мм и замораживали при минус 60°С в камере ледогенератора лиофильной сушилки SCIENZ 12-ND/D (ЦКП «Спектрометрия и хроматография», ФИЦ ИнБЮМ), до температуры образца минус 45°С в течение 3 часов и выдерживали при этой температуре 12 часов. Затем поддон с замороженным образцом помещали в морозилку при минус 20°С на 3 часа. Потом вновь помещались в камеру ледогенератора лиофильной сушилки и в течение 2 часов охлаждали до минус 45°С. Затем поддон размещали на полке лиофильной сушилки SCIENZ 12-ND/D и фаза сублимации протекала при температуре полки от минус 35°С до заданного значения 30°С при вакууме 1-5 Па в течение 16 часов. Затем температура полки повышалась до 40°С и десорбционная стадия протекала при вакууме 10-15 Па в течение 10 часов. По окончании сушки проводили определение остаточной влажности препарата, которое составляло - 9,71%.
Лиофилизат обладал приятным запахом морепродуктов и слабосоленым вкусом. Содержание соли составило 12% в пересчете на цитрат натрия. Полученный препарат весом 16,8 г в виде ТЛ измельчали на шаровой мельнице и фасовали в твердые желатиновые капсулы размера 00.
Общее время собственно лиофилизации - составило 26 часов (сублимация - 16 ч; десорбция - 10 ч). Стадия замораживания и криостабилизации с отжигом и приведением к исходной температуре для лиофилизации составила 20 ч. Срок хранения для лиофилизированных капсулированных препаратов устанавливают не менее трех лет.
Лиофилизированный продукт, полученный в соответствии с примером 3, может использоваться при изготовлении БАД, или получении смесей лиофилизатов из различных гидролизатов гидробионтов для получения БАД, сбалансированных по аминокислотному скору.

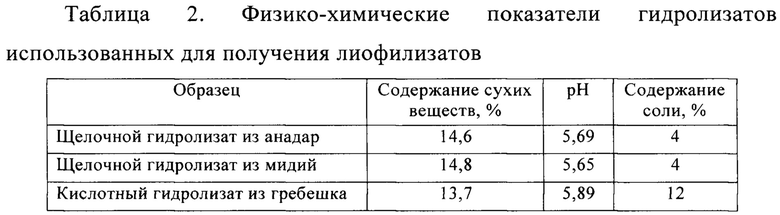
Примечание: содержание растворенных сухих веществ определяли по адаптированной методике, приведенной в ГОСТ ISO 2173-2013 Продукты переработки фруктов и овощей. Рефрактометрический метод определения растворимых сухих веществ.
Таблица 3. Параметры процесса лиофилизации и их влияние на характеристики ТЛ
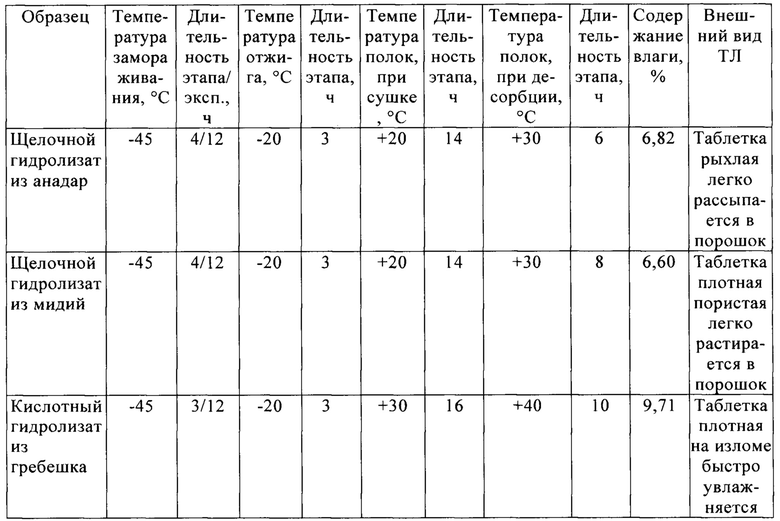
Примечание: Содержание влаги в образцах определяли по адаптированной методике, приведенной в ГОСТ 7636-85 Рыба, морские млекопитающие, морские беспозвоночные и продукты их переработки. Методы анализа.
Таким образом, изобретение позволяет получить лиофилизаты из гидролизатов двустворчатых моллюсков с увеличенным сроком хранения, и низким содержанием поваренной соли, которые можно использовать в пищевой промышленности, а также производстве БАД и/или композиций лиофилизатов, сбалансированных по аминокислотному скору.
Список источников информации, принятых во внимание:
1. Блынская Е.В. Тишков СВ., Алексеев К.В. Технологические подходы к совершенствованию процесса лиофилизации белковых и пептидных лекарственных препаратов // Российский биотерапевтический журнал. 2017. 16(1). С. 6-11. https://DOI:10.17650/1726-9784-2017-16-1-6-11
2. Блынская Е.В. Тишков С.В., Алексеев К.В., Минаев С.В. Стадия термоциклирования в оптимизации процессов замораживания в технологии получения лиофилизированного препарата // Российский биотерапевтический журнал. 2019. 18(1). С. 87-94. https://DOI:10.17650/1726-9784-2019-18-1-87-94
3. Табакаева О.В. Кислотные гидролизаты из отходов переработки двухстворчатых моллюсков дальневосточного региона. Техника и технология пищевых производств. 2009. 13(2). С. 1-4.
4. Масленникова Е.В., Черевач Е.И., Юдина Т.П., Бабин Ю.В., Цыбулько Е.И. (2009). Технология белкового гидролизата из мантии гребешка. Пищевая промышленность, (5), 18-19.
5. Машковский М.Д. Лекарственные средства. 16-е изд. М.: Новая волна. 2012. 1216 с.
6. Торкунов П.А. Кардиопротекторное действие таурина / А.П. Торкунов, Н.С Сапронов // Экспериментальная и клиническая фармакология. 1997. 60(5). С. 72-77.
7. Оруджев Я.С Применение медиаторных аминокислот (таурин) во внебольничной геронтологической практике / Я.С.Оруджев, В.В. Ростовщиков // Социальная и клиническая психиатрия. 1998. 3. С. 78-81.
8. Пивненко Т.Н. Ферментативные гидролизаты из гидробионтов Тихого океана как основа для создания биологически активных добавок к пище и продуктов функционального питания: монография / Т.Н. Пивненко, Н.Н. Ковалев, Т.С.Запорожец, Н.Н. Беседнова, Т.А. Кузнецова. Владивосток: Дальнаука, 2015. 160 с.
9. Кузнецов В.В., Лисяный Н.И., Рябушко В.И., Ерохин В.Е., Скрипченко А.Г. Влияние гидролизата из морских моллюсков Рапамид® на функциональное состояние мозга и иммунную систему у пациентов с начальными проявлениями атеросклеротической дисциркуляторной энцефалопатии. Журнал неврологии им. Б.М. Маньковського. 2014. 2(1). С. 76-85.
10. ГОСТ ISO 2173-2013 Продукты переработки фруктов и овощей. Рефрактометрический метод определения растворимых сухих веществ. Введ. 2015.07.01. М.: Стандартинформ, 2019. 8 с.
11. ГОСТ 7636-85 Рыба, морские млекопитающие, морские беспозвоночные и продукты их переработки. Методы анализа (см. Переиздание (ноябрь 1990 г.) и сборник «Рыба и рыбные продукты. Методы анализа. Маркировка. Упаковка». Издание 1998 г., 2004 г.). М.: ИПК Издательство стандартов, 2004. 31 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФУНКЦИОНАЛЬНОГО ПРОДУКТА НА ОСНОВЕ ГИДРОЛИЗАТОВ ИЗ МОЛЛЮСКОВ | 2024 |
|
RU2841252C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОЛИЗАТА ИЗ ДВУСТВОРЧАТОГО МОЛЛЮСКА ANADARA KAGOSHIMENSIS (ВАРИАНТЫ) | 2023 |
|
RU2819742C1 |
| СПОСОБ ЛИОФИЛЬНОЙ СУШКИ БИОПРЕПАРАТА | 2004 |
|
RU2261623C1 |
| СПОСОБ ПРОИЗВОДСТВА БИОПРЕПАРАТОВ В СУХОЙ ФОРМЕ ИЗ ГИДРОЛИЗАТОВ ГИДРОБИОНТОВ | 2018 |
|
RU2704829C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИЩЕВЫХ БЕЛКОВЫХ ПРОДУКТОВ | 2007 |
|
RU2331202C1 |
| ПРОДУКТ, ОБОГАЩЕННЫЙ СВОБОДНЫМИ АМИНОКИСЛОТАМИ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2000 |
|
RU2171066C1 |
| СПОСОБ ПРОИЗВОДСТВА ХЛЕБОБУЛОЧНЫХ ИЗДЕЛИЙ | 2015 |
|
RU2581880C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИЩЕВОГО ПРОДУКТА, ОБЛАДАЮЩЕГО БИОЛОГИЧЕСКИ АКТИВНЫМИ СВОЙСТВАМИ ИЗ ГИДРОБИОНТОВ | 2014 |
|
RU2580157C1 |
| Способ получения белково-витаминной добавки из икорного джуса | 2017 |
|
RU2676312C1 |
| СПОСОБ ЛИОФИЛИЗАЦИИ ЭРИТРОЦИТАРНЫХ ДИАГНОСТИКУМОВ ТУЛЯРЕМИЙНЫХ | 2020 |
|
RU2749355C1 |
Изобретение относится к области биотехнологии и может быть использовано для получения биологически активных добавок и продуктов лечебно-профилактического назначения. Способ включает подготовку сырья, измельчение моллюсков, фильтрование, упаривание, лиофильную сушку. Проводят гидролиз сырья из двустворчатых моллюсков, используя в качестве сырья анадар, гребешков или мидий, с дальнейшим упариванием полученного гидролизата под вакуумом при от минус 800 до минус 900 мбар при температуре 80°С до содержания в гидролизате сухих растворенных веществ не более 15%. После этого полученные образцы гидролизатов замораживают в камере ледогенератора лиофильной сушилки при минус 60°С в течение 3-4 ч в поддонах для лиофилизации слоем 4-8 мм, выдерживают при температуре не выше минус 45°С в течение 12 ч. Отжиг проводят при температуре минус 20°С течение 3 ч, после чего снова охлаждают до минус 45°С в течение 2 ч и проводят сублимацию льда с подогревом полки от минус 35 до 20°С в течение 14-16 ч при вакууме 1-5 Па. Затем проводят стадию десорбции при температуре полок от 30-40°С и вакууме 10-15 Па в течение 6-10 ч до получения препарата с остаточной влажностью не более 10%. Изобретение обеспечивает получение лиофилизата белковых гидролизатов из двустворчатых моллюсков и увеличение срока его хранения. 2 з.п. ф-лы, 3 табл., 3 пр.
1. Способ получения лиофилизированного продукта из гидролизатов двустворчатых моллюсков, включающий подготовку сырья, измельчение моллюсков, фильтрование, упаривание, лиофильную сушку, отличающийся тем, что проводят гидролиз сырья из двустворчатых моллюсков, используя в качестве сырья мидий, анадар или гребешков, с дальнейшим упариванием полученного гидролизата под вакуумом при от минус 800 до минус 900 мбар при температуре 80°С до содержания в гидролизате сухих растворенных веществ не более 15%, после чего полученные образцы гидролизатов замораживают при минус 60°С в течение 3-4 ч в поддонах для лиофилизации слоем 4-8 мм, выдерживают при температуре не выше минус 45°С в течение 12 ч, а отжиг проводят при температуре минус 20°С в течение 3 ч, после чего снова охлаждают до минус 45°С в течение 2 ч и проводят сублимацию льда с подогревом полки от минус 35 до плюс 20°С в течение 14-16 ч при вакууме 1-5 Па, затем стадию десорбции при температуре полок плюс 30-плюс 40°С и вакууме 10-15 Па в течение 6-10 ч до получения препарата с остаточной влажностью не более 10%.
2. Способ по п. 1, отличающийся тем, что для получения гидролизата из мидий и анадар, взятых вместе с раковинами и интерстициальной жидкостью, применяют щелочной гидролиз путем добавления 40%-ного раствора NaOH при постоянном перемешивании в течение 180 мин с постепенным повышением температуры от 80 до 95°С, после чего в отфильтрованный гидролизат добавляют 25%-ный раствор лимонной кислоты до рН 5,69 и содержания сухих растворенных веществ 5,2-5,9%.
3. Способ по п. 1, отличающийся тем, что для получения гидролизата мягких тканей гребешка применяют кислотный гидролиз, путем добавления к мягким тканям в соотношении 1:1 нагретого до 60°С 24%-ного раствора лимонной кислоты, который ведут в течение 16 ч при постепенном повышении температуры от 60 до 95°С, затем полученный гидролизат отфильтровывают и охлаждают до комнатной температуры с последующей нейтрализацией 40%-ным раствором NaOH до рН 5,89 и содержания сухих веществ 4,8%.
| СПОСОБ ПРОИЗВОДСТВА БИОПРЕПАРАТОВ В СУХОЙ ФОРМЕ ИЗ ГИДРОЛИЗАТОВ ГИДРОБИОНТОВ | 2018 |
|
RU2704829C1 |
| СПОСОБ ЛИОФИЛЬНОЙ СУШКИ БИОПРЕПАРАТА | 2004 |
|
RU2261623C1 |
| СПОСОБ ЛИОФИЛЬНОЙ СУШКИ БИОПРЕПАРАТА | 1995 |
|
RU2111426C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННОГО ПРЕПАРАТА КРОВЬ ГЕМОЛИЗИРОВАННАЯ | 2011 |
|
RU2455014C1 |
| US 6660280 B1, 09.12.2003. | |||
Авторы
Даты
2024-05-22—Публикация
2024-01-17—Подача