Изобретение относится к биотехнологии, микробиологии и, в частности, к способам стабилизации эритроцитарных диагностикумов путем лиофильного высушивания. Изобретение может быть использовано в биотехнологической схеме производства эритроцитарных диагностикумов лиофилизированных.
Разработка способов стабилизации эритроцитарных диагностикумов продолжает оставаться актуальной, так как их применение в лабораторной практике не предусматривает использование дорогостоящих импортных реактивов и оборудования. Жидкие формы выпуска препаратов дешевы и удобны в применении, так как не требуют лишних манипуляций при постановке реакции. Однако недостатком эритроцитарных диагностикумов в жидком виде является короткий срок годности (1 год) и отсутствие возможности осуществлять их транспортировку при критических температурных режимах (не соответствующих требованиям эксплуатационной документации). Нарушение температурного режима при хранении и транспортировке, как в сторону повышения, так и в сторону понижения температуры, могут приводить к полной потере активности. Кроме того, буферные растворы, содержащие клетки крови, чувствительны к присутствию микроорганизмов, поскольку являются хорошими субстратами для роста микробов.
Решить проблему стабилизации биологических препаратов для сохранения исходных свойств возможно применением метода лиофилизации. Сухие препараты - лиофилизаты не претерпевают химических изменений и сохраняют присущие им свойства при длительном хранении и в условиях критических значений температуры, вследствие чего отсутствует необходимость строгого соблюдения требований по транспортировке и хранению, увеличивается срок годности.
Сублимационное высушивание широко применяется для изготовления лиофилизатов микробных взвесей, антигенных фракций различной природы, иммунных сывороток, иммуноглобулинов, вакцин, антибиотиков, гормонов и т.д. Для каждого конкретного препарата подбираются среды высушивания, отрабатываются индивидуальные режимы замораживания и сушки.
Накоплено достаточно данных о стабилизации высушиванием компонентов крови и препаратов, полученных из крови животных. Известен способ получения лиофилизированного препарата - кровь гемолизированная [1]. Препарат охлаждают в ампулах до температуры минус (45±5)°С, с последующим промораживанием (криостабилизацией) 18-20 ч и лиофилизацией в течение 24 ч до конечной температуры материала 25°С, при этом стадия сублимации в среднем составляет 14 ч, десорбции - 10 ч.
Недостатком способа является длительность процесса лиофилизации.
Известен способ получения противотуляремийной гипериммунной сыворотки и способ получения диагностикума эритроцитарного туляремийного иммуноглобулинового сухого [2]. Установленные в кассеты ампулы с диагностикумом помещают на полки сублимационной камеры аппарата лиофильной сушки "МАСС-5" предварительно охлажденных до температуры минус (30±2)°С. Камеру герметично закрывают. Диагностикум замораживают в течение (2,5±0,5) ч до достижения температуры материала не выше минус 25°С, затем создают в камере вакуум, поддерживаемый в течение всего процесса лиофильного высушивания на уровне 1,1-1Торр (13,33 н/м2). Через (2±0,5) ч включают подогрев всех полок. Через 1 ч полки прогреваются до температуры (28±1)°С, поддерживаемой до конца лиофильного высушивания, при этом температура в ампуле с диагностикумом через (13±1) ч также достигает (28±1)°С, после чего лиофильное высушивание продолжают в течение (6±0,5) ч. Продолжительность лиофильного высушивания диагностикума - (21±1) ч. По окончании процесса ампулы запаивают и контролируют качество сухого диагностикума.
Недостатком способа является то, что замораживание препарата проводится при недостаточно низкой температуре, а резкий подъем температуры полки (через 1 ч полки прогреваются до температуры (28±1)°С), может отрицательно повлиять на качество биоматериала. Следующий недостаток - длительность процесса лиофилизации.
Наиболее близким к предлагаемому способу можно считать следующий известный способ лиофильной сушки эритроцитарного диагностикума [3], включающий глубокое замораживание препарата, перемещение в камеру для лиофилизации и его дальнейшую сублимацию в условиях вакуума с последующим формированием лиофилизата. Препарат переводят в среду высушивания, состоящую из раствора реополиглюкина 15 мас. %, сахарозы 7,5 мас. % в дистиллированной воде. Температура полки и давление в камере для сублимации не изменяются первые 8 ч и составляют соответственно 15°С и 30 Па, затем в течение последующих 14 ч плавно меняются со скоростью (2,6±0,4)°С/ч и (2±0,1) Па/ч до 22°С и 3 Па. При указанных параметрах лиофильное высушивание продолжается не менее 3 ч. Время лиофилизации 22-24 ч.
Недостатком способа является длительность процесса лиофилизации.
Целью работы стала оптимизация режимов сублимационного высушивания эритроцитарных диагностикумов и получение качественного препарата с увеличенным сроком годности и возможностью транспортирования при любых значениях температуры.
Все процессы лиофилизации (замораживание, сублимация, досушивание, герметизация) являются обязательными и от правильно подобранных параметров данных процессов зависит получение стабильных препаратов без потери их специфической активности.
Технический результат достигается тем, что серии диагностикумов эритроцитарных (антигенного/иммуноглобулинового) переводят в ранее разработанную нами среду высушивания [4], хорошо перемешивают, разливают в стерильные ампулы марки ШПВ-6 по 1 мл 10% взвеси диагностикума (каждая серия объемом по 50 ампул) и переносят в морозильный стол для замораживания.
Замораживание материала при нормальном атмосферном давлении в морозильном столе является начальным этапом лиофилизации препаратов и должно быть проведено таким образом, чтобы продукт имел желаемую кристаллическую структуру и температура продукта была ниже, чем температура полного затвердевания (эвтектическая). Так, при температурах выше эвтектической точки в присутствии солей в белковых растворах может произойти денатурация белка. Однако слишком низкая температура значительно увеличивает продолжительность процесса сушки. Поэтому замораживание проводили в течение 16-18 ч при оптимальной температуре, которая составила минус (40±1)°С, т.е. ниже эвтектической точки, что позволяет предотвратить оттаивание продукта в процессе лиофилизации.
Для сублимационного высушивания использовали лиофильную установку камерного типа Alpha 2-4 с 2 полками в комплекте и с вакуумным насосом Martin Christ. Первоначально выставляли параметры камеры, запускали в работу насос на 15 мин, быстро перегружали замороженный в ампулах препарат в вакуумную камеру сублимационной установки и включали вакуум.
В лиофильной камере, кроме датчиков контроля температуры продукта, предусмотрены датчики температуры поверхности полок, датчик температуры конденсатора и вакуумный датчик, регистрирующий давление в камере. При включении вакуума происходило снижение давления в камере. На данном этапе отмечалось незначительное изменение температуры замороженного материала за счет отвода тепла сублимации, который осуществлялся при давлении 0,15-0,20 мбар (15-20 Па) в сушильной камере без подвода тепла к просушиваемому материалу. При включении нагрева полок за счет контактного поступления тепла через полку к продукту температура последнего начинала повышаться. Происходило интенсивное испарение влаги из продукта.
Продолжительность процесса сублимационной сушки, во время которого температура высушиваемого материала достигала температуры минус 10°С, составляла 2±0,5 ч. Этот период характеризовался большой интенсивностью тепло- и массообмена. Так как движущей силой процесса сублимации является разность парциального давления насыщенных паров материала и конденсатора или разность соответствующих этим давлениям температур материала и конденсатора. Во время сублимации строго поддерживалось низкое давление в камере, порядка 0,15-0,20 мбар (10-20 Па), с температурой конденсатора (десублиматора) - минус 80-90°С.
Плавное повышение температуры препарата от минус 10°С до 10°С занимало оптимальное для препарата время - 3±0,5 ч.
Этап десорбции, т.е. удаление связанной влаги, происходил медленно, что являлось следствием увеличения энергии связи влаги с материалом. Для диагностикума (50 ампул по 1 мл 10% взвеси в ампуле) - 4±0,5 ч. Температура препарата постоянно росла до значения максимальной температуры досушивания, т.е. равновесного влагосодержания, практически равного остаточной влажности. Оптимальная температура препарата на этом этапе составляет 25-26°С. Терминальный период процесса сушки происходил до момента приближения регистрированных значений к заданным параметрам, которые не менялись в течение 3-4 ч и соответственно равнялись следующим показателям: температура конденсатора - минус 80-90°С; температура полок 30°С, вакуум 15-20 Па, температура продукта 25-26°С, время лиофилизации - 12-13 ч (рисунок 1).
После завершения процесса высушивания препарат извлекали из камеры. Ампулы с препаратом запаивали на газо-кислородной горелке в среде атмосферного воздуха. Отбирали образцы из каждой серии для контроля.
Согласно медико-биологическим требованиям, потеря в массе при высушивании биологических препаратов должна быть не более 3%. Так как все биопрепараты в лиофилизированном состоянии обладают высокой степенью гидрофильности, мы проводили расфасовку и укупорку диагностикума в сухом помещении.
Оценку качества готовых лиофилизатов проводили по следующим показателям: внешний вид (структура и цвет таблетки в ампуле); растворимость (регидратация), цветность и прозрачность; значение рН после растворения; потеря в массе при высушивании; чувствительность и специфичность препарата в РНГА.
1. Внешний вид. Сухой препарат представляет собой аморфную массу коричневого цвета в форме таблетки, без признаков микрооттаивания.
2. Растворимость. Содержимое ампулы с препаратом полностью растворяется в 1 мл 0,9% раствора натрия хлорида, время растворения 1-2 мин. После растворения - жидкость насыщенно-коричневого цвета. При отстаивании в течение 2-3 ч образовалось два слоя: бесцветная прозрачная надосадочная жидкость и осадок коричневого цвета, разбивающийся при встряхивании.
3. рН раствора 6,5±0,2.
4. Потеря в массе при высушивании не более 2,5±0,2%.
5. Чувствительность и специфичность препаратов.
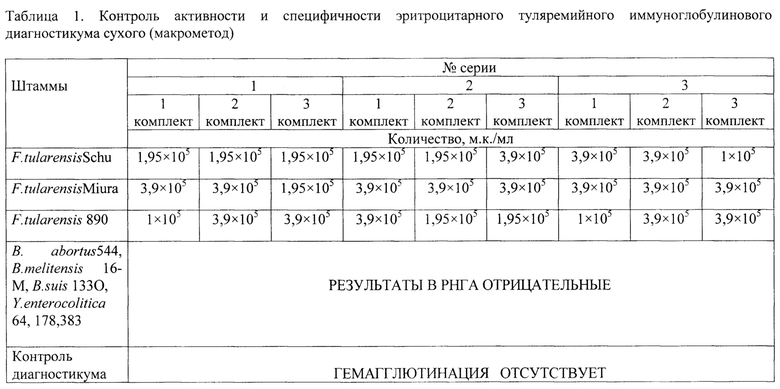
Для диагностикума эритроцитарного туляремийного антигенного установлена чувствительность (набор выявлял в РНГА специфические антитела в сыворотке диагностической туляремийной агглютинирующей в разведении 1:20000 - макрометодом и 1:10000 - микрометодом и в реакции нейтрализации антител (РНАт) культуры F. tularensisB концентрациях, эквивалентных по отраслевому стандарту мутности ОСО 42-28-85 ФГБУ «НЦЭСМП» Минздрава России 7,8×105м.к./мл макрометодом и 1,56×106 м.к./мл - микрометодом) и специфичность (набор не давал положительных результатов в РНГА с гетерологичными диагностическими сыворотками: холерной 01 адсорбированной сухой для реакции агглютинации (РА), поливалентной сальмонеллезной адсорбированной сухой О- для РА (А, В, С, Д, Е) и бруцеллезной адсорбированной агглютинирующей сухой в разведении до 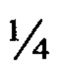 их титра).
их титра).
Для диагностикума эритроцитарного туляремийного иммуноглобулинового установлена чувствительность, диагностикум обеспечивает выявление в РНГА F.tularensis в концентрациях, эквивалентных по отраслевому стандарту мутности ОСО 42-28-85 ФГБУ «НЦЭСМП» Минздрава России 1,95×105-3,9×105 м.к./мл макрометодом и 7,8×105-1,56×106 м.к./мл микрометодом; в реакции нейтрализации антигена (РНАг) - антитела в сыворотке диагностической туляремийной агглютинирующей в разведении не менее 1:16000 - макрометодом, не менее 1:8000 - микрометодом) и специфичность (набор не давал положительных результатов в РНГА с гетерологичными штаммами: В. abortus 544, В. melitensis 16-М, В. suis 1330, Y. enterocolitica 64, 178, 383 в концентрациях, эквивалентных по отраслевому стандарту мутности ОСО 42-28-85 ФГБУ «НЦЭСМП» Минздрава России 1,0×108 м.к./мл).
Таким образом, отработан эффективный режим лиофилизации (12-13 ч): замораживание препаратов при температуре минус (40±1)°С, сокращение времени удаления не только свободной, но и связанной воды в препарате за счет глубокого вакуума -15-20 Па, плавного (до 25-26°С) подвода тепла и низкой температуры конденсатора - минус 80-90°С, тем самым исключено оттаивание и вспенивание препарата при сохранении физико-химических (растворимость, прозрачность, цветность, потеря в массе при высушивании) и иммунобиологических свойств препаратов (чувствительность, специфичность), по всем показателям полностью удовлетворяющим требованиям нормативной документации.
Возможность практического применения изобретения иллюстрируется примерами его конкретного выполнения с использованием совокупности заявляемых признаков.
Пример 1. Получали 50 мл 10% взвеси диагностикума эритроцитарного иммуноглобулинового туляремийного. Для этого диагностикум центрифугировали и осадок растворяли в среде высушивания, состоящей из 50 мл полиглюкина (6% раствора декстрана) с 1,6 мл твин-80 в разведении 1:50 и 5 мг азида натрия [4], замораживали 16-18 ч при температуре минус (40±1)°С и лиофилизировали, при постепенном подъеме температуры полки, до конечной температуры материала 25°С, выдерживали при данных параметрах 3 ч. Общее время лиофилизации - 12 ч. Герметизацию ампул после лиофилизации осуществляли в атмосфере осушенного очищенного воздуха при нормальном атмосферном давлении.
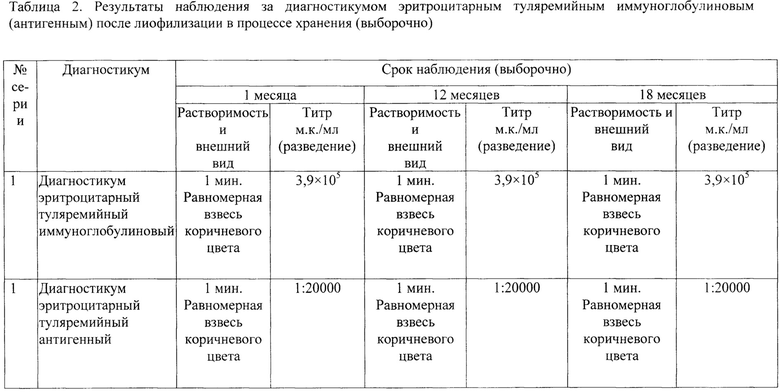
После чего препарат помещали в условия разных температурных режимов (24°С, 37°С, минус 4°С) и контролировали каждые 3 месяца в течение 1,5 лет (срок наблюдения). Лиофилизированный диагностикум растворяли в 0,9% растворе натрия хлорида и контролировали в РНГА. Препарат сохранял свою первоначальную чувствительность и специфичность. Отрицательного влияния различных температур не выявлено. Чувствительность - препарат обеспечивает выявление в РНГА F.tularensis в концентрациях, эквивалентных по отраслевому стандарту мутности ОСО 42-28-85 ФГБУ «НЦЭСМП» Минздрава России_1,95×105-3,9×105 м.к./мл макрометодом и 7,8×105-1,56×106 м.к./мл микрометодом, при отсутствии перекрестных реакций с гетерологичными штаммами.
Пример 2. Выполняли аналогично примеру 1, за исключением того, что получали диагностикум эритроцитарный антигенный туляремийный. Лиофилизированный диагностикум растворяли в 0,9% растворе натрия хлорида и ставили РНГА. Препарат сохранял свою первоначальную чувствительность и специфичность. Отрицательного влияния различных температур не выявлено. Чувствительность препарата в РНГА сохранялась и составила 1:20000 - макрометодом, при отсутствии перекрестных реакций с гетерологичными сыворотками.
Таким образом, для предотвращения разрушения жидких эритроцитарных диагностикумов во время транспортировки при температуре ниже регламентированных, препараты стабилизировали путем добавления к ним защитной среды при осуществлении лиофилизации с отработанным режимом сушки. Разработанный способ позволяет ускорить и упростить процесс получения стабильных диагностикумов при сокращении материальных и трудовых затрат, увеличивая срок годности препаратов.
При оценке качества серий лиофилизированных эритроцитарных диагностикумов, полученных по разработанной технологии лиофилизации на протяжении 18 мес установлено отсутствие изменений показателей качества. Изучение стабильности препаратов в процессе хранения продолжается. Минимальный срок годности полученных препаратов составляет 1,5 года (срок наблюдения) и может быть увеличен при накоплении экспериментальных данных, в то время как срок годности жидких препаратов - 1 год. Лиофилизированные эритроцитарные диагностикумы, полученные заявляемым способом, при хранении стабильно сохраняют физико-химические и иммунобиологические свойства (таблица 1, таблица 2).
Используемая литература
1. Патент РФ №2455014 Способ получения лиофилизированного препарата кровь гемолизированная. - Опубл. 10.07.2012. Бюл. №19.
2. Патент РФ №2240822. Способ получения противотуляремийной гипериммунной сыворотки и способ получения диагностикума эритроцитарного туляремийного иммуноглобулинового сухого. - Опубл. 27.11.2004. Бюл. №33.
3. Патент РФ №2476791. Способ лиофильной сушки эритроцитарного диагностикума. - Опубл.27.02.2013. Бюл. №2.
4. Патент РФ №2708636 Универсальная среда высушивания для стабилизации эритроцитарных диагностикумов туляремийных. - Опубл. 10.12.2019. Бюл. №34.
| название | год | авторы | номер документа |
|---|---|---|---|
| УНИВЕРСАЛЬНАЯ СРЕДА ВЫСУШИВАНИЯ ДЛЯ СТАБИЛИЗАЦИИ ЭРИТРОЦИТАРНЫХ ДИАГНОСТИКУМОВ ТУЛЯРЕМИЙНЫХ | 2019 |
|
RU2708636C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ЭРИТРОЦИТАРНОГО ДИАГНОСТИКУМА ИММУНОГЛОБУЛИНОВОГО ТУЛЯРЕМИЙНОГО | 2020 |
|
RU2747420C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА, ИСПОЛЬЗУЕМОГО В КАЧЕСТВЕ РАЗВОДЯЩЕЙ ЖИДКОСТИ И СРЕДЫ ВЫСУШИВАНИЯ ЭРИТРОЦИТАРНЫХ И ЛАТЕКСНЫХ ДИАГНОСТИКУМОВ | 2009 |
|
RU2395094C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОТУЛЯРЕМИЙНОЙ ГИПЕРИММУННОЙ СЫВОРОТКИ И СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ЭРИТРОЦИТАРНОГО ТУЛЯРЕМИЙНОГО ИММУНОГЛОБУЛИНОВОГО СУХОГО | 2002 |
|
RU2240822C2 |
| СПОСОБ ЛИОФИЛЬНОЙ СУШКИ ЭРИТРОЦИТАРНОГО ДИАГНОСТИКУМА | 2011 |
|
RU2476791C1 |
| ДИАГНОСТИКУМ ПСЕВДОТУБЕРКУЛЕЗНЫЙ ЭРИТРОЦИТАРНЫЙ МОНОКЛОНАЛЬНЫЙ | 2008 |
|
RU2377308C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ЭРИТРОЦИТАРНОГО САПНОГО ИММУНОГЛОБУЛИНОВОГО МОНОКЛОНАЛЬНОГО | 2017 |
|
RU2658434C1 |
| Способ получения бруцеллезного диагностикума | 2023 |
|
RU2831699C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННОГО ПРЕПАРАТА КРОВЬ ГЕМОЛИЗИРОВАННАЯ | 2011 |
|
RU2455014C1 |
| Способ получения бруцеллезного полистирольного латексного диагностикума | 2022 |
|
RU2798124C1 |

Изобретение относится к области биотехнологии. Изобретение представляет собой способ стабилизации эритроцитарных диагностикумов путем лиофильного высушивания. Перед замораживанием и лиофилизацией диагностикумы центрифугируют и осадок ресуспендируют в равном объеме среды высушивания. Замораживают препараты при температуре минус (40±1)°С; время удаления не только свободной, но и связанной воды в препарате, во время лиофилизации, сокращается за счет глубокого вакуума - 15-20 Па, плавного (до 25°С) подвода тепла и низкой температуры конденсатора - минус 80-90°С, тем самым исключено оттаивание и вспенивание препарата. Изобретение позволяет увеличить срок годности препарата с сохранением его качественных характеристик. При рентабельном режиме лиофилизации (12-13 ч). 2 табл., 1 ил.
Способ лиофилизации эритроцитарного туляремийного диагностикума, включающий глубокое замораживание препарата, перемещение его в камеру для лиофилизации и его дальнейшую сублимацию в условиях вакуума с последующим формированием лиофилизата, отличающийся тем, что замораживание препаратов проводилось при температуре минус (40±1)°С; лиофилизация осуществлялась при сокращении времени удаления не только свободной, но и связанной воды в препарате за счет глубоко вакуума - 15-20 Па, плавного (до 25°С) подвода тепла и низкой температуры конденсатора - минус 80-90°С и при указанных параметрах выдерживают 12-13 часов.
| СПОСОБ ЛИОФИЛЬНОЙ СУШКИ ЭРИТРОЦИТАРНОГО ДИАГНОСТИКУМА | 2011 |
|
RU2476791C1 |
| УНИВЕРСАЛЬНАЯ СРЕДА ВЫСУШИВАНИЯ ДЛЯ СТАБИЛИЗАЦИИ ЭРИТРОЦИТАРНЫХ ДИАГНОСТИКУМОВ ТУЛЯРЕМИЙНЫХ | 2019 |
|
RU2708636C1 |
| US 6294365 B1,25.09.2001. | |||
Авторы
Даты
2021-06-09—Публикация
2020-07-17—Подача