Изобретение относится к области биотехнологии и может быть использовано для лиофильной сушки биопрепаратов.
Известен способ лиофилизации биопрепарата, включающий этапы его замораживания и вакуумного обезвоживания. Перед лиофилизацией раствор биопрепарата подвергается очистке и концентрированию без введения дополнительных стабилизирующих компонентов [1].
Однако процесс лиофилизации по данной технологии зачастую ведет к значительной (иногда - полной) потере специфической активности препарата [2], а лиофилизированный материал часто "размазан" по дну флакона вследствие малого содержания суммарного сухого остатка.
Известен способ лиофилизации, включающий добавление в раствор биопрепарата перед лиофилизацией стабилизаторов - смеси глицина и маннитола [6]. Это позволяет уменьшить падение биологической активности на этапе лиофилизации и сформировать объемную таблетку.
Однако глицин и маннитол являются легко кристаллизующимися компонентами. Они склонны кристаллизовываться при замораживании их водных растворов или при хранении лиофилизированного препарата (в случае, если в процесс лиофилизации удалось достигнуть частичного стеклования). Известно [0], что процессы кристаллизации в таких случаях приводят к практически полной инактивации препарата. В случае же, когда в растворе биопрепарата уже содержатся стеклующиеся компоненты, введение двух или более кристаллизующихся компонентов нецелесообразно, поскольку они тормозят кристаллизацию друг друга, и для достижения вторичной кристаллизации нужно будет использовать повышенные концентрации дополнительно добавляемых компонентов.
Наиболее близким решением, выбранным в качестве прототипа, является способ сушки биопрепарата, включающий введение в раствор этого биопрепарата перед лиофилизацией защитной среды, которая предотвращает падение его биологической активности при лиофилизации и хранении за счет формирования стеклообразной матрицы и образования объемной таблетки. Для этого используют среды высушивания, одним из главных компонентов которых является углевод, например сахароза [3] . Защитное действие указанных компонентов связано с тем, что в ходе охлаждения раствора биопрепарата после первичной кристаллизации воды остается концентрированный раствор содержащий 15-30% "незамороженной" воды, который при дальнейшем охлаждении переходит в некристаллическое твердое состояние - стеклуется. Критической температурной характеристикой таких растворов, определяющей выбор температурного режима лиофилизации, является температура коллапса [4]. Коллапс (исчезновение пористой структуры образца] вызывается переходом этого концентрированного раствора из твердого некристаллического (стеклообразного) состояния в вязко-текучее состояние. В случае увеличения температуры материал при лиофилизации выше температуры коллапса наблюдается потеря пористой структуры материала, образующейся в результате сублимации кристаллов льда, что увеличивает время досушивания до заданной влажности и вызывает потерю качества сухого продукта ( внешнего вида, растворимости и т.д.). Типичные значения температур коллапса для водных растворов углеводов - от - 32oC до - 50oC.
Недостатком такого способа сушки является то, что при использовании в нем стабилизирующего состава требуется поддержание температуры материала на этапе сублимации не выше -30 - 40oC, чтобы избежать коллапса. Низкие температуры коллапса предъявляют специальные требования к используемому лиофильному оборудованию и удлиняют процесс сушки.
Задачей предлагаемого технического решения является создание такого способа сушки препаратов, который позволил бы обеспечить возможность проведения лиофилизации при более высоких температурах доля препаратов с низкой температурой коллапса (-30oC и ниже).
Поставленная задача решается тем, что в способе лиофильной сушки биопрепарата, включающем введение в раствор этого биопрепарата перед сушкой защитной среды с последующим замораживанием полученной смеси и вакуумной сушкой, согласно изобретению, в состав защитной среды дополнительно вводят вещество-наполнитель, кристаллизующееся при замораживании его разбавленного водного раствора в концентрации, достаточной для формирования аморфнокристаллической структуры в объеме жидкой фазы биопрепарата, остающейся после кристаллизации воды.
Причем предварительно перед сушкой приготавливают пробные образцы биопрепарата (белок или вирус) с защитной средой или одну защитную среду с разной концентрацией вещества-наполнителя, с последующим проведением термического или рентгенофазового анализа, или пробной лиофилизации при температуре сушки, равной или выше температуры коллапса исходного биопрепарата, а концентрацию вещества-наполнителя выбирают равной или более концентрации вещества-наполнителя в пробном образце биопрепарата, кривая термического или рентгенофазового анализа которого содержит дополнительный пик по сравнению с аналогичной кривой термического или рентгенофазового анализа образца исходного биопрепарата, или равной или более концентрации вещества-наполнителя в пробном образце биопрепарата, показывающем наличие таблетки после лиофилизации.
В качестве вещества-наполнителя используют хлорид натрия или хлорид калия или глицин.
Конкретная концентрация добавляемого вещества-наполнителя зависит от природы и концентрации присутствующих первоначально в растворе биопрепарата веществ. Наличие вторичной кристаллизации (образование аморфно-кристаллической матрицы в объеме жидкой фазы биопрепарата, остающейся после кристаллизации воды) определяют, как указывалось выше, одним из методов термического анализа (либо другим физическим метолом, позволяющим фиксировать наличие дополнительной кристаллической фазы, например, рентгенофазовым анализом замороженных образцов, либо просвечивающей электронной микроскопией- метод криофрактографии), либо с помощью пробной лиофилизации. В процессе термического анализа фиксируют количество переходов, соответствующих кристаллизации и плавлению, Наиболее простыми распространенными методами анализа является метод дифференциально-термического анализа (ДТА) либо дифференциальной сканирующей калориметрии (ДСК). В процессе ДТА или ДСК при охлаждении определяется количество экзотермических пиков, соответствующих кристаллизации, а при нагревании - количество эндотермических пиков, соответствующих плавлению. Для исходного биопрепарата в большинстве случаев фиксируют один экзотермический пик (кристаллизация воды) при охлаждения и один эндотермический (плавление льда) - при нагревании. Для приготовления образцов при некоторых концентрациях вещества - наполнителя больше некоторого критического значения фиксируют дополнительный экзотермический пик (кристаллизация добавленного компонента с водой) при охлаждении и дополнительный эндотермический пик (плавление добавленного компонента с водой при нагревании. При пробной лиофилизации фиксируют внешний вид образцов (наличие или отсутствие коллапса). Для составов с концентрацией вещества-наполнителя больше критического значения коллапса не наблюдается. Для основного процесса сушки биопрепарата выбирают один из составов с концентрацией вещества-наполнителя больше критического значения. При этом перед лиофилизацией к исходному раствору биопрепарата добавляют кристаллизующийся компонент в указанном количестве. После этого материал подвергают обычной процедуре лиофилизации, включающей стадии замораживания и вакуумного обезвоживания.
Растворенные вещества, присутствующие в биопрепарате или добавляемые в него в качестве вещества-наполнителей, можно разделить на два этапа, отличающиеся по фазовому поведению из разбавленных бинарных водных растворов при замораживании [3], кристаллизующиеся демонстрирующиеся (демонстрирующие эвтектическую кристаллизацию) и стеклующиеся, образующие фазу льда и пересышенную некристаллическую твердую (стеклообразную) жидкую фазу. Типичные кристаллизующиеся компоненты - хлориды калия и натрия, глицин, маннит. Типичные некристаллизующиеся компоненты - сахароза, сорбит, пептон.
Вещества, способные к кристаллизации, например, неорганические соли и глицин, входят в состав большинства биопрепаратов. Они служат для поддержания pH раствора, ионной силы, являются компонентами культуральных сред (глицин) и присутствуют в растворе биопрепарата в небольших количествах, как правило, не больше 20% от общей массы сухого остатка. Такие низкие количества кристаллизующихся веществ не обеспечивают образования при замораживании кристаллической структуры в объеме жидкой азы биопрепарата, остающейся после кристаллизации воды. Присутствие солей в растворе биопрепарата в этих концентрациях еще более понижает температуру коллапса, поэтому в известных аналогах и прототипе рекомендуется максимально обессолить раствор перед лиофилизацией [1].
В случае, когда в материале, подвергающемся лиофилизации, присутствуют только кристаллизующиеся компоненты (например, NaCl), при лиофилизации наблюдается значительная инактивация и при хранении такой препарат полостью инактивируется в течение короткого периода времени [2].
Известный прием введения в раствор биопрепарата перед лиофилизацией стабилизаторов, например смеси глицина и маннитола [8], позволяет уменьшить падение биологической активности на этапе лиофилизации и сформировать объемную таблетку. Однако глицин и маннитол являются легко кристаллизующимися компонентами, и они склонны кристаллизоваться при замораживании их водных растворов или при хранении лиофилизированного препарата (в случае, если при лиофилизации удалось достигнуть частичного стеклования). Известно [9], что процессы кристаллизации в таких случаях приводят к практически полной инактивации препарата. В случае же, когда в растворе биопрепарата уже содержатся стеклующиеся компоненты, введение двух или более кристаллизующихся компонентов нецелесообразно, поскольку они тормозят кристаллизацию друг друга, и для достижения вторичной кристаллизации нужно будет использовать повышенные концентрации дополнительно добавляемых компонентов.
Сравнение заявляемого способа получения с известными показывает, что отличительные от прототипа признаки проявляют новое неизвестное ранее свойство, а именно: возможность проведения лиофилизации при более высокой температуре, выше температуры коллапса, что свидетельствует о соответствии предлагаемого технического решения критерию "изобретательский уровень".
Такая возможность проведения лиофилизации при более высокой температуре, выше температуры коллапса, обусловлена тем, что при охлаждении раствора в объеме жидкой фазы, остающейся после первичной кристаллизации воды, происходит образование кристаллов одного из растворенных веществ (например, хлорида натрия или глицина). Стеклующиеся компоненты формируют аморфную фазу, которая содержит также некоторое количество вещества-наполнителя и воды и которая не кристаллизуется при дальнейшем охлаждении, высушивании и хранении. Кристаллы же выступают в качестве "механического стабилизатора". Поэтому температуру материала на этапе сублимации можно поддерживать выше температуры коллапса оставшейся аморфной фазы, без визуального коллапса препарата. Типичное изменение температуры коллапса для углевода при добавлении низкомолекулярного кристаллизующегося компонента изучено. При увеличении относительного количества кристаллизующегося компонента температура коллапса понижается. При некотором соотношении компонентов при охлаждении раствора наблюдается вторичная кристаллизация вода. растворенное вещество, для этих составов температура коллапса постоянна и не зависит от исходного состава раствора. Для этих составов лиофилизацию можно проводить выше температуры коллапса аморфной фазы, поскольку образовавшиеся при замораживании кристаллы образуют механический каркас, который препятствует изменению формы материала даже при переходе аморфной фазы в вязкотекучее состояние (выше температуры коллапса).
Пример осуществления предлагаемого способа.
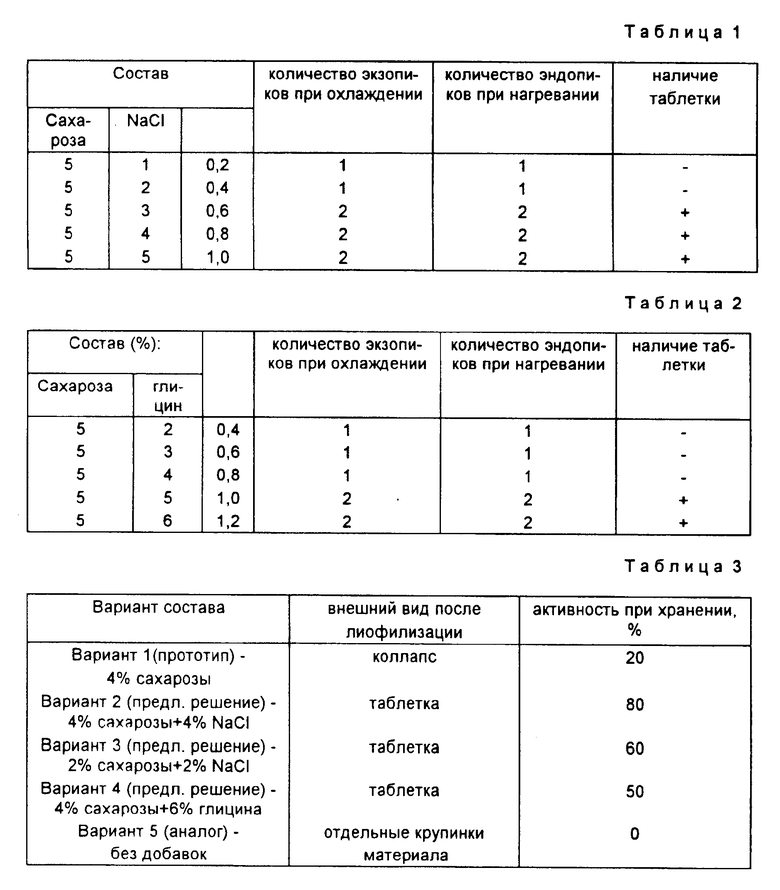
Пример 1. Выбор необходимого количества добавляемого вещества-наполнителя показан на примере защитной среды, содержащей 0,02 М фосфатно-солевого буфера (ФСБ) с содержанием 0,9% NaCl и 5% сахарозы. Указанная защитная среда используется для приготовления многих биопрепаратов. В качестве вещества-наполнителя используют хлорид натрия. Для выбора необходимого количества добавляемого вещества-наполнителя приготовлено 5 образцов препарата с содержанием хлорида натрия 1%, 2%, 3%, 4%, и 5% и выполнен дифференциально- термический анализ указанных проб, а также их пробная лиофильная сушка. Кривые ДТА снимали при охлаждении и последующем нагревании замороженных образцов. Результаты приведены в табл. 1. По табл. 1 определяют, что соотношение NaCL/сахароза в высушиваемом растворе должно быть больше 0,6.
Пробную лиофильную сушку материала проводят на установке TG-50. Препараты разливают по 0,5 мл во флаконы объемом 10 мл. Замораживание проводят при - 60oC в течение 18 ч. После чего осуществляют вакуумное обезвоживание при температуре полки -40oC. Скорость нагревания на этапе досушивания составляет 4 - 6oC/ч. Конечная температура материала 25oC. Общее время вакуумного обезвоживания составляет 20 ч. Качество продукта после лиофилизации оценивалось по внешнему виду (наличие или отсутствие таблетки). Результаты ДТА и пробной лиофилизации защитной среды при различном количестве NaCl приведены в табл. 1.
Пример 2. Для лиофильной сушки препаратов в качестве вещества-наполнителя моет быть использованы глицин. Выбор необходимого количества добавляемого вещества-наполнителя на примере защитной среды, содержащей 0,02 М ФБ + 5% сахарозы. Для выбора необходимого количества добавляемого вещества-наполнителя приготовлено 5 образцов препарата с содержание вещества-наполнителя (глицин) 2%, 3%, 4%, 5% и 6%, а также выполнен их дифференциально-термический анализ и пробная лиофильная сушка указанных образцов препарата. Кривые ДТА снимают при охлаждении и последующем нагревании замороженных образцов. Результаты приведены в табл. 2. По табл. 2 определяют, что соотношение глицин/сахароза в высушиваемом растворе должно быть больше 1.
Пробная лиофильная сушка материала проводилась на установке TG-50. Препараты разливают по 0,5 мл во флаконы объемом 10 мл. Замораживание проводят при -60 oC в течение 18 ч, после чего проводят вакуумное обезвоживание при температуре полки -40oC. Скорость нагревания на этапе досушивания составляет 4-6oC/ч. Конечная температура материала 25oC. Общее время вакуумного обезвоживания 20 ч. Качество продукта после лиофилизации оценивалось по внешнему виду/наличие или отсутствие таблетки). Результаты ДТА и пробной лиофилизации защитной среды (ФБ+сахароза) с веществом-наполнителем (глицин) при различном количестве глицина приведены в табл. 2.
Пример 3. Предлагаемый способ сушки реализован на примере биопрепарата - растворе коньюгата (Кг иммуноглобулина G с пероксидазой хрена в 0,02 М фосфатном буфере (ФБ). Для сопоставления предлагаемого способа с прототипом в раствор перед сушкой добавляют стабилизатор - 4% сахарозы (вариант 1 - прототип). В соответствии с предлагаемым решением приготавливают 2 раствора с NaCL (соотношение NaCl/сахароза R-1) и 1 раствор с глицином (соотношение глицин/сахароза R-1,5). Для этого в отобранные аликвоты раствора Кr с 4% сахарозы для получения раствора с R-1 дополнительно добавляют рассчитанное количество кристаллического NaCl (вариант 2), 4% раствор NaCl в ФСБ (вариант 3) и рассчитанное количество кристаллического глицина (варианта 4). Эти растворы демонстрируют два экзотермических пика на кривой ДТА охлаждения и два эндотермических пика - при нагревании, в отличие от варианта 1. Лиофилизацию проводят при температуре материала на этапе сублимации льда -40oC, выше температуры коллапса по варианту 1 (температура коллапса -45oC) Качество продукта после лиофилизации оценивалось по внешнему виду и специфической активности в тесте ELISA при хранении (+45oC, 2 недели). Данные по качеству сушки коньюгата G с пероксидазой хрена, имеющего различное содержание вещества-наполнителя, приведены в табл. 3.
Сопоставительный анализ результатов (табл. 3) позволяет сделать вывод о более высоком качестве биопрепарата, приготовленного по заявляемому способу сушки материала, лиофилизация которого проводилась при температуре выше температуры коллапса.
Данные, полученные при введении в высушиваемый биопрепарат хлорида калия, используемого в качестве вещества-наполнителя, аналогичны данным при использовании в качестве вещества-наполнителя хлорида натрия (табл. 1 и 3, примеры 1 и 3).
Промышленная применимость.
Изобретение может быть использовано в медицинской, микробиологической и фармацевтической промышленности для приготовления лиофилизированных биопрепаратов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СТАБИЛИЗИРУЮЩИЙ СОСТАВ ДЛЯ ПОЛУЧЕНИЯ РЕФЕРЕНС-СЫВОРОТОК, СОДЕРЖАЩИХ IGM-АНТИТЕЛА | 1997 |
|
RU2136313C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННОГО ПРОДУКТА ИЗ ГИДРОЛИЗАТОВ ДВУСТВОРЧАТЫХ МОЛЛЮСКОВ | 2024 |
|
RU2819659C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕФЕРЕНС-ПАНЕЛИ ДЛЯ КОНТРОЛЯ КАЧЕСТВА ТЕСТ-СИСТЕМ И ВАКЦИН ПРОТИВ ГЕПАТИТА В | 1999 |
|
RU2181893C2 |
| СТАБИЛИЗИРУЮЩИЙ СОСТАВ ДЛЯ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННЫХ ПРЕПАРАТОВ НА ОСНОВЕ КОНЪЮГАТА АНТИИММУНОГЛОБУЛИНА G И ПЕРОКСИДАЗЫ ХРЕНА | 1996 |
|
RU2109290C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛИРОВАННОЙ ФОРМЫ КОРЕВОЙ ВАКЦИНЫ ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ | 2001 |
|
RU2210361C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОНТРОЛЬНЫХ ПАНЕЛЕЙ СЫВОРОТОК ДЛЯ КОНТРОЛЯ КАЧЕСТВА ДИАГНОСТИКИ ГЕПАТИТА В | 1999 |
|
RU2179726C2 |
| ТАБЛЕТИРОВАННАЯ ФОРМА РЕКОМБИНАНТНОГО ЧЕЛОВЕЧЕСКОГО ЭРИТРОПОЭТИНА ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1997 |
|
RU2152206C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ КОРЕВОЙ ВАКЦИНЫ | 1998 |
|
RU2140288C1 |
| ТАБЛЕТИРОВАННАЯ ФОРМА РЕКОМБИНАНТНОГО ЧЕЛОВЕЧЕСКОГО ЭРИТРОПОЭТИНА | 2000 |
|
RU2182830C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННОГО ПРЕПАРАТА НА ОСНОВЕ РЕКОМБИНАНТНОГО α-2-ИНТЕРФЕРОНА ПРОТИВ ВИРУСНЫХ БОЛЕЗНЕЙ ПЛОТОЯДНЫХ | 1995 |
|
RU2121364C1 |
Способ используется в области биотехнологии для лиофильной сушки биопрепаратов. Способ позволяет проводить при более высоких температурах лиофилизацию материалов с низкой температурой коллапса (-30oC и ниже). Способ включает введение в раствор биопрепарата перед сушкой защитной среды с последующим замораживанием полученной смеси и вакуумной сушкой. В состав защитной среды дополнительно вводят вещество-наполнитель, кристаллизующееся при замораживании его разбавленного водного раствора, в концентрации, достаточной для формирования аморфно-кристаллической структуры в объеме жидкой фазы биопрепарата, остающейся после кристаллизации воды. Предварительно перед сушкой приготавливают пробные образцы биопрепарата с защитной средой или одну защитную среду с разной концентрацией вещества-наполнителя, с последующим проведением термического или рентгенофазового анализа, или пробной лиофилизации при температуре сушки, равной или выше температуры коллапса исходного биопрепарата, а концентрацию вещества-наполнителя выбирают равной или более концентрации вещества-наполнителя в пробном образце биопрепарата, кривая термического или рентгенофазового анализа которого содержит дополнительный пик по сравнению с аналогичной кривой термического или рентгенофазового анализа образца исходного биопрепарата, или равной или более концентрации вещества-наполнителя в пробном образце биопрепарата, показывающем наличие таблетки после лиофилизации. В качестве вещества-наполнителя используют хлорид натрия или хлорид калия или глицин. 4 з.п.ф-лы, 3 табл.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| L.O.Henderson, J.S.Hazlehurst, L.Taylor and W.H.Hannon | |||
| Preparation of lyophillzed human serum based reference materials with graded levels of apolipoproteins A-I and B | |||
| - Clin.Biochem., 1988, v | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| Прибор для записи звуковых волн | 1920 |
|
SU219A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Y.Matsuda | |||
| Factors affecting the blological activity of lyophilized myofibrils - protective substances and collapse temperatures | |||
| in: Fundamantals and applications of freeze-drying to biological materials, drugs and foodstuffs | |||
| - Proceeding of meeting of Commiss | |||
| Ci, Tokyo, May 20 - 22, 1985, -Intern.Inst.Refrigeration, 1985, p | |||
| Клапанный регулятор для паровозов | 1919 |
|
SU103A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Селезнева А.Ю., Николаева О.В., Фадеева Л.Л., Халецкая Э.В., Ролдугина В.В | |||
| Методические рекомендации по лиофилизации различных групп вирусов для целей длительного хранения | |||
| - Институт Вирусологии им.Д.И.Ивановского АМН СССР, N 2101 - 83 Деп.-М.:, 1982, с | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| F.Franks | |||
| Jap | |||
| J | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| H | |||
| Levine and L | |||
| Slade, Gryo-Lett | |||
| Механизм для сообщения поршню рабочего цилиндра возвратно-поступательного движения | 1918 |
|
SU1989A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| B.S | |||
| Chang and C.S.Randall, Cryobiology, 1992, v | |||
| Солесос | 1922 |
|
SU29A1 |
| ЭЛЕКТРИЧЕСКИЙ ПРИБОР ДЛЯ ВЫБРАСЫВАНИЯ ШАРИКОВ И УКАЗАНИЯ ЦИФР ПРИ ИГРЕ В ЛОТО | 1922 |
|
SU632A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Rey L.R | |||
| Glimpses into fundemental aspects of freeze-drying | |||
| - Develop.Biol.Stand., 1977, v | |||
| Коридорная многокамерная вагонеточная углевыжигательная печь | 1921 |
|
SU36A1 |
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| L.-M.Her, M.Deras, and S.L.Nail | |||
| Electrolyte-induced changes in glass transition temperatures of freeze-concentrated solutes | |||
| - Pharmaceutical research, 1995, v | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Снегоочиститель для городских железных дорог | 1924 |
|
SU768A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| M.J.Pikal, Karen Dellerman and M.L.Roy | |||
| Formulation and stability of freeze-dried proteins: effects of moisture and oxygen on the stability of freeze-dried formulations of human growth hormone | |||
| - Develop | |||
| biol | |||
| Stand., v | |||
| Приспособление в центрифугах для регулирования количества жидкости или газа, оставляемых в обрабатываемом в формах материале, в особенности при пробеливании рафинада | 0 |
|
SU74A1 |
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| E.Yu | |||
| Shalav, A.N.Kanev | |||
| Solid-liquid state diagram of the water-glyctine-sucrose system | |||
| - Gryobiology, 1994, v | |||
| Способ очистки нефти и нефтяных продуктов и уничтожения их флюоресценции | 1921 |
|
SU31A1 |
| Устройство для телефонирования по проводам токами высокой частоты | 1921 |
|
SU374A1 |
Авторы
Даты
1998-05-20—Публикация
1995-11-03—Подача