Область техники
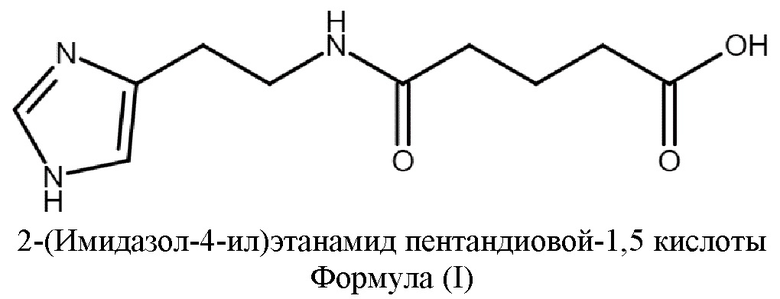
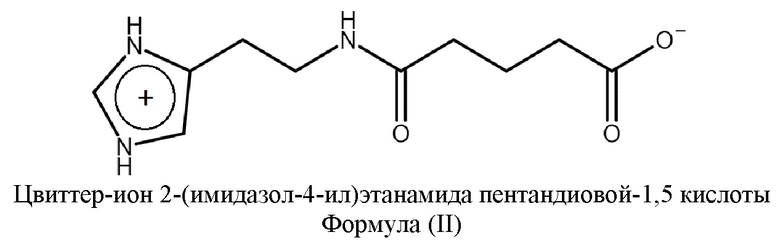
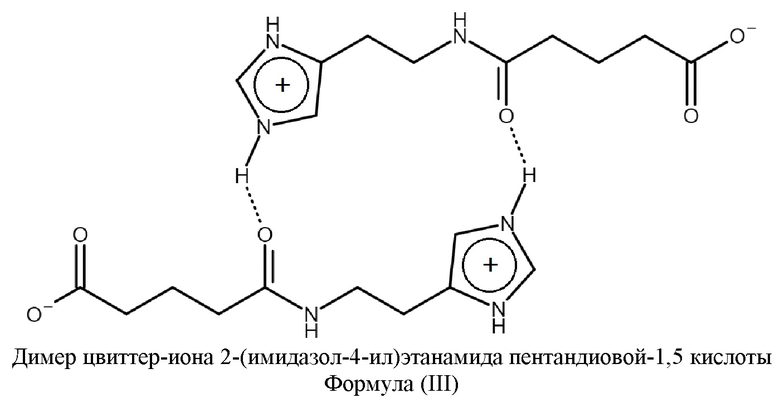
Изобретение относится к областям органической химии, фармакологии и химико-фармацевтической промышленности, а именно к новым твердым формам 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты формулы (I), содержащим 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты в виде цвиттер-иона формулы (II) или димера цвиттер-иона формулы (III). Изобретение также относится к содержащим указанные формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты фармацевтической композиции и лекарственному средству. Изобретение может найти применение для лечения и/или профилактики заболеваний, вызванных вирусными инфекциями.
Уровень техники
Инфекционные заболевания занимают третье место среди причин смертности людей по всему миру, большая часть которых приходится на вирусные заболевания. Среди вирусных инфекций одно из ведущих мест занимают герпесвирусы из-за повсеместного распространения. По данным ВОЗ около 90% населения земного шара имеют проявления герпетической инфекции, а смертность от этих инфекций находится на втором месте после вирусного гепатита. Поэтому проблема герпетических заболеваний на сегодня особенно актуальна. Науке известно более 100 видов вируса герпеса, из них 8 антигенных разновидностей вызывают заболевания у человека (вирусы простого герпеса (Herpes simplex) 1-го и 2-го типа, ветряной оспы и опоясывающего герпеса (Varicella zoster), цитомегаловирус, вирус Эпштейна-Барр, вирусы герпеса человека 6-го, 7-го и 8-го типа). Вирусы герпеса способны пожизненно находиться в организме человека и вызывать заболевания с разнообразными проявлениями от бессимптомного носительства до тяжелых форм с развитием герпетического энцефалита, менингита, заканчивающихся летальным исходом. Локализация герпетических высыпаний различна - кожа, слизистые оболочки ротовой полости и половых органов, роговица, внутренние органы. Для лечения и предотвращения рецидивов герпетической инфекции существует большой выбор препаратов с выраженным противовирусным действием, однако эти средства имеют ряд побочных эффектов, в том числе снижение устойчивости организма к вирусам (О.В.РУБЛЕВА, К вопросу о терапии и профилактике вирусных инфекций, РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ, 2012, Т.20, 11, c.571-574).
Многие вирусы поражают дыхательные пути, носовые ходы, горло, бронхи, легкие, в связи с чем такие вирусные инфекции собраны в группу острых респираторных вирусных инфекций (ОРВИ), поскольку обладают также и общностью клинических симптомов. Вирусы гриппа также относятся к группе ОРВИ, однако выделены в отдельную группу в связи с тем, что воздействуют системно на весь организм. Причиной ОРВИ могут быть более 200 различных вирусов, представителей 4 семейств РНК-содержащих вирусов (ортомиксовирусы, парамиксовирусы, коронавирусы и пикорнавирусы) и 2 семейств ДНК-содержащих вирусов (аденовирусы и герпесвирусы). По частоте инфицирования грипп составляет около 15% (тип А - 12%, В - 3%), парагрипп и риновирусы до 50%, аденовирус до 5%, респираторно-синцитиальный вирус (PC) - 4%, микоплазма - около 2%, энтеровирусы - около 1%, смешанные инфекции - около 23% случаев. К группе высокого риска относятся дети, у которых заболевания респираторного тракта составляют до 90% всей инфекционной патологии и 65% от всех регистрируемых заболеваний (О.В.РУБЛЕВА, К вопросу о терапии и профилактике вирусных инфекций, РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ, 2012, Т.20, 11, c.571-574; Е.П.СЕЛЬКОВА, Профилактика и лечение острых респираторных вирусных инфекций. Применение амиксина», Пособие для врачей, М., 2004).
Для всех ОРВИ характерны симптомы общей интоксикации (головная боль, слабость, мышечные боли, потеря аппетита), повышенная температура, катаральные явления (заложенность носа, насморк, кашель, боль в горле). Локализация очага поражения во многом зависит от вида возбудителя. Так, риновирусные заболевания характеризуются преобладанием ринита, аденовирусные инфекции - ринофарингита, для парагриппа характерен фарингит, а для гриппа - трахеит, респираторно-синцитиальный вирус поражает бронхи. Возможны и другие симптомы, например, аденовирусы могут вызывать конъюнктивиты и кератиты. Обычно симптомы ОРВИ сохраняются в течение 3-7 дней (кашель может наблюдаться более длительное время), возможная длительность гриппа составляет 1-2 недели. Среди осложнений выделяют ларингит, тонзиллит, фарингит и трахеит бактериальной природы, различные формы синуситов (гайморит, этмоидит, фронтит), а также отит, евстахиит, возможно развитие бронхита и пневмонии. Основные причины осложнений - нарушения иммунной защиты, приводящие к длительно протекающим иммунодефицитам, сочетающимся с резким снижением антибактериальной резистентности организма. При правильно выбранной тактике лечения ОРВИ риск развития осложнений заметно снижается (Ю.З.ГЕНДОН, Этиология острых респираторных заболеваний, ВАКЦИНАЦИЯ, 2001, Т.5, 17, c.4-5).
Самым эффективным способом контроля за сезонной заболеваемостью гриппом до настоящего времени остается вакцинация. Известны вакцины против гриппа, которые в зависимости от технологии изготовления делятся на два класса: живые и инактивированные. Главный недостаток вакцинации состоит в том, что ее действие ограничено только вирусами гриппа, а защита против других возбудителей ОРВИ отсутствует. Перспективным направлением профилактики является использование средств для активизации неспецифической резистентности организма (А.А.ЗАЙЦЕВ, Направления фармакотерапии и профилактики острых респираторных вирусных инфекций, РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ, 2009, Т.17, 23, с.1525-1529). Профилактическая эффективность противовирусных средств в период вспышки заболевания является высокой и достигает 70-80%. При этом, профилактику противовирусными средствами можно проводить как для иммунизированных лиц, так и для лиц, не прошедших вакцинацию.
Таким образом, существует потребность в разработке новых стабильных средств и доступных терапевтических форм для лечения и профилактики гриппа и ОРВИ для создания стратегических государственных резервов на случай эпидемий или пандемий.
Наиболее близким аналогом для рассматриваемого изобретения является соединение 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты. Для него известно применение в качестве антиоксидантного (RU2141483C1), и противовирусного (EA020283B1, RU2496512C1) средств.
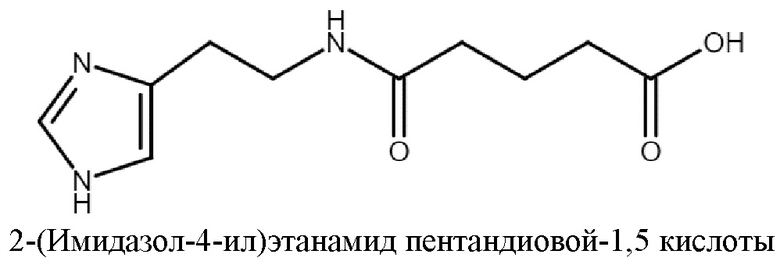
2-(Имидазол-4-ил)этанамид пентандиовой-1,5 кислоты нашел применение в клинической практике в качестве средства, эффективного против вируса гриппа типа А (Регистрационное удостоверение ЛП-006482).
Одной из актуальных задач при разработке лекарственных препаратов остается получение стабильного в течение длительного срока хранения действующего вещества. Учитывая, что невозможно предсказать антигенную структуру будущего эпидемического (пандемического) вируса, заблаговременное конструирование эффективных вакцин затруднительно, поэтому важно иметь в арсенале лекарственные средства для профилактики и лечения заболеваний, вызываемых высокопатогенными штаммами вирусов. При этом, как показала ситуация с пандемией COVID-19 во всем мире (Y.WANG et al., Unique epidemiological and clinical features of the emerging 2019 novel coronavirus pneumonia (COVID-19) implicate special control measures, JOURNAL OF MEDICAL VIROLOGY, 2020, V.92, N.6, pp.568-576), для своевременного обеспечения граждан противовирусными лекарственными средствами в условиях пандемии целесообразно создание государственных резервов таких средств. Стратегические государственные резервы на случай пандемий подлежат долгосрочному хранению и обновлению по истечении срока годности зарезервированных лекарственных средств. В такой ситуации крайне важным является увеличение долгосрочной стабильности для продления сроков хранения и снижения государственных затрат на создание и обновление стратегических резервов противовирусных средств.
Среди лекарственных средств, применяемых при гриппе и ОРВИ, приоритет принадлежит этиотропным препаратам. Одним из таких соединений и является 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты. Соответственно разработка более стабильных форм 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты, подходящих для долгосрочного хранения, является одной из наиболее актуальных задач в текущих условиях.
Для увеличения срока хранения композиций, содержащих 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты, ранее было предложено использовать субстанцию, дополнительно содержащую N,N'-бис-[2-(1Н-имидазол-4-ил)этил]пентандиамид (RU2746692С1). Сложностью указанного решения является необходимость наличия N,N'-бис-[2-(1Н-имидазол-4-ил)этил]пентандиамида в составе композиции, содержащей 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты. Настоящее техническое решение предлагает твердую форму 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты, хранение которой возможно без добавления вспомогательных веществ.
Таким образом, задачами настоящего изобретения являются разработка промышленно доступной, стабильной при хранении формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты для лечения и профилактики заболеваний дыхательных путей, в частности, гриппа и ОРВИ, обеспечивающей высокую противовирусную активность, а также расширение арсенала лекарственных средств, обладающих противовирусным действием, и подходящих для создания стратегических государственных резервов на случай эпидемий или пандемий.
Раскрытие изобретения
Технический результат
Соединения с заряженными группами (ионы аммония, фосфония и т.д.) привлекают внимание медицинских химиков благодаря своим уникальным физико-химическим свойствам. Например, известно, что соли фосфония накапливаются в воспаленных тканях человека, вследствие чего оказывают избирательное действие на пораженные органы. Это связано с тем, что фосфониевая группа благодаря своему делокализованному положительному заряду и высокой гидрофобности позволяет конъюгированным с ней определенным образом как известным, так и новым лекарственным молекулам легко проникать не только через клеточные мембраны, но и преодолевать высокий мембранный потенциал митохондрий (J.ZIELONKA et al., Mitochondria-targeted triphenylphosphonium-based compounds: syntheses, mechanisms of action, and therapeutic and diagnostic applications, CHEMICAL REVIEWS, 2017, V.117, N.15, pp.10043-10120). Распределение зарядов обеспечивает больше возможностей для соединения ориентироваться в структуре мишеней, за счет чего достигается эффективность лекарственного средства. Поэтому разработка соединений и их форм с делокализованными или разделенными зарядами имеет большие перспективы.
Отдельно следует отметить цвиттер-ионные формы вещества, поскольку их преимущества с точки зрения фармакологии могут быть достаточно значительными. Такие соединения обладают высоким дипольным моментом и очень хорошо растворяются в полярных растворителях, что может привести к повышенной биодоступности и ускорению наступления терапевтического эффекта, а также возможности внедрения новых путей доставки лекарственного средства, например, трансбуккального, сублингвального, ректального, ингаляционного или с использованием трансдермальных терапевтических систем.
Технические результаты, на достижение которых направлено настоящее изобретение заключаются в:
- увеличении растворимости 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты;
- ускорении наступления терапевтического эффекта 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты;
- сохранении высокой эффективности 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты;
- повышении долгосрочной стабильности твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты (в течение 20 лет);
- улучшении прессуемости с сохранением хороших показателей сыпучести без заметных электростатических явлений фармацевтической композиции и лекарственной формы, содержащих твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты;
- эффективном жаропонижающем действии;
- расширении арсенала лекарственных средств для лечения и/или профилактики ринитов, фарингитов;
- возможность получения стабильной ингаляционной композиции без добавления традиционных для уровня техники носителей с нереспирабельным размером частиц;
- расширении арсенала противовирусных средств;
- качественном и/или количественном изменении некоторых типов биологической активности, включая антиоксидантную, сахаропонижающую, гиполипидемическую, антигипоксическую активности, а также виды биологической активности, указанные в RU2141483C1.
Технические результаты относятся как к твердым формам 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, так и содержащим их фармацевтическим композициям и лекарственным средствам.
Новые формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты
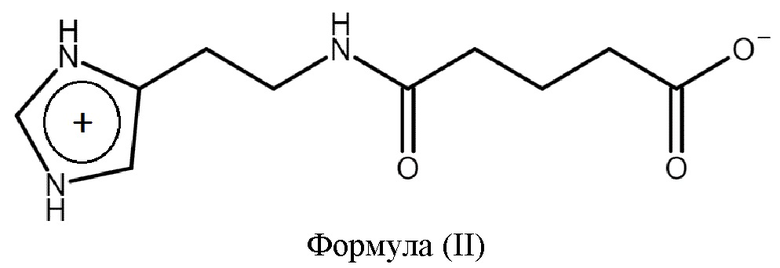
Указанная проблема решается, а заявленные технические результаты достигаются благодаря новым твердым формам 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты. Было неожиданно обнаружено, что в указанных формах 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты содержится цвиттер-ион формулы (II)
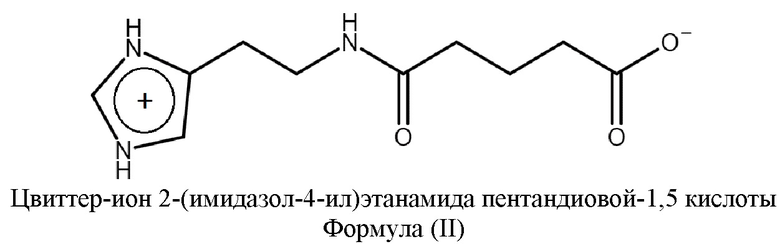
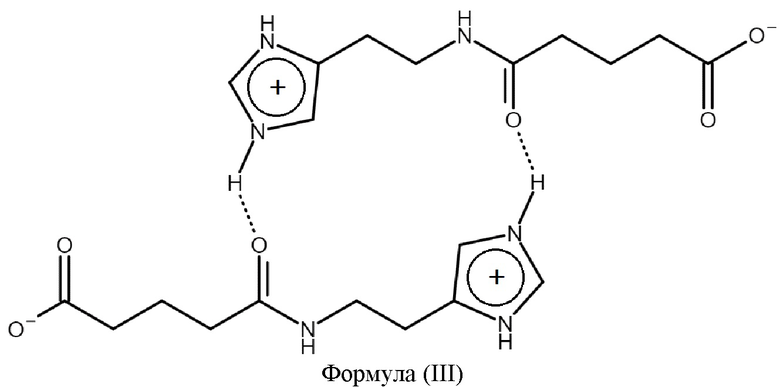
или его димер формулы (III)
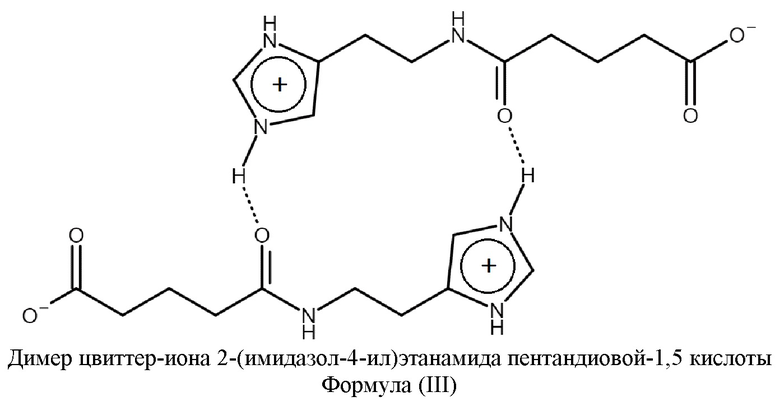
Под цвиттер-ионом понимают нейтральные молекулы, в которых есть пространственно разделенные и противоположные по знаку заряды. В цвиттер-ионе 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты формулы (II) карбоксильная группа заряжена отрицательно (карбоксилат-ион), а имидазольная группа - положительно.
Цвиттер-ионное строение было исследовано методами твердотельного ЯМР 13С и РСА и полностью подтверждается материалами настоящей заявки.
Понятие «новые твердые формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты» означает формы, содержащие 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты в виде цвиттер-иона формулы (II) или димера цвиттер-иона формулы (III).
Понятие твердая форма относится к кристаллическим и аморфным твердым формам.
В одном из вариантов твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты содержит димер формулы (III) и относятся к кристаллической форме, характеризующейся моноклинной сингонией кристаллической решетки и величинами ребер кристаллической ячейки (в ангстрем, Å): 8.71±0.50 Å, 20.01±0.50 Å и 12.16±0.50 Å и величиной угла (в град) 93.10 ± 5.00o. В более предпочтительном варианте твердая форма имеет слоистую структуру, в пределах каждого слоя димеры цвиттер-ионов 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты связаны между собой водородными связями. Дополнительно кристаллическая ячейка и кристаллическая решетка твердой формы могут быть охарактеризованы данными Фиг.1-3.
В другом варианте твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты содержит цвиттер-ион формулы (II) и относится к кристаллической форме, характеризующейся моноклинной сингонией кристаллической решетки и величинами ребер кристаллической ячейки (в ангстрем, Å): 5.39±0.50, 10.08±0.50 и 19.85±0.50 и величиной угла (в град) 100.26 ± 5.00°. В более предпочтительном варианте в полученной форме молекулы цвиттер-ионов 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты связаны между собой водородными связями таким образом, что расположены приблизительно перпендикулярно (если провести через молекулы условные плоскости), примерно под углом 90° (от 80 до 100°) друг относительно друга. Дополнительно кристаллическая ячейка и кристаллическая решетка твердой формы могут быть охарактеризованы данными Фиг.4-6.
Кристаллическая ячейка представляет собой условный параллелепипед, построенный на узлах кристаллической решетки, параллельные переносы (трансляции) которого в трех измерениях позволяют построить всю кристаллическую решетку. Параметрами кристаллической решетки являются величины ребер (a, b и c) и величины углов между ними (α, β и γ). В моноклинной сингонии кристаллической решетки каждая кристаллическая ячейка характеризуется тремя разными ребрами (a, b и c), одним углом, отличным от прямого, и двумя прямыми углами.
Настоящее изобретение также относится к твердым формам, включающим все возможные мезомеры цвиттер-иона формулы (II) и димера цвиттер-иона формулы (III), включая:
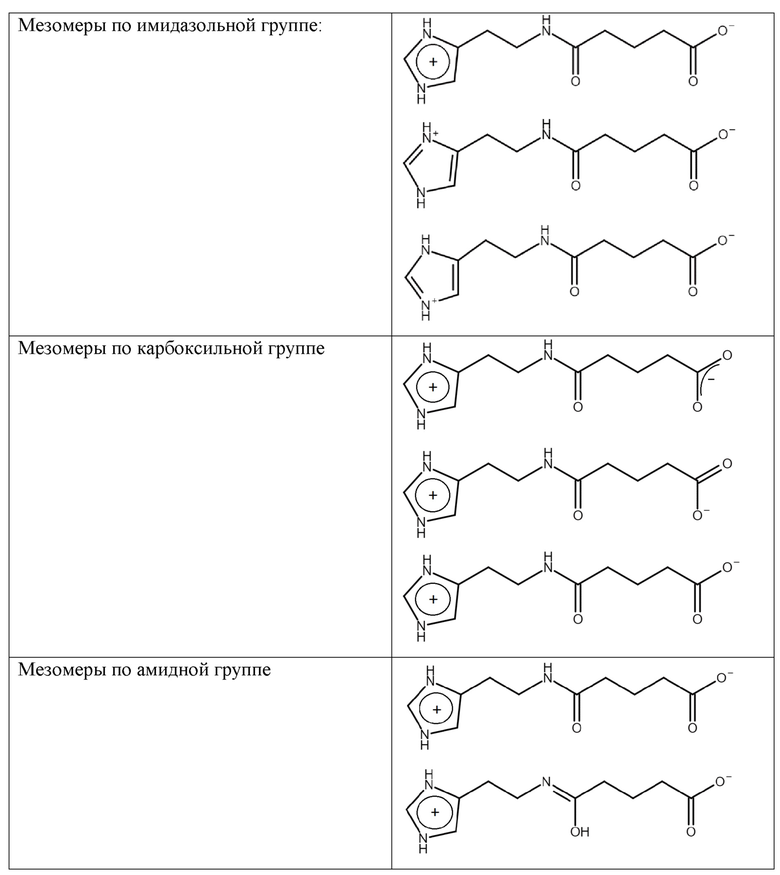
Специалисту в данной области будет понятно, что все мезомеры соединения формулы (II) и формулы (III), полученные по известным правилам химии, также относятся к указанным структурам.
Под мезомером (мезомерной структурой) понимают структуру в теории химического резонанса, возникающую из-за сопряжения кратных связей и/или неподеленных электронных пар в молекуле. В структуре формулы (II) мезомерный эффект возможен у имидазольной, карбоксильной и амидной групп.
Учитывая мезомерный эффект альтернативными обозначениями 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты согласно настоящему изобретению являются:
Имидазолилэтанамид пентандиовой кислоты;
2-(Имидазол-5-ил)этанамида пентандиовой-1,5 кислоты;
5-[2-(1H-Имидазол-4-ил)этиламино]-5-оксопентановая кислота;
5-[2-(1H-Имидазол-5-ил)этиламино]-5-оксопентановая кислота;
4-{[2-(1H-Имидазол-4-ил)этил]карбамоил}бутановая кислота;
4-{[2-(1H-Имидазол-5-ил)этил]карбамоил}бутановая кислота;
Способ получения новых форм 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты
В качестве исходных веществ для получения твердых форм 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты могут быть использованы глутаровый ангидрид и гистамин или соль гистамина. Способ получения твердых форм включает следующие стадии:
Стадия 1 (необязательная стадия). Взаимодействие дигидрохлорида гистамина или другой соли гистамина с основанием с образованием гистамина в форме свободного амина;
Стадия 2. Взаимодействие гистамина с глутаровым ангидридом;
Стадия 3. Обработка полученного на стадии 2 продукта минеральной кислотой;
Стадия 4. Подщелачивание полученного продукта (или добавление основания) до завершения выпадения осадка твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащую 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты в виде цвиттер-иона;
Стадия 5 (необязательная стадия). Очистка твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты известными методами.
Стадии 1-4 могут быть выполнены в одном реакторе (реакционной колбе) или в разных реакторах (реакционных колбах) с промежуточным выделением продуктов после каждой стадии.
Схема синтеза:
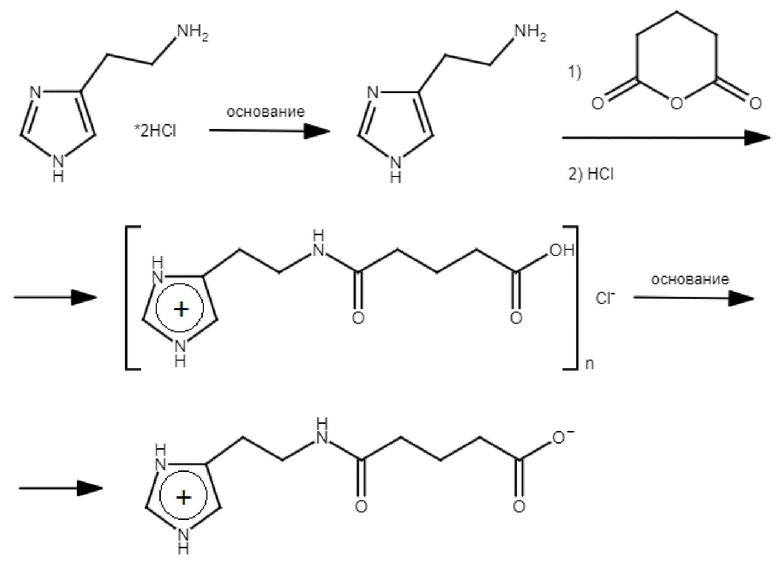
Далее приведено подробное описание каждой стадии.
Стадия 1. Взаимодействие дигидрохлорида гистамина с основанием
Реакцию дигидрохлорида гистамина с основанием проводят для получения гистамина в виде свободного основания.
Готовят раствор дигидрохлорида гистамина в любом подходящем растворителе. Подходящий растворитель может быть выбран из спирта, эфира, галогеналкана, ароматического углеводорода или нитроалкана. Примерами спирта являются метиловый спирт (метанол), этиловый спирт (этанол) и изопропиловый спирт (изопропанол). Примерами эфиров являются диэтиловый эфир (этоксиэтан), тетрагидрофуран (ТГФ), диоксан. Примерами галогеналканов являются хлороформ, хлористый метилен. Примерами ароматических углеводородов являются бензол, толуол и ксилолы. Примерами нитроалканов являются нитрометан и нитроэтан. В предпочтительном варианте количество растворителя выбирают таким образом, чтобы обеспечить полное растворение дигидрохлорида гистамина. Концентрация соединения может составлять от 0.01 моль/л (ммоль/мл) до 0.5 моль/л (ммоль/мл), например, 0.01 моль/л, 0.05 моль/л, 0.1 моль/л, 0.2 моль/л, 0.25 моль/л, 0.3 моль/л, 0.4 моль/л и 0.5 моль/л.
После растворения дигидрохлорида гистамина к раствору добавляют подходящее основание. В качестве подходящего основание могут быть выбраны, например, гидроксид натрия или гидроксид калия. Также могут быть применены сильные амины, например, триэтиламин.
После завершения реакции нейтрализации полученный амин может быть выделен известными методами, например, экстракцией с последующей отгонкой растворителей. Гистамин в виде свободного основания может без выделения введен в следующую стадию. Кроме того, стадия 1 может быть проведена совместно со стадией 2. Для этого стадию 2 проводят в присутствии подходящего основания, например, в присутствии пиридина, триэтиламина, морфолина.
Если в качестве исходного соединения используется гистамин в виде свободного основания, то стадию 1 проводить необязательно.
Стадия 2. Взаимодействие гистамина с глутаровым ангидридом
Для проведения реакции готовят раствор гистамина в любом подходящем растворителе. Подходящий растворитель может быть выбран из спирта, эфира, галогеналкана, ароматического углеводорода или нитроалкана. Примерами спирта являются метиловый спирт (метанол), этиловый спирт (этанол) и изопропиловый спирт (изопропанол). Примерами эфиров являются диэтиловый эфир (этоксиэтан), тетрагидрофуран (ТГФ), диоксан. Примерами галогеналканов являются хлороформ, хлористый метилен. Примерами ароматических углеводородов являются бензол, толуол и ксилолы. Примерами нитроалканов являются нитрометан и нитроэтан. В предпочтительном варианте количество растворителя выбирают таким образом, чтобы обеспечить полное растворение гистамина. Концентрация гистамина может составлять от 0.01 моль/л (ммоль/мл) до 0.5 моль/л (ммоль/мл), например, 0.01 моль/л, 0.05 моль/л, 0.1 моль/л, 0.2 моль/л, 0.25 моль/л, 0.3 моль/л, 0.4 моль/л и 0.5 моль/л.
После растворения гистамина к раствору добавляют глутаровый ангидрид. Глутаровый ангидрид берут в эквимолярном или избыточном количестве. Глутаровый ангидрид может быть добавлен в виде белого твердого вещества без растворителя или в виде раствора в подходящем растворителе, например, в том же растворителе, который был выбран для растворения гистамина.
В предпочтительном варианте реакцию проводят при комнатной температуре и при перемешивании. Если реакция протекает медленно, смесь может быть нагрета до 30-50°C или выше. Максимальная температура определяется точкой кипения растворителя. Если реакция протекает слишком бурно, смесь может быть охлаждена до 5-15°C.
Время реакции определяется количествами взятых гистамина и глутарового ангидрида и может составлять от 0.1 часа до 24 часов, в предпочтительном варианте от 1 до 6 часов, в еще более предпочтительном варианте от 2 до 3 часов. Момент завершения реакции может быть определен, например, методом тонкослойной хроматографии по исчезновению пятна гистамина. Также момент завершения реакции может быть определен по прекращению образования осадка продукта.
Продукт реакции из реакционной смеси может быть выделен известными методами, например, фильтрованием. Продукт также может быть введен в следующую стадию без промежуточного выделения.
Стадия 3. Обработка осадка минеральной кислотой
Полученный на стадии 2 осадок обрабатывают водным раствором минеральной кислоты. В качестве такой кислоты может быть выбрана соляная, серная, фосфорная, хлороводородная, азотная и другие сильные кислоты, в предпочтительном варианте кислота представляет собой соляную кислоту.
Количество кислоты определяют исходя из количества растворяемого осадка. Для более полного растворения может быть взят небольшой избыток кислоты (10-30% от количества осадка).
Допустимая концентрация кислоты составляет от 0.01 М (моль/л) до 5.00 М (моль/л), в более предпочтительном варианте от 0.1 М до 0.2 М. Момент завершения реакции может быть определен визуально по завершению растворения осадка.
Стадия 4. Подщелачивание полученного продукта
В полученный на стадии 3 раствор добавляют подходящее основание. При этом наблюдается помутнение раствора и/или выпадение осадка в виде кристаллов 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащей цвиттер-ион формулы (II) или его димер формулы (III). Подходящим основанием может быть щелочь (NaOH, KOH), сода (Na2CO3*10H2O, Na2CO3, K2CO3, NaHCO3), амин (триэтиламин, диэтиламин, морфолин, пиридин и т.д.).
Для ускорения выпадения кристаллов к раствору может быть добавлен вспомогательный растворитель, например, этанол или метанол.
Реакцию проводят при комнатной температуре или при охлаждении до 5-15°C. Рекомендуется контроль pH реакционной смеси. Момент завершения реакции может быть определен по значению pH 5.0-6.5 реакционной смеси, в предпочтительном варианте pH составляет 5.2-6.2. В другом варианте реакцию завершают после прекращения выпадения кристаллов.
Полученные кристаллы выделяют известными методами, например, отфильтровывают.
Стадия 5. Очистка продукта
Осадок 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты может быть дополнительно очищен известными методами. Например, осадок может быть промыт органическими растворителями (гексан, эфир), после чего дополнительно высушен.
Фармацевтическая композиция
Под фармацевтической композицией понимается пригодная для использования для людей или животных композиция (смесь, состав и т.д.), включающая активную фармацевтическую субстанцию. Активная фармацевтическая субстанция в фармацевтической композиции включает действующее вещество - твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения или смесь твердых форм 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения.
Смесь твердых форм 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения, в свою очередь, содержит твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащую цвиттер-ион формулы (II)
и твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащую димер цвиттер-иона формулы (III)
Соотношение указанных твердых форм может быть выбрано в диапазоне (по массе) от 1 : 10 до 10 : 1, предпочтительно от 5 : 1 до 1 : 5, более предпочтительно от 2 : 1 до 1 : 2, например, 1 : 1.
Активная фармацевтическая субстанция может применяться для лечения и/или профилактики заболеваний, вызванных вирусными инфекциями.
Настоящая техническая проблема решается, а указанные технические результаты достигаются благодаря фармацевтической композиции для лечения и/или профилактики заболеваний, вызванных вирусными инфекциями, содержащей определенную выше активную фармацевтическую субстанцию, а именно твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения или смесь твердых форм 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения и по меньшей мере один фармацевтически приемлемый эксципиент.
Специалисту в данной области будет понятно, что к фармацевтической композиции настоящего изобретения будут относиться также композиции, содержащие одно или несколько других активных фармацевтических субстанций, например, другие противовирусные фармацевтические субстанции.
Понятие «включает» и «содержит» в контексте настоящего изобретения означает, что указанные фармацевтические композиции (лекарственные средства, группы компонентов и т.д.) включают перечисленные далее компоненты/ингредиенты, но не исключают содержание других компонентов/ингредиентов.
В предпочтительном варианте фармацевтическая композиция представляет собой состав в виде твердой формы. Примерами твердых лекарственных форм являются порошки, гранулы, брикеты, капсулы, таблетки, драже и т.д. Специалисту в данной области будет понятно, что фармацевтическая композиция настоящего изобретения может иметь любую другую форму, обеспечивающую сохранность положительных свойств активной фармацевтической субстанции. В наиболее предпочтительном варианте твердая форма представляет собой порошок, гранулу, капсулу или таблетку. Порошком является твердая недозированная лекарственная форма, состоящая из твердых отдельных сухих частиц различной дисперсности, обладающая свойством сыпучести. Капсулой является твердая дозированная или недозированная лекарственная форма, включающая твердую (как правило, желатиновую) оболочку, внутри которой заключен инкапсулят, содержащий одно или более действующих веществ с добавлением или без вспомогательных веществ. Гранулой является твердая дозированная лекарственная форма в виде крупинок (агрегатов частиц порошка) круглой, цилиндрической или неправильной формы, содержащая одно или несколько действующих веществ с добавлением вспомогательных веществ. Таблеткой является твердая дозированная лекарственная форма, чаще всего получаемая прессованием порошков или гранул, содержащих одно или более действующих веществ с добавлением или без вспомогательных веществ.
Количественное содержание твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты в фармацевтической композиции выбирается из диапазона от 0.01 до 99.99 мас.%, в предпочтительном варианте от 1.00 до 80.00 мас.%, в более предпочтительном от 10.00 до 60.00 мас.%, например, 5.00 мас.%, 10.00 мас.%, 15.00 мас.%, 20.00 мас.%, 25.00 мас.%, 30.00 мас.%, 35.00 мас.%, 40.00 мас.%, 45.00 мас.%, 50.00 мас.%, 55.00 мас.%, 60.00 мас.%, от 10.00 мас.% до 20.00 мас.%; от 20.00 мас.% до 30.00 мас.%; от 30.00 мас.% до 40.00 мас.%; от 40.00 мас.% до 50.00 мас.%; от 50.00 мас.% до 60.00 мас.%, включая все промежуточные значения с шагом в 1.00 мас.%. Например, значение 23.00 мас.% входит в качестве одного из значений в диапазон от 20.00 мас.% до 30.00 мас.%.
В другом предпочтительном варианте фармацевтическая композиция включает твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения в эффективном количестве.
Понятие «эффективное количество» в контексте настоящего изобретения относится к количеству фармацевтической композиции или лекарственного средства, которое при введении субъекту является достаточным для воздействия такого лечения на заболевание, нарушение или симптом. «Эффективное количество» может изменяться, например, в зависимости от того, в какой форме находится вещество, от природы заболевания, нарушения и/или симптомов заболевания или нарушения, от тяжести заболевания, нарушения и/или симптомов заболевания или нарушения, от возраста субъекта, подлежащего лечению, и/или от веса субъекта, подлежащего лечению. Надлежащее количество в каждом конкретном случае будет очевидно специалисту в данной области или может быть определено путем стандартных экспериментов.
В предпочтительном варианте твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты содержится в фармацевтической композиции или лекарственном средстве и используется в определенной дозировке. Дозировка твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты согласно настоящему изобретению, может находиться в диапазоне от 1 мг до 1000 мг в сутки, предпочтительно от 20 мг до 100 мг, наиболее предпочтительно от 30 мг до 90 мг в сутки. Указанная дозировка может быть введена как одной дозой, так и разделена на несколько приемов в течение суток, например, 2, 3 или 4 раза в сутки.
Понятие «дозировка», используемое здесь, характеризует содержание одного или нескольких действующих веществ в количественном выражении на единицу дозы, или единицу объема, или единицу массы в соответствии с лекарственной формой, либо для некоторых видов лекарственных форм количество высвобождаемого из лекарственной формы действующего вещества за единицу времени.
Фармацевтическая композиция настоящего изобретения включает по меньшей мере один фармацевтически приемлемый эксципиент, являющийся носителем действующих веществ, обеспечивающий требуемый объем/массу и необходимые характеристики лекарственного средства в определенной лекарственной форме. В предпочтительном варианте фармацевтическая композиция включает фармацевтически приемлемый эксципиент, который выбирают из группы, включающей наполнитель, связывающее вещество, смазывающее вещество, разрыхляющее вещество, скользящее вещество, консервант, корригент и краситель.
Термин «наполнитель» или «разбавитель» означает вспомогательные вещества, используемые для придания твердым лекарственным формам заданного объема или массы. В качестве наполнителей могут быть использованы крахмал, глюкоза, сахароза, лактоза (молочный сахар), магния карбонат основной, магния окись, натрия хлорид, натрия гидрокарбонат, глина белая (каолин), желатин, целлюлоза микрокристаллическая (МЦК), метилцеллюлоза (МЦ), натриевая соль карбоксиметилцеллюлозы (Na КМЦ), кальция карбонат, кальция фосфат двузамещенный, глицин (аминоуксусная кислота), декстрин, амилопектин, ультраамилопектин, сорбит, маннит, пектин и др. Группа не исчерпывается данным списком.
Термин «связывающие» означает вещества, входящие в состав таблетируемой массы для придания ей необходимой вязкости. В качестве связывающих веществ используются вода, спирт этиловый, крахмальный клейстер, сахарный сироп, растворы: карбоксиметилцеллюлозы (КМЦ), оксиэтилцеллюлозы (ОЭЦ), оксипропилметилцеллюлозы (ОПМЦ); поливиниловый спирт (ПВС), поливинилпирролидон (ПВП), альгиновая кислота, натрия альгинат, желатин и др. Группа не исчерпывается данным списком.
Термин «скользящее вещество» означает вспомогательные вещества, используемые в технологическом процессе производства таблеток на стадии прессования для улучшения текучести гранул или порошка за счет уменьшения трения между частицами. Скользящее вещество может быть представлено одним или несколькими из числа крахмала, талька, полиэтиленоксида-4000, стеариновой кислоты, кальция и магния стеарата и др. Группа не исчерпывается данным списком.
Термин «смазывающее вещество» или «лубрикант» означает вспомогательные вещества, способствующие уменьшению силы трения между поверхностью таблетки и стенками кюветы пуансона, в которой таблетка формируется, используемые в технологическом процессе производства таблеток на стадии прессования. Смазывающее вещество может быть представлено одним или несколькими из числа стеарата магния, стеарата кальция, стеарил фумарата натрия, полиэтиленгликоля (с молекулярной массой свыше 3350), лаурилсульфата натрия, талька, минерального масла, лейцина и полоксамера и др. Группа не исчерпывается данным списком.
Термин «разрыхлитель» означает вещества, использующиеся для улучшения распадаемости или растворения, обеспечивая механическое разрушение таблеток в жидкой среде, что необходимо для скорейшего высвобождения действующего вещества. Разрыхлитель может быть представлен одним или несколькими из числа микрокристаллической целлюлозы, кроскармеллозы натрия, кросповидона, натриевой соли гликолята крахмала, крахмала, пектина, желатина, амилопектина, ультраамилопектина, агар-агар, альгиновой кислоты, калия и натрия альгината, твин-80 и др. Группа не исчерпывается данным списком.
Дополнительные компоненты, корригенты, используются для улучшения вкуса (подсластитель) и запаха (ароматизатор). К ним относятся, например, сахар, какао, ванилин. Красители (пигменты) используются для улучшения внешнего вида фармацевтической композиции и лекарственной формы. Примерами красителей являются диоксид титана, индигокармин.
Количество, состав и форма фармацевтически приемлемого эксципиента могут быть выбраны специалистом в данной области произвольно при условии полного или частичного сохранения цвиттер-иона 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты формулы (II) или его димера формулы (III).
В предпочтительном варианте фармацевтическая композиция согласно настоящему изобретению содержит
твердую форму 2-(имидазол-4-ил)этанамида настоящего изобретения в качестве активного вещества и
маннит (E421), сукралозу - в качестве вспомогательных веществ.
В еще более предпочтительном варианте фармацевтическая композиция согласно настоящему изобретению содержит
твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения в количестве 0.09 г;
смесь маннита (E421), сукралозы, ароматизатора лимон лайм - до 3.0 г.
Пути введения фармацевтической композиции по настоящему изобретению включают, но не ограничиваются пероральным, ингаляционным, местным, трансдермальным, сублингвальным и ректальным путями. В предпочтительном варианте фармацевтическую композицию вводят перорально или сублингвально.
В некоторых вариантах осуществления фармацевтическую композицию согласно настоящему изобретению можно получить с помощью известных общепринятых способов в области фармацевтики.
Лекарственное средство
Настоящая техническая проблема решается, а указанные технические результаты достигаются также благодаря лекарственному средству для лечения и/или профилактики заболеваний, вызванных вирусными инфекциями, содержащему твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения или фармацевтическую композицию настоящего изобретения.
Под лекарственным средством (лекарственным препаратом) понимается пригодная для использования у людей или животных фармацевтическая композиция в виде лекарственной формы.
В предпочтительном варианте настоящее изобретение относится к лекарственному средству в твердой лекарственной форме. Лекарственные формы по настоящему изобретению включают, но не ограничиваются указанным, таблетки, в частности, буккальные таблетки, шипучие таблетки, таблетки, покрытые оболочкой, таблетки с замедленным высвобождением, обычные таблетки, таблетки с контролируемым высвобождением, диспергируемые в полости рта таблетки, лиофилизированные быстрорастворимые таблетки и т.п.; капсулы, такие как твердые капсулы, мягкие капсулы, желатиновые капсулы и т.п.; порошки для инъекций, такие как лиофилизированные порошки для инъекций, обычные порошки для инъекций и т.п.; растворы, аэрозоли, спреи, трансдермальные лекарственные средства, например, пластыри, гранулы, суппозитории и другие лекарственные формы.
Специалисту в данной области будет понятно, что лекарственное средство настоящего изобретения может иметь любую форму, обеспечивающую сохранность положительных свойств активной фармацевтической субстанции. В наиболее предпочтительном варианте твердая форма представляет собой порошок, гранулу, капсулу или таблетку.
В предпочтительном варианте лекарственное средство согласно настоящему изобретению содержит
твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения в качестве активного вещества и
маннит (E421), сукралозу - в качестве вспомогательных веществ;
и представляет собой порошок.
В еще более предпочтительном варианте лекарственное средство согласно настоящему изобретению содержит
твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения в количестве 0.09 г;
смесь маннита (E421), сукралозы, ароматизатора лимон лайм - до 3.0 г состава;
и представляет собой порошок.
В качестве лекарственного средства настоящего изобретения может выступать активная фармацевтическая субстанция и фармацевтическая композиция, содержащие твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения. В предпочтительном варианте лекарственное средство также включает по меньшей мере один фармацевтически приемлемый эксципиент, однако его наличие не является обязательным.
Количественное содержание твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты в лекарственном средстве выбирается из диапазона от 0.01 до 99.99 мас.%, в предпочтительном варианте от 1.00 до 80.00 мас.%, в более предпочтительном от 10.00 до 60.00 мас.%, например, 5.00 мас.%, 10.00 мас.%, 15.00 мас.%, 20.00 мас.%, 25.00 мас.%, 30.00 мас.%, 35.00 мас.%, 40.00 мас.%, 45.00 мас.%, 50.00 мас.%, 55.00 мас.%, 60.00 мас.%, от 10.00 мас.% до 20.00 мас.%; от 20.00 мас.% до 30.00 мас.%; от 30.00 мас.% до 40.00 мас.%; от 40.00 мас.% до 50.00 мас.%; от 50.00 мас.% до 60.00 мас.%. Указанные диапазоны содержания означают, что твердая форма по изобретению может содержать каждое из указанных значений в рамках заявленного диапазона, включая крайние точки. Например, содержание от 30 до 60 мас.% включает каждое значение в интервале от 30 до 60 мас.% с шагом 0,01 мас. %, например, 43.21 мас.%.
Лекарственные средства по настоящему изобретению могут вводиться (не ограничиваясь указанным) перорально, парентерально, ингаляционно, подкожно, внутрибрюшинно, местно, ректально. Терапевтическая дозировка лекарственного средства, содержащего твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты , или фармацевтическую композицию по настоящему изобретению, или фармацевтическую композицию для лечения заболеваний, вызванных вирусными инфекциями, которая содержит в терапевтически эффективном количестве твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты по настоящему изобретению, у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента.
Ингаляционная композиция
Авторы настоящего изобретения неожиданно обнаружили, что твердые формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения пригодны для создания лекарственного средства в форме сухого порошка для ингалятора (ингаляционной композиция) без добавления каких-либо вспомогательных эксципиентов.
Наиболее распространенным носителем для создания ингаляционных композиций является лактоза, например, альфа-лактоза моногидрат или безводная бета-лактоза. Лактоза как носитель улучшает заполнение, дозирование и подачу лекарства из ингалятора. Чтобы проникать в легкие, размер частиц активной фармацевтической субстанции должен быть в диапазоне 1-10 мкм. Для достижения такого малого аэродинамического размера частиц активное вещество обрабатывают путем высушивания или микронизации. Тем не менее, микронизированные частицы часто формируют слипающийся порошок, который плохо дозируется. Смешивание с лактозой позволяет искусственно разрушить агломераты активного вещества и улучшить его использование. Предполагается, что на выходе из ингалятора частицы препарата и частицы лактозы должны разделиться (дезагрегация). Крупные частицы лактозы нереспирабельны и оседают в полости рта, а существенно более мелкие частицы препарата под воздействием воздушного потока перемещаются в дыхательные пути (В.В.Архипов и Н.Б.ЛАЗАРЕВА, Принципы адекватного выполнения ингаляции, ПРАКТИЧЕСКАЯ ПУЛЬМОНОЛОГИЯ, 2018, 3, c.66-74). Такой подход был реализован в патенте EA016363B1, где предложена ингаляционная композиция, содержащая 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты и биологически инертный носитель на примере лактозы.
Отличительными преимуществами ингаляционной композиции настоящего изобретения являются стабильность, минимизация электростатических взаимодействий и слеживания, сохранение распределения по размерам частиц в процессе хранения, отсутствие традиционных для уровня техники носителей с нереспирабельным размером частиц.
Ингаляционная композиция настоящего изобретения может применяться не только для лечения и/или профилактики заболеваний, вызванных вирусными инфекциями, но и для лечения и/профилактики ХОБЛ, астмы и хронического бронхита.
Применение твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты и содержащих ее фармацевтической композиции и лекарственного средства
Каждая твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения, содержащие ее фармацевтическая композиция и лекарственное средство настоящего изобретения могут применяться для лечения и/или профилактики заболеваний, вызванных вирусными инфекциями. В предпочтительном варианте к вирусным инфекциям относятся риновирус, респираторно-синцитиальный вирус, вирус парагриппа, вирус гриппа, в том числе гриппа А, В, С и D, аденовирус, норавирус, метапневмовирус, коронавирус, хантавирус, бокавирус, вирус Коксаки, вирусы группы ЕСНО, энтеровирус, ротавирус, вирус герпеса. В еще более предпочтительном варианте вирусные инфекции относятся к вирусу гриппа типа А. В другом еще более предпочтительном варианте вирусные инфекции относятся к коронавирусу SARS-CoV-2. Вирусные инфекции могут относиться к ДНК и РНК-вирусам.
Каждая твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения, содержащие ее фармацевтическая композиция и лекарственное средство настоящего изобретения могут применяться для лечения и/или профилактики ринита, фарингита и синута (риносинусита).
Каждая твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения, содержащие ее фармацевтическая композиция и лекарственное средство настоящего изобретения могут применяться в качестве эффективных жаропонижающих средств. Жаропонижающее действие может проявляться в снижении температуры тела при лихорадке.
Каждая твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты и содержащая ее фармацевтическая композиция настоящего изобретения могут применяться для изготовления лекарственного средства настоящего изобретения.
В одном из вариантов настоящего изобретения твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения в составе фармацевтической композиции или лекарственного средства по настоящему изобретению вводят в количестве от 1 мг до 1000 мг в сутки, предпочтительно от 20 мг до 100 мг, наиболее предпочтительно от 30 мг до 90 мг в сутки. Указанная дозировка может быть введена как одной дозой, так и разделена на несколько приемов в течение суток, например, 2, 3 или 4 раза в сутки. Наиболее предпочтительные варианты доз могут быть определены, исходя из возраста и/или массы тела пациента, а также из характера проявляемых симптомов.
Если не указано иное, все технические и специальные термины, использованные в данном контексте, имеют общепринятое в данной области техники значение.
Краткое описание чертежей
Фиг.1 - Димер цвиттер-иона 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты в твердой форме;
Фиг.2 - Строение кристаллической ячейки твердой формы, содержащей димер цвиттер-иона 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты;
Фиг.3 - Упаковка молекул в кристаллической решетке твердой формы, содержащей димер цвиттер-иона 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты;
Фиг.4 - Цвиттер-ион 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты в твердой форме;
Фиг.5 - Строение кристаллической ячейки твердой формы, содержащей цвиттер-ион 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты;
Фиг.6 - Упаковка молекул в кристаллической решетке твердой формы, содержащей димер цвиттер-ион 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты;
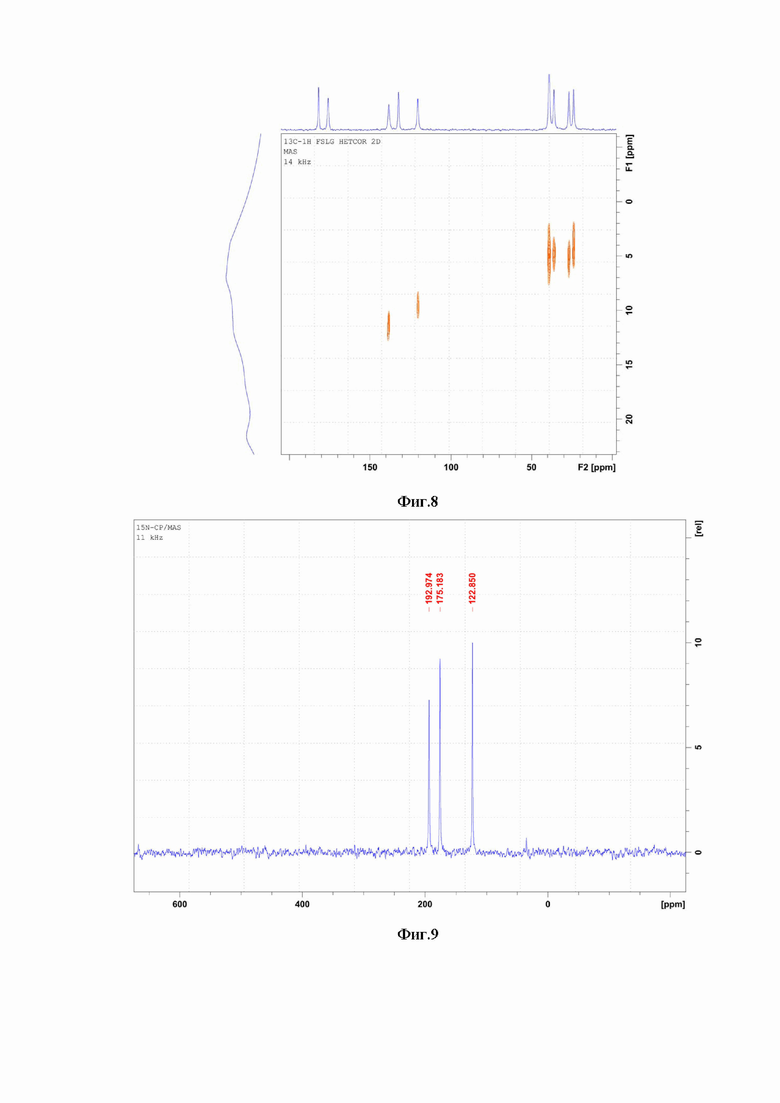
Фиг.7 - Общий вид спектра 13С-CP/MAS твердой формы настоящего изобретения;
Фиг.8 - Общий вид корреляции 13C - 1H HETCOR/MAS;
Фиг.9 - Общий вид спектра 15N-CP/MAS;
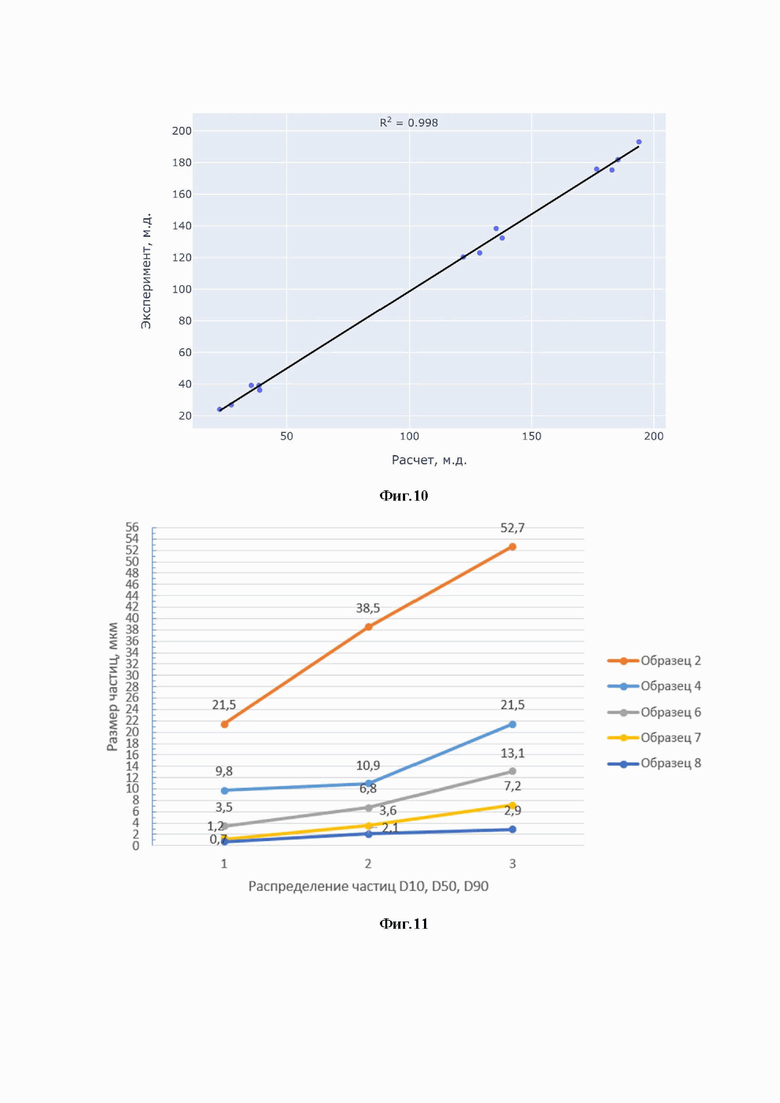
Фиг.10 - Корреляция расчетных и экспериментальных химических сдвигов 13С и 15N;
Фиг.11 - Сводные данные по распределению частиц в пробах в ингаляционной композиции;
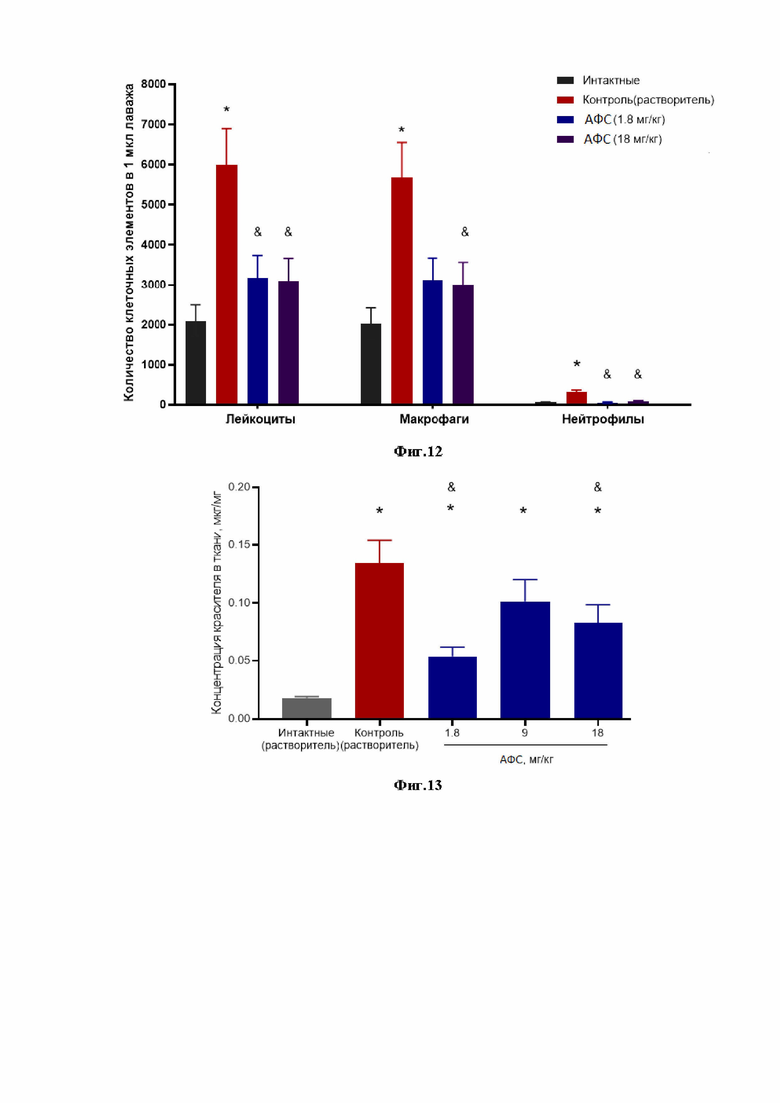
Фиг.12 - Исследование активности в модели острого риносинусита у крыс;
* - различия статистически значимы по сравнению с группой интактных (p <0.05, 1-way Anova тест);
& - различия статистически значимы по сравнению с группой контроля (растворитель) (p <0.05, 1-way Anova тест);
Фиг.13 - Исследование активности в модели неинфекционного фарингита у крыс;
* - различия статистически значимы по сравнению с группой интактных (p <0.05, 1-way Anova тест);
& - различия статистически значимы по сравнению с группой контроля (растворитель) (p <0.05, 1-way Anova тест);
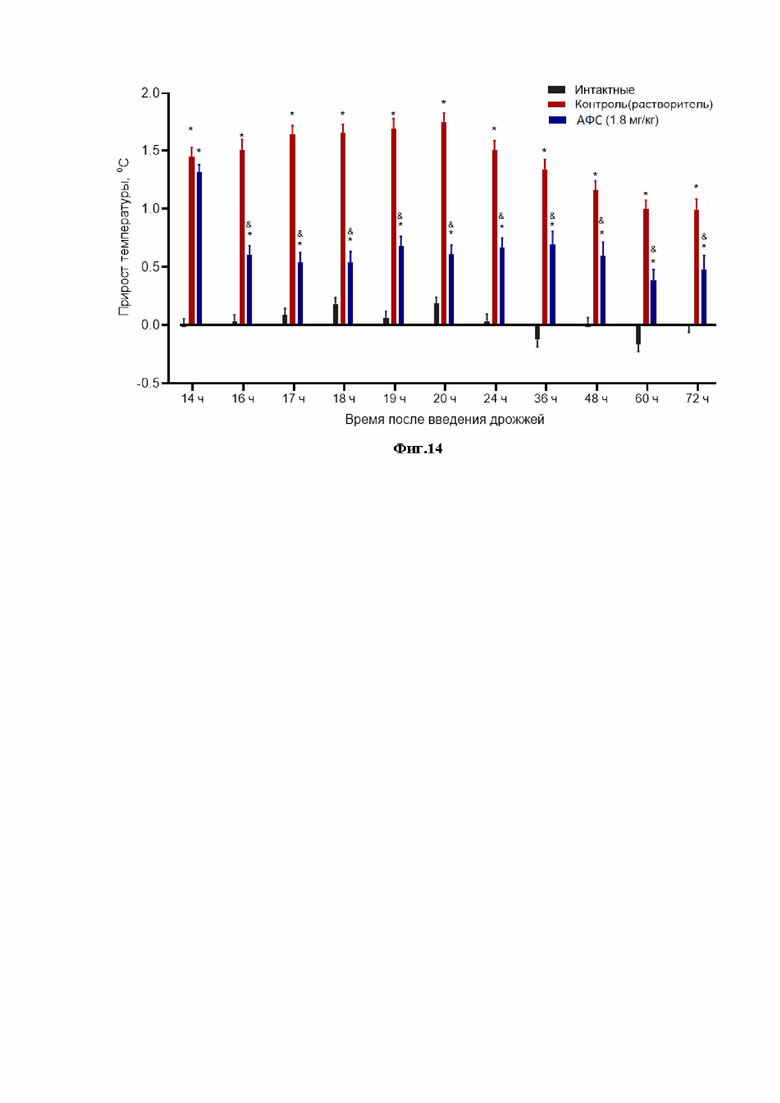
Фиг.14 - Исследование активности в модели лихорадочной реакции у крыс;
* - различия статистически значимы по сравнению с группой интактных (p <0.05, 1-way Anova тест);
& - различия статистически значимы по сравнению с группой контроля (растворитель) (p <0.05, 1-way Anova тест).
Осуществление изобретения
Настоящее изобретение дополнительно поясняется, но не ограничивается следующими примерами.
Пример 1. Получение твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты
К раствору 0.500 г (4.5 ммоль) гистамина в 10 мл тетрагидрофурана (ТГФ) добавляли по каплям при перемешивании раствора 0.670 г глутарового ангидрида в 10 мл ТГФ. Смесь перемешивали при комнатной температуре в течение 2 часов. Выпавший осадок отфильтровывали и растворяли в минимальном количестве 0.1 M соляной кислоты. Для нейтрализации полученного раствора к нему приливали 5-кратное количество этилового спирта (по объему), после чего к смеси медленно добавляли свежеперегнанный триэтиламин до значения pH 5.2-5.7. При достижении нужного значения pH продукт реакции начинал осаждаться в виде бесцветных кристаллов. Добавление основания прекращали после завершения выпадения осадка. Кристаллический осадок отфильтровывали и промывали от следов амина охлажденным до 5°C эфиром. Продукт сушили на воздухе. Получено: 0.640 г (63%) твердой формы, содержащей димер цвиттер-иона 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты.
Пример 2. Подтверждение цвиттер-ионного строения методами РСА
Рентгеноструктурное исследование провели на дифрактометре Bruker Quest. Экспериментальный набор отражений был получен с монокристалла при 100К и излучении MoKα (λ = 0.71073). Используя программное обеспечение Olex2 (O.V.DOLOMANOV et al., OLEX2: a complete structure solution, refinement and analysis program, JOURNAL OF APPLIED CRYSTALLOGRAPHY, 2009, V.42, N.2, pp.339-341), структура была решена с помощью комплекса программ SHELXL (G.M.Sheldrick, Crystal structure refinement with SHELXL, ACTA CRYSTALLOGRAPHICA SECTION C: STRUCTURAL CHEMISTRY, 2015, V.71, N.1, pp.3-8) и уточнена на основе метода наименьших квадратов. Рисунок расшифрованной молекулы представлен на Фиг.1.
Из полученных данных следует, что получена твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащая димер цвиттер-иона следующей формулы:
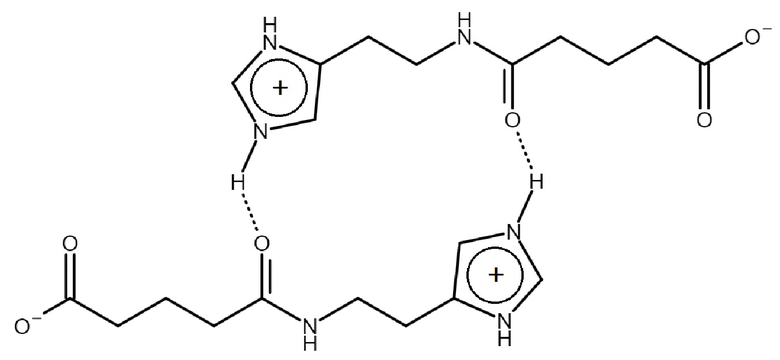
Кристаллографическая информация для ячейки C20H30N6O6 (M = 450.59 г/моль): моноклинная сингония, пространственная группа P21/c, a = 8.7166 Å, b = 20.0076 Å, c = 12.1681 Å, α = 90°, β = 93.101°, γ = 90°, V = 2118.99 Å3, Z = 4, T = 140 K.
Дополнительно было проанализировано взаимное расположения молекул в кристаллической ячейке и кристаллической решетке. Результаты представлены на Фиг.2 и Фиг.3 соответственно. Установлено, что полученная форма имеет слоистую структуру, в пределах каждого слоя димеры цвиттер-ионов 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты связаны между собой водородными связями. Водородные связи димеров между соседствующими слоями отсутствуют, можно четко выделить кристаллографические плоскости, разделяющие отдельные слои (см. Фиг.3).
Пример 3. Получение твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты
К раствору 0.500 г (4.5 ммоль) гистамина в 10 мл диоксана добавляли по каплям при перемешивании раствора 0.670 г глутарового ангидрида в 10 мл диоксана. Смесь перемешивали при комнатной температуре в течение 2 часов. Выпавший осадок отфильтровывали и растворяли в минимальном количестве 0.1 M соляной кислоты. Для нейтрализации полученного раствора к нему приливали 5-кратное количество этилового спирта (по объему), после чего к смеси медленно добавляли 10% раствор карбоната натрия до значения pH 6.0-6.5. При достижении нужного значения pH продукт реакции начинал осаждаться в виде бесцветных кристаллов. Добавление основания прекращали после завершения выпадения осадка. Кристаллический осадок отфильтровывали и промывали от следов амина охлажденным до 5°C гексаном. Продукт сушили на воздухе. Получено: 0.812 г (80%) цвиттер-иона 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты
Пример 4. Подтверждение цвиттер-ионного строения методами РСА и твердотельного ЯМР
Рентгеноструктурное исследование провели на дифрактометре Bruker Quest. Экспериментальный набор отражений был получен с монокристалла при 100К и излучении MoKα (λ = 0.71073). Используя программное обеспечение Olex2 (O.V.DOLOMANOV et al., OLEX2: a complete structure solution, refinement and analysis program, JOURNAL OF APPLIED CRYSTALLOGRAPHY, 2009, V.42, N.2, pp.339-341), структура была решена с помощью комплекса программ SHELXL (G.M.SHELDRICK, Crystal structure refinement with SHELXL, ACTA CRYSTALLOGRAPHICA SECTION C: STRUCTURAL CHEMISTRY, 2015, V.71, N.1, pp.3-8) и уточнена на основе метода наименьших квадратов. Рисунок расшифрованной молекулы представлен на Фиг.4.
Из полученных данных следует, что получена твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащая цвиттер-ион следующей формулы:
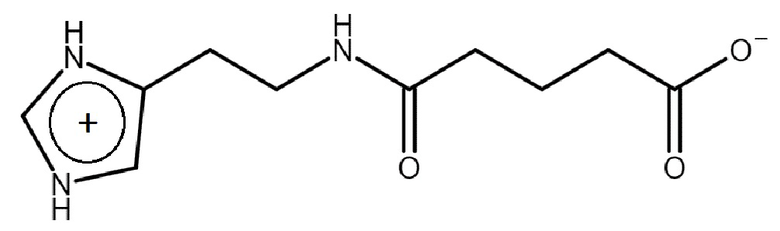
Кристаллографическая информация для C10H15N3O3 (M = 225.24 г/моль): моноклинная сингония, пространственная группа P21/c, a = 5.3967 Å, b = 10.0809 Å, c = 19.8540 Å, α = 90°, β = 100.258°, γ = 90°, V = 1062.88 Å3, Z = 4, T = 140 K.
Дополнительно было проанализировано взаимное расположения молекул в кристаллической ячейке и кристаллической решетке. Результаты представлены на Фиг.5 и Фиг.6 соответственно. В отдельной ячейке димеры цвиттер-ионов не просматривались. Кроме того, установлено, что в полученной форме молекулы цвиттер-ионов 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты связаны между собой водородными связями таким образом, что расположены примерно под углом 90° (80-100°) друг относительно друга (см. Фиг.6).
Для регистрации спектров твердотельного ЯМР использовали методику кросс-поляризации при вращении исследуемого образца под магическим углом (CP/MAS). Эксперименты по твердотельному ЯМР регистрировали на спектрометре Bruker 400 МГц. Образцы вращались с частотой от 11 до 14 кГц под магическим углом (MAS) с использованием роторов из ZrO2. Все спектры 13C и 15N регистрировались в условиях развязки от протонов
В твердотельном ЯМР 1H все сигналы были сильно уширены из-за особенностей эксперимента. Поэтому для облегчения отнесения сигналов ядер атомов водорода были применена методика HETCOR заключающаяся в получении корреляции химических сдвигов 1H и 13С.
В твердотельном ЯМР 13С наблюдали интенсивные пики при 179, 173, 135, 129, 117, 36, 33, 24 и 21 м.д. Кроме того, присутствовали относительно слабые пики при 258, 254, 252, 214, 208, 197, 98, 95, 93, 55 и 49 м.д., которые представляли собой полосы вращения основных изотропных пиков. Спектр представлен на Фиг.7. Спектр, зарегистрированный по методике HETCOR, представлен на Фиг.8. Аналогичные сигналы наблюдали и для твердой формы по примеру 2.
В твердотельном ЯМР 15N наблюдали интенсивные пики при 123, 175 и 193 м.д., а сам спектр представлен на Фиг.9. Расчетные химические сдвиги ядер 13C и 15N представлены в таблице 1. Общий вид молекулы и нумерация атомов приведены на Фиг.4.
Далее химические сдвиги максимумов рассчитали с помощью методов квантовой химии. В качестве стартовой точки для квантовохимического расчета была использована структура на Фиг.4, уточнённая с помощью данных порошковой дифракции. Для улучшения сходимости данных расчета и эксперимента координаты атомов были предварительно оптимизированы.
Для прямого расчета химических сдвигов атома азота и углерода использовалась программа VASP 5.4.1, метод GI-PAW (см. G.KRESSE and J.HAFNER, Ab initio molecular dynamics for liquid metals, PHYSICAL REVIEW B, 1993, V.47, N.1, p.558; G.KRESSE and J.HAFNER, Ab initio molecular-dynamics simulation of the liquid-metal-amorphous-semiconductor transition in germanium, Physical Review B, 1994, V.49, N.20, pp.14251-14269; G.KRESSE and J.FURTHMÜLLER, Efficient iterative schemes for ab initio total-energy calculations using a plane-wave basis set, PHYSICAL REVIEW B, 1996, V.54, N.16, p.11169; G.KRESSE and J.FURTHMÜLLER, Efficiency of ab-initio total energy calculations for metals and semiconductors using a plane-wave basis set, COMPUTATIONAL MATERIALS SCIENCE, 1996, V.6, N.1, pp.15-50; G.KRESSE and D.JOUBERT, From ultrasoft pseudopotentials to the projector augmented-wave method, PHYSICAL REVIEW B, 1999, V.59, N.3, p.1758). Для решения уравнений Кона-Шэма в этом случае использовалась сетка с 16 к-точками в независимой части зоны Бриллюэна. Порог сходимости в процедуре самосогласования при определении энергии был задан как 10-10 эВ. В качестве стандарта были использованы ромбическая модификация SiMe4 (см. A.K.WOLF et al. Predicted crystal structures of tetramethylsilane and tetramethylgermane and an experimental low-temperature structure of tetramethylsilane, ACTA CRYSTALLOGRAPHICA SECTION B: STRUCTURAL SCIENCE, 2010, V.66, N.2, pp.229-236) и кристаллическая структура аммиака (см. R.BOESE et al. Single-crystal structure and electron density distribution of ammonia at 160 k on the basis of X-ray diffraction data, THE JOURNAL OF PHYSICAL CHEMISTRY B, 1997, V.101, N.30, pp.5794-5799). Для обоих стандартов также были проведены квантово-химические расчеты с оптимизацией геометрии и вычислены тензоры магнитного экранирования атомных ядер.
Наиболее значимые отличия между расчетом и экспериментом наблюдаются для атомов N4 и N5. Прямое сравнение значений химических сдвигов позволяет сделать вывод, что квантвохимический расчет несколько переоценивает силу водородных связей N-H…O. По-видимому, упрочнение этих связей может привести к некоторому локальному переносу электронной плотности с группы N-H на карбонильный атом кислорода и сдвигу в сильное поле всех сигналов 15N.
Согласие между расчетом и экспериментов в случае химических сдвигов 13C заметно лучше. Наибольшее расхождение отмечено для атома С8 находящегося между атомами азота N5 и N6. Природа данного отклонения, по-видимому, такая же как в случае химических сдвигов 15N и обусловлена упрочнением водородных связей по результатам квантовохимического расчета по сравнению с экспериментом. Остальные химические сдвиги 13С воспроизведены в квантовохимическом расчете в пределах 3.0-3.5 м.д.
Сравнение расчетных и экспериментальных данных представлено на Фиг.10 и демонстрирует наличие линейной корреляции. Рассчитанные величины R2 и стандартной ошибки составляют 0.998 и 1.69 м.д. Доверительный интервал равен 5.76 м.д.
Измерение химических сдвигов 13C и 15N методом ЯМР и квантовохимический расчет этих параметров показали, что состав образца твердой формы в виде димера цвиттер-иона полностью соответствует структуре установленной при помощи метода порошковой рентгеновской дифракции.
Пример 5. Получение фармацевтической композиции и лекарственной формы в виде капсул
Для приготовления фармацевтической композиции и лекарственной формы использовали:
Композиция 1:
Композиция 2:
Лекарственную форму в виде твердых капсул получали путем взвешивания и просеивания веществ, их смешивания и капсулирования машинным способом.
Пример 6. Получение фармацевтической композиции и лекарственной формы в виде порошка
Для приготовления фармацевтической композиции и лекарственной формы использовали:
Композиция 3:
Композиция 4:
Лекарственную форму в виде порошка получали путем взвешивания и смешивания указанных ингредиентов.
Пример 7. Получение активной фармацевтической субстанции в виде порошка
К 100 мг твердой формы по примеру 1 добавляли 10 мг твердой формы по примеру 3. Полученную смесь тщательно перемешивали, взвешивали и помещали в бюкс с плотно закрывающейся крышкой. Получили 110 мг активной фармацевтической субстанции настоящего изобретения.
К 100 мг твердой формы по примеру 3 добавляли 10 мг твердой формы по примеру 1. Полученную смесь тщательно перемешивали, взвешивали и помещали в бюкс с плотно закрывающейся крышкой. Получили 110 мг активной фармацевтической субстанции настоящего изобретения.
К 50 мг твердой формы по примеру 1 добавляли 50 мг твердой формы по примеру 3. Полученную смесь тщательно перемешивали, взвешивали и помещали в бюкс с плотно закрывающейся крышкой. Получили 100 мг активной фармацевтической субстанции настоящего изобретения.
Пример 8. Получение ингаляционной лекарственной формы
Навески 200 мг твердой формы по примеру 1 (образец А), 200 мг твердой формы по примеру 3 (образец B) и формы, полученной согласно прототипу RU2141483 (образец С), гомогенизировали до респирабельного размера 2-3 мкм.
Был выбран тип измельчения с использованием шаровой мельницы. Данный тип мельниц использует принцип высокоэнергичных ударов мелющими шарами.
Среди оборудования в которых используется данный тип измельчения шаровые планетарные мельницы являются наиболее простыми и надежными, одновременно с этим они обеспечивают эффективный помол.
Размольные стаканы с измельчаемым материалом и шарами дополнительно поворачиваются на быстро вращающимся планетарном диске в противоположном направлении вокруг собственной оси. В таком положении центробежная сила с определённой скорости вызывает отделение измельчаемого материала и шаров от внутренней стенки размольного стакана. При этом мелющие шары пересекают стакан с максимальной скоростью и размалывают измельчаемый материал на противоположной стенке стакана как благодаря раздроблению, так и в следствии столкновению шаров друг с другом.
Для измельчения использовали планетарную шаровую мельницу Pulveresetta 6, Fritsch, Германия. С размольными стаканами объёмом 500 мл. Шары диаметром 5 мм из оксида циркония (ZrO2). Тестовые измерения проводили на образце А.
Для подбора оптимальных параметров измельчения были проведены несколько экспериментов. Было исследовано влияние времени на степень измельчения. Для достижения заданного размера частиц было принято решение увеличить время измельчения.
Таблица 2. Параметры эксперимента по измельчению образца.
Сводные данные по распределению частиц в пробах предоставлены на Фиг.11. В опыте 8 для образца А был получен размер частиц менее 3 мкм. 10% частиц менее чем 0.7 мкм (D10), 50% частиц менее чем 2.1 мкм (D50) и 90% менее чем 2.9 мкм (D90). Размеры частиц определяли на лазерном дифракционном анализаторе частиц MASTERSIZER 3000. В аналогичных условиях были измельчены образцы B и С.
Полученные образцы помещали в бюксы с плотно закрывающимися крышками и хранили при комнатной температуре.
Через две недели полученные образцы исследовали повторно на лазерном дифракционном анализаторе частиц MASTERSIZER 3000. Образцы А и B сохранили распределения по размерам респирабельных частиц в процессе хранения.
В образце С были выявлены частицы размером более 100 мкм. Без вспомогательных эксципиентов такая форма непригодна для использования в ингаляторе.
Пример 9. Исследование противовоспалительной активности твердых форм 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты на модели каррагининового отека лапы у крыс.
Проводили серию экспериментов на крысах, которых рандомизированно делили на группы, в каждой группе по 5 животных. Данные в контроле объединяли. Для проведения исследований была использована модель каррагининового отека лапы крыс линии Вистар. Отек вызывали субплантарным введением 0,1 мл 1%-ного водного раствора λ-каррагинина в заднюю конечность животных опытных и контрольных групп. Животные экспериментальных групп получали исследуемые соединения сразу после индукции каррагининового отека перорально при помощи зонда. Твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты настоящего изобретения, полученной согласно примеру 1, вводили животным в дозе 10 мг/кг. Аналогичным образом животные контрольной группы получали соответствующее количество плацебо. Оценку отека проводили измерением объема стопы с помощью механического онкометра до введения флагогена (λ -каррагинина), через два часа после его введения и через четыре часа после его введения. О степени отека судили по разнице в объеме между отечной стопой и стопой до индукции воспаления. Противовоспалительную активность определяли при помощи формулы А=(ΔVк-ΔVэ/ΔVк)·100%, где А- противовоспалительная активность в процентах; ΔVэ и ΔVк - разница между отечной и нормальной стопами у животных экспериментальных и контрольной групп.
Степень уменьшения отека стопы (среднее значение по группе) через 2 часа исследования у экспериментальной группы была на 40% выше, чем у контрольной.
Аналогичные результаты были достигнуты для твердой формы, полученной в примере 3.
Представленные данные свидетельствуют о том, что твердые формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты согласно настоящему изобретению проявляют противовоспалительную активность.
Пример 10. Исследование стабильности при хранении новых твердых форм 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты
Стабильность твердых форм 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты оценивали методом ускоренного старения согласно ОФС.1.1.0009.15 Сроки годности лекарственных средств, государственной фармакопеи РФ. При повышенных температурах, как правило, ускоряются протекающие в лекарственных средствах физико-химические процессы, приводящие со временем к нежелательным изменениям качества. Таким образом, при повышенной температуре промежуток времени, в течение которого контролируемые показатели качества лекарственного средства сохраняются в допустимых пределах (экспериментальный срок годности), искусственно сокращается.
В качестве предполагаемых условий хранения твердых форм 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты были выбраны 10 лет при температуре не выше 25°С.
Срок годности (С) при температуре хранения (tхр) связан с экспериментальным сроком годности (СЭ) при повышенной температуре экспериментального хранения (tэ) уравнением Вант-Гоффа:
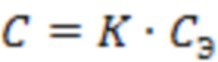 ;
; 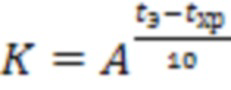 ;
;
где А - температурный коэффициент, который принимается равным 2.5.
Были выбраны условия хранения в эксперименте ускоренного старения: 40 дней при температуре 75°C. Для проведения исследования образец твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты оставляли в климатической камере на 40 дней при температуре 75°C. Состав полученного образца исследовали методом высокоэффективной жидкостной хроматографии. Количество примесей на полученной хроматограмме не превысило 0.5% для каждой формы, что подтверждает их стабильность.
Пример 11. Исследование активности в модели острого риносинусита у крыс
Методика эксперимента . В экспериментальную группу были отобраны животные (крысы-самцы линии Вистар) без признаков отклонений внешнего вида таким образом, чтобы индивидуальное значение массы отклонялось от среднего значения в пределах пола не более чем на ±10%. Индукцию острого риносинусита проводили путем однократного интраназального введения 20 мкл 7,5% формалина в каждый носовой ход. Твердую форму по примеру 1 (далее - активная фармацевтическая субстанция или АФС) в дозах 1.8, 18 мг/кг вводили внутрижелудочно, ежедневно, 1 раз в сутки, начиная через 24 ч после введения формалина, последнее введение происходило на 7-е сутки.
На 8-е сутки животных анестезировали путем внутрибрюшинного введения смеси Золетила и Ксилазина (1:5) в объеме 1 мл/кг. Канюли через трахею вставляли в носоглотку и промывали при помощи шприца физиологическим раствором в объеме 2 мл с такой скоростью, чтобы из носа раствор стекал капельно. C помощью камеры Горяева определяли абсолютное количество клеток в лаваже (в трех повторах). Назальный лаваж центрифугировали в течение 10 минут и из клеточного осадка готовили мазки, которые фиксировали в метаноле и окрашивали по Романовскому-Гимзе. По мазкам под микроскопом определяли относительное количество нейтрофилов, макрофагов. Подсчет производили на 300 клеток.
Для всех данных применена описательная статистика: подсчитаны среднее арифметическое (Mean) и ошибка среднего значения (SEM). С помощью критерия Шапиро-Уилка проверена нормальность распределения полученных в ходе эксперимента значений. В случае отличного от нормального распределения для оценки межгрупповых различий использовался анализ 1-way ANOVA (с постанализом Данна). В случае нормального распределения для сравнения нескольких групп использовался анализ 1-way ANOVA (с постанализом Тьюки). Статистический анализ проводился с использованием программы GraphPad Prism. 9.0. Различия определялись при p<0.05.
Условия эксперимента представлены в таблице 2, а результаты исследования - на Фиг.12.
на 7-е сутки
Проведенное исследование показывает, что твердая форма по примеру 1 может использоваться для лечения или профилактики острого риносинусита.
Пример 12. Исследование активности в модели неинфекционного фарингита у крыс
Модель неинфекционного фарингита у крыс реализовали по стандартной методике (см. G.L.VISWANATHA et al. Novel experimental model of non-infectious pharyngitis in rats, JOURNAL OF PHARMACOLOGICAL AND TOXICOLOGICAL METHODS, 2014, V.69, N.2, pp.189-195). В экспериментальную группу были отобраны животные (крысы-самцы линии Вистар) без признаков отклонений внешнего вида, таким образом, чтобы индивидуальное значение массы отклонялось от среднего значения в пределах пола не более чем на 10%. Крысам производили анестезию натрий-тиопентоном (50 мг/кг, внутрибрюшинно) и в наружную яремную вену вставляли канюлю с трубкой из силиконового каучука RenaSil® (SIL 037, Braintree Scientific, Inc., Braintree, MA). Краситель Эванса голубой (ЭГ) вводили всем животным в дозе 30 мг/кг внутривенно через катетер; через 10 мин после введения красителя ЭГ на поверхность слизистой глотки наносили формалин (раствор формальдегида в концентрации 30%) следующим образом: язык слегка вытаскивали, область глотки открывали глубоко с помощью тупых щипцов и осторожно стерильным ватным тампоном наносили формалин (50 мкл) трижды в течение 5 сек при каждом нанесении. В интактной группе применяли физиологический раствор. Твердую форму по примеру 3 (далее - активная фармацевтическая субстанция или АФС) в дозах 1.8, 9, 18 мг/кг вводили внутрижелудочно за 24 и 1 ч до нанесения формальдегида.
Через 60 минут после нанесения формальдегида животных забивали путем обескровливания. Головную часть каждой крысы перфузировали гепаринизированным физиологическим раствором (40 ЕД/мл), чтобы удалить внутрисосудистый краситель ЭГ.
Степень эффективности в лечении фарингита оценивали по тесту экссудации красителя Эванса голубого (ЭГ). Краситель ЭГ из ткани экстрагировали в формамид при 55°С в течение 24 часов, и поглощение определяли спектрофотометрически при 620 нм. Количество красителя ЭГ в ткани рассчитывали, используя стандартную кривую для красителя ЭГ, и выражали в микрограммах красителя на милиграмм сырого веса ткани (мкг/мг).
Для всех данных применена описательная статистика: подсчитаны среднее арифметическое (Mean) и ошибка среднего значения (SEM). Для сравнения групп использовался тест Манна-Уитни. Статистический анализ проводился с использованием программы GraphPad Prism. 9.0. Различия определялись при p<0.05.
Условия эксперимента представлены в таблице 3, а результаты исследования - на Фиг.13.
нанесения формалина
Проведенное исследование показывает, что твердая форма по примеру 3 может использоваться для лечения или профилактики неинфекционного фарингита.
Пример 13. Исследование активности в модели лихорадочной реакции у крыс
Модель лихорадочной реакции у крыс реализовали по стандартной методике (F.ZHANG et al., Metabolomic study of the fever model induced by baker's yeast and the antipyretic effects of aspirin in rats using nuclear magnetic resonance and gas chromatography-mass spectrometry, JOURNAL OF PHARMACEUTICAL AND BIOMEDICAL ANALYSIS, 2013, V.81, pp.168-177). В экспериментальную группу были отобраны животные (крысы-самцы линии Вистар) без признаков отклонений внешнего вида, таким образом, чтобы индивидуальное значение массы отклонялось от среднего значения в пределах пола не более чем на ±10%. Крысам линии Вистар подкожнo вводили 20% суспензию пекарских дрожжей (12 мл/кг). Твердую форму по примеру 1 (далее - активная фармацевтическая субстанция или АФС) в дозе 1.8 мг/кг вводили внутрижелудочно, однократно через 14 ч после введения дрожжей. Ректальную температуру измеряли электротермометром (AT-12R PHYSITEMP, производство Израиль) до введения пирогена и через 14, 16, 17, 18, 19, 20, 24, 36, 48, 60 и 72 ч после него. Результаты выражали в виде прироста температуры по отношению к значениям до введения пирогена.
Для всех данных применена описательная статистика: подсчитаны среднее арифметическое (Mean) и ошибка среднего значения (SEM). С помощью критерия Шапиро-Уилка проверена нормальность распределения полученных в ходе эксперимента значений. В случае отличного от нормального распределения для оценки межгрупповых различий использовался анализ 1-way ANOVA (с постанализом Данна). В случае нормального распределения для сравнения нескольких групп использовался анализ 1-way ANOVA (с постанализом Тьюки). Статистический анализ проводился с использованием программы GraphPad Prism. 9.0. Различия определялись при p<0.05.
Условия эксперимента представлены в таблице 4, а результаты исследования - на Фиг.14.
через 14 часов после
введения дрожжей
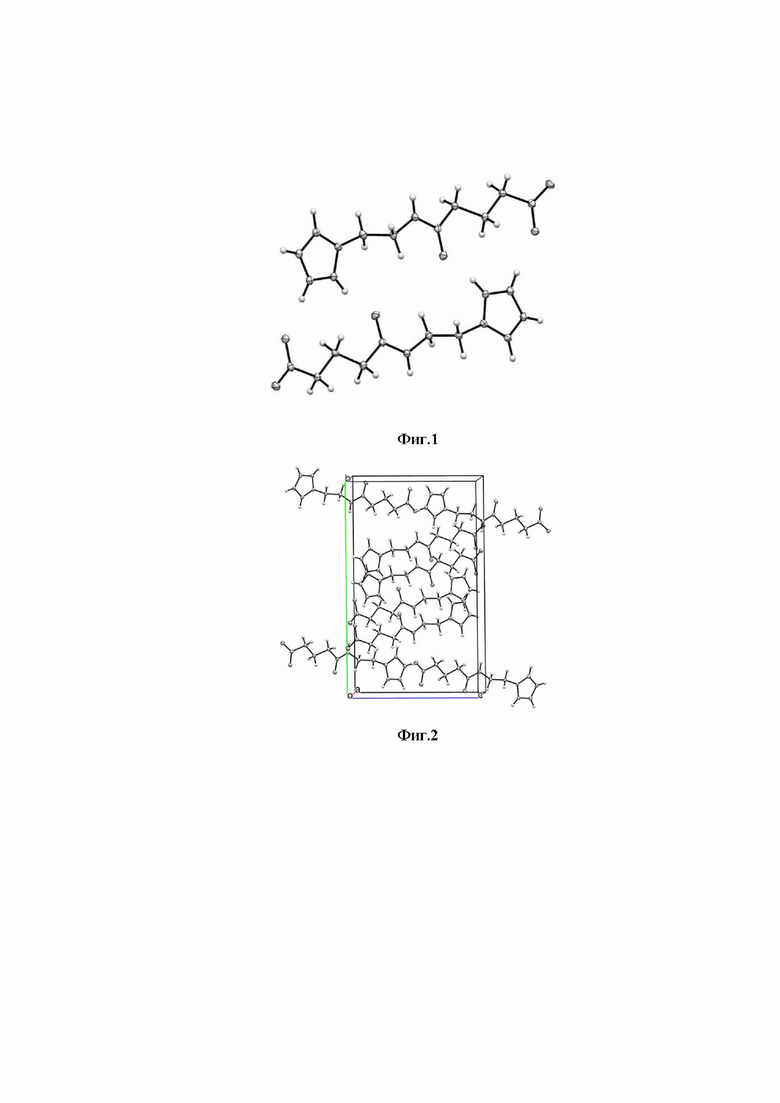
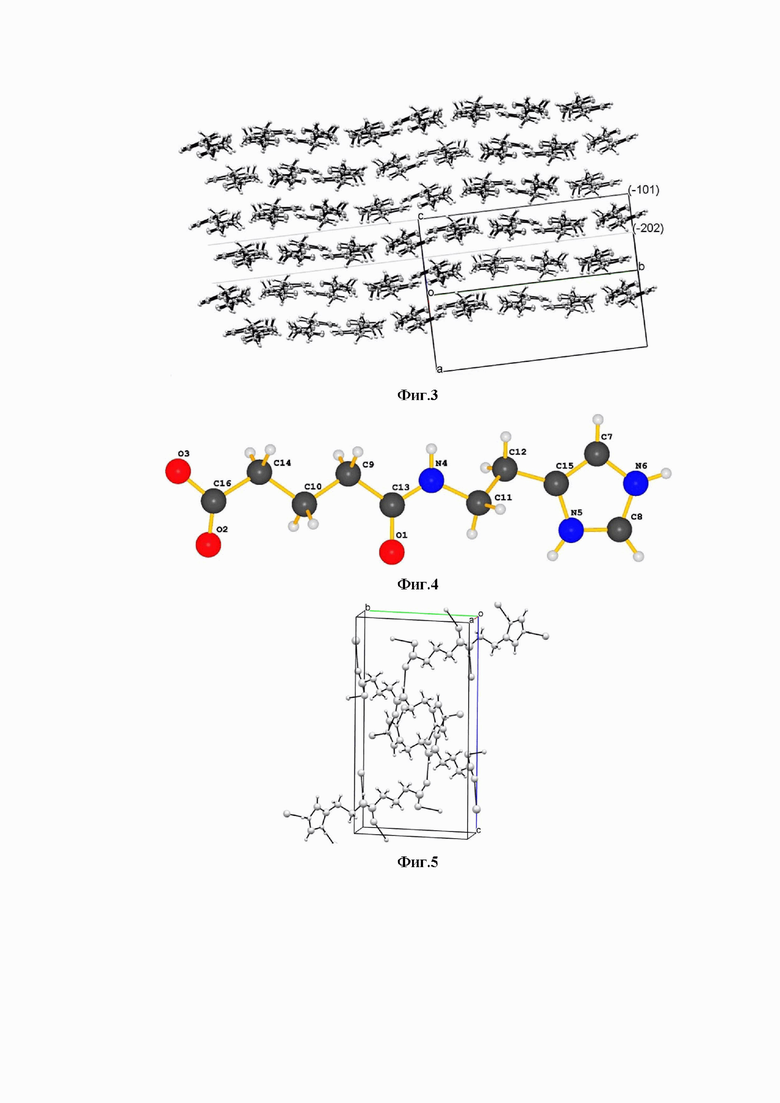
Изобретение относится к твердой форме 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащей цвиттер-ион, формулы (II), характеризующейся моноклинной сингонией кристаллической решетки и величинами ребер кристаллической ячейки (в ангстрем,  ): 5.39±0.50
): 5.39±0.50  , 10.08±0.50
, 10.08±0.50  и 19.85±0.50
и 19.85±0.50  и величиной угла (в град) 100.26±5.00. Твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты формулы (II) получают путем взаимодействия гистамина с глутаровым ангидридом и обработки полученного продукта минеральной кислотой с последующим подщелачиванием или добавлением основания до завершения выпадения осадка твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащей 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты в виде цвиттер-иона формулы (II). Изобретение относится к фармацевтической композиции для лечения или профилактики заболеваний, вызванных вирусными инфекциями, содержащей твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащей цвиттер-ион формулы (II), и по меньшей мере один фармацевтически приемлемый эксципиент, при этом вирусные инфекции представляют собой вирус парагриппа, вирус гриппа, в том числе гриппа А, В, С и D, коронавирус. Твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащей цвиттер-ион, формулы (II), применяют для лечения или профилактики заболеваний, вызванных вирусными инфекциями, при этом вирусные инфекции представляют собой вирус парагриппа, вирус гриппа, в том числе гриппа А, В, С и D, коронавирус. 5 н. и 9 з.п. ф-лы, 14 ил., 5 табл., 13 пр.
и величиной угла (в град) 100.26±5.00. Твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты формулы (II) получают путем взаимодействия гистамина с глутаровым ангидридом и обработки полученного продукта минеральной кислотой с последующим подщелачиванием или добавлением основания до завершения выпадения осадка твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащей 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты в виде цвиттер-иона формулы (II). Изобретение относится к фармацевтической композиции для лечения или профилактики заболеваний, вызванных вирусными инфекциями, содержащей твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащей цвиттер-ион формулы (II), и по меньшей мере один фармацевтически приемлемый эксципиент, при этом вирусные инфекции представляют собой вирус парагриппа, вирус гриппа, в том числе гриппа А, В, С и D, коронавирус. Твердую форму 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащей цвиттер-ион, формулы (II), применяют для лечения или профилактики заболеваний, вызванных вирусными инфекциями, при этом вирусные инфекции представляют собой вирус парагриппа, вирус гриппа, в том числе гриппа А, В, С и D, коронавирус. 5 н. и 9 з.п. ф-лы, 14 ил., 5 табл., 13 пр.
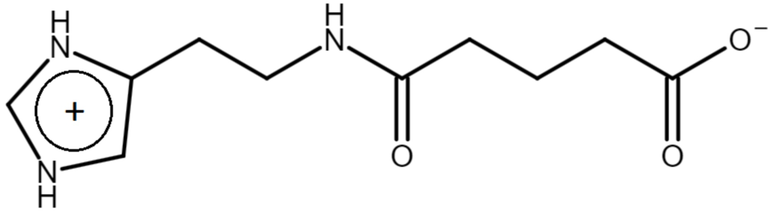
Формула (II)
1. Твердая форма 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащая цвиттер-ион формулы (II)
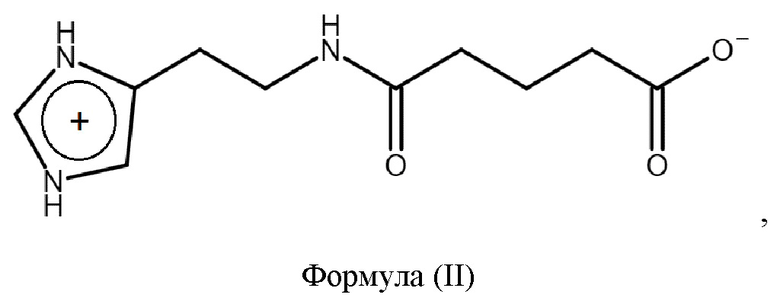
отличающаяся тем, что твердая форма относится к кристаллической форме, характеризующейся моноклинной сингонией кристаллической решетки и величинами ребер кристаллической ячейки (в ангстрем,  ): 5.39±0.50
): 5.39±0.50  , 10.08±0.50
, 10.08±0.50  и 19.85±0.50
и 19.85±0.50  и величиной угла (в град) 100.26±5.00.
и величиной угла (в град) 100.26±5.00.
2. Твердая форма по п.1, отличающаяся тем, что молекулы цвиттер-ионов 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты связаны между собой водородными связями таким образом, что расположены перпендикулярно относительно друг друга.
3. Способ получения твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты по любому из пп.1 или 2, включающий взаимодействие гистамина с глутаровым ангидридом и обработку полученного продукта минеральной кислотой с последующим подщелачиванием или добавлением основания до завершения выпадения осадка твердой формы 2-(имидазол-4-ил)этанамида пентандиовой-1,5 кислоты, содержащей 2-(имидазол-4-ил)этанамид пентандиовой-1,5 кислоты в виде цвиттер-иона формулы (II).
4. Способ по п.3, дополнительно включающий стадию получения гистамина путем взаимодействия дигидрохлорида гистамина с подходящим основанием.
5. Способ по п.3, дополнительно включающий добавление растворителя, выбранного из метанола или этанола, на стадии подщелачивания.
6. Фармацевтическая композиция для лечения или профилактики заболеваний, вызванных вирусными инфекциями, содержащая твердую форму по любому из пп.1 или 2 и по меньшей мере один фармацевтически приемлемый эксципиент, при этом вирусные инфекции представляют собой вирус парагриппа, вирус гриппа, в том числе гриппа А, В, С и D, коронавирус.
7. Фармацевтическая композиция по п.6, содержащая твердую форму 2-(имидазол-4-ил)этанамида по любому из пп.1 или 2 в качестве активного вещества и маннит (E421), сукралозу в качестве вспомогательных веществ.
8. Лекарственное средство в твердой форме для лечения или профилактики заболеваний, вызванных вирусными инфекциями, содержащее твердую форму по любому из пп.1 или 2 или фармацевтическую композицию по любому из пп.6 или 7, при этом вирусные инфекции представляют собой вирус парагриппа, вирус гриппа, в том числе гриппа А, В, С и D, коронавирус.
9. Лекарственное средство по п.8, отличающееся тем, что твердая форма представляет собой порошок, гранулу, капсулу или таблетку.
10. Лекарственное средство по п.8 в форме порошка, содержащее твердую форму 2-(имидазол-4-ил)этанамида по любому из пп.1 или 2 в качестве активного вещества и маннит (E421), сукралозу в качестве вспомогательных веществ.
11. Лекарственное средство по п.8 в форме порошка для ингаляции, содержащее твердую форму 2-(имидазол-4-ил)этанамида по любому из пп.1 или 2, отличающееся тем, что указанное лекарственное средство не содержит вспомогательных веществ.
12. Лекарственное средство по п.8 в форме капсул для ингаляции, содержащее твердую форму 2-(имидазол-4-ил)этанамида по любому из пп.1 или 2, отличающееся тем, что указанное лекарственное средство не содержит вспомогательных веществ.
13. Лекарственное средство по п.8, отличающееся тем, что включает по меньшей мере один фармацевтически приемлемый эксципиент.
14. Применение твердой формы по любому из пп.1 или 2 для лечения или профилактики заболеваний, вызванных вирусными инфекциями, при этом вирусные инфекции представляют собой вирус парагриппа, вирус гриппа, в том числе гриппа А, В, С и D, коронавирус.
| WO 1999001103 A2, 14.01.1999 | |||
| R | |||
| Thakuria и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Atwood, Elsevier, 2017, с.283-309, doi: 10.1016/B978-0-12-409547-2.12570-3 | |||
| Клиническая фармакокинетика: теоретические, прикладные и аналитические аспекты: руководство / Под | |||
Авторы
Даты
2024-06-17—Публикация
2022-08-25—Подача