Изобретение относится к области медицины, более конкретно к офтальмологии и может быть использовано с лечебной целью при патологии роговицы, включая первичные и вторичные кератоэктазии, а также их профилактику при лазерных, хирургических, фоторефракционных, фототерапевтических и комбинированных операциях на роговой оболочке.
Известен способ и устройство для кросслинкинга роговицы, включающие проведение под местной анестезией деэпителизации в зоне 8-9 мм, 30-минутную инстилляцию 0,1% раствора фотосенсибилизатора рибофлавина и ультрафиолетовое облучение роговицы с применением специального устройства, с расположенным в нем источником УФ-излучения. Для УФ излучения использовались длины волн 365 нм, 370 нм или 375 нм и мощность излучения 3 мВт/см². Облучение проводилось в течение 30 минут и суммарная доза составляла 5,4 Дж/см² [1]. Данный способ получил название стандартного Дрезденского протокола кросслинкинга роговицы. Известны различные модификации стандартного способа проведения кросслинкинга. Это касается проведения кросслинкинга без удаления эпителия, который получил название трансэпителиальный кросслинкинг. Однако по сравнению со стандартным протоколом кросслинкинга, при трансэпителиальной технологии в среднем на 40% снижался эффект кросслинкинга. На это указывала меньшая глубина расположения демаркационной линии в строме по данным ОКТ роговицы.
Для профилактики кератоэктазий в лазерной рефракционной хирургии роговицы были разработаны различные варианты ускоренного кросслинкинга. При этом сокращалось время насыщения стромы рибофлавином, время УФ облучения, за счёт повышения плотности потока и мощности на единицу площади. Прежде всего, это касалось операции лазерного in situ кератомилёза (ЛАСИК). Для проведения ускоренного кросслинкинга нашли применение 0,22%, 0,25% и 0,30% растворы рибофлавина. Дальнейшее увеличение концентрации до 0,5% оказалось не целесообразным, поскольку это приводило к полному поглощению УФ излучения в слоях стромы на глубине 100 мкм. Это снижало объёмный эффект кросслинкинга в строме при лечении первичных и вторичных эктазий роговой оболочки. При ускоренном кросслинкинге роговицы использовались различные плотности мощности УФ излучения равные 9, 18 или 30 мВТ/см2. Соответственно продолжительность облучения составляла в 10, 5 и 3 минуты и суммарная доза УФ облучения равнач 5,4 Дж/см². При операции лазерного кератомилёза в сочетании с кросслинкингом (LASIK Xtra) дозу облучения было предложено уменьшить до 3,6 Дж/см² [2] и даже 1,4 Дж/см² [3]. Повышение плотности мощности потока УФ излучения до 9 мВт/см² и выше снижало эффект кросслинкинга. Увеличение концентрации рибофлавина более 0,1% не приводило к улучшению результатов ускоренного кросслинкинга. По данным оптической когерентной томографии при ускоренном кросслинкинге отмечалась меньшая глубина расположения демаркационной линии в строме роговицы.
В исследованиях, проведенных в компании Avedro, было обнаружено полное поглощение кислорода в строме роговицы, сразу же после УФ облучения с плотностью 30 мВт/см2 в течение одной секунды. Аналогичный эффект наблюдался примерно через пять секунд при плотности УФ излучения равной 3 мВт/см2. В связи с этим возникли вопросы о необходимом уровне кислорода в строме и целесообразности её дополнительной оксигенации. Были проведены исследования, которые показали, что при дополнительном насыщении стромы газовой смесью с 90% содержанием кислорода, также наблюдалось его быстрое потребление.
При применении технологии фоторефракционной кератоэктомии (ФРК) или трансэпителиальной фоторефракционной кератэктомии (ТрансФРК) в случаях тонкой роговицы и большого объёма фотокератоабляции было предложено проведение профилактического кросслиннкинга.
Следует отметить широкий диапазон различных способов деэпителизации и временных интервалов насыщения роговицы рибофлавином. Так, преимуществом лазерной абляции эпителия явилось то, что при такой бесконтактной технологии можно было строго дозировать площадь деэпителизации. При этом меньше травмировался эпителиальный край, повреждалась Боуменовая мембрана и поверхностные слои стромы. Что же касается временных интервалов насыщения роговицы рибофлавином, то они колебались в очень широком диапазоне от 1,5 до 30 минут, в зависимости от технологии кросслинкинга и применяемой плотности энергии УФ излучения.
Однако, при традиционном, трансэпителиальном и различных вариантах ускоренного кросслинкинга наблюдались осложнения. Это ограничивало диапазон практического применения кросслинкинга при офтальмопатологии. Прежде всего, это касалось проведения профилактического ускоренного кросслинкинга в лазерной рефракционной хирургии роговицы при исходно тонкой роговице и при коррекции высоких степеней аметропии.
Наиболее близким к предлагаемому способу кросслинкинга и устройству для его осуществления является способ фоторефракционной абляции с рибофлавином. Суть данного способа сводится к лазерной абляции эпителия, насыщению стромы рибофлавином и выполнению фоторефракционной кератоэктомии. При таком способе фоторефракционной абляции, насыщенные рибофлавином слои стромы роговицы срабатывали, как спектральные фильтры и поглощали вторичное излучение индуцированное абляцией. Это защищало слои стромы, прилежащие к зоне абляции, от негативного влияния вторичного излучения на кератоциты и нервные волокна. Наряду с фотопротекторными свойствами рибофлавина в слоях истонченной стромы роговицы, прилежащих к зоне абляции, был выявлен сопутствующий затухающий эффект кросслинкинга. Данный эффект первоначально был подтверждён при сравнении биомеханических свойств образцов роговиц при абляции без, и с предварительным насыщением рибофлавином. По данным трансмиссионной микроскопии после абляции с рибофлавином в слоях истонченной стромы было обнаружено формированию стабильных поперечных сшивок в коллагеновых волокнах и повышение плотности их упаковки на единицу площади. Кроме того, важным преимуществом такого способа фоторефракционной абляции с рибофлавином явилось снижение негативного влияния индуцированного абляцией вторичного излучения на глубжележащие слои истончённой стромы роговицы. Именно индуцируемое при абляции вторичное излучение способствовало накоплению перекисных радикалов, их повреждающему действию на кератоциты, нервы и тканевые структуры в подлежащих слоях истонченной стромы роговицы. Постабляционный оксидативный стресс, в свою очередь, запускал асептическую воспалительную реакцию в раннем послеоперационном периоде. В случае проведения абляции с рибофлавином воспалительная реакция была значительно меньшей. Это снижало выраженность регенераторных процессов в строме, развитие субэпителиальной или стромальной фиброплазии, Всё это способствовало более ранней стабилизации рефракционных и визуальных результатов после фоторефракционных и фототерапевтических операциях на роговице. Такой способ фоторефракционной кератоабляции с фотопротекцией рибофлавином и эффектом кросслинкинга был защищён патентом на изобретение (Корниловский И.М. с соавт. “Способ фоторефракционной абляции роговицы”, Патент РФ №2578388 C1 с приоритетом от 21.10.2014. [6]. Экспериментальные исследования с биомеханическим тестированием образцов роговиц после абляции с рибофлавином, показали, что лазер-индуцированных эффект кросслинкинга был достаточным для компенсации ослабления биомеханических свойств истонченной роговицы. Однако, сам факт абляции при таком способе кросслинкинга был не приемлем при кератоконусе и вторичных эктазиях роговицы различной этиологии.
Суть предлагаемого нового технического решения в заявляемом способе кросслинкинга роговицы, и его отличие от прототипа, заключается в поэтапном насыщении стромы охлажденным раствором рибофлавином и его активации лазерным излучением дальнего спектрального диапазона при плотностях энергии ниже порога абляции стромы для частоты следования импульсов в применяемой эксимерной лазерной офтальмологической установки на аргон-фторе. При этом сканирование роговицы лучом с пятном малого диаметра обеспечивает возможность проведения персонализированного локального кросслинкинга роговицы по данным компьютерной кератотопографии.
Все значения плотности энергии в импульсе ниже 50 мДж/см2 являются субабляционными, и не сопровождаются испарением стромы роговицы. В предлагаемом нами способе лечебного кросслинкинга предлагается использовать плотности энергии в импульсе 16 мДж/см2 и 25 мДж/см2. В ряде случаев для усиления биомеханического эффекта и формирования Боуменоподобной мембранной структуры большей толщины были применением плотности энергии в импульсе в диапазоне от 25 до 48 мДж/см2. Во всех случаях это были плотности энергии ниже порога абляции роговичной стромы для применяемой частоты следования импульсов 500 Гц.
При лечебном лазер-индуцированном кросслинкинге общее количество этапов и энергетическая доза, каждого из них рассчитывались таким образом, чтобы суммарная доза не превышала таковую при традиционном кросслиникинге (5,4 Дж/см2). При профилактическом кросслинкинге в фоторефракционной и фототерапеввтической хирургии суммарная доза предопределялась длительностью вторичного излучения, индуцированного в ходе кератоабляции. В ряде случаев, например, при подозрении на субклинический кератоконус, применяли дополнительное облучение при плотностях энергии в импульсе ниже порога абляции для усиления эффекта кросслинкинга. Важным преимуществом такого профилактического и лечебного роговичного кросслинкинга явился тот факт, что вторичное излучение носило затухающий характер, а его спектр перекрывал всё четыре пика максимального поглощения рибофлавином. Кроме того, воздействие осуществлялось в сканирующем режиме пятном менее 1,0 мм в диаметре. Это позволило впервые реализовать проведение персонализированного кросслинкинга по данным компьютерной кератотопографии. Применение для роговичного кросслинкинга сканирующего режима облучения пятном малого диаметра обеспечивало поддержание лучшей оксигенации в строме роговицы.
Во всех современных эксимерных лазерных установках размер пятна в сканирующем луче меньше 1,0 мм. Это было обусловлено тем, что при большем диаметре пятна трудно реализовать проведение персонализированной абляции по данным кератотопографии или аберрометрии. Кроме того, увеличение размеров пятна влечёт за собой необходимость повышения мощности лазерного генератора излучения, что значительно удорожает стоимость офтальмологического эксимерного лазера.
Важным преимуществом предлагаемого способа роговичного кросслинкинга явилось то, что зона облучения могла быть персонализирована в широком диапазоне с учётом данных кератотопографии. При таком способе лечебного кросслинкинга суммарная доза облучения рассчитывалась по количеству импульсов с учётом плотности энергии в импульсе ниже порога абляции стромы роговицы для выбранной частоты их следования. При этом, как показали исследования, в зависимости от конкретных решаемых задач и вида офтальмопатологии применялась частота следования импульсов в диапазоне от 100 до 500 Гц. Использование частоты следования импульсов менее 100 Гц было не целесообразным, поскольку это значительно увеличивало время проведения процедуры кросслинкинга. Кроме того, требовалась более длительная фиксация глазом пациента прицельного луча лазера при проведении персонализированного топографически ориентированного кросслинкинга. Увеличение частоты следования импульсов более 500 Гц также было не желательным, из-за большего снижения степени оксигенации стромы и повышения её температуры.
В предлагаемом способе кросслинкинга предпочтение было отдано удалению эпителия путём лазерной абляции с учётом толщины, определяемой по данным оптической когерентной томографии роговицы. Диаметр зоны сканирования уменьшали не менее чем на 1 мм относительной зоны деэпителизации. Этопредотвращало возможность негативного влияния субабляционных плотностей энергии на эпителиальный край При этом минимальный отступ от эпителиального края составил 0,5 мм. В ряде случаев при резких перепадах в толщине эпителия применяли комбинированную абляцию эпителия с различной толщиной в центральных, парацентральных и периферических отделах или проводили его механическую скарификацию. Такой подход использовался, например, при значительном истончении эпителия на вершине кератоконуса.
Время насыщения стромы рибофлавином перед и между этапами определялось, исходя из профилактической или лечебной направленности проведения роговичного кросслинкинга, степени аметропии, объёма аблируемой стромы и вида роговичной патологии. Применялись капельная, аэрозольная или комбинированная методика насыщения. Для аэрозольной методики был использован ультразвуковой небулайзер с инновационной меш-технологией диспригнирования раствора. Это позволяло получать размер аэрозольных частиц раствора рибофлавина размером от 1 до 5 мкм (более 60% частиц имели средний размер 3,7±25% мкм), что улучшало их всасывание стромой с деэпителизированной поверхности роговицы.
Согласно данным литературы для кросслинкинга роговицы используются растворы рибофлавина в концентрации от 0,1% до 0,3%, содержащие 20% декстрана или без него [4,5]. В предлагаемом способе кросслинкинга роговицы после лазерной абляции эпителия для насыщения стромы применяли изотонический 0,1% или 0,25% растворы рибофлавина, охлажденные до температуры не превышающей +7°C. При аэрозольном насыщении изотонический раствор рибофлавина помещался в стерильную кювету ультразвукового небулайзера. При комбинированном способе насыщения стромы рибофлавином дополнительно подготавливались шприцы ёмкостью 5-10 мл с 0,1% или 0,25% изотоническим раствором рибофлавина, охлажденным до +5-7°C. Одноразовые шприцы с приготовленным 0,25% изотоническим раствором рибофлавина размещались на стерильной поверхности контейнера с температурой хладоагента не выше +7°C. В ранее проведенных нами исследованиях было показано, что положительный эффект умеренной локальной гипотермии роговицы отмечается при воздействии на неё хладоагентами в температурном диапазоне от +5 до +7°C. Такой температурный режим использовался при капельном, аэрозольном или комбинированном способах насыщения роговицы рибофлавином. Локальная гипотермия снижала температуру роговицы на 1-3°С, что позволяло нивелировать её повышение, в частности, при проведении фоторефракционной абляции с рибофлавином. Температуру роговицы измеряли бесконтактным инфракрасным термометром.
Положительный эффект применения умеренной локальной гипотермии был доказан в ранее проведенных исследованиях по транспалпебральной и эпибульбарной гипотермии на этапах проведения фоторефракционной кератоабляции [7,8]. Предлагаемый подход к проведению кросслинкинга при пониженной температуре стромы роговицы имел ряд преимуществ перед предложением проведения кросслинкига в условиях понижения внешней температуры воздуха до +4º С [9]. Целесообразность локальной гипотермии при кросслинкинге подтверждали данные литературы об увеличении концентрация кислорода в роговицы при пониженной температуре [10]. Кроме того, имеются сообщения о регулирующем влиянии кислорода на эффективность формирования сшивок при роговичном кросслинкинге [11].
Впервые комбинация абляционных и субабляционных плотностей энергии в импульсе излучения эксимерного лазера на аргон-фторе с длиной волны 193 нм была применена нами при удалении эпителия. Применялись плотности энергии в импульсе, лежащие ниже порога абляции Боуменовой оболочки и стромы. На такой способ абляции эпителия при фоторефракционных и фототерапевтических оперциях на роговице был получен патент на изобретение (Корниловский И.М. “Cпособ абляции эпителия при фоторефракционных и фототерапевтических оперциях на роговице”, Патент РФ на изобретение № 2718260 C1, с приоритетом от 27.12.2018 [12].
В предлагаемом способе роговичного лазер-индуцированного кросслинкинга перед насыщением стромы роговицы рибофлавином проводилась лазерная абляция эпителия. Абляционные режимы были применены для профилактического лазер-индуцированного кросслинкинга в слоях стромы роговицы при проведении фоторефракционной или фототерапевтической кератоэктомии с рибофлавином. Это сопровождалось эффектом кросслинкинга в истончённых слоях стромы. Получаемый при этом биомеханический эффект повышения прочностных характеристик истончённой стромы уступал таковому при традиционном способе кросслинкинга. Тем не менее, как показали клинические наблюдения, этого было достаточно для компенсации абляционного ослабления истонченной стромы роговицы. Как показали клинические наблюдения, такой способ профилактического кросслинкинга излучением эксимерного лазера на аргон-фторе оказался достаточным для компенсации ослабления прочностных свойств роговицы при абляционном её истончении.
Проведенные нами экспериментально-клинические исследования, показали, что излучение эксимерного лазера на аргон-фторе с длиной волны 193 нм может быть применено для лечебного кросслинкинга при плотностях энергии ниже порога абляции. При таких параметрах лазерного излучения в строме наблюдались все классические признаки кросслинкинга традиционной технологии кросслинкинга с формированием демаркационной линии в строме. Это было подтверждено клиническими и объективными критериями оценки по данным оптической когерентной томографии и денситометрии. Аналогов предлагаемого нового способа лечебного роговичного кросслинкинга найдено не было. Всё вышеизложенное позволило применить лечебный лазер-индуцированный кросслинкинг при различной патологии роговицы, включая кератоконусе и вторичные кератоэктазии различной этиологии.
В устройствах разработанных для проведения кросслинкинга роговицы использовались непрерывный или импульсный режимы ультрафиолетового излучения, длины волн от 365 или 370 нм и различные плотности энергии от от 3 мВт/cм2 до 45 мВт/cм2. В различных модификациях таких устройств дополнительно применяли световые и низкоинтенсивные лазерные источники прицеливания, видеокамеры и контролирующие мониторы за проведением процедуры на глазу. Как правило, при выполнении роговичного кросслининга с применением тех или иных устройств проводился дополнительный визуальный контроль под операционным микроскопом или щелевой лампой.
Известно устройство и способ его применения для кросслинкинга роговицы, в котором предлагается использование лазерного излучения в широком спектральном диапазоне от 300 до 1900 нм, в интервалах 300-650, 650-1050, 650-1050, 1050-1250 или 1100-1900 нм. В данном устройстве и способе его применения для кросслинкинга роговиц предлагалось использование одной и той же длины волны в режимах фотодеструкции и фотоактивации. Режим фотодекструкции использовался на этапе обеспечения насыщения стромы роговицы рибофлавином. Режим фотоактивации при плотностях энергии, лежащих ниже порога деструкции, применяли непосредственно для рибофлавина (Патент США - US20150313756A1). “APPARATUS FOR CORNEAL CROSSLINKING” International Publication Date WO 2017/070637 Al27 April 2017 (27.04.2017) PO PCT) [13] Однако, в описание устройства для кросслинкинга роговицы имеется целый ряд признаков, которые уже реализованы в имеющихся лазерных офтальмологических установках. Это, в частности, касается эксимерных и фемтоскундных офтальмологических лазеров различных фирм. Следует также отметить, что заявленный в патенте широкий спектральный диапазон лазерного излучения для проведения кросслинкинга роговицы рассчитан на использование в будущем целого ряда других фотосенсибилизаторов, целесообразность и безопасность которых в клинической офтальмологии ещё требуется доказать. Это касается видимого и инфракрасных диапазонов, которые не поглощаются рибофлавином, а следовательно не могут его активировать. В заявленном патенте только теоритически обосновывается возможность применения того или иного диапазона лазерного излучения в двух режимах. Это касается энергетических параметров в режимах фотодеструкции и ниже порога деструкции. Следует отметить, что применение фемтосекундного лазерного излучения ультрафиолетового среднего спектрального диапазона в режиме фотодеструкции (фотоабляции) и ниже порога фотодеструкции (фотоабляции) не безопасно по критерию канцерогенного и мутагенного действия. Именно по этой причине средний диапазон лазерного ультрафиолетового излучения, который был заявлен в патенте, не нашел применения в клинической офтальмологии при фоторефракционных и фототерапевтических операциях на роговой оболочке. Из описания заявленного устройства не ясно, как может быть реализована его работа на глазу пациента. Это особенно важно при выполнении фотодеструкции для преодоления эпителиального барьера в той или иной зоне роговицы. Из описания технических решений заявленного устройства не понятно, как осуществляется фокусировка излучения в трёхмерном пространстве по осям x, y z относительно зрительной оси. В устройстве отсутствует визуальный контроль под микроскопом и система слежения за глазом, а также дополнительные источники излучения для прицеливания относительно зрительной оси. Таким образом, в заявленной совокупности технических решений предлагаемое устройство для проведения кросслинкинга роговицы не может быть реализовано в клинике. Данное устройство не только повторяет, но и по целому ряду технических решений уступает уже имеющимся лазерным офтальмологическим установкам сканирующего типа ультрафиолетового, видимого и инфракрасного диапазонов, в которых после проведения калибровки возможен переход к режимам ниже порога фотодеструкции и фотоабляции.
Для реализации предлагаемого нами способа кросслинкинга роговицы впервые предлагается применение широко используемых в клинической практике офтальмологических эксимерных лазерных установок различных фирм, работающих в дальнем ультрафиолетовом диапазоне. Большим преимуществом современных офтальмологических эксимерных лазерных установок является возможность проведения персонализированного сканирования различных зон роговицы, например, с учетом данных кератотопографичческих исследований. Эксимерный офтальмологический лазер дальнего ультрафиолетового диапазона на аргон-фторе с длиной волны 193 нм для кросслинкинга роговицы никогда не применялся. В данном случае речь идёт о применении известного устройства, например, эксимерной лазерной офтальмологической установкой на аргон-фторе, по новому назначению.
Необходимо отметить, что с этой же целью могут быть рекомендованы офтальмологические твёрдотельные ультрафиолетовые лазерные установки с длиной волны 213 нм, применяемые для рефракционной и лечебной кератоабляции. Эффекты взаимодействия 213 нм излучения со стромой роговицы также сопровождаются индуцированным вторичным излучением близким по спектру к индуцированному вторичному излучению лазерного излучения на аргон-фторе с длиной волны 193 нм.
Во всех газоразрядных и твёрдотельных лазерных ультрафиолетовых офтальмологических установках рекомендованных для клинического применения используются абляционные плотности энергии импульсного излучения дальнего ультрафиолетового диапазона от 193 до 222 нм, которое безопасно по канцерогенному и мутагенному потенциалу.
В офтальмологических эксимерных лазерных установках различных фирм предусмотрено использование только абляционного режима и обязательное проведение калибровки перед началом работы. Для каждой установки абляционный режим устанавливается исходя из длительности и частоты следования импульсов. Применение эксимерных лазерных офтальмологических установок для профилактического и лечебного лазер-индуцированного роговичного кросслинкинга предлагается впервые. При этом, для лечебного кросслинкинга в данных установках возможны дополнительные технические решения, предусматривающие пошаговую смену частоты следования импульсов в диапазоне 100-500 Гц и быстрый переход к плотностям энергии ниже порога абляции, без каких-либо дополнительных калибровок. Пошаговая смена частоты следования импульсов не представляет, каких либо, технических трудностей. Как уже отмечалось при описании предлагаемого способа лечебного лазер-индуцированного кросслинкинга, применение частоты следования импульсов менее 100 Гц было не целесообразным, из-за увеличения времени проведения процедуры кросслинкинга. Повышение частоты следования импульсов более 500 Гц также снижало степень оксигенации стромы и повышало её температуру. Исследования показали, что 100 Гц кратность смены частоты шага является вполне достаточной.
Для быстрого перехода от абляционных к субабляционным плотностям энергии в импульсе может быть применён широкий диапазон устройств с различными техническими решениями для интеграции в соответствующую модель лазерной офтальмологической установки. Каждое из таких устройств и технических решений в зависимости от новизны могут быть защищены самостоятельным патентом на изобретение.
Эксимерные офтальмологические лазеры и субабляционные плотности энергии с различной частотой следования импульсов никогда не применялись в лазерной хирургии роговицы и, в частности, для проведения кросслинкинга роговицы. С практической точки зрения в клинике предпочтительным является применение быстрого перехода от абляционного к субабляционным режимам. Это касается тех случаев, когда необходимо перед насыщением рибофлавина проводить лазерную абляцию эпителия. Более того, в некоторых случаях возникает необходимость поэтапного применении абляционных и субабляционных режимов. В частности, при проведении профилактического кросслинкинга в фоторефракционной или фототерапевтической хирургии роговицы, включая выполнение персонализированной рефракционной кератоабляции. С этой целью предлагается применение не менее одного специального оптического аттенюатора последовательно вводимого и выводимого из оптической системы передачи лазерного излучения к роговице. Возможно применение нескольких откалиброванных оптических аттенюаторов, которые бы были размещены, например, во вращающемся диске. Это позволяет осуществлять быстрый переход от абляционных к субабляционным плотностям энергии в импульсе без каких либо дополнительных калибровок. Технические решения самого оптического аттенюатора, механизма его введения и выведения из оптической системы передачи лазерного излучения могут быть самыми разнообразными, исходя из конструктивных особенностей той или иной модели офтальмологической эксимерной лазерной установки. В зависимости от новизны данных технических решений, последние могут быть защищены самостоятельными патентами на изобретение. Аналогичный подход может быть применён и в офтальмологических твёрдотельных ультрафиолетовых лазерных установках, которые рассматриваются, как альтернативные офтальмологическим газоразрядным эксимерным лазерам.
Применение в предлагаемом способе офтальмологических эксимерных лазерных установок и субабляционных режимов облучения позволило впервые реализовать проведение персонализированного кросслинкинга роговицы по данным кератотопографии. В применяемом нами для лечебного роговичного кросслинкинга эксимерном лазере “Микроскан Визум” размер сканирующего пятна был равен 0,9 мм с оптимизированным Гауссовым профилем распределения энергии. Частота сканирования по роговице равнялась 37 Гц.
Преимущества заявляемого способа и устройства для осуществления лазер-индуцированного кросслинкинга в дальнем ультрафиолетовом спектральном диапазоне, например, при применении импульсного лазерного излучения с длиной волны 193 нм и эксимерной лазерной офтальмологической установки заключалось в следующем:
- впервые реализовать проведение персонализированного локального кросслинкинга по данным компьютерной кератотопографии путём сканирования роговицы пятном малого диаметра излучения эксимерного лазера на аргон-фторе;
- впервые осуществить активацию рибофлавина индуцированным вторичным лазерным УФ излучением дальнего спектрального, широкий спектр которого перекрывает все 4 пика максимального поглощения рибофлавином;
- обеспечить лучшую оксигенацию стромы роговицы при её сканировании летающим пятном малого диаметра импульсного излучения эксимерного лазера;
- значительно сократить время облучения роговицы;
- уменьшить ответную асептическую воспалительную реакцию и ускорить эпителизацию роговицы за счёт большего поглощения УФ спектрального диапазона вторичного индуцированного излучения в слоях стромы насыщенных рибофлавином.
- применение сканирующего летающего пятная малого диаметра позволило впервые реализовать проведение персонализированного локального воздействвия по данным кератотопографических исследований;
- активация рибофлавина индуцированным вторичным излучением лазерным УФ излучением дальнего спектрального во всех 4-х пиках максимального поглощения рибофлавином, вместо только одного пика при традициннной технологии кросслинкигга с облучение УФ излучением с длиной волны 365 или 370 нм;
- не нарушает оксигенации в строме роговицы;
- сокращение времени облучения роговицы;
- большее поглощение вторичного индуцированного излучения в слоях
стромы с рибофлавином меньшая ответная асептическая воспалительная реакция и сокращение сроков эпителизации роговицы.
Предлагаемый способ кросслинкинга и устройство для его осуществления предполагают использование вторичного излучения для активации рибофлавина в слоях стромы насыщенных рибофлавином. При этом вторичное излучение может индуцироваться независимо от того, применяются абляционные или субабляционные плотности энергии в импульсе. Разница лишь в том, что при применении абляционных плотностей энергии по её завершению имеет место сопутствующий эффект кросслинкинга в слоях стромы, прилежащих к зоне абляции. Клинические наблюдения показали, что данный эффект в целом ряде случаев оказывается достаточным для профилактического кросслинкинкинга в эксимерлазерной хирургии роговицы и не требует дополнительного применения субабляционных режимов. При лечебном кросслинкинге при первиных и вторичных эктазиях роговицы, различных её заболеваниях, наряду с поверхностной рефракционной абляцией и абляцией изменённых поверхностных слоёв стромы возникает необходимость в усиление эфффекта кросслинкинга, без и с формированием Боуменоподобной мембранной структуры. Это может быть достигнуто дополнительным УФ лазерным воздействием при плотностях энергии в импульсе ниже порога абляции. В зависимости от тяжести эктазии и степени истончения роговицы показано выполнение кросслинкинга только с применением субабляционных плотностей энергии в импульсе.
В виду того, что иллюстрацию заявляемого способа лазер-индуцированного кросслинкинга излучением эксимерного лазера на аргон-фторе невозможно представить в виде рисунков или чертежей, то в примерах приводятся фотографии компьютерной оптической когерентной томографии и денситометрии роговицы пациентов, которым выполнялся кросслинкинг по заявляемому способу.
Способ проведения кросслинкинга роговицы и устройство для его осуществления иллюстрируется следующими примерами
Пример 1. Молодой человек, 22 лет.
Обратился с жалобами на снижение зрения на правом глазу
При проверке острота зрения правого глаза
0,1 с корр. Sph (-) 2,0 Cyl (-) 2,00 ax 70°= 0,5
При обследовании на приборе TMS-5 (Topcon) по данным кератотографиии и Шеймфлюг сканирования был выявлен кератоконус II степени на правом глазу. Индекс кератэктазии по Клайс 64%.
В режиме ФТК выполнена абляция эпителия на глубину 52 мкм, толщина которого определена по данным ОКТ роговицы. Оптическая зона абляции 7 мм, переходная 8,6 мм. После этого посредством ультразвукового небулайзайзера в течение 10 минут проведено насыщение роговицы 0,25% изотоническим раствором рибофлавина охлажденным до +5°C. Далее в течение 1 минуты было проведено облучение в оптической зоне 6,0 мм с переходной зоной до 7,6 мм. Это позволило избежать негативного влияния субаляционного облучения на эпителиальный край. Применялась плотность энергии 25 мДж/см2. Для быстрого перехода к данной плотности энергии в импульсе использовали ослабляющий оптический аттенюатор, который последовательно вводился и выводился из оптической системы доставки излучения к глазу в эксимерной лазерной офтальмологической установки “Профиль-500”. Было сделано 12600 импульсов, частота их следования составила 500 Гц, время облучения 56 секунд. Суммарная доза облучение не превысила 5,4 Дж/см2. С учётом перерасчёта на зону облучения она составила 3,6 Дж/cм2. На заключительном этапе была наложена мягкая контактная линза. Полная эпителизация под контактной линзой наступила через 48 часов. Первичный эффект такого способа эксимерлазерного кросслинкинга в строме роговицы был подтверждён при проведении оптической когерентной томографии (Рис.1.).
На рисунке 1 представлена ОКТ роговицы в контактной линзе с хорошо определяемой зоной первичного эффекта эксимерлазерного кросслинкинга через 24 часа после его проведения по поводу прогрессирующего кератоконуса II cт.
Через 6 дней после операции пациент отметил значительное улучшение зрения. Острота зрения на правом глазу 0,6 с корр. цилиндр (-) 2,0 ax 60° = 0,9. Больше на контрольные осмотры пациент не являлся в виду переезда в другой город.
Пример 2. Мужчина 42 лет. Диагноз: Кератоконус III на левом глазу, миопия средней степени, субклинический кератоконус на правом глазу. По поводу кератоконуса наблюдался в течение 10 лет, пользовался индивидульно изготовленной жесткой контактной линзой. В течение последних 6-ти месяцев отметил снижение зрения на левый глаз и дискомфорт при ношении контактной линзы.
Острота зрения правого глаза: 0,1 с корр. сфера (-) 4,00 D = 1,0
Острота зрения левого глаза: 0,05 с корр. Sph (-)10,50 Cyl (-) 6,00 ax 105°= 0,4
По данным компьютерной кератотопографии и оптического Шеймпфлюг сканирования на приборе TMS-5 (Topcon), оптической когерентной томографии роговицы на приборе RTVueXR100 (Optovue, Fremont, USA) отмечено прогрессирование кератоконуса на левом глазу. При последнем исследовании индекс кератоэктазии по Клайс на правом глазу 14%. на левом глазу 95%. На худшем левом глазу был выполнен лазер-индуцированный кросслинкинг на эксимерной лазерной офтальмологической установке “Микроскан-Визум”.
После абляции эпителия на глубину 50 мкм с оптической зоной 6,5 мм и переходной 8,4 мм было проведено насыщение стромы охлажденным до +6°С изотоническим 0,25% раствором рибофлавина в три этапа. После первого и второго этапа проводилось облучение субабляционными дозами излучения эксимерного лазера на аргон-фторе при плотности энергии в импульсе 16 мДж/см2 и частотой их следования 500 Гц. После третьего этапа облучение проводили при плотности энергии в импульсе 25 мДж/см2. Количество импульсов было рассчитано исходя из суммарной дозой облучения не превышающей 5,4 Дж/см2. На заключительном этапе была наложена лечебная мягкая контактная линза. Ответная асептическая воспалительная реакция на лазер-индуцированный кросслинкинг была слабо выражена. Полная эпителизация наступила через три дня, и контактная линза была удалена. Динамика остроты зрения до и в различные сроки после лазер-индуцированного кросслинкинга была следующей:
-исходная 0,05 с коррекцией сфера (-)10,5 дптр., цилиндр -6,0 дптр. ax 105° составила 0,4;
- через 7 повысилась до 0,4 и коррекции не поддавалась;
- через 14 дней 0,5 с коррекцией сфера (-) 3,25 дптр. повысилась до 0,6;
- через 1 месяц 0,1 с коррекцией сфера (-) 3,5 дптр. 0,9.
При контрольных обследованиях через 3, 6, 12 и 18 месяцев данные остроты зрения и коррекция не изменились. Пациент полностью перешёл на очковую коррекцию правого глаза сфера (-) 4,0 (острота зрения 1,0) и на левый глаз сфера (-) 3,5 дптр (острота зрения 0,9). Бинокулярная острота зрения 1,2.
Пример 3. Юноша 18 лет. Диагноз: Прогрессирующий кератоконус II степени на левом глаза, миопия средней степени обоих глаз.
Обратился с жалобами на ухудшение зрения на левый глаз в очках, которые не менял в течение последних 3-х лет.
По данным компьютерной кератотопографии и оптического Шеймпфлюг сканирования на приборе TMS-5 (Topcon), оптической когерентной томографии роговицы на приборе RTVueXR100 (Optovue, Fremont, USA) отмечено прогрессирование кератоконуса на левом глазу. На этом глазу был выполнен эксимерный лазер-индуцированный кросслинкинг по предлагаемому способу.
После эпибульбарной анестезии излучением эксимерного лазера с длиной волны 193 нм была проведена абляция эпителия в зоне 8,4 мм. После этого посредством ультразвукового небулайзера с меш-технологией диспрегирования раствора в течение 10 минут проведено насыщение стромы роговицы охлажденным 0,25% изотоническим раствором рибофлавина. Предварительно было рассчитано количество импульсов с суммарной дозой облучения не превышающей 5,4 Дж/см2. Полученное количество импульсов разделено на три равных этапа облучения с насыщением стромы охлажденным до +7°C 0,25% изотоническим раствором рибофлавина в течение 5 минут после каждого этапа. Далее переходили к сканированию деэпителизированной зоны роговицы летающим пятном с плотностью энергии в импульсе равной 25 мДж/см2 с частотой следования импульсов 500 Гц и частотой сканирования по площади равной 37 Гц. При таком режиме плотность энергии в импульсе была в два раза ниже пороговой. На заключительном этапе для формирования на абляционной поверхности Боуменоподобной мембранной структуры большей толщины была применена плотность энергии в импульсе 48 мДж/cм2. Кросслинкинг был проведён на эксимерной лазерной офтальмологической установке “Микроскан Визум -500”. Для перехода к субабляционной плотности энергии был применён специальный оптический аттенютиатор, который последовательно вводился и выводился из оптической системы доставки лазерного излучения к роговой оболочке. На первом этапе было выполнено 8995 импульсов. На втором этапе продолжили насыщение стромы роговицы вышеизложенным способом в течение 5 минут и вновь перешли к сканированию деэпителизированной зоны роговицы летающим пятном с плотностью энергии в импульсе равной 25 мДж/см2, сделано 8995 импульсов. Не третьем этапе насыщение в течение 5 минут 0,25% изотоническим раствором рибофлавина с последующим сканированием летающим пятном излучения эксимерного лазера с плотностью энергии в импульсе равной 25 мДж/см2, сделано также 8995 импульсов. На четвёртом заключительном этапе после насыщения 0,25% изотоническим раствором рибофлавина в течение 3-х минут было сделано 3200 импульсов с плотностью энергии 48 мДж/см2.
Первоначально на эксимерной лазерной офтальмологической установке по программе фототерапевтической абляции роговицы (ФТК) было выполнено удаление эпителия на глубину 56 мкм в зоне 8,4 мкм и в течение 10 минут проведено насыщение стромы роговицы 0,25% изотоническим раствором рибофлавина посредством ультразвукового небулайзера. Таким образом, суммарное время насыщения стромы роговицы рибофлавином составило 20 минут. После этого плотность энергии была переведена в субабляционный режим равный 25 мДж/см2. Время облучения субпороговыми дозами эксимерлазерного излучения с длиной волны 193 нм при частоте следования импульсов 500 Гц составило 95 секунд. Ранний послеоперационный период без особенностей, полная эпителизация и снятие контактной линзы через 48 часов.
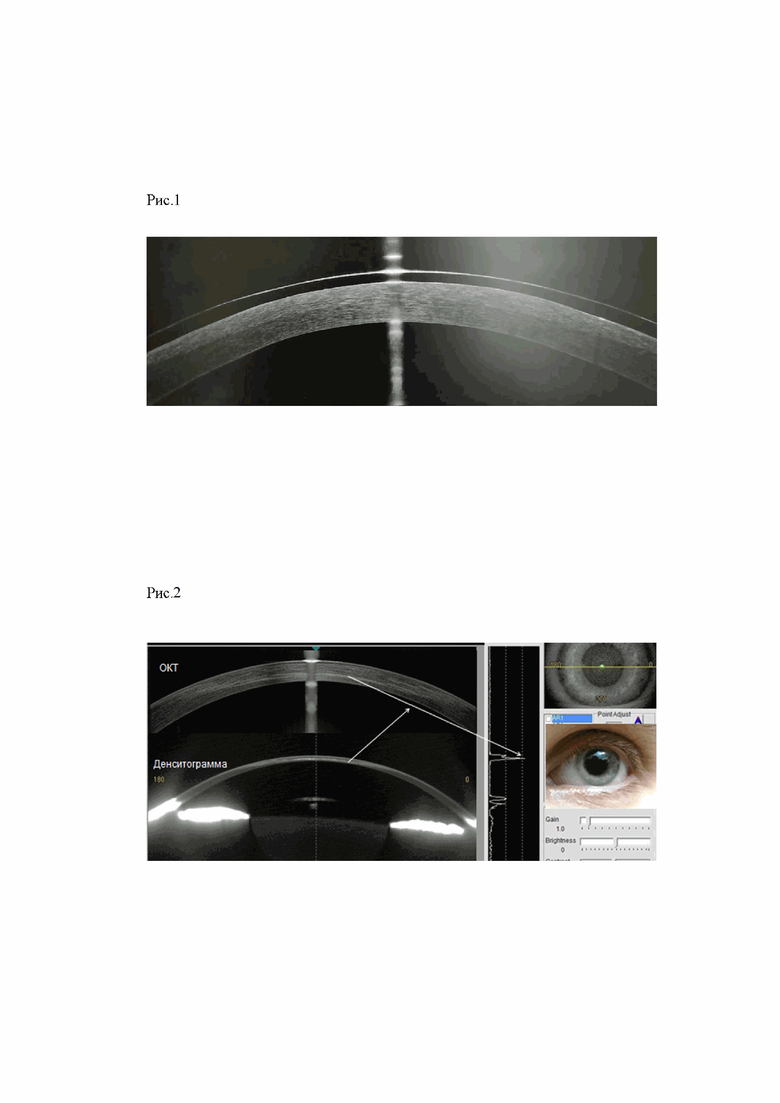
Через месяц при ОКТ и денситометрии роговицы были выявлена все классические признаки роговичного кросслинкинга (рис.2).
На рисунке 2 представлена ОКТ и денситограмма роговицы через 1 месяц после лечебного лазер-индуцированного кросслинкинга излучением эксимерного лазера на аргон-фторе, по-поводу прогрессирующего кератокнуса II степени.
Динамика остроты зрения на левом глазу после эксимерного лазер-индуцированного кросслинкинга была следующей:
- исходная 0,15 с коррекцией сфера (-)3,5 дптр. повысилась до 0,4;
- через 6 дней 0,2 с коррекцией сфера (-) 3,5 повысилась до 0,7;
- через 1 месяц 0,2 с коррекцией сфера (-) 3,5 дптр. 0,7;
При контрольных осмторах спустя 3, 6 и 12 месяцев осстрота зрения и коррекция не изменились
Пример 4. Девушка 23 лет, Диагноз кератоконус II ст. обоих глаз.
Обратилась с жалобами на ухудшение зрения на левый глаз.
По данным компьютерной кератотопографии и оптического Шеймпфлюг сканирования на приборе TMS-5 (Topcon), оптической когерентной томографии роговицы на приборе RTVueXR100 (Optovue, Fremont, USA) был выявлен кератоконус на обеих глазах.
Первоначально на эксимерной лазерной офтальмологической установке по программе фототерапевтической абляции роговицы (ФТК) было выполнено удаление эпителия на глубину 56 мкм в оптической зоне 6,5 мм с переходной зоной д.о 8,4 мкм После этого плотность энергии посредством откаллиброванного оптическогоо аттенюатора введенного в оптическую систему доставки излучения к роговице была переведена в субабляционный режим равный 25 мДж/см2. .В течение 10 минут проведено посредством ультразвукового небулайзера насыщение стромы роговицы 0,25% охлажденным до +7°С изотоническим раствором рибофлавина в два тапа по 10 минут Таким образом, суммарное время насыщения стромы роговицы рибофлавином составило 20 минут. По программе персонализированного сканирования роговицы по данным кератотопографии было выполнено сканирование в два этапа. Облучение проводили субпороговыми дозами эксимерлазерного излучения с длиной волны 193 нм при частоте следования импульсов 100 Гц . Общее время воздействия составило 175 секунд.
Через месяц при ОКТ и денситометрии роговицы были выявлена все классические признаки роговичного кросслинкинга.
Динамика остроты зрения на левом глазу до и в различные сроки после эксимерного лазер-индуцированного кросслинкинга была следующей:
- исходная 0,1 с корр. сфера (-) 3,0 дптр.  цил. (-) 4,0 дптр., ось 86º = 0,4;
цил. (-) 4,0 дптр., ось 86º = 0,4;
- через 6 дней 0,15 с корр. сфера (-) 2,0 дптр.  цил. (-) 3,0 дптр., ось 81º =0,5;
цил. (-) 3,0 дптр., ось 81º =0,5;
- через 1 месяц 0,2 с корр. сфера (-) 2,0 дптр.  цил. (-) 2,5 дптр., ось 82º = 0,6;
цил. (-) 2,5 дптр., ось 82º = 0,6;
- через 6 месяцев 0,2 с корр. сфера (-) 2,0 дптр.  цил. (-) 2,5 дптр., ось 83° = 0,6.
цил. (-) 2,5 дптр., ось 83° = 0,6.
Данные топографии и ОКТ роговицы стабильные.
Пример 5. Девушка, 29 лет. Обратилась для лазерной коррекции миопии средней степени на обоих глазах. На фоне ношения мягких контактных линз периодически возникали дискомфорт и покраснение глаз. Очки не устраивали по косметическим причинам.
Была проведена трансэпителиальная фоторефракционная кератэктомия с фотопротекицей и эффектом кросслинкинга с дополнительным формированием на абляционной поверхности Боуменоподобной мембранной структуры большей толщины. Для этого, по завершению абляционной абляции с предварительным насыщением 0,1% изотоническим раствором рибофлавина, было проведено дополнительное насыщение в течение 2-х минут 0,25% изотоническим раствором рибофлавина. Далее в оптической и переходной зона диаметром меньше на 1 мм было проведено воздействие излучением эксимерного лазера на аргон-фторе при плотности энергии в импульсе 48 Дж/см2, количество импульсов 4600. Полная эпителизация под контактной линзой через 2 дня. На ОКТ роговицы под эпителием определяется тонкая мембранная структура (Рис.3).
На рисунке 3 представлена ОКТ роговицы с полной эпителизацией под контактной линзой через 48 часов после ТрансФРК с рибофлавином. Под эпителием визуализируется тонкая мембранная структура.
Спустя месяц острота зрения на правом и левом глазу равна 1,0, бинокулярно 1.2, рефракция эмметропическая.
Источники информации.
1. Wollensak G, Spoerl E, Seiler T. Riboflavin/ultraviolet-a-induced collagen crosslinking for the treatment of keratoconus. Am J Ophthalmol 2003;135:620-627.
2. Konstantopoulos A et al. Corneal stability of LASIK and SMILE when combined with collagen cross-linking. Transl Vis. Sci. Technol., 2019 May 20;8(3):21.
3. Jin Rong Low, Li Lim*, Jane Chwee Wah Koh, Daniel Kai Peng Chua and Mohamad Rosman. Simultaneous Accelerated Corneal Crosslinking and Laser In situ Keratomileusis for the Treatment of High Myopia in Asian Eyes. The Open Ophthalmology Journal, 2018,12, (Suppl-1, M3)143-153.
4. Lang PZ, Hafezi NL, Khandelwal SS, Torres-Netto EA, Hafezi F, Randleman JB Comparative functional outcomes after corneal crosslinking using standard, accelerated, and accelerated with higher total fluence protocols. Cornea, 2019 38(4):433-441.
5. Brar S, Gautam M, Sute SS, Ganesh S. Refractive surgery with simultaneous collagen cross-linking for borderline corneas - A review of different techniques, their protocols and clinical outcomes. Indian J Ophthalmol 2020;68:2744-56.
6. Корниловский И.М., Бурцев А.А., Султанова А.И., Миришова М.Ф., Сафарова А.Н. Способ фоторефракционной абляции роговицы. Патент РФ №2578388 C1 с приоритетом от 21.10.2014.
7. Корниловский И.М., Годжаева А.М., Стегайло И.В. Локальная гипотермия в фоторефракционной хирургии. Офтальмология, 2005,2(2):5-12.
8. Стегайло И.В. Локальная гипотермия в фоторефракционной хирургии роговицы. Авт.Дисс….канд.мед.наук. М.2005., С.24.
9. Torres-Netto E.A., Kling S. The Role of Oxygen in Corneal Cross-Linking. In book: Controversies in the Management of Keratoconus (pp.83-86)
10. Jui-teng Lin The Role of Riboflavin Concentration and Oxygen in the Efficacy and Depth of Corneal Crosslinking. Investigative Ophthalmology & Visual Science September 2018, Vol.59, 4449-4450.
11. Theo G. Seiler; Maria A. Komninou; Malavika H. Nambiar; Kaspar Schuerch; Beatrice E. Frueh; Philippe Büchler. Oxygen kinetics during corneal crosslinking with and without supplementary oxygen. American Journal of Ophthalmology ( IF 4.013 ) Pub Date : 2020-11-21 , DOI: 10.1016/j.ajo.2020.11.001ю
12. Корниловский И.М. Cпособ абляции эпителия при фоторефракционных и фототерапевтических оперциях на роговице. Патент РФ на изобретение № 2718260 C1, с приоритетом от 27.12.2018.
13. Патент США - US20150313756A1). APPARATUS FOR CORNEAL CROSSLINKING International Publication Date WO 2017/070637 Al27 April 2017 (27.04.2017) P O P C T.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ФОТОРЕФРАКЦИОННОЙ АБЛЯЦИИ РОГОВИЦЫ | 2014 |
|
RU2578388C1 |
| СПОСОБ УДАЛЕНИЯ ЭПИТЕЛИЯ ПРИ ФОТОРЕФРАКЦИОННЫХ И ФОТОТЕРАПЕВТИЧЕСКИХ ОПЕРАЦИЯХ НА РОГОВИЦЕ | 2018 |
|
RU2718260C1 |
| Способ лечения кератоконуса, в том числе у пациентов с толщиной роговицы менее 450 микрон, методом ультрафиолетового кросслинкинга коллагена роговицы в сочетании с персонализированной трансэпителиальной фоторефракционной кератэктомией | 2023 |
|
RU2814093C1 |
| Способ коррекции аметропии у пациентов с I стадией кератоконуса | 2023 |
|
RU2801483C1 |
| СПОСОБ КАЛИБРОВКИ ОФТАЛЬМОЛОГИЧЕСКОГО ЛАЗЕРА ДЛЯ АБЛЯЦИИ РОГОВИЦЫ | 2022 |
|
RU2807869C1 |
| Способ лечения кератоконуса | 2018 |
|
RU2684472C1 |
| СПОСОБ ЛЕЧЕНИЯ КЕРАТОКОНУСА | 2016 |
|
RU2620757C1 |
| СПОСОБ ЛЕЧЕНИЯ КЕРАТОКОНУСА И ИНСТРУМЕНТ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2015 |
|
RU2602221C1 |
| Способ докоррекции остаточной миопической аметропии после ранее проведенных кераторефракционных операций | 2022 |
|
RU2786592C1 |
| СПОСОБ УЛЬТРАФИОЛЕТОВОГО КРОССЛИНКИНГА РОГОВИЦЫ С УЧЕТОМ ТОПОГРАФИЧЕСКОЙ ПАХИМЕТРИИ И КЕРАТОТОПОГРАФИИ У ПАЦИЕНТОВ С ТОНКОЙ РОГОВИЦЕЙ | 2020 |
|
RU2735377C1 |

Изобретение относится к медицине, а именно к офтальмологии, и может быть использовано при выполнении кросслинкинга роговицы. Для этого удаляют эпителий роговицы. Выполняют абляцию эпителия лазерным излучением дальнего ультрафиолетового диапазона с частотой следования импульсов 100-500 Гц, пятном не более 1,0 мм. Насыщают строму охлаждённым до +5-7°С изотоническим 0,1% или 0,25% раствором рибофлавина комбинированным капельно-аэрозольным способом с меш-технологией диспрегнирования раствора. Переходят к плотности энергии лазерного излучения ниже порога абляции стромы равной 16 мДж/см2, или 25 мДж/см2, или 48 мДж/см2. Проводят сканирование деэпителизированной зоны роговицы, отступив от эпителиального края не менее 0,5 мм. Суммарную дозу облучения рассчитывают по энергии в импульсе и их количеству, разбивают не менее чем на 3 этапа с насыщением стромы рибофлавином перед каждым этапом не более 5 мин. При этом ограничиваются одним этапом при профилактическом кросслинкинге с формированием мембранной структуры на абляционной поверхности роговицы. Изобретение обеспечивает возможность проведения персонализированного локального кросслинкинга роговицы. 3 ил., 5 пр.
Способ кросслинкинга роговицы путём удаления эпителия, насыщения стромы рибофлавином и её ультрафиолетового облучения, отличающийся тем, что выполняют абляцию эпителия лазерным излучением дальнего ультрафиолетового диапазона с частотой следования импульсов 100-500 Гц, пятном не более 1,0 мм, насыщают строму охлаждённым до +5-7°С изотоническим 0,1% или 0,25% раствором рибофлавина, используя комбинированный капельно-аэрозольной способ с меш-технологией диспрегнирования раствора, переходят к плотности энергии лазерного излучения ниже порога абляции стромы равной 16 мДж/см2, или 25 мДж/см2, или 48 мДж/см2, проводят сканирование деэпителизированной зоны роговицы, отступив от эпителиального края не менее 0,5 мм, суммарную дозу облучения рассчитывают по энергии в импульсе и их количеству, разбивают не менее чем на 3 этапа с насыщением стромы рибофлавином перед каждым этапом не более 5 мин и ограничиваются 1 этапом при профилактическом кросслинкинге с формированием мембранной структуры на абляционной поверхности роговицы.
| СПОСОБ ФОТОРЕФРАКЦИОННОЙ АБЛЯЦИИ РОГОВИЦЫ | 2014 |
|
RU2578388C1 |
| СПОСОБ УДАЛЕНИЯ ЭПИТЕЛИЯ ПРИ ФОТОРЕФРАКЦИОННЫХ И ФОТОТЕРАПЕВТИЧЕСКИХ ОПЕРАЦИЯХ НА РОГОВИЦЕ | 2018 |
|
RU2718260C1 |
| JP 3158398 U, 02.04.2010 | |||
| СУЛТАНОВА А.И | |||
| и др | |||
| Фотопротекция рибофлавином с эффектом кросслинкинга при фоторефракционной абляции роговицы | |||
| Вестник офтальмологии | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| БУРЦЕВ А.А | |||
| Фоторефракционная кератоабляция с фотопротекцией и эффектом кросслинкинга | |||
| Диссертация на | |||
Авторы
Даты
2024-07-01—Публикация
2021-12-15—Подача