Группа изобретений относится к медицине и медицинской технике и может быть использована в кардиологии, сердечно-сосудистой хирургии, флебологии, при рентген-эндоваскулярных вмешательствах для определения и оценки степени абляционного воздействия при проведении катетерных операций и обеспечении контроля при проведении малоинвазивных катетерных вмешательств в различных областях медицины.
Известен способ оценки уровня лазерного воздействия с помощью измерения разности потенциалов между электродами на кончике оптоволоконного абляционного катетера и/или снижению импеданса ткани во время лазерной абляции (за счет нагрева ткани) [Н. Weber, L. Schmitz, A. Heinze, L. Ruprecht, M. Sagerer-Gerhardt The Development of a laser catheter with improved monitoring of lesion formation during arrhythmia ablation // Nova Science Piblishers, Inc. 2017, P. 4-49].
Указанный способ является эмпирическим и косвенным, вынуждающим проводить анализ по недостаточно точным данным. Так, изменение импеданса может не наблюдаться при недостаточно плотном контакте электрода катетера с тканью, а также не всегда соответствует эффективной абляции миокарда; снижение амплитуды электрического потенциала не всегда наблюдается ввиду специфики расположения контактов электродов вне зоны повреждения лазерным лучом и технически сложной задачей размещения контактов электродов внутри зоны абляции. В связи с этим обратная связь во время проведения операции оказывается недостаточной и замедленной.
Также известен способ верификации гибели ткани и клеток in vivo, а также обнаружение остаточных жизнеспособных клеток в пределах зоны абляции (US 2009292211 от 26.11.2009 «Methods and Apparatus for Optical Spectroscopic Detection of Cell and Tissue Death»). Способ основан на регистрации спектра отраженного излучения и спектра флуоресценции никотинамидадениндинуклеотида (NADH) в тканях при радиочастотной абляции тканей.
Недостатком описанного способа является необходимость использования двух источников излучения определенного диапазона для возбуждения флуоресценции и получения отраженного спектра или дополнительного использования системы ультразвукового мониторинга.
Наиболее близким к заявляемому изобретению по использованию, технической сущности и достигаемому техническому результату являются способ и устройство мониторинга абляции тканей (WO 2016/073476 А1 от 12.05.2016 «SYSTEM AND METHOD FOR LESION ASSESSMENT»). Способ основан на регистрации спектра флуоресценции восстановленного NADH, возбуждаемой в тканях оптическим излучением с длиной волны от 300 до 400 нм и от 450 до 470 нм одновременно с оказанием абляционного воздействия. Излучение, возбуждающее флуоресценцию NADH, подводят через световод к месту оказания абляционного воздействия, которое может осуществляться оптическим, радиочастотным, термическим, акустическим, крио- и другими методами абляции. Излучение флуоресценции тканей принимается оптическим световодом и направляется на устройство спектрального анализа. Степень абляционного воздействия определяют по интенсивности сигнала флуоресценции и по ее динамике.
Устройство, реализующее способ, помимо источника энергии, оказывающей абляционное воздействие, содержит источники оптического излучения с длиной волны в диапазоне от 300 до 400 нм и от 450 до 470 нм, соединенные с оптическим световодом, доставляющим это излучение к месту абляционного воздействия, устройство спектрального анализа излучения, полученного от области абляционного воздействия. Устройство сконфигурировано таким образом, чтобы собирать и анализировать излучение флуоресценции, полученное от области абляционного воздействия.
Недостатки прототипа заключаются в следующем. Способ подразумевает использование как минимум двух источников излучения определенного спектрального диапазона для возбуждения флуоресценции, или же одного широкополосного источника совместно со спектральными фильтрами. Это усложняет конструкцию устройства и делает его неудобным при применении. Вследствие относительно малой интенсивности излучения флуоресценции предъявляются высокие требования к спектральной чувствительности прибора, регистрирующего спектр флуоресценции NADH. При недостаточной интенсивности сигнала флуоресценции возникает необходимость в продолжительном накоплении и осреднении замеров сигнала и, как следствие, это приводит к снижению быстродействия системы. При достаточно малых значениях интенсивности флуоресценции время накопления и обработки сигнала может быть соизмеримым с временем, необходимым для принятия решения о прекращении абляционного воздействия. В такой ситуации возможно чрезмерное воздействие и повреждение тканей. Компенсация указанных недостатков приводит к усложнению и удорожанию способа.
Техническим результатом заявленного изобретения является расширение арсенала технических средств для определения степени абляционного воздействия на биологические ткани.
Заявленный технический результат достигается использованием заявленного способа определения степени абляционного воздействия на биологические ткани, в соответствии с которым ткани, подвергаемые абляционному воздействию, освещают широкополосным светом видимого диапазона, измеряют интенсивность и спектральную характеристику света, обратно рассеянного от области абляционного воздействия, и степень абляционного воздействия на биологические ткани определяют по изменению в режиме реального времени интенсивности и спектральной характеристики света, обратно рассеянного от области абляционного воздействия.
Денатурирование белковых структур тканей в результате абляционного воздействия приводит к существенным изменениям оптических свойств тканей, в том числе, в видимом оптическом диапазоне. При катетерном вмешательстве, проводимом для абляции (деструкции) биологических тканей посредством лазерного, радиочастотного, криотермического, ультразвукового или иного воздействия, осуществляемого посредством введения катетера, освещение области абляционного воздействия широкополосным светом видимого диапазона, измерение в режиме реального времени интенсивности и спектральной характеристики сигнала, обратно рассеянного от области абляционного воздействия, позволяет определить степень абляционного воздействия на биологические ткани по изменению интенсивности и спектральной характеристики обратно рассеянного света.
Предпочтительно при проведении катетерной абляции с использованием лазерного излучения, доставляемого к тканям посредством световода, доставку широкополосного света видимого диапазона на область абляционного воздействия, а также прием обратно рассеянного от области абляционного воздействия оптического сигнала и передачу оптического сигнала на устройство измерения интенсивности и спектральной характеристики, осуществлять по упомянутому световоду.
Также для достижения заявленного технического результата заявлено устройство для оценки степени абляционного воздействия на биологические ткани, содержащее источник широкополосного света видимого диапазона, световод, соединенный с указанным источником света, выполненный с возможностью вывода световой энергии на область абляционного воздействия и приема обратно рассеянного от области абляционного воздействия оптического сигнала, и устройство измерения спектральных или фотометрических величин обратно рассеянного от области абляционного воздействия оптического сигнала.
Целесообразно в качестве устройства измерения спектральных или фотометрических величин использовать дисперсионный спектрометр.
При абляционном воздействии энергией лазерного излучения предпочтительно устройство, в котором световод доставки широкополосного света видимого диапазона на область абляционного воздействия одновременно является средством доставки упомянутой энергии лазерного излучения. Для реализации указанной функции устройство содержит оптическую систему, осуществляющую объединение энергии лазерного излучения, оказывающего абляционное воздействие, с излучением широкополосного света видимого диапазона, а также отделение обратно рассеянного от области абляционного воздействия оптического сигнала и его передачу на устройство измерения спектральных или фотометрических величин.
Оптическая система содержит светоделительный оптический элемент, дихроический оптический элемент, первый коллимирующий оптический элемент, второй коллимирующий оптический элемент, первый фокусирующий оптический элемент, второй фокусирующий оптический элемент, при этом источник широкополосного света видимого диапазона в направлении этого излучения оптически связан со световодом катетера последовательно через первый коллимирующий оптический элемент, светоделительный оптический элемент, дихроический оптический элемент и первый фокусирующий оптическим элемент; источник лазерного излучения в направлении этого излучения оптически связан со световодом катетера последовательно через второй коллимирующий оптический элемент, дихроический оптический элемент и первый фокусирующий оптическим элемент; световод катетера в направлении обратно рассеянного от области абляционного воздействия оптического сигнала и обратно прошедшего через световод катетера, оптически связан со входом устройства измерения спектральных или фотометрических величин последовательно через первый фокусирующий оптический элемент, дихроический оптический элемент, светоделительный оптический элемент и второй фокусирующий оптический элемент.
Сущность изобретения поясняется фигурой со схемой устройства для определения степени абляционного воздействия на биологические ткани.
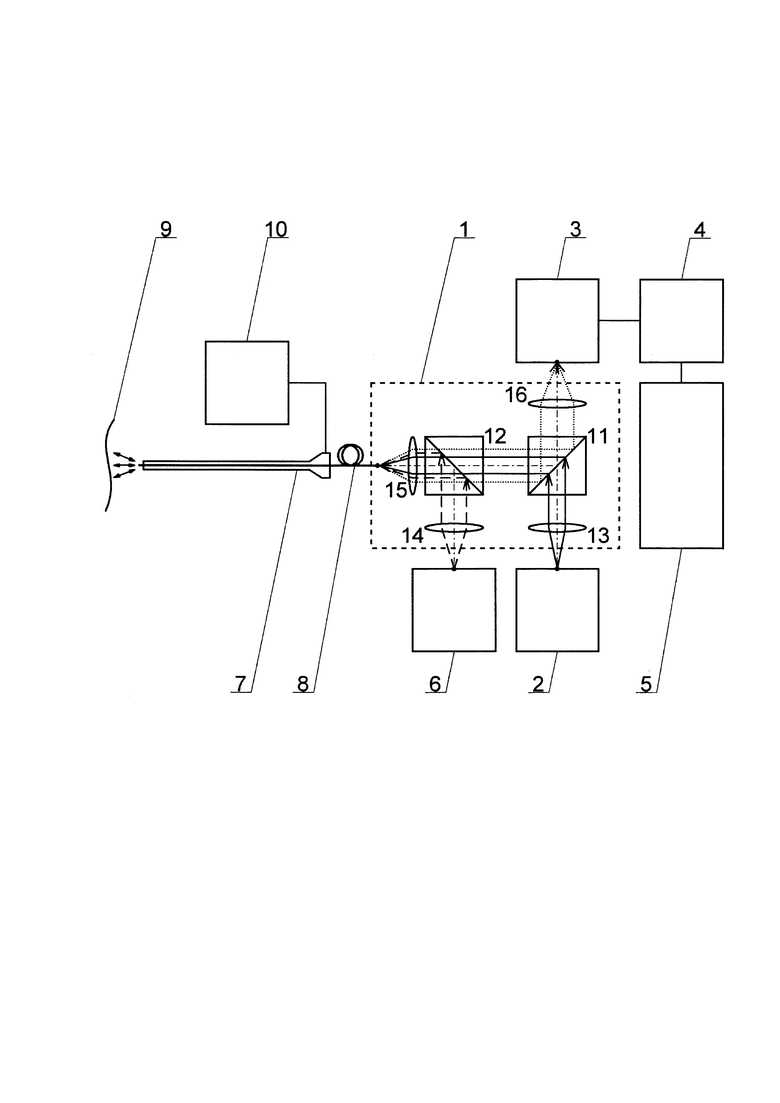
Устройство содержит оптическую систему 1, источник широкополосного света видимого диапазона 2, дисперсионный спектрометр 3 в качестве устройства измерения спектральных или фотометрических величин, вычислитель (ЭВМ) 4, а также дисплей 5 для отображения информации. Устройство для определения степени абляционного воздействия на биологические ткани применяется совместно с системой оказания абляционного воздействия на биологические ткани, содержащей источник лазерного излучения 6, катетер 7, имеющий в своем составе световод 8, подводимый к области абляционного воздействия 9, а также систему орошения 10, подающую орошающую жидкость в катетер 7.
Оптическая система 1, в свою очередь, содержит светоделительный оптический элемент 11, дихроический оптический элемент 12, первый коллимирующий оптический элемент 13, второй коллимирующий оптический элемент 14, первый фокусирующий оптический элемент 15, второй фокусирующий оптический элемент 16. Коллимирующие оптические элементы 13, 14 и фокусирующие оптические элементы 15, 16 могут быть выполнены в виде линзы, в т.ч. асферической, группы линз, линзовой склейки или зеркала, в т.ч. внеосевого параболического.
Оптические элементы 11-16 взаимно ориентированы и оптически связаны между собой таким образом, что:
1) Широкополосный свет видимого диапазона, излучаемый источником 2, коллимируется в параллельный пучок первым коллимирующим оптическим элементом 13 и направляется им на светоделительный оптический элемент 11, где большая его часть отражается и направляется через оптическую ось дихроического оптического элемента 12, прозрачного для широкополосного света видимого диапазона, на первый фокусирующий оптический элемент 15, который фокусирует свет и осуществляет его ввод в световод 8 катетера 7.
2) Лазерное излучение, излучаемое источником лазерного излучения 6, коллимируется в параллельный пучок вторым коллимирующим оптическим элементом 14 и направляется им на дихроический оптический элемент 12, отражающий лазерное излучение на первый фокусирующий оптический элемент 15, который фокусирует лазерное излучение и осуществляет его ввод в световод 8 катетера 7 совместно с широкополосным светом видимого диапазона.
3) Обратно рассеянный от области абляционного воздействия оптический сигнал, обратно прошедший через световод 8 катетера 7, коллимируется в параллельный пучок первым фокусирующим оптическим элементом 15 и через оптическую ось дихроического оптического элемента 12, прозрачного для широкополосного света видимого диапазона и отражающего лазерное излучение, направляется на светоделительный оптический элемент 11 и фокусируется вторым фокусирующим оптическим элементом 16 на вход дисперсионного спектрометра 3.
Дисперсионный спектрометр 3 подключен к вычислителю (ЭВМ) 4, который отображает информацию посредством дисплея 5.
Источник лазерного излучения 6, источник широкополосного света видимого диапазона 2, дисперсионный спектрометр 3, световод 8 катетера 7 подключают к оптической системе 1. Перед началом операции в катетер 7 с помощью системы орошения 10 подают орошающую жидкость, если это предусмотрено процедурой проведения операции. Широкополосный свет видимого диапазона, излучаемый источником 2, проходит через оптическую систему 1 и подключенный к ней световод 8 катетера 7 к месту абляционного воздействия 9 и освещают область абляционного воздействия 9. Обратно рассеянный от области абляционного воздействия оптический сигнал проходит через световод 8 и оптическую систему 1 на вход дисперсионного спектрометра 3. С помощью дисперсионного спектрометра 3 и вычислителя (ЭВМ) 4 производят замер спектральной или фотометрической характеристики обратно рассеянного от области абляционного воздействия оптического сигнала и отображают ее на дисплее 5. В момент, предшествующий началу абляционного воздействия, производят запись интенсивности и спектральной характеристики обратно рассеянного от области абляционного воздействия оптического сигнала, а результат измерения отражается на дисплее 5 и записывается. Затем начинают оказывать абляционное воздействие, при этом во время оказания абляционного воздействия в масштабе реального времени производят постоянную запись интенсивности и спектральной характеристики сигнала, обратно рассеянного от области абляционного воздействия, одновременно сравнивая текущую интенсивность и спектральную характеристику упомянутого сигнала с характеристикой, полученной в момент, предшествующий началу абляционного воздействия. Сравнение интенсивности и спектральной характеристики сигнала производят путем нормировки текущей характеристики по отношению к базовой характеристике, полученной в момент, предшествующий началу абляционного воздействия. Результаты сравнения непрерывно визуализируются в виде двумерного или трехмерного графика и непрерывно записываются. По динамике изменения результата сравнения оптических характеристик делают вывод о достаточности абляционного воздействия. Постепенное возрастание нормированной интенсивности и спектральной характеристики обратно рассеянного от области абляционного воздействия оптического сигнала по отношению к базовой характеристике ассоциируют с началом абляционного процесса, приводящего к денатурации белковых соединений и омертвению тканей. Стабилизацию нормированной интенсивности и спектральной характеристики обратно рассеянного от области абляционного воздействия оптического сигнала по отношению к базовой характеристике ассоциируют со стабилизацией степени приповерхностной абляции тканей и с началом распространения абляционного процесса вглубь тканей, при этом длительность абляционного воздействия при стабилизации упомянутой нормированной характеристики соотносят с глубиной распространения абляционного воздействия. Резкое изменение нормированной интенсивности и спектральной характеристики обратно рассеянного от области абляционного воздействия оптического сигнала по отношению к базовой характеристике ассоциируют с чрезмерным абляционным воздействием, приводящим к локальному обугливанию (карбонизации) тканей, вскипанием внутритканевой жидкости, разрушением тканей, локальным кровотечением и т.п. В случае начала резкого изменения нормированной интенсивности и спектральной характеристики обратно рассеянного от области абляционного воздействия оптического сигнала по отношению к базовой характеристике абляционное воздействие немедленно прекращают.
С использованием заявленной группы изобретений были проведены эксперименты Для экспериментов использовали свиные сердца со вскрытыми левым и правым желудочками, каждое сердце помещали в полимерный контейнер при комнатной температуре с 500 мл раствора NaCl 9%. Специально изготовленный лазерный катетер подключали к устройству определения степени абляционного воздействия, а от него к лазерному источнику. Выполняли постоянное орошение катетера раствором NaCl 9% через внутренний просвет с помощью перистальтического насоса со скоростью 10 мл/мин и со скоростью 40 мл/мин при абляции. Катетер устанавливали под углом 45-90 градусов на эндокардиальной поверхности, абляцию выполняли мощностью от 5 до 15 Вт, наносили от 6 до 9 аппликаций в левом и правом желудочках продолжительностью от 5 до 120 секунд. Во время каждой аппликации с помощью специально разработанного программного обеспечения проводили постоянный контроль спектра отраженного света от поверхности миокарда. Моменты увеличения амплитуды отраженного спектра, а также снижения амплитуды спектра более 10% отмечались. После каждой аппликации сердце обследовали для определения характеристик повреждения миокарда, измеряли диаметр и глубину каждого повреждения, а также площадь и объем повреждения с помощью формул. Проводили диссекцию миокарда через середину точек абляции, измерения диаметра и глубины повреждения проводили с помощью миллиметровой линейки. Всего было нанесено 30 аппликаций. Было отмечено, что рост амплитуды отраженного спектра строго соответствует изменению цвета области воздействия на белый. В то же время, резкое снижение амплитуды спектра строго соответствует обугливанию ткани внутри зоны воздействия. Обугливание происходило на всех испытанных мощностях воздействия (от 5 до 15 Вт), при этом длительность аппликации до момента обугливания укорачивалась при увеличении мощности воздействия.
В 18 случаях из 19 (94,7%) момент потемнения области воздействия (обугливания) сопровождался резким снижением амплитуды отраженного спектра - более 10% в течение 1 с. В то же время, в 26 из 30 (86,7%) случаев изменение цвета миокарда на белый в зоне воздействия сопровождалось значительным увеличением амплитуды отраженного спектра - более 10% за 3-4 с. Изменение цвета миокарда на белый сопровождалось повреждением более глубоких слоев миокарда на 1-5 мм.
Таким образом, проведенные с использованием заявленной группы изобретений экспериментальные исследования позволили с высокой вероятностью получить положительную обратную связь об эффективности лазерной аппликации (абляционное воздействие на миокард) и развивающимся негативном следствии перегрева миокарда - обугливании.
Группа изобретений позволяет расширить арсенал средств для определения и оценки степени абляционного воздействия при проведении катетерных операций и обеспечить контроль при проведении малоинвазивных катетерных вмешательств в различных областях медицины.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОЦЕНКА ВИДОИЗМЕНЕНИЯ ТКАНИ С ИСПОЛЬЗОВАНИЕМ ОПТОВОЛОКОННОГО УСТРОЙСТВА | 2007 |
|
RU2445041C2 |
| УСТРОЙСТВО ДЛЯ ОТОБРАЖЕНИЯ С ВЫСОКИМ РАЗРЕШЕНИЕМ И АНАЛИЗА ЭЛЕМЕНТОВ В ТВЕРДОМ ТЕЛЕ | 2011 |
|
RU2584375C2 |
| Способ лазерной деструкции патологических очагов проводящей системы сердца | 2018 |
|
RU2680916C1 |
| ОПТИЧЕСКИ КОГЕРЕНТНАЯ ТОМОГРАФИЯ И ОСВЕЩЕНИЕ С ИСПОЛЬЗОВАНИЕМ ОБЩЕГО ИСТОЧНИКА ОСВЕЩЕНИЯ | 2011 |
|
RU2580971C2 |
| Катетер для абляции биологической ткани | 2019 |
|
RU2816632C2 |
| КР-газоанализатор | 2021 |
|
RU2755635C1 |
| СПОСОБ ЛАЗЕРНОЙ АБЛЯЦИИ ПАТОЛОГИЧЕСКОЙ ОБЛАСТИ СЕРДЦА | 2016 |
|
RU2654764C2 |
| ОПТИЧЕСКАЯ ОЦЕНКА ПОРАЖЕНИЯ | 2013 |
|
RU2665022C2 |
| СПОСОБ ГИПЕРПИРЕКСИЧЕСКОГО ВОЗДЕЙСТВИЯ НА БИОТКАНИ ТРЕХРЕЖИМНЫМ ЛАЗЕРНО-ПОЛИХРОМАТИЧЕСКИМ ОБЛУЧАТЕЛЕМ | 2011 |
|
RU2458713C1 |
| УСТРОЙСТВО ВИЗУАЛИЗАЦИИ | 2010 |
|
RU2540090C2 |
Группа изобретений относится к медицине. Способ определения достаточности абляционного воздействия на биологические ткани включает освещение ткани, подвергаемой абляционному воздействию, световой энергией. Ткани, подвергаемые абляционному воздействию, освещают широкополосным светом видимого диапазона. В режиме реального времени измеряют интенсивность и спектральную характеристику оптического сигнала, обратно рассеянного от области абляционного воздействия. Производят сравнение интенсивности и спектральной характеристики сигнала путем нормировки текущей характеристики по отношению к базовой характеристике, полученной до начала абляционного воздействия. При резком изменении нормированной интенсивности и спектральной характеристики обратно рассеянного от области абляционного воздействия оптического сигнала по отношению к базовой характеристике абляционное воздействие прекращают. Устройство для осуществления способа содержит источник световой энергии, световод, соединенный с источником световой энергии, выполненный с возможностью вывода световой энергии на область абляционного воздействия и приема обратно рассеянного от области абляционного воздействия оптического сигнала, и средство измерения обратно рассеянного от области абляционного воздействия оптического сигнала. В качестве источника световой энергии используют источник широкополосного света видимого диапазона, а в качестве средства измерения обратно рассеянного от области абляционного воздействия оптического сигнала используют устройство измерения спектральных и фотометрических величин. Группа изобретений позволяет расширить арсенал средств для определения и оценки степени абляционного воздействия при проведении катетерных операций и обеспечить контроль при проведении малоинвазивных катетерных вмешательств в различных областях медицины. 2 н. и 5 з.п. ф-лы, 1 ил.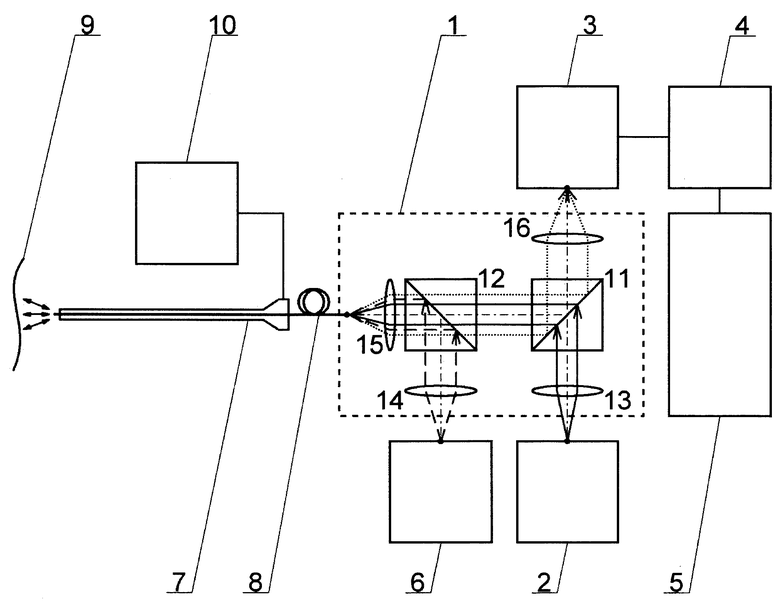
1. Способ определения достаточности абляционного воздействия на биологические ткани, включающий освещение ткани, подвергаемой абляционному воздействию, световой энергией, отличающийся тем, что ткани, подвергаемые абляционному воздействию, освещают широкополосным светом видимого диапазона; в режиме реального времени измеряют интенсивность и спектральную характеристику оптического сигнала, обратно рассеянного от области абляционного воздействия; производят сравнение интенсивности и спектральной характеристики сигнала путем нормировки текущей характеристики по отношению к базовой характеристике, полученной до начала абляционного воздействия; при резком изменении нормированной интенсивности и спектральной характеристики обратно рассеянного от области абляционного воздействия оптического сигнала по отношению к базовой характеристике абляционное воздействие прекращают.
2. Способ по п. 1, отличающийся тем, что при проведении катетерной абляции с использованием лазерного излучения, доставляемого к тканям посредством световода, доставку широкополосного света видимого диапазона на область абляционного воздействия, а также прием обратно рассеянного от области абляционного воздействия оптического сигнала и передачу оптического сигнала на устройство измерения интенсивности и спектральной характеристики, осуществляют по упомянутому световоду.
3. Устройство для осуществления способа по пп. 1, 2, содержащее источник световой энергии, световод, соединенный с источником световой энергии, выполненный с возможностью вывода световой энергии на область абляционного воздействия и приема обратно рассеянного от области абляционного воздействия оптического сигнала, и средство измерения обратно рассеянного от области абляционного воздействия оптического сигнала, отличающееся тем, что в качестве источника световой энергии используют источник широкополосного света видимого диапазона, а в качестве средства измерения обратно рассеянного от области абляционного воздействия оптического сигнала используют устройство измерения спектральных и фотометрических величин.
4. Устройство по п. 3, отличающееся тем, что в качестве устройства измерения спектральных и фотометрических величин используют дисперсионный спектрометр.
5. Устройство по п. 3, отличающееся тем, что при абляционном воздействии энергией лазерного излучения, световод доставки широкополосного света видимого диапазона на область абляционного воздействия одновременно является средством доставки упомянутой энергии лазерного излучения.
6. Устройство по п. 5, отличающееся тем, что оно содержит оптическую систему, осуществляющую объединение энергии лазерного излучения, оказывающего абляционное воздействие, с излучением широкополосного света видимого диапазона, а также отделение обратно рассеянного от области абляционного воздействия оптического сигнала и его передачу на устройство измерения спектральных и фотометрических величин.
7. Устройство по п. 6, отличающееся тем, что оптическая система содержит светоделительный оптический элемент, дихроический оптический элемент, первый коллимирующий оптический элемент, второй коллимирующий оптический элемент, первый фокусирующий оптический элемент, второй фокусирующий оптический элемент, при этом источник широкополосного света видимого диапазона в направлении этого излучения оптически связан со световодом катетера последовательно через первый коллимирующий оптический элемент, светоделительный оптический элемент, дихроический оптический элемент и первый фокусирующий оптический элемент; источник лазерного излучения в направлении этого излучения оптически связан со световодом катетера последовательно через второй коллимирующий оптический элемент, дихроический оптический элемент и первый фокусирующий оптический элемент; световод катетера в направлении обратно рассеянного от области абляционного воздействия оптического сигнала и обратно прошедшего через световод катетера, оптически связан с входом устройства измерения спектральных и фотометрических величин последовательно через первый фокусирующий оптический элемент, дихроический оптический элемент, светоделительный оптический элемент и второй фокусирующий оптический элемент.
| WO 2016073476 A1, 12.05.2016 | |||
| ОПТИЧЕСКАЯ ОЦЕНКА ПОРАЖЕНИЯ | 2013 |
|
RU2665022C2 |
| УСТРОЙСТВО ДЛЯ ЭНДОЛЮМИНАЛЬНОГО ЛЕЧЕНИЯ КРОВЕНОСНОГО СОСУДА | 2014 |
|
RU2557888C1 |
| УСТРОЙСТВО ДЛЯ МОНИТОРИНГА ОТНОСИТЕЛЬНОГО РАСПРЕДЕЛЕНИЯ ОТРАЖЕННОГО ОТ БИОЛОГИЧЕСКИХ ТКАНЕЙ ЛАЗЕРНОГО ИЗЛУЧЕНИЯ | 2017 |
|
RU2652965C1 |
| КАТЕТЕР ДЛЯ ДЕСТРУКЦИИ С ОПТИЧЕСКИ ПРОЗРАЧНОЙ ЭЛЕКТРОПРОВОДЯЩЕЙ ГОЛОВКОЙ | 2008 |
|
RU2473319C2 |
| СПЕКТРОГРАФ | 2016 |
|
RU2715485C2 |
Авторы
Даты
2024-07-01—Публикация
2022-06-24—Подача