Изобретение относится к области аналитической химии и может быть использовано в медицинских, ветеринарных и других биологических исследованиях для оценки биодоступности препаратов, моделирования процессов их растворения и всасывания, а также для изучения особенностей процессов пищеварения свиньи.
Известен состав для моделирования желудочного сока натощак FaSSGF, разработанный Дженнифер Дрессман (Dressman Jennifer, Institute of Pharmaceutical Technology, Johann Wolfgang Goethe University) и содержащий натрия таурохолат, лецитин, дигидрофосфат калия, хлорид калия, гидроксид натрия и воду деминерализованную (см. Е.А. Волкова, И.Е. Шохин, Г.В. Раменская, А.Ю. Савченко Биорелевантные среды растворения - современный инструмент для моделирования процессов растворения и всасывания ЛС. Биомедицина № 3, 2011, C. 135, табл. 2).
В качестве ближайшего аналога принята биорелевантная среда натощак, содержащая лецитин, хлорид калия и воду деминерализованную (см. Е.А. Волкова, И.Е. Шохин, Г.В. Раменская, А.Ю. Савченко Биорелевантные среды растворения - современный инструмент для моделирования процессов растворения и всасывания ЛС. Биомедицина № 3, 2011, C. 134, табл. 1).
Однако аналоги предназначены для моделирования кишечного сока человека in vitro, где на кинетику распада пищи влияют физиологические условия в пищеварительной системе, такие как механические силы, pH, температура и ферменты, наличие поверхностно-активных веществ пищи, а также свойства, такие как состав, массовая доля, текстура, структура и вязкость.
Задачей, на решение которой направлено заявляемое изобретение, является разработка биорелевантной среды желудка свиньи натощак.
Технический результат, проявляющийся при решении поставленной задачи, выражается в имитации желудочного сока свиньи in vitro натощак с высокой достоверностью.
Поставленная задача решается тем, что биорелевантная среда желудка свиньи натощак, содержащая лецитин, хлорид калия и воду деминерализованную, отличается тем, что дополнительно содержит желчь крупного рогатого скота, соляную кислоту и ферменты, в качестве которых используют пепсин, альфа-амилазу с концентрацией 800 ед/мл, протеазу с концентрацией 50000 ед/г, липазу с концентрацией 2000000 ед/г при следующем соотношении компонентов на 1 л воды деминерализованной:
Сопоставительный анализ признаков заявляемого изобретения с признаками прототипа и аналогов свидетельствует о соответствии заявляемого решения критерию «новизна».
При этом отличительные признаки формулы изобретения обеспечивают решение следующих функциональных задач.
Признак «дополнительно содержит желчь крупного рогатого скота, соляную кислоту и ферменты» позволяет с высокой достоверностью имитировать желудочный сок свиньи натощак.
Признаки «в качестве [ферментов] используют пепсин, альфа-амилазу с концентрацией 800 ед/мл, протеазу с концентрацией 50000 ед/г и липазу с концентрацией 2000000 ед/г» описывают тип и концентрацию используемых ферментов.
Признаки «при следующем соотношении компонентов на 1 л воды деминерализованной:
описывают оптимальное соотношение компонентов.
Заявляемый состав готовят на стандартном оборудовании по стандартной технологии.
Лецитин, хлорид калия, желчь крупного рогатого скота, ферменты, в качестве которых используют пепсин, а также альфа-амилазу, протеазу, липазу в заданной концентрации, и воду деминерализованную в заданном соотношении смешивают в общей емкости при температуре 20-25°С, в конце при перемешивании вносят соляную кислоту до достижения pH 1,6.
Авторы применяли заявляемую биорелевантную среду для определения содержания кормового микрокапсулированного витамина А (в форме ретинол ацетата).
Исследования проводили в несколько этапов на стандартном оборудовании.
1. Подготовка контрольного образца.
В мерную колбу объемом 100 мл вносят 20-25 мг аналитического или фармацевтического стандарта витамина А в форме ретинола ацетата, добавляют 50 мл изопропилового спирта и тщательно перемешивают содержимое до полного растворения указанного стандарта.
Полученный раствор доводят до метки изопропиловым спиртом, плотно закрывают пробкой и еще раз перемешивают.
Концентрация контрольного образца составляет приблизительно 0,250 мг/мл. Действительное значение концентрации витамина А в контрольном образце (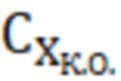 ), выраженное в мг/мл, вычисляют по формуле:
), выраженное в мг/мл, вычисляют по формуле:
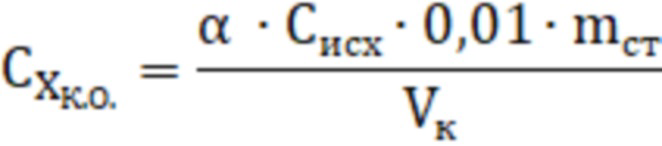
где 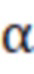 - активность витамина А в исходном аналитическом или фармацевтическом стандарте;
- активность витамина А в исходном аналитическом или фармацевтическом стандарте;
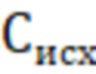 - концентрация витамина А в исходном аналитическом или фармацевтическом стандарте, указанная в сертификате качества, %;
- концентрация витамина А в исходном аналитическом или фармацевтическом стандарте, указанная в сертификате качества, %;
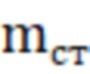 - масса навески аналитического или фармацевтического стандарта витамина А, взятая для приготовления контрольного образца, мг;
- масса навески аналитического или фармацевтического стандарта витамина А, взятая для приготовления контрольного образца, мг;
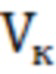 - объем колбы, использованной для приготовления контрольного образца, мл.
- объем колбы, использованной для приготовления контрольного образца, мл.
Срок годности контрольного образца составляет 14 дней в холодильнике.
1. Подготовка исследуемого образца включает 2 основные стадии.
1.1. Экспозиция кормового микрокапсулированного витамина А (в форме ретинол ацетата) в заявляемой биорелевантной среде при их соотношении 5,16 мг : 30 мл соответственно и постоянном перемешивании на биореакторе (например RTS-1) со скоростью 50 об/мин.
Параметры экспозиции витамина А в форме ретинол ацетата приведены в таблице 1.
Таблица 1
Параметры экспозиции витамина А в биорелевантных средах
1.1. Приготовление исследуемого образца из раствора витамина А в заявляемой биорелевантной среде.
Аликвоту раствора витамина А в заявляемой биорелевантной среде объемом 5 мл переносят в коническую колбу вместимостью 100 мл и добавляют 10 мл раствора, для приготовления которого в химическом стакане растворяют 1 г аскорбиновой кислоты в 10 мл воды для анализа, после чего аккуратно перемешивают так, чтобы вся проба была смочена внесенным раствором, далее вносят 20 мл раствора, для приготовления которого в химическом стакане 2 г гидроксида калия растворяют в смеси, состоящей из 2 мл воды для анализа и 18 мл.
Содержимое колбы тщательно, но аккуратно перемешивают, соединяют с обратным холодильником и подвергают омылению в течение 30 минут на водяной бане при температуре 55-60°С.
После охлаждения реакционной смеси до 20°С к полученному гидролизату добавляют 10 мл дистиллированной воды для анализа, содержимое колбы перемешивают, переносят в делительную воронку вместимостью 100 мл и подвергают двукратной экстракции двумя порциями гексана по 10 мл, тщательно ополаскивая очередным объемом экстрагента колбу, в которой проводился гидролиз. Продолжительность каждой экстракции - не менее 1 минуты.
Гексановые экстракты отделяют, объединяют в круглодонной колбе и упаривают досуха. Полученный сухой остаток незамедлительно растворяют в 10 мл изопропилового спирта и выдерживают в течение 10 минут в темном месте.
1. Отбор проб одинакового объема у контрольного и исследуемого образцов, их перенос в хроматографическую виалу и ввод в хроматограф по отдельности.
2. Проведение высокоэффективной жидкостной хроматографии.
Для разделения многокомпонентных смесей использовали жидкостный хроматограф высокого давления Shimadzu LC-20 Prominence HPLC (Shimadzu, Япония), оборудованный UV-VIS-детектором SPD-20A (Shimadzu, Япония) и обратнофазной колонкой Shodex. ODP2 HPG-4A (4.6 × 10 мм, размер частиц: 5 мкм; Shodex, Япония).
Термостатирование колонки проводили при 30 °С. Постоянный расход элюента составлял 0,4 мл/мин. Был использован следующий градиент элюции (элюент А - деионизованная вода с добавлением 0,1 % муравьиной кислоты; элюент B - ацетонитрил с добавлением 0,1 % муравьиной кислоты): 0 мин - 70% B, 0,1-1 мин - 70-0% B, 1-4 мин - 0-70% B, 4-5 мин - стабилизация колонки при 70% B. Регистрация UV-VIS-детектором проводилась при длине волны 328 нм (для определения витамина А). Объем впрыска образца составлял 10 мкл.
Строят хроматограммы проб контрольного и исследуемого образцов.
3. Обработка результатов измерений.
Количественное определение содержания витамина А в образцах проводят путем соотнесения площади пика на хроматограмме пробы исследуемого образца с аналогичными параметрами пика на хроматограмме пробы контрольного образца.
Массовую концентрацию витамина А в исследуемом образце (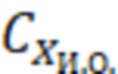 ), выраженную в мкг/мл, определяют по формуле
), выраженную в мкг/мл, определяют по формуле
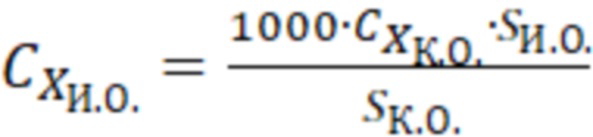 ,
,
где 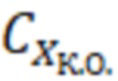 - действительное значение концентрации витамина А в контрольном образце, мг/мл;
- действительное значение концентрации витамина А в контрольном образце, мг/мл;
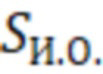 - площадь пика на хроматограмме пробы исследуемого образца;
- площадь пика на хроматограмме пробы исследуемого образца;
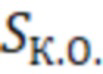 - площадь пика на хроматограмме пробы контрольного образца.
- площадь пика на хроматограмме пробы контрольного образца.
Массовую долю витамина А в исследуемом образце (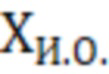 ), выраженную в МЕ/г, определяют по формуле
), выраженную в МЕ/г, определяют по формуле
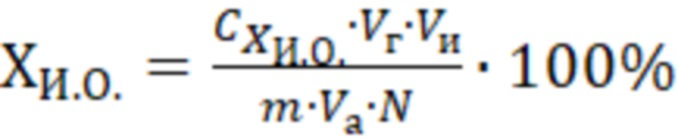 ,
,
где 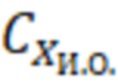 - массовая концентрация витамина А в исследуемом образце, мкг/ мл;
- массовая концентрация витамина А в исследуемом образце, мкг/ мл;
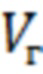 - суммарный объем гексана, используемого для экстракции (20 мл);
- суммарный объем гексана, используемого для экстракции (20 мл);
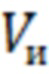 - объем изопропилового спирта, используемый для растворения сухого остатка (10 мл);
- объем изопропилового спирта, используемый для растворения сухого остатка (10 мл);
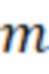 - масса навески исследуемого образца, г;
- масса навески исследуемого образца, г;
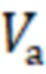 - объем аликвотной части гексанового экстракта, взятый для упаривания (1 мл);
- объем аликвотной части гексанового экстракта, взятый для упаривания (1 мл);
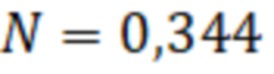 - фактор пересчета в международные единицы.
- фактор пересчета в международные единицы.
Результат измерения массовой доли витамина А в образцах, выраженный в МЕ/г, представляют в виде:
(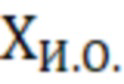 ±0,01·δ·
±0,01·δ·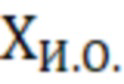 ),
),
где 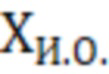 - массовая доля витамина А в исследуемом образце, МЕ/г;
- массовая доля витамина А в исследуемом образце, МЕ/г;
δ - относительная суммарная погрешность результатов измерений.
Режимные характеристики для подготовки образцов и результаты их исследований приведены в таблице 2.
Таблица 2
Режимные характеристики для подготовки образцов и результаты их исследований
По данным таблицы 2 можно сделать вывод, что после экспозиции кормового микрокапсулированного витамина А (в форме ретинол ацетата) в условиях биорелевантной среды желудка свиньи произошло растворение защитной оболочки микрокапсул и выделение витамина в среду, что свидетельствует об имитации физиологических условий желудочно-кишечного тракта свиньи и растворимости указанного препарата в данных условиях, аналогичное заключение можно сделать и при использовании известных биорелевантных сред.
Таким образом, заявляемый состав биорелевантной среды может быть использован для оценки биодоступности препаратов, моделирования процессов их растворения и всасывания, а также для изучения особенностей процессов пищеварения свиньи.
| название | год | авторы | номер документа |
|---|---|---|---|
| Биорелевантная среда желудка крупного рогатого скота натощак | 2023 |
|
RU2822252C1 |
| Биорелевантная среда желудка сельскохозяйственной птицы натощак | 2023 |
|
RU2822250C1 |
| Способ определения витамина А в форме ретинол ацетата в исследуемом образце | 2022 |
|
RU2825784C2 |
| Биорелевантная среда двенадцатиперстной кишки свиньи натощак | 2022 |
|
RU2799589C1 |
| Биорелевантная среда двенадцатиперстной кишки крупного рогатого скота натощак | 2022 |
|
RU2799319C1 |
| Биорелевантная среда кишечника крупного рогатого скота натощак | 2022 |
|
RU2799519C1 |
| ПИЩЕВАРИТЕЛЬНОЕ СРЕДСТВО НА ОСНОВЕ ФЕРМЕНТОВ МИКРОБНОГО ПРОИСХОЖДЕНИЯ | 2009 |
|
RU2429291C1 |
| ФЕРМЕНТЫ ДЛЯ ФАРМАЦЕВТИЧЕСКОГО ПРИМЕНЕНИЯ | 2005 |
|
RU2389504C2 |
| ПРИМЕНЕНИЕ АКТИВНЫХ ПРИ НИЗКОМ ЗНАЧЕНИИ pH АЛЬФА-1,4/1,6-ГЛИКОЗИДГИДРОЛАЗ В КАЧЕСТВЕ КОРМОВОЙ ДОБАВКИ ДЛЯ ЖВАЧНЫХ ЖИВОТНЫХ ДЛЯ УЛУЧШЕНИЯ ПЕРЕВАРИВАНИЯ КРАХМАЛА | 2021 |
|
RU2791882C2 |
| ПРИМЕНЕНИЕ АКТИВНЫХ ПРИ НИЗКОМ ЗНАЧЕНИИ pH АЛЬФА-1,4/1,6-ГЛИКОЗИДГИДРОЛАЗ В КАЧЕСТВЕ КОРМОВОЙ ДОБАВКИ ДЛЯ ЖВАЧНЫХ ЖИВОТНЫХ ДЛЯ УЛУЧШЕНИЯ ПЕРЕВАРИВАНИЯ КРАХМАЛА | 2017 |
|
RU2763378C2 |
Изобретение относится к области аналитической химии, а именно к биорелевантной среде желудка свиньи натощак. Биорелевантная среда желудка свиньи натощак, содержащая лецитин, хлорид калия и воду деминерализованную, согласно изобретению дополнительно содержит желчь крупного рогатого скота, соляную кислоту и ферменты, в качестве которых используют пепсин, альфа-амилазу с концентрацией 800 ед/мл, протеазу с концентрацией 50000 ед/г, липазу с концентрацией 2000000 ед/г при следующем соотношении компонентов на 1 л воды деминерализованной: лецитин – 0,75 мкМоль/л; хлорид калия – 7,7 г; соляная кислота – для обеспечения pH 1,6; вода деминерализованная – 1 л; желчь крупного рогатого скота – 5 г/л; пепсин – 3,9 г; альфа-амилаза с концентрацией 800 ед/мл – для обеспечения активности 8000; протеаза с концентрацией 50000 ед/г – для обеспечения активности 45000; липаза с концентрацией 2000000 ед/г – для обеспечения активности 1500000. Изобретение позволяет имитировать желудочный сок свиньи in vitro натощак с высокой достоверностью. 2 табл.
Биорелевантная среда желудка свиньи натощак, содержащая лецитин, хлорид калия и воду деминерализованную, отличающаяся тем, что дополнительно содержит желчь крупного рогатого скота, соляную кислоту и ферменты, в качестве которых используют пепсин, альфа-амилазу с концентрацией 800 ед/мл, протеазу с концентрацией 50000 ед/г, липазу с концентрацией 2000000 ед/г при следующем соотношении компонентов на 1 л воды деминерализованной:
| ВОЛКОВА Е.А | |||
| и др | |||
| Биорелевантные среды растворения - современный инструмент для моделирования процессов растворения и всасывания ЛС | |||
| Биомедицина | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Топочная решетка для многозольного топлива | 1923 |
|
SU133A1 |
| WO 2013144374 A1, 03.10.2013 | |||
| WO 2007054342 A1, 18.05.2007 | |||
| WO 2020201779 A1, 08.10.2020 | |||
| HENZE, L.J., et al | |||
| Development and evaluation of a biorelevant medium simulating | |||
Авторы
Даты
2024-07-03—Публикация
2023-12-11—Подача