Настоящее изобретение относится к экспериментальной медицине и биологии, в частности к созданию средств для перорального применения, содержащих биологически активное вещество - глутатион, которое защищено от деструктивного действия желудочного сока и обладающего энтеральной биодоступностью.
Глутатион представляет собой трипептид, синтезируемый на цитозольном уровне, который существует в клетках в восстановленной форме (тиол-восстановленный-GSH-) и в окисленной форме (дисульфид-окисленный). Антиоксидантная функция GSH привела к предположениям о его терапевтической роли при многочисленных хронических заболеваниях, характеризующихся изменением окислительно-восстановительного баланса и снижением уровня GSH, включая, например, нейродегенеративные расстройства, рак и хронические заболевания печени (Santacroce G, Gentile A, Soriano S, Novelli A, Lenti MV and Di Sabatino A Glutathione: Pharmacological aspects and implications for clinical use in non-alcoholic fatty liver disease. Front. Med., 2023, 10:1124275). Основной проблемой для широкого использования глутатиона в медицинской практике является его нестабильность к кислотному и ферментативному гидролизу в среде желудочного сока, в связи с чем в медицинской практике применяются в основном парентеральные, инъекционные формы глутатиона.
Глутатион в восстановленной форме (GluSH) и глутатион в окисленной форме (GluSSGlu) являются одной из важнейших физиологических систем антиоксидантной защиты клеток от токсического воздействия активных форм кислорода [О.А. Толпыгина Роль глутатиона в системе антиоксидантной защиты (обзор). Бюллетень ВСНЦ СО РАМН, 2012, №2 (84), Часть 2, С. 178-180].
Глутатион в настоящее время является одним из наиболее популярных компонентов для пищевых добавок. При пероральном приеме его значительная часть всасывается в тонком кишечнике, в то время как в желудке он не всасывается, а подвергается кислотному гидролизу и ферментативному лизису пепсином, находящимся в желудочном соке. Соответственно, биодоступность глутатиона при пероральном приеме в основном будет определяться степенью его защиты компонентами композиции биологически активной добавки от разрушающего действия желудочного сока (Valencia, Erick; Hardy, Gil. Practicalities of glutathione supplementation in nutritional support. Current Opinion in Clinical Nutrition and Metabolic Care 5(3):p 321-326, May 2002).
Чтобы биологически активные добавки к пище, содержащие глутатион, достоверно повышали содержание глутатиона в крови, его приходится применять в очень высоких дозах (до 1 г ежедневного приема) в течение длительного времени (до 6 месяцев). Это обусловлено в основном тем, что он быстро разрушается в желудочном соке и в тонкий кишечник, в котором он всасывается в системный кровоток, поступает лишь незначительная часть глутатиона от суммарно вводимой дозы (Richie, J.P., et al. Randomized controlled trial of oral glutathione supplementation on body stores of glutathione. Eur J Nutr 54, 251-263 (2015).
В последнее время появились сообщения о создании биологически активных пищевых добавок на основе модифицированного глутатиона. В частности, для повышения энтеральной биодоступности предлагается вместо глутатиона (GluSH) использовать S-ацетил-L-глутатион, который, по мнению авторов, является стабильным и легкоусвояемым при пероральном приеме [С.В. Орлова, Е.А. Никитин. Глутатион для защиты печени. Журнал для медицинских работников Терапия Эвалар, №1(6) от 30.11.2022 г., С.1 2-14].
Основным недостатком известных биологически активных пищевых добавок является то, что они содержат не глутатион (GluSH), а его ацетилированную по -SH группе форму. В настоящее время практически отсутствуют данные, подтверждающие биоэквивалентность глутатиона и его ацетилированной формы, особенно на клеточном уровне и в исследованиях in vivo. Возможно, что механизмы биологического действия этих веществ в системе in vivo не эквивалентны и существенно различаются.
На сегодняшний день известен большой ассортимент биологически активных добавок к пище, содержащих глутатион, обладающих выраженным общеукрепляющим действием, общим недостатком которых является их многокомпонентность, в которой невозможно выделить и оценить биологические эффекты глутатиона, его стабильность в желудочном соке и биодоступность в тонком кишечнике (патент RU 2538220 С1, опубл. 10.01.2015; патент RU 2751842 С2, опубл. 19.07.2021; патент RU 2588843 С2, опубл. 10.07.2016).
Заявляемые биологические эффекты представленных биологически активных пищевых добавок, содержащих глутатион, обусловлены большим количеством детально изученных с фармакологической точки зрения растительных экстрактов. В составе биологически активных добавок отсутствуют компоненты, которые препятствуют деструктивному действию желудочного сока на глутатион.
В медицинской практике глутатион, как в виде монокомпонента, так и в составе сложных фармацевтических композиций применяется исключительно парентерально, ввиду его нестабильности в среде желудочного сока.
Так, известна фармацевтическая композиция для парентерального капельного введения, предназначенная для лечения неинфекционных заболеваний печени. Предложенная композиция содержит комплекс активных веществ: 10-30 мг флавинадениндинуклеотида натрия, 100 мг никотинамидадениндинуклеотидфосфата, 60 мг пиридоксальфосфат гидрата, 1 мг метилкобаламина, 600-3000 мг глутатиона, 12,5 мг оротовой кислоты, 12,5 мг аденозина фосфата, 106 мг моноаммоний глицирризината (80 мг в пересчете на глицирризиновую кислоту), 750 мг L-метионина, 200 мг L-цистеин гидрохлорида, 800 мг L-глицина, 100-250 мг декспантенола, 1-3 мг биотина, 15 мг фолиевой кислоты, 25 мг альфа-липоевой (тиоктовой) кислоты, 25 мг убидекаренона, 1000 мг аскорбиновой кислоты и дистиллированную воду (патент RU 2720134 С1, опубл. 24.04.2020).
Недостатком фармацевтической композиции является возможность ее использования только для парентерального (внутривенного, капельного) введения.
Известен композит гексапептида со стабилизированной дисульфидной связью с веществом металлом, фармацевтические композиции для парентерального выведения на его основе, способы их получения и применения для лечения заболеваний на основе регуляции метаболизма, пролиферации, дифференцировки и механизмов апоптоза в нормальных и патологически измененных тканях. Композит включает соединение на основе окисленного глутатиона и вещества-металла в соотношении 3000:1 и 1:1, в котором вещество-металл включает металл, выбираемый из группы, состоящей из платины и палладия, при этом соединение на основе окисленного глутатиона может быть дериватом или солью, выбираемой из группы, состоящей из солей щелочных металлов, солей щелочноземельных металлов и солей переходных металлов (патент RU 2153350 С1, опубл. 27.07.2000). Недостатком известной композиции является отсутствие данных о биологической активности композита при пероральном введении.
Парентеральное введение лекарственных препаратов, особенно внутривенное введение, как правило, предусматривает кратковременные терапевтические схемы из-за сложности процедуры и высоких рисков инфицирования и тромбообразования.
Для предупреждения гидролиза глутатиона соляной кислотой и пепсином в желудке, глутатион содержащие композиции часто изготавливают в виде полимерных микропористых гранул, нерастворимых в желудке.
Например, известна твердая фармацевтическая композиция для перорального введения, содержащая L-цистеин в сочетании с одним или более дополнительными активными агентами, по меньшей мере, один из которых выбран из цистина, глутатиона и метионина, а также нетоксичный носитель. Фармацевтическую композицию изготавливают в виде полимерных микропористых гранул, нерастворимых в желудке. В качестве таких полимеров используют метакрилат, например, эудрагит RS или S, или этилцеллюлозу (ЭЦ). Полимерные микрогранулы содержат от 10 до 50 мас. % полимера (патент RU 2698196 С2, опубл. 23.08.2019).
Недостатком известной композиции является низкая эффективность глутатиона в составе сложной фармацевтической композиции, а также ее многокомпонентность и сложность изготовления.
Глутатион, равно как и другие компоненты, очень медленно диффундируют из полимерных микрогранул, так как в кишечнике нет ферментативных систем для их растворения и выход глутатиона определяется исключительно за счет неконтролируемой пассивной диффузии через микропоры, которая может приводить к неполному высвобождению глутатиона из микрогранул, большим потерям действующего вещества и, соответственно, низкой терапевтической эффективностью.
Наиболее близким к заявляемому средству - прототипом, является средство, содержащее глутатион и сывороточный протеин в массовом соотношении 1:1,25. Повышение стабильности и энтеральной биодоступности средства достигается тем, что глутатион находится в капсулах в комбинации с сывороточным протеином. Белки сывороточного протеина (α-лактальбумин, α-лактоглобулин и бычий сывороточный альбумин) при контакте с водой образуют высоковязкие гели с множественными межмолекулярными сшивками. Подобный гель сывороточного протеина защищает глутатион от действия кислой среды желудка и ферментативного лизиса пепсином, повышая его биодоступность за счет пролонгированного высвобождения в кишечнике (Zhang, S. et al. А. Polymerized Whey Protein Concentrate-Based Glutathione Delivery System: Physicochemical Characterization, Bioavailability and Sub-Chronic Toxicity Evaluation. Molecules 2021, 26, 1824). Известное средство получали путем смешивания сшитого сывороточного протеина с порошком глутатиона в массовом соотношении 1:1,25, перемешивания в течение 30 мин для полного взаимодействия с последующим помещением в капсулы. Предварительно получали концентрат сывороточного протеина в виде порошка, который растворяли в деионизированной воде и полученный раствор сывороточного протеина (8%, масс.) хранили при температуре 4°С в течение ночи для полной гидратации. Раствор сывороточного протеина возвращали к температуре окружающей среды и доводили рН до 7 с последующей термической обработкой при 80°С в течение 15 минут на водяной бане. Раствор сшитого сывороточного протеина получали путем быстрого охлаждения нагретого раствора сывороточного протеина в смеси вода-лед до комнатной температуры (25±1°С).
Недостатком известного средства является относительно невысокая защита глутатиона от ферментативного лизиса пепсином желудочного сока, так как сывороточный протеин является хорошим субстратом для пепсина и при высокой активности последнего быстро подвергается ферментативному лизису, в результате чего значительная часть глутатиона подвергается разрушению. В результате комплекс глутатиона с сывороточным протеином обладает низкой биологической эффективностью на моделях in vivo. Подобная система защиты глутатиона эффективна только в условиях пониженной кислотности желудочного сока в сочетании с недостаточной выработкой пепсина, что так же является недостатком средства прототипа.
Задачей настоящего изобретения является разработка средства, содержащего глутатион, обладающего повышенной стабильностью от разрушающего действия желудочного сока.
Технический результат: повышение стабильности и энтеральной биодоступности средства, содержащего глутатион.
Поставленная задача достигается предлагаемым средством, содержащим глутатион в комбинации с полиэтиленоксидом с мол. массой 6000 Да (ПЭО 6000) и танином, которые при контакте с водными средами (желудочный сок) образуют клейкую смолоподобную структуру, защищающую глутатион от разрушающего действия желудочного сока. Также в состав заявляемого средства дополнительно включены аскорбиновая кислота и рутин для защиты глутатиона от окисления, а также хитозан, дополнительно защищающий глутатион от кислотного гидролиза в желудочном соке. Заявляемое средство содержит вышеперечисленные компоненты в следующем количестве, в мас. %:
Назначение компонентов заявляемого средства:
1. Глутатион - основной биологически активный компонент.
2. Танин и полиэтиленоксид 6000 - комбинация этих веществ при контакте с водными средами (например, желудочный сок) образует клейкую смолоподобную структуру, которая обволакивает и объединяет все остальные сухие компоненты заявленного средства, включая глутатион и таким образом защищает глутатион от контакта с желудочным соком. При щелочных значениях рН (среда кишечника) смолоподобная структура комплекса танин - полиэтиленоксид медленно растворяется, высвобождая глутатион.
3. Аскорбиновая кислота и рутин - восстановители, препятствующие окислению глутатиона и повышающие стабильность средства при хранении
4. Хитозан низкомолекулярный (ТУ 9289-067-00472124-03, мМ 50-80 кДа) - за счет положительного заряда дополнительно нейтрализует соляную кислоту желудочного сока, защищая глутатион от кислотного гидролиза.
5. Целлюлоза микрокристаллическая - инертный наполнитель.
Предлагаемое средство получают путем смешивания порошкообразных компонентов. Заявляемое средство представляет собой порошкообразную субстанцию, из которой могут быть изготовлены таблетки, драже или она может быть расфасована в капсулы по известной технологии.
Для оценки биологической эффективности заявляемого средства в сравнении со средством прототипом использовали модель in vivo - циклофосфамидную миелосупрессию у мышей. Подобная модель позволяет оценить профилактическое действие глутатиона на глубину лейкопении и скорость восстановления уровня лейкоцитов в периферической крови при однократной в/б инъекции циклофосфамида в высокой дозе. В настоящее время инъекционные формы глутатиона используются в качестве дезинтоксикационного средства для лечения цитостатической миелосупрессии у онкологических больных при химиотерапии злокачественных новообразований (Манихас Г.М., Жукова Н.В. Применение препарата глутоксим у больных раком желудка, получающих платиносодержащую химиотерапию. Онкология. Журнал им. П.А. Герцена. 2012; 1(1):44-46). Однако, для пероральных форм глутатиона в современной научной литературе результатов подобных исследований нет. Выбор такой модели для оценки биологической эффективности заявленного средства in vivo был продиктован с одной стороны, возможностью оценить степень защищенности глутатиона в составе средства от деструкции желудочным соком, с другой стороны оценить энтеральную биодоступность и биологическую активность глутатиона при пероральном введении средства.
Материалы и методы: эксперимент был проведен на 20 самцах мышей линии ARC с массой тела 20-22 г, которые были разделены на 2 группы: 1 группа (моделирование цитостатической лейкопении + введение средства прототипа), 2 группа (моделирование цитостатической лейкопении + введение заявляемого средства). В качестве цитостатика использовали циклофосфамид в дозе 5 мг на 20 г веса мыши в 0,2 мл при внутрибрюшинном введении (в/б).
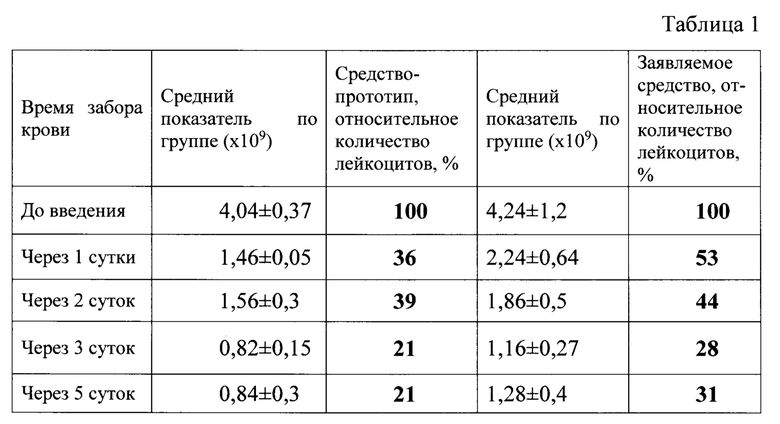
Для оценки эффективности средств с глутатионом проводили подсчет количества лейкоцитов в периферической крови. Для этого растворяли 20 мкл перефирической крови, взятой из хвостовой вены мыши в 0,4 мл 3% уксусной кислоте, подкрашенной метиленовым синим. Раствор помещали в камеру Горяева и, поместив ее под микроскоп, производили подсчет лейкоцитов в 100 больших квадратах. Динамику изменений количества лейкоцитов оценивали через каждые 24 часа. Данные по количеству лейкоцитов в периферической крови у мышей после внутрибрюшинного введения циклофосфана и перорального однократного введения заявляемого средства и средства прототипа представлены в таблице 1.
Как видно из представленных результатов, внутрижелудочное введение мышам защищенного от гидролиза (протеолиза) средства с глутатионом (присутствует комплекс полиэтиленоксида с танином) отчетливо снижает глубину цитостатической лейкопении, что свидетельствует о повышенной стабильности заявляемого средства в желудочном соке, относительно более высокой энтеральной биодоступности глутатиона в составе заявляемого средства и, соответственно более высокой биологической эффективностью заявляемого средства в сравнении со средством - прототипом.
Для подтверждения защищенности глутатиона от кислотной и ферментативной деструкции в среде желудочного сока были проведены исследования диффузии глутатиона в составе заявляемого средства в среды, имитирующие желудочный сок и среду тонкого кишечника.
Для имитации желудочного сока капсулы, содержащие заявляемое средство помещали в раствор фармацевтического препарата «Ацидин-пепсин», производства РУП «Белмедпрепараты» (0,5 таблетки на 50 мл воды) на 30 минут. После инкубации раствор сливали, капсулы двукратно ополаскивали дистиллированной водой, а затем помещали на 30 минут в 0,1 М трис-фосфатный буфер с рН 7,1 для имитации среды тонкого кишечника. Для анализа методом ВЭЖХ отбирали после 30 минутной инкубации пробы растворов, имитирующих желудочный сок и среду тонкого кишечника соответственно. Для среды, имитирующей среду тонкого кишечника, дополнительно отбирали пробы через 60 минут инкубации капсулы с заявленным средством. Все растворы перед анализом ВЭЖХ центрифугировала 5 минут при 12000 об/мин на центрифуге Eppendorf.
Высокоэффектиная жидкостная хроматография
Хроматографический комплекс Shimadzu LC-20 (Japan), объем пробы 20 мкл, колонка для проникающей хроматографии BioSep-SEC-S 3000 Phenomenex (USA), 75 × 7,80 мм, элюент - 0,1 М трис-фосфатный буфер с рН 7,1 и добавкой 0,05% лаурилсульфата натрия, скорость подачи элюента 1 мл/мин, давление 7,1 МПа
Спектрофотометрический детектор SPD-M20A, длина волны детектирования 210 нм. Изократическое элюирование до 10 минуты, с 10 по 20 минуту промывка колонки изократическим элюированием 5% уксусной кислоты, затем смена элюента на 0,1 М трис-фосфатный буфер с рН 7,1, содержащий 0,05% лаурилсульфата натрия и подготовка колонки к анализу изократическим элюированием в течение 10 минут. Общий цикл ВЭЖХ 30 минут. Время выхода пика глутатиона (контрольный раствор с расчетной концентрацией 3 мг/мл) составило 2,55 минут с площадью пика (S) 19943868. В пробе, имитирующей желудочный сок, глутатион не определялся и специфический пик со временем выхода 2,55 минут отсутствовал, в то время как в среде, имитирующей кишечный сок, пик глутатиона отчетливо определялся уже через 30 минут со временем выхода пика 2,55 минут и площадью пика (S) 8108850 (41% от максимального расчетного значения), а через 60 минут площадь пика (S) увеличилась до 18937118 (95% от максимального расчетного значения). Полученные результаты подтверждают, что заявляемое средство обеспечивает защиту глутатиона от деструктивного действия желудочного сока за счет образования смолоподобной структуры комплекса танин -полиэтиленоксид, затрудняющей диффузию глутатиона из средства в желудочный сок. При попадании средства в среду тонкого кишечника смолоподобная структура комплекса танин - полиэтиленоксид разрушается, за счет чего происходит достаточно быстрое высвобождение глутатиона. Уже через 30 минут инкубации капсулы с заявляемым средством в среде, имитирующей тонкий кишечник, высвобождается до 41%, а через 60 минут до 95% глутатиона.
Неочевидность заявляемого технического решения основана на том, что ни один из компонентов, входящих в заявляемое средство отдельно, не обладает способностью защищать глутатион от деструктивного действия желудочного сока, и не обеспечивает высокую энтеральную биодоступность глутатиона, обеспечивающую его специфическую биологическую активность на моделях патологических процессов in vivo. В настоящее время в научно-технической литературе отсутствуют сведения об использовании комплекса танин - полиэтиленоксид в качестве смолоподобного структурного компонента для связывания глутатион содержащих композиций и защите его от деструктивного действия желудочного сока. Заявляемое средство обладает более высокой биологической эффективностью по сравнению с прототипом. Выбор интервальных значений компонентов заявленного средства подобран экспериментально с учетом достижения максимальной энтеральной биодоступности и биологической эффективности глутатиона.
Предлагаемое средство может быть использовано в составе биологически активных добавок, что позволит повысить стабильность и энтеральную биодотупность глутатиона, а также расширить ассортимент стабильных глутатион содержащих композиций для перорального применения. Кроме этого, использование средства, содержащего глутатион, с повышенной стабильностью, позволит снизить стоимость целевого продукта, поскольку не потребуется специальных условий охлаждения для хранения, что также сказывается на большем удобстве при работе с заявляемым средством в процессе его использования.
Настоящее изобретение иллюстрируется следующими примерами конкретного исполнения.
Пример 1.
40 г глутатиона, 10 г танина, 2 г полиэтиленоксида с м.М. 6000, 6 г аскорбиновой кислоты, 6 г низкомолекулярного хитозана и 6 г рутина растирают в фарфоровой ступке до однородного гомогенного порошкообразного состояния, затем добавляют 30 г микрокристаллической целлюлозы и смесь тщательно гомогенизируют. Выход готового средства составляет 95% от расчетного.
Пример 2.
46 г глутатиона, 12 г танина, 3 г полиэтиленоксида с м.М. 6000, 7 г аскорбиновой кислоты, 7 г низкомолекулярного хитозана и 7 г рутина растирают в фарфоровой ступке до однородного гомогенного порошкообразного состояния, затем добавляют 18 г микрокристаллической целлюлозы и смесь тщательно гомогенизируют. Выход готового средства составляет 96% от расчетного.
Пример 3.
42 г глутатиона, 11 г танина, 2 г полиэтиленоксида с м.М. 6000, 6 г аскорбиновой кислоты, 6 г низкомолекулярного хитозана и 6 г рутина растирают в фарфоровой ступке до однородного гомогенного порошкообразного состояния, затем добавляют 27 г микрокристаллической целлюлозы и смесь тщательно гомогенизируют. Выход готового средства составляет 96% от расчетного.
Пример 4.
40 г глутатиона, 12 г танина, 3 г полиэтиленоксида с м.М. 6000, 7 г аскорбиновой кислоты, 7 г низкомолекулярного хитозана и 7 г рутина растирают в фарфоровой ступке до однородного гомогенного порошкообразного состояния, затем добавляют 24 г микрокристаллической целлюлозы и смесь тщательно гомогенизируют. Затем смесь таблетируют по известной технологии. Выход готового таблетированного средства составляет 96% от расчетного.
Пример 5.
46 г глутатиона, 10 г танина, 2 г полиэтиленоксида с м.М. 6000, 6 г аскорбиновой кислоты, 6 г низкомолекулярного хитозана и 6 г рутина растирают в фарфоровой ступке до однородного гомогенного порошкообразного состояния, затем добавляют 24 г микрокристаллической целлюлозы и смесь тщательно гомогенизируют. Затем смесь расфасовывают в желатиновые капсулы по 350 мг. Выход готового капсулированного средства составляет 95% от расчетного.
Предлагаемое средство может быть использовано в качестве готовой субстанции для включения в состав разрабатываемых новых биологически активных добавок и фармпрепаратов, в которых предусмотрено наличие глутатиона, а также в качестве самостоятельного средства с известной фармакологической активностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОВЫШЕНИЯ БИОДОСТУПНОСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2006 |
|
RU2328309C1 |
| ГЕПАТОПРОТЕКТОРНАЯ И АНТИГЕПАТОТОКСИЧЕСКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПЕЧЕНИ, ВКЛЮЧАЮЩИЙ ВВЕДЕНИЕ УКАЗАННОЙ КОМПОЗИЦИИ | 2008 |
|
RU2381800C1 |
| ПРЕПАРАТ, СОДЕРЖАЩИЙ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ЖЕЛЕЗА (III) И АКТИВНОЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОЕ ВЕЩЕСТВО | 2006 |
|
RU2394597C2 |
| Биологически активная добавка к пище и способ ее получения | 2023 |
|
RU2825783C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВИЧ-ИНФЕКЦИИ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 2012 |
|
RU2505286C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ КОМПОЗИЦИЯ | 2008 |
|
RU2410979C2 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ, ОБЛАДАЮЩАЯ ГЕПАТОПРОТЕКТОРНЫМИ И ИММУНОСТИМУЛИРУЮЩИМИ СВОЙСТВАМИ | 2012 |
|
RU2516932C2 |
| СУХОЙ КОНЦЕНТРАТ НАПИТКА ДЛЯ ВОССТАНОВЛЕНИЯ КОСТНОЙ ТКАНИ | 2023 |
|
RU2817886C1 |
| Способ выведения из организма солей тяжелых металлов | 2021 |
|
RU2777203C1 |
| ТРАНСПОРТИРУЮЩИЙ НАПОЛНИТЕЛЬ ДЛЯ ЭНТЕРАЛЬНОГО ПРИМЕНЕНИЯ | 2005 |
|
RU2377019C2 |
Изобретение относится к фармацевтической промышленности, а именно к стабильной глутатионсодержащей композиции для перорального применения. Предложена биологически активная добавка, включающая: 40-46 мас.% глутатиона в качестве биологически активного вещества; 10-12 мас.% танина и 2-3 мас.% полиэтиленоксида 6000 в качестве стабилизирующих компонентов; 6-7 мас.% аскорбиновой кислоты, 6-7 мас.% хитозана низкомолекулярного и 6-7 мас.% рутина в качестве дополнительных компонентов; целлюлозу микрокристаллическую в качестве наполнителя (до 100 мас.%). Изобретение обеспечивает повышение стабильности (от разрушающего действия желудочного сока) и энтеральной биодоступности средства, содержащего глутатион. 1 табл., 5 пр.
Биологически активная добавка, содержащая глутатион в качестве биологически активного вещества, отличающаяся тем, что также содержит танин и полиэтиленоксид 6000 в качестве стабилизирующих компонентов, аскорбиновую кислоту, хитозан низкомолекулярный и рутин в качестве дополнительных компонентов и целлюлозу микрокристаллическую в качестве наполнителя при следующем содержании компонентов, мас.%:
| Zhang S | |||
| Polymerized Whey Protein Concentrate-Based Glutathione Delivery System: Physicochemical Characterization, Bioavailability and Sub-Chronic Toxicity Evaluation / Molecules 2021, V | |||
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| Электрический поворотный выключатель | 1918 |
|
SU1824A1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ | 2013 |
|
RU2538220C1 |
| ТЕРМИНАЛЬНОЕ УСТРОЙСТВО, УСТРОЙСТВО БАЗОВОЙ СТАНЦИИ И СПОСОБ СВЯЗИ | 2018 |
|
RU2769717C2 |
| US 20100311837 A1, 09.12.2010 | |||
| КОМПОЗИЦИЯ ДЛЯ ПРЕДОТВРАЩЕНИЯ ГОЛОВНЫХ БОЛЕЙ | 2013 |
|
RU2698196C2 |
Авторы
Даты
2024-07-10—Публикация
2023-10-18—Подача