Данное изобретение относится к транспортирующему наполнителю, применяемому при энтеральном введении биологически активных соединений.
В данном описании, когда упоминаются или обсуждаются документ, акт или предмет знания, такое упоминание или обсуждение не могут рассматриваться как допущение, что данный документ, акт или предмет знания существовали на дату приоритета или же связаны с попыткой решить какую-либо задачу, связанную с данным описанием изобретения.
Основная цель доставки лекарства состоит в том, чтобы получить соответствующий биологический эффект в желаемом месте действия. Выбор состава лекарства может быть критически важным для его эффективности, поскольку биоактивность лекарства будет ниже оптимальной, если оно не обладает необходимыми физиолого-химическими свойствами для того, чтобы лекарство выделилось из состава в желаемом месте его действия.
Лекарства имеют различные формы, которые обычно классифицируются как энтеральные и парентеральные. Термин "энтеральные" означает лекарственные формы, которые поступают в организм через желудочно-кишечный тракт. Термин "парентеральный" означает все формы введения, где желудочно-кишечный тракт не участвует. Эта классификация подчеркивает тот факт, что при введении через желудочно-кишечный тракт возникают некоторые проблемы фармако-кинетического характера, которые не проявляются при парентеральных путях введения, в частности, метаболизм первого прохождения через печень. Как правило, формы введения существенно различаются, как показано в приведенной ниже таблице.
Энтеральная доставка предполагает введение лекарства через желудочно-кишечный тракт, где лекарство поглощается и доносится кровотоком к целевому месту действия. Лекарства, вводимые перорально, впитываются через кишечник, лекарства, вводимые трансбуккально, - через ротовую полость, а лекарства, вводимые ректально, - через прямую кишку.
Пероральная доставка зависит от пищеварительных процессов в желудочно-кишечном тракте. Когда состав перорального лекарства проглочен, он проходит через пищевод в желудок. Желудок выполняет три задачи:
(1) накопление, для которого верхняя часть желудка должна расслабиться и принимать большие объемы проглоченной пищи;
(2) соединение проглоченной пищи с пищеварительным соком, для чего нижняя часть желудка перемешивает эти вещества своим мышечным действием; и
(3) медленное опустошение содержимого желудка, которое выводится в тонкую кишку.
На опустошение желудка влияют несколько факторов, в том числе характер пищи (в основном содержание в ней жиров и белков) и степень мышечного действия опустошающегося желудка и тонкой кишки. По мере того, как пища переваривается в тонкой кишке и растворяется в пищеварительных соках, поступающих из поджелудочной железы, печени и кишечника, содержимое кишечника перемешивается и проталкивается вперед для осуществления дальнейшего пищеварения. Наконец, все переваренные питательные вещества всасываются через стенки кишечника. Непереваренные вещества выталкиваются в толстую кишку и выделяются из организма.
Нормальные пищеварительные процессы, которые регулируют степень доставки лекарства в целевое место, действие и удаление из него, следующие: (1) когда желудок выводит лекарство в тонкую кишку и (2) время, проводимое в кишечном тракте до всасывания. К сожалению, эти процессы невозможно регулировать. Однако, прописывая пациенту прием лекарства до, после или во время еды, можно регулировать эффективность этих процессов.
Химическая среда желудочно-кишечного тракта также имеет важное значение для доставки лекарства, принимаемого перорально. Лекарство должно иметь форму, стабильную при различных pH различных частей желудочно-кишечного тракта. Если лекарство образует неабсорбируемый комплекс или же химически или ферментативно разрушается, это уменьшает всасывание. Кроме того, для того чтобы всасываться, лекарство должно растворяться в жидкостях желудочно-кишечного тракта. При осаждении лекарства оно образует твердые частицы и тем самым выводится из раствора. Адсорбция на люминальные твердые частицы приводит к тому, что твердые частицы адсорбируют лекарство, то есть выводят его из раствора. Как осаждение, так и адсорбция уменьшают всасывание лекарства. Во многих случаях разрушения и образования комплексов можно избежать или, по крайней мере, свести его к минимуму химическим способом или подбором оптимального состава лекарства так, чтобы он не ограничивал усвояемость лекарства.
Кроме того, если лекарство всасывается через стенку кишечника или желудка, оно затем должно пройти через печень. Печень служит для того, чтобы выводить инородные соединения из организма. В результате значительная часть лекарства (например, 40-50%) может быть метаболизирована и быть выведена из организма до того, как она достигнет кровотока.
Воздействие печени при энтеральном введении можно уменьшить, если лекарство будет поглощаться через оболочку ротовой полости (трансбуккально/подъязычно) или оболочку прямой кишки (суппозитории), однако эти пути доставки не всегда целесообразны.
Роль состава лекарственного средства в доставке лекарства к его целевому месту действия нельзя игнорировать. Можно существенно увеличить биодоступность любого лекарства, изменив состав лекарственного средства, в которое оно входит. Поскольку для того, чтобы лекарство усваивалось из желудочно-кишечного тракта, оно должно быть в растворе, следует ожидать, что биодоступность лекарства уменьшается в следующем порядке: раствор>суспензия>капсула>таблетка>таблетка в оболочке. Этот порядок, возможно, не всегда соблюдается, но на него полезно ориентироваться.
Попытки увеличить биодоступность вводимых энтерально биологически активных соединений сводились либо к формированию пролекарств, например, морфина сульфата, либо к использованию наполнителей, улучшающих всасывание. Однако все еще существует потребность в составах для энтерального применения, которые бы еще более повысили биодоступность биологически активных соединений.
Сущность изобретения.
Установлено, что состав транспортирующего наполнителя, содержащий фосфаты агентов электронного переноса, повышает эффективность вводимых энтерально биологически активных соединений.
Согласно первому аспекту изобретения предлагается транспортирующий наполнитель, используемый при энтеральном введении биологически активных соединений, который содержит эффективное количество одного или более фосфатных производных одного или более агентов электронного переноса.
Данное изобретение предусматривает также использование эффективного количества одного или более фосфатных производных одного или более агентов электронного переноса, таких как фосфатные производные токоферола или токотриенола, вместе с другими наполнителями при изготовлении транспортирующего наполнителя для вводимых энтерально биологически активных соединений.
Данное изобретение предусматривает также фармацевтический состав, используемый для энтерального применения, который содержит одно или более одного биологически активных соединений, а также транспортирующий наполнитель, содержащий эффективное количество одного или более фосфатных производных одного или более агентов электронного переноса, таких как фосфатные производные токоферола или токотриенола.
Согласно второму аспекту изобретения предлагается способ повышения эффективности и улучшения транспорта вводимых энтерально биологически активных соединений, включающий операцию объединения биологически активного соединения с транспортирующим наполнителем, содержащим эффективное количество одного или более фосфатных производных одного или более агентов электронного переноса.
Предпочтительно фосфатное производное агента электронного переноса выбирается из группы, состоящей из фосфатных производных токоферола, фосфатных производных токотриенола и их смесей.
Согласно третьему аспекту изобретения предлагается способ повышения эффективности и улучшения транспорта вводимых энтерально биологически активных соединений, включающий операцию объединения биологически активного соединения с транспортирующим наполнителем, содержащим эффективное количество одного или более комплексов фосфатных производных агента электронного переноса.
Согласно четвертому аспекту изобретения предлагается транспортирующий наполнитель, используемый при энтеральном введении биологически активных соединений, который содержит эффективное количество одного или более комплексов фосфатных производных агента электронного переноса.
В одном предпочтительном варианте изобретения транспортирующий наполнитель и биологическое соединение представлены в форме, защищенной энтеросолюбильным покрытием. Энтеросолюбильное покрытие должно быть нерастворимо в желудке (низкий рН), быть стойким к ферментам слюны, но разрушаться в месте всасывания, которое находится сразу же за желудком, при рН выше 6. Обычно такое покрытие представляет собой водорастворимый полимер, такой как простой эфир целлюлозы, поливинилпирролидон или полиэтиленгликоль. Преимущество энтеросолюбильного покрытия заключается в том, что благодаря ему повышается вероятность того, что транспортирующий наполнитель и биологически активное соединение окажутся близко друг к другу в месте всасывания, что обеспечит максимальное влияние транспортирующего наполнителя на эффективность и транспорт биологически активного соединения. Например, таблетка или капсула могут иметь энтеросолюбильное покрытие, или же функциональное питание может содержать частицы в виде микрокапсул с энтеросолюбильным покрытием.
Термин "транспортирующий наполнитель" в том смысле, в каком он используется в данном описании, включает все формы для энтерального применения. Он включает (но не ограничительно) пилюли, таблетки, капсулы, жидкие составы, функциональное питание, пищевые добавки, лепешки, суппозитории.
Термин "эффективное количество" здесь обозначает количество одного или более фосфатных производных агента электронного переноса, которое помогает биологически активному веществу всасываться в количестве, дающем измеримый эффект, который заключается в уменьшении одного или более симптомов, имеющихся у пациента. Эффективное количество может составлять до 99,99% весовых от общего веса транспортирующего наполнителя. Специалист поймет, что фактическое количество будет различным в зависимости от биологически активного соединения.
Эффективного количества будет достаточно для доставки такого количества биологически активного соединения, которое находится в пределах терапевтического диапазона этого биологически активного соединения. Используемое эффективное количество будет зависеть также от того, используется ли фосфатное производное агента электронного переноса для усиления свойств лекарственного состава, например, растворимости или поверхностной активности.
Если фосфатное производное агента электронного переноса действует как усилитель растворимости, эффективное количество будет зависеть от концентрации лекарства в составе и может составлять от 40 до 90% весовых, предпочтительно от 45 до 75% весовых, еще более предпочтительно от 50 до 60% весовых. Если фосфатное производное агента электронного переноса не требуется для усиления растворимости, эффективное количество может быть в диапазоне от 0,01 до 20% весовых, предпочтительно от 1 до 15% весовых, еще более предпочтительно от 5 до 10% весовых.
Предпочтительно (когда свойства усиления растворимости не требуются) эффективное количество одного или более фосфатных производных агента электронного переноса находится в диапазоне от 0,1 до 10% весовых общего веса транспортирующего наполнителя. Более предпочтительно оно составляет от 5 до 10%, а наиболее предпочтительно - 7,5% весовых.
Термин "агенты электронного переноса" в данном документе означает класс химических соединений, которые могут быть фосфорилированы и которые (в нефосфорилированном виде) могут принимать электрон с образованием относительно стабильного молекулярного радикала или принимать два электрона, что позволяет соединению участвовать в обратимой окислительно-восстановительной системе. Среди примеров классов агентов электронного переноса, которые могут быть фосфорилированы, можно назвать гидроксихроманы, в том числе альфа-, бета-, гамма- и дельта-токолы в энантиомерной и рацемической формах; хинолы, которые являются восстановленными формами витамина К1 и убихинона; гидроксикаратиноиды, в том числе ретинол, кальциферол и аскорбиновую кислоту. Предпочтительно агент электронного переноса выбирается из группы, состоящей из токоферола и других токолов, ретинола, витамина К1 и их смесей.
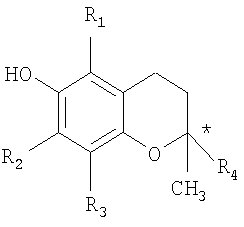
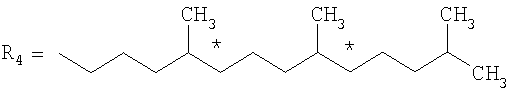
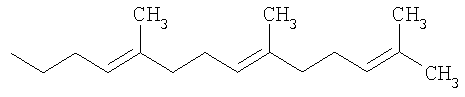
Более предпочтительно агент электронного переноса выбирается из группы, состоящей из токолов и их смесей. Токолы включают все изомеры производных 6:гидрокси-2:метилхромана (структурная формула приводится ниже), где R1, R2 и R3 могут быть водородом или метильными группами, то есть производными α-5:7:8-триметила, β-5:8-диметила, γ-7:8-диметила и δ-8-метила. У токоферолов R4 замещен 4:8:12-триметилтридеканом, а позиции 2, 4 и 8 (см.*) могут быть заняты стереоизомерами с R или S активностью или рацемическими. У токотриенолов R4 замещен 4:8:12-триметилтридека-3:7:11-триеновой группой, а позиция 2 может быть стереоактивной, например, она может быть занята стереоизомерами R или S, или рацемической. Более предпочтительным агентом электронного переноса является α-токоферол или токотриенол.
 ,
, 
Термин “фосфатные производные” используется здесь для обозначения кислотных форм фосфорилированных агентов электронного переноса, солей фосфатов, в том числе металлических солей, таких как натриевые, магниевые, калийные и кальциевые, а также любых других производных, в которых протон фосфата заменен на другие заместители, такие как этильные либо метильные группы или фосфатидильные группы. Термин включает смеси фосфатных производных, особенно полученные в результате реакций фосфорилирования, а также каждое из фосфатных производных по отдельности. Например, термин включает смесь монотокоферилфосфата (TP) и дитокоферилфосфата (T2P), а также TP и T2P по отдельности. Смеси, пригодные для использования, описаны в международной патентной заявке № WO 02/40033.
Предпочтительно одно или более фосфатных производных одного или более агентов электронного переноса выбирается из группы, состоящей из монотокоферилфосфата, дитокоферилфосфата, монотокотриенилфосфата, дитокотриенилфосфата и их смесей. Более предпочтительно одно или более фосфатных производных одного или более агентов электронного переноса представляет собой смесь, состоящую из одного или более из следующих соединений: монотокоферилфосфат, дитокоферилфосфат, монотокотриенилфосфат и дитокотриенилфосфат.
В некоторых ситуациях возникает необходимость использовать такое фосфатное производное, как фосфатид, обладающий дополнительными свойствами, например, лучшей растворимостью в воде. Фосфатидильные производные являются аминоалкильными производными органических фосфатов. Эти производные можно получить из аминов, имеющих структуру R1R2N(CH2)nOH, где n - целое число от 1 до 6, а R1 и R2 могут представлять собой либо H, либо короткие алкильные цепи с 3 или менее атомами углерода. R1 и R2 могут быть одинаковыми или различными. Фосфатидильные производные получают путем замещения гидроксильного протона агента электронного переноса фосфатом, который затем реагирует с амином, таким как этаноламин или N,N-диметиламин, с образованием фосфатидильного производного агента электронного переноса. В одном из методов получения фосфатидильных производных используется основный растворитель, такой как пиридин или триэтиламин с хлорокисью фосфора, для получения промежуточного соединения, которое затем реагирует с гидроксигруппой амина с образованием соответствущего фосфатидильного производного, такого как дигидрофосфат Р-холила Р-токоферила.
В некоторых ситуациях, если требуются дополнительные свойства, такие как повышенная стабильность или улучшенная доставка, могут использоваться также комплексы фосфатных производных агентов электронного переноса.
Термин "комплексы фосфатных производных" обозначает продукт реакции одного или более фосфатных производных агентов электронного переноса с одним или несколькими комплексообразующими агентами, выбранными из группы, включающей амфотерные поверхностно-активные вещества, катионные поверхностно-активные вещества, аминокислоты с азотными функциональными группами, а также белки, богатые такими аминокислотами, как описано в международной патентной заявке № WO 02/40034, включенной в данный документ путем отсылки.
Предпочтительные комплексообразующие агенты выбираются из группы, состоящей из аргинина, лизина и третично-замещенных аминов, например, следующей формулы:
NR1R2R3,
где R1 выбирается из группы, включающей смешанные алкильные радикалы с прямой или разветвленной цепью от С6 до С22 и их карбонильные производные;
R2 и R3 независимо выбираются из группы, содержащей H, CH2COOX, CH2CHOHCH2SO3X, CH2CHOHCH2OPO3X, CH2CH2COOX, CH2COOX, CH2CH2CHOHCH2SO3X или CH2CH2CHOHCH2OPO3X, причем X представляет собой H, Na, K или алканоламин, при условии, что R2 и R3 оба не являются H; и
где, если R1 представляет собой RCO, то R2 может быть CH3, а R3 может быть (CH2CH2)N(C2H4OH)-H2CHOPO3, либо R2 и R3 вместе могут быть
N(CH2)2N(C2H4OH)CH2COO-.
Предпочтительные комплексообразующие агенты включают аргинин, лизин или лаурилиминодипропионовую кислоту, где комплексообразование происходит между основным центром на азоте и сложным эфиром фосфорной кислоты с образованием стабильного комплекса.
Термин "биологически активное соединение" используется в данном документе для обозначения соединений, оказывающих биологическое действие на людей или животных при медицинских или ветеринарных применениях. Биологически активные соединения включают фармацевтические препараты, пищевые добавки, лекарства, витамины, косметические средства, нутрацевтики, питательные вещества и другие полезные для здоровья добавки, применяемые для профилактики или лечения людей или животных. Примеры биологически активных соединений включают, но не ограничительно, наркотические анальгетики, такие как морфин и леворфанол, ненаркотические анальгетики, такие как кодеин и ацетаминофен, кортикостероиды, такие как кортизон, анестетики, такие как пропофол, противорвотные средства, такие как скополамин, симпатомиметические средства, такие как адреналин и допамин, антиэпилептические средства, такие как фосфенитоин, противовоспалительные средства, такие как ибупрофен, тиреоидные гормоны и антитиреоидные средства, в том числе тироксин, фитохимические средства, в том числе α-биcаболол, эвгенол, силибин, изофлавоны сои, иридоид-гликозиды, в том числе аукубин и каталпол, сесквитерпен-лактоны, в том числе псевдогваянолид, получаемый из арники Шамиссо, терпены, в том числе розмариновая кислота и розманол, фенолгликозиды, в том числе салицилаты салицин, салигенин и салициловая кислота, тритерпены таксастерол или α-лактуцерол и изолактуцерол, производное p-гидроксифенилуксусной кислоты тараксозид, производные гидрохинона, в том числе арбутин, фенилалканоны, в том числе гингеролы и шогаолы, гиперцин, статины и ацилфлороглюциды, в том числе ксантогумол, лупулон, гумулон и 2-метилбут-3-ен-2-ол.
Примеры питательных веществ и нутрацевтиков включают витамины, молекулы-прекурсоры, важные для образования гормонов, минеральные добавки, белки, аминокислоты, экстракты растений, такие как экстракт семян винограда, эфедрин, дегидроэпиандростерол, изофлавоны, фитостеролы и подобные им биоагенты. Биологические активное соединение может также быть пептидом, полипептидом или протеином. Биологически активное соединение может быть в любой пригодной форме, включая фосфатные производные.
Специалисту будет понятно, какие другие наполнители можно включить в транспортирующий наполнитель. Выбор других наполнителей зависит от характеристик биологически активного соединения. Среди примеров других наполнителей можно назвать растворители, поверхностно-активные вещества, мягчители, консерванты и т.п. Выбор других наполнителей зависит также от формы введения лекарства.
Краткое описание чертежей
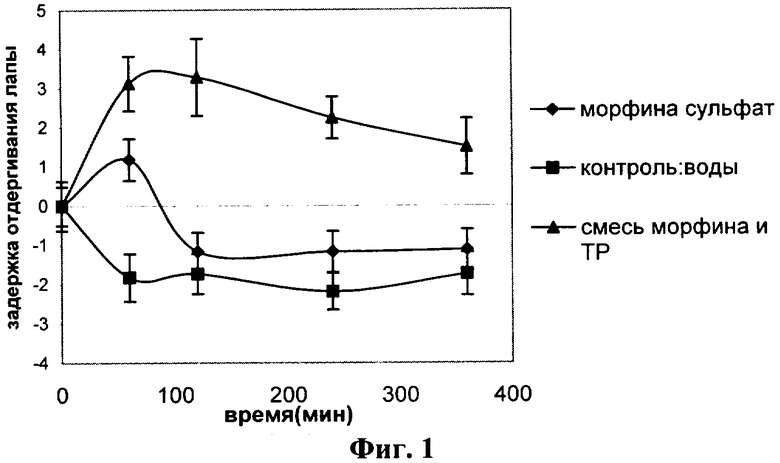
Фиг.1: Влияние сульфата морфина в дозе 5 мг/кг, морфина с транспортирующим наполнителем токоферилфосфатом, соответствующим изобретению, в дозе 5 мг/кг и контроля на замедление отдергивания лапы у крыс; испытания проводились в течение 3 часов (совокупные данные).
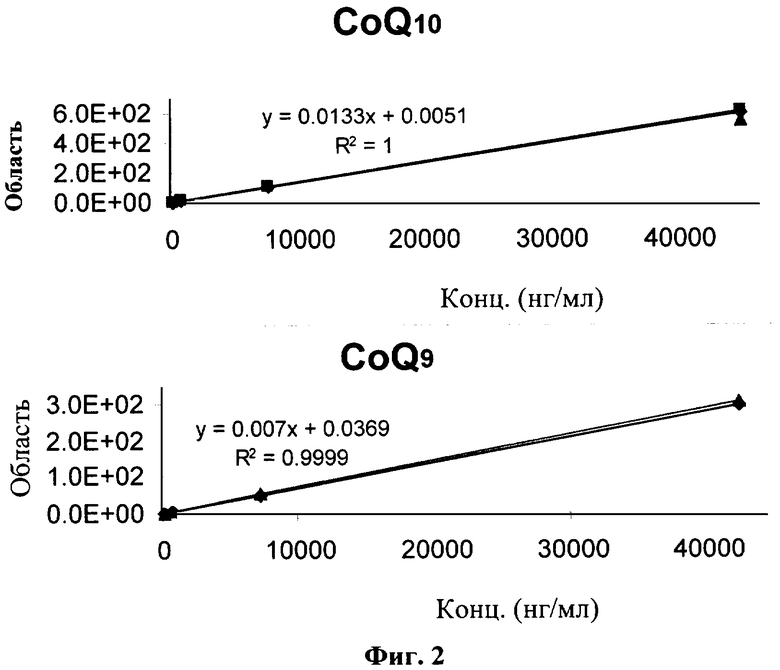
Фиг.2: Стандартные кривые CoQ10 и CoQ9
Примеры
Ниже мы объясняем и иллюстрируем изобретение на конкретных примерах, не носящих ограничительного характера.
Пример 1
В данном эксперименте сравнивали эффективность состава с морфином, соответствующего настоящему изобретению, с эффективностью морфина сульфата, часто применяемого препарата с морфином для энтерального применения. Эффект измеряли, сравнивая время отдергивания лапы в ответ на приложение тепла у крыс, получавших и не получавших морфин.
Материалы
Животные: Девять находящихся в сознании крыс Sprague-Dawley весом каждая 350-450 граммов.
Группы составов:
1. Контроль: вода.
2. Морфина сульфат.
3. Морфин с TPm: морфин HCl (14%) в транспортирующем наполнителе, содержащем воду (59%) и токоферилфосфатную смесь (TPm) (27%). Смесь TPm содержала монотокоферилфосфат и дитокоферилфосфат.
Составы 2 и 3 разбавили водой, доведя конечную концентрацию морфина до 5 мг/мл. Например, 0,357 грамма состава 3 смешали с 0,643 грамма воды, получив конечную концентрацию морфина 5%. Этот жидкий состав затем вводили животным через желудочный зонд.
Метод
В эксперименте использовали девять крыс, разделенных на 3 группы. После первого введения состава крысам давали отдохнуть, а затем каждой группе вводили другой состав. Процесс повторяли, пока каждая крыса не получала каждый из трех составов.
Воду, морфина сульфат и морфин с TPm вводили через желудочный зонд в дозе 5 мг/кг веса тела. Тест на обезболивание проводили через 1, 2, 4 и 6 часов, каждый раз измеряя задержку отдергивания лапы три раза у каждой крысы (по крайней мере, с пятиминутным интервалом, если использовали одну и ту же лапу).
Использовался подошвенный анальгезиометр, предназначенный для быстрой и эффективной оценки уровня обезболивания у мелких лабораторных животных. Это устройство служит для прикладывания источника тепла (~45°C от инфракрасного излучения) к задней лапе животного и измерения времени, через которое оно отдернет лапу (задержка отдергивания лапы). Источник тепла (пластина) обеспечивает постоянную температуру поверхности, которая контролируется встроенным термометром с точностью 0,1°C; имеется также таймер с точностью 0,1 секунды. Животное помещают на нагревательную пластину, окруженную прозрачной акриловой клеткой, и прослеживают реакцию отдергивания лапы. Увеличенное время реакции служит показателем обезболивания. Каждое животное тестировали 3 раза в каждой временной точке (т.е. каждой одной крысе прикладывали тепло к задней лапе три раза в каждой временной точке).
Результаты представлены на фиг.1. Как морфина сульфат, так и морфин в токоферилфосфатном транспортирующем наполнителе вызывали увеличение задержки реакции, что указывает на обезболивание. Морфин в токоферилфосфатном транспортирующем наполнителе давал более длительную задержку, которая сохранялась дольше, чем при использовании морфина сульфата. А именно морфин, вводимый в транспортирующем наполнителе, соответствующем изобретению, давал устойчивый обезболивающий эффект в течение периода длительностью до 2 часов после орального введения, тогда как морфина сульфат обеспечивал обезболивающий эффект только в течение первого часа. Стандартные планки погрешностей на точках графика накладываются друг на друга только во временной точке 1 час, где водный раствор морфина сульфата и состав морфина с TPm имели аналогичное действие. В более поздних временных точках состав морфина с TPm давал устойчивое обезболивание.
Статистический анализ: Сравнение между морфина сульфатом и морфином с TPm:
- через 60 мин t=2,598 (p<0,02).
- через 120 мин t=4,815 (p<0,0005).
- через 240 мин t=4,351 (p<0,001).
- через 360 мин t=3,094 (p=0,005).
Выводы
Использование транспортирующего наполнителя TPm давало стойкое обезболивание в течение более длительного периода, чем использование морфина в виде морфина сульфата. Хотя результаты не были значимыми во временной точке 1 час, состав с TPm показал статистическую значимость во всех более поздних временных точках.
Пример 2
В этом примере исследуется биодоступность для морских свинок препарата CoQ10, вводимого в следующих составах:
A. CoQsol
B. CoQsol плюс TPM в масле триглицерида со срединной цепью (MCT)
C. Масло МСТ (контроль)
Материалы и методы
Составы
Токоферилфосфатная смесь (TPM), содержащая монотокоферилфостфат (TP) и дитокоферилфосфат (T2P) в весовом соотношении 2:1, была изготовлена фирмой Phosphagenics Ltd.
Препарат CoQsol был приобретен у фирмы Doctor's Trust Vitamins, США.
Триглицерид со срединной цепью (MCT) был изготовлен Abitec Corp, США.
Составы состояли из следующего:
A. CoQsol: Каждая мягкая гелевая капсула содержит 60 мг CoQ, причем маслянистое содержание каждой пилюли составляет 0,44 мл по объему. Следовательно, концентрация CoQ равна 60 мг/0,44 мл=136 мг CoQ/мл содержимого капсулы. Каждый миллилитр состава CoQsol содержит также 136 МЕ d-α-токоферола и 3705 МЕ витамина A. Наполнителями являются масло из рисовых отрубей, желатин, глицерин, вода, пчелиный воск, экстракт аннато и двуокись титана.
B. CoQsol+TPM: состав приготавливали с такой концентрацией CoQ, чтобы доза 30 мг/кг вводилась в одном и том же объеме относительно веса тела для группы экспериментальных животных, т.е. в объемах приблизительно 0,21 мл на кг веса тела. Каждый миллилитр состава содержал CoQ и TPM, оба в концентрации 140 мг/мл, с МСТ в качестве разбавителя.
C. MCT: (среда): контрольная группа получала МСТ в дозировке 0,21 мл/кг веса тела.
Животные
Взрослые морские свинки (самки) были приобретены в Animal Services, Монашский университет, и акклиматизировались в ведомственном виварии не менее 5 дней до начала эксперимента. Животных случайным образом распределили на группы (n=10), пометили уникальными идентификационными метками на спинках (выбритая шерсть и цветовые коды) и разместили по группам в загон размером приблизительно 1х·4 м с обогащенной окружающей средой. Средний вес тела животных, получавших CoQsol, в день 0 составлял 0,795 кг. Средний вес тела в группе CoQsol+TPM в день 0 был 0,746 кг. Средний вес тела в контрольной группе в день 0 был 0,796 кг.
Пища и вода: Стандартный лабораторный гранулированный корм для кроликов и морских свинок (Barastoc, Австралия). Воду давали без ограничений.
Способ введения и метод дозировки: животные получали составы через желудочный зонд с дозировкой с помощью пластиковой канюли, прикрепленной к подающему шприцу, в объемах приблизительно 0,21 мл на кг веса тела.
Методы
Доза CoQsol: 30 мг/кг веса тела/день.
Доза TPM: 30 30 мг/кг веса тела/день.
Режим введения: один раз в день.
Период введения: 26 дней.
Вес тела измеряли еженедельно.
По завершении периода введения составов свинок умерщвляли асфиксией с использованием газа CO2. Кровь собирали пункцией сердца в трубки с гепарином, центрифугировали для отделения плазмы и хранили при -80°C до экстрагирования CoQ.
Экстрагирование CoQ и анализы путем жидкостной хроматографии высокого давления проводили в основном методом, описанным в работе Aberg и др. (1992) "Распределение и окислительно-восстановительное состояние убихинонов в тканях крыс и человека", Arch. Biochem. Biophys. 295: 230-34.
Повышенные уровни CoQ10 и CoQ9 свидетельствуют об увеличении биодоступности и усвоения. Измерялись как CoQ9, так и CoQ10, поскольку морские свинки могут синтезировать обе формы CoQ (9 и 10). Поэтому важно оценивать уровни обеих этих форм после введения, так как введение CoQ10 может увеличивать оба уровня in vivo.
Результаты:
Приведенные выше результаты не включают какой-либо статистической информации, поскольку, как известно специалистам в области питательных микроэлементов, всегда существуют значительные расхождения между отдельными животными, так как каждое животное имеет различную потребность в CoQ10, и он поглощается только в том случае, если эта потребность не удовлетворена. Большая вариабельность между животными приводит к высоким цифрам стандартного отклонения, которые неточно отражают значение результатов.
На фиг.2 представлены стандартные кривые, полученные при анализе CoQ10 и CoQ9 в плазме до прогонки образцов на жидкостном хроматографе высокого давления (чем ближе r2 к 1, тем точнее результаты).
Обсуждение
Результаты, представленные на фиг.2 и в приведенных выше таблицах, показывают, что уровни CoQ в плазме выше у животных, получавших CoQsol+TPM, чем у животных, получавших CoQsol или контроль. Это свидетельствует, что смесь токоферилфосфатов увеличивает биодоступность CoQ10.
Слова "содержащий" или "включающий" и их формы, используемые в данном описании и формуле изобретения, не ограничивают заявляемого изобретения и не исключают какие-либо его варианты и дополнения.
Модификации и усовершенствования изобретения будут очевидны специалистам. Такие модификации и усовершенствования будут входить в объем изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТРАНСПОРТИРУЮЩИЙ НАПОЛНИТЕЛЬ, СОДЕРЖАЩИЙ ОДИН ИЛИ БОЛЕЕ ДИ И/ИЛИ МОНО-(ЭЛЕКТРОННЫЙ ПЕРЕДАЮЩИЙ АГЕНТ) ФОСФАТНЫХ ПРОИЗВОДНЫХ ИЛИ ИХ СОЕДИНЕНИЙ | 2006 |
|
RU2434643C2 |
| АЛКАЛОИДНЫЕ СОСТАВЫ | 2005 |
|
RU2477136C2 |
| СОСТАВЫ, ОБЛАДАЮЩИЕ ЛИПИДОПОНИЖАЮЩИМИ СВОЙСТВАМИ | 2006 |
|
RU2428973C2 |
| СОСТАВЫ, ОБЛАДАЮЩИЕ АНТИКАНЦЕРОГЕННЫМИ СВОЙСТВАМИ | 2006 |
|
RU2435580C2 |
| КОМПОЗИЦИЯ НОСИТЕЛЯ | 2010 |
|
RU2577233C2 |
| КОНТРОЛИРУЕМОЕ ВЫСВОБОЖДЕНИЕ ФЕНОЛЬНЫХ ОПИАТОВ | 2007 |
|
RU2469038C2 |
| СИНТЕТИЧЕСКОЕ АНАЛЬГЕТИЧЕСКОЕ СРЕДСТВО ПЕПТИДНОЙ ПРИРОДЫ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2017 |
|
RU2656188C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РАКА И ВИРУСНЫХ ЗАБОЛЕВАНИЙ, СПОСОБ ЛЕЧЕНИЯ РАКА, СПОСОБ ЛЕЧЕНИЯ ВИРУСНЫХ ИНФЕКЦИЙ НА ЕЕ ОСНОВЕ | 1996 |
|
RU2177316C2 |
| АЛЬБУМИН-СВЯЗЫВАЮЩИЕ ПРОЛЕКАРСТВА НА ОСНОВЕ ПРОИЗВОДНЫХ АУРИСТАТИНА Е | 2018 |
|
RU2795101C2 |
| СОСТАВ И СПОСОБ ПОЛУЧЕНИЯ АНАЛЬГЕТИЧЕСКОГО СРЕДСТВА ПЕПТИДНОЙ СТРУКТУРЫ | 2017 |
|
RU2669386C1 |
Изобретение относится к области фармацевтики и касается использования транспортирующего наполнителя для энтерального применения биологически активных веществ, содержащего эффективное количество одного или более фосфатных производных одного или более агентов электронного переноса. Изобретение позволяет повысить эффективность и улучшить транспорт вводимых энтерально биологически активных соединений. 6 н. и 12 з.п. ф-лы, 2 ил.
1. Способ повышения эффективности и улучшения транспорта вводимых энтерально биологически активных соединений, включающий объединение биологически активного соединения с транспортирующим наполнителем, содержащим эффективное количество одного или более фосфатных производных одного или более агентов электронного переноса.
2. Способ по п.1, в котором агент электронного переноса выбран из группы, состоящей из гидроксихроманов, в том числе альфа-, бета-, гамма- и дельта-токолов в энантиомерной и рацемической формах; хинолов, которые являются восстановленными формами витамина К1 и убихинона; гидроксикаратиноидов, в том числе ретинола, кальциферола и аскорбиновой кислоты.
3. Способ по п.2, в котором агент электронного переноса выбран из группы, состоящей из токоферола и других токолов, ретинола, витамина К1 и их смесей.
4. Способ по п.3, в котором агент электронного переноса выбран из группы, состоящей из токолов и их смесей.
5. Способ по п.4, в котором фосфатное производное агента электронного переноса выбрано из группы, состоящей из фосфатных производных токоферола, фосфатных производных токотриенола и их смесей.
6. Способ по п.5, в котором фосфатное производное агента электронного переноса выбрано из группы, состоящей из монотокоферилфосфата, дитокоферилфосфата, монотокотриенилфосфата, дитокотриенилфосфата и их смесей.
7. Способ по п.6, в котором смесь фосфатных производных агентов электронного переноса является смесью монотокоферилфосфата и дитокоферилфосфата.
8. Способ по п.1, в котором фосфатное производное выбрано из группы, состоящей из фосфатов, фосфатидов, комплексов фосфатов и их смесей.
9. Способ по п.1, дополнительно содержащий защиту объединенных транспортирующего наполнителя и биологически активного соединения энтеросолюбильным покрытием.
10. Способ по п.1, в котором объединенные транспортирующий наполнитель и биологически активное вещество имеют форму пилюли, таблетки, капсулы, жидкого состава, функционального питания, пищевой добавки, лепешки или суппозитория.
11. Способ по п.1, в котором биологически активное соединение выбрано из группы, состоящей из фармацевтических средств, пищевых добавок, лекарств, витаминов, фитохимических средств, космецевтиков, нутрацевтиков, питательных веществ и оздоровительных добавок.
12. Способ по п.1, в котором биологически активное соединение представляет собой морфин.
13. Способ по п.1, в котором биологически активное соединение представляет собой кофермент Q10.
14. Транспортирующий наполнитель для энтерального применения биологически активных соединений, содержащий эффективное количество одного или более фосфатных производных одного или более агентов электронного переноса.
15. Применение эффективного количества одного или более фосфатных производных одного или более агентов электронного переноса вместе с другими наполнителями при изготовлении транспортирующего наполнителя для энтерального применения биологически активных соединений.
16. Фармацевтический состав для энтерального применения, содержащий одно или более одного биологически активных соединений и транспортирующий наполнитель, содержащий эффективное количество одного или более фосфатных производных одного или более агентов электронного переноса.
17. Способ повышения эффективности и улучшения транспорта вводимых энтерально биологически активных соединений, включающий объединение биологически активного соединения с транспортирующим наполнителем, содержащим эффективное количество одного или более комплексов фосфатных производных агента электронного переноса.
18. Транспортирующий наполнитель для энтерального применения биологически активных соединений, содержащий эффективное количество одного или более комплексов фосфатных производных агента электронного переноса.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
Авторы
Даты
2009-12-27—Публикация
2005-08-03—Подача