Изобретение относится к аналитической химии, а именно к способам определения содержания триптофана в водных модельных растворах методом циклической вольтамперометрии.
Известен способ определения триптофана методом вольтамперометрии на стеклоуглеродном электроде, покрытом пленкой из углеродных нанотрубок, основанный на реакции окисления триптофана при потенциале 1,08В на фоне буферного раствора Na2HPO4-лимонная кислота с рН 2,5 в сыворотке крови человека. Линейная область определяемых концентраций триптофана изменяется в диапазоне от 4⋅10-8 до 1⋅10-5 моль/л. Предел обнаружения триптофана составляет 1⋅10-8 моль/л. [Huang W., Mai G., Y. Li, Yang C, Qua W. Voltammetric determination of tryptophan at a single-wall carbon nanotubes modified electrode. // Journal of Nanoscience and Nanotechnology. 2004. V. 4. №4. P. 423-427].
Недостатками данного способа являются низкий предел обнаружения, трудоемкость изготовления модифицированного электрода, использование графитовых нанотрубок, имеющих высокую стоимость, применение критических токов для процесса модифицирования поверхности, приводящее к снижению количества рабочих циклов индикаторного электрода.
Известен способ определения триптофана методом дифференциально-импульсной вольтамперометрии на сенсоре, полученном на основе композита из полиариленфталида и графитированной сажи Carboblack С, модифицированной хелатными комплексами L-аргенато-L-аланината меди (II), для распознавания и селективного определения энантиомеров триптофана в биологических жидкостях и биологически активных добавках. [Зильберг Р.А., Терес Ю.Б., Загитова Л.Р., Яркаева Ю.А., Берестова Т.В. Вольтамперометрический сенсор на основе аминокислотного комплекса меди (II) для определения энантиомеров триптофана // Аналитика и контроль. 2021. Т. 25, №3. С. 193-204]. Окисление триптофана происходит при потенциале Е=0,8В в фосфатном буфере при рН 6,86 в диапазоне изменения рабочих потенциалов 0,5-1,2В при скорости сканирования потенциала 20 мВ/с, время выдерживания электрода в исследуемом растворе составляет 5 с. Данный композитный сенсор обладает большим линейным диапазоном концентраций энантиомеров триптофана от 1,25⋅10-6 до 1,0⋅10-3 моль/л с пределами обнаружения 0,90⋅10-6 моль/л для L-триптофана и 0,66⋅10-6 моль/л для D-триптофана.
Недостатками данного способа являются низкий предел обнаружения, использование для регенерации поверхности сенсора токсичного вещества N,N-диметилформамида.
Известен способ определения триптофана методом циклической вольтамперометрии с использованием энантиоселективного сенсора на основе пастового электрода из графитированной сажи CarboblackC, модифицированной цеолитом MFI-И, при соотношении CarboblackC и модификатора цеолита MFI-И 0,1 г: 0,006 г в моче и плазме человека. Линейный характер зависимости тока пика окисления триптофана от его содержания в растворе находится в диапазоне от 5⋅10-5 до 1⋅10-3 моль/л с пределами обнаружения 4,98⋅10-7 и 3,20⋅10-7 и нижними границами определяемых концентраций 1,66⋅10-6 и 1,07⋅10-6 моль/л для L- и D-триптофана соответственно [Ионина А. М., Сычева М. А., Гиззатуллина Р. М. Вольтамперометрический сенсор для распознавания и определения энантиомеров триптофана на основе графитированной сажи Carboblack С и цеолита MFI-И // Инновационные материалы и технологии - 2023: материалы Международной научно-технической конференции молодых ученых, Минск, 21-23 марта 2023 г. - Минск: БГТУ, 2023. - С. 187-188.].
Недостатками данного способа являются низкий предел обнаружения, использование непроводящего компонента электрода, который необходимо модифицировать в чувствительную поверхность сенсора, что накладывает ограничения в применении.
Известен способ вольтамперометрического определения триптофана в модельных растворах, содержащих триптофан, на электроде, модифицированном углеродными нанотрубками и полифолиевой кислотой. Максимум триптофана наблюдаются при потенциале 0,42В. Предел обнаружения триптофана составляет 1⋅10-7 моль/л. [Altyev А. М., Shelkovnikov V. V., Fryanova М. S. Electrochemical behavior of tryptophan and 5-hydroxytryptophan on an electrode modified with multi-walled carbon nanotubes and polyfolic acid // Journal of Siberian Federal University. Chemistry. 2023. 16(1). P. 36-6].
Недостатками данного способа являются низкая чувствительность определения, а также нанесение пленки полифиолиевой кислоты на поверхность углеродсодержащего электрода методом циклической вольтамперометрии в широком диапазоне потенциалов от -2 до +2В, что негативно влияет на работу и срок службы рабочего электрода.
Известен способ определения триптофана в модельном растворе методом дифференциально импульсной вольтамперометрии с использованием стеклоуглеродного электрода, модифицированного пленкой из нафиона и TiO2-нанокомпозита графена в 0,1 моль/л фосфатном буфере. Ток пика линейно изменяется в области от 5 до 140⋅10-6 моль/л. Предел обнаружения равен 0,7⋅10-6 моль/л [Fan Y., Liu J.-H., Lu H.-T., Qin Z. Electrochemistry and voltammetric determination of L-tryptophan and L-tyrosine using a glassy carbon electrode modified with a Nafion/TiO2-graphene composite film//Microchim acta. 2011. V. 173. P. 241-247].
Недостатками данного способа являются низкая чувствительность определения, длительность и многостадийность приготовления рабочей поверхности электрода, использование в качестве растворителя вещества второго класса опасности - диметилформамида.
Известен, принятый за прототип, способ определения триптофана в образцах мочи методом квадратноволновой вольтамперометрии на модифицированном электроде из пасты, состоящей из графитового порошка, ферроцендикарбоновой кислоты, многостенных углеродных нанотрубок и парафина [S. Е. Baghbamidi, Beitollahi Н., Karimi-Maleh Н., Soltani-Nejad S., Soltani-Nejad V., Roodsaz S. Modified carbon nanotube paste electrode for voltammetric determination of carbidopa, folic acid, and tryptophan // Journal analytical methods in chemistry. 2012. 8 p., https://doi.org/10.1155/2012/305872], заключающийся в том, что механически проводят получение пасты, смешивая в течение 20 минут 0,01 г ферроцендикарбоновой кислоты с 0,89 г графитового порошка и углеродных нанотрубок, с последующими стадиями: формовка в стеклянной трубке, введение медной проволоки для проводимости и полирование поверхности на фильтровальной бумаги. Пик окисления триптофана при потенциале 1,03 В получают в дифференциально импульсном режиме в области изменения потенциала от 0,1 до 1,2В со скоростью изменения потенциала 10 мВ/с на фоне фосфатного буфера с рН 6,6. Минимально определяемая концентрация триптофана составляет 6,5⋅10-8 моль/л. Диапазон определяемых концентраций составляет от 1⋅10-7 до 7,5⋅10-4 моль/л.
Однако известный способ позволяет определять содержание триптофана при минимальной концентрации, равной 6,5⋅10-8 моль/л, время одного измерения составляет 20 минут. В результате многочисленных опытов были выявлены недостатки данного способа, устранение которых позволило расширить диапазон определяемых концентраций и повысить экспрессность определения.
Техническим результатом предлагаемого изобретения является создание способа определения триптофана в модельных растворах методом циклической вольтамперометрии на графитовом электроде, позволяющего снизить и расширить диапазон определяемых концентраций триптофана и повысить экспрессность определения в 4 раза.
Предложенный способ определения триптофана в модельных растворах методом циклической вольтамперометрии на графитовом электроде, модифицированном коллоидными частицами серебра, заключается в том, что проводят модифицирование графитового электрода коллоидными частицами серебра из золя серебра в течение 120 с при потенциале накопления -0,8В с последующей регистрацией катодных максимумов при скорости изменения потенциала 100 мВ/с на фоне 0,1 М раствора NaOH в диапазоне потенциалов от -0,6 до 1,5В. Концентрацию триптофана определяют по величине катодных максимумов вольтамперных кривых в диапазоне потенциалов от минус 0,2 до 0,0В относительно насыщенного хлоридсеребряного электрода методом добавок аттестованных смесей.
В предлагаемом способе впервые установлена способность триптофана окисляться на графитовом электроде, модифицированном коллоидными частицами серебра, полученными с использованием цитрата натрия при мольном соотношении нитрата серебра (AgNO3) и цитрата натрия (Na3C6H5O7) 1:3 в течение 120 с.
Предлагаемый в заявляемом изобретении фон 0,1 М NaOH позволяет снизить и расширить диапазон определяемых концентраций триптофана от 1⋅10-12 до 1⋅10-10 моль/л с хорошей воспроизводимостью при минимальной концентрации триптофана равной 1⋅10-12 моль/л.
Предлагаемый вольтамперометрический способ позволяет улучшить метрологические характеристики анализа триптофана, снизить минимально определяемую концентрацию триптофана на 4 порядка и расширить диапазон определяемых концентраций триптофана на два порядка с 1⋅10-12 до 1⋅10-10 моль/л, а также повысить экспрессность определения в 4 раза по сравнению с прототипом.
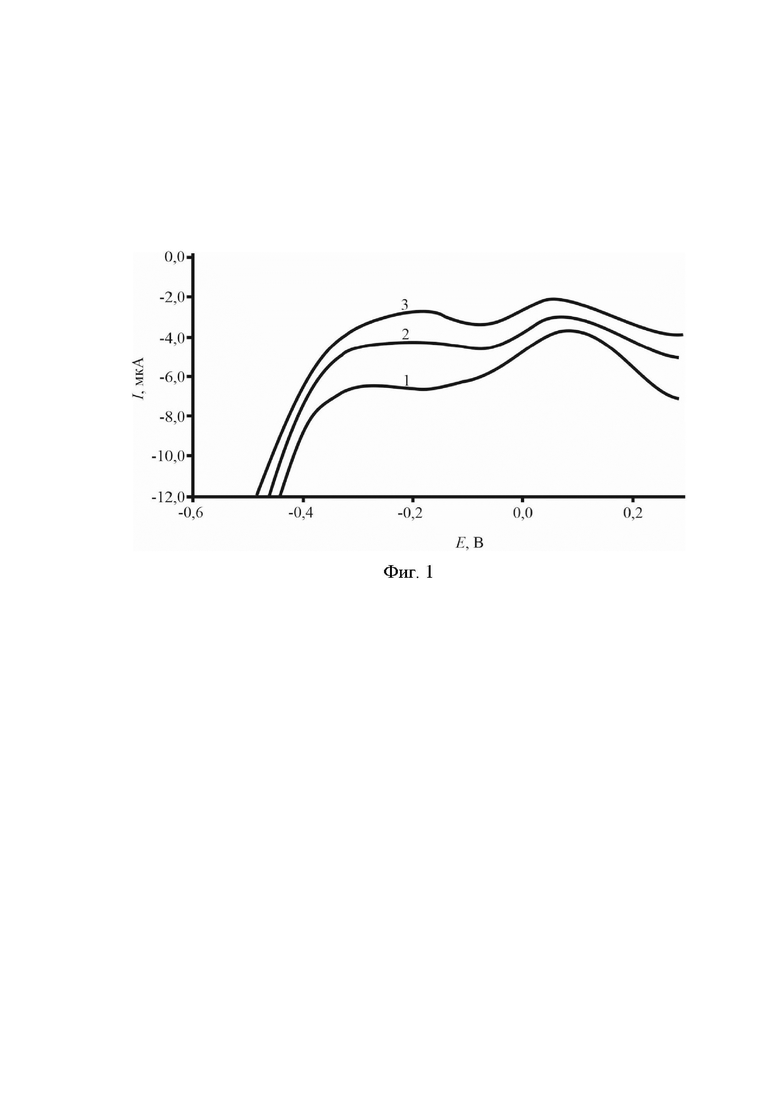
На Фиг. 1 представлены катодные вольтамперные кривые модельного раствора триптофана, полученные на графитовом электроде, предварительно электрохимически модифицированном коллоидными частицами серебра, где кривая 1 - фон 0,1 М NaOH, кривая 2 - концентрация триптофана (СТгу)=5⋅10-12 моль/л, кривая 3 - концентрация триптофана (CTry)=10⋅10-12 моль/л.
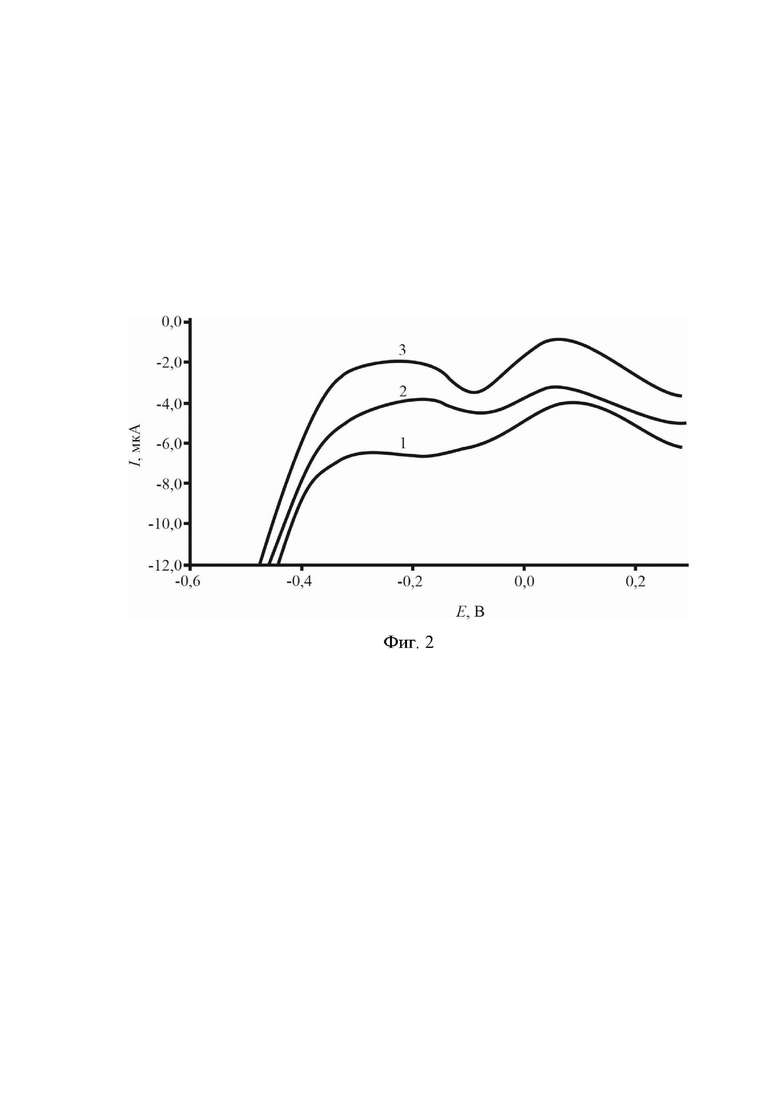
На Фиг. 2 представлены катодные вольтамперные кривые модельного раствора триптофана, полученные на графитовом электроде, предварительно электрохимически модифицированном коллоидными частицами серебра, где кривая 1 - фон 0,1 М NaOH, кривая 2 - концентрация триптофана (СТгу)=5⋅10-11 моль/л, кривая 3 - концентрация триптофана (CTry)=10⋅10-11 моль/л.
Пример 1. Измерения были проведены в модельном водном растворе 1. Графитовый электрод помещали в электрохимическую ячейку (кварцевый стаканчик), заполненную 10 мл золя серебра (мольное соотношение AgNO3:Na3C6H5O7=1:3). Далее проводили электролиз раствора для модификации графитового электрода коллоидными частицами серебра при условии: Еэ=-0,8В, τэ=120с, где Еэ - потенциал накопления, τэ - время модифицирования. Полученный модифицированный графитовый электрод ополаскивали бидистиллированной водой и помещали в другую электрохимическую ячейку (кварцевый стаканчик), заполненную 10 мл 0,1 М раствора NaOH. Не проводя накопления, регистрировали анодную ветвь, а затем катодную ветвь циклической вольтамперной кривой фонового электролита при скорости изменения потенциала 100 мВ/с, начиная от потенциала минус 0,6В и заканчивая плюс 1,5В. На катодной ветви вольтамперной кривой фонового электролита не наблюдался катодный максимум в диапазоне потенциалов от минус 0,2В до 0,0В (Фиг. 1, кривая 1). При добавлении раствора триптофана (первая добавка) происходило увеличение высоты катодного максимума в диапазоне потенциалов от минус 0,2В до 0,0В (Фиг. 1, кривая 2). При добавлении второй добавки раствора триптофана происходило пропорциональное увеличение высоты катодного максимума в диапазоне потенциалов от минус 0,2В до 0,0В (Фиг. 1, кривая 3).
Пример 2. Измерения были проведены в модельном водном растворе 2. Получение модифицированного графитового электрода наночастицами серебра проводили как в Примере 1. Полученный модифицированный графитовый электрод ополаскивали бидистиллированной водой и помещали в другую электрохимическую ячейку (кварцевый стаканчик), заполненную 10 мл 0,1 М раствора NaOH. Не проводя накопления, регистрировали анодную ветвь, а затем катодную ветвь циклической вольтамперной кривой фонового электролита при скорости изменения потенциала 100 мВ/с, начиная от потенциала минус 0,6В и заканчивая плюс 1,5В. На катодной ветви вольтамперной кривой фонового электролита не наблюдался катодный максимум в диапазоне потенциалов от минус 0,2В до 0,0В (Фиг. 2, кривая 1). При добавлении раствора триптофана (первая добавка) происходило увеличение высоты катодного максимума в диапазоне потенциалов от минус 0,2В до 0,0В (Фиг. 2, кривая 2). При добавлении второй добавки раствора триптофана происходило пропорциональное увеличение высоты катодного максимума в диапазоне потенциалов от минус 0,2В до 0,0В (Фиг. 2, кривая 3).
В Таблице 1 представлены результаты определения триптофана в модельных водных растворах методом циклической вольтамперометрии на графитовом электроде, модифицированном коллоидными наночастицами серебра.

Таким образом, впервые установлена способность количественного определения триптофана по катодным максимумам.
Предложенный способ прост, при его осуществлении не используются токсические вещества. Способ может быть использован в любой лаборатории, имеющей компьютеризированные анализаторы типа ТА или полярограф.
Изобретение относится к аналитической химии, а именно к способу определения триптофана в модельных водных растворах методом циклической вольтамперометрии на графитовом электроде, модифицированном коллоидными частицами серебра. Сущность: способ включает модифицирование графитового электрода коллоидными частицами серебра из золя серебра в течение 120 с при потенциале накопления -0,8 В с последующей регистрацией катодных максимумов при скорости изменения потенциалов 100 мВ/с на фоне 0,1 М раствора NaOH в диапазоне потенциалов от -0,6 до 1,5 В. Концентрацию триптофана определяют по величине катодных максимумов вольтамперных кривых в диапазоне потенциалов от минус 0,2 до 0,0 В относительно насыщенного хлоридсеребряного электрода методом добавок аттестованных смесей. Технический результат: снижение минимально определяемой концентрации 1⋅10-12 моль/л и расширение диапазона определяемых концентраций 1⋅10-12 -1⋅10-10 моль/л, сокращение времени проведения анализа. 2 ил., 1 табл.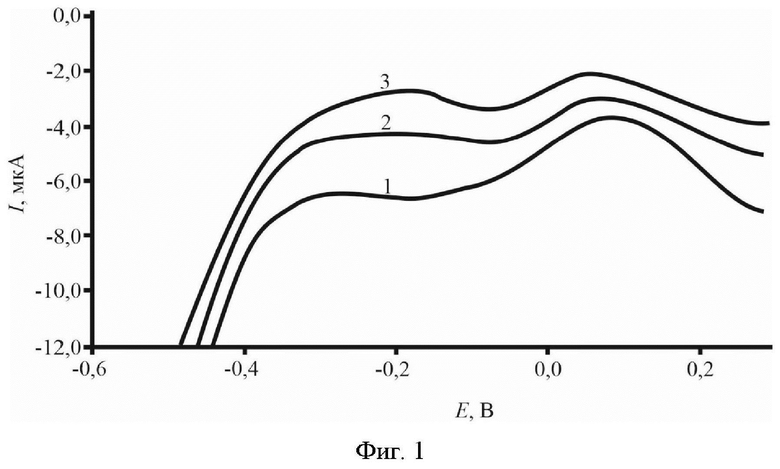
Способ определения триптофана в модельных водных растворах методом циклической вольтамперометрии на графитовом электроде, модифицированном коллоидными частицами серебра, отличающийся тем, что проводят модифицирование графитового электрода коллоидными частицами серебра из золя серебра в течение 120 с при потенциале накопления -0,8 В с последующей регистрацией катодных максимумов при скорости изменения потенциала 100 мВ/с на фоне 0,1 М раствора NaОН в диапазоне потенциалов от -0,6 до 1,5 В, концентрацию триптофана определяют по величине катодных максимумов вольтамперных кривых в диапазоне потенциалов от минус 0,2 до 0,0 В относительно насыщенного хлоридсеребряного электрода методом добавок аттестованных смесей.
| СПОСОБ ОПРЕДЕЛЕНИЯ МЕТИОНИНА В МОДЕЛЬНЫХ ВОДНЫХ РАСТВОРАХ МЕТОДОМ ЦИКЛИЧЕСКОЙ ВОЛЬТАМПЕРОМЕТРИИ НА ГРАФИТОВОМ ЭЛЕКТРОДЕ, МОДИФИЦИРОВАННОМ КОЛЛОИДНЫМИ ЧАСТИЦАМИ ПАЛЛАДИЯ | 2022 |
|
RU2793604C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЛУТАТИОНА В МОДЕЛЬНЫХ ВОДНЫХ РАСТВОРАХ МЕТОДОМ ЦИКЛИЧЕСКОЙ ВОЛЬТАМПЕРОМЕТРИИ НА ГРАФИТОВОМ ЭЛЕКТРОДЕ, МОДИФИЦИРОВАННОМ КОЛЛОИДНЫМИ ЧАСТИЦАМИ СЕРЕБРА | 2012 |
|
RU2510016C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЦИСТЕИНА В ВОДНЫХ РАСТВОРАХ МЕТОДОМ ЦИКЛИЧЕСКОЙ ВОЛЬТАМПЕРОМЕТРИИ НА ГРАФИТОВОМ ЭЛЕКТРОДЕ, МОДИФИЦИРОВАННОМ КОЛЛОИДНЫМИ ЧАСТИЦАМИ ЗОЛОТА | 2011 |
|
RU2463587C1 |
| CN 102507686 A, 20.06.2012 | |||
| CN 109187690 A, 11.01.2019 | |||
| CN 106290538 A, 04.01.2017. | |||
Авторы
Даты
2024-07-18—Публикация
2024-04-15—Подача