Настоящее изобретение относится к глутарату 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина или его фармацевтически приемлемому сольвату, к его кристаллу и к полиморфу указанного кристалла. Оно дополнительно относится к медицинскому применению каждого из них, в частности, в лечении или профилактике наркотической зависимости или воспаления.
Уровень техники
Воспаление представляет собой защитный ответ на вредные стимулы, такие как окислительный стресс, раздражители, патогены и поврежденные клетки. Воспалительный ответ включает выработку и высвобождение модуляторов воспаления, которые исцеляют поврежденную ткань и разрушают поврежденные клетки благодаря прямой или опосредованной выработке и/или передаче сигнала для высвобождения агентов, которые вырабатывают активные формы кислорода. Таким образом, надлежащий воспалительный ответ подразумевает баланс между разрушением поврежденных клеток и исцелением поврежденной ткани.
Неконтролируемый иммунный ответ может приводить к окислительному стрессу и появлению разных воспалительных болезненных патологий. Действительно, воспалительные процессы лежат в основе крупного числа патологий, включая иммунные и аутоиммунные заболевания, заболевания желудочно-кишечного тракта, разные типы рака, сосудистые нарушения, заболевания сердца и нейродегенеративные заболевания. В данной области техники существует необходимость в агентах, которые могут снижать ненадлежащий уровень воспаления.
Краткое описание изобретения
Настоящее изобретение относится к глутарату 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина (который в настоящем документе также называют глутаратом анатабина) или его фармацевтически приемлемому сольвату, к его кристаллу или к полиморфу указанного кристалла. Оно дополнительно относится к медицинскому применению каждого из них, в частности, в лечении или профилактике наркотической зависимости или воспаления.
Фармацевтическая композиция, содержащая терапевтически эффективную дозу глутарата анатабина, его фармацевтически приемлемого сольвата, его кристалла и/или полиморфа кристалла, может быть введена индивидууму для ослабления симптома или нарушения, включающего NFKB-опосредованный воспалительный компонент, и/или для снижения риска развития указанного нарушения. NFKB-опосредованный воспалительный компонент предпочтительно представляет собой хроническое воспаление, которое возникает, например, при тиреоидите, раке, артрите, болезни Альцгеймера и рассеянном склерозе. Терапевтически эффективные дозы глутарата анатабина, его фармацевтически приемлемого сольвата, его кристалла и/или полиморфа кристалла также могут быть обеспечены в составе с пролонгированным высвобождением. В других вариантах реализации выделенные формы глутарата анатабина, его фармацевтически эффективного сольвата, его кристалла и/или полиморфа могут быть обеспечены в продукте на основе бутилированной воды, содержащем, например, от примерно 1 мл до примерно 2000 мл очищенной воды и от примерно 0,00001 до примерно 0,0001 масс.% глутарата анатабина. Заявленное соединение, кристалл, полиморф и/или фармацевтическая композиция могут обладать эффектом ингибирования моноаминоксидазы (MAO). В дополнение или в качестве альтернативы, соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению могут обладать эффектом ингибирования фосфорилирования STAT3.
В частности, настоящее изобретение относится к следующим вариантам реализации:
1. Соединение, которое представляет собой глутарат 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина или его фармацевтически приемлемый сольват.
2. Соединение согласно варианту реализации 1, отличающееся тем, что указанный глутарат 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина имеет мольное отношение 1:1 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина к глутарату.
3. Соединение согласно вариантам реализации 1 или 2, отличающееся тем, что указанный 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридин представляет собой 3-[(2S)-1,2,3,6-тетрагидропиридин-2-ил]пиридин.
4. Соединение согласно варианту реализации 1, отличающийся тем, что указанный глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина имеет следующую формулу (I):
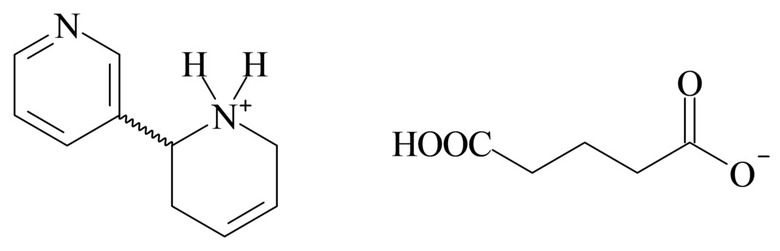
5. Соединение согласно любому из вариантов реализации 1-4, отличающееся тем, что указанный глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина имеет следующую формулу (Ia):
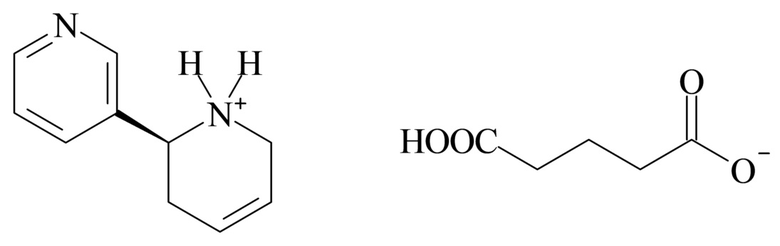
6. Кристалл соединения согласно любому из вариантов реализации 1-5.
7. Полиморфная форма соединения согласно любому из вариантов реализации 1-5 или кристалла согласно варианту реализации 6.
8. Полиморфная форма согласно варианту реализации 7, отличающаяся тем, что указанная полиморфная форма имеет дифрактограмму рентгеновской порошковой дифракции (CuKα) по существу такую, как показано на фиг. 1.
9. Полиморфная форма согласно вариантам реализации 7 или 8, отличающаяся тем, что указанная полиморфная форма имеет дифрактограмму рентгеновской порошковой дифракции (CuKα), содержащую один или более пиков, выбранных из 8,0 ± 0,2 °2θ, 11,0 ± 0,2 °2θ, 13,3 ± 0,2 °2θ, 16,5 ± 0,2 °2θ, 18,0 ± 0,2 °2θ, 20,7 ± 0,2 °2θ, 21,0 ± 0,2 °2θ, 21,4 ± 0,2 °2θ, 22,0 ± 0,2 °2θ, 22,3 ± 0,2 °2θ, 23,3 ± 0,2 °2θ и 24,5 ± 0,2 °2θ.
10. Соединение согласно любому из вариантов реализации 1-5, кристалл согласно варианту реализации 6 или полиморфная форма согласно любому из вариантов реализации 7-9 для применения в качестве лекарственного средства.
11. Соединение согласно любому из вариантов реализации 1-5, кристалл согласно варианту реализации 6 или полиморфная форма согласно любому из вариантов реализации 7-9 для применения в лечении или профилактике наркотической зависимости или воспаления.
12. Фармацевтическая композиция для применения в лечении или профилактике наркотической зависимости или воспаления, содержащая фармацевтически эффективное количество одного или более соединений согласно любому из вариантов реализации 1-5, кристалла согласно варианту реализации 6 или полиморфной формы согласно любому из вариантов реализации 7-9 необязательно совместно с одним или более фармацевтически приемлемыми вспомогательными веществами.
13. Способ лечения или предотвращения наркотической зависимости или воспаления у пациента-человека или животного, не являющегося человеком, нуждающегося в этом, где указанный способ включает введение указанному пациенту терапевтически эффективного количества по меньшей мере одного соединения согласно любому из вариантов реализации 1-5, кристалла согласно варианту реализации 6, полиморфной формы согласно любому из вариантов реализации 7-9 или фармацевтической композиции согласно варианту реализации 12.
14. Способ получения соединения согласно любому из вариантов реализации 1-5, кристалла согласно варианту реализации 6 или полиморфной формы согласно любому из вариантов реализации 7-9, включающий стадии:
получения раствора, содержащего 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридин, глутаровую кислоту и растворитель,
обеспечения образования соли 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина с глутаровой кислотой, и
выделения соли 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина с глутаровой кислотой.
15. Способ согласно варианту реализации 14, отличающийся тем, что указанный растворитель, применяемый для получения раствора 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, глутаровой кислоты и растворителя, содержит 2-метилтетрагидрофуран, ацетонитрил и/или этилацетат.
16. Соединение согласно любому из вариантов реализации 1-5, кристалл согласно варианту реализации 6, полиморфная форма согласно любому из вариантов реализации 7-9 для применения согласно варианту реализации 11 или фармацевтическая композиция для применения согласно варианту реализации 12, отличающиеся тем, что указанное вещество, вызывающее зависимость, выбрано из группы, состоящей из никотина, кокаина, героина, марихуаны и алкоголя.
17. Соединение согласно любому из вариантов реализации 1-5, кристалл согласно варианту реализации 6, полиморфная форма согласно любому из вариантов реализации 7-9 для применения согласно варианту реализации 11 или фармацевтическая композиция для применения согласно варианту реализации 12, отличающиеся тем, что указанное воспаление выбрано из группы, состоящей из болезни Альцгеймера, тиреоидита и рассеянного склероза.
18. Соединение согласно любому из вариантов реализации 1-5, кристалл согласно варианту реализации 6, полиморфная форма согласно любому из вариантов реализации 7-9 для применения согласно варианту реализации 11 или фармацевтическая композиция для применения согласно варианту реализации 12 в ингаляторе сухих порошков.
19. Соединение согласно любому из вариантов реализации 1-5, кристалл согласно варианту реализации 6, полиморфная форма согласно любому из вариантов реализации 7-9 для применения согласно варианту реализации 11 или фармацевтическая композиция для применения согласно варианту реализации 12 в устройстве для термического испарения аэрозоля.
Описание фигур
Фиг. 1: Дифрактограмма рентгеновской порошковой дифракции (CuKα) предпочтительного полиморфа глутарата анатабина
Фиг. 2: Спектр1H ЯМР глутарата анатабина, полученного согласно примеру 1
Фиг. 3: Хроматограмма общего ионного тока глутарата анатабина в режиме ионизации с образованием положительных ионов
Фиг. 4: Масс-спектр глутарата анатабина в режиме ионизации с образованием положительных ионов
Фиг. 5: Спектр FTIR глутарата анатабина
Фиг. 6: Спектр FTIR свободного основания анатабина
Фиг. 7: Рентгеновская дифрактограмма глутарата анатабина и положения пиков
Фиг. 8: Термограмма ТГА глутарата анатабина
Фиг. 9: Термограмма ДСК глутарата анатабина
Фиг. 10: График DVS глутарата анатабина
Фиг. 11: Ионная хроматограмма глутарата анатабина
Фиг. 12: Образец глутарата анатабина для определения стабильности в условиях окружающей среды через T=0, 3 и 7 дней.
Фиг. 13: Дифрактограмма XRPD тартрата анатабина
Фиг. 14: Дифрактограмма XRPD цитрата анатабина
Подробное описание изобретения
Настоящее изобретение относится к глутарату анатабина для лечения нарушений, включающих воспалительных компонент, включая хроническое слабое воспаление. Анатабин представляет собой алкалоид, присутствующий в табаке и, в более низких концентрациях, в разных пищевых продуктах, включая зеленые помидоры, зеленый картофель, спелый красный перец, мексиканские томаты и сушеные помидоры. Он является основным активным компонентом реализуемой на рынке пищевой добавки Anatabloc, обеспечивающей поддерживающее противовоспалительное действие, как описано в патенте США № US9387201 и публикации WO 2013/032558. Получение выделенных форм анатабина описано в WO 2011/119722, а также в следующих ссылках от Ref-1 до Ref-11.
Ref-1: Rossi, F. V.; Ballini, R.; Barboni, L.; Allegrini, P.; Palmieri, A. A practical and efficient synthesis of (±)-anatabine. Synthesis 2018, 50(9), 1921-1925.
Ref-2: Puthiaparampil, T. T.; David, T. K.; Raju, M. S. Methods of synthesizing anatabine. Патент США №8207346.
Ref-3: Puthiaparampil, T. T.; David, T. K.; Raju, M. S. Pharmaceutical, dietary supplement, and food grade salts of anatabine. Патент США №8557999.
Ref-4: Saloranta, T.; Leino, R. From building block to natural products: a short synthesis and complete NMR spectroscopic characterization of (±)-anatabine and (±)-anabasine. Tetrahedron Letters 2011, 52(36), 4619-4621.
Ref-5: Rouchaud, A.; Kem, W. R. A convenient racemic synthesis of two isomeric tetrahydropyridyl alkaloids: isoanatabine and anatabine. Journal of Heterocyclic Chemistry 2010, 47(3), 569-581.
Ref-6: Ayers, J. T.; Xu, R.; Dwoskin, L. P.; Crooks, P. A. A general procedure for the enantioselective synthesis of the minor Tobacco alkaloids nornicotine, anabasine, and anatabine. The AAPS Journal 2005; 7(3), статья 75.
Ref-7: Felpin, F.-X.; Vo-Thanh, G.; Robins, R. J.; Villieras, J.; Lebreton, J. Total synthesis of (S)-anabasine and (S)-anatabine. Synlett 2000, (11), 1646-1648.
Ref-8: Yang, C.-M.; Tanner, D. D. A simple synthesis of (±)-1,2,3,6-tetrahydro-2,3'-bipyridine (anatabine) and (±)-3-(2-piperidinyl)pyridine (anabasine) from lithium aluminum hydride and pyridine. Canadian Journal of Chemistry 1997, 75(6), 616-620.
Ref-9: Deo, N. M.; Crooks, P. A. Regioselective alkylation of N-(diphenylmethylidine)-3-(aminomethyl)pyridine: a simple route to minor tobacco alkaloids and related compounds. Tetr. Lett. 1996, 37 (8), 1137-1140.
Ref-10: Genisson, Y.; Mehmandoust, M.; Marazano, C.; Das, B. C. Chiral 1,2-dihydropyridines and 2,5-dihydropyridinium salt equivalents. Synthesis of (+)-anatabine and a chiral benzomorphane. Heterocycles 1994, 39(2), 811-818.
Ref-11: Quan, P. M.; Karns, T. K. B.; Quin, L. D. Total synthesis of dl-anatabine. Chemistry & Industry (London, United Kingdom) 1964, (36), 1553.
3-[1,2,3,6-тетрагидропиридин-2-ил]пиридин (анатабин) существует в виде двух энантиомеров, а именно R-(+)-анатабина и S-(-)-анатабина. Способы энантиоселективного синтеза S- и R-энантиомеров анатабина описаны, например, в Ayers, J. T.; Xu, R.; Dwoskin, L. P.; Crooks, P. A. A general procedure for the enantioselective synthesis of the minor Tobacco alkaloids nornicotine, anabasine, and anatabine. The AAPS Journal 2005; 7(3) статья 75. В настоящем изобретении анатабин может применяться в качестве рацемической смеси двух его энантиомеров, в виде очищенной формы S-(-)-анатабина или очищенной формы R-(+)-анатабина. Если из контекста очевидно не следует иное, то термин «анатабин» в настоящем документе относится к любому из (1) рацемической смеси анатабина (R, S), (2) очищенной формы S-(-)-анатабина, или (3) очищенной формы R-(+)-анатабина.
Фармацевтически приемлемые соли анатабина описаны в патенте США №8207346 и патенте США №8557999. В частности, в примере 6 в патенте США №8207346 и в примере 6 в патенте США №8557999 описано получение тартрата анатабина и цитрата анатабина путем добавления винной кислоты или лимонной кислоты в раствор анатабина в ацетоне. Выделяли полученное твердое вещество путем декантации, растирания с диэтиловым эфиром и сушки в вакууме, но выход солей не указан.
Глутарат анатабина
Настоящее изобретение относится, в одном из вариантов реализации, к соединению, которое представляет собой глутарат 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина (который также называют в настоящем документе глутаратом анатабина), или его фармацевтически приемлемому сольвату. Глутарат 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина также может быть описан как соль 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина с глутаровой кислотой. Предпочтительно, глутарат 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина имеет мольное отношение 1:1 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина к глутарату.
Следует понимать, что любое упоминание «глутарата 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина» или «глутарата анатабина» в настоящем документе также относится к любому его фармацевтически приемлемому сольвату.
Более предпочтительно, глутарат 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина имеет химическую структуру, представленную следующей формулой (I):
 .
.
Следует отметить, что 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридин (анатабин) существует в виде двух энантиомеров, а именно R-(+)-анатабина и S-(-)-анатабина. В настоящем изобретении 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридин предпочтительно представляет собой 3-[(2S)-1,2,3,6-тетрагидропиридин-2-ил]пиридин.
В предпочтительном варианте реализации глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, таким образом, может иметь следующую формулу (Ia):

Авторы настоящего изобретения неожиданно обнаружили, что глутарат анатабина и, что было еще более удивительно, кристалл и полиморфная форма кристалла, обладают предпочтительными свойствами, такими как высокая степень кристалличности, морфология, термическая и механическая устойчивость к полиморфным превращениям и/или дегидратации, стабильность при хранении, низкое содержание остаточного растворителя, пониженный уровень гигроскопичности, текучесть и предпочтительные технологические и рабочие характеристики. Кроме того, авторы настоящего изобретения обнаружили, что глутарат анатабина перекристаллизуется в виде кристаллической соли даже при воздействии влаги и после удаления влаги подходящими средствами, такими как сушка в вакууме. Такой результат является крайне неожиданным.
Как можно увидеть из вышеизложенного, анатабин существует в форме разных изомеров, в частности, стереоизомеров (включая энантиомеры и диастереомеры) или таутомеров. Все указанные изомеры глутарата анатабина, которые могут присутствовать как в смеси, так и в чистой или по существу чистой форме, рассматриваются как часть настоящего изобретения. Что касается стереоизомеров, то изобретение включает отдельные оптические изомеры соединений согласно изобретению, а также любые их смеси (включая, в частности, рацемические смеси/рацематы). Рацематы могут быть разделены физическими способами, такими как, например, фракционная кристаллизация, разделение или кристаллизация диастереомерных производных или разделение путем хиральной колоночной хроматографии. Отдельные оптические изомеры также могут быть получены из рацематов путем образования соли с оптически активной кислотой и последующей кристаллизации. Настоящее изобретение дополнительно включает любые таутомеры соединений, предложенных в настоящем документе.
Следует понимать, что любое упоминание глутарата 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина в настоящем документе также включает любые его сольваты и/или смешанные кристаллы. Сольваты включают любые типы сольватов, включая, например, сольваты с водой, например, гидраты, или с органическими растворителями, такими как, например, метанол, этанол или ацетонитрил, т.е. метанолат, этанолат или ацетонитрилат, соответственно, или любую полиморфную форму.
В объем изобретения также включен глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, в котором один или более атомов заменены на конкретный изотоп соответствующего атома. Например, изобретение включает глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, в котором один или более атомов водорода (или, например, все атомы водорода) заменены на атомы дейтерия (т.е., 2H; который также обозначают как «D»). Соответственно, изобретение также включает глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, который обогащен дейтерием. Природный водород представляет собой смесь изотопов, содержащую примерно 99,98 мол.% водорода-1 (1H) и примерно 0,0156 мол.% дейтерия (2H или D). Содержание дейтерия в качестве одного или более атомов водорода в глутарате 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина может быть увеличено способами дейтерирования, известными в данной области техники. Например, соединение формулы (I) или реагент, или прекурсор, применяемый в синтезе глутарата 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, может быть обработано(-ан) в условиях реакции обмена H/D с использованием, например, тяжелой воды (D2O). Дополнительные подходящие способы дейтерирования описаны в: Atzrodt J et al., Bioorg Med Chem, 20(18), 5658-5667, 2012; William JS et al., Journal of Labelled Compounds and Radiopharmaceuticals, 53(11-12), 635-644, 2010; Modvig A et al., J Org Chem, 79, 5861-5868, 2014. Содержание дейтерия может быть определено, например, путем масс-спектрометрии или ЯМР-спектроскопии. Если конкретно не указано иное, то, предпочтительно, глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина не обогащен дейтерием. Соответственно, наличие атомов водорода в природном отношении или атомов водорода 1H в глутарате 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина является предпочтительным.
Способы селективного получения энантиомеров анатабина описаны, например, в «A General Procedure for the Enantioselective Synthesis of the Minor Tobacco Alkaloids Nornicotine, Anabasine, and Anatabine», The AAPS Journal 2005; 7(3) статья 75. Любые из способов или композиций, описанных в настоящем документе, могут включать обеспечение анатабина в виде рацемической смеси двух его энантиомеров, в очищенной форме S-(-)-анатабина или в очищенной форме R-(+)-анатабина. Если из контекста очевидно не следует иное, то термин «анатабин» в настоящем документе относится к любому из (1) рацемической смеси анатабина (R, S), (2) очищенной формы S-(-)-анатабина, или (3) очищенной формы R-(+)-анатабина.
Настоящее изобретение дополнительно относится к кристаллу глутарата 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина. Кристалл не ограничен каким-либо конкретным образом и может иметь любую морфологию.
Настоящее изобретение дополнительно относится к конкретному полиморфу (который в настоящем документе также называют полиморфной формой) глутарата 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина и, в частности, кристалла глутарата 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина. Полиморф предпочтительно имеет дифрактограмму рентгеновской порошковой дифракции (CuKα) по существу такую, как показано на фиг. 1. Полиморф предпочтительно имеет дифрактограмму рентгеновской порошковой дифракции (CuKα), содержащую один или более пиков, выбранных из 8,0 ± 0,2 °2θ, 11,0 ± 0,2 °2θ, 13,3 ± 0,2 °2θ, 16,5 ± 0,2 °2θ, 18,0 ± 0,2 °2θ, 20,7 ± 0,2 °2θ, 21,0 ± 0,2 °2θ, 21,4 ± 0,2 °2θ, 22,0 ± 0,2 °2θ, 22,3 ± 0,2 °2θ, 23,3 ± 0,2 °2θ и 24,5 ± 0,2 °2θ. Более предпочтительно, полиморф имеет дифрактограмму рентгеновской порошковой дифракции (CuKα), содержащую один или более пиков, выбранных из 8,0 ± 0,2 °2θ, 13,3 ± 0,2 °2θ, 16,5 ± 0,2 °2θ, 21,4 ± 0,2 °2θ, 22,0 ± 0,2 °2θ и 24,5 ± 0,2 °2θ.
Еще более предпочтительно, полиморф имеет дифрактограмму рентгеновской порошковой дифракции (CuKα), содержащую один или более пиков, выбранных из 8,0 ± 0,1 °2θ, 11,0 ± 0,1 °2θ, 13,3 ± 0,1 °2θ, 16,5 ± 0,1 °2θ, 18,0 ± 0,1 °2θ, 20,7 ± 0,1 °2θ, 21,0 ± 0,1 °2θ, 21,4 ± 0,1 °2θ, 22,0 ± 0,1 °2θ, 22,3 ± 0,1 °2θ, 23,3 ± 0,1 °2θ и 24,5 ± 0,1 °2θ. Еще более предпочтительно, полиморф имеет дифрактограмму рентгеновской порошковой дифракции (CuKα), содержащую один или более пиков, выбранных из 8,0 ± 0,1 °2θ, 13,3 ± 0,1 °2θ, 16,5 ± 0,1 °2θ, 21,4 ± 0,1 °2θ, 22,0 ± 0,1 °2θ и 24,5 ± 0,1 °2θ.
Еще более конкретно, полиморф предпочтительно имеет дифрактограмму рентгеновской порошковой дифракции (CuKα), содержащую один или более пиков, выбранных из 7,960 ± 0,2 °2θ, 10,907 ± 0,2 °2θ, 13,291 ± 0,2 °2θ, 14,413 ± 0,2 °2θ, 15,239 ± 0,2 °2θ, 16,479 ± 0,2 °2θ, 17,933 ± 0,2 °2θ, 20,610 ± 0,2 °2θ, 20,977 ± 0,2 °2θ, 21,318 ± 0,2 °2θ, 21,927 ± 0,2 °2θ, 22,203 ± 0,2 °2θ, 22,792 ± 0,2 °2θ, 23,246 ± 0,2 °2θ, 24,426 ± 0,2 °2θ и 24,769 ± 0,2 °2θ. Еще более конкретно, полиморф предпочтительно имеет дифрактограмму рентгеновской порошковой дифракции (CuKα), содержащую один или более пиков, выбранных из 7,960 ± 0,1 °2θ, 10,907 ± 0,1 °2θ, 13,291 ± 0,1 °2θ, 14,413 ± 0,1 °2θ, 15,239 ± 0,1 °2θ, 16,479 ± 0,1 °2θ, 17,933 ± 0,1 °2θ, 20,610 ± 0,1 °2θ, 20,977 ± 0,1 °2θ, 21,318 ± 0,1 °2θ, 21,927 ± 0,1 °2θ, 22,203 ± 0,1 °2θ, 22,792 ± 0,1 °2θ, 23,246 ± 0,1 °2θ, 24,426 ± 0,1 °2θ и 24,769 ± 0,1 °2θ.
Для подтверждения наличия глутарата при отношении 1:1 анатабин:глутарат проводили анализ ионной хроматографии. В экспериментальных примерах показано, что глутарат анатабина является очень стабильным и не имеет признаков разрушения даже в условиях ускоренного состаривания (40°C/75% отн.вл.) по прошествии 7 дней. Представленные данные дополнительно показывают, что глутарат анатабина может быть получен в отдельной кристаллической форме с характерной кристаллической структурой и физическими свойствами, такими как температура плавления, дифрактограмма рентгеновской дифракции, характеристический спектр инфракрасного поглощения.
Скрининг полиморфов не привел к получению новых полиморфных форм глутарата анатабина. Это было дополнительно подтверждено путем сканирующей электронной микроскопии и сравнения профилей ДСК и XRPD образцов, которые выдерживали в этилацетате и ацетонитриле для «созревания» кристаллов. Термические свойства глутарата анатабина были определены путем термогравиметрического анализа (ТГА) и дифференциальной сканирующей калориметрии (ДСК), которые использовали для описания характеристик кристаллической формы.
В отличие от глутарата, тартрат (фиг. 13) и цитрат (фиг. 14) имеют аморфную форму. Цитрат и тартрат очень гигроскопичны, что затрудняет их обработку и создает проблемы, в частности, при крупномасштабном производстве и получении составов. Кроме того, способ получения цитрата, который описан в патенте США №8207346 и патенте США №8557999, включает осаждение из ацетона. В результате, твердые формы цитрата содержат захваченный ацетон, который трудно удалить без превращения твердого вещества в пену/вязкое вещество.
Настоящее изобретение также относится к способу получения глутарата 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина и, в частности, кристалла глутарата 3-(1,2,3,6-тетрагидропиридин-2-ил)пиридина.
Указанный способ включает стадии
a) получения раствора, содержащего 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридин, глутаровую кислоту и растворитель,
b) обеспечения образования соли 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина с глутаровой кислотой, и
c) выделения соли 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина с глутаровой кислотой.
Растворитель, применяемый для получения раствора 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, глутаровой кислоты и растворителя, предпочтительно содержит 2-метилтетрагидрофуран, ацетонитрил и/или этилацетат. Более предпочтительно, растворитель содержит 2-метилтетрагидрофуран.
Способ может дополнительно включать стадию d) перекристаллизации соли 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина с глутаровой кислотой. Подходящие растворители для указанной перекристаллизации включают ацетонитрил.
На стадии a) глутарат анатабина может быть получен путем объединения свободного основания анатабина, растворителя и глутаровой кислоты для получения реакционной смеси. Глутарат анатабина, как правило, образуется в указанной реакционной смеси в результате приведения свободного основания анатабина в контакт с глутаровой кислотой. Предпочтительно, свободное основание анатабина в виде 1-5 масс.% раствора в ацетонитриле объединяют с глутаровой кислотой.
Предпочтительно, раствор или суспензию свободного основания анатабина, растворитель и глутаровую кислоту объединяют для получения реакционной смеси, затем глутаратную соль анатабина осаждают и выделяют из смеси. Глутаровая кислота может быть добавлена либо в виде твердого вещества, либо в виде раствора или суспензии в растворителе.
Растворитель предпочтительно выбран из группы, состоящей из алканолов, содержащих от 1 до 8 атомов углерода, алифатических сложных эфиров, содержащих от 3 до 8 атомов углерода, алифатических линейных или циклических простых эфиров, содержащих от 3 до 8 атомов углерода, алифатических кетонов, содержащих от 3 до 8 атомов углерода, C6-12 ароматических углеводородов (таких как бензол и нафталин), ацетонитрила, воды и любых их смесей. Предпочтительно, растворитель выбран из алифатических сложных эфиров, содержащих от 3 до 8 атомов углерода, алифатических циклических простых эфиров, содержащих от 3 до 8 атомов углерода, ацетонитрила и их смеси. Более предпочтительно, растворитель выбран из этилацетата, ацетонитрила, 2-метилтетрагидрофурана и любых их смесей. Еще более предпочтительно, растворитель содержит ацетонитрил. Еще более предпочтительно, растворитель представляет собой ацетонитрил.
Свободное основание анатабина, глутаровую кислоту и по меньшей мере один растворитель предпочтительно объединяют для получения реакционной смеси примерно при комнатной температуре (т.е. предпочтительно, в диапазоне от 15°C до 25°C). Концентрация глутаровой кислоты, присутствующей в указанной реакционной смеси, предпочтительно представляет собой концентрацию, близкую к концентрации насыщения (например, по меньшей мере 80%, предпочтительно 90%, более предпочтительно 95% от максимальной достижимой концентрации). Глутарат анатабина, как правило, осаждается из смеси. Осаждение может происходить само по себе или может быть вызвано, например, внесением затравочных кристаллов. Реакционную смесь можно перемешивать до, во время или после осаждения.
Реакционную смесь можно нагревать, а затем охлаждать для улучшения осаждения глутарата анатабина. Нагревание можно проводить до любой температуры (например, от примерно 50°C до примерно 80°C) в диапазоне от комнатной температуры до температуры кипения растворителя. Затем, в общем случае, проводят охлаждение до температуры ниже 40°C, предпочтительно от примерно 30°C до примерно 20°C, более предпочтительно до комнатной температуры (т.е. предпочтительно, в диапазоне от 15°C до 25°C), для улучшения осаждения.
Полученный осадок может быть выделен разными способами, такими как фильтрование. Осадок можно сушить при давлении окружающей среды или пониженном давлении и/или при повышенной температуре.
Медицинские применения
Подходящие соединения в соответствии со способом согласно настоящему изобретению обладают способностью проникать через гематоэнцефалический барьер пациента. Таким образом, указанные соединения обладают способностью поступать в центральную нервную систему пациента. Логарифмированные значения P для типовых соединений, подходящих для реализации настоящего изобретения, в целом, составляют более 0, во многих случаях более чем примерно 0,1 и часто более чем примерно 0,5. Логарифмированные значения P для указанных типовых соединений, в целом, составляют менее чем примерно 3,0, во многих случаях менее чем примерно 2,5 и часто менее чем примерно 2,0. Логарифмированные значения P представляют собой меру способности соединения проникать через диффузионный барьер, такой как биологическая мембрана. См., Hansch, et al., J. Med. Chem., том 11, стр. 1 (1968).
Подходящие соединения в соответствии со способом согласно настоящему изобретению обладают способностью связывать никотиновые холинергические рецепторы и тем самым вызывать их активацию в мозге пациента. Таким образом, указанные соединения обладают способностью к действию в качестве агонистов никотина. Константы связывания с рецептором для типовых соединений, подходящих для реализации настоящего изобретения, в целом, составляет более чем примерно 1 нМ, во многих случаях более чем примерно 200 нМ и часто более чем примерно 500 нМ. Константы связывания с рецептором для указанных типовых соединений, в целом, составляют менее чем примерно 10 мкМ, во многих случаях менее чем примерно 7 мкМ и часто менее чем примерно 2 мкМ. Константы связывания с рецептором представляют собой меру способности соединения связывать половину соответствующих рецепторных участков в определенных клетках мозга пациента. См., Cheng, et al., Biochem. Pharmacol., том 22, стр. 3099-3108 (1973).
Подходящие соединения в соответствии со способом согласно настоящему изобретению обладают способностью проявлять функцию никотина благодаря эффективной секреции нейротрансмиттеров от измененных нервных окончаний (т.е. синаптосом). Таким образом, указанные соединения обладают способностью к индуцированию высвобождения или секреции ацетилхолина, дофамина и других нейротрансмиттеров в соответствующих нейронах. В целом, типовые соединения, подходящие для реализации настоящего изобретения, обеспечивают секрецию дофамина в количествах, которые составляют по меньшей мере примерно 3 процента, во многих случаях по меньшей мере 25 процентов и часто по меньшей мере 50 процентов от уровня, обеспечиваемого таким же мольным количеством (s)-(-)-никотина.
Таким образом, настоящее изобретение включает соединения, кристалл или полиморфную форму, описанные в настоящем документе, для применения в качестве лекарственного средства. Лекарственное средство предпочтительно предназначено для применения в лечении или профилактике наркотической зависимости или воспаления. Способ лечения или предотвращения никотиновой зависимости или воспаления у пациента-человека или животного, не являющегося человеком, нуждающегося в этом, также является частью настоящего изобретения. Настоящее изобретение дополнительно относится к фармацевтической композиции для применения в лечении или профилактике наркотической зависимости или воспаления, содержащей фармацевтически эффективное количество одного или более соединений, кристаллов или полиморфных форм, описанных в настоящем документе, необязательно совместно с одним или более фармацевтически приемлемыми вспомогательными веществами.
«Пациент-человек или животное, не являющееся человеком» в настоящем документе включает теплокровных животных, как правило, млекопитающих, включая человека и других приматов. В некоторых вариантах реализации пациент представляет собой животное, такое как комнатное животное, животное-поводырь, сельскохозяйственное животное или зоопарковое животное. Указанные животные включают, но не ограничиваются указанными, собачьих (включая собак, волков), кошачьих (включая домашних кошек, тигров, львов), хорьков, кроликов, грызунов (например, крыс, мышей), морских свинок, хомяков, песчанок, лошадей, коров, свиней, овец, коз, жирафов и слонов. Таким образом, глутарат анатабина, такой как описано в настоящем документе, можно применять как для терапии человека, так и в ветеринарии.
В некоторых вариантах реализации выделенная форма глутарата анатабина может быть введена для снижения риска развития нарушения, включающего NFKB-опосредованный воспалительный компонент (т.е. для профилактики). Специалист может легко выявить индивидуумов с повышенным риском или семейным анамнезом указанного нарушения. Другие общепризнанные показатели повышенного риска определенных нарушений могут быть определены в стандартных клинических испытаниях или по анамнезу.
В некоторых вариантах реализации выделенная форма глутарата анатабина может быть введения для снижения риска развития нарушения, включающего STAT3-опосредованный воспалительный компонент (т.е. для профилактики). Специалист может легко выявить индивидуумов с повышенным риском или семейным анамнезом указанного нарушения. Другие общепризнанные показатели повышенного риска определенных нарушений могут быть определены в стандартных клинических испытаниях или по анамнезу.
Воспаление предпочтительно выбрано из группы, состоящей из болезни Альцгеймера, тиреоидита и рассеянного склероза. Тем не менее, спектр заболеваний, которые можно лечить соединением, кристаллом, полиморфной формой или фармацевтической композицией, намного шире и представлен далее:
- тиреоидит,
- иммунное или аутоиммунное нарушение,
- артрит, такой как ревматоидный артрит, первичный и вторичный остеоартрит (также называемый дегенеративным заболеванием суставов),
- спондилоартропатия, такая как псориатический артрит, ювенильный хронический артрит с поздним формированием паннуса и энтерогенные спондилоартропатии, такая как энтерогенный реактивный артрит, урогенитальная спондилоартропатия и недифференцированная спондилоартропатия,
- миопатия, такая как «ревматизм мягких тканей» (например, «теннисный локоть», «замороженное плечо», синдром запястного канала, подошвенный фасциит и тендинит ахиллова сухожилия);
- диабет, либо сахарный диабет I типа, либо сахарный диабет II типа,
- воспалительное нарушение желудочно-кишечного тракта, такое как воспалительная болезнь кишечника, например, болезнь Крона, синдром Барретта, илеит, синдром раздраженного кишечника, синдром раздраженной толстой кишки, язвенный колит, псевдомембранозный колит, геморрагический колит, гемолитико-уремический синдром с колитом, коллагенозный колит, ишемический колит, радиационный колит, колит, вызванный лекарственными средствами и химическими веществами, диверсионный колит, колит при таких состояниях, как хроническая гранулематозная болезнь, целиакия, спру-целиакия, пищевая аллергия, гастрит, инфекционный гастрит, энтероколит (например, хронический активный гастрит, вызванный инфекцией Helicobacter pylori), и воспаление илеоанального кармана,
- болезнь трансплантат против хозяина (БТПХ), системная красная волчанка (СКВ), волчаночный нефрит, болезнь Аддисона, тяжелая миастения, васкулит (например, гранулематоз Вегенера), аутоиммунный гепатит, остеопороз и некоторые виды бесплодия,
- сосудистое воспалительное заболевание, патологии, связанные с сосудами, атеросклероз, ангиопатия, атеросклеротическая или тромбоэмболическая макроангиопатия, вызванная воспалением, ишемическая болезнь сердца, цереброваскулярная болезнь, заболевание периферических сосудов, сердечно-сосудистое заболевание системы кровообращения, такое как ишемия/реперфузия, заболевание периферических сосудов, рестеноз после ангиопластики, воспалительная аневризма аорты, васкулит, инсульт, повреждение спинного мозга, застойная сердечная недостаточность, геморрагический шок, ишемическая болезнь сердца/реперфузионное повреждение, спазм сосудов после субарахноидального кровотечения, спазм сосудов после острого нарушения мозгового кровообращения, плеврит, перикардит, воспалительный миокардит, или сердечно-сосудистое осложнение при диабете,
- отек головного мозга или нейродегенеративное заболевание, такое как рассеянный склероз, болезнь Альцгеймера или болезнь Паркинсона,
- воспаление, связанное с заболеванием почек, нефритом, гломерулонефритом, диализом, перитонеальным диализом, перикардитом, хроническим простатитом, васкулитом, подагрой или панкреатитом,
- анемия,
- язвенное заболевание, такое как пептическая язва, острый панкреатит или афтозная язва,
- возрастное заболевание, такое как атеросклероз, фиброз и остеопороз, или заболевание, связанное с недоношенностью, такое как ретинопатия, хроническое заболевание легких, артрит и нарушения пищеварения,
- преэклампсия, воспаление, связанное с химической или тепловой травмой, вызванной ожогами, кислотами и щелочами, химическое отравление (МФТП/конкавалин/химическое средство/отравление пестицидами), укусы змей, пауков или насекомых, нежелательные эффекты, вызванные лекарственной терапией (включая нежелательные эффекты, вызванные лечением амфотерицином В); нежелательные эффекты иммуносупрессивной терапии (например, при лечении интерлейкином-2), нежелательные эффекты при лечении OKT3, нежелательные эффекты при лечении ГМ-КСФ, нежелательные эффекты при лечении циклоспорином и нежелательные эффекты при лечении аминогликозидами, стоматит и мукозит, вызванные подавлением иммунитета, или воздействие ионизирующего излучения, такое как воздействие солнечного ультрафиолетового излучения, облучение на атомной электростанции или в результате взрыва атомной бомбы, или лучевая терапия, такая как терапия рака,
- рак, такой как острый лимфобластный лейкоз, острый миелоидный лейкоз, карцинома коры надпочечников, лимфома, связанная со СПИД, рак анального канала, рак аппендикса, астроцитома I степени (анапластическая), астроцитома II степени, астроцитома III степени, астроцитома IV степени, атипическая тератоидная/рабдоидная опухоль центральной нервной системы, базальноклеточная карцинома, рак мочевого пузыря, рак молочной железы, саркома молочной железы, рак бронхов, бронхоальвеолярная карцинома, лимфома Беркитта, рак шейки матки, хронический лимфоцитарный лейкоз, хронический миелогенный лейкоз, рак толстой кишки, колоректальный рак, краниофарингиома, кожная Т-клеточная лимфома, рак эндометрия, эндометриальный рак матки, эпендимобластома, эпендимома, рак пищевода, эстезионейробластома, Саркома Юинга, экстракраниальная герминогенная опухоль, экстрагонадная герминогенная опухоль, рак внепеченочных желчных протоков, фиброзная гистиоцитома, рак желчного пузыря, рак желудка, карциноидная опухоль желудочно-кишечного тракта, стромальная опухоль желудочно-кишечного тракта, гестационная трофобластическая опухоль, гестационная трофобластическая опухоль, глиома, волосатоклеточный лейкоз, рак головы и шеи, рак сердца, печеночноклеточный рак, внутрипротоковая холангиокарцинома, лимфома Ходжкина, гипофарингеальный рак, внутриглазная меланома, опухоль из островковых клеток, Саркома Капоши, гистиоцитоз из клеток Лангерганса, крупноклеточная недифференцированная карцинома легкого, рак гортани, рак губы, аденокарцинома легкого, лимфома, макроглобулинемия, злокачественная фиброзная гистиоцитома, медуллобластома, медуллоэпителиома, меланома, карцинома из клеток Меркеля, мезотелиома, эндокринная неоплазия, множественная миелома, грибовидный микоз, миелодисплазия, миелодисплазия/миелопролиферативные новообразования, миелопролиферативные нарушения, рак носовой полости, рак носоглотки, нейробластома, неходжкинская лимфома, рак полости рта, рак ротоглотки, остеосаркома, светлоклеточная карцинома яичника, эпителиальный рак яичника, герминогенная опухоль яичника, рак поджелудочной железы, папилломатоз, рак околоносовых пазух, рак паращитовидной железы, рак пениса, рак глотки, пинеальная паренхимальная опухоль, пинеобластома, опухоль гипофиза, новообразование из клеток плазмы, новообразование из клеток плазмы, плевропульмональная бластома, первичная лимфома центральной нервной системы, рак предстательной железы, рак прямой кишки, почечно-клеточный рак, рак дыхательных путей с изменениями хромосомы 15, ретинобластома, рабдомиосаркома, рак слюнной железы, Синдром Сезари, мелкоклеточный рак легкого, рак тонкого кишечника, саркома мягких тканей, плоскоклеточная карцинома, плоскоклеточный немелкоклеточный рак легкого, плоскоклеточный рак шеи, супратенториальная примитивная нейроэктодермальная опухоль, супратенториальная примитивная нейроэктодермальная опухоль, рак яичка, рак горла, карцинома вилочковой железы, тимома, рак щитовидной железы, рак почечной лоханки, рак мочеиспускательного канала, саркома матки, рак влагалища, рак женских наружных половых органов, макроглобулинемия Вальденстрема или опухоль Вильмса,
- нарушения, связанные с воспалением желудка и/или пищевода, такие как кислотный рефлюкс.
В WO 2011/119722 показано, что анатабин снижает транскрипцию, опосредованную ядерным фактором κΒ (NFKB). NFKB представляет собой транскрипционный фактор, который функционирует в клетках, участвующих в воспалительных и иммунных реакциях. NFKB-опосредованная транскрипция связана с разнообразными нарушениями, включая нарушения с воспалительным компонентом, нарушенным иммунным ответом и/или ненадлежащей пролиферацией клеток. Заявленный глутарат анатабина особенно подходит для лечения нарушений, включающих «NFKB-опосредованный воспалительный компонент», т.е. воспаление, характеризующееся, вызванное, являющееся результатом или подверженное влиянию NFKB-опосредованной транскрипции. NFKB-опосредованную транскрипцию связывают с разными заболеваниями. С учетом неожиданной эффективности глутарата анатабина в отношении нарушения или прекращения указанной ключевой связанной с воспалением активности можно ожидать, что глутарат анатабина обладает широким спектром терапевтических применений. Таким образом, как ожидается, соединения, кристаллы, полиморфные формы и фармацевтические композиции согласно настоящему изобретению могут подходить для лечения или профилактики разных заболеваний, приведенных выше.
Соединения, кристаллы, полиморфные формы и/или фармацевтические композиции согласно настоящему изобретению также можно применять совместно с (т.е. до, после или во время) другими способами терапии какого-либо нарушения с NFKB-опосредованным компонентом. В некоторых вариантах реализации указанные способы терапии включают другие продукты, которые ингибируют выработку NFKB-опосредованных воспалительных частиц. Указанные продукты включают, но не ограничиваются указанными, дексаметазон, глюкокортикоиды (например, преднизон, метилпреднизолон), циклоспорин, такролимус, деоксиспергуалин, нестероидные противовоспалительные препараты (НПВП), такие как аспирин и другие салицилаты, тепоксалин, синтетические пептидные ингибиторы протеасомы, антиоксиданты (например, N-ацетил-L-цистеин, витамин C, витамин E, производные дитиокарбамата, куркумин), IL-10, оксид азота (II), цАМФ, золотосодержащие соединения и глиотоксин.
Соединения, кристаллы, полиморфные формы и фармацевтические композиции согласно настоящему изобретению могут быть введены индивидууму в дозе, достаточной для ослабления симптома нарушения с компонентом с NFKB-опосредованной транскрипцией.
Также, в частности, в Paris et al. (2013) Europan Journal of Pharmacology 698, 145-153, было показано, что анатабин обладает противовоспалительной активностью как в периферической, так и в ЦНС, посредством регулирования сигнальных систем STAT3 и NFkB. Соответственно, соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению могут, одновременно с или в качестве альтернативы с NFKB, ингибировать и STAT3. Заявленный глутарат анатабина особенно подходит для лечения нарушений, включающих «STAT3-опосредованный воспалительный компонент», т.е. воспаление, характеризующееся, вызванное, являющееся результатом или подверженное влиянию STAT3-опосредованной транскрипции. STAT3-опосредованную транскрипцию связывают с разными заболеваниями. С учетом неожиданной эффективности глутарата анатабина в отношении нарушения или прекращения указанной ключевой связанной с воспалением активности можно ожидать, что глутарат анатабина обладает широким спектром терапевтических применений. Таким образом, как ожидается, соединения, кристаллы, полиморфные формы и фармацевтические композиции согласно настоящему изобретению могут подходить для лечения или профилактики разных заболеваний, приведенных выше.
Соединения, кристаллы, полиморфные формы и/или фармацевтические композиции согласно настоящему изобретению также можно применять совместно с (т.е. до, после или во время) другими способами терапии какого-либо нарушения с STAT3-опосредованным компонентом. В некоторых вариантах реализации указанные способы терапии включают другие продукты, которые ингибируют выработку STAT3-опосредованных воспалительных частиц. В конкретном варианте реализации соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению обладает ингибирующим эффектом в отношении как STAT3, так и NFKB.
Соединения, кристаллы, полиморфные формы и фармацевтические композиции согласно настоящему изобретению могут быть введены индивидууму в дозе, достаточной для ослабления симптома нарушения с компонентом с STAT3-опосредованной транскрипцией.
В другом варианте реализации настоящего изобретения выделенная форма глутарата анатабина может быть введена для предотвращения или лечения наркотической зависимости. Глутарат анатабина может быть введен индивидуумам, страдающим от наркотической зависимости, для преодоления зависимости. Глутарат анатабина также может быть введен индивидуумам, преодолевшим наркотическую зависимость, для предотвращения рецидивов. Кроме того, глутарат анатабина может быть введен индивидуумам, не страдающим от наркотической зависимости, для предотвращения появления у них наркотической зависимости. Вещество, вызывающее зависимость, предпочтительно выбрано из группы, состоящей из никотина, кокаина, героина, марихуаны и алкоголя.
В WO 2012/2005885 показано, что композиции, содержащие анатабин, эффективны для временного снижения тяги к курению, ослабления влечения к никотину, лечения после отказа от курения, симптомов после отказа от табака, табачной зависимости, снижения массы тела и/или родственных нарушений, даже не связанных с наличием никотина. Сообщалось, что анатабин и другие второстепенные алкалоиды также связывают никотиновые рецепторы. В WO2015/009500 дополнительно показано, что анатабин может активировать никотиновые ацетилхолиновые рецепторы человека, но, вероятно, крайне высокие концентрации, превышающие любые рекомендованные или переносимые дозы, требуются для выработки значительных агонистических эффектов. Это предположение подтверждается поведенческими данными, которые показали, что грызуны, обученные самостоятельному введению никотина, не считают анатабин источником подкрепляющего действия, и что введение анатабина не обращает вспять спровоцированную никотиновую абстиненцию. Настоящее изобретение основано на том неожиданном открытии, что глутарат анатабина особенно эффективен в указанном отношении. Кроме того, конкретные кристаллические/полиморфные формы, такие как предложено в настоящем документе, являются особенно эффективными.
В дополнительном варианте реализации в настоящем изобретении предложен способ лечения определенных медицинских, психиатрических и/или неврологических состояний или нарушений. В одном из вариантов реализации изобретения способ включает введение эффективного для ингибирования MAO количества соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению млекопитающему, в частности, человеку, для лечения медицинских, психиатрических и/или неврологических состояний и нарушений, включая, но не ограничиваясь указанными, болезнь Альцгеймера, болезнь Паркинсона, большую депрессию, малую депрессию, атипичную депрессию, дистимию, расстройство дефицита внимания, гиперактивность, расстройство поведения, нарколепсию, социофобию, обсессивно-компульсивное расстройство, атипичную лицевую боль, расстройства пищевого поведения, наркотические абстинентные синдромы и синдромы лекарственной зависимости, включая зависимость от алкоголя, опиоидов, амфетаминов, кокаина, табака и каннабиса (марихуаны), меланхолию, паническое расстройство, булимию, анергическую депрессию, устойчивую к лечению депрессию, головную боль, синдром хронической боли, генерализованное тревожное расстройство и другие состояния, при которых изменение активности МАО может иметь терапевтическую ценность.
В дополнительном варианте реализации изобретения способ включает введение эффективного для ингибирования MAO количества соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению млекопитающему, в частности, человеку, для лечения медицинских, психиатрических и/или неврологических состояний и нарушений, включая, но не ограничиваясь указанными, болезнь Альцгеймера, болезнь Паркинсона, большую депрессию, малую депрессию, атипичную депрессию, дистимию, расстройство дефицита внимания, гиперактивность, расстройство поведения, нарколепсию, социофобию, обсессивно-компульсивное расстройство, атипичную лицевую боль, расстройства пищевого поведения, наркотические абстинентные синдромы и синдромы лекарственной зависимости, включая зависимость от алкоголя, опиоидов, амфетаминов, кокаина, табака и каннабиса (марихуаны), меланхолию, паническое расстройство, булимию, анергическую депрессию, устойчивую к лечению депрессию, головную боль, синдром хронической боли, генерализованное тревожное расстройство и другие состояния, при которых изменение активности МАО может иметь терапевтическую ценность.
В дополнительном варианте реализации изобретения способ включает введение эффективного для ингибирования MAO количества соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению млекопитающему, в частности, человеку, для лечения медицинских, психиатрических и/или неврологических состояний и нарушений, включая, но не ограничиваясь указанными, болезнь Альцгеймера, болезнь Паркинсона, большую депрессию, малую депрессию, атипичную депрессию, дистимию, расстройство дефицита внимания, гиперактивность, расстройство поведения, нарколепсию, социофобию, обсессивно-компульсивное расстройство, атипичную лицевую боль, расстройства пищевого поведения, наркотические абстинентные синдромы и синдромы лекарственной зависимости, включая зависимость от алкоголя, опиоидов, амфетаминов, кокаина, табака и каннабиса (марихуаны), меланхолию, паническое расстройство, булимию, анергическую депрессию, устойчивую к лечению депрессию, головную боль, синдром хронической боли, генерализованное тревожное расстройство и другие состояния, при которых изменение активности МАО может иметь терапевтическую ценность.
В дополнительном варианте реализации изобретения способ включает введение эффективного для ингибирования MAO количества соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению в виде содержащих их жевательных резинок и леденцов млекопитающему, в частности, человеку, для лечения медицинских, психиатрических и/или неврологических состояний и нарушений, включая, но не ограничиваясь указанными, болезнь Альцгеймера, болезнь Паркинсона, большую депрессию, малую депрессию, атипичную депрессию, дистимию, расстройство дефицита внимания, гиперактивность, расстройство поведения, нарколепсию, социофобию, обсессивно-компульсивное расстройство, атипичную лицевую боль, расстройства пищевого поведения, наркотические абстинентные синдромы и синдромы лекарственной зависимости, включая зависимость от алкоголя, опиоидов, амфетаминов, кокаина, табака и каннабиса (марихуаны), меланхолию, паническое расстройство, булимию, анергическую депрессию, устойчивую к лечению депрессию, головную боль, синдром хронической боли, генерализованное тревожное расстройство и другие состояния, при которых изменение активности МАО может иметь терапевтическую ценность.
В еще одном дополнительном варианте реализации соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению могут быть введены для лечения/предотвращения нарушения или заболевания из группы расстройств аутистического спектра (РАС). Расстройства аутистического спектра (РАС) представляют собой общие расстройства психологического развития, диагностируемые в раннем детстве при утрате приобретенных навыков или задержке приобретения новых навыков. РАС проявляются в раннем детстве и связаны с разными степенями нарушения коммуникативных функций и социальных навыков, помимо повторяющихся и стереотипных форм поведения. Во многих случаях (25%-50%) после периода предположительно нормального развития его направление резко изменяется по мере утраты приобретенных навыков или задержки приобретения новых навыков. Примеры расстройств аутистического спектра включают «классический» аутизм, синдром Аспергера, синдром Ретта, детское дезинтегративное расстройство и атипичный аутизм, который иначе называют неуточненным общим расстройством психологического развития (PDD-NOS).
Аутизм представляет собой детский психоз, возникающий в младенческом возрасте и характеризующийся широким спектром психологических симптомов, прогрессирующих с возрастом (например, отсутствие ответственности в социальных отношениях, отклонения языковых навыков и потребность в постоянном наличии стимулов окружающей среды). В общем случае, он возникает у детей в возрасте от двух до трех лет и приводит к утрате развитых навыков, ранее приобретенных ребенком. Индивидуумы с аутизмом подвержены повышенному риску развития судорожных расстройств, таких как эпилепсия.
В толстой кишке, пищеводе и двенадцатиперстной кишке у пациентов с аутизмом был обнаружен избыточный уровень воспаления, и в посмертных исследованиях также было показано повышение уровня экспрессии нескольких маркеров нейровоспаления (см. таблицу 1). Провоспалительные цитокины, включая ФНОα и IL-1, вырабатываются в повышенных количествах у подгруппы пациентов с аутизмом, это указывает на наличие у указанных пациентов избыточных врожденных иммунных ответов и/или на нарушенную выработку регуляторных цитокинов для T-клеточных ответов (например, 20030148955). Выделенные формы анатабина, включая S-(-)-анатабин, или соли указанных выделенных форм особенно подходят для лечения нарушений, включающих «NFκB-опосредованный воспалительный компонент», т.е. воспаление, характеризующееся, вызванное, являющееся результатом или подверженное влиянию NFκB-опосредованной транскрипции. Таким образом, соединение формулы I (например, анатабин или S-(-)-анатабин или его фармацевтически приемлемая соль) в выделенной форме может подходить для лечения или ослабления симптома РАС. Применение выделенных форм соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению предотвращает токсичность, связанную с табаком, экстрактами табака, экстрактами алкалоидов и никотином.
Нейровоспаление представляет собой точно установленный ответ на повреждение центральной нервной системы (Minghetti, Curr Opin Neurol 2005; 18:315-21). Исследования патологии у человека, in vitro и in vivo исследования болезни Альцгеймера позволили предположить, что опосредованный клетками глии нейровоспалительный ответ как участвует в патофизиологии заболевания (Mrak & Griffin, Neurobiol Aging 26:349-54, 2005), так и является мишенью для лечения (Hu et al., Bioorgan Med Chem Lett 17:414-18, 2007; Ralay et al„ J Neurosci 26:662-70, 2006; Crafl et al., Exp Opin Therap Targets 9:887-900, 2005). Было сделано предположение о том, что активация клеток микроглии, приводящая к повышенной экспрессии IL-1, является ключевой стадией для инициирования самораспространяющегося цитокинового цикла, конечным итогом которого является нейродегенерация (Mrak & Griffin, Neurobiol Aging 26:349-54, 2005; Sheng el al., Neurobiol Aging 17:761-66. 1996). IL-1β и провоспалительные цитокины могут функционировать при эпилепсии в качестве проконвульсивных сигнальных молекул, не зависящих от указанного цикла (Vezzani et al., Epilepsia 43:S30- S35, 2002), что обеспечивает возможную терапевтическую мишень при эпилепсии и других судорожных расстройствах (Vezzani & Granata, Epilepsia 46: 1724-43, 2005).
В некоторых вариантах реализации выделенную форму соединения, кристалл, полиморф и/или фармацевтическую композицию согласно изобретению вводят для лечения приступов, включая генерализованные и парциальные приступы.
Как описано в The Pharmacological Basis of Therapeutics, 9е изд., (McGraw-Hill), имеются два класса приступов: парциальные приступы и генерализованные приступы. Парциальные приступы включают фокальные и локальные приступы. Парциальные приступы дополнительно подразделяют на простые парциальные приступы, сложные парциальные приступы и парциальные приступы с вторичной генерализацией. Генерализованные приступы подразделяют на судорожные и несудорожные приступы. Их дополнительно подразделяют на абсансные (которые ранее называли малыми) приступы, атипичные абсансные приступы, миоклонические приступы, клонические приступы, тонические приступы, тонико-клонические приступы и атонические приступы.
Генерализованные приступы включают инфантильные спазмы, абсансные приступы, тонико-клонические приступы, атонические приступы и миоклонические приступы. Нарушение двигательной функции и потеря сознания являются основными отличительными признаками указанных приступов. Пациент также может ощущать эпилептическую ауру с сенсорными, автономными или психическими признаками. Аура может включать парестезию, появление эпигастральных признаков, нарушения обоняния, чувство страха или ощущение дежавю. За генерализованным приступом часто следует постиктальное состояние, при котором пациент может глубоко спать, испытывать спутанность сознания и/или головную боль или боль в мышцах. Паралич Тодда (слабость конечностей, противоположная очагу приступа) может проявляться в постиктальном состоянии.
Инфантильные спазмы характеризуются частым сгибанием и сложением рук и наклоном туловища вперед, как правило, имеющим короткую продолжительность. Они происходят только в первые 5 лет жизни.
Типичные абсансные приступы (также называемые малыми приступами) характеризуются потерей сознания с дрожанием век, как правило, в течение 10-30 секунд или более. Потеря аксиального мышечного тонуса может происходить или может не происходить. Судороги отсутствуют; вместо этого пациенты резко прекращают деятельность, а затем резко возобновляют ее, часто не осознавая, что произошел приступ. Абсансные приступы определяются генетикой. Они возникают преимущественно у детей, часто по нескольку раз за день.
Атипичные абсансные приступы возникают в рамках синдрома Леннокса-Гасто, тяжелой формы эпилепсии. Они длятся дольше чем типичные абсансные приступы, а резкие подергивания мышц или непроизвольные движения более выражены.
Атонические приступы чаще всего возникают у детей, как правило, в рамках синдрома Леннокса-Гасто. Они характеризуются полной потерей мышечного тонуса и сознания.
Тонические приступы также чаще всего возникают у детей, как правило, в рамках синдрома Леннокса-Гасто. Они характеризуются тоническим (устойчивым) сокращением аксиальных и проксимальных мышц, обычно во время сна, которое длится от 10 до 15 секунд. При более длительных тонических приступах в конце приступа могут происходить резкие клонические подергивания мышц.
Тонико-клонические приступы, также называемые большими приступами, могут представлять собой приступы с первичной или вторичной генерализацией. Пациент, испытывающий первично-генерализованный тонико-клонический приступ, часто вскрикивает, а затем теряет сознание и падает. Затем начинаются тонические сокращения, за которыми следуют клонические (быстро чередующееся сокращение и расслабление) движения мышц конечностей, туловища и головы. Пациент может терять способность удержания мочи и кала, прикусывать язык, может появляться пена изо рта. Приступы, как правило, длятся от 1 до 2 минут. Аура не возникает. Вторично-генерализованные тонико-клонические приступы начинаются с простых парциальных или сложных парциальных приступов, а затем прогрессируют до генерализованного приступа.
Миоклонические приступы характеризуются краткосрочными резкими подергиваниями конечности, нескольких конечностей или туловища. Они могут повторяться и приводить к тонико-клоническим приступам. Подергивания могут быть двусторонними или односторонними. Потеря сознания не происходит, если только приступы не прогрессируют до генерализованного тонико-клонического приступа.
Ювенильная миоклоническая эпилепсия представляет собой эпилептический синдром, характеризующийся миоклоническими, тонико-клоническими и абсансными приступами. Пациентами, как правило, являются подростки. Приступы, как правило, начинаются с двусторонних синхронных миоклонических подергиваний, после которых в 90% случаев следуют генерализованные тонико-клонические приступы. Они часто возникают при подъеме по утрам. Треть пациентов может отмечать абсансные приступы.
Фебрильные приступы связаны с повышением температуры, но не с внутричерепной инфекцией. Доброкачественные фебрильные приступы характеризуются генерализованными тонико-клоническими приступами короткой продолжительности. Указанные приступы распространены у детей и поражают вплоть до четырех процентов детей младше шести лет. Осложненные фебрильные приступы характеризуются фокальными приступами продолжительностью более пятнадцати минут или происходящими более двух раз за двадцать четыре часа. У двух процентов детей с фебрильными приступами впоследствии развивается судорожное расстройство. Риск этого повышен у детей с осложненными фебрильными приступами, с уже существующими неврологическими отклонениями, с приступами, проявившимися в возрасте до 1 года или с семейным анамнезом судорожных расстройств.
Эпилептический статус представляет собой судорожное расстройство, характеризующееся тонико-клонической судорожной готовностью, продолжающейся более пяти-десяти минут, или двумя или более приступами, между которыми пациенты не полностью приходят в сознание. При отсутствии лечения приступы продолжительностью более шестидесяти минут могут вызывать повреждение головного мозга или смерть.
Сложный парциальный эпилептический статус и эпилептический статус абсансов характеризуются продолжительными приступами с изменениями психического статуса. Генерализованный судорожный эпилептический статус может быть связан с резким прекращением приема противосудорожных средств или с травмой головы.
Простые парциальные приступы характеризуются двигательными, сенсорными или психомоторными симптомами без потери сознания. Приступы в разных частях головного мозга часто вызывают разные симптомы.
Аура часто предшествует сложным парциальным приступам. Пациенты, как правило, осознают обстановку, в которой они находятся, но могут испытывать нарушение сознания. Пациенты также могут испытывать оральный автоматизм (непроизвольное жевание или причмокивание губами), автоматизм кистей рук или конечностей (непроизвольные бесцельные движения), издание неразборчивых звуков, тоническое или дистоническое «застывание» контралатеральной конечности относительно очага приступа, девиацию головы и глаз, как правило, в направлении, противоположном очагу приступа, и движения ног, напоминающие езду на велосипеде или кручение педалей, в частности, если приступ происходит в медиальной фронтальной или орбито-фронтальной области головы. Двигательные симптомы исчезают через одну или две минуты, и часто наблюдается спутанность сознания и потеря ориентации через одну-две минуты после постиктальной амнезии.
Эпилепсия является важным примером судорожного расстройства. «Эпилепсия» описывает группу нарушений центральной нервной системы, которые характеризуются повторяющимися приступами, которые являются внешним проявлением чрезмерной и/или гиперсинхронной аномальной электрической активности нейронов коры головного мозга и других областей головного мозга. Указанная аномальная электрическая активность может проявляться в виде двигательных, судорожных, сенсорных, автономных или психических симптомов.
Сотни эпилептических синдромов были определены как расстройства, характеризующиеся специфическими симптомами, которые включают приступы эпилепсии. Они включают, но не ограничиваются указанными, абсансную эпилепсию, психомоторную эпилепсию, эпилепсию височной доли, эпилепсию лобной доли, эпилепсию затылочной доли, эпилепсию теменной доли, синдром Леннокса-Гасто, энцефалит Расмуссена, детскую абсансную эпилепсию, Синдром Рамсея-Ханта II типа, доброкачественный эпилептический синдром, доброкачественную инфантильную энцефалопатию, доброкачественные судороги новорожденных, раннюю миоклоническую энцефалопатию, прогрессирующую эпилепсию и инфантильную эпилепсию. Пациент может страдать от любой комбинации разных типов приступов. Наиболее распространены парциальные приступы, которые составляют примерно 60% от всех типов приступов.
Примеры генерализованных приступов, которые можно лечить, включают инфантильные спазмы, типичные абсансные приступы, атипичные абсансные приступы, атонические приступы, тонические приступы, тонико-клонические приступы, миоклонические приступы и фебрильные приступы. Примеры парциальных приступов, которые можно лечить, включают простые парциальные приступы, поражающие лобную долю, контралатеральную лобную долю, дополнительную моторную кору, островок головного мозга, островково-орбито-фронтальную кору, антеромедиальную часть височной доли, миндалины (включая оперкулярную и/или другие области), височную долю, заднюю часть височной доли, миндалину, гиппокамп, теменную долю (включая сенсорную кору и/или другие области); затылочную долю и/или другие области головного мозга.
В некоторых вариантах реализации выделенную форму соединения, кристалл, полиморф и/или фармацевтическую композицию согласно изобретению вводят для лечения эпилептического синдрома, включая, но не ограничиваясь указанными, абсансную эпилепсию, психомоторную эпилепсию, эпилепсию височной доли, эпилепсию лобной доли, эпилепсию затылочной доли, эпилепсию теменной доли, синдром Леннокса-Гасто, энцефалит Расмуссена, детскую абсансную эпилепсию, синдром Рамсея-Ханта II типа, доброкачественный эпилептический синдром, доброкачественную инфантильную энцефалопатию, доброкачественные судороги новорожденных, раннюю миоклоническую энцефалопатию, прогрессирующую эпилепсию и инфантильную эпилепсию.
Выделенная форма соединения, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению также могут подходить для лечения ауры, сопровождающей приступы. Таким образом, также можно лечить нарушения сознания, оральный автоматизм, автоматизм кистей рук или конечностей, издание неразборчивых звуков, тоническое или дистоническое «застывание» конечностей, девиацию головы и глаз, движения ног, напоминающие езду на велосипеде или кручение педалей, и другие симптомы, включающие ауру.
Судороги новорожденных связаны с проявляющимся позднее нарушениями нейро-психологического развития и когнитивной функции, включая умственную отсталость, аутизм и эпилепсию, и по оценкам, до 40% пациентов с аутизмом страдают эпилепсией или имеют приступы в анамнезе или приступы, происходившие ранее. Соответственно, важными целевыми пациентами являются младенцы, в частности, новорожденные, а также люди, имеющие в личном или семейном анамнезе приступы, умственную отсталость или аутизм.
В настоящем изобретении также предложены способы и композиции для лечения пациента после приступа. В одном из вариантов реализации выделенную форму соединения, кристалл, полиморф и/или фармацевтическую композицию согласно изобретению вводят совместно со вторым терапевтическим агентом, таким как ингибитор нейротрансмиттерного рецептора (например, ингибитор рецептора AMPA, рецептора AMPA, рецептора GABA, хлоридных котранспортеров или метаботропного глутаматного рецептора), ингибитор киназы/фосфатазы (например, ингибитор кальмодулин-зависимой киназы II (CamK II), протеинкиназы A (PKA), протеинкиназы С (ПКК), MAP киназы, Src-киназы, ERK киназы или фосфатазы кальциневрина), и/или ингибитор трансляции белка.
Ингибиторы кальмодулин-зависимой киназы II (CamK II) включают KN-62, W-7, HA-1004, HA-1077 и стауроспорин. Ингибиторы протеинкиназы A (PKA) включают H-89, HA-1004, H-7, H-8, HA-100, PKI и стауроспорин.
Ингибиторы протеинкиназы C (PKC) включают конкурентные ингибиторы АТФ-связывающего участка PKC, включая стауроспорин и его бисиндолилмалеимидные производные, Ro-31-7549, Ro-31-8220, Ro-31-8425, Ro-32-0432 и сангивамицин; лекарственные средства, которые взаимодействуют с регуляторным доменом PKC посредством конкурентного взаимодействия по участкам связывания диацилглицерина и сложных эфиров форбола, такие как калфостин C, сафингол, D-эритросфингозин; лекарственные средства, которые нацелены на каталитический домен PKC, такие как хелеритрина хлорид и мелиттин; лекарственные средства, которые ингибируют PKC посредством ковалентного связывания PKC под действием УФ-излучения, такие как деквалиния хлорид; лекарственные средства, которые специфически ингибируют Ca-зависимую PKC, такие как Go6976, Go6983, Go7874 и другие гомологи, полимиксина B сульфат; лекарственные средства, содержащие конкурентные пептиды, выделенные из последовательности PKC; и ингибиторы [0056]PKC, такие как кардиотоксины, эллагиновая кислота, HBDDE, 1-O-гексадецил-1-2-O-метил-рац-глицерин, гиперцин, K-252, NGIC-1, флоретин, пикеатаннол и тамоксифена цитрат.
Ингибиторы MAP киназы включают SB202190 и SB203580. Ингибиторы SRC включают PP1, PP2, ингибитор Src №5, SU6656 и стауроспорин. Ингибиторы ERK киназы включают PD 98059, SL327, оломуцин и 5-йодтуберцидин. Ингибиторы кальциневрина включают такролимус и циклоспорин.
Ингибиторы трансляции белка включают ингибиторы mTOR, такие как рапамицин, CCI-779 и RAD 001.
Выделенную форму соединения, кристалл, полиморф и/или фармацевтическую композицию согласно изобретению вводят индивидууму в дозе, достаточной для ослабления симптома расстройства аутистического спектра, или в дозе, достаточной для ослабления симптома судорожного расстройства. Дозы, как правило, составляют от примерно 1 мкг/кг до примерно 7 мг/кг массы тела (например, примерно 1, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4, 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9 или 5 мкг/кг или примерно 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4, 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9 или 5 мг/кг), от примерно 1,5 мкг/кг до примерно 5 мкг/кг, от примерно 1 мкг/кг до примерно 10 мкг/кг, от примерно 0,01 мг/кг до примерно 7 мг/кг массы тела, от примерно 0,1 мг/кг до примерно 5 мг/кг; от примерно 0,1 мг/кг до примерно 2 мг/кг, от примерно 1 мг/кг до примерно 3 мг/кг, от примерно 0,5 мг/кг до примерно 2 мг/кг, от примерно 1 мг/кг до примерно 2 мг/кг, от примерно 3 мг/кг до примерно 5 мг/кг, от примерно 2 мг/кг до примерно 4 мг/кг, от примерно 2 мг/кг до примерно 5 мг/кг или от примерно 0,5 мг/кг до примерно 1,5 мг/кг. Определенные факторы могут влиять на дозу, достаточную для ослабления симптома нарушения (т.е. на эффективную дозу), включая тяжесть заболевания или нарушения, предшествующее лечение, общее состояние здоровья, возраст и/или массу тела индивидуума, частоту введения, скорость высвобождения из композиции и другие имеющиеся заболевания. Указанная доза может быть разной в зависимости от факторов, таких как болезненное состояние, возраст и масса тела субъекта. Например, более высокие дозы могут быть введены для лечения состояний на запущенной стадии и/или угрожающих жизни. Режимы введения также могут быть скорректированы для обеспечения оптимального терапевтического ответа.
В некоторых вариантах реализации доза, достаточная для ослабления симптома нарушения, может включать несколько процедур введения. Например, индивидуум может получать лечение дозой выделенной формы соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению несколько раз в день (например, 2-12 или 4-10 раз в день), раз в день или реже, например, 1-6 раз в неделю. В других вариантах реализации вводимое соединение представляет собой соединение формулы I, IA или IB, которое вводят несколько раз в день (например, 2-12 или 4-10 раз в день), раз в день или реже, например, 1-6 раз в неделю. Лечение может длиться от примерно 1 до 10 недель (например, от 2 до 8 недель, от 3 до 7 недель, в течение примерно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 недель). Также следует понимать, что дозу в рамках режима введения, применяемого для лечения, можно повышать или снижать по ходу конкретного лечения.
В одном из вариантов реализации изобретения глутарат анатабина вводят пациенту для лечения или предотвращения наркотической зависимости или воспаления. Дозы, как правило, составляют от примерно 1 мкг/кг до примерно 7 мг/кг массы тела (например, примерно 1, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4, 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9 или 5 мкг/кг или примерно 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4, 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9 или 5 мг/кг), от примерно 1,5 мкг/кг до примерно 5 мкг/кг, от примерно 1 мкг/кг до примерно 10 мкг/кг, от примерно 0,01 мг/кг до примерно 7 мг/кг массы тела, от примерно 0,1 мг/кг до примерно 5 мг/кг; от примерно 0,1 мг/кг до примерно 2 мг/кг, от примерно 1 мг/кг до примерно 3 мг/кг, от примерно 0,5 мг/кг до примерно 2 мг/кг, от примерно 1 мг/кг до примерно 2 мг/кг, от примерно 3 мг/кг до примерно 5 мг/кг, от примерно 2 мг/кг до примерно 4 мг/кг, от примерно 2 мг/кг до примерно 5 мг/кг или от примерно 0,5 мг/кг до примерно 1,5 мг/кг. Определенные факторы могут влиять на дозу, достаточную для ослабления симптома нарушения (т.е. на эффективную дозу), включая тяжесть заболевания или нарушения, предшествующее лечение, общее состояние здоровья, возраст и/или массу тела индивидуума, частоту введения, скорость высвобождения из композиции и другие имеющиеся заболевания. Указанная доза может быть разной в зависимости от факторов, таких как болезненное состояние, возраст и масса тела субъекта. Например, более высокие дозы могут быть введены для лечения состояний на запущенной стадии и/или угрожающих жизни. Режимы введения также могут быть скорректированы для обеспечения оптимального терапевтического ответа.
Например, таблетки, содержащие примерно 600 мкг глутарата анатабина, вводят от одного до 25 раз в день (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 раз в день).
Доза, достаточная для ослабления симптома нарушения, необязательно может включать несколько процедур введения. Например, индивидуума можно лечить дозой выделенной формы глутарата анатабина несколько раз в день, раз в день или реже, например, 1-6 раз в неделю. Лечение воспаления может длиться от примерно 1 до 10 недель (например, от 2 до 8 недель, от 3 до 7 недель, в течение примерно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 недель). Введение глутарата анатабина для предотвращения воспаления можно проводить в течение неограниченных периодов времени, и дозу можно регулировать соответствующим образом. Глутарат анатабина можно вводить в течение неограниченного периода времени для предотвращения и лечения наркотической зависимости, по мере необходимости для удовлетворения тяги к веществу, вызывающему зависимость, или с интервалами, такими как раз в день, два раза в день или три или более раз в день, в зависимости от таких факторов, как количество глутарата анатабина и физиологическое состояние субъекта. Также следует понимать, что дозу в рамках режима введения, применяемого для лечения, можно повышать или снижать по ходу конкретного лечения.
Как правило, степень чистоты глутарата анатабина, применяемого в настоящем изобретении, составляет по меньшей мере примерно 95%, чаще по меньшей мере примерно 96%, примерно 97%, примерно 98% или более. Например, степень чистоты может составлять примерно 98,5%, 99,0%, 99,1%, 99,2%, 99,3%, 99,4%, 99,5%, 99,6%, 99,7%, 99,8%, 99,9% или более.
Глутарат анатабина может быть обеспечен совместно с другими ингредиентами, например, в виде эликсира, сольвата, напитка, жевательной конфеты, таблетки, леденца, жевательной резинки и т.д. В одном из вариантов реализации, например, напиток может иметь форму продукта на основе бутилированной воды, содержащего от примерно 100 мл до примерно 2000 мл очищенной воды и от примерно 0,00001 до примерно 0,0001 масс.% водорастворимой соли глутарата анатабина. Дополнительные неактивные ингредиенты могут быть добавлены для улучшения характеристик продукта, таких как вкус, цвет/прозрачность и/или стабильность. Продукт на основе бутилированной воды также может содержать другие предпочтительные компоненты, такие как витамины, белковые ингредиенты и т.д. Композиция, в качестве альтернативы, может быть обеспечена в твердой (например, порошковой) форме, такой как пакетик, и может быть объединена с водой или другой жидкостью (например, конечным потребителем) для получения напитка.
Фармацевтические композиции, содержащие соединения, кристаллы или полиморфные формы согласно настоящему изобретению, могут быть получены совместно с одним или более фармацевтически приемлемыми вспомогательными веществами. В настоящем документе термин «фармацевтически приемлемое вспомогательное вещество» обозначает нетоксичный инертный твердый, полутвердый или жидкий наполнитель, разбавитель, инкапсулирующий материал или добавку для состава любого типа. Например, сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлоза и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетат целлюлозы; порошковый трагакант; солод; желатин; тальк; вспомогательные вещества, такие как масло какао и воски для суппозиториев; масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные агенты, такие как гидроксид магния и гидроксид алюминия; альгиновая кислота; апирогенная вода; изотонический солевой раствор; раствор Рингера; этиловый спирт и фосфатные буферные растворы, а также совместимые смазывающие вещества, такие как лаурилсульфат натрия и стеарат магния, красители, высвобождающие агенты, агенты покрытий, подсластители, вкусоароматические добавки и ароматизаторы, консерванты и антиоксиданты, также могут присутствовать в композиции в соответствии с выбором специалиста, получающего состав.
Жидкие лекарственные формы для перорального введения включают приемлемые для применения в фармацевтике или пищевых продуктах эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. Помимо активных соединений, жидкие лекарственные формы могут содержать инертные разбавители, традиционно применяемые в данной области техники, такие как, например, вода или другие растворители, агенты, повышающие растворимость, и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилсульфоксид (ДМСО) диметилформамид, масла (в частности, хлопковое, арахисовое, кукурузное, зародышевое, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот и сорбитана, и их смеси. Помимо инертных разбавителей, пероральные композиции также могут включать адъюванты, такие как смачивающие агенты, эмульгаторы и суспендирующие агенты, подсластители, вкусоароматические добавки и ароматизаторы.
Жидкие фармацевтические композиции для применения в устройствах для термического испарения аэрозоля, как правило, содержат другие компоненты, такие как вода, органические растворители, подсластители и/или вкусоароматические добавки и т.д. Примеры растворителей, которые обычно применяют в жидких композициях для устройств для термического испарения аэрозоля, включают многоатомные спирты, такие как 1,2-пропиленгликоль (PG или MPG); одноатомные спирты, такие как этанол; этилацетат и т.д.. Количество присутствующей воды, как правило, составляет от примерно 0,1 до примерно 10 масс.%, обычно от примерно 0,5 до примерно 5 масс.%. Количество присутствующего органического растворителя, как правило, составляет от примерно 50 до примерно 99 масс.%, часто от примерно 75 до примерно 95 масс.%. При желании в композицию могут быть добавлены одна или более вкусоароматических добавок, неограничивающие примеры которых включают перечную мяту, ментол, винтергрен, колосистую мяту, прополис, эвкалипт, корицу и т.д. Общее количество вкусоароматических добавок, как правило, составляет от примерно 0,5 до примерно 15 масс.%, часто от примерно 1 до примерно 10 масс.% в пересчете на общую массу композиции. В качестве примера, количество глутарата анатабина может составлять от примерно 0,1 до примерно 25 мг, от примерно 0,5 до примерно 20 мг или от примерно 1 до примерно 10 мг на грамм композиции в целом.
Твердые лекарственные формы для перорального введения включают капсулы, таблетки, леденцы, пилюли, порошки и гранулы. В указанных твердых лекарственных формах активное соединение смешивают по меньшей мере с одним инертным приемлемым для применения в фармацевтике и пищевых продуктах вспомогательным веществом или носителем, таким как цитрат натрия или фосфат дикальция, и/или с a) наполнителями или объемообразующими веществами, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота, b) связывающими веществами, такими как карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и аравийская камедь, c) увлажнителями, такими как глицерин, d) разрыхлителями, такими как агар-агар, карбонат кальция, картофельный или тапиоковый крахмал, альгиновая кислота, некоторые силикаты и карбонат натрия, e) агентами, замедляющими растворение, такими как парафин, f) ускорителями всасывания, такими как четвертичные аммонийные соединения, g) смачивающими агентами, такими как цетиловый спирт и глицерилмоностеарат, h) абсорбентами, такими как каолин и бентонитовая глина, i) смазывающими веществами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси, и j) подсластителями, вкусоароматическими добавками, ароматизаторами и их смесями. В случае капсул, леденцов, таблеток и пилюль лекарственная форма также может содержать буферные агенты. Твердые лекарственные формы согласно изобретению могут быть получены с возможностью замедленного высвобождения.
Для продления эффекта соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению часто желательно замедлять всасывание вещества после подкожной или внутримышечной инъекции. Это может быть реализовано за счет применения жидкой суспензии кристаллического или аморфного вещества с плохой растворимостью в воде. В результате, скорость всасывания вещества зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера кристалла и кристаллической формы. В качестве альтернативы, задержка всасывания вводимой парентерально формы вещества реализуется путем растворения или суспендирования вещества в масляном носителе. Инъекционные формы депо получают путем формирования микроинкапсулированных матриц вещества в биоразлагаемых полимерах, таких как полилактид-полигликолид. При помощи отношения вещества к полимеру и природы конкретного применяемого полимера можно контролировать скорость высвобождения вещества. Примеры других биоразлагаемых полимеров включают сложные поли(ортоэфиры) и поли(ангидриды). Составы с пролонгированным высвобождением известны в данной области техники. Например, набухающие частицы изучаются в патентах США №5582837, 5972389 и 6723340. Полимерные матрицы изучаются в патентах США №6210710, 6217903 и 6090411. Типовыми материалами, применяемыми в составах с пролонгированным высвобождением, являются полимеры поли(этиленоксид) и гидроксипропилметилцеллюлоза. Инъекционные составы депо также получают путем заключения вещества внутри липосом или микроэмульсий, которые совместимы с тканями организма.
Фармацевтические композиции могут быть получены любым подходящим способом и не ограничены каким-либо конкретным способом получения. Например, глутарат анатабина можно объединять со вспомогательными веществами и связывающим веществом, а затем гранулировать. Гранулят можно смешивать в сухом виде с любыми оставшимися ингредиентами и прессовать в твердую форму, такую как таблетка.
Твердые лекарственные формы, такие как таблетки, капсулы, пилюли и гранулы, могут быть получены совместно с покрытиями и оболочками, такими как кишечнорастворимые покрытия и другие покрытия, хорошо известные в области фармацевтических составов. Они могут необязательно содержать замутнители и также могут иметь состав, при котором они высвобождают активный(-е) ингредиент(-ы) исключительно, или предпочтительно, в определенной части кишечного тракта или, необязательно, с задержкой или пролонгированным образом. Примеры заливочных композиций, которые можно применять, включают полимерные вещества и воски. Составы в форме таблеток с пролонгированным высвобождением также описаны в патенте США №5942244.
Фармацевтические композиции могут содержать любые традиционные нетоксичные фармацевтически приемлемые носители, адъюванты или наполнители. В некоторых случаях pH состава можно регулировать при помощи приемлемых для применения в фармацевтике или пищевых продуктах кислот, оснований или буферов для повышения стабильности получаемой композиции или формы для ее доставки.
Соединения, кристаллы, полиморфные формы и фармацевтические композиции согласно настоящему изобретению могут быть введены любым подходящим способом. Например, композиции могут быть введены перорально, парентерально, путем ингаляции, местно, ректально, интраназально, трансбуккально, внутривагинально, при помощи имплантируемого резервуара или могут употребляться внутрь в качестве пищевой добавки или продукта питания. Термин парентеральный в настоящем документе включает способы подкожной, внутрикожной, внутривенной, внутримышечной и интракраниальной инъекции или инфузии. Предпочтительные способы введения включают ингаляцию при помощи ингалятора сухих порошков или устройств для испарения аэрозоля, таких как устройство для термического испарения аэрозоля. Устройства для термического испарения аэрозоля описаны, например, в WO 02/098496, WO 02/098389 и WO 03/095012.
Один из аспектов изобретения относится к соединению, кристаллу или полиморфной форме согласно настоящему изобретению или к фармацевтической композиции для применения согласно изобретению в устройстве для термического испарения аэрозоля. Количество глутарата анатабина может быть разным в зависимости от таких факторов, как тип устройства для термического испарения аэрозоля и возможное наличие других активных компонентов. Устройство для термического испарения аэрозоля может иметь разные типы конфигураций, подробное описание которых не является частью настоящего изобретения. В общем случае, устройства для термического испарения аэрозоля могут представлять собой устройства для однократного или разового применения или могут быть выполнены с возможностью повторного наполнения жидкими композициями алкалоидов и/или введения картриджей, содержащих жидкие композиции, для облегчения повторного применения.
Другой аспект изобретения относится к соединению, кристаллу или полиморфной форме согласно настоящему изобретению или к фармацевтической композиции для применения согласно изобретению в ингаляторе сухих порошков. В технологии с применением ингалятора сухих порошков пакеты с сухим порошковым составом глутарата анатабина, помещенные в устройство, могут содержать разные количества, например, от 0,01 до 10 мг глутарата анатабина в каждой дозе, от 0,05 до 5 мг глутарата анатабина в каждой дозе или от 0,1 до 1 мг глутарата анатабина в каждой дозе, или может быть получен глутарат анатабина с разными концентрациями в виде частиц разного размера, и форма может содержать составы, которые модулируют скорость высвобождения и всасывания глутарата анатабина в организме после ингаляции. Они также могут содержать модуляторы pH и добавки, изменяющие вкус, запах или цвет. Превращение порошкового состава глутарата анатабина в аэрозоль может быть реализовано с использованием в качестве источника энергии дыхания потребителя или сжатого газа, или батарейки, которая питает электрический мотор с ходовым винтом, или источника колебаний, которые обеспечивают диспергирование порошка.
Благодаря обеспечению соединения, кристалла или полиморфной формы согласно настоящему изобретению или фармацевтической композиции для применения согласно изобретению в ингаляторе сухих порошков или устройстве для термического испарения аэрозоля тяга к традиционному курению табака может быть понижена и при этом минимизируется токсичность и другие нежелательные побочные эффекты, связанные с никотином и другими компонентами табака. Ингалятор сухих порошков или устройство для термического испарения аэрозоля можно применять по мере необходимости для удовлетворения тяги к курению или с интервалами, такими как раз в день, два раза в день или три или более раз в день, в зависимости от таких факторов, как концентрация активных компонентов и физиологическое состояние субъекта.
Таким образом, изобретение также относится к бездымному табачному продукту, содержащему соединение, кристалл, полиморф и/или фармацевтическую композицию согласно изобретению.
Бездымный табачный продукт содержит порошковую форму соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению. В одном из вариантов реализации бездымный табачный продукт, таким образом, содержит табак совместно с соединением, кристаллом, полиморфом и/или фармацевтической композицией согласно изобретению.
В одном из предпочтительных вариантов реализации настоящего изобретения бездымный табачный продукт представляет собой твердую жевательную форму, содержащую порошковый табак и соединение, кристалл, полиморф и/или фармацевтическую композицию согласно изобретению. Порошковый табак может быть получен из ферментированных табачных стеблей, листовых пластинок или обоих указанных материалов (которые далее, в целом, называют «табачным материалом»). Относительная доля табачного материала в бездымном табачном продукте зависит от таких факторов, как конкретный состав табачного листа. Твердая жевательная форма часто содержит от примерно 10% до примерно 80% порошкового табака по массе, чаще от примерно 25% до примерно 55% по массе.
Предпочтительно, ферментированный табачный материал растирают, например, измельчают, для получения порошкового табака. Таким образом, табачный материал измельчают достаточно мелко для обеспечения легко проглатываемого продукта. В качестве альтернативы, экстракт табачного материала сушат для получения порошка. В процессе экстракции ферментированный табачный материал экстрагируют растворителем, как правило, водой или водяным паром. Полученный раствор содержит водорастворимые компоненты табака, включая никотин. Затем раствор сушат, после чего измельчают по мере необходимости, для получения порошкового табака.
Затем можно применять порошковый табак для получения твердой жевательной формы. Тем не менее, перед получением твердой жевательной формы может требоваться обработка порошкового табака для получения более крупных частиц, такая как гранулирование или вальцевание и измельчение. Указанные способы обеспечивают частицы, которые значительно легче могут быть превращены в твердую жевательную форму, и формируют твердые жевательные формы, которые не распадаются при использовании и хранении в упаковке. Кроме того, более крупные частицы легче в использовании по сравнению с мелкими частицами и не образуют «пыль», как в случае мелких частиц порошка. Кроме того, более крупные частицы легче прессуются в твердые жевательные формы по сравнению с порошковыми частицами. Это позволяет повышать скорость получения твердых жевательных форм и упрощает механическую обработку твердых жевательных форм. Кроме того, применение как грануляции, так и вальцевания и прессования, обеспечивает равномерное распределение вкусоароматических добавок, красителей и т.д., в конечной твердой жевательной форме.
Другие аспекты настоящего изобретения относятся к соединению, кристаллу, полиморфу и/или фармацевтической композиции согласно изобретению для электронных сигарет, которые выполнены с возможностью обеспечения разнообразных композиций алкалоидов, содержащих соединение, кристалл, полиморф и/или фармацевтическую композицию согласно изобретению, для более эффективного обеспечения эффекта получения удовольствия от курения по сравнению с курением традиционных сигарет и, при этом, недопущения или снижения воздействия никотина. В одном из вариантов реализации композиция алкалоида содержит по меньшей мере примерно 25 масс.% соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению в пересчете на общую массу алкалоида. В некоторых примерах соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению представляет собой единственный алколоид, присутствующий в композиции, например, соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению составляет 100 масс.% от общей массы алкалоида. В других примерах может присутствовать вплоть до примерно 75 масс.% одного или более других алкалоидов, таких как никотин, норникотин и/или анабазин, помимо соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению. Например, соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению и никотин могут быть объединены при массовом отношении (анатабин к никотину) от примерно 50:1 до примерно 1:3 или от примерно 25:1 до примерно 1:2, от примерно 10:1 до примерно 3:2 или от примерно 5:1 до примерно 1:1.
Количество соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению, присутствующего(-ей) в композиции, может быть разным в зависимости от таких факторов, как тип электронной сигареты и возможное наличие других активных компонентов, таких как никотин и/или другие алкалоиды. В качестве примера, количество соединения, кристалла, полимофра и/или фармацевтической композиции согласно изобретению может составлять от примерно 0,1 до примерно 25 мг, от примерно 0,5 до примерно 20 мг или от примерно 1 до примерно 10 мг на грамм композиции в целом.
Помимо соединения, кристалла, полиморфа и/или фармацевтической композиции согласно изобретению, композиция может содержать вплоть до примерно 75 масс.% одного или более других алкалоидов, таких как никотин, норникотин и/или анабазин, в пересчете на общую массу алкалоидов. Указанные алкалоиды могут быть экстрагированы из табака или других растительных материалов и очищены известными способами и/или могут быть получены синтетически известными способами синтеза. Соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению и дополнительный(-е) алкалоид(-ы), такой(-ие) как никотин, могут быть объединены при массовом отношении (анатабин к другим алкалоидам, в целом) от примерно 50:1 до примерно 1:3 или от примерно 25:1 до примерно 1:2, от примерно 10:1 до примерно 3:2 или от примерно 5:1 до примерно 1:1.
Композиция, как правило, содержит другие компоненты, такие как вода, органические растворители, подсластители и/или вкусоароматические добавки и т.д. Примеры растворителей, которые традиционно применяют в жидких композициях для электронных сигарет, включают многоатомные спирты, такие как 1,2-пропиленгликоль (PG или MPG); одноатомные спирты, такие как этанол; этилацетат; и т.д. Количество присутствующей воды, как правило, составляет от примерно 0,1 до примерно 10 масс.%, часто от примерно 0,5 до примерно 5 масс.% Количество присутствующего органического растворителя, как правило, составляет от примерно 50 до примерно 99 масс.%, часто от примерно 75 до примерно 95 масс.%.
При желании в композицию могут быть добавлены одна или более вкусоароматических добавок, неограничивающие примеры которых включают перечную мяту, ментол, винтергрен, колосистую мяту, прополис, эвкалипт, корицу и т.д. Общее количество вкусоароматических добавок, как правило, составляет от примерно 0,5 до примерно 15 масс.%, часто от примерно 1 до примерно 10 масс.% в пересчете на общую массу композиции.
Электронная сигарета может иметь разные конфигурации. В целом, электронные сигареты могут представляет собой сигареты для однократного или разового применения или могут быть выполнены с возможностью повторного наполнения жидкими композициями алкалоидов и/или введения картриджей, содержащих жидкие композиции, для облегчения повторного применения. Один из примеров электронной сигареты показан на ФИГ. 1 в заявке на патент США US 15/679731. Устройство для ввода воздуха обеспечено на внешней стенке оболочки, в которой размещены светодиод, ячейка, электронная плата, полость с нормальным давлением, датчик, устройство отделения пара-жидкости, распылитель, бутыль для подачи жидкости, мундштук, микропереключатель, отверстие для вывода газа и канал для воздуха. Электронная плата имеет схему электронного переключения и высокочастотный генератор. Полость с отрицательным давлением обеспечена в датчике и отделена от датчика волнистой пленкой. Полость для распыления обеспечена в распылителе. Стопорное кольцо обеспечено для фиксации одной стороны бутыли для подачи жидкости относительно оболочки; и канал для аэрозоля обеспечен с другой стороны бутыли для подачи жидкости. Другие подробности описаны в патенте США №7832410 B2, автор Хон (Hon), описание которого включено в настоящий документ во всей полноте посредством ссылки.
За счет обеспечения сбалансированной композиции алкалоидов, содержащей соединение, кристалл, полиморф и/или фармацевтическую композицию согласно изобретению в качестве значительной части алкалоидного компонента, появляется возможность изготавливать электронные сигареты, которые снижают тягу к традиционному курению табака и при этом минимизируют токсичность и другие нежелательные побочные эффекты, связанные с никотином и другими компонентами табака. Электронную сигарету можно применять по мере необходимости для удовлетворения тяги к курению или с интервалами, такими как раз в день, два раза в день или три или более раз в день в зависимости от таких факторов, как концентрация активных компонентов и физиологическое состояние субъекта.
В альтернативном варианте реализации не содержащий табак состав содержит композицию алкалоидов, содержащую от примерно 25 масс.% до примерно 95 масс.% анатабина и от примерно 5 масс.% до примерно 75 масс.% второго алкалоида в пересчете на общую массу алкалоидов в композиции. Второй алкалоид может представлять собой никотин, норникотин, анабазин или комбинацию двух или более указанных веществ. Не содержащий табак продукт может иметь твердую жевательную форму с прессованным порошком, форму жевательной резинки, капсулы, пилюли, леденца и т.д. Термин «не содержащий табак» означает, что продукт по существу не содержит листья табака или экстракт табака, тем не менее, с тем исключением, что некоторые или все алкалоиды, присутствующие в не содержащем табак продукте, могут быть экстрагированы из табака и очищены традиционными способами, такими как жидкостная хроматография.
Дополнительные ингредиенты могут быть добавлены к не содержащим табак продуктам для улучшения вкуса или стабильности. Указанные дополнительные компоненты включают, но не ограничиваются указанными, подсластители, натуральные вкусоароматические добавки, искусственные вкусоароматические добавки, красители, антиоксиданты, консерванты, хелатообразующие агенты, модуляторы вязкости, регуляторы тоничности, отдушки, замутнители, суспендирующине агенты, связывающие вещества, загустители и их смеси, включая, но не ограничиваясь указанными, ксантановую камедь, карбоксиметилцеллюлозу, карбоксиэтилцеллюлозу, гидроксипропилцеллюлозу, метилцеллюлозу, микрокристаллическую целлюлозу, крахмалы, декстрины, ферментированную молочную сыворотку, тофу, мальтодекстрины, полиолы (включая сахарные спирты, такие как сорбит или маннит), углеводы (например, лактозу), альгинат пропиленгликоля, геллановую камедь, гуар, пектин, трагакантовую камедь, аравийскую камедь, камедь плодов рожкового дерева, гуммиарабик, желатин, маннит, натуральные и/или искусственные мятные ароматизаторы, сукралозу, диоксид кремния, стеариновую кислоту, гидроксипропилметилцеллюлозу, стеарат магния, диоксид титана, натуральную глазурь, метилпарабен, пропилпарабены, триэтилцитрат, лимонную кислоту, бутилированный гидрокситолуол (БГТ), моно- и диглицериды, полисорбат 80 и т.д.
Не содержащие табак продукты могут иметь разные формы, например, для перорального употребления, такие как пилюли, таблетки, капсулы, мягкие желатиновые капсулы, желатиновые капсулы, жидкости, сиропы, суспензии, порошки, жевательные пастилки, леденцы, жевательные резинки, жевательные пластинки, или для введения другими способами, например, парентерально, в распыляемом составе для ингаляции, через имплантируемый резервуар и т.д. Композиции алкалоидов также могут быть получены с возможностью введения с пищевыми продуктами или напитками. Например, они могут поставляться в виде высушенного или порошкового продукта для перерастворения водой или другим подходящим носителем перед применением (например, молоком, фруктовым соком и т.д.).
Соединение, кристалл, полиморф и/или фармацевтическая композиция или какая-либо другая композиция, предложенная в настоящем документе, могут дополнительно содержать один или более витаминов, таких как витамин A (ретинол), витамин B1 (тиамин), витамин C (аскорбиновая кислота), витамин D (кальциферол), витамин D2 (эргокальциферол), витамин D3 (холекальциферол), витамин B2 (рибофлавин), витамин E (токоферол), витамин B12 (кобаламин), витамин K1 (филлохинон), витамин B5 (пантотеновая кислота), витамин B7 (биотин), витамин B6 (пиридоксин), витамин B3 (ниацин), витамин B9 (фолиевая кислота). Способы синтеза витаминов хорошо известны, и витамины могут быть получены из любого надежного коммерческого источника. В некоторых вариантах реализации соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению дополнительно содержит витамин A. В некоторых вариантах реализации соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению дополнительно содержит витамин D3. В некоторых вариантах реализации соединение, кристалл, полиморф и/или фармацевтическая композиция согласно изобретению дополнительно содержит витамин A и витамин D3.
Количество анатабина и витаминов в композициях согласно настоящему изобретению может быть разным. В некоторых вариантах реализации количество соединения, кристалла, полиморфа составляет от примерно 0,1 мг до примерно 10 мг (например, примерно 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 3,0, 4,0, 5,0, 6,0, 7,0, 8,0, 9,0 или 10 мг).
В некоторых вариантах реализации количество витамина A составляет от примерно 200 до примерно 500 МЕ (например, примерно 200, 250, 300, 350, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 450, 475 или 500 МЕ). Витамин A может быть обеспечен, например, в виде ретинилацетата.
В некоторых вариантах реализации количество витамина D3 составляет от примерно 15 МЕ до примерно 50 МЕ (например, примерно 15, 20, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 40, 45 или 50 МЕ). Витамин D3 может быть обеспечен в виде холекальциферола.
В некоторых вариантах реализации соединение, кристалл и/или полиморф и витамин A обеспечены в равных относительных количествах (например, по 1 мг каждого). В некоторых вариантах реализации один или два леденца, содержащих 1 мг соединения, кристалла и/или полиморфа, можно принимать один, два или три раза в день. В некоторых вариантах реализации дневные дозы не превышают 1, 2, 3, 4, 5 или 6 леденцов. В некоторых вариантах реализации дневные дозы могут превышать 1, 2, 3, 4, 5 или 6 леденцов. В некоторых вариантах реализации продукт имеет форму леденца, который содержит 1 мг соединения, кристалла, полиморфа и/или композиции согласно изобретению, 417 МЕ витамина A (в виде ретинилацетата), 33 МЕ витамина D3 (в виде холекальциферола) и маннит, натуральные и искусственные мятные ароматизаторы, сукралозу, диоксид кремния, стеариновую кислоту, гидроксипропилметилцеллюлозу, стеарат магния, диоксид титана, натуральную глазурь, метилпарабены, пропилпарабены, триэтилцитрат, лимонную кислоту, БГТ, моно- и диглицериды и полисорбат 80.
В настоящем описании цитируется ряд документов, включая патентные заявки и научную литературу. Описание указанных документов, хотя и не рассматривают как значимое для патентоспособности настоящего изобретения, включено в настоящий документ во всей своей полноте посредством ссылок. Более конкретно, содержание всех справочных документов включено посредством ссылки в той же степени, как если бы конкретным образом и по отдельности было указано, что содержание каждого отдельного документа включено посредством ссылки.
Изобретение далее будет описано при помощи следующих примеров, которые являются исключительно иллюстративными и не должны толковаться как ограничивающие объем настоящего изобретения.
Примеры
Пример 1
Получение глутарата анатабина
Превращали свободное основание анатабина в 1:1 глутарат анатабина следующими способами:
a) В раствор глутаровой кислоты (16,5 г, 125 ммоль, 1,00 экв.) в ацетонитриле (500 мл) по каплям добавляли анатабин (20,0 г, 125 ммоль, 1,00 экв.) при 25°C и перемешивали смесь при 25°C в течение 1 часа. Анализ ТСХ (дихлорметан:метанол=20:1) указывал на израсходование анатабина (Rf=0,5). Фильтровали смесь. Собирали осадок и концентрировали досуха с получением глутарата анатабина (30,0 г, 103 ммоль, выход 82,2%, чистота 100%) в виде беловатого твердого вещества.
b) В раствор анатабина (11,6 г, 72 ммоль) в ацетонитриле (700 мл) добавляли глутаровую кислоту (9,6 г, 72 ммоль). Реакционная смесь становилась мутной. Затем грели реакционную смесь до получения прозрачного желтого раствора. Оставляли смесь охлаждаться до комнатной температуры (20°C) и перемешивали в течение 2 часов. Образовывалось клейкое твердое вещество, которое соскабливали шпателем. Перемешивали смесь еще 30 минут и отфильтровывали полученное бледно-желтое твердое вещество в атмосфере аргона, промывали ацетонитрилом (500 мл) и сушили при пониженном давлении при 45°C в течение 45 минут с получением глутарата анатабина (18,3 г, 87%) в виде бледно-желтого твердого вещества.
1H ЯМР (D2O), δ: 8,84-8,45 (m, 2H), 7,99 (d, J=7,8 Гц, 1H), 7,59-7,55 (m, 1H), 6,08 (d, J=8,4 Гц, 1H), 5,85 (d, J=10,4 Гц, 1H), 4,63-4,59 (m, 1H), 3,97-3,87 (m, 1H), 3,81-3,70 (m, 1H), 2,80-2,53 (m, 2H), 2,25 (t, J=7,6 Гц, 4H), 1,82-1,74 (m, 2H). Оценивали химическую чистоту глутарата анатабина на системе СВЭЖХ Waters Acquity UPLC H-class, оборудованной детектором PDA и масс-спектрометром SQD, колонкой BEH C18, 2,1×50 мм, 1,7 мкм, элюировали с градиентом, проводили детектирование при 261 нм. Время удерживания глутарата анатабина составляло 1,125 мин, чистота составляла 99,41%, [M+H]+ 161,0 (фиг. 3, 4). Сравнение спектров FTIR анатабина глутарата (фиг. 5) и свободного основания анатабина (фиг. 6) указывает на изменение полосы N-H, которое позволяет предположить образование соли.
Перекристаллизовывали глутарат анатабина, полученный таким образом, из 2,5 мл ацетонитрила при охлаждении после нагревания до температуры обратной конденсации. Выделяли твердую фазу и сушили.
Анализировали глутаратную соль анатабина путем рентгеновской порошковой дифракции (XRPD) в диапазоне 2-40°2Ɵ с использованием силиконовых пластин с нулевым фоном (с полостями 9 мм). Было обнаружено, что она имела чистоту более 99% согласно СВЭЖХ.
Пример 2
Ионная хроматография глутарата анатабина
Для изучения стехиометрии глутарата анатабина проводили ионный хроматографичесей анализ (фиг. 11). Растворяли глутарат анатабина в воде для ИХ (90 мкг/мл), анализировали раствор на ионном хроматографе с большим градиентом давления Metrohm 940 с использованием охлажденного автоматического пробоотборника Metrohm 889, раствора элюента 3,2 мМ карбонат натрия и 1 мМ бикарбонат натрия, раствора для регенерации 150 мМ серная кислота/100 мМ щавелевая кислота на колонке A Supp 5 (IC004 или эквивалент). Анализ глутарата анатабина проводили дважды, результаты приведены в следующей таблице:
(% (масс./масс.))
(% (масс./масс.))
Уровень выделения в 98,0% от теоретического подтверждает наличие глутарата при отношении 1:1 анатабин:глутарат. Результаты ионной хроматографии согласуются со спектром протонного ЯМР (фиг. 2).
Пример 3
Исследование динамической сорбции паров глутаратом анатабина
Помещали глутарат анатабина (20 мг) непосредственно в предварительно взвешенную кювету для образца и переносили в прибор (DVS1 Advantage). Использовали способ с двойным циклом 0-90-0-90-0% отн.вл. с шагом 10% отн.вл. Для образца был показан прирост массы на 55% во время первого цикла сорбции, при этом основной прирост массы происходил при отн.вл. более 70%. В первом цикле десорбции наблюдали снижение массы примерно на 50%, такой же результат наблюдали и во втором цикле, но при этом во втором цикле сорбции прирост массы составлял только примерно 50%. Указанный прирост массы согласуется с изотермой, на которой показан прирост массы примерно на 5% между начальной массой и конечной массой (фиг.10).
Пример 4
Титрование глутарата анатабина по Карлу Фишеру
Определяли количество воды в полученной глутарате анатабина на совмещенном волюметрическом/кулонометрическом титраторе по методу Карла Фишера Metrohm 852 Combined Volumetric/Coulometric Karl Fischer Titrando с термостатом 860 Oven с использованием 100 мг образца. Было обнаружено, что глутарат анатабина содержал 0,21% (масс./масс.) воды.
Пример 5
Оценка стабильности глутарата анатабина
Анализировали глутарат анатабина в момент времени T=0, а затем хранили аликвоту в стеклянной пробирке с завинчивающейся крышкой в условиях ускоренного состаривания (40°C/75% отн.вл.) в инкубаторе в течение 7 дней перед проведением дальнейшего анализа. Визуально оценивали образец после хранения для определения стабильности в моменты времени T=0, 3 и 7 дней, изменения окраски или какие-либо признаки расплывания не наблюдались. Также оценивали образец в момент времени T=0 и снова после хранения в течение T=7 дней путем ТГА, XRPD и ВЭЖХ-УФ.
На термограмме ТГА для образца через T=7 дней показано незначительное снижение массы в диапазоне 20-130°C, составляющее 0,5%, после этого происходило разлождение, и наблюдали снижение массы на 80% в диапазоне от 150°C до 400°C. При наложении термограмм, полученных в моменты T=0 дней и T=7 дней, были показаны незначительные различия, и разница в снижении массы составляла только 2%. Таким образом, можно увидеть, что изменения термической стабильности отсутствовали при хранении глутарата анатабина при 40°C/75% отн.вл. в течение 7 дней.
На дифрактограмме XRPD образца через T=7 дней отсутствуют различия по сравнению с дифрактограммой в момент времени T=0, материал сохранял исходную структуру, что, таким образом, указывает на отсутствие изменений кристаллической формы глутарата анатабина после хранения при 40°C/75% отн.вл. в течение 7 дней.
Для оценки стабильности путем ВЭЖХ-УФ готовили 200 мкг/мл раствор образца анатабина и глутарата анатабина в двух повторностях путем взвешивания примерно 10 мг и растворения в 50 мл мерной колбе и доведения колбы до объема деионизированной водой. Во время оптимизации способа ВЭЖХ настраивали продолжительность цикла и градиент для анализа стабильности. После оптимизации способа проводили испытание с принудительным разрушением для облегчения запланированного анализа для оценки стабильности путем определения любых продуктов разложения или примесей, присутствующих в образце глутарата анатабина. В испытании с принудительным разрушением анализировали образцы в пяти условиях - воздействие кислоты, основания, контроль, нагревание и окисление - и проводили исследования в моменты времени T=0, 4 и 18 часов. Единственным образцом, в котором было продемонстрировано хоть какое-то разрушение (>1% площади пика), был окисленный образец, в который добавляли 3% пероксид водорода (H2O2).
Для оценки стабильности в условиях окружающей среды взвешивали глутарат анатабина (100 мг) в прозрачной стеклянной чашке Петри и выдерживали в условиях окружающей среды в открытом состоянии в вытяжном шкафу в течение 7 дней. Визуально оценивали образец после хранения в моменты времени T=0, 3 и 7 дней. Изменения окраски или какие-либо признаки расплывания не наблюдались (фиг. 12).
Пример сравнения 1
Получение цитрата анатабина
Растворяли свободное основание анатабина (160 мг, 1 ммоль) в безводном ацетоне (2,5 мл). В полученный раствор добавляли раствор безводной лимонной кислоты (192 мг, 1 ммоль) в безводном ацетоне (3 мл, требовалась обработка ультразвуком) при перемешивании в атмосфере азота. Перемешивали смесь в течение 2 часов, а затем фильтровали под азотной подушкой. Промывали твердое вещество небольшим количеством безводного ацетона и сушили в вакууме. Получали 340 мг (выход 96,6%) цитрата анатабина. Так как было продемонстрировано, что указанная соль является крайне гигроскопичной, ее хранили в атмосфере азота. Подтверждали химическую структуру и стехиометрию путем протонного ЯМР. Твердая форма цитрата содержит захваченный ацетон.
Аналогичным образом получали и тартратную форму, и было обнаружено, что как тартрат (фиг. 13), так и цитрат (фиг. 14) (описание в патенте США №8207346 и патенте США №8557999), существуют в аморфной форме.
Общее описание способов
Модулированную дифференциальную сканирующую калориметрию (мДСК) проводили на Perkin Elmer DSC 8000 с использованием 40 мкл алюминиевых кювет. Помещали примерно 6 мг каждого образца в предварительно взвешенную алюминиевую кювету для ДСК с использованием аналитических весов. Нагревали образец от -70 до 175°C с шагом 5°C при помощи программы модулирования температуры в атмосфере азота. Изучали данные на наличие каких-либо тепловых явлений.
Инфракрасную спектроскопию с преобразованием Фурье (FT-IR) проводили на Jasco 420 FT-IR с использованием модуля с нарушенным полным внутренним отражением (НПВО). Помещали 1-2 мг образца на кристалл в модуле с НПВО и закрепляли. Проводили анализ при помощи программного обеспечения Jasco Spectra Manager версии v1.51.00.
Рентгеновскую порошковую дифракцию (XRPD) определяли на Bruker D8 Advance XRPD с использованием 9 мм полости и плоских пластинчатых держателей образцов. Готовили образцы, нанося покрытие из них на держатели образцов, оборудованные силиконовыми пластинами с нулевым фоном (5 1 0). Проводили анализ с использованием источника рентгеновского излучения Cu Kα, который эксплуатировали при 40 кВ и 40 мА, и детектора Lynx Eye TM; все образцы анализировали в диапазоне 2-40 °2Ɵ.
Термогравиметрический анализ (ТГА) проводили на Perkin Elmer PYRIS 1 TGA с использованием 40 мкл алюминиевых кювет (вентилируемых) в керамических тиглях. Нагревали образцы от комнатной температуры до 400°C со скоростью 10°C/мин (если не утверждается иное) в токе газообразного азота.
Спектроскопию 1H ядерного магнитного резонанса (ЯМР) проводили на спектрометре Bruker 400 Avance, оборудованном 5 мм зондом QNP. Растворяли 5-7 мг образца в дейтерированном метаноле или диметилсульфоксиде. Переносили раствор в 5 мм пробирки для ЯМР, удовлетворяющие требованиям магнитного поля, для анализа.
Динамическую сорбцию паров (DVS) проводили на приборе для динамической сорбции паров SMS DVS с использованием контрольного программного обеспечения DVS версии v1.0.6.0. Взвешивали 30 мг образца в сетчатом держателе образца из нержавеющей стали для DVS, после чего отправляли на анализ. Анализировали образцы в диапазоне 0-90% отн.вл. при максимальной продолжительности стадии выдерживания при определенной влажности 6 часов. Каждый образец обрабатывали в условиях двойного цикла. Проводили анализ для определения изменения массы в процентах в диапазоне 0-90% отн.вл., также изучали графики с построенными изотермами. Анализ XRPD всех образцов проводили после DVS.
Подтверждали химическую целостность и стехиометрию глутарата анатабина путем спектроскопии 1H ЯМР.
Ионную хроматографию проводили на ионном хроматографе с большим градиентом давления Metrohm 940 с использованием охлажденного пробоотборника Metrohm 889, раствора элюента 3,2 мМ карбонат натрия и 1 мМ бикарбонат натрия, раствора для регенерации 150 мМ серная кислота/100 мМ щавелевая кислота.
В анализе DVS данного образца был показан прирост массы на 55% в диапазоне 0-90% отн.вл. во время первого цикла сорбции, а затем снижение массы во время десорбции до тех пор, пока она не достигла значения на 5% выше начальной массы. Это указывает на захват влаги. Во втором цикле сорбции наблюдали прирост массы на 50%, и после второго цикла десорбции конечная масса была на 5% выше начальной массы. Это указывает на удерживание воды, захваченной во время первого цикла сорбции. Это было дополнительно подтверждено графиком с построенной изотермой указанного образца.
Оставляли образец на ночь, было обнаружено, что после этого он перекристаллизовывался с образованием твердой формы. При сравнении дифрактограмм рентгеновской дифракции образцов до и после DVS было установлено их соответствие. Это указывает на то, что кристаллические формы до и после DVS были идентичными.
Глутарат анатабина обладает предпочтительными свойствами, такими как высокая степень кристалличности, морфология, термическая и механическая устойчивость к полиморфным превращениям и/или дегидратации, стабильность при хранении, низкое содержание остаточного растворителя, пониженный уровень гигроскопичности, текучесть и предпочтительные технологические и рабочие характеристики.
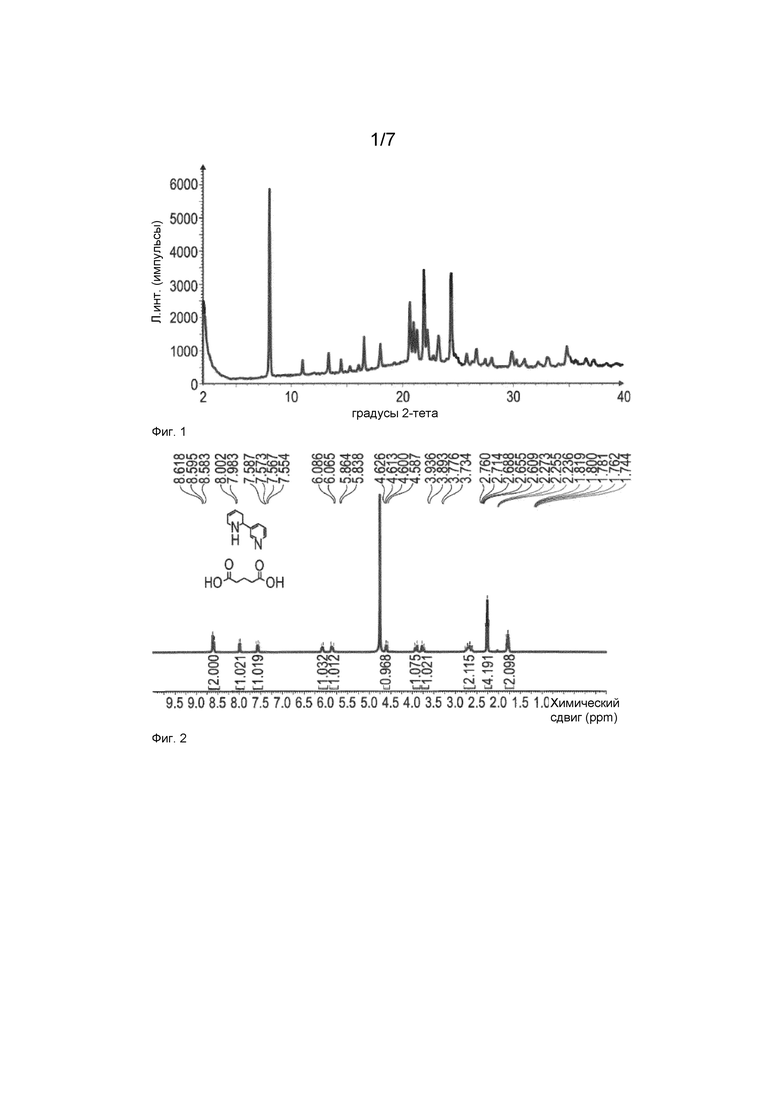
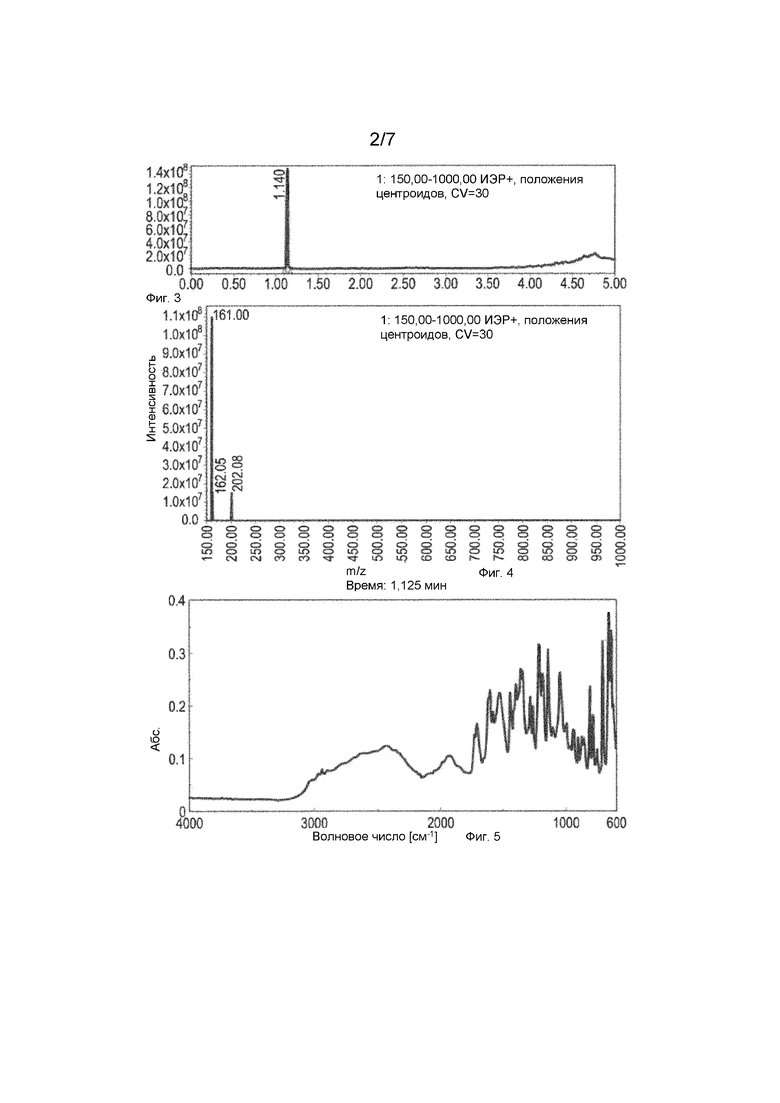
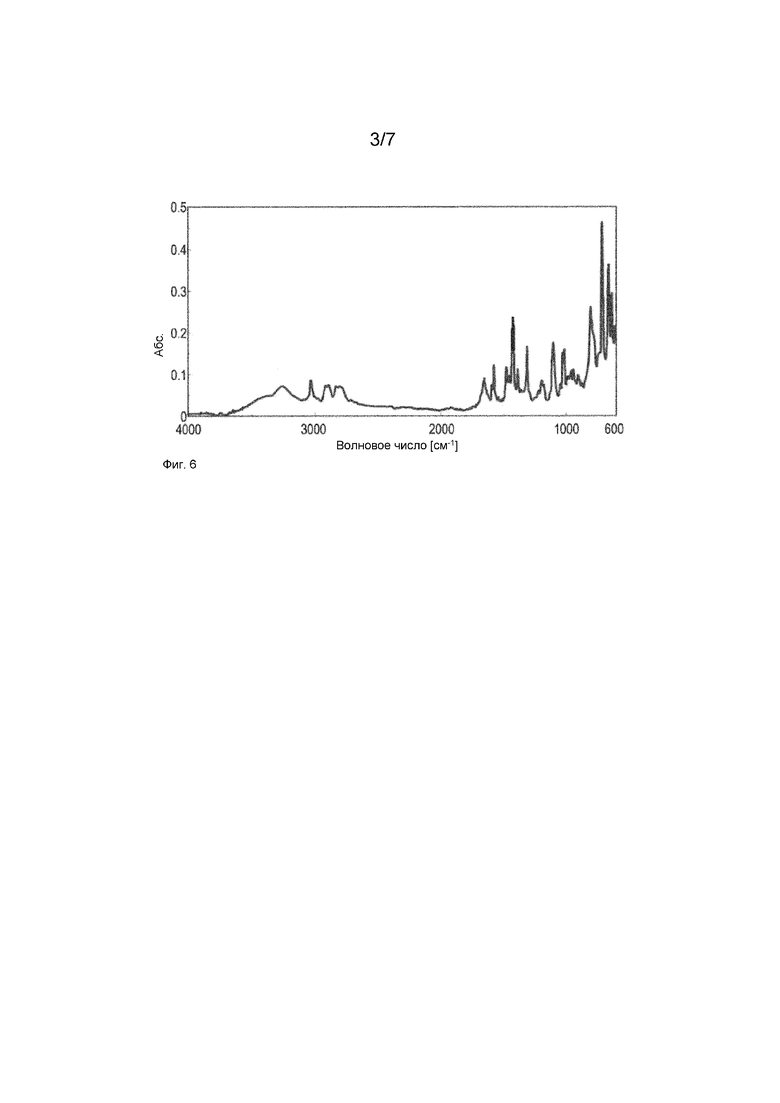
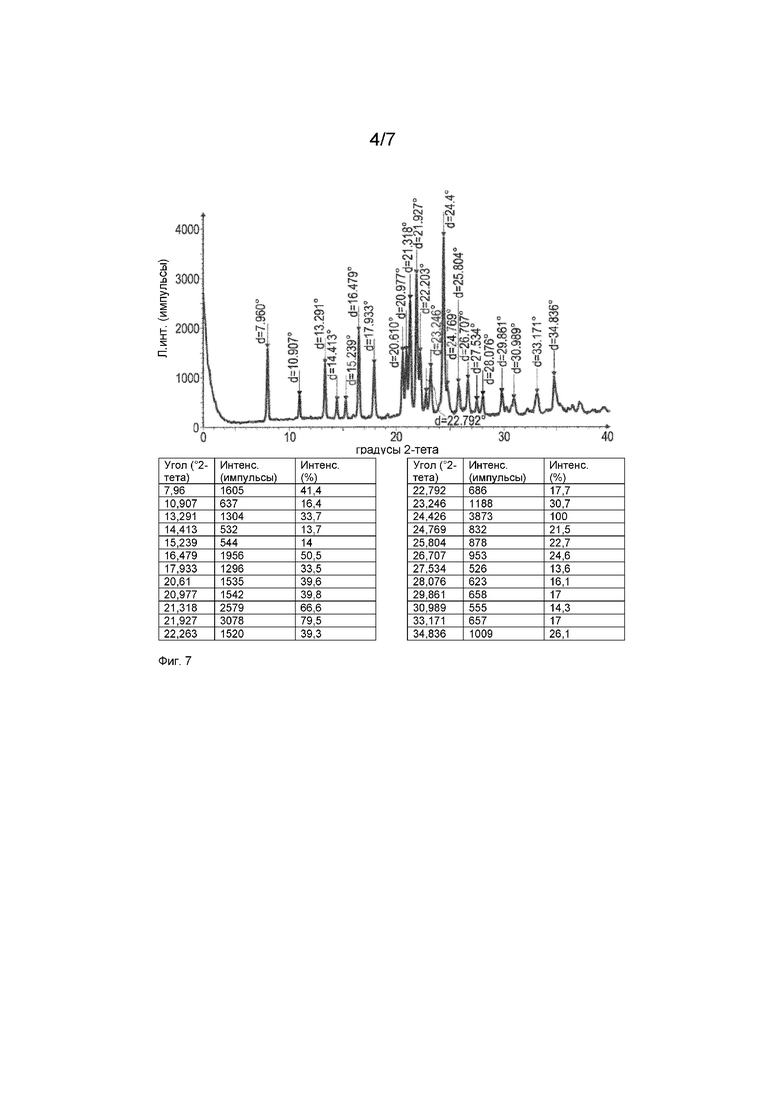
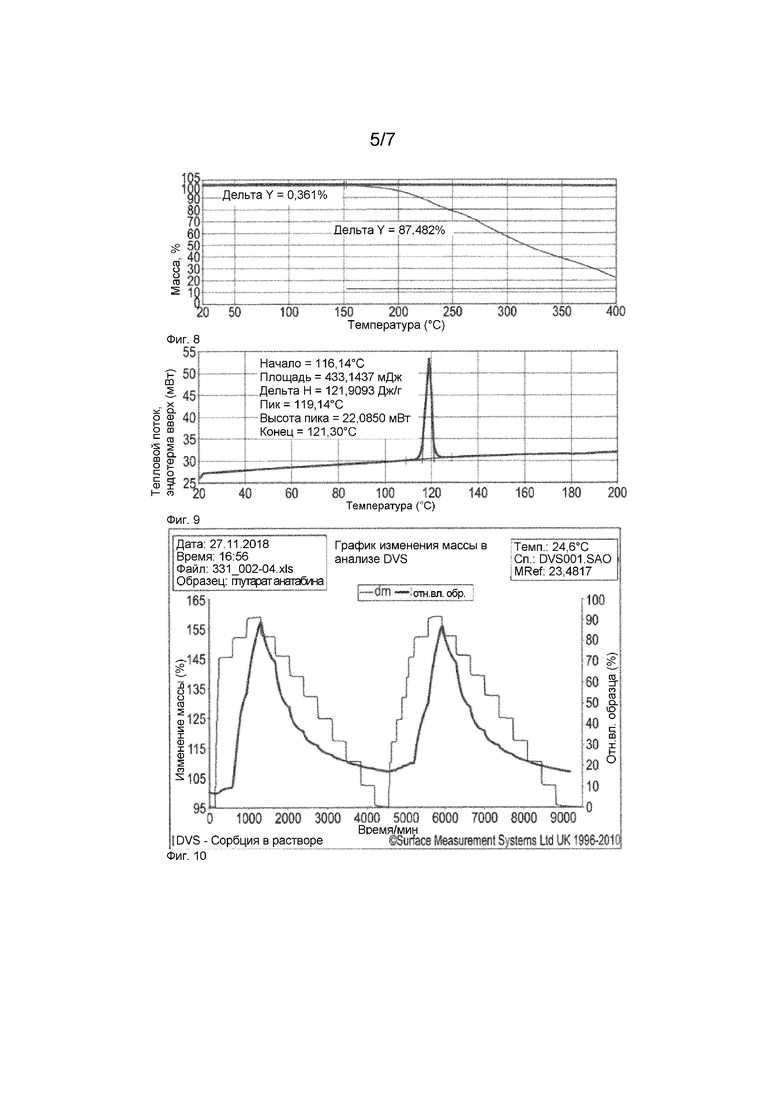
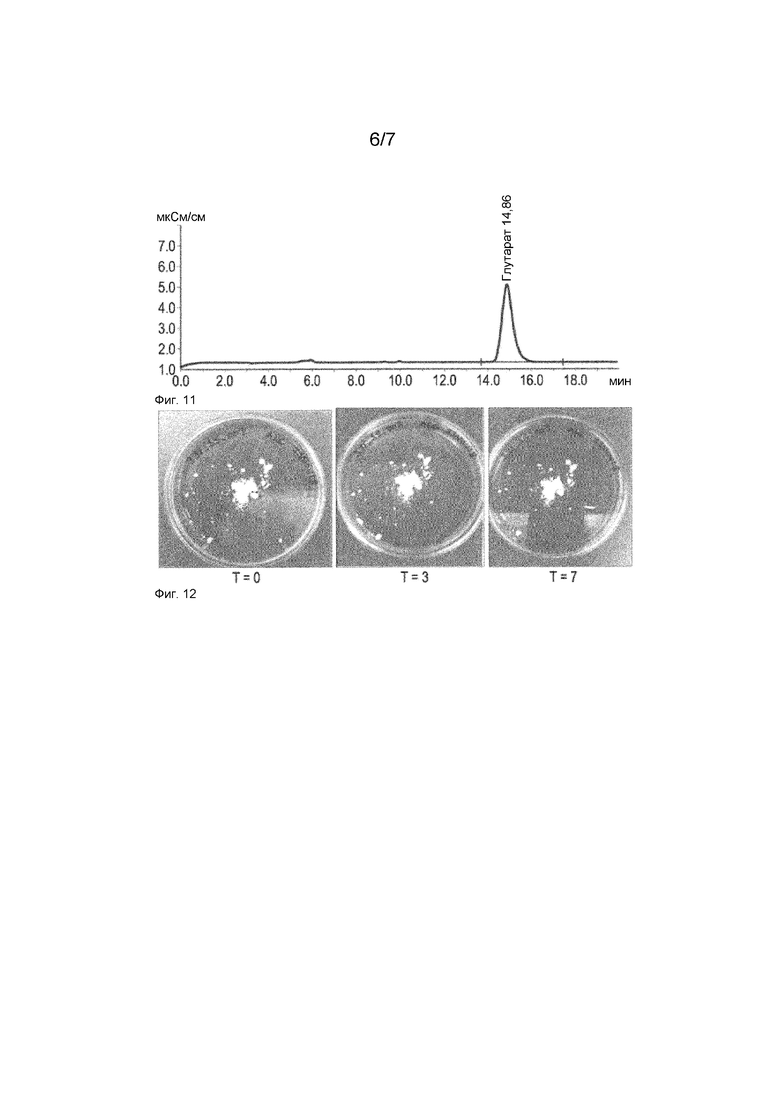
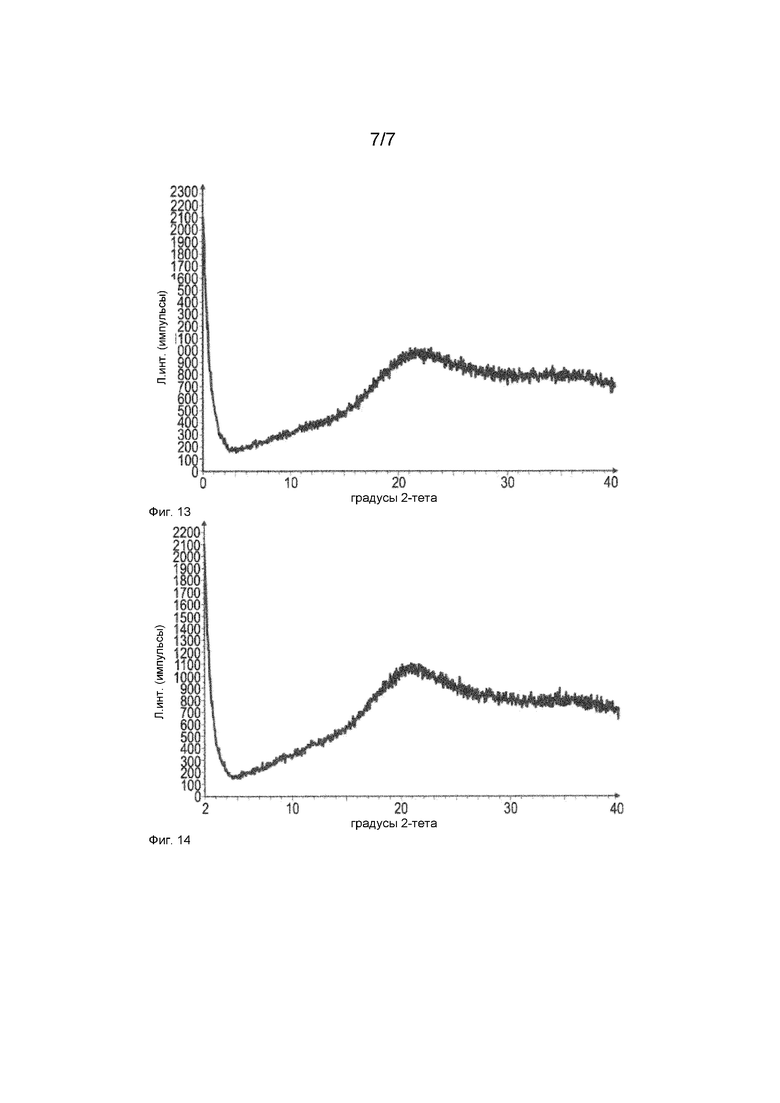
Изобретение относится к способу получения глутарата 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина. Способ получения глутарата 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, при соотношении 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина к глутарату 1:1, включает стадии получения раствора, содержащего 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридин, глутаровую кислоту и растворитель; нагревания полученного раствора; обеспечения образования соли 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина с глутаровой кислотой и выделения соли 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина глутаровой кислоты, где указанный растворитель, применяемый для получения раствора 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, глутаровой кислоты и растворителя, представляет собой ацетонитрил. Полученный глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина находится в полиморфной форме, которая имеет дифрактограмму рентгеновской порошковой дифракции (CuKα), содержащую три или более пиков, выбранных из 8,0±0,2°2θ, 11,0±0,2°2θ, 13,3±0,2°2θ, 16,5±0,2°2θ, 18,0±0,2°2θ, 20,7±0,2°2θ, 21,0±0,2°2θ, 21,4±0,2°2θ, 22,0±0,2°2θ, 22,3±0,2°2θ, 23,3±0,2°2θ и 24,5±0,2°2θ. Технический результат – получение глутарата анатабина, обладающего такими свойствами, как высокая степень кристалличности, стабильность при хранении, пониженный уровень гигроскопичности, текучесть. 4 з.п. ф-лы, 1 табл., 14 ил., 6 пр.
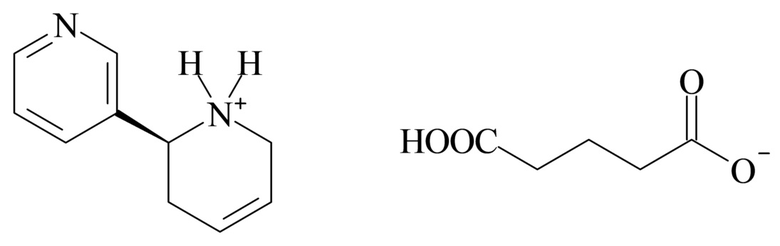
1. Способ получения глутарата 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, где глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина находится в соотношении 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина к глутарату 1:1, включающий стадии:
получения раствора, содержащего 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридин, глутаровую кислоту и растворитель,
нагревания полученного раствора;
обеспечения образования соли 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина с глутаровой кислотой и
выделения соли 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина глутаровой кислоты,
где указанный растворитель, применяемый для получения раствора 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина, глутаровой кислоты и растворителя, представляет собой ацетонитрил.
2. Способ по п. 1, отличающийся тем, что указанный 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридин представляет собой 3-[(2S)-1,2,3,6-тетрагидропиридин-2-ил]пиридин.
3. Способ по п. 1, отличающийся тем, что указанный глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина имеет следующую формулу (I):
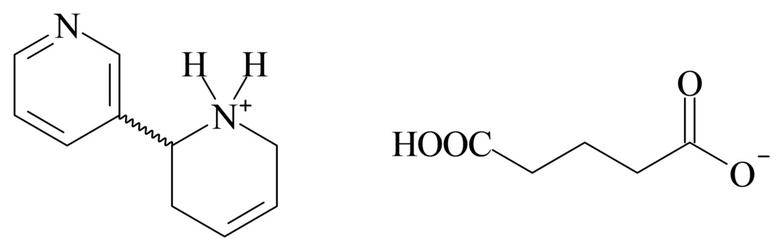
4. Способ по любому из пп. 1-3, отличающийся тем, что указанный глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина имеет следующую формулу (Ia):
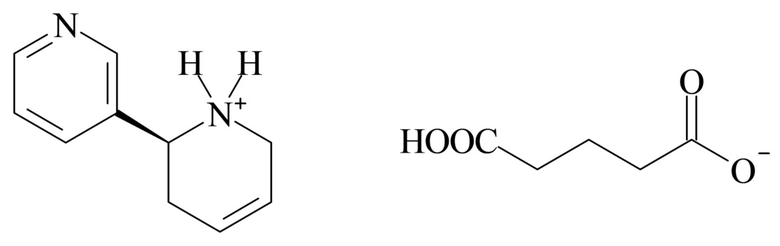
5. Способ по любому из пп. 1-4, где глутарат 3-[1,2,3,6-тетрагидропиридин-2-ил]пиридина находится в полиморфной форме, отличающийся тем, что указанная полиморфная форма имеет дифрактограмму рентгеновской порошковой дифракции (CuKα), содержащую три или более пиков, выбранных из 8,0±0,2°2θ, 11,0±0,2°2θ, 13,3±0,2°2θ, 16,5±0,2°2θ, 18,0±0,2°2θ, 20,7±0,2°2θ, 21,0±0,2°2θ, 21,4±0,2°2θ, 22,0±0,2°2θ, 22,3±0,2°2θ, 23,3±0,2°2θ и 24,5±0,2°2θ.
| WO 2011119722 A2, 29.09.2011 | |||
| Richard J.Bastin et al.: "Salt selection and Optimisation Procedures for Pharmaceutical New Chemical Entities", ORGANIC PROCESS RESEARCH & DEVELOPMENT, 2000, vol.4, p.427-435 | |||
| M.R.CAIRA, Crystalline polymorphism of organic compounds, TOPICS IN CURRENT CHEMISTRY, Springer Verlag Berlin Heidelberg, 1998, v.198, |
Авторы
Даты
2024-07-31—Публикация
2019-12-17—Подача