ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ НАСТОЯЩЕЕ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к полиморфным формам икотиниба, способам получения этих полиморфных форм, фармацевтическим композициям с ними и к применению новых полиморфных форм и фармацевтических композиций для лечения рака и заболеваний, связанных с возникновением рака.
УРОВЕНЬ ТЕХНИКИ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Тирозинкиназные рецепторы представляют собой трансмембранные белки, которые в ответ на внеклеточный стимул распространяют cигнальный каскад для контроля клеточной пролиферации, ангиогенеза, апоптоза и других важных характеристик клеточного роста. Один класс таких рецепторов, тирозинкиназы рецептора эпидермального фактора роста (EGFR), чрезмерно экспрессируются при многих формах рака у человека, в том числе при раке головного мозга, легкого, печени, мочевого пузыря, молочной железы, головы и шеи, пищевода, желудочно-кишечного тракта, яичника, шейки матки или щитовидной железы.
EGFR экспрессируется у многих типов опухолевых клеток. Связывание когнатных лигандов (в том числе EGF, TGFα (т.е. трансформирующего фактора роста α) и нейрегулинов) с внеклеточным доменом вызывает образование гомо- или гетеродимеров между представителями семейства. Непосредственное соседство цитоплазматических доменов тирозинкиназ приводит в результате к трансфосфорилированию специфических тирозиновых, сериновых и треониновых остатков в каждом цитоплазматическом домене. Образованные фосфотирозины действуют как участки стыковки для различных адапторных молекул и последующей активации каскадов сигнальной трансдукции (Ras/митоген-активируемый, PI3K/Akt и Jak/STAT), которые запускают связанные с пролиферацией клеточные ответы.
Различные исследования в молекулярной и клеточной биологии и клинические исследования продемонстрировали, что ингибиторы тирозинкиназы EGFR могут блокировать пролиферацию и метастазирование раковых клеток, а также другие ответы, основанные на связанной с EGFR сигнальной трансдукции, для достижения клинических противоопухолевых терапевтических эффектов. Гефитиниб (Иресса, AstraZeneca), одобренный Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA) для распространенного немелкоклеточного рака легкого в 2003 году (и позднее отозванный), и эрлотиниба гидрохлорид (Тарцева, Roche и OSI), одобренный FDA США для лечения распространенного немелкоклеточного рака легкого и рака поджелудочной железы в 2004 году, являются двумя пероральными ингибиторами киназы EGFR с подобными химическими структурами.
Многие фармацевтически активные органические соединения могут образовывать кристаллы с трехмерной кристаллической структурой более чем одного типа. То есть соединения могут кристаллизоваться в различных кристаллических формах. Это явление (идентичная химическая структура, но различная кристаллическая структура) называется полиморфизмом, а разновидности, характеризующиеся различными молекулярными структурами, называются полиморфами.
Полиморфы конкретного органического фармацевтического соединения могут характеризоваться различными физическими свойствами, такими как растворимость и гигроскопичность, вследствие их отличающихся трехмерных кристаллических структур. Тем не менее, обычно невозможно предсказать, будет ли конкретное органическое соединение образовывать различные кристаллические формы, не говоря уже о том, чтобы предсказать структуру и свойства самих кристаллических форм. Открытие новой кристаллической или полиморфной формы полезного с точки зрения фармацевтики соединения может обеспечить новую возможность для улучшения общих характеристик фармацевтического продукта. Это расширяет спектр материалов, которые доступны для разработки ученому, специализирующемуся на получении составов. Это может обеспечить преимущество в случае, когда этот спектр расширяется при открытии новых полиморфов полезного соединения.
В публикации патентного документа Китая № CN1305860C раскрыта структура икотиниба (свободное основание), на странице 29, пример 15, соединение 23, а в документе WO 2010/003313 раскрыт икотиниба гидрохлорид и его новые кристаллические полиморфы.
ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к икотинибу (т.е. соединению формулы I), его практически чистым полиморфным формам и его фармацевтически приемлемой соли.

формула I
Соединение формулы I по настоящему изобретению существует в одной или нескольких полиморфных формах. Эти полиморфные формы обозначены как форма I, форма II, форма III и форма IV. Соединение формулы I и его полиморфные формы имеют лучшую растворимость и химическую стабильность, что делает их предпочтительными для клинических применений.
В одном аспекте полиморфная форма представляет собой полиморфную форму I, и ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих примерно 7,6°, 14,7°, 20,9°, 23,1° и 27,5° ± 0,2°.
В некоторых других вариантах осуществления полиморфной формы I ее рентгеновская порошковая дифрактограмма имеет характеристические пики, выраженные в пересчете на межплоскостное расстояние, составляющее 11,6Å, 6,0Å, 4,3Å, 3,9Å и 3,3Å.
В некоторых вариантах осуществления полиморфной формы I ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих примерно 7,6°, 14,7°, 20,9°, 23,1°, 24,2°, 27,5°, 29,8° и 30,9° ± 0,2°.
Кроме того, в некоторых других вариантах осуществления полиморфной формы I, ее рентгеновская порошковая дифрактограмма имеет характеристические пики, выраженные в пересчете на межплоскостное расстояние, составляющее 11,6Å, 6,0Å, 4,3Å, 3,9Å, 3,7Å, 3,3Å, 3,0Å и 2,9Å.
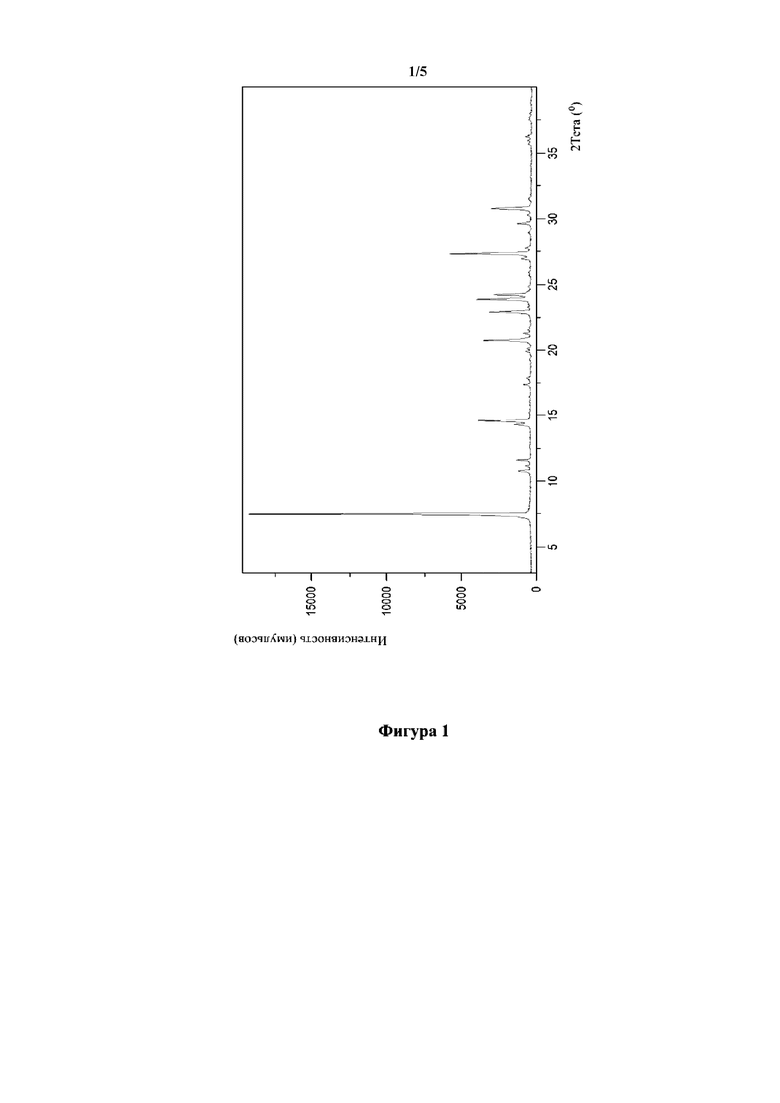
Предпочтительно рентгеновская порошковая дифрактограмма представлена в том же виде, как и на фигуре 1.
Предпочтительно температура плавления полиморфной формы I составляет 175-177°C.
Настоящее изобретение также предлагает способ получения полиморфа, предусматривающий стадии растворения икотиниба гидрохлорида в смеси C1-C4спирта и воды, причем смесь нагревают до 60°C и раствор основания добавляют по каплям. Реакционный раствор перемешивали в течение 1 часа и охлаждали до комнатной температуры. Осадок фильтровали и промывали очищенной водой и сушили 8 часов в вакууме при температуре ниже 60°C с получением в результате полиморфной формы I.
В другом аспекте полиморфная форма представляет собой полиморфную форму II, и ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих примерно 5,5°, 19,7° и 22,6° ± 0,2°.
Кроме того, в некоторых других вариантах осуществления полиморфной формы II ее рентгеновская порошковая дифрактограмма имеет характеристические пики, выраженные в пересчете на межплоскостное расстояние, составляющее 16,0Å, 4,5Å и 3,9Å.
В некоторых вариантах осуществления полиморфной формы II ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих примерно 5,5°, 11,0°, 19,7°, 20,9° и 22,6° ± 0,2°.
Кроме того, в некоторых других вариантах осуществления полиморфной формы II ее рентгеновская порошковая дифрактограмма имеет характеристические пики, выраженные в пересчете на межплоскостное расстояние, составляющее 16,0Å, 8,0Å, 4,5Å, 4,3Å и 3,9Å.
В некоторых вариантах осуществления полиморфной формы II ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих примерно 5,5°, 8,8°, 11,0°, 16,5°, 19,7°, 20,9°, 22,6° и 23,7° ± 0,2°.
Кроме того, в некоторых других вариантах осуществления полиморфной формы II ее рентгеновская порошковая дифрактограмма имеет характеристические пики, выраженные в пересчете на межплоскостное расстояние, составляющее 16,0Å, 10,1Å, 8,0Å, 5,4Å, 4,5Å, 4,3Å, 3,9Å и 3,8Å.
Предпочтительно рентгеновская порошковая дифрактограмма представлена в том же виде, как и на фигуре 2.
Предпочтительно температура плавления полиморфной формы II составляет 176-178°C.
Настоящее изобретение также предлагает способ получения полиморфа, предусматривающий стадии нагревания полиморфа, относящегося к форме I, приблизительно до 165°C в N2 и естественного охлаждения до комнатной температуры с извлечением полученной в результате полиморфной формы II.
В другом аспекте полиморфная форма представляет собой полиморфную форму III, и ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих примерно 5,1°, 16,7°, 20,9°, 21,7° и 23,9° ± 0,2°.
В некоторых вариантах осуществления полиморфной формы III ее рентгеновская порошковая дифрактограмма имеет характеристические пики, выраженные в пересчете на межплоскостное расстояние, составляющее 17,3Å, 5,3Å, 4,3Å, 4,1Å и 3,7Å.
В некоторых вариантах осуществления полиморфной формы III ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих примерно 5,1°, 7,6°, 16,7°, 19,8°, 20,9°, 21,7°, 23,9° и 24,7° ± 0,2°.
Кроме того, в некоторых других вариантах осуществления полиморфной формы III ее рентгеновская порошковая дифрактограмма имеет характеристические пики, выраженные в пересчете на межплоскостное расстояние, составляющее 17,3Å, 11,7Å, 5,3Å, 4,5Å, 4,3Å, 4,1Å, 3,7Å и 3,6Å.
Предпочтительно рентгеновская порошковая дифрактограмма представлена в том же виде, как и на фигуре 3.
Предпочтительно температура плавления полиморфной формы III составляет 175-178°C.
Настоящее изобретение также предлагает способ получения полиморфа, предусматривающий стадии помещения полиморфа, относящегося к форме I, в насыщенные пары ацетонитрила при комнатной температуре на неделю и извлечения полученной в результате полиморфной формы III.
В еще одном аспекте полиморфная форма представляет собой полиморфную форму IV, и ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих приблизительно 6,1°, 11,2°, 15,8°, 19,5° и 22,5° ± 0,2°.
В некоторых вариантах осуществления полиморфной формы IV ее рентгеновская порошковая дифрактограмма имеет характеристические пики, выраженные в пересчете на межплоскостное расстояние, составляющее 14,5Å, 7,9Å, 5,6Å, 4,6Å и 4,0Å.
В некоторых вариантах осуществления полиморфной формы IV ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих примерно 6,1°, 11,2°, 12,9°, 14,2°, 15,8°, 18,3°, 19,5° и 22,5° ± 0,2°.
Кроме того, в некоторых других вариантах осуществления полиморфной формы IV ее рентгеновская порошковая дифрактограмма имеет характеристические пики, выраженные в пересчете на межплоскостное расстояние, составляющее 14,5Å, 7,9Å, 6,9Å, 6,2Å, 5,6Å, 4,9Å, 4,6Å и 4,0Å.
Предпочтительно рентгеновская порошковая дифрактограмма представлена в том же виде, как и на фигуре 4.
Предпочтительно температура плавления полиморфной формы IV составляет 175-177°C.
Настоящее изобретение также предлагает способ получения полиморфа, предусматривающий стадии помещения полиморфа, относящегося к форме I, в насыщенные пары метанола при комнатной температуре на неделю и извлечения полученной в результате полиморфной формы IV.
Полиморфная форма I, II, III или IV по настоящему изобретению может иметь чистоту ≥85%, ≥95% или даже ≥99%.
В еще одном аспекте настоящее изобретение предлагает способы получения полиморфной формы икотиниба, предусматривающий стадию осуществления реакции икотиниба гидрохлорида с основанием в среде с получением икотиниба в полиморфной форме. Эту реакцию можно проводить, например, при температуре 40-80°C.
Примеры подходящего основания включают гидроксид натрия, гидроксид калия, карбонат натрия и карбонат калия.
Вторая реакционная среда может включать, например, воду и этанол, воду и изопропанол, воду и метанол или воду и тетрагидрофуран.
Полиморфные формы по настоящему изобретению, в частности, полиморфная форма I, полиморфная форма II, полиморфная форма III и полиморфная форма IV, неожиданно проявляли значительно лучшую биодоступность и химическую стабильность,чем икотиниба гидрохлорид, активный ингредиент лекарственного средства, присутствующего в настоящее время на рынке. Соответственно, настоящее изобретение также предлагает фармацевтические композиции, содержащие терапевтически эффективное количество полиморфной формы по настоящему изобретению и фармацевтически приемлемый вспомогательное средство, добавочное средство или носитель.
Фармацевтическая композиция может дополнительно включать второй терапевтически активный ингредиент и может присутствовать в форме, подходящей для перорального введения (например, таблетки или капсулы).
Также в пределах объема настоящего изобретения находится применение полиморфной формы или фармацевтической композиции по настоящему изобретению в производстве лекарственного препарата для предупреждения или лечения у млекопитающих интенсивного незлокачественного заболевания, панкреатита, заболевания почек, рака, ангиогенеза или заболевания сосудов или для трансплантации клеток эмбриона млекопитающего.
Интенсивное незлокачественное заболевание может представлять собой, например, доброкачественную гиперплазию кожи или доброкачественную гиперплазию предстательной железы. Или интенсивное незлокачественное заболевание, панкреатит, заболевание почек, рак, болезнь, связанную с ангиогенезом или возникновением сосудов, выбраны из опухолевого ангиогенеза, хронического воспалительного заболевания, такого как ревматоидный артрит, атеросклероза, кожных заболеваний, таких как псориаз и склеродерма, вызванных диабетом кожных заболеваний, диабетической ретинопатии, ретинопатии недоношенных, возрастной дегенерации желтого пятна, гемангиомы, глиомы, внутренней опухоли Капоши, рака яичника, рака молочной железы, рака легкого, рака поджелудочной железы, лимфомы, опухоли предстательной железы, толстой кишки и кожи, а также их осложнений.
Все полиморфы по настоящему изобретению являются практически чистыми.
Используемое в данном документе выражение “практически чистый” относится к тому, что по меньшей мере 85 вес. %, предпочтительно по меньшей мере 95 вес. %, более предпочтительно по меньшей мере 99 вес. % соединения формулы I существует в полиморфной форме по настоящему изобретению, в частности, в полиморфных формах, относящихся к форме I, форме II, форме III или форме IV.
Главные пики, описанные для вышеприведенных полиморфов, являются воспроизводимыми и находятся в пределах погрешности (определенное значение ± 0,2).
Согласно настоящему изобретению фраза “рентгеновская порошковая дифрактограмма представлена в том же виде, как и на фигуре 1” относится к рентгеновской порошковой дифрактограмме, на которой основные пики представлены, как на фигуре 1, где основные пики относятся к пикам с относительной интенсивностью, большей чем 10%, предпочтительно большей чем 30% в сравнении с наивысшим пиком (причем его относительная интенсивность определяется как 100%) на фигуре 1. Аналогично, согласно настоящему изобретению рентгеновская порошковая дифрактограмма, представленная в том же виде, как и на фигуре 2, 3 или 4, относится к рентгеновской порошковой дифрактограмме, на которой основные пики представлены, как на фигуре 2, 3 или 4, где основные пики относятся к пикам с относительной интенсивностью, большей чем 10%, предпочтительно большей чем 30% в сравнении с наивысшим пиком (причем его относительная интенсивность определяется как 100%) на фигуре 2, 3 или 4, соответственно.
Кристаллизация согласно настоящему изобретению относится к динамике и равновесию между различными полиморфными формами в определенных условиях. Таким образом, специалист в данной области поймет, что получаемая в результате полиморфная форма зависит от кинетики и термодинамики процесса кристаллизации. В определенных условиях (система растворителей, температура, давление и концентрация соединения согласно настоящему изобретению) одна полиморфная форма может быть более стабильной, нежели другая (или фактически может быть более стабильной, чем все прочие полиморфные формы). Тем не менее полиморфы, которые характеризуются меньшей термодинамической стабильностью, могут быть выгодны с точки зрения кинетики. На полиморфную форму также могут оказывать воздействие факторы, отличные от кинетики, такие как время, распределение примесей, встряхивание, наличие или отсутствие полиморфной затравки. В контексте настоящего изобретения различные гидратные и сольватные формы включены в объем выражения “полиморф”.
Настоящее изобретение также предлагает фармацевтическую композицию, содержащую терапевтически эффективное количество одного или нескольких полиморфов формы I, формы II, формы III или формы IV соединения формулы I и фармацевтически приемлемое вспомогательное средство, добавочное средство или носитель. При этом фармацевтическая композиция содержит 0,01 вес. - 99 вес. %, предпочтительно 1 вес. - 70 вес %, более предпочтительно 10 вес. - 50 вес % любого полиморфа, относящегося к форме I, форме II, форме III или форме IV соединения формулы I.
Используемое в данном документе выражение “терапевтически эффективное количество” относится к количеству соединения, которое при введении субъекту для лечения заболевания или по меньшей мере одного из клинических симптомов заболевания или нарушения является достаточным для воздействия такого лечения на заболевание, нарушение или симптом. “Терапевтически эффективное количество” может изменяться в зависимости от соединения, заболевания, нарушения и/или симптомов заболевания или нарушения, тяжести заболевания, нарушения и/симптомов заболевания или нарушения, возраста субъекта, подлежащего лечению, и/или веса субъекта, подлежащего лечению. Надлежащее количество в каждом конкретном случае будет очевидно специалисту в данной области или может быть определено путем стандартных экспериментов. В случае комбинированной терапии выражение “терапевтически эффективное количество” относится к общему количеству объектов в комбинации для эффективного лечения заболевания, нарушения или состояния.
Фармацевтическую композицию, содержащую соединение по настоящему изобретению, можно вводить посредством перорального, ингаляционного, ректального, парентерального или местного введения субъекту, который нуждается в лечении. Для перорального введения фармацевтическая композиция может представлять собой стандартный состав в виде твердого вещества, такой как таблетки, порошок, гранула, капсулы и т.п., жидкий состав, такой как водная или масляная суспензия, или другой жидкий состав, такой как сироп, раствор, суспензия или подобное; для парентерального введения фармацевтическая композиция может представлять собой раствор, водный раствор, концентрат масляной суспензии, лиофилизированный порошок или подобное. Предпочтительно состав фармацевтической композиции выбран из таблетки, покрытой таблетки, капсулы, суппозитория, назального спрея или инъекционной формы, более предпочтительно из таблетки или капсулы. Фармацевтическая композиция может представлять собой одну единицу для введения с точной дозировкой. Кроме того, фармацевтическая композиция может также содержать дополнительные активные ингредиенты.
Все составы фармацевтической композиции по настоящему изобретению можно получить с помощью общепринятых способов в области фармацевтики. Например, активный ингредиент можно смешать с одним или несколькими вспомогательными средствами, чтобы затем получить необходимый состав. Выражение "фармацевтически приемлемый носитель" относится к общепринятым фармацевтическим носителям, подходящим для необходимого фармацевтического состава, например: разбавитель, среда, такая как вода, различные органические растворители и т.д., наполнитель, такой как крахмал, сахароза и т.д; связующее, такое как производные целлюлозы, альгинаты, желатин и поливинилпирролидон (PVP); смачивающее средство, такое как глицерин; разрыхлитель, такой как агар, карбонат кальция и бикарбонат натрия; усилитель абсорбции, такой как соединение четвертичного аммония; поверхностно-активное вещество, такое как гексадеканол; абсорбционный носитель, такой как каолин и мыльная глина; смазывающее средство, такое как тальк, стеарат кальция, стеарат магния, полиэтиленгликоль и т.д. Кроме того, фармацевтическая композиция дополнительно содержит другие фармацевтически приемлемые вспомогательные средства, такие как разукрупняющее средство, стабилизатор, загуститель, комплексообразующее средство, буферное средство, усилитель проницаемости, полимер, душистые вещества, подсластитель и краситель. Предпочтительно вспомогательное средство является подходящим для необходимого типа состава и введения.
Выражение "заболевание", или "нарушение", или "состояние" относится к любому заболеванию, недомоганию, болезни, симптомам или признакам.
В другом аспекте настоящее изобретение предлагает применение соединений (икотиниба и его полиморфов) и/или фармацевтических композиций в производстве лекарственного препарата для лечения или предупреждения у млекопитающих незлокачественного заболевания, связанного с чрезмерной гиперплазией, панкреатита, заболевания почек, рака, болезни, связанной с ангиогенезом или возникновением сосудов, или для трансплантации клеток эмбриона млекопитающего. Незлокачественное заболевание, связанное с чрезмерной гиперплазией, может представлять собой доброкачественную гиперплазию кожи или доброкачественную гиперплазию предстательной железы.
Предпочтительно полиморфы или фармацевтическую композицию согласно настоящему изобретению можно применять в производстве лекарственного препарата для лечения или предупреждения у животных незлокачественного заболевания, связанного с чрезмерной гиперплазией, панкреатита, заболевания почек, рака, болезни, связанной с ангиогенезом или возникновением сосудов, выбранных из опухолевого ангиогенеза, хронических воспалительных заболеваний, таких как ревматоидный артрит, атеросклероза, кожных заболеваний, таких как псориаз и склеродерма, связанных с диабетом кожных заболеваний, диабетической ретинопатии, ретинопатии недоношенных, возрастной дегенерации желтого пятна, гемангиомы, глиомы, внутренней опухоли Капоши, рака яичника, рака молочной железы, рака легкого, рака поджелудочной железы, лимфомы, опухолей предстательной железы, толстой кишки и кожи, а также их осложнений.
Среди млекопитающих, упомянутых в данном документе, люди являются предпочтительными.
Настоящее изобретение предлагает способ лечения у млекопитающих злокачественной гиперплазии ткани. Этот способ лечения включает применение эффективного количества икотиниба и/или его полиморфных форм и/или фармацевтических композиций у пациентов-млекопитающих с заболеванием, связанным с гиперплазией. В некоторых вариантах осуществления способ лечения также включает применение ингибитора MMP (матриксной металлопротеиназы), ингибиторов киназы VEGFR (рецептора фактора роста эндотелия сосудов), ингибитора HER2, лекарственных средств на основе антител к VEGFR и/или лекарственных средств на основе эндостатина. В некоторых вариантах осуществления способ лечения также включает применение одного или нескольких противоопухолевых средств, таких как ингибиторы митоза, алкилирующие средства, антиметаболиты, противоопухолевые антибиотики, ингибиторы факторов роста, ингибиторы клеточного цикла, ферменты, ингибиторы ферментов, модификаторы биологического ответа, антигормональные лекарственные средства и так далее. Противоопухолевые средства можно выбрать из карбоплатина, паклитаксела, гемцитабина, метотрексата, 5-FU, кампотецина, циклофосфамида, BCNU и других cредств для лечения.
Другой целью настоящего изобретения является обеспечения применения соединений (икотиниба и его полиморфов) и/или фармацевтических композиций в производстве лекарственного препарата для лечения заболевания, связанного с дисфункцией тирозинкиназы.
Предпочтительно, настоящее изобретение предлагает способ лечения заболевания, вызванного дисфункцией тирозинкиназы. Данный способ лечения включает введение пациенту с заболеванием, вызванным дисфункцией тирозинкиназы, эффективного количества соединений (икотиниба и его полиморфов) и/или фармацевтических композиций. Заболевания, связанные с дисфункцией тирозинкиназы, включают без ограничения заболевания, связанные с опухолями головного мозга, легкого, печени, мочевого пузыря, молочной железы, головы и шеи, пищевода, желудочно-кишечного тракта, яичника, шейки матки или щитовидной железы, а также их осложнения.
Заболевание-мишень для вышеописанного способа лечения предпочтительно выбрано из рака головного мозга, рака легкого (такого как немелкоклеточный рак легкого (NSCLC)), рака почки, рака кости, рака печени, рака мочевого пузыря, рака грудной клетки, лимфомы или опухолей щитовидной железы, а также их осложнений.
Вышеописанные способы можно применять в комбинации с любой химиотерапией, биологической терапией или лучевой терапией.
Вышеописанные способы лечения могут дополнительно включать применение антител к EGFR, антител к EGF или и тех, и других в одном и том же лечении.
Доза активного ингредиента или соединения в случае введения будет определяться индивидуальными потребностями пациента, получающего лечение, путем введения, тяжестью заболевания или болезни, схемой дозирования, а также оценкой и решением уполномоченного врача. Тем не менее, с учетом активного соединения, предпочтительный диапазон эффективной дозы может составлять приблизительно 0,01-120 мг в сутки на килограмм массы тела; или более предпочтительно 1-50 мг в сутки на килограмм массы тела в виде одной или отдельных доз. В некоторых случаях более подходящим является применение нижнего предела вышеописанного диапазона дозы, тогда как в других случаях можно применять более высокую дозу, не вызывая вредных побочных эффектов.
Другим аспектом настоящего изобретение является обеспечение икотиниба для клинических применений. В частности, настоящее изобретение относится к клиническому лечению икотинибом со следующими вариантами лечения онкологических больных: доза икотиниба и/или полиморфной формы I, II, III или IV может составлять 25-2100 мг/сутки, причем частота введения составляет 1-3 раза в сутки; предпочтительная доза составляет 75-1200 мг/сутки, причем частота введения составляет 2-3 раза в сутки; еще более предпочтительная доза составляет 100-1200 мг/сутки, причем частота введения составляет 2-3 раза в сутки.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигура 1: рентгеновская порошковая дифрактограмма полиморфной формы I соединения формулы I.
Фигура 2: рентгеновская порошковая дифрактограмма полиморфной формы II соединения формулы I.
Фигура 3: рентгеновская порошковая дифрактограмма полиморфной формы III соединения формулы I.
Фигура 4: рентгеновская порошковая дифрактограмма полиморфной формы IV соединения формулы I.
Фигура 5: кривые зависимости концентрации в плазме от времени для кристаллической формы I икотиниба гидрохлорида и полиморфной формы II соединения формулы I.
ПРИМЕРЫ
Настоящее изобретение дополнительно поясняется, но не ограничивается следующими примерами, которые иллюстрируют настоящее изобретение. Методики или способы, применяемые в этих примерах, если явно не указывается иное, представляли собой общепринятые методики или способы, хорошо известные из уровня техники.
Рентгеновские порошковые дифрактограммы (XRPD) для кристаллических форм икотиниба получали на рентгенодифракционной системе PANalytical с консолью Empyrean. Положения дифракционных пиков калибровали с использованием кремниевого порошка, который имел величину 2θ, составляющую 28,443 градуса. В качестве источника использовали K-альфа излучение рентгеновской трубки Empyrean Cu LEF.
Пример 1
Получение формы I

100 г икотиниба гидрохлорида растворяли в смеси 300 мл этанола и 200 мл воды. Раствор 11,2 г гидроксида натрия в 100 мл воды добавляли по каплям при 60°C к раствору икотиниба гидрохлорида до тех пор, пока значение pH реакционного раствора не достигало 13. Далее реакционный раствор перемешивали в течение часа, а затем охлаждали до комнатной температуры. Осадок фильтровали и промывали очищенной водой и сушили в течение 8 часов в вакууме при температуре ниже 60°C с получением 90 г необходимой формы I. При этом температура плавления полиморфной формы I составляла 175-177°C.
Пример 2
Получение формы I

Вначале 10 г икотиниба гидрохлорида растворяли в смеси 30 мл изопропанола и 20 мл воды, раствор 1,6 г гидроксида калия в 10 мл воды добавляли к раствору икотиниба гидрохлорида до тех пор, пока значение pH реакционной смеси не достигало 13. Реакционный раствор затем перемешивали в течение 1-2 часов и охлаждали до комнатной температуры. Осадок фильтровали и промывали очищенной водой и сушили в вакууме в течение 8-10 часов при температуре ниже 50°C с получением 7,9 г необходимой формы I.
Пример 3
Получение формы I
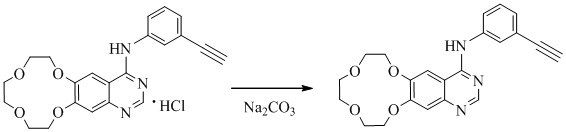
5 г икотиниба гидрохлорида растворяли в смеси 20 мл метанола и 15 мл воды. Затем к этому раствору икотиниба гидрохлорида добавляли по каплям раствор 1,5 г карбонат натрия в 10 мл воды при 40°C до тех пор, пока значение pH полученной в результате смеси не достигало 13. Реакционный раствор затем перемешивали в течение 1-2 часов перед охлаждением до комнатной температуры. Осадок фильтровали и промывали очищенной водой, а затем сушили в вакууме в течение 8-10 часов при температуре ниже 60°C с получением 4 г необходимой формы I.
Пример 4
Получение формы I

5 г икотиниба гидрохлорида растворяли в смеси 20 мл тетрагидрофурана и 15 мл воды, а затем к этому раствору икотиниба по каплям добавляли раствор 1,9 г карбоната калия в 10 мл при 50°C до тех пор, пока значение pH полученной в результате реакционной смеси не достигало 13. Реакционный раствор затем перемешивали в течение 1-2 часов перед охлаждением до комнатной температуры с получением осадка. Осадок фильтровали и промывали очищенной водой, а затем сушили в течение 8-10 часов в вакууме при температуре ниже 60°C с получением 4 г необходимой формы I.
Пример 5
Получение формы II
Форму I, полученную с помощью способа согласно примеру 1, нагревали до 150°C в N2, затем охлаждали до комнатной температуры естественным образом с получением необходимой формы II. При этом температура плавления полиморфной формы II составляла 176-178°C.
Пример 6
Получение формы II
Форму I, полученную с помощью способа согласно примеру 1, нагревали до 160°C в N2, затем охлаждали до комнатной температуры естественным образом с получением необходимой формы II.
Пример 7
Получение формы II
Форму I, полученную с помощью способа согласно примеру 1, нагревали до 170°C в N2, затем охлаждали до комнатной температуры естественным образом с получением необходимой формы II.
Пример 8
Получение формы II
Форму I, полученную с помощью способа согласно примеру 1, нагревали до 180°C в N2, затем охлаждали до комнатной температуры естественным образом с получением необходимой формы II.
Пример 9
Получение формы II
Форму I, полученную с помощью способа согласно примеру 1, нагревали до 165°C в N2, затем охлаждали до комнатной температуры естественным образом с получением необходимой формы II.
Пример 10
Получение формы III
15 мг формы I, полученной с помощью способа согласно примеру 1, помещали в 3 мл пузырек. Этот пузырек помещали внутрь 20 мл пузырька, заполненного насыщенными парами ацетонитрила. Большой пузырек запаивали и хранили при комнатной температуре в течение одной недели, извлекали необходимый полиморф. При этом температура плавления полиморфной формы III составляла 175-178°C.
Пример 11
Получение формы IV
15 мг формы I, полученной с помощью способа согласно примеру 1, помещали в 3 мл пузырек. Этот пузырек помещали внутрь 20 мл пузырька, заполненного насыщенными парами метанола. Больший пузырек запаивали и хранили при комнатной температуре в течение одной недели и извлекали необходимый полиморф. При этом температура плавления полиморфной формы IV составляла 175-177°C.
Пример 12
Фармакокинетическое исследование икотиниба гидрохлорида и полиморфной формы II икотиниба
Лекарственные средства и реактивы: икотиниба гидрохлорид, используемый в данном исследовании, относился к кристаллической форме I, раскрытой в документе WO2010/003313. Полиморфную форму II икотиниба и икотиниба гидрохлорид размалывали до мелких частиц. Содержание материала (чистота) составляло не менее чем 99,0%. Карбоксиметилцеллюлоза натрия имела степень чистоты, пригодной для медицинского применения.
Экспериментальные животные: крыс SD делили на группу икотиниба гидрохлорида и группу полиморфной формы II.
Приготовление фармацевтического средства: отвешивали определенное количество каждого соединения, а затем добавляли карбоксиметилцеллюлозу натрия с получением в результате концентрации тестируемого соединения 0,5%. Затем добавляли смесь в твердом состоянии для приготовления из нее суспензии в конечной концентрации 10 мг/мл в воде.
Введение и сбор образцов: каждую суспензию вводили перорально крысам SD натощак в дозе, эквивалентной 50 мг/кг икотиниба в объеме дозы 5 мл/кг. 0,4 мл крови собирали в предварительно заполненные антикоагулянтом EDTA-K пробирки с временными интервалами 0,5, 1, 1,5, 2, 4, 6, 8 и 24 часа после введения тестируемого соединения, центрифугировали при 3000 об/мин в течение 10 минут, и 120 мкл плазмы отбирали и хранили в холодильнике.
Образцы анализировали с помощью высокоэффективной жидкостной хроматографии. В хроматографии использовали C18-силан-связанный диоксид кремния в качестве неподвижной фазы, 0,02 моля/л дигидрофосфата натрия в ацетонитриле (40:60, с использованием раствора гидроксида натрия для доведения pH до 5,0) в качестве подвижной фазы, и длина волны детектирования 334 нм. Сравнение PK профиля для полиморфной формы II икотиниба и кристаллической формы I икотиниба гидрохлорида кратко изложено в таблице 1 и на фигуре 5. Полиморфная форма II икотиниба показывала более высокую биодоступность, нежели кристаллическая форма I икотиниба гидрохлорида.
Таблица 1
(мг/л*час)
(мг/л*час)
(час)
(час)
(мг/л)
Пример 13
Состав для твердой гелевой капсулы
В конкретном варианте осуществления композиции для перорального введения приблизительно 100 мг полиморфной формы из примеров 1-11 составляют с достаточно тонкодисперсной лактозой с получением общего количества от примерно 580 мг до приблизительно 590 мг для заполнения твердой гелевой капсулы размера 0.
Хотя настоящее изобретение было в полной мере описано применительно к вариантам его осуществления со ссылкой на прилагаемые графические материалы, следует отметить, что различные изменения и модификации будут очевидны для специалистов в данной области. Такие изменения и модификации следует считать включенными в объем настоящего изобретения, который определяется прилагаемой формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИМОРФНЫЕ ФОРМЫ ИКОТИНИБА МАЛЕАТА И ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2708079C2 |
| НОВЫЕ ПОЛИМОРФНЫЕ ФОРМЫ ИКОТИНИБА ФОСФАТА И ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2712169C2 |
| СОЛЬ АГОНИСТА ОПИОИДНОГО РЕЦЕПТОРА (MOR), КРИСТАЛЛИЧЕСКАЯ ФОРМА I ЕГО ФУМАРАТНОЙ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2018 |
|
RU2779119C2 |
| ПОЛИМОРФНЫЕ И АМОРФНАЯ ФОРМЫ ФОСФАТНОЙ СОЛИ 8-ФТОР-2-{4-[(МЕТИЛАМИНО)МЕТИЛ]ФЕНИЛ}-1,3,4,5-ТЕТРАГИДРО-6Н-АЗЕПИНО[5.4.3-CD]ИНДОЛ-6-ОНА | 2005 |
|
RU2355691C2 |
| КРИСТАЛЛИЧЕСКИЕ СОЛЬВАТЫ ГИДРОХЛОРИДА 6-(ПИПЕРИДИН-4-ИЛОКСИ)-2Н-ИЗОХИНОЛИН-1-OHA | 2012 |
|
RU2619129C2 |
| НОВЫЕ ПОЛИМОРФЫ И СОЛИ | 2011 |
|
RU2573384C2 |
| ПОЛИМОРФНАЯ ФОРМА КРИСТАЛЛИЧЕСКОГО ГИДРОХЛОРИДА ИРИНОТЕКАНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ | 2003 |
|
RU2300535C2 |
| ПОЛИМОРФ РИФАКСИМИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2593750C2 |
| НОВЫЕ ПОЛИМОРФНЫЕ ФОРМЫ ТРИМЕБУТИНА МАЛЕАТА, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2019 |
|
RU2770301C2 |
| НОВЫЕ ПОЛИМОРФНЫЕ ФОРМЫ ТРИМЕБУТИНА МАЛЕАТА, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2019 |
|
RU2770300C2 |




Изобретение относится к полиморфной форме соединения формулы I,
 формула I
формула I
Полиморфная форма представляет собой форму II, и ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих 5,5°, 11,0°, 19,7°, 20,9° и 22,6°± 0,2°. Также предложен способ получения полиморфной формы. Предложенная полиморфная форма II обладает более высокой биодоступностью. 2 н. и 5 з.п. ф-лы, 5 ил., 1 табл., 13 пр.
1. Полиморфная форма соединения формулы I,
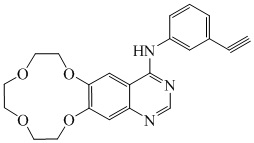
формула I,
где полиморфная форма представляет собой форму II, и ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих 5,5°, 11,0°, 19,7°, 20,9° и 22,6° ± 0,2°.
2. Полиморфная форма по п. 1, где ее рентгеновская порошковая дифрактограмма имеет характеристические пики при углах дифракции 2θ, составляющих 5,5°, 8,8°, 11,0°, 16,5°, 19,7°, 20,9°, 22,6° и 23,7° ± 0,2°.
3. Полиморфная форма по п. 1, где рентгеновская порошковая дифрактограмма представлена в том же виде, как и на фигуре 2.
4. Полиморфная форма по п. 1, где температура плавления составляет 176-178°C.
5. Способ получения полиморфной формы по п. 1, предусматривающий:
a) растворение икотиниба гидрохлорида в смеси этанола и воды, причем смесь нагревают до 40-60°C и раствор основания добавляют по каплям; затем раствор перемешивают в течение 1 часа, охлаждают до комнатной температуры и извлекают полиморфную форму; и
b) нагревание полиморфной формы из a) до температуры 150-180°C в N2, а затем охлаждение до комнатной температуры естественным образом с получением в результате полиморфной формы по любому из пп. 1-4.
6. Способ по п. 5, где температура для b) составляет 160-170°C.
7. Способ по п. 6, где температура составляет 165°C.
| WO 2003082830 A1, 09.10.2003 | |||
| CA 2854083 A1, 10.05.2013 | |||
| HU S | |||
| et al, Synthesis and biological evaluation of crown ether fused quinazoline analogues as potent EGFR inhibitors, Bioorg | |||
| Med | |||
| Chem | |||
| Lett., 2012, v | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| РАЗБОРНЫЙ ПЛАСТИНЧАТЫЙ РАДИАТОР | 1925 |
|
SU6301A1 |
| ЗАЩИТНЫЙ КОМПЛЕКТ ДЛЯ ГОЛОВЫ | 2008 |
|
RU2392576C2 |
Авторы
Даты
2019-12-24—Публикация
2014-06-09—Подача