Изобретение относится к области производственной трансфузиологии, фармацевтической биотехнологии и может быть использовано для получения антирезусной плазмы для производства лекарственных препаратов антирезусного иммуноглобулина человека.
Иммунопрофилактика антирезусным иммуноглобулином осуществляется в целях уменьшения риска резус-иммунизации беременных женщин, заболеваемости новорожденных гемолитической болезнью и перинатальной смертности, а также при лечении первичной иммунной тромбоцитопении у пациентов с положительным резус-фактором [Оловникова Н.И., Николаева Т.Л., Эршлер М.А. Иммунопрофилактика резус-иммунизации: перспектива создания моноклонального иммуноглобулина для предупреждения гемолитической болезни новорожденных. Иммунология. 2018; 1 (39): 74-80; El-Habil M.K. Anti-D immunoglobulin versus immunoglobulin G for the treatment of acute immune thrombocytopenia in children: a 10-year retrospective study. Lancet. 2021; S25 (398): 25]. Для производства этого препарата используют плазму крови доноров, которая содержит антитела к D-антигену эритроцитов в титре 1:64 и выше [Приказ Минздрава России от 21.11.2022 N 750н "Об утверждении порядка иммунизации доноров для заготовки иммуноспецифической плазмы" (Зарегистрировано в Минюсте России 30.11.2022 N 71216]. Для получения такой плазмы из уровня техники известен способ иммунизации доноров D-положительными эритроцитами. Для достаточной продукции анти-D антител может быть проведено до 4 курсов иммунизации. Каждый курс включает в себя 3-4 внутривенных или внутримышечных инъекции эритроцитов подходящего фенотипа в объеме по 5-10 мл. При использовании такого способа получения антирезусной плазмы целевой показатель уровня антител оценивается в титрах [Приказ Минздрава России от 21.11.2022 N 750н «Об утверждении порядка иммунизации доноров для заготовки иммуноспецифической плазмы» (Зарегистрировано в Минюсте России 30.11.2022 N 71216].
Известно, что дозу препарата, необходимую для предотвращения резус-иммунизации, назначают, исходя из следующего соотношения: для нейтрализации 0,5 мл резус-положительных эритроцитов плода, попавших в кровоток матери, необходимо 50 международных единиц анти-D антител [Guideline on the clinical investigation of human anti-D Immunoglobulin for intravenous and/or intramuscular use: EMA CPMP/BPWG/575/99 Rev. 1]. То есть более информативным является выражение количества антител в препарате в международных единицах, что позволяет рассчитать эффективную дозу препарата. Соответственно и активность донорской плазмы, которая служит сырьем для производства антирезусного иммуноглобулина человека, целесообразно определять в указанных единицах.
Кроме того, нтирезусная плазма может быть получена от естественно иммунизированных лиц, например, резус-отрицательных женщин, аллоиммунизированных к D-антигену в результате беременности. Получение сырья без дополнительной антигенной стимуляции безопасно для донора и позволяет значительно снизить затраты, связанные с проведением иммунизации.
Описание сущности изобретения
В связи с тем, что существует потребность в решении вышеизложенной проблемы поставлена техническая задача разработать способ получения антирезусной плазмы от естественно иммунизированных лиц, который может быть использован для заготовки иммунного сырья для производства антирезусного иммуноглобулина человека и позволяет стандартизовать плазму по содержанию анти-D антител в международных единицах.
Техническим результатом заявленного изобретения является повышение эффективности иммунопрофилактики резус-иммунизации, более полное использование донорского ресурса и упрощение процедуры получения иммунного сырья за счет применения плазмы от естественно иммунизированных лиц.
Технический результат достигается за счет того, что способ получения антирезусной плазмы крови человека включает в себя
проведение поиска в доступной информационной системе трансфузиологии потенциальных доноров антирезусной плазмы с отрицательной резус-принадлежностью и отводенных от донаций по причине выявления в крови антиэритроцитарных антител;
формирование пула доноров с титром анти-D антител 1:64 и выше;
заготовку плазмы и определение в ней содержания анти-D антител в сравнении с эталоном с известным содержанием анти-D антител, выраженным в международных единицах, причем для определения содержания анти-D антител готовят последовательные 1,5-кратные разведения образцов плазмы, начиная с разведения в два раза ниже, чем титр антител, выявленный в крови доноров, и 1,5-кратные разведения эталона в диапазоне содержания анти-D антител от 0,002 до 0,020 МЕ/мл, а содержание анти-D антител в исследуемом образце определяют путем умножения количества анти-D антител в максимальном разведении эталона, при котором наблюдается агглютинация эритроцитов, на максимальное разведение исследуемого образца с наличием гемагглютинации.
При этом индивидуальные единицы плазмы крови доноров заготавливают методом автоматического плазмафереза в объеме в среднем 600 мл, или из дозы крови методом центрифугирования в объеме в среднем 250 мл.
Заявляемое изобретение разработано в ФГБУН КНИИГиПК ФМБА России в соответствии с планом научно-исследовательской работы на тему: «Разработка стандартного образца содержания антирезус Rh0(D) антител для определения специфической (антирезусной) активности препаратов иммуноглобулина человека антирезус Rho(D)» (шифр: «Стандартные образцы-20», № гос. регистрации АААА-А20-120022090028-2 от 20.02.2020).
Способ осуществляется следующим образом:
Поиск потенциальных доноров проводят с помощью доступной информационной системы трансфузиологии. К параметрам поиска относятся: отрицательная резус-принадлежность и отвод от донаций по причине выявления антиэритроцитарных антител. Потенциальных доноров антирезусной плазмы направляют на иммуногематологическое обследование для определения титра анти-D антител. Плазму заготавливают методом автоматического афереза или из дозы крови от доноров с титром анти-D антител 1:64 и выше. В заготовленной плазме определяют содержание анти- D антител методом непрямой гемагглютинации с использованием эталона, аттестованного в международных единицах. При этом не требуется проведения предварительной иммунизации доноров резус-положительными эритроцитами человека. Полученная таким образом антирезусная плазма стандартизована по количеству анти-D антител в международных единицах, что способствует повышению качества выпускаемых отечественных препаратов антирезусного иммуноглобулина человека и повышению эффективности анти-D иммунопрофилактики.
Возможность осуществления заявленного способа раскрыта в следующих примерах.
Пример 1. Поиск потенциальных доноров антирезусной плазмы
Поиск потенциальных доноров может быть осуществлен с использованием автоматизированной информационной системы трансфузиологии (АИСТ) по заданным параметрам (отрицательная резус-принадлежность и отвод от донаций по причине выявления антиэритроцитарных антител). В плазме крови лиц, соответствующих заданным параметрам, определяют содержание анти-D антител в реакции непрямой гемагглютинации, например, с использованием гелевых карт ID Кумбс Анти-IgG и оборудования производства BioRad DiaMed GmbH, Швейцария.
За период январь 2015 г. - декабрь 2022 г. критериям поиска соответствовали 510 доноров. По результатам иммуногематологического исследования у 28 доноров в крови выявлены анти-D антитела в количестве 1:64 и выше. Таким образом, среди лиц, которые отведены от донорства по причине наличия в крови антиэритроцитарных антител, каждый 18-ый потенциально может стать донором антирезусной плазмы.
Пример демонстрирует возможность получения антирезусной плазмы от естественно иммунизированных к D-антигену лиц и повышение эффективности использования донорского ресурса за счет увеличения числа доноров, допущенных к донации, на 5,5%.
Пример 2. Заготовка антирезусной плазмы крови человека
После допуска донора к донации заготавливают плазму методом автоматического плазмафереза, при этом объем заготовленного таким образом компонента составляет в среднем 600 мл, или из дозы крови методом центрифугирования, объем компонента - в среднем 250 мл. Заготовленную плазму замораживают в быстрозамораживателе при температуре минус 80°С в течение не менее 30 минут и хранят при температуре не ниже минус 25°С для сохранения функциональной активности и биологической полноценности белков плазмы крови.
Пример демонстрирует возможность получения индивидуальных единиц антирезусной плазмы от естественно иммунизированных лиц в объеме в среднем 600 мл или 250 мл.
Пример 3. Определение диапазона разведения образцов донорской плазмы
Исследуемые образцы:
А - образец донорской плазмы с титром анти-D антител 1:64;
Б - образец донорской плазмы с титром анти-D антител 1:512;
B - образец донорской плазмы с титром анти-D антител 1:2560.
Образцы предварительно разводят фосфатным буферным раствором 0,01 М, рН 7,4, содержащим 2 г/л бычьего сывороточного альбумина. Предварительное разведение выбирают в два раза ниже, чем титр анти-D антител, выявленный в крови донора: образец А - 1:32, образец Б - 1:256, образец В -1:1280. Последующие 1,5-кратные разведения готовят в лунках U- или V-образного 96-луночного планшета. В первый ряд лунок переносят по 225 мкл приготовленных разведений, в четыре следующих ряда - по 150 мкл фосфатного буферного раствора. Содержимое лунок тщательно перемешивают и последовательно переносят по 75 мкл смеси. Из лунок крайнего (пятого) ряда 75 мкл смеси удаляют в емкость с дезинфицирующим раствором.
Проводят реакцию гемагглютинации в геле, например, с использованием гелевых карт ID Кумбс Анти-IgG и оборудования производства BioRad DiaMed GmbH, Швейцария. В промаркированные микропробирки гелевой карты вносят по 25 мкл приготовленных разведений исследуемых образцов и по 50 мкл 0,8% суспензии папаинизированных эритроцитов человека предпочтительно с фенотипом 0R2R2 (например, входящих в набор готовых эритроцитарных реагентов ID-DiaCell IP-IIP-IIIP производства BioRad DiaMed GmbH, Швейцария). Для контроля специфичности используют эритроциты с фенотипом 0rr (например, входящие в набор готовых эритроцитарных реагентов ID-DiaCell IP-IIP-IIIP производства BioRad DiaMed GmbH, Швейцария) и исследуемый образец в наименьшем разведении. Карты термостатируют в инкубаторе в течение 15 минут при (37 ± 1)°С, по окончании инкубации помещают в центрифугу для гелевых карт и проводят центрифугирование в течение 10 минут при скорости 1175 об/мин.
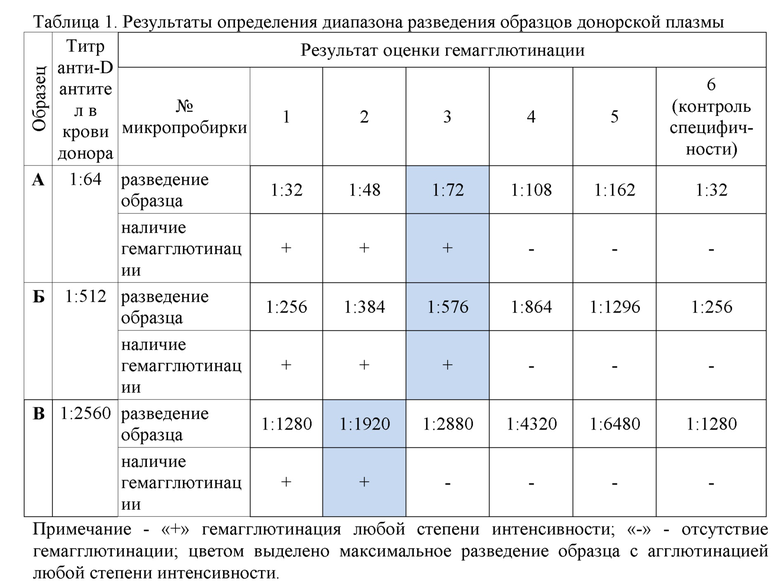
Учитывают результат реакции. Результат реакции учитывают, если в микропробирках с эритроцитами с фенотипом 0rr гемагглютинация отсутствует (контроль специфичности). Регистрируют степень агглютинации в микропробирках и максимальное разведение образца, при котором заметна гемагглютинация любой интенсивности. Результаты представлены в таблице 1. Согласно представленным данным максимальное разведение образцов, при котором наблюдается гемагглютинация, соответствует 2 и 3 микропробиркам гелевой карты. Специфичность подтверждена отсутствием гемагглютинации в пробах с эритроцитами с фенотипом 0rr (микропробирка № 6).
Пример демонстрирует возможность регистрации результата реакции при использовании 1,5-кратных разведений образцов плазмы, начиная с разведения в два раза ниже, чем титр анти-D антител, выявленный в крови доноров.
Пример 4. Определение диапазона разведения эталона
В качестве эталона, аттестованного в международных единицах, используют, например, 3-ий международный стандартный образец (МСО) анти-D иммуноглобулина c активностью 297 МЕ/мл (3nd WHO International Standard for anti-D Immunoglobulin, code: 16/332, производства NIBSC, Великобритания).
МСО предварительно разводят фосфатным буферным раствором 0,01 М, рН 7,4, содержащим 2 г/л бычьего сывороточного альбумина, до содержания анти-D антител 0,200 МЕ/мл (1), 0,020 МЕ/мл (2), 0,015 МЕ/мл (3), 0,010 МЕ/мл (4), 0,005 МЕ/мл (5). Последующие 1,5-кратные разведения готовят в лунках U- или V-образного 96-луночного планшета. В первый ряд лунок переносят по 225 мкл приготовленных разведений МСО (1) - (5), в четыре следующих ряда - по 150 мкл фосфатного буферного раствора. Содержимое лунок тщательно перемешивают и последовательно переносят по 75 мкл смеси. Из лунок крайнего (пятого) ряда 75 мкл смеси удаляют в емкость с дезинфицирующим раствором.
Проводят реакцию гемагглютинации в геле, например, с использованием гелевых карт ID Кумбс Анти-IgG и оборудования производства BioRad DiaMed GmbH, Швейцария. В промаркированные микропробирки гелевой карты вносят в дублях по 25 мкл приготовленных разведений МСО и по 50 мкл 0,8% суспензии папаинизированных эритроцитов человека предпочтительно с фенотипом 0R2R2 (например, входящих в набор готовых эритроцитарных реагентов ID-DiaCell IP-IIP-IIIP производства BioRad DiaMed GmbH, Швейцария). Для контроля специфичности используют эритроциты с фенотипом 0rr (например, входящие в набор готовых эритроцитарных реагентов ID-DiaCell IP-IIP-IIIP производства BioRad DiaMed GmbH, Швейцария) и МСО в наименьшем разведении. Карты термостатируют в инкубаторе в течение 15 минут при температуре от (37 ± 1)°С, по окончании инкубации помещают в центрифугу для гелевых карт и проводят центрифугирование в течение 10 минут при скорости 1175 об/мин.
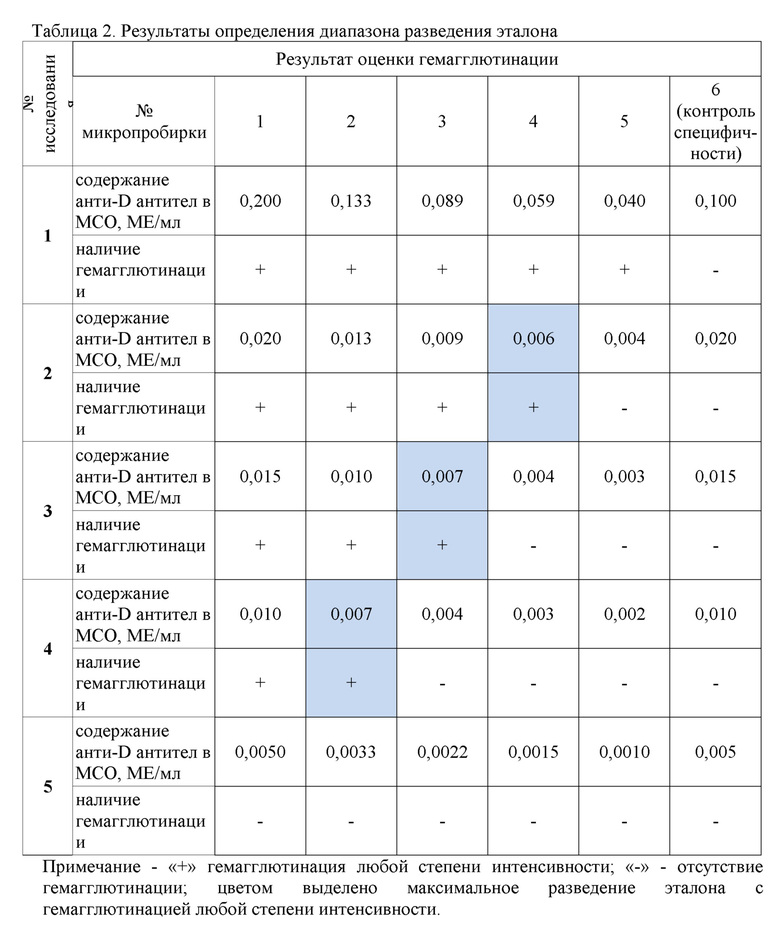
Учитывают результат реакции. Результат реакции учитывают, если в микропробирках с эритроцитами с фенотипом 0rr агглютинация отсутствует (контроль специфичности). Регистрируют степень агглютинации в микропробирках и максимальное разведение МСО, при котором наблюдается гемагглютинация. Результаты представлены в таблице 2. Согласно представленным данным в первом ряду разведений (от 0,200 до 0,040 МЕ/мл) во всех микропропробирках отмечено наличие гемагглютинация. В этом случае для определения максимального разведения необходимо тестировать МСО в больших разбавлениях. В пятом ряду разведений (от 0,0050 до 0,0010 МЕ/мл), напротив, отмечено отсутствие агглютинации эритроцитов. Для определения максимального разведения, дающего гемагглютинацию, необходимо тестировать МСО в меньших разведениях.
Диапазон разведений МСО, при котором может быть определено максимальное разведение, соответствует рядам:
от 0,020 до 0,004 МЕ/мл (2);
от 0,015 до 0,003 МЕ/мл (3);
от 0,010 до 0,002 МЕ/мл (4),
Значения максимального разведения составляют 0,006, 0,007 и 0,007 МЕ/мл. Специфичность подтверждена отсутствием гемагглютинации во всех пробах с эритроцитами с фенотипом 0rr (микропробирка № 6).
Пример демонстрирует возможность регистрации результата реакции при использовании 1,5-кратных разведений эталона в диапазоне содержания анти-D антител от 0,002 до 0,020 МЕ/мл.
Пример 5. Определение содержания анти-D антител в антирезусной плазме в международных единицах
Исследуемые образцы
А - образец донорской плазмы с титром анти-D антител 1:64;
Б - образец донорской плазмы с титром анти-D антител 1:128;
B - образец донорской плазмы с титром анти-D антител 1:256;
Г - образец донорской плазмы с титром анти-D антител 1:512;
Д - образец донорской плазмы с титром анти-D антител 1:640;
Е - образец донорской плазмы с титром анти-D антител 1:2560;
Содержание анти-D антител в образцах донорской плазмы определяют в реакции непрямой гемагглютинации в сравнении с эталоном, аттестованным в международных единицах, например, с 3-им международным стандартным образцом (МСО) анти-D иммуноглобулина c активностью 297 МЕ/мл (3nd WHO International Standard for anti-D Immunoglobulin, code: 16/332 производства NIBSC, Великобритания).
Для приготовления разведений используют фосфатный буферный раствора 0,01 М, рН 7,4, содержащий 2 г/л бычьего сывороточного альбумина.
В микроцентрифужных пробирках предварительно разводят исследуемые образцы плазмы и МСО. При приготовлении предварительного разведения образцов плазмы ориентируются на титр анти-D антител, выявленный в крови донора: готовят разведение в два раза ниже, чем титр анти-D антител по примеру 3. МСО разводят до содержания анти-D антител в диапазоне от 0,002 до 0,020 МЕ/мл по примеру 4. Готовят предварительное разведение МСО, например, в 20000 раз до ожидаемого содержания анти-D антител 0,015 МЕ/мл.
Последующие разведения готовят в лунках U- или V-образного 96-луночного планшета. В первый ряд лунок переносят по 225 мкл приготовленных разведений, в четыре следующих ряда - по 150 мкл фосфатного буферного раствора 0,01 М, рН 7,4, содержащего 2 г/л бычьего сывороточного альбумина. Содержимое лунок тщательно перемешивают и последовательно переносят по 75 мкл смеси. Из лунок крайнего (пятого) ряда 75 мкл смеси удаляют в емкость с дезинфицирующим раствором.
В промаркированные микропробирки гелевой карты вносят в дублях по 25 мкл приготовленных разведений исследуемых образцов и МСО и по 50 мкл 0,8 % суспензии папаинизированных эритроцитов человека предпочтительно с фенотипом 0R2R2 (например, входящих в набор готовых эритроцитарных реагентов ID-DiaCell IP-IIP-IIIP производства BioRad DiaMed GmbH, Швейцария). Для контроля специфичности исследуемый образец и МСО в наименьших разведениях инкубируют с эритроцитами с фенотипом 0rr (например, входящих в набор готовых эритроцитарных реагентов ID-DiaCell IP-IIP-IIIP производства BioRad DiaMed GmbH, Швейцария) в течение 15 минут при температуре от (37 ± 1)°С, по окончании термостатирования помещают в центрифугу для гелевых карт и проводят центрифугирование в течение 10 минут при скорости 1175 об/мин.
Учитывают результат реакции. Результат реакции учитывают, если в микропробирках с эритроцитами с фенотипом 0rr гемагглютинация отсутствует (контроль специфичности). Определяют максимальное разведение образца, при котором заметна гемагглютинация любой интенсивности.
Содержание анти-D антител рассчитывают по отношению к МСО с использованием формулы:

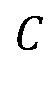 - содержание анти-D антител в испытуемом образце, МЕ/мл;
- содержание анти-D антител в испытуемом образце, МЕ/мл;
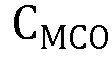 - содержание анти-D антител в максимальном разведение МСО, при котором наблюдается гемагглютинация любой интенсивности, МЕ/мл;
- содержание анти-D антител в максимальном разведение МСО, при котором наблюдается гемагглютинация любой интенсивности, МЕ/мл;
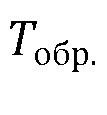 - величина, обратная максимальному разведению исследуемого образца, при котором наблюдается гемагглютинация любой интенсивности.
- величина, обратная максимальному разведению исследуемого образца, при котором наблюдается гемагглютинация любой интенсивности.
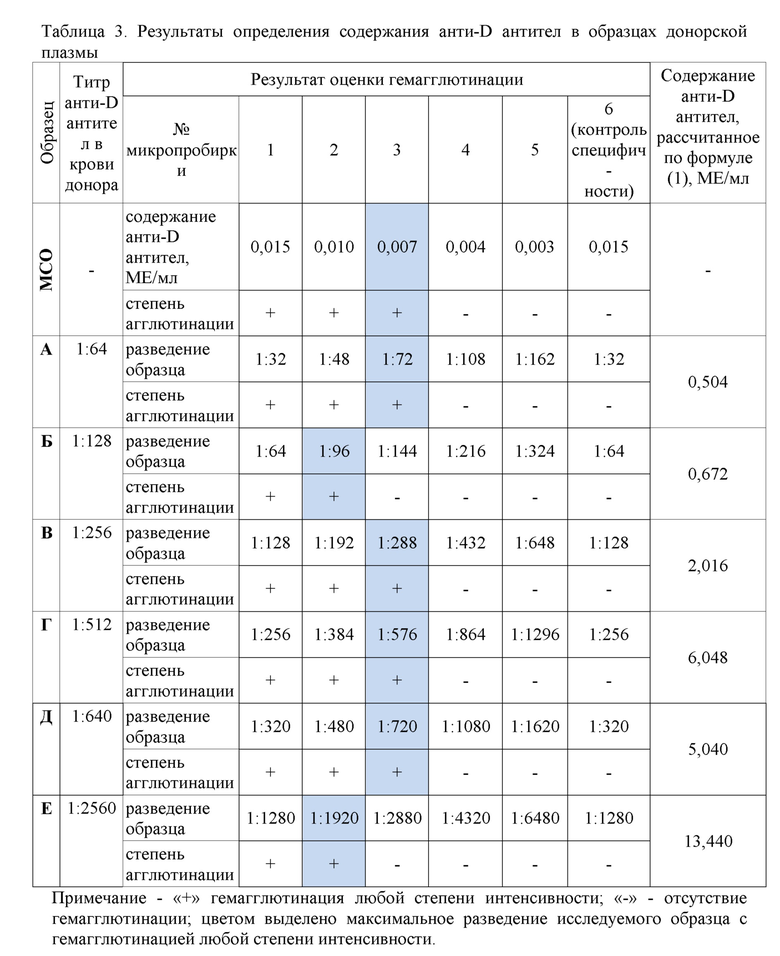
Результаты определения анти-D антител согласно вышеизложенному примеру приведены в таблице 3. Рассчитанное по формуле (1) содержание анти-D антител в образцах донорской плазмы составляет от 0,504 до 13,44 МЕ/мл.
Пример демонстрирует возможность стандартизации антирезусной плазмы по содержанию анти-D антител в международных единицах.
Представленные примеры не ограничивают объем притязаний настоящего изобретения и служат только для цели иллюстрации и раскрытия заявленного способа.
Промышленная применимость
Все приведенные примеры подтверждают возможность осуществления заявленного способа с целью получения антирезусной плазмы от естественно иммунизированных лиц и ее стандартизации по содержанию анти-D антител в международных единицах.
Поставленная техническая задача, а именно разработка способа получения антирезусной плазмы, который может быть использован в производстве антирезусного иммуноглобулина человека и который позволяет получать сырье от естественно иммунизированных лиц, стандартизованное по содержанию анти-D антител в международных единицах, достигнута, что подтверждается приведенными примерами.
Применение поставленного технического решения в области производственной трансфузиологии, фармацевтической биотехнологии является эффективным и может быть применено для получения антирезусной плазмы для производства лекарственных препаратов антирезусного иммуноглобулина человека.
| название | год | авторы | номер документа |
|---|---|---|---|
| Стандартный образец содержания анти-D антител в препаратах иммуноглобулинов человека | 2017 |
|
RU2682714C1 |
| Стандартный образец содержания анти-А и анти-В гемагглютининов в препаратах крови человека | 2017 |
|
RU2671415C1 |
| Способ количественного определения анти-D-антител IgG в препаратах иммуноглобулина человека антирезус Rh0(D) | 2021 |
|
RU2777845C1 |
| Способ определения уровня посттрансплантационного химеризма путем оценки экспрессии антигенов системы Резус и Келл в гелевых картах | 2021 |
|
RU2761100C1 |
| Способ определения антиэритроцитарных аллоантител у больных множественной миеломой | 2021 |
|
RU2790833C1 |
| МОНОКЛОНАЛЬНЫЙ ИММУНОГЛОБУЛИН ЧЕЛОВЕКА КЛАССА IGGI ПРОТИВ АНТИГЕНА D СИСТЕМЫ РЕЗУС | 1995 |
|
RU2094462C1 |
| Способ приготовления тестовой сыворотки для определения резус-фактора | 1977 |
|
SU719632A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТРАНСФУЗИИ ГОМОЛОГИЧНОЙ КРОВИ ПРИ ДОПИНГОВОМ КОНТРОЛЕ СПОРТСМЕНОВ | 2011 |
|
RU2470304C2 |
| ТЕСТ-СИСТЕМА ДЛЯ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНТИ-HBS В БИОЛОГИЧЕСКОМ ОБРАЗЦЕ | 2005 |
|
RU2290642C2 |
| ПРЕПАРАТ ИММУНОГЛОБУЛИНА ЧЕЛОВЕКА ПРОТИВ ЦИТОМЕГАЛОВИРУСА ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2404250C1 |
Изобретение относится к области производственной трансфузиологии, фармацевтической биотехнологии и может быть использовано для получения антирезусной плазмы для производства лекарственных препаратов антирезусного иммуноглобулина человека. Способ включает в себя поиск потенциальных доноров антирезусной плазмы с помощью доступной информационной системы трансфузиологии по заданным параметрам (отрицательная резус-принадлежность и отвод от донаций по причине выявления в крови антиэритроцитарных антител); формирование пула доноров с титром анти-D антител 1:64 и выше; заготовку плазмы методом автоматического плазмафереза объемом в среднем 600 мл или из дозы крови методом центрифугирования объемом в среднем 250 мл; определение содержания анти-D антител методом непрямой гемагглютинации в сравнении с эталоном с известным содержанием анти-D антител. Для этого готовят последовательные 1,5-кратные разведения образцов плазмы, начиная с разведения в два раза ниже, чем титр антител, выявленный в крови донора, и 1,5-кратные разведения эталона в диапазоне содержания анти-D антител от 0,002 до 0,020 МЕ/мл. Содержание анти-D антител в исследуемом образце определяют путем умножения количества анти-D антител в максимальном разведении эталона, при котором наблюдается агглютинация эритроцитов, на максимальное разведение исследуемого образца с наличием гемагглютинации. Использование изобретения позволяет повысить эффективность использования донорской плазмы, снизить трудозатраты, связанные с проведением технологически сложной процедуры иммунизации доноров эритроцитами человека, за счет использования плазмы крови доноров естественно иммунизированных к D-антигену, и стандартизовать донорскую плазму по содержанию анти-D антител в международных единицах. 1 з.п. ф-лы, 3 табл., 5 пр.
1. Способ получения антирезусной плазмы крови человека, заключающийся в том, что
проводят поиск потенциальных доноров антирезусной плазмы в доступной информационной системе трансфузиологии по отрицательной резус-принадлежности и отводу от донаций по причине выявления антиэритроцитарных антител,
формируют пул доноров с титром анти-D антител 1:64 и выше,
заготавливают плазму и определяют в ней содержание анти-D антител в сравнении с эталоном с известным содержанием анти-D антител, выраженным в международных единицах,
отличающийся использованием плазмы крови лиц, естественно иммунизированных к D-антигену, и стандартизацией антирезусной плазмы по содержанию анти-D антител в международных единицах, причем для определения содержания анти-D антител готовят последовательные 1,5-кратные разведения образцов плазмы, начиная с разведения в два раза ниже, чем титр антител, выявленный в крови доноров, и 1,5-кратные разведения эталона в диапазоне содержания анти-D антител от 0,002 до 0,020 МЕ/мл, а содержание анти-D антител в исследуемом образце определяют путем умножения количества анти-D антител в максимальном разведении эталона, при котором наблюдается агглютинация эритроцитов, на максимальное разведение исследуемого образца с наличием гемагглютинации.
2. Способ по п.1, отличающийся тем, что индивидуальные единицы плазмы крови доноров заготавливают методом автоматического плазмафереза в объеме в среднем 600 мл или из дозы крови методом центрифугирования в объеме в среднем 250 мл.
| Устройство для измерения структурной характеристики показателя преломления атмосферы | 1980 |
|
SU934427A1 |
| WO 1998012347 A1, 26.03.1998 | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| ОЛОВНИКОВА Н.И | |||
| и др | |||
| Иммунопрофилактика резус-иммунизации: перспектива создания моноклонального иммуноглобулина | |||
Авторы
Даты
2024-09-25—Публикация
2023-12-21—Подача