Изобретение относится к ветеринарной медицине, а именно к средствам, регулирующим метаболические процессы, и может быть использовано для снижения заболеваемости и повышения продуктивности телят.
Нарушения условий содержания, несбалансированность рационов кормления негативно влияют на состояние здоровья продуктивных животных, путем снижения иммунологической реактивности и обмена веществ в организме [1]. Известно, что новорожденные животные наиболее восприимчивы к воздействию неблагоприятных факторов внешней среды [2]. Высокая заболеваемость и гибель телят в первые дни жизни объясняется, прежде всего, отсутствием у них развитой системы регуляции их жизненно-важных функций, несовершенством пищеварительной системы и иммунной защиты организма [3]. Все это диктует необходимость разработки, поиска и внедрения в ветеринарную практику новых средств, способных конкурировать с синтетическими препаратами. В данном аспекте особого внимания заслуживают инъекционные средства растительного происхождения, имеющие ряд преимуществ. Они обладают более высокой усвояемостью, мягким, пролонгированным действием, низким уровнем токсичности, минимальными побочными эффектами и доступностью при производстве [4].
Лекарственные средства, полученные из растительного сырья, не уступают синтетическим аналогам, а порой и превосходят их по некоторым показателям, что связано с рядом преимуществ таких препаратов. Ряд авторов [5, 6], помимо вышеперечисленных достоинств связывают эффективность фитопрепаратов с эволюционно схожим химическим составом растительных и животных клеток, а также уникальным комплексом биологически активных веществ, входящих в их состав.
Известен препарат из растительного сырья, для повышения физической выносливости организма в условиях ультрафиолетового облучения, приготовленный в виде настоя из сбора крапивы, подорожника и травы звездчатки, при соотношении 1:1:1, измельченного и залитого кипящей водой из расчета 8 г сбора на 200 мл воды при времени настаивания 60 минут (Патент РФ №.2533446 МПК A61K 36/68, A61K 36/185, A61K 36/36) [7]. Настой применяют ежедневно из расчета 5 мл/кг массы в течение 21 дня.
Недостатком данного препарата является то, что настой плохо храниться и при этом теряет свои свойства в результате деятельности микроорганизмов: бактерий, плесени, грибков и других патогенов. К тому же, использование настоя характеризуется длительным периодом выпаивания, что увеличивает трудозатраты на обслуживание животных. Кроме того, препарат приготовленный данным способом не может быть использован в качестве инъекционного средства. При оральном введении препарата происходит медленное поступление лекарственного вещества в системный кровоток. Скорость всасывания непостоянна и зависит от наличия пищи в ЖКТ, его моторики (если моторика снижается, скорость всасывания падает). На принятые внутрь лекарственные средства воздействуют ферменты желудка и кишечного сока, метаболические ферментные системы печени, которые разрушают часть вещества еще до того, как они проникнут в системный кровоток. При инъекционном пути введения лекарство всасываясь через капилляры, сразу попадает в системный кровоток и доставляется к органам и тканям мишеням, минуя протоки воротной вены и печень [8].
Известно инъекционное лечебное средство, а именно экстракт алоэ, полученный путем консервации листьев алоэ в темноте при температуре +2-4°С в течение 7-10 суток, измельчения сырья и экстрагирования дистиллированной водой, при соотношении вода и сырье 1:3, настаивания 1 час, кипячения в течении 8-10 мин и фильтрации. Оставшийся шрот заливают водой в соотношении 1:2, кипятят 10 минут, фильтруют, после чего оба фильтрата объединяют (Патент РФ №2125882, МПК. А61К 36/886, А61К 9/08, А61К 127/00) [9].
Недостатком данного средства следует считать, прежде всего узкий спектр фармакологического действия, обусловленный ограниченным выбором биологически активных веществ, входящих в его состав, а именно антроцена, функцией которых является участие в окислительно-восстановительных процессах (См. ФС 42-1443-98, экстракт алоэ жидкий для инъекций ЛСР 007787/09) Далее, не смотря на то, что листья алоэ и сок алоэ древовидного содержат ферменты, витамины, фитонциды (алонин, наталоин и др.), смолистые вещества, следы эфирных масел, высокотемпературная обработка листьев алоэ приводит к инактивации ферментов, термолобильных витаминов и других биологически активных веществ, при этом происходит (свертывание) белковых соединений как в протоплазме так и клеточном соке, в результате этих процессов белки теряют способность растворяться, удерживать воду и переходят в нерастворимые соединения замедляя или прекращая процесс экстракции белковых соединений [10]. Так же при кипячении происходит растворение пектиновых веществ, полуклетчатки и пентозанов самих клеточных оболочек, что значительно ослабляет их, но не приводит к полному разрушению. Поэтому клеточная структура растительного сырья сохраняется, в следствии этого, снижается выход сопутствующих и балластных веществ.
Однако, лекарственные растения, как правило содержат не только биологически активные вещества (БАВ), но и сопутствующие и балластные вещества, которые оказывают фармакологическое действие, например: балластные вещества (крахмал, хлорофилл, каротиноиды) способны усиливать, или ослаблять действие основных веществ [11]. Полезные сопутствующие вещества (витамины, сахара, минеральные вещества) оказывают благоприятное действие на организм, а некоторые из них влияют на фармакотерапевтическое действие БАВ. Например, растворимые или набухающие полисахариды, дубильные вещества пролонгируют действие БАВ [12].
Известно средство для предупреждения развития и лечения воспалительных процессов у животных и как следствие, влияющих на обменные процессы, характеризующееся тем, что представляет собой смесь измельченных лекарственных растений, обработанных ультрафиолетовыми лучами, которую помещают в сухую стерильную емкость темного стекла, растительное сырье массой 800,0 г (10 мас. %) перемешивают с 2700,0 г (90 мас. %) 0,9% стерильного раствора натрия хлорида, смесь при перемешивании оставляют при комнатной температуре до 1,5 суток, затем помещают емкость со смесью в водяную баню до 10 ч с температурой смеси до 42°С при перемешивании, после чего отделяют жидкую часть от растительного сырья (Патент РФ №2395290, МПК А61К 36/00, А61К 36/28, А61К 36/534, А61К 36/66, А61К 36/38, А61К 36/72, А61К 36/738, А61К 29/00) [13].
Недостатком данного средства является то, что требуются особые условия при его хранении и использовании, так как при случайном попадании даже сапрофитной, не говоря уже об условно или патогенной микрофлоре, которая является неотъемлемой составляющей всех без исключения животноводческих помещений, полученное средство будет непригодно к использованию. Кроме этого, сам процесс «многоступенчатый» и продолжительный по времени, с низкотемпературной экстракцией (42°С), что так же требует особых, практически стерильных условий при его изготовлении. Многокомпонентное растительное средство в своем составе содержит как минимум 3 лекарственных растения относящихся к ядовитым, которые необходимо применять с особой осторожностью, например, чистотел содержит боле 2 десятков алкалоидов, 5 из которых очень опасны, пижма относится к условно ядовитым растениям, из-за эфирных масел, содержащих танацетум - который относиться к токсическим веществам, переходящий в настой при низкой тепловой обработке.
Задача, на решение которой направлено заявленное изобретение является разработка инъекционного средства из растительного сырья с высокой фармакологической эффективностью.
Указанный технический результат достигается тем, что заявленное инъекционное средство представляет собой смесь предварительно измельченных до размера частиц 0,3-0,8 мм, следующих лекарственных растений: листья алоэ древовидного, листья подорожника большого, листья крапивы двудомной, травы змееголовника тимьяноцветкового, цветки клевера розового, эхинацеи пурпурной, взятые в соотношении 5:1:1:1:1:1 соответственно, которую закладывают в ультразвуковой экстрактор, добавляют дистиллированную воду из расчета сырье : вода 1:10 и подвергают 10 минутному ультразвуковому озвучиванию с последующей 30 минутной выдержкой сырья в экстракторе для завершения мацерации, после чего экстракцию набухшего сырья осуществляют путем ультразвукового озвучивания в течении 1-1,2 часа до достижения температуры экстрагируемой массы 60°С при этом режим ультразвукового озвучивания, как при мацерации так при экстрагировании находится в пределах 37 кГц при мощности 264 Вт, после чего производят фильтрацию экстракта при использовании полиэфирных тканей (например, UVMILK® Fabric пищевой полипропилен РР НОЗО) с пористостью не более 25 мкм, в соответствии с технологическим стандартом для инъекционных растворов [14], фасуют и автоклавируют.Листья алоэ перед смешиванием с остальными компонентами смеси консервируют в темноте при температуре +2-4°С в течение 7-10 суток. Заявленное средство инъецируется в дозе из расчета 4,0 мг сухого вещества на 1 кг массы тела животного.
Подбор компонентов смеси трав, используемой в качестве сырья, при производстве заявленного средства производился с учетом разнообразия фармакологических свойств и химического состава, представленного комплексом биологически активных веществ, дополняющих друг друга при решении поставленной задачи, обеспечивающий нормализацию биохимических, иммунологических показателей крови, обменных процессов и других параметров.
Листья крапивы двудомной являются природным поливитаминным концентратом, улучшающим обмен веществ, благодаря витамину К, жидкий экстракт и настой листьев крапивы применяю как кровоостанавливающее средство при легочных, печеночных и других кровотечениях. Содержание ситостерина, фенольных кислот, флавоноидов, способствует увеличению общего количества гемоглобина, тромбоцитов и эритроцитов в периферической крови, регенерации слизистых оболочек желудочно-кишечного тракта [15, 16].
В листьях подорожника находятся флавоноиды и их производные. Также в растении присутствуют стероидные вещества, органические, оксикоричные кислоты, аминокислоты, витамины макро- и микроэлементы. Настой листьев подорожника обладает противовоспалительным, спазмолитическим, кровоостанавливающим, бактериостатическим действием, стимулирует процессы регенерации, способствует повышению секреции желудочного сока [17].
Лечебные свойства травы змееголовника тимьяноцветкового определяются такими компонентами, входящими в его состав как: органические и другие кислоты, микроэлементы, глютаминовая и аспарагиновая аминокислота, флавоноиды, наличие этих веществ, в составе лекарственных препаратов, способствуют улучшению пищеварения, восстанавливают и укрепляют иммунитет, помогают организму справляться с неблагоприятными внешними факторами [15].
Наземная часть клевера розового содержит гликозиды, углеводы, стероиды, сапонины, витамины С, В, Е и К, каротин, фенолкарбоновые кислоты, кумарины, жирное масло, дубильные вещества, хиноны, высшие жирные кислоты, микроэлементы и др. Клевер обладает мочегонным, желчегонным, противовоспалительным, противосклеротическим, антитоксическим, кровоостанавливающим, ранозаживляющим, болеутоляющим свойствами [18].
Эхинацея пурпурная - прекрасный иммуностимулятор, стимулирует как клеточный (активность Т-лимфоцитов), так и гуморальный (выработка антител) иммунитет. Водорастворимые полисахариды стимулируют клеточную иммунную систему, а жирорастворимые компоненты усиливают фагоцитоз. Флавоноиды содержащиеся в траве эхинацеи проявляют антиоксидантное, желчегонное, мембраностабилизирующее, противоаллергическое, противовоспалительное, спазмолитическое действие, а также повышают устойчивость организма к внешним отрицательным факторам, усиливают иммуномодулирующее действие полисахаридов на иммунную систему [19].
Алоэ древовидное. Листья алоэ содержат смолистые вещества, горечи, полисахариды, кислоту янтарную и др. Инъекционные препараты алоэ оказывают общее биостимулирующее действие и стимулируют иммунитет, что объясняет наличием биогенных стимуляторов, образующихся в тканях алоэ при неблагоприятных условиях (пониженная температура, отсутствие света); как средство неспецифической стимуляции, биостимуляторы из листьев алоэ обладают способностью повышать защитные функции организма и усиливать репаративные процессы в тканях, стимулировать кроветворение. (Листья алоэ древовидного свежие - ФС 42-2191-84.) [20].
Сущность заявленного изобретения характеризуется тем, что при производстве (изготовлении) средства использована низкотемпературная экстракция (до +60°С) позволяющая максимально сохранить термолабильные биологически активные, сопутствующие (витамины, органические кислоты, микро-, макроэлементы) и балластные (лигнин, пектин, клетчатка, полисахариды и др.) вещества. Оптимальный температурный максимум достигается, без постороннего подогрева, только при использовании ультразвукового озвучивания, при котором происходит медленное (без скачков температуры) нагревание экстрагируемой массы. При этом ультразвук усиливает в тканях проницаемость клеточных мембран и диффузные процессы, изменяет концентрацию водородных ионов в тканях, что способствует расщеплению высокомолекулярных соединений на составляющие и приводит к интенсификации процесса экстракции и дает возможность увеличить содержание биологически активных соединений в растворе [21].
При разработке технологических параметров получения заявленного средства из сырья, представленного в виде листьев и соцветий, провели ряд исследований. Известно, например, что время замачивания растительного сырья перед процессом экстракции зависит от скорости вытеснения воздуха из клетки, то есть от значения капиляропроводимости сырья. В нашем случае были проведены исследования, по влиянию взаимозависимости времени предварительного озвучивания сырья 5, 10, 15 минут и времени набухания (мацерация) 15, 30, 45, 60 минут, на выход сухого вещества в процессе дальнейшей экстракции с учетом разведения сырье: вода 1:5, 1:10, 1:20 при использовании ультразвуковой частоты 37 кГц при мощности ультразвука 132 Вт, 264 Вт, 330 Вт (табл. 1).
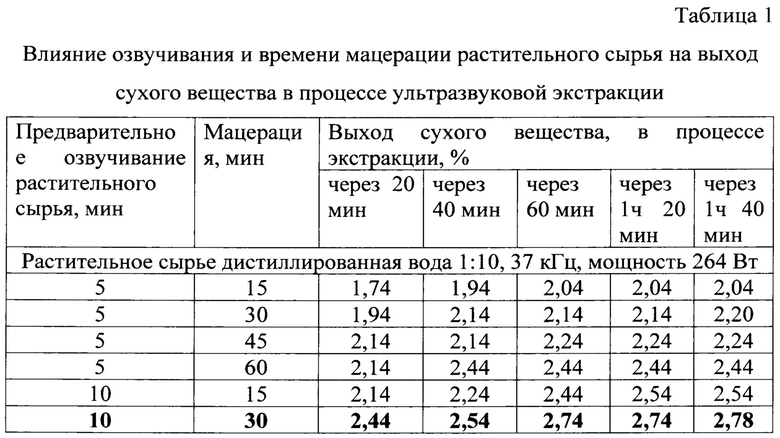
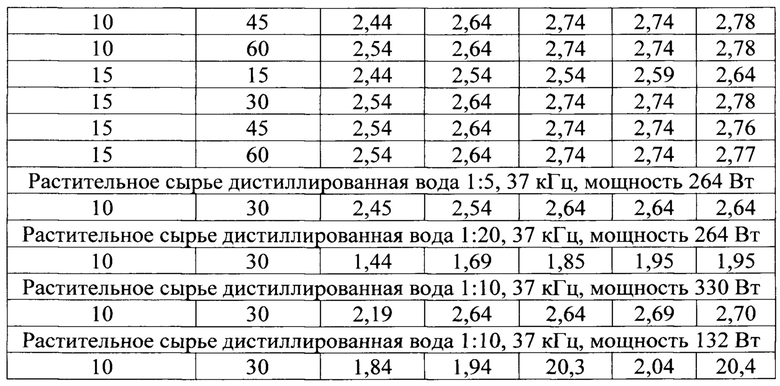
Пробы для определения содержания в экстракте сухого вещества брали через каждые 20, 40, 60, 80 минут. Как показали исследования, оптимальным режимом процесса экстракции для задействованного сырья было: время предварительного озвучивания - 10 мин, время мацерации 30 минут, время последующей экстракции 60-80 минут, при частоте ультразвука 37 кГц и мощности 264 Вт, где выход сухого вещества был на уровне 2,74%. Количество сухого вещества в пробе при использовании вместо 37 кГц 80 кГц, при прочих оптимальных параметрах процесса экстракции было на 7,30% ниже оптимальной и составила 2,54%.
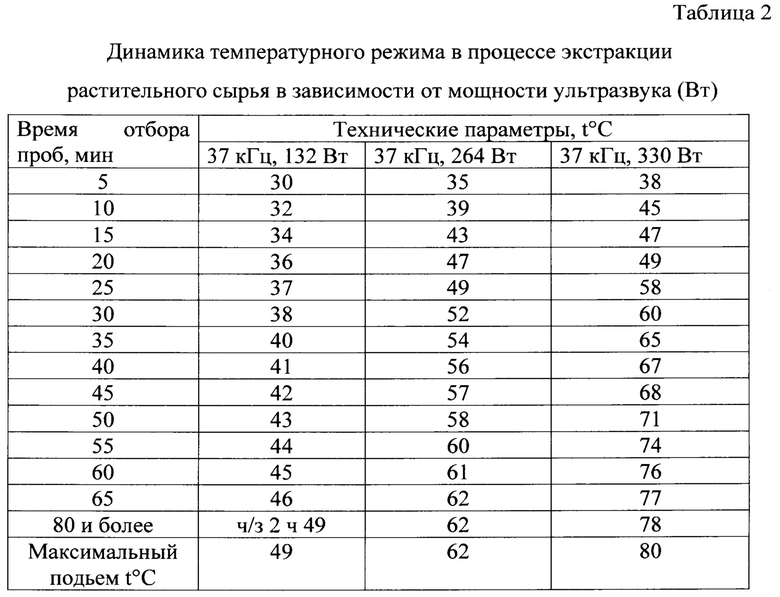
Исследование динамики температурного режима в процессе экстракции при различных ультразвуковых режимах показало отсутствие скачков температуры (плавный подъем в течение часа) таблица 2, оптимальным режимом с максимальным подъемом температуры до 62°С, при длительности ультразвуковой экстракции в течение 1-1,2 часа, следует считать технологические параметры с частотой ультразвука 37 кГц при мощности 264 Вт.
Для определения оптимальной дозы, проводили доклиническое испытание заявленного средства, с учетом фармакокинетических свойств лекарственных растений, на их основании прогнозировали клинические параметры (гематологические, иммунологические и др), путем сравнения с контрольными животными. Для этого сформировали 6 групп (n=10) аналогов новорожденных телят 1-3 дневного возраста, телятам контрольной группы (фон) испытуемое средство не инъецировали, телятам 5 опытных групп вводили инъекционное заявленное растительное средство подкожно в область средней трети шеи, в дозе 2,0, 3,0, 4,0, 5,0, 6,0 мг сухого вещества на 1 кг массы тела, что соответствует 2,7, 4,0, 5,4, 6,7, 8,1 мл заявленного средства при средней живой массе телят 37,0 кг. Инъецирование проводили 4 кратно с интервалом 7 дней. С увеличением живой массы, в процессе роста телят, объем введения (мл) от инъекции к инъекции увеличивался, при постоянной дозе сухого вещества на 1 кг массы тела. В месячном возрасте произвели забор крови на гематологические иммуно-биохимические исследования (табл. 3). Во время проведения опыта дополнительно учитывалась заболеваемость, сохранность, прирост массы тела животных.
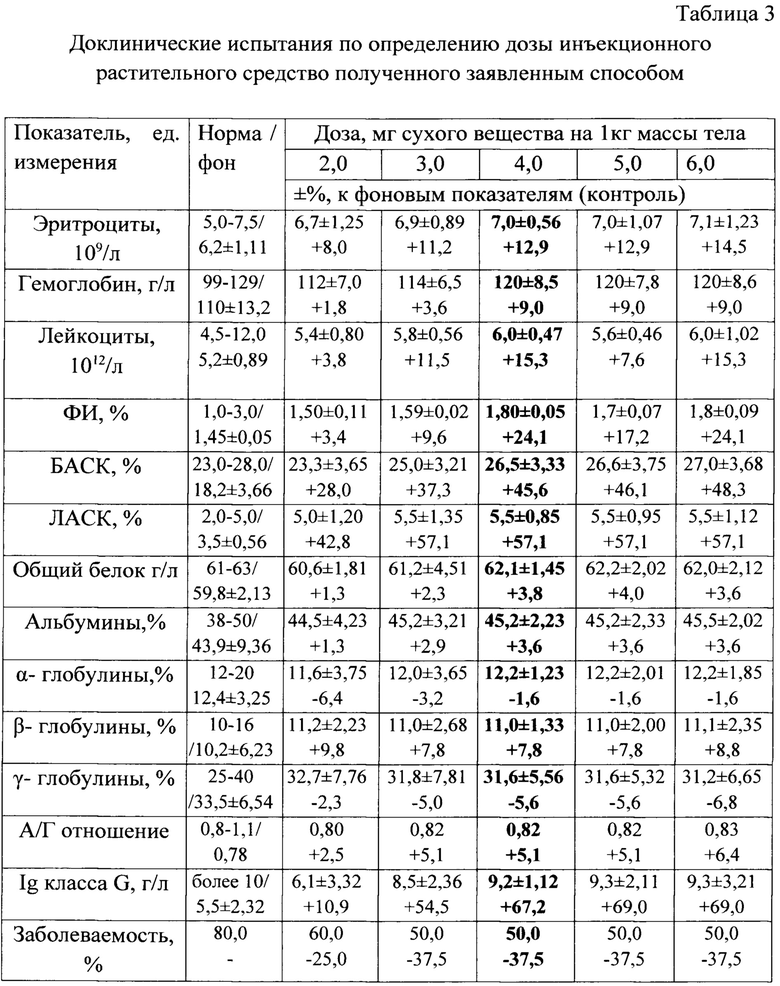
При анализе результатов исследований, представленных в табл. 3, с увеличением инъекционной дозы заявленного средства, прослеживается закономерная положительная динамика улучшения гемопоэза, в пределах референтных границ, таких показателей как, общее количество эритроцитов увеличилось на 8,0-14,5%, гемоглобина на 1,9-9,0%, лейкоцитов, соответственно на 3,8-15,3% в сравнении с интактными животными контроля.
При рассмотрении иммунологических показателей крови телят (фагоцитарный индекс (ФИ), лизоцимная и бактерицидная активность сыворотки крови (ЛАСК, БАСК), иммуноглобулин G (IgG)), получавших заявленное средство, прослеживается та же тенденция, лучшие результаты отмечены при дозе 4,0 мг сухого вещества.
Увеличение общего количества белка, сывороточных альбуминов, основной функцией которых является поддержание онкотического давления крови, транспорт различных химических веществ и участие в метаболических процессах, еще раз указывает на благотворное влияние испытуемого средства. А снижение, α- и γ-глобулиновых фракций сыворотки крови, подопытных телят, в пределах физиологической нормы, является положительным моментом, так как эти белки являются белками острой фазы и обладают высокой подвижностью, ингибирующими свойствами защищая организм от инфекций, токсических и аутоиммунных реакций. Их снижение в референтных пределах, в данном случае свидетельствует об отсутствии циркуляции инфекционного начала в популяции или перераспределении функций в иммунной системе биологических структур и процессов организма (см. увеличение иммунологических показателей крови), обеспечивающая его защиту от инфекций, токсинов и других патогенов.
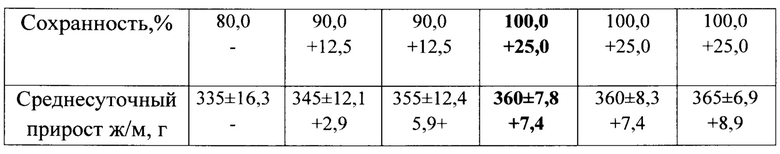
Необходимо отметить, что подкожное введение заявленного растительного средства, в дозе 4,0 мг сухого вещества, на 1 кг массы животного способствует снижению заболеваемости на 37,5%, 100,0% сохранности телят, увеличению среднесуточных привесов на 7,4%, то есть доза 4,0 мг сухого вещества, является оптимальной и способствует улучшению метаболических процессов в организме животных и может быть использовано для улучшения и коррекции обменных процессов и патологических состояний, с целью снижения заболеваемости и повышения, сохранности и продуктивности телят.
Результаты научно-производственного опыта по изучению биологической активности заявленного растительного средства, в ранний постнатальный период выращивания телят, представлены в таблице 4. Телятам контрольной группы (n=9) применяли традиционную специфическую схему профилактики желудочно-кишечных болезней, в то время как телятам опытной группы (n=12), дополнительно в первый и 10 дни жизни инъецировали заявленное средство. Забор крови для исследования проводили в первый день жизни до инъекций и повторно в 20 дневном возрасте. За телятами вели клинические наблюдения в течение 90 дней, учитывали заболеваемость, падеж, продуктивность.
При первичном исследовании отмечали снижение содержания общего количества белка в сыворотке крови телят ниже допустимой нормы на 18,6%, альфа-глобулиновой фракции на 2,3%. Иммуноглобулины класса G (IgG) находились ниже физиологических границ у 40,0% подопытных, у 60% телят отсутствовали вовсе.
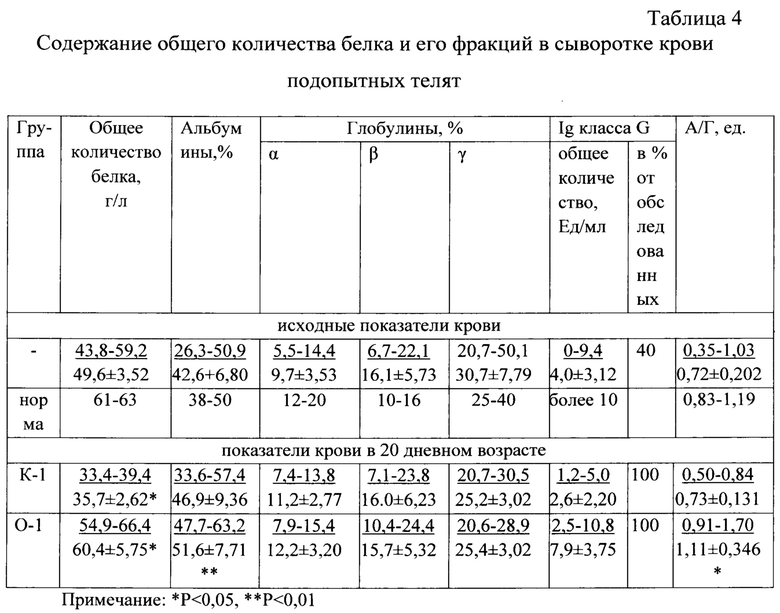
При повторном исследовании крови, через (20 дней), у телят подопытных групп, отмечали достоверное снижение общего количества белка в К-1 группе на 28,0% (Р<0,05), по сравнению с исходными показателями. Достоверное увеличение общего количества белка, альбуминовой фракции (Р≤0,05) регистрировали у телят опытной группы в сравнении с контролем. Главная роль сывороточных альбуминов -сохранение коллоидно-осмотического давления плазмы на постоянном уровне, распределение воды между кровеносными сосудами и интерстициальным пространством. Альбумины выполняют важную функцию транспорта многих биологически активных веществ. Иммуноглобулин класса G (IgG) один из лабораторных показателей, отражающий функционирование гуморального звена иммунной системы, у подопытных телят в 20 дневном возрасте обнаружен в 100% обследованных, но у телят опытной группы данный показатель был выше в 3 раза по сравнению с контрольными. Альбумин глобулиновое соотношение достоверно увеличилось (Р<0,05) в опытной группе, по сравнению с контролем. Его изменение, в сторону уменьшения может свидетельствовать о диспротеинемии, воспалительных процессах, аутоиммунной патологии, поражении печени, почек, нарушениях в работе других внутренних органов.
Гематологический профиль телят, участвующих в опыте, представлен в таблице 5. Общее количество эритроцитов и лейкоцитов находилось в пределах физиологической нормы, при снижении общего количества гемоглобина на 21,8%, цветного показателя на 2,8%. Превышение метгемоглобина в 4 раза выше референтных границ, БАСК на 27,8%, ЛАСК на 90,0%.
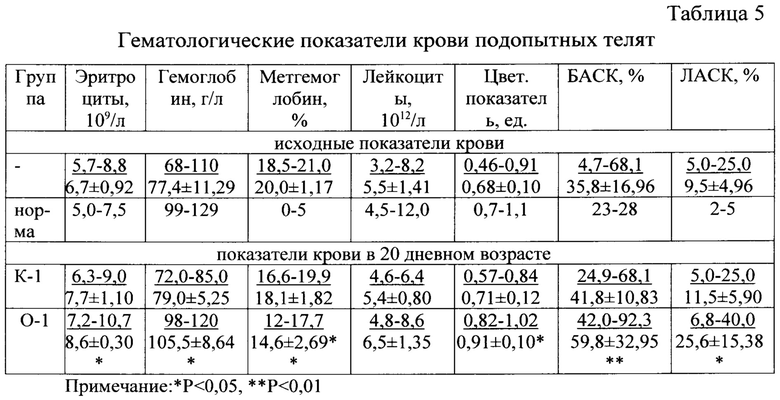
При исследовании крови телят подопытных групп, в 20 дневном возрасте, установили достоверное увеличение общего количества эритроцитов у телят опытной группы на 11,6%, общего количества гемоглобина по отношению к исходным данным и к крови контрольных животных на 36,3% и 33,5% (Р<0,05). Одной из главных задач эритроцитов является доставка кислорода из легких к тканям тела, а углекислого газа - в обратном направлении, из тканей в легкие. При увеличении общего количества эритроцитов в крови телят, газообмен в организме улучшается, а также эритроциты участвуют в иммунологических реакциях организма, за счет наличия в мембранах эритроцитов комплекса полисахаридо-аминокислотных соединений. Достоверное снижением метгемоглобина регистрировали в O-l группе (Р<0,01), что указывает на снижение токсичности организма телят данным соединением. Лейкоциты находились в границах референтных значений. Цветной показатель в опытной группе телят по сравнению с контрольной группой возрос на 28,1% (Р<0,05), соответственно БАСК усилилась на 46,1% (Р<0,01), ЛАСК в опытной группе достоверно превышала в 2,2 раза, данный показатель контрольной группы.
Сохранность телят в опытной группе, которым во время специфической профилактике желудочно-кишечных болезней, дополнительно в первый и 10 дни жизни инъецировали заявленное средство, составила 91,7%, в контрольной соответственно 77,7%, в результате чего сохранность телят в опытной группе улучшилась на 18,0%, по сравнению с аналогами в контроле.
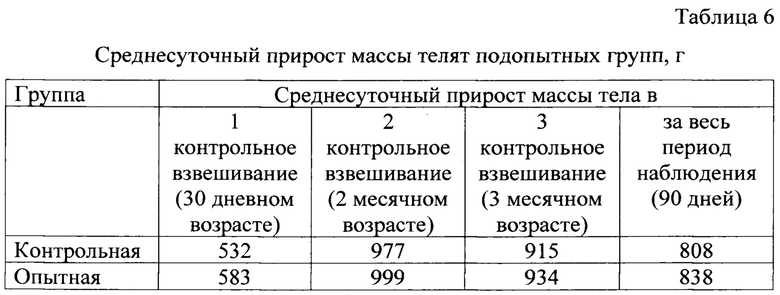
Данные представленные в таблице 6 свидетельствуют о том, что абсолютный прирост живой массы телят в опытной группе в 1 контрольное взвешивание, в месячном возрасте, увеличился на 9,5%, в сравнении с контролем. За 3 месячный период наблюдений, среднесуточный прирост массы тела у телят опытной группы в среднем составил 838 г, что на 3,7% выше, чем у аналогов контрольной группы.
Результаты эксперимента по изучению влияния заявленного средства, на иммунологические показатели крови телят приведены в таблице 7. В неблагополучном хозяйстве по респираторно вирусным инфекциям крупного рогатого скота (КРС) одновременно с внутиримышечным введением «Вакцины инактивированной для профилактики инфекционного ринотрахеита (ИРТ), парагриппа-3 (ПГ-3), вирусной диареи (ВД) и пастереллеза КРС («БелВироПаст»), внутримышечно, в область крупа, инъецировали заявленное средство, в дозе 4,0 мг сухого вещества на 1 кг массы тела, с учетом живой массы.
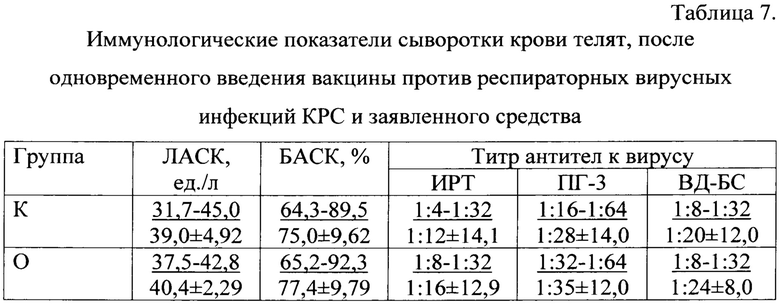
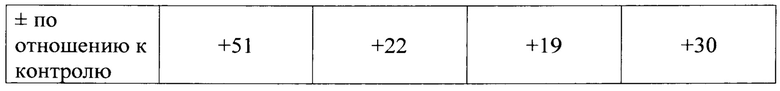
Через 30 дней после проведения двукратной вакцинации телят против респираторных инфекций КРС вакциной «БелВироПаст» и одновременном ведении в ходе вакцинации заявленного средства, отмечали повышение бактерицидной и лизоцимной активности сыворотки крови (БАСК и ЛАСК) в опытной группе на 3,2% и 3,5%. А также увеличение титра антител к вирусу ИРТ КРС на 33,3%, ПГ-3 на 25,0%, к ВД-БС на 20,0% в сравнении с телятами контрольной группы.
В период проведения опытов не выявлено нежелательных явлений в клинико-физиологическом состоянии телят и побочных реакций на одновременное введение вакцины против респираторных вирусных инфекций КРС в сочетании с заявленным средством.
Кратность и интервал введения заявленного средства определяется не только режимом дозирования, а зависит от большого количества факторов, таких как, моно- или комбинированного назначения (см. пример 2 и 3), клинической ситуации, тяжести течения патологического процесса и вызываемых им расстройств и так далее… Например, кратность и интервал введения заявленного средства, во время вакцинации телят, определяются в соответствии с официальным регламентом к использованию «Вакцины инактивированной для профилактики инфекционного ИРТ, ПГ-3, ВД и пастереллеза КРС («БелВироПаст») (см. пример 3).
Пример 1. Технология приготовления заявленного средства. Нужное количество отобранных лекарственных растений: листья алоэ, подорожника большого, крапивы двудомной, соцветия клевера розового, змеиголовника тимьяноцветкового, эхинацеи пурпурной взятых в соотношении 5:1:1:1:1:1, соответственно измельчали до размера частиц не более 0,8 мм, при этом листья алоэ предварительно выдерживали в холодильнике при температуре +2-+4°С в течение 10 дней. Измельченное растительное сырье закладывали в ультразвуковой экстрактор Elmasonic P120 Н, добавляли дистиллированную воду из расчета сырье: вода 1:10 и проводили 10 минутное ультразвуковое озвучивание смеси с частотой ультразвуковых колебаний 37 кГц и при мощности ультразвука 264 Вт с последующей 30 минутной выдержкой сырья в экстракторе для завершения мацерации (набухания), после чего в течение 1,0 часа осуществляли экстракцию набухшего сырья путем ультразвукового озвучивания при том же режиме (37 кГц. 264 Вт) ультразвука до достижения температуры экстрагируемой массы 60°С. Предварительное 10 минутное озвучивание позволило значительно сократить длительность мацерации, по сравнению с пассивным замачиванием сырья для набухания (8-10 часов), а ультразвуковой режим (37 кГц, 264 Вт) при мацерации и экстрагировании предопределил, как время экстрагирования 1 час (до полного истощения сырья), так и температуру, доводя ее к завершению процесса экстракции до 60,0°С, при которой сохраняется большинство термолобильных биологически активных веществ. Полученный экстракт фильтровали при использовании полиэфирных тканей с пористостью не более 25 мкм, в соответствии с технологическим стандартом для инъекционных растворов, фасовали и автоклавировали. В ходе стерилизации, полученного средства, на завершающей стадии изготовления, автоклавирование не оказывает влияния на целостность белковых структур, полученных в ходе экстракции (аминокислот, аминокислотных остатков, нуклеиновых кислот и др.), которые при всасывании, током крови разносятся по всему организму и являются строительным материалом для синтеза новых белков. При увеличении температуры полученного экстракта во время стерилизации, возникают перекрестные связи между отдельными аминокислотами, в результате чего образуются полиаминокислотные комплексы, пептидные гормоны и нейропептиды, которые обладают высокой физиологической активностью, регулируют большинство процессов в организме животных, в том числе принимают участие в процессах регенерации клеток. Пептиды иммунологического действия защищают организм от попавших в него токсинов [22, 23].
Пример 2. Использование заявленного растительного средства, в общепринятой схеме специфической профилактики желудочно-кишечных заболеваний телят с использованием поливалентной гипериммунной сыворотки. Заявленный препарат с профилактической целью вводили телятам в 1 и 10 дни жизни, подкожно, в область средней трети шеи, в дозе из расчета 4 мг сухого вещества на 1 кг массы тела. Новорожденным телятам с массой тела 36-39 кг, заявленное средство, полученное из растительного сырья, инъецировали подкожно в дозе 5,2-5,7 мл, в 10 дневном возрасте с массой тела 41-45 кг, соответственно по 6,0-6,5 мл, поливалентную гипериммунную сыворотку в обоих случаях вводилась в дозе 0,5 мл на 1 кг массы тела, внутримышечно. Контрольным животным поливалентную гипериммунную сыворотку инъецировали в той же дозе, кратности и интервале, внутримышечно. Заболеваемость телят в контрольной группе составила 66,6% в опытной, соответственно 41,6%, использование заявленного средства позволяет улучшить эффективность специфической профилактики против желудочно-кишечных инфекций и сократить заболеваемость телят на 37,5%.
Необходимую дозу в мл, для введения заявленного средства телятам, находим путем умножения живой массы животного на оптимальнуюдозу (4,0 мг сухого вещества 1 кг массы тела), пример Хмг=(37 кг × 4,0 мг)=148 мг сухого вещества. Составляем пропорцию, пример Хмл=(148×100/2740 мг)=5,4 мл, где 2740 мг это количество сухого вещемства содержащееся в 100 мл заявленного средства (см. табл. 1).
Пример 3. Использование заявленного средства при иммунизации телят, в неблагополучном хозяйстве по респираторным вирусным болезням (ИРТ, ПГ-3, ВД КРС). Клинически здоровым животным, двукратно инъецировали вакцину инактивированную для профилактики ИРТ, ВД, ПГ-3 и пастереллеза КРС («БелВироПаст»), 1 раз в 14 дневном возрасте, 2 раз через 15 суток, в дозе 1 см3, внутримышечно, одновременно в день вакцинации внутримышечно в область крупа, вводили заявленное средство полученное из растительного сырья в дозе 4 мг сухого вещества на 1 кг массы тела животного. В 14 дневном возрасте телят с массой тела 45 кг заявленное средство вводится дозе 6,5 мл, 2-й раз через 15 дней при массе тела 52 кг, соответственно 7,6 мл. Титр антител в сыворотке крови телят, опытной группы, к вирусу ИРТ, ПГ-3, ВД-БС КРС в среднем увеличился на 26,1%, которым одновременно с вакциной вводили заявленное средство. При проведении клинических испытаний, отмечена аналогичная положительная динамика иммунологических показателей и при подкожном введении заявленного средства в день вакцинации против респираторных вирусных болезней.
Таким образом заявленное инъекционное средство из растительного сырья обладает высокой фармакологической эффективностью с разнообразным механизмом действия на иммунологические, гематологические, биохимические показатели крови и может быть использовано для снижения заболеваемости и повышения продуктивности телят.
Литература
1. Козицына А.И. Применение «Элитокса» для нормализации обменных процессов коров-матерей и повышение резистентности телят. Диссертация канд. веет. наук по специальности 06.02.05 Вет. санитария, экология, зоогигиена и ветеринарная экспертиза. - С-Петербург - 2018. - 179 с.
2. Шахов А. Г. Достижения и основные направления исследований по изучению болезней молодняка сельскохозяйственных животных. // Практик. - 2010.- №2. - С. 26-33.
3. Петрянкин Ф.П., Петрова О.Ю. Болезни молодняка животных. - СПб.: Лань. 2-е изд. перераб. и доп.- 2014. - 352 с.
4. Карасев, М. М. Лекарственное растительное сырье - перспективы использования в современной клинической практике. Современные наукоемкие технологии. - 2014. - №6. - С. 48-50.
5. Aminah, N. S. Chemical constituents and their biological activities from Taunggyi (Shan state) medicinal plants. // Heliyon. - 2021. - Vol. 7. - P. 68-73.
6. Siddique, H. Medicinal plants used to treat infectious diseases in the central part and a northern district of Bangladesh - An ethnopharmacological perception. Journal of Herbal Medicine. - 2021. - Vol. 29. - P 420-428.)
7. Симонова H.B., Ли O.H., Доровских B.A., Симонова Н.П., Лашин А.П. Способ повышения физической выносливости организма в условиях ультрафиолетового облучения. Патент РФ 2533446 С2. Заявка: 2013105881/15,2013.02.12. Опубликовано: 2014.11.20.
8. Крылов Ю.Ф., Бобырев В.М. Фармакология. 1.1.1. Пути введения лекарственных веществ. - Москва, 1999. - 350 с.
9. Соловьева В.П, Сотникова Е.П., Абрамова А.Б., Соколова Б.Н., Тимошенко Я.Г. Способ получения экстракта алоэ. Патент РФ №2125882 С1. Заявка: 96115632/14, 1996.07.26. Опубликовано: 1999.02.10.
10. Рубанка Е.В. Влияние температуры экстракции на физико-химические показатели ягодных экстрактов. Переработка и управление качеством сельскохозяйственной продукции сборник статей III международной научно-практической конференции Минск, 23-24 марта 2017. - БГАТУ. - 2017. С. 398-399.
11. Конакова И.А., Медетханов Ф.А., Афанасьва Л.В. Химический состав лекарственных растений и их применение в ветеринарии. //Ученые записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. - 2022. - №2 том 250. - С. 98-102.
12. Шулепова И.И. Фармакогнозия: учебное пособие для обучающихся по специальности 36.05.01 Ветеринария ФГБОУ ВО Приморская ГСХА / ФГБОУ ВО Приморская ГСХА. - 2-е изд., перераб. и доп.- Уссурийск: ФГБОУ ВО ПГСХА, 2016. - 80 с.
13. Моисеев О.Н. Средство для предупреждения развития и лечения воспалительных процессов у животных. Птент РФ №2395290 С1. Заявка: №2009114397/15, 15.04.2009. Опубликовано: 27.07.2010. Бюл. №21.
14. Общая фармакопейная статья 1.4.2.0006.15, приказ №749 31.10.2018. Невидимые механические включения в лекарственных формах для парентерального применения. Государственная фармакопея РФ. XIV издание. Том II.
15. Самылина И.А., Северцева В.А. Лекарственные растения государственной фармакопеи. Фармакогнозия. - М., «АМНИ», - 1999. - 93 с.
16. Червяков Д.К. Лекарственные средства в ветеринарии. Справочник. Изд. 2-е, переработанное и дополненное. - М., Колос. - 1977. С. 116.
17. Куликов В.В. Лекарственные растения Алтайского края. Алтайское книжное издательство Барнаул. Изд. 2. - 1975. - С. 76-79, 119-121.
18. Гринкевич Н.И., Баландина И.А., Ермакова В.А. и др. Лекарственные растения: Справочное пособие. - М.: Высшая школа, 1991. - 398 с.
19. Бирман Б.Я., Голубев Д.С.Эхинацея- прикуликов В.Вродный иммномодулятор. Международный вестник ветеринарии, №1 2006. - С. 23-26.
20. Путырский И.Н., Прохоров В.Н. Универсальная энциклопедия лекарственных растений. - М.: Махаон, 2000. - С.115-116.
21. Левринц К.Й., Синицын А.А. Разработка ультразвукового миниэкстрактора для создания полезных питьевых настоев в повседневном рационе жизни человека. Текст: непосредственный // Молодой ученый. - 2017. - №17 (151). - С. 6-8.
22. URL: https://www.activestudy.info/soderzhanie-belkovyx-veshhestv-posle-vliyaniya-texnologicheskoj-obrabotki-na-pishhevye-produkty/?ysclid=ljz4p8he7f34652883.
23. URL: hudoogorod.ru/produkty/izmenenie-belkovyx-veshhestv-v-pishhevyx-produktax-pri-teplovoj-obrabotke.html?ysclid=ljz5ixrr8322589673
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫРАЩИВАНИЯ ТЕЛЯТ В ХОЗЯЙСТВАХ, НЕБЛАГОПОЛУЧНЫХ ПО ОРВИ | 2015 |
|
RU2625022C2 |
| Способ выращивания поросят в хозяйствах, неблагополучных по гемофилезному полисерозиту | 2021 |
|
RU2780858C1 |
| СПОСОБ ПРОФИЛАКТИКИ РЕСПИРАТОРНЫХ БОЛЕЗНЕЙ ТЕЛЯТ | 2022 |
|
RU2806816C1 |
| СПОСОБ ПРОФИЛАКТИКИ МАССОВЫХ ЖЕЛУДОЧНО-КИШЕЧНЫХ И РЕСПИРАТОРНЫХ БОЛЕЗНЕЙ МОЛОЧНЫХ ПОРОСЯТ | 2013 |
|
RU2524664C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ СТИМУЛЯТОР И СПОСОБ КОРРЕКЦИИ ВТОРИЧНЫХ ИММУНОДЕФИЦИТОВ У ТЕЛЯТ С ЕГО ПРИМЕНЕНИЕМ | 2006 |
|
RU2311189C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО ДЛЯ МОЛОДНЯКА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВИРУСНЫХ ЖЕЛУДОЧНО-КИШЕЧНЫХ БОЛЕЗНЕЙ ТЕЛЯТ С ЕГО ПРИМЕНЕНИЕМ | 2006 |
|
RU2315610C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО ДЛЯ МОЛОДНЯКА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЖЕЛУДОЧНО-КИШЕЧНЫХ БОЛЕЗНЕЙ ТЕЛЯТ С ЕГО ПРИМЕНЕНИЕМ | 2006 |
|
RU2303993C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЛЕЙКОЗА КРУПНОГО РОГАТОГО СКОТА | 2009 |
|
RU2421184C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ СТИМУЛЯТОР И СПОСОБ КОРРЕКЦИИ ВТОРИЧНЫХ ИММУНОДЕФИЦИТОВ У ТЕЛЯТ С ЕГО ПРИМЕНЕНИЕМ | 2008 |
|
RU2371191C1 |
| СПОСОБ ИММУНОПРОФИЛАКТИКИ РЕСПИРАТОРНЫХ БОЛЕЗНЕЙ ТЕЛЯТ | 2011 |
|
RU2464999C1 |
Изобретение относиться к ветеринарной медицине и представляет собой инъекционное средство для снижения заболеваемости и повышения продуктивности телят. Средство представляет собой смесь лекарственных трав алоэ, подорожника, крапивы, змеиголовника, клевера, эхинацеи, которую подвергают ультразвуковому озвучиванию, как на стадии мацерации, так при экстрагировании в ультразвуковом режиме, обеспечивающим проведение процесса при температуре не выше 60°С в течение 1-1,2 часа, при этом фильтрацию экстракта осуществляют при использовании фильтров с пористостью не более 25 мкм. Инъекционное средство обладает высокой фармакологической эффективностью с разнообразным механизмом действия на иммунологические, гематологические, биохимические показатели крови. 2 з.п. ф-лы, 7 табл., 3 пр.
1. Инъекционное средство для снижения заболеваемости и повышения продуктивности телят, характеризующееся тем, что представляет собой смесь предварительно измельченных до размера частиц 0,3-0,8 мм, следующих лекарственных растений: листья алоэ древовидного, подорожника большого, крапивы двудомной, травы змееголовника тимьяноцветкового, соцветий клевера розового, эхинацеи пурпурной, взятые в соотношении 5:1:1:1:1:1 соответственно, которую закладывают в ультразвуковой экстрактор, добавляют дистиллированную воду из расчета сырье : вода 1:10 и подвергают 10 минутному ультразвуковому озвучиванию с последующей 30 минутной выдержкой сырья в экстракторе для завершения мацерации, после чего экстракцию набухшего сырья осуществляют путем ультразвукового озвучивания в течении 1-1,2 часа до достижения температуры экстрагируемой массы 60°С при этом режим ультразвукового озвучивания, как при мацерации так при экстрагировании находится в пределах 37 кГц при мощности ультразвука 264 Вт, после чего производят фильтрацию экстракта при использовании полиэфирных тканей с пористостью не более 25 мкм, фасуют и автоклавируют.
2. Средство по п. 1 характеризуется тем, что средство инъецируется в дозе из расчета 4,0 мг сухого вещества на 1 кг массы тала животного.
3. Средство по п. 1 характеризуется тем, что лисья алоэ перед смешиванием с остальными компонентами смеси консервируют в темноте при температуре +2-4°С в течение 7-10 суток.
| СРЕДСТВО ДЛЯ ПРЕДУПРЕЖДЕНИЯ РАЗВИТИЯ И ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ У ЖИВОТНЫХ | 2009 |
|
RU2395290C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКСТРАКТА АЛОЭ | 1996 |
|
RU2125882C1 |
| СПОСОБ ПОВЫШЕНИЯ ПРОДУКТИВНОСТИ ТЕЛЯТ | 2006 |
|
RU2301535C1 |
| Фитопробиотическая кормовая добавка для телят | 2023 |
|
RU2816330C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЖЕЛУДОЧНО-КИШЕЧНЫХ БОЛЕЗНЕЙ НОВОРОЖДЕННЫХ ТЕЛЯТ | 2014 |
|
RU2553364C1 |
| ПРЕПАРАТ ДЛЯ УЛУЧШЕНИЯ ЗДОРОВЬЯ И ПРОДУКТИВНОСТИ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И ПТИЦ | 2016 |
|
RU2652824C1 |
Авторы
Даты
2024-10-02—Публикация
2023-10-17—Подача