Область техники, к которой относится изобретение
Настоящее изобретение относится к химии пептидов или белков, или пептидомиметиков и более предпочтительно к их получению химическим путем исходя из дифункциональных соединений и предпочтительно из α-, β- или γ-аминокислот и/или α-, β- или γ-гидроксикислот, и/или α-, β- или γ-меркаптокислот.
Более точно настоящее изобретение относится к способу получения пептидов или белков, или пептидомиметиков в растворе. В указанном способе не используют традиционные защитные группы, такие как трет-бутоксикарбонильная группа (Boc) или фторфенилметоксикарбонильная группа (Fmoc), для защиты аминогрупп α-, β- или γ-аминокислот. Аналогичным образом, в этом способе не требуется использовать защитные группы для защиты гидроксигрупп α-, β- или γ-гидроксилкислот или меркаптогрупп α-, β- или γ-меркаптокислот.
Способ основан на применении α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, активированных в форме соответственно 2,2-бис(трифторметил)-1,3-оксазолидин-5-она или 2,2-бис(трифторметил)-1,3-оксазинан-6-она, или 2,2-бис(трифторметил)-1,3-оксазепан-7-она, или 2,2-бис(трифторметил)-1,3-диоксолан-4-она, или 2,2-бис(трифторметил)-1,3-диоксан-4-она, или 2,2-бис(трифторметил)-1,3-диоксепан-4-она, или 2,2-бис(трифторметил)-1,3-оксатиолан-5-она, или 2,2-бис(трифторметил)-1,3-оксатиан-6-она, или 2,2-бис(трифторметил)-1,3-оксатиепан-7-она или их производных, и группы линкеров, а именно производных соединений полиолефинов или полиолефиновых или полиалкеновых олигомеров. Линкер связан с соединением, имеющим по меньшей мере две электрофильные и/или нуклеофильные функциональные группы, и предпочтительно первую α-, β- или γ-аминокислоту или α-, β- или γ-гидроксикислоту, или α-, β- или γ-меркаптокислоту, которые затем используются на последующих стадиях удлинения/итерации для получения пептидов или белков, или пептидомиметиков.
Указанный способ позволяет получать пептиды или белки, или пептидомиметики более эффективно (то есть с меньшим числом стадий), быстрее, с большей чистотой или с более легкой процедурой очистки, чем принятые в настоящее время способы на твердой подложке или в растворе. Способ можно легко автоматизировать.
Предшествующий уровень техники
Заметный рост числа научных разработок в области пептидов или белков, или пептидомиметиков терапевтического назначения в течение последнего десятилетия привел к появлению на рынке большого числа новых соединений, одобренных для реализации на рынке (см. публикации: J. Med. Chem., 2018, 22, 1382-1414, Bioorg. Med. Chem., 2018, 26, 2700-2707); таким образом, терапия на основе пептидов или белков, или пептидомиметиков стала одним из наиболее динамичных сегментов, связанных с производством фармацевтических средств. Раковые заболевания, болезни, связанные с метаболизмом, и болезни центральной нервной системы представляют собой основные цели терапии, ускоряющие запросы на новые пептиды или белки, или пептидомиметики терапевтического назначения.
Однако некоторые проблемы препятствуют широкому внедрению пептидов или белков, или пептидомиметиков в терапию. Можно назвать, например, их короткое время метаболического полураспада и их гидрофильную природу. Другой ключевой фактор, являющийся с давних пор более важным и замедляющим расширение терапевтического применения пептидов или белков, или пептидомиметиков, представляет собой способ их получения.
Самый первый синтез пептидов в жидкой среде был осуществлен больше века тому назад Э. Фишером и Э. Фурно (Ber. Dtsch. Chem. Ges. 1901, 34, 2868-2879). С того времени многие химики внесли свои улучшения: например, Бодански и Дю Виньо (J. Am. Chem. Soc., 1959, 51, 5688-5691), Байерман и соавт. (Rec. Trav. Chim., Pays Bas 1973, 92, 481-492), Р. К. Шарма и Р. Джайн (Synlett 2007, 603-606), Нодаль и соавт. (Nature Chemistry 2017, 9, 571-577), Лиу и соавт. (Org. Lett., 2018, 20, 612-615) и Мурамацу и соавт. (ACS Catal., 2018, 8, 2181-2187).
В случае более часто используемых путей синтеза пептидов или белков, или пептидомиметиков осуществляют временную защиту аминогрупп (Nα) аминокислот. В настоящее время основные используемые защитные группы представляют собой трет-бутоксикарбонильная группа (этот подход обычно называют стратегией "Boc") и фторфенилметоксикарбонильная группа (этот подход обычно называют стратегией "Fmoc"). Эти два пути синтеза хорошо известны специалистам в данной области техники (см. раздел 7-5 справочника "D. Voet et J.G. Voet "Biochimie", 2eme edition, Bruxelles 2005). На практике аминокислоты переводят в защищенное состояние по аминогруппе (Nα) группами Fmoc или Boc и используют непосредственно в реакциях активации/присоединения.
Аминокислоты могут быть использованы в жидкой среде или на твердом носителе; в последнем случае аминокислота, защищенная по аминогруппе (Nα), зафиксирована на смоле, нерастворимой в органических растворителях, что представляет собой синтез Меррифилда (J. Am. Chem. Soc., 1963, 85, 2149-2154). Указанный способ хорошо отработан, но имеет, однако, несколько недостатков, таких как стоимость реагентов, используемых с избытком, и недостаточная однородность синтезированных пептидов. В данном случае говорят, что система является вырожденной, что вызывает удорожание очистки с использованием препаративной высокоэффективной жидкостной хроматографии.
Во время синтеза пептидов в жидкой среде (SPPL) все реакции происходят в гомогенном растворе. Этот способ был описан Бодански и Дю Виньо (J. Am. Chem. Soc., 1959, 51, 5688-5691). Карбоксигруппу (C-терминальную группу) исходной аминокислоты защищают в форме сложного метилового эфира, а последующие аминокислоты последовательно присоединяют после защиты их аминогрупп (Nα) бензилоксикарбонильной группой (сокращенно Cbz) и активации их карбоксигрупп (C-терминальных групп) сложным нитрофениловым эфиром. Все синтезированные промежуточные соединения очищают осаждением или промывкой водой (экстракцией). Этот способ синтеза пептидов является долгим и утомительным и позволяет получать пептиды с низким выходом. В качестве примера можно назвать синтез ACTH с общим выходом около 7%, описанный Швицером и Зибером (Helv. Chim. Acta 1966, 49, 134-158).
О модификации этого способа было сообщено Байерманом и соавт. (Rec. Trav. Chim. Pays Bas 1973, 92, 481-492). Она состоит в том, чтобы защитить карбоксигруппу (C-терминальную группу) аминокислоты или пептида в форме сложного бензилового эфира и осуществить реакцию присоединения (или конденсации) в присутствии избытка ангидрида Nα-защищенной аминокислоты с целью улучшения выхода. В конечном счете, хотя выход реакций присоединения был увеличен, было отмечено ухудшение растворимости пептида в органической среде, когда образованный пептид содержит порядка пяти остатков аминокислот.
Были разработаны другие стратегии, обеспечивающие солюбилизацию аминокислот для того, чтобы облегчать синтез пептидов. Можно упомянуть работы Нариты (Bull. Chem. Soc. Jap., 1978, 51, 1477-1480), работы Байера и Муттера (Nature 1972, 237, 512-513) в связи с использованием полиэтиленгликоля в качестве адъюванта солюбилизации и патенты EP 0017536 (Sanofi) и EP 2612845 A1 и US 2014/0296483 (Ajinomoto Co., Inc.) в связи с использованием солюбилизирующих линкеров.
Известны также стратегии синтеза пептидов, в которых используют дифункциональные группы, то есть группы, которые способны одновременно активировать карбоксигруппу (C-терминальную группу) и защищать аминогруппу (Nα) аминокислоты, образуя промежуточные циклические структуры, являющиеся сильно реакционноспособными. Это относится к случаю N-карбоксиангидридов (сокращенно NCAs) (см.: Ber. Dtsch. Chem. Ges., 1906, 39, 857-861; Ber. Dtsch. Chem. Ges., 1907, 40, 3235-3249; Ber. Dtsch. Chem. Ges., 1908, 41, 1721-172; J. Am. Chem. Soc., 1957, 79, 2153-2159; J. Am. Chem. Soc., 1947, 69, 1551-1552). Промежуточные реагенты были синтезированы исходя из аминокислот и производных соединений дихлордиметилсиланов (см. "S.H. van Leeuwen et al., Tetrahedron Letters 2002, 43, 9203-9207" и патент WO 00/37484 A1). Для синтеза пептидов были разработаны производные соединения аминокислот, активированные эфиратом трифторида бора (см. "S.H. van Leeuwen et al., Tetrahedron Letters 2005, 46, 653-656"). Также была описана активация аминокислот в присутствии гексафторацетона (см. "Chem. Ztg., 1990, 114, 249-251" и "J. Spengler et al., Chem. Rev., 2006, 106, 4728-4746").
Все указанные способы синтеза пептидов или белков, или пептидомиметиков в растворе или на твердом носителе обладают по меньшей мере одним или более недостатками из перечисленных далее: использование защитных групп, использование избытка реагентов, возможность рацемизации, низкая растворимость пептидов в ходе синтеза в органических растворителях, ограничение размера пептида, дорогостоящие и загрязняющие способы очистки, сложные экспериментальные методики или возможность полимеризации. В общем случае, ознакомление с многочисленными доступными литературными источниками в области синтеза пептидов показывает, что существуют затруднения, препятствующие получению пептидов или белков, или пептидомиметиков высокой чистоты с хорошим выходом, низкой стоимостью и с незначительным воздействием на экологию.
Проблема, которую предлагается решить настоящей заявкой, состоит в разработке концепции новой методики синтеза пептидов или белков, или пептидомиметиков, позволяющей устранить препятствия, связанные с их доступностью или получением и остающиеся на предшествующем уровне техники.
Цель изобретения
Согласно настоящему изобретению проблема решается за счет способа синтеза пептидов или белков, или пептидомиметиков в жидкой среде, в котором сочетаются два существенных аспекта, подробно описанных далее.
Первой целью настоящего изобретения является способ синтеза пептидов или белков, или пептидомиметиков последовательным удлинением второй терминальной части соединения типа Qa - E - Qb, где Qa и Qb могут быть одинаковыми или разными и представляют собой электрофильные и/или нуклеофильные функциональные группы, а E означает спейсер. Указанная вторая терминальная часть предпочтительно может представлять собой первичную или вторичную аминогруппу, гидроксигруппу или меркаптогруппу α-, β-, γ- или δ-аминокислоты или α-, β-, γ- или δ-гидроксикислоты, или α-, β-, γ- или δ-меркаптокислоты, или пептида, или белка, или пептидомиметика, отличающихся тем, что указанные звенья выбраны из группы, которую составляют α-, β-, γ- или δ-аминокислоты или α-, β-, γ- или δ-гидроксикислоты, или α-, β-, γ- или δ-меркаптокислоты (природные или неприродные, или синтетические). К тому же, первая терминальная часть указанного соединения типа Qa - E - Qb (например, α-, β-, γ- или δ-аминокислоты или α-, β-, γ- или δ-гидроксикислоты, или α-, β-, γ- или δ-меркаптокислоты) или указанного пептида или белка, или пептидомиметика связана с линкером, растворимым в органических растворителях, таких как галогенпроизводные растворители (метиленхлорид, хлороформ), этилацетат, тетрагидрофуран, 2-метилтетрагидрофуран, изооктан, циклогексан, гексаны, метилциклогексан, метил-трет-бутиловый эфир или ароматические растворители, такие как бензол или толуол, или любой другой приемлемый растворитель.
Первым существенным аспектом является применение специфической группы линкеров. Согласно настоящему изобретению линкеры представляют собой полиолефины или полиолефиновые или полиалкеновые олигомеры. Способ по настоящему изобретению позволяет получать пептиды или белки, или пептидомиметики (природные или неприродные, или синтетические) высокой чистоты. Этот способ обеспечивает сокращение числа стадий и экономию на атомарном уровне в силу отказа от применения защитных групп (для защиты амино-, гидрокси- или меркаптогрупп основной цепи) и линкеров и в силу этого обеспечивает финансовую экономию. Наконец, способ является более щадящим в отношении окружающей среды.
Вторым существенным аспектом является применение дифункциональных соединений типа Qa - E - Qb, в которых группы Qa и Qb могут быть одинаковыми или разными и выбраны из электрофильных и/или нуклеофильных групп, а E означает спейсер. Qa и Qb предпочтительно выбирают из группы, которую составляют функциональные химические группы, такие как спиртовые, альдегидные группы, первичные аминогруппы, вторичные аминогруппы, азидные, этинильные группы, галогены, тиольные, винильные группы, и/или спейсер E выбирают из группы, которую составляют структурные звенья, такие как ароматические, гетероароматические звенья, насыщенные (разветвленные или неразветвленные) алкильные цепи, ненасыщенные (разветвленные или неразветвленные) алкильные цепи, гликоли (и предпочтительно полиэтиленгликоль).
В предпочтительном случае, когда в качестве дифункционального соединения типа Qa - E - Qb применяют α-, β- или γ-аминокислоту или α-, β- или γ-гидроксикислоту, или α-, β- или γ-меркаптокислоту, эти соединения используют в их активированных формах, таких как 2,2-бис(трифторметил)-1,3-оксазолидин-5-он или 2,2-бис(трифторметил)-1,3-оксазинан-6-он, или 2,2-бис(трифторметил)-1,3-оксазепан-7-он, или 2,2-бис(трифторметил)-1,3-диоксолан-4-оны, или 2,2-бис(трифторметил)-1,3-диоксан-4-он, или 2,2-бис(трифторметил)-1,3-диоксепан-4-он, или 2,2-бис(трифторметил)-1,3-оксатиолан-5-он, или 2,2-бис(трифторметил)-1,3-оксатиан-6-он, или 2,2-бис(трифторметил)-1,3-оксатиепан-7-он или их производные.
На схеме 1 показана структура этих активированных форм. Эти формы получают исходя из соответствующих α-, β- или γ-аминокислот (это выражение в данном случае обозначает α-аминокислоты, β-аминокислоты или γ-аминокислоты) или из α-, β- или γ-гидроксикислот (это выражение в данном случае обозначает α-гидроксикислоты, β-гидроксикислоты или γ-гидроксикислоты), или из α-, β- или γ-меркаптокислот (это выражение в данном случае обозначает α-меркаптокислоты, β-меркаптокислоты или γ-меркаптокислоты).
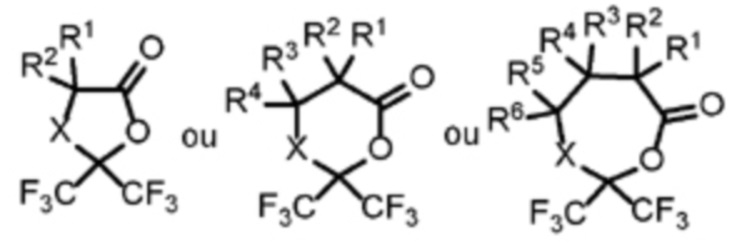
X=NH, N-алкил, N-арил, O, S
R1, R2, R3, R4, R5, R6=алкил или арил
Схема 1. Структуры активированных форм
До настоящего времени не была показана возможность легкого получения в растворе пептидов, состоящих из более чем четырех разных или одинаковых аминокислот, использованием производных соединений аминокислот, активированных в форме 2,2-бис(трифторметил)-1,3-оксазолидин-5-она.
Именно это является целью настоящего изобретения, в котором предлагается использование кислот, активированных в форме 2,2-бис(трифторметил)-1,3-оксазолидин-5-она или 2,2-бис(трифторметил)-1,3-оксазинан-6-она, или 2,2-бис(трифторметил)-1,3-оксазепан-7-она, или 2,2-бис(трифторметил)-1,3-диоксолан-4-онов, или 2,2-бис(трифторметил)-1,3-диоксан-4-она, или 2,2-бис(трифторметил)-1,3-диоксепан-4-она, или 2,2-бис(трифторметил)-1,3-оксатиолан-5-она, или 2,2-бис(трифторметил)-1,3-оксатиан-6-она, или 2,2-бис(трифторметил)-1,3-оксатиепан-7-она или их производных в присутствии линкера, позволяющего получать пептиды или белки, или пептидомиметики высокой чистоты в жидкой среде (или в растворе).
Способ синтеза пептидов или белков, или пептидомиметиков согласно настоящему изобретению представляет собой способ последовательного удлинения второй терминальной части (с первичной или вторичной аминогруппой, гидроксигруппой или меркаптогруппой) цепи пептида или белка, или пептидомиметика, первая терминальная часть которых связана с линкером, растворимым в органическом растворителе. Указанный линкер содержит полиолефиновую цепь или цепь полиолефиновых или полиалкеновых олигомеров, содержащую по меньшей мере 10 мономерных звеньев и предпочтительно от 15 до 350 мономерных звеньев.
В предпочтительном варианте осуществления указанная полиолефиновая цепь представляет собой полиизобутеновую цепь (PIB). Указанный линкер предпочтительно может представлять собой полиолефин. Цепь полиолефина может быть функционализирована по меньшей мере в одной из своих терминальных частей. В одном из вариантов цепь полиолефина или полиолефинового или полиалкенового олигомера может содержать ненасыщенные связи "углерод-углерод" в количестве, не превосходящем 5% и предпочтительно не превосходящем 3%, и/или линкер может иметь среднемассовую молекулярную массу в интервале от 600 до 20 000 и предпочтительно от 700 до 15 000.
В предпочтительном варианте осуществления указанный линкер содержит полиолефиновую цепь (или представляет собой полиолефиновую цепь), оканчивающуюся по меньшей мере одной группировкой, выбранной из группы, которую составляют:
- функциональная группа -Xa, где Xa выбрана из группы, которую составляют -OH, -NH2, -NHRa (Ra=алкил или арил), -SH;
- функциональная группа -Y-C6H4Xb, где:
- Y означает O, S, CH2 или отсутствует;
- Xb выбрана из группы, которую составляют -OH, -NH2, -NHRa, -SH, -CXaRaRb, -C6H3Rc(CRaXa), где Rb выбрана из группы, которую составляют -H, -арил, -гетероарил, -алкил, а Rc выбрана из группы, которую составляют -H, -алкил, -O-алкил, -арил, -O-арил, -гетероарил, -O-гетероарил;
- функциональная группа -CRd=CH-CHXa или функциональная группа -CRdH-CH=CH-CHXa, где Xa имеет определенные ранее значения, а Rd означает метил или этил.
Xa предпочтительно может представлять собой первичную или вторичную аминогруппу, спиртовую группу, меркаптогруппу или фенильную группу.
В предпочтительном варианте осуществления среднемассовая молекулярная масса линкеров, за исключением терминальной функциональной группы (например, -Xa, -Z-C6H4Xb или -CRd=CH-CHXa, определенные ранее), находится в интервале от 600 до 20 000 и предпочтительно от 700 до 15 000. При среднемассовой молекулярной массе более 20 000 эти соединения могут обладать слишком большой вязкостью, что будет создавать риск ограничения их растворимости в органических растворителях, используемых для стадии связывания/удлинения или итерации.
Некоторые производные соединения PIB, применяемые в рамках настоящего изобретения, имеются в продаже в качестве лигандов для гомогенного катализа. Например, можно использовать 2-метил-3-[полиизобутил(12)]пропанол (среднемассовая молекулярная масса составляет 757, включая терминальную функциональную группу), или 4-[полиизобутил(18)]фенол (среднемассовая молекулярная масса составляет 1104, включая терминальную функциональную группу), которые реализует компания "Strem Chemicals" под артикулами 06-1037 и 06-1048 соответственно. Эти два соединения представляют собой производные соединения полиизобутенов, цепь которых оканчивается группой -CH2-C(CH3)(H)-CH2-OH (т.е. изопропанольной) и группой -CH2-C(CH3)2-C6H5-OH (т.е. фенильной) соответственно.
Согласно одному аспекту настоящего изобретения использование линкера, растворимого в органическом растворителе, соответственно описанному ранее (и более предпочтительно использование полиолефинов) позволяет действовать ему также в качестве жидкой подложки или защитной группы для защиты карбоксигруппы (C-терминальной группы) или любой другой химической функциональной группы (одной или более боковых цепей) α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или любого другого соединения, имеющего по меньшей мере две функциональные группы. Оно обеспечивает также солюбилизацию связанных пептидов или белков, или пептидомиметиков и их синтез в органическом растворе (галогенпроизводные и/или негалогенпроизводные растворители).
Согласно другому аспекту настоящего изобретения использование соответственно описанному ранее линкера (более предпочтительно использование полиолефинов), растворимого в органическом растворителе и нерастворимого в некоторых полярных растворителях (таких как вода и/или этанол, и/или ацетонитрил), облегчает очистку связанных α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, или пептидов, или белков, или пептидомиметиков простой экстракцией (промывкой) или простым фильтрованием через диоксид кремния. Таким образом, простая экстракция или простое фильтрование позволяет получать связанные пептиды или белки, или пептидомиметики с высокой химической чистотой.
Согласно еще одному аспекту настоящего изобретения используют линкеры, имеющиеся в торговой сети, или также линкеры, которые могут быть синтезированы простым образом и непосредственно из предшественников, имеющихся в торговой сети, предпочтительно из некоторых производных соединений полиизобутенов (PIB).
Согласно еще одному аспекту настоящего изобретения α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты в их активированных формах, таких как 2,2-бис(трифторметил)-1,3-оксазолидин-5-он или 2,2-бис(трифторметил)-1,3-диоксолан-4-он, или 2,2-бис(трифторметил)-1,3-оксатиолан-5-он, или (2,2-бис(трифторметил)-1,3-оксазинан-6-он, 2,2-бис(трифторметил)-1,3-диоксан-4-он, 2,2-бис(трифторметил)-1,3-оксатиан-6-он, 2,2-бис(трифторметил)-1,3-оксазепан-7-он, 2,2-бис(трифторметил)-1,3-диоксепан-4-он, 2,2-бис(трифторметил)-1,3-оксатиепан-7-он и их производные, приводят во взаимодействие в присутствии линкера в приемлемом растворителе (или в смеси растворителей) при температуре в интервале от -20 до 150°C. В варианте реализации взаимодействие осуществляют в любом текучем инертном растворителе (или в смеси), способном растворять реагенты. Растворители, приемлемые для применения, содержат, без наложения ограничений, галогенпроизводные или негалогенпроизводные углеводороды. Предпочтительные растворители представляют собой тетрагидрофуран, этилацетат, 2-метилтетрагидрофуран, пропиленкарбонат или любой другой растворитель или смесь растворителей, способные растворять два указанных химических вещества.
Согласно еще одному аспекту настоящего изобретения взаимодействие между производными соединениями PIB и активированными α-, β- или γ-аминокислотами или α-, β- или γ-гидроксикислотами, или α-, β- или γ-меркаптокислотами осуществляют в периодическом режиме партиями (предпочтительно в реакторе или в резервуаре), но предпочтительно взаимодействие осуществляют в режиме потока (называемом также непрерывным режимом).
Согласно еще одному аспекту настоящего изобретения α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, имеющие боковые цепи, не совместимые с условиями реакции связывания/удлинения или итерации, могут быть временно защищены приемлемой защитной группой. Защитная группа предпочтительно может быть выбрана из группы, которую составляют:
- трет-бутоксикарбонильная группа (сокращенно Boc);
- фторфенилметоксикарбонильная группа (сокращенно Fmoc),
- бензильная группа (сокращенно Bzl);
- тритильная группа (сокращенно Trt);
- карбоксибензильная группа (сокращенно Cbz);
- 2,2,4,6,7-пентаметилдигидробензофуран-5-сульфонильная группа (сокращенно Pbf);
- 4-метокси-2,3,6-триметилбензолсульфонильная группа (сокращенно Mtr).
Также можно использовать любые другие защитные группы, приемлемые для настоящего способа.
Согласно еще одному аспекту настоящего изобретения указанный линкер взаимодействует с первой активной α-, β- или γ-аминокислотой или α-, β- или γ-гидроксикислотой, или α-, β- или γ-меркаптокислотой (в данном случае сокращенно AAA1), образуя ковалентную связь между α-, β- или γ-аминокислотой или α-, β- или γ-гидроксикислотой, или α-, β- или γ-меркаптокислотой и линкером.
Согласно еще одному аспекту настоящего изобретения указанная цепь пептида или белка, или пептидомиметика образована n звеньями α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот; ее вторая терминальная часть представляет собой другое звено α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты (в данном случае сокращенно AAAn). Во время технологического процесса цепь пептида или белка, или пептидомиметика удлиняется за счет последовательного удлинения или итерации, при этом на каждой из этих стадий прибавляется другое звено активированной α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты (в данном случае сокращенно AAA(n+1)) ко второй терминальной части (свободной первичной или вторичной аминогруппы, спиртовой группы или меркаптогруппы). Эта последовательность реакций представлена далее на схеме реакций 2.
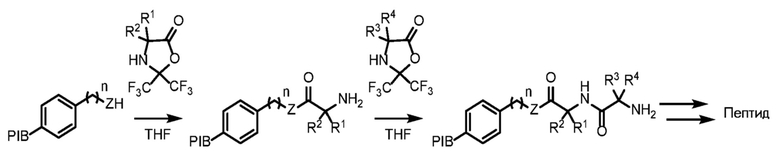
Z=NH, N-алкил, N-арил, O, S
R1, R2, R3, R4=H и/или алкил и/или арил
n=0,1
Схема реакций 2. Общий способ получения пептида
Согласно еще одному аспекту настоящего изобретения в указанной цепи пептида или белка, или пептидомиметика можно использовать природные и/или неприродные, и/или синтетические α-, β- или γ-аминокислоты и/или α-, β- или γ-гидроксикислоты, и/или α-, β- или γ-меркаптокислоты.
Согласно еще одному аспекту настоящего изобретения в указанной цепи пептидомиметика можно использовать одно или более звеньев типа Qa - E - Qb, имеющих по меньшей мере две функциональные группы, которые являются одинаковыми или разными, выбраны из электрофильных и/или нуклеофильных групп и отделены звеном спейсера E. Группы Qa и/или Qb необязательно могут быть терминальными группами. Спейсер E может представлять собой звено, выбранное из группы, которую составляют:
- алифатические цепи (разветвленные или неразветвленные и насыщенные или ненасыщенные);
- арилы или гетероарилы (необязательно замещенные).
Звенья типа Qa - E - Qb предпочтительно содержат терминальную функциональную группу, выбранную из группы, которую составляют первичная аминогруппа, вторичная аминогруппа, гидроксигруппа или меркаптогруппа.
Можно легко видеть, что указанные ранее α-, β- или γ-аминокислоты, α-, β- или γ-гидроксикислоты и α-, β- или γ-меркаптокислоты представляют собой особые случаи дифункциональных соединений типа Qa - E - Qb. Так же обстоит дело и с указанными ранее δ-аминокислотами, δ-гидроксикислотами и δ-меркаптокислотами, которые при этом необязательно используют в реакции в их активированной форме, аналогично другим дифункциональным соединениям, которые не представляют собой α-, β- или γ-аминокислоты, α-, β- или γ-гидроксикислоты или α-, β- или γ-меркаптокислоты.
Дифункциональное соединение Qa - E - Qb может иметь молекулярную структуру, выбранную предпочтительно из эпоксидов, азиридинов и тииранов. Таким образом, согласно настоящему изобретению можно получать пептидомиметики, содержащие эпоксисукцинатную группу, аналогично пептиду E-64 или также азиридопептиды аналогично миразиридину.
Можно привести несколько примеров дифункциональных соединений типа Qa - E - Qb, которые могут быть использованы в рамках настоящего изобретения: саркозин, 2-(1-аминоэтил)-1,3-оксазол-4-карбоновая кислота и (2R,3R,4R)-3-гидрокси-2,4,6-триметилгептановая кислота.
Указанное дифункциональное соединение Qa - E - Qb предпочтительно может представлять собой аминокислоту согласно определению, приведенному далее. Оно также может представлять собой пептид, например дипептид, трипептид, тетрапептид, пентапептид, гексапептид, гептапептид, октапептид, нонапептид, декапептид или еще более длинный пептид.
Эти дифункциональные соединения могут быть введены в цепь пептида или белка, или пептидомиметика известными химическими реакциями. Они не содержат защитную группу для защиты терминальной функциональной группы, выбранной из группы, которую составляют первичная аминогруппа, вторичная аминогруппа, гидроксигруппа или меркаптогруппа. Например, если дифункциональное соединение представляет собой аминокислоту или пептид, то оно не имеет защиты N-терминальной группы; при этом можно защищать его боковые цепи или его боковые функциональные группы, которые не модифицируются при удлинении пептида.
Соответственно описанному ранее, указанные α-, β- или γ-аминокислоты, α-, β- или γ-гидроксикислоты и α-, β- или γ-меркаптокислоты предпочтительно используют в их активированных формах.
Исходные звенья дифункциональных соединений, выбранные не из α-, β- или γ-аминокислот, α-, β- или γ-гидроксикислот и α-, β- или γ-меркаптокислот, предпочтительно могут быть связаны с C-терминальной частью указанного пептидомиметика или с терминальной частью (предпочтительно функционализацией введением первичной или вторичной аминогруппы, гидроксигруппы или меркаптогруппы), или также с боковой цепью (по меньшей мере одной α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты), или также между двух звеньев, выбранных из α-, β- или γ-аминокислот, α-, β- или γ-гидрокскислот и α-, β- или γ-меркаптокислот.
Согласно предпочтительному варианту осуществления число исходных звеньев дифункциональных соединений, выбранных не из α-, β- или γ-аминокислот, α-, β- или γ-гидроксикислот и α-, β- или γ-меркаптокислот, не превосходит 50% от общего числа звеньев и предпочтительно не превосходит 25% от общего числа звеньев.
Согласно еще одному аспекту настоящего изобретения имеется по меньшей мере одна стадия, на которой указанную цепь пептида или белка, или пептидомиметика связывают с линкером и очищают от реакционной смеси экстракцией органическим растворителем (таким как циклогексан, гептаны или любой другой приемлемый растворитель), который не смешивается с водой (или со смесью "вода/этанол" или "вода/ацетонитрил"), или фильтрованием через диоксид кремния.
Согласно еще одному аспекту настоящее изобретение позволяет получать пептиды или белки, или пептидомиметики высокой чистоты после снятия защиты с боковых цепей (в случае необходимости) с последующим отделением их от линкера после последней стадии итерации для применения согласно назначению, например, в качестве активного вещества для доклинических испытаний, клинической практики или для любых других вариантов применения.
Согласно еще одному аспекту настоящего изобретения линкеры в случае способа по настоящему изобретению могут быть использованы повторно (рециклированы).
Второй целью настоящего изобретения является соединение, приемлемое для получения способом по настоящему изобретению. Указанное соединение представляет собой α-, β- или γ-аминокислоту или α-, β- или γ-гидроксикислоту, или α-, β- или γ-меркаптокислоту, или пептид, или белок, или пептидомиметик, связанные с линкером.
Описание
1. Определения
В рамках настоящего изобретения под термином "аминокислота" понимают природные аминокислоты и неприродные или синтетические аминокислоты. "Природные" аминокислоты имеют L-форму протеиногенных аминокислот, которые называют стандартными и которые могут быть найдены в белках природного происхождения, то есть аланин (Ala), аргинин (Arg), аспарагин (Asn), аспарагиновая кислота (Asp), цистеин (Cys), глутамин (Gln), глутаминовая кислота (Glu), глицин (Gly), гистидин (His), изолейцин (ILe), лейцин (Leu), лизин (Lys), метионин (Met), фенилаланин (Phe), пролин (Pro), серин (Ser), треонин (Thr), триптофан (Trp), тирозин (Tyr) и валин (Val). Они представляют собой также другие протеиногенные аминокислоты и предпочтительно пирролизинселеноцистеин.
"Неприродные" аминокислоты имеют D-форму определенных ранее природных аминокислот, гомоформы некоторых природных аминокислот (таких как аргинин, лизин, фенилаланин и серин) и нор-формы лейцина и валина.
К "неприродным" аминокислотам относятся также все синтетические аминокислоты. К ним относятся также неприродные аминокислоты, такие как:
Abu=2-аминобутировая кислота CH3-CH2-CH(COOH)(NH2);
iPr=изопропиллизин (CH3)2C-NH-(CH2)4-CH(COOH)(NH2);
Aib=2-аминоизобутировая кислота;
F-trp=N-формилтриптофан;
Orn=орнитин;
Nal(2')=2-нафтилаланин.
Этот перечень совершенно очевидно не является исчерпывающим.
Также можно использовать ненасыщенные α- и β-аминокислоты природного или неприродного происхождения.
В рамках настоящего изобретения термин "активированная аминокислота" в данном случае применяют для обозначения α-, β- или γ-аминокислот, активированных соответственно в форме 2,2-бис(трифторметил)-1,3-оксазолидин-5-она, или (2,2-бис(трифторметил)-1,3-оксазинан-6-она, или 2,2-бис(трифторметил)-1,3-оксазепан-7-она и их производных соединений необязательно с возможностью присоединения защитной группы к боковой цепи.
Настоящее изобретение относится также к синтезу пептидомиметиков. Предшественники, применяемые для указанного синтеза, определены далее.
Термин "α-, β- или γ-гидроксикислота" в данном случае применяют согласно правилам терминологии ИЮПАК, известным специалистам в данной области техники. Примеры представляют собой такие соединения, как молочная кислота, яблочная кислота, винная кислота, салициловая кислота или также γ-гидроксибутировая кислота, встречающиеся в природе. В рамках настоящего изобретения также можно использовать любые "неприродные" α-, β- или γ-гидроксикислоты, к которым относятся также любые синтетические α-, β- или γ-гидроксикислоты.
Термином "активированная α-, β- или γ-гидроксикислота" обозначают любые природные и/или неприродные, и/или синтетические α-, β- или γ-гидроксикислоты, которые были активированы соответственно в форме 2,2-бис(трифторметил)-1,3-диоксолан-4-она или 2,2-бис(трифторметил)-1,3-диоксан-4-она, или 2,2-бис(трифторметил)-1,3-диоксепан-4-она и их производных соединений необязательно с возможностью присоединения защитной группы к боковой цепи.
Термин "α-, β- или γ-меркаптокислота" в данном случае применяют согласно правилам терминологии ИЮПАК, известным специалистам в данной области техники. Примеры представляют собой такие соединения, как тиогликолевая кислота, 3-меркаптопропионовая кислота, меркаптобутановая кислота. В рамках настоящего изобретения также можно использовать любые "неприродные" α-, β- или γ-меркаптокислоты, к которым относятся также любые синтетические α-, β- или γ-меркаптокислоты.
Термином "активированная α-, β- или γ-меркаптокислоты" означает любые соединения, образующиеся после активации α-, β- или γ-меркаптокислот (природных, неприродных или синтетических) в форме соответственно 2,2-бис(трифторметил)-1,3-оксатиолан-5-она или 2,2-бис(трифторметил)-1,3-оксатиан-6-она, или 2,2-бис(трифторметил)-1,3-оксатиепан-7-она и их производных соединений необязательно с возможностью присоединения защитной группы к боковой цепи.
Специалисты в данной области техники знают, что в этом контексте обозначение α, β, γ и δ относится к положению углерода, связанного с аминогруппой (первичной или вторичной) или гидроксигруппой, или меркаптогруппой по отношению к углероду карбоксигруппы (C-терминальной группы).
Термин "пептидомиметик" применяют согласно предшествующему уровню техники в качестве функционального термина для обозначения соединения, способного имитировать или блокировать пептид относительно его взаимодействия со специфическим рецептором. В частности, пептидомиметик может содержать звенья, которые не представляют собой остатки аминокислот.
Сокращения "DMF", "DMSO", и "THF", хорошо известные химикам, обозначают диметилформамид, диметилсульфоксид и тетрагидрофуран соответственно.
2. Подробное описание
Первой существенной характеристикой способа по настоящему изобретению является применение α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, активированных в форме соответственно 2,2-бис(трифторметил)-1,3-оксазолидин-5-она или (2,2-бис(трифтор-метил)-1,3-оксазинан-6-она, или 2,2-бис(трифторметил)-1,3-оксазепан-7-она, или 2,2-бис(три-фторметил)-1,3-диоксолан-4-она, или 2,2-бис(трифторметил)-1,3-диоксан-4-она, или 2,2-бис(три-фторметил)-1,3-диоксепан-4-она, или 2,2-бис(трифторметил)-1,3-оксатиолан-5-она, или 2,2-бис(трифторметил)-1,3-оксатиан-6-она, или 2,2-бис(трифторметил)-1,3-оксатиепан-7-она и их производных, в присутствии линкера, растворимого в органическом растворителе. В данном случае под выражением "органический растворитель" понимают любой текучий инертный растворитель (или смесь), способный (в нагретом и/или холодном состоянии) растворять реагенты. Растворители, приемлемые для применения, содержат, без наложения ограничений, галогенпроизводные или негалогенпроизводные углеводороды.
При этом α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, активированные в форме соответственно 2,2-бис(трифторметил)-1,3-оксазолидин-5-она или (2,2-бис(трифторметил)-1,3-оксазинан-6-она, или 2,2-бис(трифторметил)-1,3-оксазепан-7-она, или 2,2-бис(трифторметил)-1,3-диоксолан-4-она, или 2,2-бис(трифторметил)-1,3-диоксан-4-она, или 2,2-бис(трифторметил)-1,3-диоксепан-4-она, или 2,2-бис(трифторметил)-1,3-оксатиолан-5-она, или 2,2-бис(трифторметил)-1,3-оксатиан-6-она, или 2,2-бис(трифторметил)-1,3-окса-тиепан-7-она и их производных, получают известными способами исходя из природных или неприродных α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот (имеющих боковую цепь (необязательно защищенную)) и гексафторацетона. На схеме реакций 3 представлена активация различных кислот по реакции, которая как таковая известна:
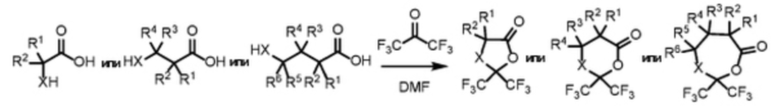
X=NH, N-алкил, N-арил, O, S
R1, R2, R3, R4, R5, R6=алкил или арил
Схема реакций 3. Активация α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот
Согласно варианту настоящего изобретения, который будет описан более подробно далее, линкеры (или защитные группы, или солюбилизирующие соединения) представляют собой полиолефины или более точно полиолефиновые олигомеры (при этом полиолефины называют также полиалкенами) и их производные, являющиеся функционализированными.
Согласно другому аспекту настоящего изобретения указанный способ синтеза пептидов или белков, или пептидомиметиков (необязательно защищенных по их боковым цепям) в жидкой среде отличается тем, что исходят из линкера и α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, активированной соответственно в форме 2,2-бис(трифторметил)-1,3-оксазолидин-5-она или (2,2-бис(трифторметил)-1,3-оксазинан-6-она, или 2,2-бис(трифторметил)-1,3-оксазепан-7-она, или 2,2-бис(трифторметил)-1,3-диоксолан-4-она, или 2,2-бис(трифторметил)-1,3-диоксан-4-она, или 2,2-бис(трифторметил)-1,3-диоксепан-4-она, или 2,2-бис(трифторметил)-1,3-оксатиолан-5-она, или 2,2-бис(трифтор-метил)-1,3-оксатиан-6-она, или 2,2-бис(трифторметил)-1,3-оксатиепан-7-она или их производных. При этом между двумя этими соединениями образуется ковалентная связь. Стадия удлинения/итерации состоит в том, что присоединяют или связывают последующие активированные α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-гидроксикислоты, которые в случае необходимости защищены по их боковым цепям (в форме сложного эфира, простого эфира, сложного тиоэфира, простого тиоэфира или любых других функциональных химических групп, приемлемых для настоящего способа). Таким образом, линкер играет роль защитной группы для защиты карбоксигруппы (C-терминальной группы) первой α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты.
Согласно другому аспекту настоящего изобретения указанный способ синтеза пептида или белка, или пептидомиметика может быть осуществлен при использовании надлежащим образом защищенного фрагмента пептида или белка, или пептидомиметика и α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика, связанных с молекулой PIB, что позволяет после взаимодействия получать более длинный пептид или белок, или пептидомиметик.
Согласно другому аспекту настоящего изобретения указанный способ синтеза пептида или белка, или пептидомиметика может быть осуществлен при использовании соединений Qa - E - Qb, имеющих по меньшей мере две функциональные группы Qa и Qb, которые являются одинаковыми или разными и выбраны из электрофильных и/или нуклеофильных функциональных химических групп. Примеры этих структур представляют собой оксид стирола, аминотиофенолы или 1-азидо-4-(бромметил)бензол. Эти соединения могут быть непосредственно связаны с линкером или соединены в ходе синтеза с аминогруппой (первичной или вторичной) или гидроксигруппой, или меркаптогруппой связанных α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, или пептидов, или белков, или пептидомиметиков.
Способ по настоящему изобретению может быть осуществлен в любом текучем инертном (галогенпроизводном или негалогенпроизводном) растворителе (или в смеси), способном растворять реагенты, при температуре, как правило, в интервале приблизительно от -20°C до приблизительно 150°C в реакторе (в периодическом или непрерывном режиме).
Согласно другому аспекту настоящего изобретения α-, β- или γ-аминокислота или α-, β- или γ-гидроксикислота, или α-, β- или γ-меркаптокислота, или пептид, или белок, или пептидомиметик, связанные с молекулой PIB, отличаются тем, что терминальная функциональная группа α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика, или любого другого соединения, имеющего по меньшей мере две функциональные группы, связана ковалентной связью (в форме сложного эфира, простого эфира, амида, сложного тиоэфира или любых других функциональных химических групп), придающей таким образом очень низкую растворимость в воде (< 30 мг/мл). Именно в этом смысле производное соединение PIB действует в качестве жидкой подложки или солюбилизирующего соединения для синтеза пептидов или белков, или пептидомиметиков.
В порядке пояснения на схеме реакций 4 показана реакция аминокислоты, активированной в форме 2,2-бис(трифторметил)-1,3-оксазолидин-5-она, с производным соединением полиизобутена (сокращенно PIB), имеющим терминальную фенильную группу. В данном случае α-аминокислота представляет собой L-фенилаланин (Phe).
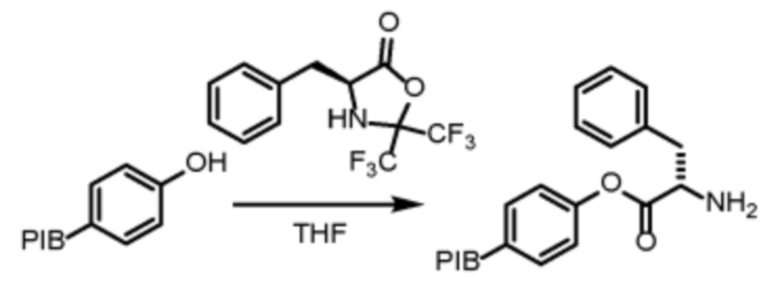
Схема реакций 4. Связывание с жидкой подложкой
Таким образом, первая α-аминокислота будущего пептида связывается с линкером посредством ковалентной связи типа сложного эфира.
На схеме реакций № 5 показана стадия удлинения или итерации, т.е. присоединение второго звена аминокислоты к первой аминокислоте, связанной с линкером. В данном случае вторая α-аминокислота представляет собой L-триптофан (Trp).
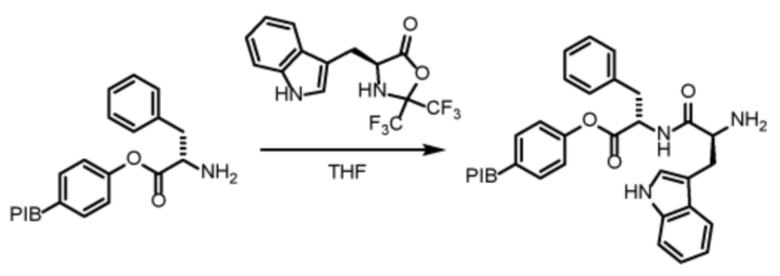
Схема реакций 5. Удлинение
Можно легко видеть, что указанный способ позволяет последовательными итерациями прибавлять звенья α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот к последней α-, β- или γ-аминокислоте или α-, β- или γ-гидроксикислоте, или α-, β- или γ-меркаптокислоте, или пептиду, или белку, или пептидомиметику, связанным с производным соединением PIB, в ходе синтеза для получения пептида или белка, или пептидомиметика, имеющего требуемую последовательность. Пептид или белок, или пептидомиметик, будучи химически связанным с линкером, может быть отделен в любой момент и предпочтительно после последней стадии итерации от всех полярных продуктов экстракцией органическим растворителем, таким как один или более гексанов или циклогексан, и водой или смесью "вода/этанол" или "вода/ацетонитрил". В конце последовательности итераций и в случае необходимости после снятия защиты с боковых цепей можно отделить пептид или белок, или пептидомиметик от линкера; таким образом, пептид или белок, или пептидомиметик утрачивает свою растворимость в неполярном растворителе и может быть отделен от линкера для использования соответственно его назначению.
Согласно другому аспекту настоящего изобретения получение производного соединения (или связывание) α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика (необязательно защищенных по их боковым цепям) с производным соединением PIB вызывает увеличение в значительной степени растворимости в жидкой органической среде указанных связанных α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика. Более точно эти α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептиды, или белки, или пептидомиметики, связанные с производным соединением PIB, становятся растворимыми в органических растворителях, таких как галогенпроизводные растворители (метиленхлорид, хлороформ), этилацетат, тетрагидрофуран, 2-метилтетрагидрофуран, изооктан, циклогексан, гексаны, метилциклогексан, метил-трет-бутиловый эфир, пропиленкарбонат или ароматические растворители, такие как бензол или толуол, или любой другой приемлемый растворитель. Таким образом, α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептиды, или белки, или пептидомиметики, связанные с производным соединением PIB, имеют большой коэффициент распределения относительно органической фракции во время экстракции/декантации, что обеспечивает, таким образом, простую и быструю очистку. В то же время, их растворимость в таких растворителях, как вода или смесь "вода/этанол" или "вода/ацетонитрил", является очень низкой.
Согласно другому аспекту настоящего изобретения реакция между производным соединением PIB и первой активированной α-, β- или γ-аминокислотой или α-, β- или γ-гидроксикислотой, или α-, β- или γ-меркаптокислотой, имеющей в случае необходимости необязательно защищенную боковую цепь (в форме сложного эфира, амида, сложного тиоэфира или любых других функциональных химических групп), ведет к получению соединения, растворимость которого в воде является низкой (< 30 мг/мл).
Таким образом, когда α-, β- или γ-аминокислота или α-, β- или γ-гидроксикислота или α-, β- или γ-меркаптокислота или пептид или белок, или пептидомиметик связаны с производным соединением PIB, последний действует в качестве жидкой подложки (или линкера, или солюбилизирующего соединения), поскольку конечное соединение этой реакция становится растворимым в органических растворителях, но остается нерастворимым в таких растворителях, как вода или смесь "вода/этанол" или "вода/ацетонитрил"; это обстоятельство позволяет отделять его от реакционной смеси разделением сред.
На схеме реакций 6 показан пример стадии отделения октапептида, имеющего последовательность Phe-Tpr-Cys(Bzl)-Trp-Cys(Bzl)-Trp-Trp-Cys(Bzl)-NH2, от линкера (производного соединения PIB, имеющего терминальную фенильную группу), с которым пептид связан карбоксигруппой (C-терминальной группой) L-фенилаланина. Боковые цепи остатков L-цистеинов защищены бензильной группой (Bzl). Свободный пептид нерастворим в неполярных растворителях (т.е. в циклогексане, гексанах), что позволяет легко отделять линкер. Линкер можно рекуперировать с целью его повторного использования в технологическом процессе.
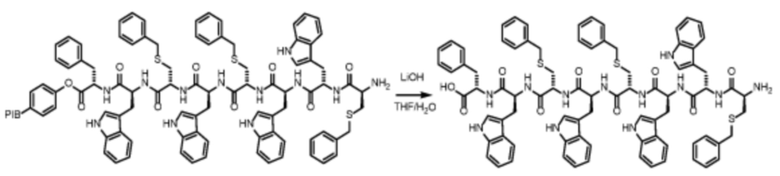
Схема реакций 6. Отделение октапептида от линкера
Пептид осаждается в таких растворителях, как диэтиловый эфир, циклогексан или любой другой приемлемый растворитель. Затем пептид может быть использован соответственно его назначению.
Далее описана вторая существенная характеристика способа получения пептидов или белков, или пептидомиметиков согласно настоящему изобретению, а именно использование линкеров, растворимых в некоторых органических растворителях, таких как этилацетат, тетрагидрофуран, 2-метилтетрагидрофуран, изооктан, циклогексан, гексаны, метилциклогексан, метил-трет-бутиловый эфир или галогенпроизводные растворители.
В способе по настоящему изобретению предпочтительно применяют полиолефины или более точно полиолефиновые олигомеры (при этом полиолефины называют также полиалкенами) и их производные в качестве линкеров или жидкой подложки или защитной группы для защиты карбоксигруппы (C-терминальной группы) α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика, или боковой цепи указанной α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика (в форме сложного эфира, амида, простого эфира, сложного тиоэфира, простого тиоэфира или любых других приемлемых функциональных химических групп) в жидкой среде. Молекулы полиолефинов содержат цепь атомов углерода, соединенных между собой простыми связями. Они могут содержать ответвления, образованные одинаковыми или разными алкильными группами, но предпочтительно одинаковыми. Полимеры предпочтительно состоят из мономерных звеньев, число которых составляет по меньшей мере 10 и предпочтительно от 15 до 350. Предпочтительными являются гомополимеры, но могут быть использованы сополимеры (необязательно насыщенные). В случае ненасыщенных полимеров или сополимеров число ненасыщенных связей в цепи атомов углерода преимущественно не превышает 5% и предпочтительно не превышает 3%.
Предпочтительно речь идет о производных соединениях полиизобутенов (PIB), представляющих собой класс полимеров, известный с 30-х годов прошлого века, но также можно использовать производные соединения полипропиленов.
Эти линкеры предпочтительно применяют в случае способа по настоящему изобретению в форме производных соединений, имеющих функциональные группы, что будет пояснено дальше более подробно. На схеме 7 показано некоторое число производных соединений PIB с введенными в них функциональными группами, являющихся приемлемыми в качестве жидкой подложки для осуществления настоящего изобретения.
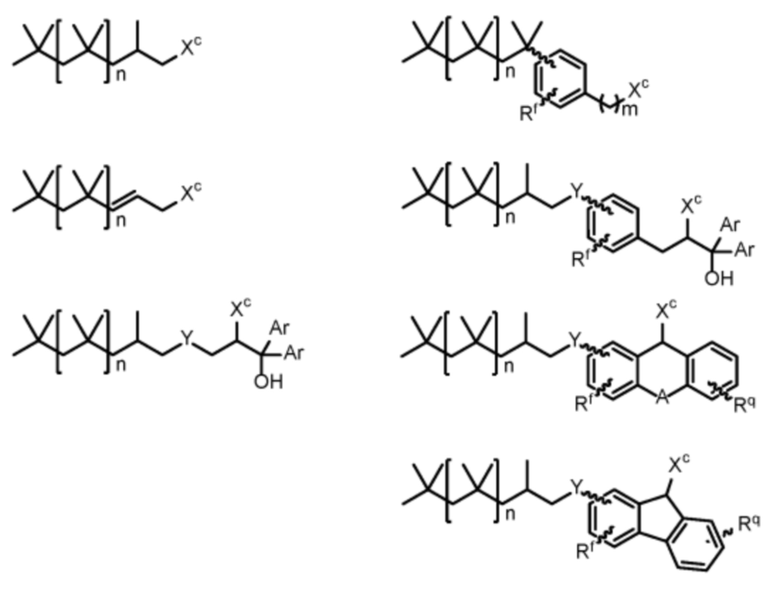
Схема 7. Общие структуры линкеров
В этих формулах:
- Xc означает группировку, выбранную из группы, которую составляют -OH, -NH2, -NHRa (Ra=алкил или арил), -SH;
- Ar означает ароматическую или гетероароматическую группу, необязательно имеющую заместители;
- A отсутствует или представляет собой группировку, выбранную из группы, которую составляют CH2, CH2-CH2, S;
- Rf означает группировку, выбранную из группы, которую составляют H, арил, гетероарил, алкил, O-алкил, O-арил, O-гетероарил;
- Rq означает группировку, выбранную из группы, которую составляют H, алкил, O-алкил, арил, гетероарил, O-арил, O-гетероарил;
- число n означает целое число, которое, как правило, превышает 10 и предпочтительно находится в интервале от 15 до 350.
Число m равно 0 или 1. В частности, группировка Xa может представлять собой первичную или вторичную аминогруппу, спиртовую группу, меркаптогруппу или фенильную группу.
Согласно настоящему изобретению эти линкеры связываются с карбоксигруппой α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты (с C-терминальной группой) или любыми функциональными химическими группами соединения, имеющего по меньшей мере две функциональные группы, посредством ковалентной связи. Тем самым предполагается, что линкеры будут использованы в надлежащим образом функционализированной форме, которая в настоящем описании обозначается как "производные соединения PIB". Этот термин в данном случае охватывает также производные линкеров, которые не являются производными соединениями полиизобутена, но которые представляют собой производные соединения других полиолефинов согласно определению, приведенному ранее; он предпочтительно охватывает производные соединения полиолефиновых олигомеров. Эта функционализация линкера, как правило, представляет собой введение функциональной группы в терминальную часть, предпочтительно в одну из терминальных частей цепи атомов углерода, что описано далее.
Согласно настоящему изобретению α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептиды, или белки, или пептидомиметики могут быть функционализированы в их боковых цепях производными соединениями PIB в форме сложного эфира, простого эфира, простого тиоэфира, сложного тиоэфира или любых других функциональных химических групп, приемлемых для настоящего способа. Это сводится к приданию производным соединениям PIB роли защитной группы для защиты одной или более боковых цепей указанных α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, или пептидов, или белков, или пептидомиметиков.
Цепи полиолефинов или полиолефиновых или полиалкеновых олигомеров, используемые в качестве линкеров, как правило, характеризуются среднемассовой молекулярной массой, но также можно использовать цепи полиолефинов или полиолефиновых или полиалкеновых олигомеров, называемых "однородными" и имеющих одинаковые молекулы с заданной длиной цепи.
Более точно способ синтеза пептидов или белков, или пептидомиметиков, в случае необходимости защищенных по их боковым цепям, в жидкой среде (в растворе) согласно настоящему изобретению отличается тем, что солюбилизируют α-, β- или γ-аминокислоту или α-, β- или γ-гидроксикислоту, или α-, β- или γ-меркаптокислоту, или пептид, или белок, или пептидомиметик в органической среде производным соединением PIB, связанным с карбоксигруппой α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика, или любого другого соединения, имеющего по меньшей мере две функциональные группы. Производное соединение PIB действует в качестве линкера (называемого в данном случае также "жидкой подложкой" или "солюбилизирующим соединением") α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика, или любого другого соединения, имеющего по меньшей мере две функциональные группы. Указанный пептид или белок, или пептидомиметик, связанный с этим линкером, синтезируют последовательным присоединением α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, или любых других соединений, имеющих по меньшей мере две функциональные группы, к последней α-, β- или γ-аминокислоте или α-, β- или γ-гидроксикислоте, или α-, β- или γ-меркаптокислоте, или любому другому соединению, имеющему по меньшей мере две функциональные группы. Таким образом, линкер служит также защитной группой для защиты карбоксигруппы (C-терминальной группы) во время синтеза пептида или белка, или пептидомиметика в ходе последовательных итераций.
Карбоксигруппа (C-терминальная группа) указанной α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика, в случае необходимости защищенных по их боковым цепям, связана ковалентной связью типа сложного эфира, амида, сложного тиоэфира или любыми другими химическими ковалентными связями с липофильным производным соединением PIB, придающим очень низкую растворимость в воде (< 30 мг/мл). Именно в этом смысле производное соединение PIB действует в качестве жидкой подложки или солюбилизирующего соединения для синтеза пептидов или белков, или пептидомиметиков.
Получение такого производного соединения α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика (необязательно защищенных по одной или более боковым цепям) с производным соединением PIB в значительной степени увеличивает растворимость в жидкой органической среде связанных α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептида, или белка, или пептидомиметика. Более точно эти α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептиды, или белки, или пептидомиметики, связанные с производным соединением PIB, становятся растворимыми в органических растворителях, таких как галогенпроизводные растворители (метиленхлорид, хлороформ), этилацетат, тетрагидрофуран, 2-метилтетрагидрофуран, изооктан, циклогексан, гексаны, метилциклогексан, метил-трет-бутиловый эфир или ароматические растворители, такие как бензол или толуол, или любой другой приемлемый растворитель. Следовательно, α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, или пептиды, или белки, или пептидомиметики, связанные с производным соединением PIB, имеют большой коэффициент распределения относительно органической фракции во время экстракции/декантации в присутствии циклогексана или одного или более гексанов и воды или смеси "вода/этанол" или также "вода/ацетонитрил", что позволяет, таким образом, осуществлять их простую и быструю очистку.
В варианте осуществления способа синтеза пептидов или белков, или пептидомиметиков (необязательно защищенных по их боковым цепям) в жидкой среде согласно настоящему изобретению исходят из соединения, имеющего по меньшей мере две функциональные группы, или α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты, активированной соответственно в форме 2,2-бис(трифторметил)-1,3-оксазолидин-5-она или (2,2-бис(трифторметил)-1,3-оксазинан-6-она, или 2,2-бис(трифторметил)-1,3-оксазепан-7-она, или 2,2-бис(трифторметил)-1,3-диоксолан-4-она, или 2,2-бис(трифторметил)-1,3-диоксан-4-она, или 2,2-бис(трифторметил)-1,3-диоксепан-4-она, или 2,2-бис(трифторметил)-1,3-оксатиолан-5-она, или 2,2-бис(трифторметил)-1,3-оксатиан-6-она, или 2,2-бис(трифторметил)-1,3-оксатиепан-7-она или их производных, которые будут связаны с одним из определенных ранее линкеров посредством ковалентной связи, и соединяют или связывают последовательными итерациями с соединениями, имеющими по меньшей мере две функциональные группы, или активированными α-, β- или γ-аминокислотами или α-, β- или γ-гидроксикислотами, или α-, β- или γ-гидроксикислотами, в случае необходимости защищенных по их боковым цепям.
Способ синтеза пептида или белка, или пептидомиметика согласно настоящему изобретению может быть осуществлен при использовании фрагмента пептида или белка, или пептидомиметика, надлежащим образом защищенного по его боковым цепям, и последовательности пептида или белка, или пептидомиметика, связанной с молекулой PIB, что позволяет, после взаимодействия, получать более длинный пептид или белок, или пептидомиметик.
Способ синтеза пептида или белка, или пептидомиметика согласно настоящему изобретению может быть осуществлен при использовании соединений, имеющих по меньшей мере две функциональные группы, а именно группировку Qa и группировку Qb, которые могут быть одинаковыми или разными и выбраны из электрофильных и/или нуклеофильных группировок. В качестве примера в первом варианте осуществления Qa может представлять собой электрофильную группировку, а Qb может представлять собой нуклеофильную группировку или также, во втором варианте осуществления, Qa может представлять собой первую электрофильную группировку, а Qb может представлять собой вторую электрофильную группировку, или также, в третьем варианте осуществления, Qa может представлять собой первую нуклеофильную группировку, а Qb может представлять собой вторую нуклеофильную группировку; в других вариантах Qa и Qb могут также представлять собой одну и ту же электрофильную группировку или также одну и ту же нуклеофильную группировку. Эти соединения, имеющие по меньшей мере две функциональные группы, могут быть непосредственно связаны с линкером или соединены в ходе синтеза с аминогруппой (первичной или вторичной) или гидроксигруппой, или меркаптогруппой связанных α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, или пептидов, или белков, или пептидомиметиков.
В ходе каждой стадии связывания, удлинения и/или итерации предпочтительно используют небольшой избыток относительно стехиометрического количества активированной α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты.
Эти дифункциональные соединения могут быть введены в цепь пептида или белка, или пептидомиметика известными химическими реакциями. В случае необходимости они могут быть защищены или замаскированы (по их нуклеофильной функциональной группе или любым другим функциональным химическим группам, для которых требуется такая защита, за счет известных реакций) и активированы известными способами.
Исходные звенья дифункциональных соединений, выбранные не из α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, предпочтительно могут быть связаны с C-терминальной частью указанного пептида или белка, или пептидомиметика или с N-, O- или S- терминальной частью (предпочтительно функционализацией введением аминогруппы, гидроксигруппы или меркаптогруппы), или также с боковой цепью, или также введены между двух звеньев, выбранных из α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот.
Согласно предпочтительному варианту осуществления число исходных звеньев дифункциональных соединений, выбранных не из α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, не превосходит 50% от общего числа звеньев, предпочтительно не превосходит 25% от общего числа звеньев и еще более предпочтительно не превосходит 10% от общего числа звеньев.
В качестве примера, способом по настоящему изобретению может быть получен семаглутид, представляющий собой пептидомиметик, содержащий в боковой цепи звено α-аминобутировой кислоты.
Далее приведен перечень соединений типа α-, β-, γ- или δ-аминокислот, которые могут быть использованы в качестве звеньев в рамках способа по настоящему изобретению, в дополнение к аминокислотам, уже указанным ранее: δ-аминолевулиновая кислота, γ-аминобутировая кислота, β-аминобутировая кислота (также известная под аббревиатурой BABA), β-аланин, β-лизин, β-аминоизобутировая кислота, β-N-метиламино-L-аланин, (2S,3S,8S,9S)-3-амино-9-метокси-2,6,8-триметил-10-фенилдека-4,6-диеновая кислота (также известный под аббревиатурой ADDA), (2R)-2-(метиламино)бутандиовая кислота (также известная под аббревиатурой NMDA) и 4-амино-3-гидроксибутановая кислота.
Далее приведен перечень соединений типа α-, β-, γ- или δ-гидроксикислот, которые могут быть использованы в качестве звеньев в рамках способа по настоящему изобретению: 4-гидроксибутановая кислота, 2-(гидроксиметил)-3-метилбутановая кислота и (2R,3R,4R)-3-гидрокси-2,4,6-триметилгептановая кислота.
Далее приведен перечень соединений типа α-, β-, γ- или δ-меркаптокислот, которые могут быть использованы в качестве звеньев в рамках способа по настоящему изобретению: 4-сульфанилбутановая кислота, 2-циклопропил-3-сульфанилпропановая кислота, 2-циклобутил-3-сульфанилпропановая кислота и 2-(2-сульфанилфенил)бутановая кислота.
Способ по настоящему изобретению обладает несколькими преимуществами.
Первое преимущество состоит в том, что способ позволяет получать пептиды или белки, или пептидомиметики (необязательно защищенные по их боковым цепям), связанные с линкером в жидкой органической среде.
Второе преимущество состоит в том, что способ позволяет получать связанные пептиды или белки, или пептидомиметики высокой чистоты (необязательно защищенные по их боковым цепям) простой промывкой (экстракцией) в органическом неполярном растворителе и водой или смесью "вода/этанол" или также "вода/ацетонитрил" или фильтрованием, обеспечивая таким образом удаление побочных продуктов (солей, кислот или любых других соединений), которые не представляют собой связанные производные соединения полиолефинов или полиолефиновых или полиалкеновых олигомеров, такие как избыток реагентов. Органические растворители, такие как циклогексан, гептан, гексаны, имеющие температуру вспышки < 15°C, являются приемлемыми для солюбилизации производных соединений полиолефинов или полиолефиновых или полиалкеновых олигомеров во время экстракции или промывки. Следовательно, способ по настоящему изобретению позволяет ограничить число стадий очистки, необходимых в способах предшествующего уровня техники.
Третье преимущество, являющееся особенно важным, состоит в том, что способ по настоящему изобретению позволяет синтезировать пептиды или белки, или пептидомиметики, регулируя длину производного соединения полиолефинов или полиолефиновых или полиалкеновых олигомеров, то есть делая их более липофильными.
Четвертое преимущество состоит в возможности регулировать чистоту пептида или белка, или пептидомиметика в ходе синтеза в любой момент времени отбором аликвоты с последующим анализом различными способами, известными специалистам в данной области техники (такими как масс-спектрометрия, высокоэффективная жидкостная хроматография, протонный магнитный резонанс или ядерный магнитный резонанс с углеродом-13).
Пятое преимущество заключается в том, что в этом способе не требуется использовать группировку, защищающую аминогруппу (первичную или вторичную) или гидроксигруппу, или меркаптогруппу соответственно α-, β- или γ-аминокислот или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот, что, в общем случае, исключает две стадии (стадию защиты и стадию снятия защиты). В более общем плане способ по настоящему изобретению обеспечивает оптимальную экономию на атомарном уровне, поскольку в его случае не требуется применять ни защитные группы для защиты аминогрупп (первичных или вторичных) или гидроксигрупп, или меркаптогрупп соответствующих кислот, ни линкеры. Эта экономия на атомарном уровне и сокращение числа стадий способа по настоящему изобретению в промышленном масштабе обеспечивает сокращение финансовых расходов, уменьшая при этом образование отходов, что является благоприятным экологическим фактором в отличие от способов, существующих в настоящее время.
Шестое преимущество настоящего изобретения состоит в том, что активация карбоксигруппы (C-терминальной группы) попутно обеспечивает защиту аминогруппы (первичной или вторичной) или гидроксигруппы, или меркаптогруппы, уменьшая, следовательно, число стадий.
Седьмое преимущество настоящего изобретения, являющееся особенно выгодным, заключается в получении пептидов или белков, или пептидомиметиков высокой чистоты после отщепления защитных групп от боковых цепей и затем линкера. Это обстоятельство позволяет избежать необходимости очищать синтезированный пептид или белок, или пептидомиметик. Следовательно, это обеспечивает дополнительную экономию по сравнению с известными способами. Это в еще большей степени ограничивает воздействие производства пептидов или белков, или пептидомиметиков на экологию.
Восьмое преимущество настоящего изобретения заключается в возможности получать пептиды или белки, или пептидомиметики с более крупными размерами молекул, изменяя размер молекул жидкой подложки или вводя в одну или более боковых цепей активированные α-, β- или γ-аминокислоты или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты.
Другие преимущества состоят в возможности автоматизировать способ по настоящему изобретению и в возможности рециклировать растворители-экстрагенты и линкеры (полиолефины или полиолефиновые или полиалкеновые олигомеры). Действительно, когда серия итераций для получения требуемой последовательности пептида или белка, или пептидомиметика завершена, из боковых цепей удаляют защитные группы и затем удаляют линкер реакциями, обычно используемыми в синтезе пептидов, такими как гидролиз, омыление, гидрогенолиз, или любой другой реакцией, приемлемой для настоящего способа.
Благодаря своей высокой чистоте, пептиды или белки, или пептидомиметики, получаемые этим способом, могут быть использованы в качестве фармацевтических препаратов (лекарственных средств и вакцин), косметических изделий, препаратов для борьбы с болезнями растений, продовольственных продуктов или в качестве промежуточных соединений для получения таких веществ.
Пример
Октапептид получали способом по настоящему изобретению.
На первой стадии активировали следующие аминокислоты: активированный L-фенилаланин (в данном случае обозначен как AAA1), активированный L-триптофан (в данном случае обозначен как AAA2) и активированный L-цистеин (защищенный бензильной защитной группой (Bzl)) (в данном случае обозначен как AAA3). Эта реакция соответствует приведенной ранее схеме реакций 3.
К раствору аминокислоты (10 ммоль) в N-N-диметилформамиде (5 мл) при комнатной температуре с использованием конденсатора газов, охлаждаемого сухим льдом (углекислотой), и барботера прибавляли избыток сконденсированного гексафторацетона (> 2 эквивалентов). После перемешивания в течение шестнадцати часов при комнатной температуре реакционную смесь сгущали досуха и остаток лиофилизовали. Полученное неочищенное вещество растворяли в дихлорметане, фильтровали, затем растворитель удаляли при пониженном давлении и лиофилизацию повторяли (три раза). 2,2-Бис(трифторметил)-1,3-оксазолидин-5-оны или активированные аминокислоты были получены в виде маслоподобных или твердых веществ с выходом 80-95%. Их формулы приведены далее на схеме 8.
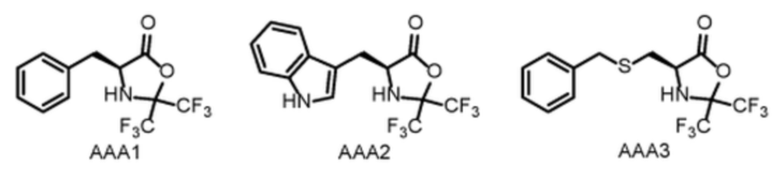
Схема 8. Структуры активированных аминокислот
На второй стадии связывали активированную аминокислоту (активированный L-фенилаланин в данном случае обозначен как AAA1) с линкером, в данном случае с производным соединением PIB. Эта реакция соответствует приведенной ранее схеме реакций 4.
Раствор производного соединения PIB (31,1 мг, 0,028 ммоль) и активированной аминокислоты (в данном случае AAA1) (9,8 мг, 0,031 ммоль) в смеси "тетрагидрофуран/гексафторизопропанол" (2 мл) нагревали при 50°C в течение 2 часов и затем охлаждали до комнатной температуры. К реакционной смеси прибавляли насыщенный водный раствор гидрокарбоната натрия (2 мл) и смесь перемешивали при комнатной температуре в течение тридцати минут. Из реакционной смеси три раза осуществляли экстракцию циклогексаном, промывали насыщенным раствором хлорида натрия, сушили над сульфатом натрия, фильтровали и сгущали при пониженном давлении для получения производного H2N-Phe-PIB.
На третьей стадии осуществляли удлинение пептида присоединением другой активированной аминокислоты (в данном случае AAA2). Эта реакция соответствует приведенной ранее схеме реакций 5.
Раствор производного соединения H2N-Phe-PIB (1 эквивалент) и последующей активированной аминокислоты (AAA2) (1,1 эквивалента) в смеси "тетрагидрофуран/гексафторизопропанол" (2 мл, 9/1) нагревали при 50°C в течение 2 часов и затем охлаждали до комнатной температуры. Реакционную смесь обрабатывали так же, как и ранее, для получения соответствующего связанного дипептида (H2N-Trp-Phe-PIB) и далее действовали так же. В данном случае, итерацию повторяли с активированной аминокислотой AAA3 в таких же условиях для получения соответствующего связанного трипептида (H2N-Cys(Bzl)-Trp-Phe-PIB).
Затем осуществляли другие итерации до получения связанного октапептида с последовательностью H2N-Cys(Bzl)-Trp-Trp-Cys(Bzl)-Trp-Cys(Bzl)-Trp-Phe-PIB.
На последней стадии пептид отделяли от линкера. Эта реакция соответствует приведенной ранее схеме реакций 6.
К раствору связанного октапептида (H2N-Cys(Bzl)-Trp-Trp-Cys(Bzl)-Trp-Cys(Bzl)-Trp-Phe-PIB) (8 мг) в смеси "тетрагидрофуран/вода" (8:2, 2 мл) при комнатной температуре прибавляли раствор гидроксида лития (1 М, 2 мл). Реакционную смесь перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь разбавляли раствором "диоксан/HCl" и осадок промывали циклогексаном.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> STRAINCHEM
<120> СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДОВ ИЛИ БЕЛКОВ, ИЛИ ПЕПТИДОМИМЕТИКОВ
<130> BR 2836 FR
<140> FR1904604
<141> 2019-05-02
<160> 2
<170> PatentIn version 3.5
<210> 1
<211> 8
<212> PRT
<213> Неизвестно
<220>
<223> Данная последовательность предоставлена в качестве примера
в поданной заявке.
<220>
<221> ПЕПТИД
<222> (1)..(8)
<223> Xaa3, Xaa5 и Xaa8 представляют собой остатки L-цистеинов, боковые
цепи которых защищены бензильной группой (Bzl).
<400> 1
Phe Trp Xaa Trp Xaa Trp Trp Xaa
1 5
<210> 2
<211> 8
<212> PRT
<213> Неизвестно
<220>
<223> Данная последовательность предоставлена в качестве примера
в поданной заявке.
<220>
<221> пептид
<222> (1)..(8)
<223> Xaa3, Xaa5 и Xaa8 представляют собой остатки L-цистеинов, боковые
цепи которых защищены бензильной группой (Bzl).
Xaa1 представляет собой остаток Phe, модифицированный производным
соединением PIB.
<400> 2
Xaa Trp Xaa Trp Xaa Trp Trp Xaa
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕРАПЕВТИЧЕСКИЕ ПЕПТИДЫ | 2010 |
|
RU2548905C2 |
| ТЕРАПЕВТИЧЕСКИЕ ПЕПТИДЫ | 2010 |
|
RU2676713C2 |
| НОВЫЕ АНАЛОГИ ГЛЮКАГОН-ПОДОБНОГО ПЕПТИДА, КОМПОЗИЦИЯ И СПОСОБ ПРИМЕНЕНИЯ | 2010 |
|
RU2557301C2 |
| МЕЧЕНЫЕ РАДИОАКТИВНЫМ ИЗОТОПОМ ПЕПТИДЫ ДЛЯ ДИАГНОСТИКИ И ТЕРАПИИ | 1996 |
|
RU2171117C2 |
| ПЕПТИДОМИМЕТИЧЕСКИЕ МАКРОЦИКЛЫ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2639523C2 |
| АНТИБИОТИЧЕСКИЕ ПЕПТИДЫ | 2008 |
|
RU2472805C2 |
| ИНГИБИТОРЫ АПОПТОЗА И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2582247C2 |
| RGD-СОДЕРЖАЩИЕ ПЕПТИДОМИМЕТИКИ И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2519736C2 |
| КОНЪЮГАТЫ АМАТОКСИНОВ С УЛУЧШЕННЫМИ ЛИНКЕРАМИ | 2011 |
|
RU2601411C2 |
| КОНЪЮГАТЫ ЦИТОКИНОВ ДЛЯ ЛЕЧЕНИЯ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2787201C2 |
Настоящее изобретение относится к области биотехнологии, в частности к новому способу получения полипептидов. Изобретение раскрывает способ жидкофазного синтеза полипептидов последовательным удлинением второй терминальной части (первичной или вторичной аминогруппы, гидроксигруппы или меркаптогруппы) цепи пептида звеньями, отличающийся тем, что звенья выбраны из группы, которую составляют α-, β- или γ-аминокислоты, α-, β- или γ-гидроксикислоты, α-, β- или γ-меркаптокислоты (природные или неприродные или синтетические), молекулы которых содержат по меньшей мере две функциональные группы. 11 з.п. ф-лы, 1 пр.
1. Способ синтеза пептидов или белков последовательным удлинением второй терминальной части, содержащей первичную или вторичную аминогруппу, гидроксигруппу или меркаптогруппу, цепи пептида или белка звеньями, отличающийся тем, что:
- звенья выбраны из группы, которую составляют соединения типа Qa - E - Qb, где Qa и Qb могут быть одинаковыми или разными и выбраны из электрофильных и нуклеофильных групп, а E означает спейсер;
- первая терминальная часть пептида или белка связана ковалентной связью с линкером, растворимым в органических растворителях, таких как галогенпроизводные растворители (предпочтительно метиленхлорид или хлороформ), этилацетат, тетрагидрофуран, 2-метилтетрагидрофуран, изооктан, циклогексан, гексаны, метилциклогексан, метил-трет-бутиловый эфир или ароматические растворители, такие как бензол или толуол;
- причем в способе не применяют защитные группы для защиты первичной или вторичной аминогруппы, или гидроксигруппы, или меркаптогруппы;
- указанные звенья Qa - E - Qb выбраны из группы, которую составляют природные или неприродные или синтетические α-, β- или γ-аминокислоты, природные или неприродные или синтетические α-, β- или γ-гидроксикислоты, природные или неприродные или синтетические α-, β- или γ-меркаптокислоты;
- указанные звенья α-, β- или γ-аминокислот, или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот применяют соответственно в форме 2,2-бис(трифторметил)-1,3-оксазолидин-5-она или (2,2-бис(трифторметил)-1,3-оксазинан-6-она, или 2,2-бис(трифторметил)-1,3-оксазепан-7-она, или 2,2-бис(трифторметил)-1,3-диоксолан-4-она, или 2,2-бис(трифторметил)-1,3-диоксан-4-она, или 2,2-бис(трифторметил)-1,3-диоксепан-4-она, или 2,2-бис(трифторметил)-1,3-оксатиолан-5-она, или 2,2-бис(трифторметил)-1,3-оксатиан-6-она, или 2,2-бис(трифторметил)-1,3-оксатиепан-7-она, или их производных,
где указанный способ включает:
(i) стадию закрепления исходного звена Qa - E - Qb на липофильном линкере, где на свободном конце такого исходного звена останется функциональная группа, выбранная из -NH2, -NH-алкил, -NH-арил, -OH или –SH;
(ii) стадию получения активированной формы исходного звена Qa - E - Qb в реакции с гексафторацетоном;
(iii) стадию прикрепления указанной активированной формы, полученной на стадии (ii), на группе на свободном конце продукта стадии (i);
(iv) стадию экстракции продукта реакции удлинения со стадии (iii);
(v) повторение стадий (ii), (iii) и (iv) до тех пор, пока не будет получен целевой пептид или белок желаемой длины;
(vi) стадию отделения целевого пептида или белка от указанного линкера,
и где указанный линкер
- включает полиолефиновую цепь или представляет собой цепь полиолефина или полиолефинового или полиалкенового олигомера с по меньшей мере 10 мономерными звеньями, и
- имеет среднемассовую молекулярную массу в интервале от 600 до 20 000 и предпочтительно от 700 до 15 000.
2. Способ по п. 1, отличающийся тем, что группы Qa и Qb выбраны из группы, которую составляют спиртовые, альдегидные группы, первичные аминогруппы, вторичные аминогруппы, азидные, этинильные группы, галогены, тиольные, винильные группы, и/или тем, что спейсер E выбран из группы, которую составляют ароматические соединения, гетероароматические соединения, насыщенные алкильные цепи (разветвленные или неразветвленные), ненасыщенные алкильные цепи (разветвленные или неразветвленные), гликоли (и предпочтительно полиэтиленгликоль).
3. Способ по п. 1 или 2, отличающийся тем, что звенья α-, β- или γ-аминокислот, или α-, β- или γ-гидроксикислот, или α-, β- или γ-меркаптокислот применяют в активированной форме.
4. Способ по любому из пп. 1-3, отличающийся тем, что линкер содержит полиолефиновую цепь или представляет собой цепь полиолефина или полиолефинового или полиалкенового олигомера с от 15 до 350 мономерных звеньев, и предпочтительно представляет собой полиизобутеновую цепь.
5. Способ по любому из пп. 1-4, отличающийся тем, что цепь полиолефина или полиолефинового или полиалкенового олигомера содержит функциональную группу по меньшей мере в одной из своих терминальных частей.
6. Способ по любому из пп. 1-5, отличающийся тем, что цепь полиолефина или полиолефинового или полиалкенового олигомера содержит ненасыщенные связи "углерод-углерод" в количестве, не превосходящем 5% и предпочтительно не превосходящем 3%.
7. Способ по любому из пп. 1-6, отличающийся тем, что линкер содержит цепь полиолефина (или представляет собой полиолефиновую цепь) или полиолефинового или полиалкенового олигомера, оканчивающуюся по меньшей мере одной группировкой, выбранной из группы, которую составляют:
- функциональная группа -Xa, где Xa выбрана из группы, которую составляют -OH, -NH2, -NHRa (Ra=алкил или арил), -SH;
- функциональная группа -Y-C6H4Xb, где:
- Y означает O, S, CH2 или отсутствует;
- Xb выбрана из группы, которую составляют -OH, -NH2, -NHRa, -SH, -CXaRaRb, -C6H3Rc(CRaXa), где Rb выбрана из группы, которую составляют -H, -арил, -гетероарил, -алкил, а Rc выбрана из группы, которую составляют -H, -алкил, -O-алкил, -арил, -O-арил, -гетероарил, -O-гетероарил;
- функциональная группа -CRd=CH-CHXa или функциональная группа -CRdH-CH=CH-CHXa, где Xa имеет определенные ранее значения, а Rd означает метил или этил.
8. Способ по любому из пп. 1-7, отличающийся тем, что:
- первая терминальная часть цепи пептида или белка представляет собой первое звено α-, β- или γ-аминокислоты, или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты;
- цепь пептида или белка образована n звеньями α-, β- или γ-аминокислоты, и/или α-, β- или γ-гидроксикислоты, и/или α-, β- или γ-меркаптокислоты;
- вторая терминальная часть пептидной цепи представляет собой другое звено α-, β- или γ-аминокислоты, или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты.
9. Способ по любому из пп. 1-8, отличающийся тем, что во время удлинения прибавляют другое звено α-, β- или γ-аминокислоты, или α-, β- или γ-гидроксикислоты, или α-, β- или γ-меркаптокислоты ко второй терминальной части исходя из их соответствующих активированных форм.
10. Способ по любому из пп. 1-9, отличающийся тем, что пептид или белок получают соединением пептида или белка, связанного с линкером, с фрагментом пептида или белка, надлежащим образом защищенного по его боковым цепям.
11. Способ по любому из пп. 1-10, включающий по меньшей мере одну стадию, на которой цепь пептида или белка, связанную с линкером, отделяют от реакционной смеси экстракцией органическим растворителем (таким как циклогексан, гептан, гексаны), или промывкой водой или смесью "вода/этанол" или "вода/ацетонитрил", или простым фильтрованием.
12. Способ по любому из пп. 1-11, включающий стадию, на которой пептид или белок отделяют от линкера.
| US 2012059149 A1, 08.03.2012 | |||
| ALBERICO F | |||
| et al | |||
| A New Strategy for Solid-Phase Depsipeptide Synthesis Using Recoverable Building Blocks, Organic Letters, 2005, v | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| RU 2017113219 A1, 02.11.2018 | |||
| Устройство для подогревания полозьев механических саней | 1926 |
|
SU8305A1 |
Авторы
Даты
2024-10-07—Публикация
2020-05-04—Подача