Настоящее изобретение относится к составу для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий, содержащему триазинон, такой как толтразурил и многоядерное комплексное соединение железо (III)-полисахарид вместе со специфически выбранным поверхностно-активным веществом.
Экономически успешное производство мяса в настоящее время отличается высокоинтенсивным животноводством, то есть содержанием большого количества животных, специально отобранных для оптимизации разведения. Эти фермы отличаются, например, использованием большого количества техники, дополнительным кормлением пищевыми добавками и участием как можно меньшего количества персонала. В случае ферм по разведению поросят это означает, что большое количество свиноматок, которых выращивают для большого количества поросят в помете, содержат в достаточно больших свинарниках. Оптимизация кормов и соответствующий отбор в процессе разведения позволяют поросятам быстро расти.
Этот тип содержания животных часто является причиной увеличения числа определенных типичных заболеваний и недостаточностей. Помимо стресса, которому, в частности, очень подвержены свиньи при интенсивном содержании, у поросят проявляются, среди прочего, такие явления как протозойные инфекции (кокцидиозы) и анемические состояния, и то и другое уже необходимо держать под контролем с помощью профилактического использования медикаментов.
Кокцидиозы представляют собой часто встречающиеся паразитарные инфекционные заболевания животных. Так, например, простейшие родов Eimeria, Isospora, Neospora, Sarcosporidia и Toxoplasma вызывают кокцидиозы во всем мире. Примерами экономически важных кокцидиозов являются инфекции свиней, вызванные кокцидиями рода Isospora, или инфекции крупного рогатого скота, вызванные кокцидиями рода Eimeria. Инфекции, вызываемые Isospora suis, только в последние годы были признаны причиной диареи у поросят и интенсивно изучаются. Как правило, инфекция передается поросятам из окружающей среды или от поросенка к поросенку через ооцисты, содержащие в каждом случае две спороцисты с двумя спорозоитами в каждом случае. Паразитические стадии протекают в эпителиальных клетках ворсинок тонкой кишки. Клиническая картина заболевания включает некротическое воспалительное разрушение эпителиальных клеток кишечника с атрофией ворсинок и, как следствие, нарушение всасывания и пищеварения. Характерным признаком острого заболевания является жидкий понос от беловатого до желтого цвета, который чаще всего возникает на 2-3 неделе жизни. У инфицированных поросят снижается набор веса. Лечение и терапия заболевания на сегодняшний день являются недостаточными.
Антибиотики являются неэффективными, несмотря на то, что сульфонамиды одобрены для лечения кокцидиоза, их действие находится под вопросом, и частые повторные введения в любом случае непригодны для применения на практике. Другие возможные способы лечения находятся под вопросом, так как введение, например, монензина, ампролиума или фуразолидона, не показало успеха в профилактике заболевания у экспериментально инфицированных поросят. В более поздних исследованиях Isospora suis были обнаружены в до 92% всех пометов на некоторых фермах, несмотря на хорошую гигиену. Этот тип заболевания не ограничивается свиньями, но также встречается у многих других видов животных, например, в птицеводстве, у телят, ягнят или мелких животных (кроликов).
Примером недостаточности является железодефицитная анемия у новорожденных поросят. Из-за быстрого роста в первые дни после рождения запасы железа в организме быстро истощаются, и их необходимо компенсировать из внешних источников. Из-за большого количества молочных поросят такое замещение при питании молоком свиноматки не может происходить в достаточной степени. Если, более того, содержание животных происходит на бетоне или пластике, поросята также не могут усваивать соединения железа, извлекаемые из земли. У поросят развивается анемия.
Клинически значимое анемическое состояние возникает, когда содержание гемоглобина в крови падает до менее 80 г/л. Согласно рекомендациям NRC (National Research Council, Nutrient Requirements of Domestic Animals, No. 6, Nutrient Requirements of Swine, National Academy of Sciences, Washington DC, 1979) минимальный уровень гемоглобина, при котором поросята растут здоровыми и не проявляют признаки анемии, составляет 90 г/л. Однако заметные симптомы, такие как потеря веса или задержка роста, наблюдаются только тогда, когда содержание гемоглобина в крови падает до значений ниже 80 г/л. Другими показателями запаса железа являются гематокрит и количество эритроцитов на единицу объема. Тяжелая форма железодефицитной анемии также приводит к гибели поросят.
Препараты для борьбы с вышеупомянутыми заболеваниями и недостаточностями уже доступны.
С кокцидиозом можно успешно бороться посредством введения активных ингредиентов группы триазинона. С этой целью различают триазиндионы, примерами которых являются активные ингредиенты клазурил, диклазурил, летразурил, и триазинтрионы, примерами которых являются активные ингредиенты толтразурил, толтразурил сульфоксид и поназурил. Триазиноны, в частности толтразурил, понзазурил или диклазурил, и их активность против кокцидий известны из серии публикаций, см., среди прочего, DE-A 2718799 и DE-A 2413722.
В WO 99/62519 раскрываются полутвердые препараты толтразурил сульфона (поназурил) на водной основе. Так же известно, что толтразурил, в частности, подходит для лечения кокцидиоза (например, вызванного Isospora suis) у свиней.
Наиболее важными имеющимися в продаже соединения для лечения кокцидиоза являются диклазурил (2,6-дихлор-α-(4-хлорфенил)-4-(4,5-дигидро-3,5-диоксо-1,2,4-триазин-2(3Н)-ил)бензенацетонитрил, CAS №101831-37-2) для добавления в корм и толтразурил (1-метил-3-[3-метил-4-[4-[(трифторметил)тио]фенокси]фенил]-1,3,5-триазин-2,4,6(1Н,3Н,5Н)трион, CAS №69004-03-1).
Толтразурил доступен для приобретения, например, в виде состава для питьевой воды для домашней птицы и в виде пероральной суспензии, среди прочего, для лечения молочных поросят. Поросятам рекомендуют вводить дозу 20 мг/кг массы тела на 3-5 день после рождения.
Общая концепция комбинирования активного вещества для лечения кокцидиоза с соединением железа также известна.
В качестве наилучшего примера в ЕР 2164496 А1 раскрываются составы для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий, содержащие триазинон, такой как толтразурил, и многоядерные комплексные соединения железа (III), и показан синергизм этих двух соединений в отношении клинического результата, состоящего в прибавке веса у поросят, получавших лечение таким комбинированным составом.
В ЕР 2164496 А1 также показано, что поиск состава, который может быть составлен из триазинона и указанного многоядерного комплексного соединения железа (III), является не простым.
Положительную корреляцию, обнаруженную в ЕР 2164496 А1, применяли для инъекционного применения согласно раскрытию WO 2014/086958 А1 и WO 2014/086959 А1.
Во всех указанных выше ЕР 2164496 Al, WO 2014/086958 А1 и WO 2014/086959 А1, среди прочего, используют железо (III) типа поли-β-FeO(ОН) со связанными посредством образования комплекса полимерными углеводными соединениями. В ЕР 2164496 А1, показано, что в контексте комбинирования таких многоядерных комплексных соединений железа (III) с триазиновыми соединениями предпочтительными являются многоядерные комплексные соединения железо (III)-полисахарид.
Среди таких многоядерных комплексных соединений железо (III)-полисахарид коммерческое значение приобрели в основном, но не исключительно, железо (III)-декстран (CAS №9004664), железа (III) гидроксид-полимальтоза (железа (III) гидроксид-декстрин, CAS №53858-86-9), железо (III)-сахароза (сахароза железа (III), железо (III)-«caxap», CAS №8047-67-4) и комплекс натрий/железо (III)-глюконат в растворе сахарозы (CAS №34089-81-1).
В литературе встречаются разные названия этих соединений. В контексте настоящего изобретения под такими соединениями, как Глептоферрон, железо (III)-декстран, железо (III)-полимальтоза, железо (III)-декстрин, железо (III)-сахароза, железо (III)-глюконат, железо (III)-сахар, понимают комплексы иона железа (3+) с гидроксид-ионами (ОН-), группами воды (H2O) и кислородом (О), которые присутствуют в олигомерной или полимерной форме и являются ассоциированными в их координационной сфере в форме комплексов с одним или несколькими из указанных выше олигомерных и полимерных углеводных соединений.
По этой причине эти соединения также называют железа (III) гидроксид-полисахаридами или железа (III) оксигидрокси-полисахаридами, причем «полисахарид» означает вышеуказанные олигомерные или полимерные углеводные соединения или их производные или, в общем, соединения из группы олигомерных или полимерных углеводов.
Многоядерные комплексы железа (III) этого типа описаны, например, в D.S. Kudasheva et al., "Structure of Carbohydrate-bound Polynuclear Oxyhydroxide Nanoparticles in Parenteral Formulation", J. Inorg. Biochem. 98 (2004) 1757-1769, а также I. Erni et al., "Chemical Characterization of Iron(III) Hydroxide-Dextrin Complexes" Arzneim.-Forsch./Drug Res. 34 (II) (1984) 1555-1559, F. Funk et al., "Physical and Chemical Characterization of Therapeutic Iron Containing Materials", Hyperfine Interactions 136 (2001) 73-95, E. London "The Molecular Formula and Proposed Structure of the Iron-Dextran Complex, IMFERON", J. Pharm. Sci. 93 (2004) 1838-1846 и A. John "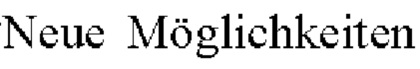 der Eisenversorgung neugeborener Ferkel unter Beachtung biochemischer Aspekte" [Novel possibilities of supplying iron to new born piglets, taking account of biochemical aspects],
der Eisenversorgung neugeborener Ferkel unter Beachtung biochemischer Aspekte" [Novel possibilities of supplying iron to new born piglets, taking account of biochemical aspects], 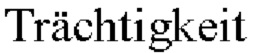 und Geburt beim Schwein [Pregnancy and birth in pigs]: 8th Bernburger Biotechnology Workshop, Bernburg (2002) 89-94.
und Geburt beim Schwein [Pregnancy and birth in pigs]: 8th Bernburger Biotechnology Workshop, Bernburg (2002) 89-94.
Поскольку состав этих соединений во многих случаях не описан количественно, а также может варьировать в пределах соединений в зависимости от типа получения, под этими многоядерными комплексными соединениями железо (III)-полисахарид следует понимать все комплексы описанных выше классов соединений, которые известны специалисту в данной области техники.
Эти соединения железа применяют почти исключительно при изготовлении медицинских и ветеринарных препаратов для инъекций. В ветеринарии дополнительно также применяют некоторое количество препаратов для перорального введения.
Помимо первого раскрытого преимущества комбинирования триазинового соединения с многоядерными комплексными соединениями железа (III) согласно ЕР 2164496 А1, существуют другие потенциальные параметры, которые могут дополнительно влиять на эффективность и полезность состава для применения для одновременного лечения кокцидиоза и железодефицитных анемий.
В качестве примера в WO 2014/086960 А1 раскрывается, что пенообразование, очевидно, является нежелательным признаком для любого состава. Поэтому в WO 2014/086960 А1 раскрывается, что для того, чтобы избежать чрезмерного пенообразования следует использовать водные суспензии, содержащие триазин, комплекс железа и одно или несколько поверхностно-активных веществ, имеющих особенно низкий показатель ГЛБ.
Несмотря на то, что в WO 2014/086960 А1 раскрывается, что другие поверхностно-активные вещества могут использоваться в комбинации с поверхностно-активными веществами с низким показателем ГЛБ и могут быть добавлены в соответствующий состав, в WO 2014/086960 А1 не раскрывается какая-либо либо причина добавления или пороговое значения в отношении указанных других поверхностно-активных веществ, помимо того, что они имеют более высокий показатель ГЛБ, чем те, которые согласно WO 2014/086960 А1 уменьшают пенообразование.
Поверхностно-активное вещество с высоким показателем ГЛБ согласно раскрытию WO 2014/086960 А1 представляет собой любое поверхностно-активное вещество, которое имеет показатель ГЛБ выше 8, в то время как те поверхностно-активные вещества, которые оказались предпочтительными для подавления пенообразования, представляют собой поверхностно-активные вещества с показателем ГЛБ до 8.
В заключение, поверхностно-активные вещества согласно WO 2014/086960 А1 подразделяются на поверхностно-активные вещества, которые полезны для подавления пенообразования и имеют показатель ГЛБ, равный 8 или ниже, и поверхностно-активные вещества, которые могут присутствовать или отсутствовать и которые не обладают таким свойством.
Поверхностно-активные вещества, упомянутые в WO 2014/086960 А1, которые имеют высокий показатель ГЛБ и, следовательно, не способствуют эффекту подавления пенообразования, представляют собой полиэтиленовые производные касторового масла, алкиловый простой эфир полиоксиэтилена, сложные эфиры полиоксиэтиленсорбитана и жирных кислот, полиоксиэтиленстеарат, лаурилсульфат натрия, докузат натрия, цетримид, фосфолипиды или хлорид цетилпиридиния.
Однако такой перечень поверхностно-активных веществ с предполагаемым высоким показателем ГЛБ не является достаточно уточненным, чтобы получить из него какое-либо фактическое поверхностно-активное вещество, которое в действительности как таковое будет иметь такой высокий показатель ГЛБ. В качестве примера, любое из вышеупомянутых и раскрытых соединений, содержащих полиоксиэтилен, будет соответствовать ограничению наличия высокого показателя ГЛБ только в том случае, если такое соединение будет иметь достаточно длинную полиоксиэтиленовую часть, что делает его более гидрофильным и, таким образом, приводит к более высокому показателю ГЛБ.
Кроме того, описанные фосфолипиды обычно вообще не имеют рассчитываемый показатель ГЛБ, а если имеют, то он обычно будет значительно ниже 10. Это также может служить причиной того, что лецитин (являющийся фосфолипидом) упоминается в WO 2014/086960 А1 в качестве как поверхностно-активного вещества с низким показателем ГЛБ, так и поверхностно-активного вещества с высоким показателем ГЛБ.
Из этих структурных классов потенциальных поверхностно-активных веществ с высоким показателем ГЛБ только два конкретных члена обнаружены в более поздних примерах и конкретно раскрытых составах согласно WO 2014/086960 А1.
Они представляют собой полиэтиленовые производные касторового масла, которые уточнены как сополимер Полиоксил 35 - гидрогенизированное касторовое масло и докузат натрия. В WO 2014/086960 А1 явно раскрыты 14 отдельных составов, демонстрирующих влияние на пенообразование в разные моменты времени, и еще три точных состава, которые не уточнены в отношении их влияния на подавление пенообразования (стр. 18, строки 13-22).
Что касается 14 приведенных в качестве примера составов, Примеры 4, 5, 7 и 8 содержат поверхностно-активное вещество сополимер Полиоксил 35 гидрогенизированное касторовое масло в качестве поверхностно-активного вещества с высоким показателем ГЛБ, которое присутствует в продаже, например, под торговым наименованием Кремофор EL (CAS 61791-12-6), и Примеры 9-14 содержат докузат натрия в качестве поверхностно-активного вещества.
Что касается конкретно упомянутых составов на стр. 18 в WO 2014/086960 А1, которые не были протестированы в отношении пенообразования, где первые два содержат сополимер Полиоксил 35 гидрогенизированное касторовое масло, а третий, как раскрыто, содержит докузат натрия.
Докузат натрия имеет показатель ГЛБ, равный приблизительно 10, согласно US 2014/0127320 Al, тогда как Кремофор EL имеет показатель ГЛБ, равный 12-14, согласно данным продавца.
Рассматривая Примеры 9-14 в WO 2014/086960 А1, которые содержат докузат натрия, очевидно, что они являются сравнительными примерами, поскольку ни один из них не содержит поверхностно-активное вещество с показателем ГЛБ, равным 8 или ниже, которое, как утверждают, является причиной подавления пенообразования.
Об этом свидетельствует тот факт, что все составы в примерах 9-14 показывают чрезмерное пенообразование (по меньшей мере при t=0 мин).
Рассматривая Примеры 4, 5, 7 и 8, касающиеся предполагаемого подавления пенообразования, составы согласно этим примерам содержат либо сорбитан моноолеат, который также известен как SPAN 80 (CAS 1338-43-8) и имеет показатель ГЛБ, равный приблизительно 4,6, (примеры 4, 5 и 8), либо пропиленгликоля монолаурат (CAS 27194-74-7), который имеет показатель ГЛБ, равный приблизительно от 4,3 до 4,5 (Пример 7).
Помимо предполагаемого эффекта подавления пенообразования при добавлении либо сорбитан моноолеата, либо пропиленгликоля монолаурата в качестве поверхностно-активных веществ, имеющих показатель ГЛБ, равный приблизительно 4,6 или от 4,3 до 4,5, соответственно, не упоминается какой-либо эффект, который может или мог бы быть связан с дополнительным добавление сополимера Полиоксил 35 - гидрогенизированное касторовое масло, имеющего показатель ГЛБ, равный от 12 до 14.
Согласно WO 2014/086960 А1, другим поверхностно-активным веществом с предполагаемым низким показателем ГЛБ, которое считается предпочтительным, является эмульсия симетикона, при этом указанная эмульсия симетикона недостаточно уточнена в WO 2014/086960 А1 в отношении показателя ГЛБ, который мог бы быть присущ ей. Из раскрытия WO 2014/086960 А1 также неясно, действительно ли указанная эмульсия симетикона должна рассматриваться как подпадающая под определение поверхностно-активного вещества с низким показателем ГЛБ в соответствии с WO 2014/086960 А1, в то время как в WO 2014/086960 А1 ясно указано, что добавление эмульсии симетикона полезно для подавления пенообразования.
Симетикон сам по себе представляет собой смесь α-(триметилсилил)-ω-метилполи[окси(диметилсилилена)] с диоксидом кремния, где соотношение этих двух соединений по меньшей мере в контексте WO 2014/086960 А1 не уточнено, и раскрытая эмульсия также не описана более конкретно.
Не указан растворитель или диспергирующее средство смеси α-(триметилсилил)-ω-метилполи[окси(диметилсилилена)] с диоксидом кремния для образования указанной эмульсии, также не указаны какие-либо дополнительные добавки к такой эмульсии для поддержания эмульсии. Это означает, что положительный эффект присутствия указанной эмульсии симетикона в составах согласно WO 2014/086960 А1 скорее связан с неизвестным поверхностно-активным веществом, необходимым для стабилизации эмульсии, чем с диоксидом кремния или α-(триметилсилил)-ω-метилполи[окси(диметилсилиленом)] самим по себе.
Следовательно, причина предпочтительного добавления симетикона (эмульсии) к составам, раскрытым в WO 2014/086960 А1, остается неясной, особенно принимая во внимание Примеры 9-14.
Специфические составы, раскрытые в WO 2014/086960 А1, которые также содержат поверхностно-активное вещество с показателем ГЛБ более 8 более конкретно представляют собой перечисленные далее.
Пример 4 описывает состав, состоящий из 3,5% толтразурила, 17,8% железа (в виде Глептоферрона), 0,3% сорбитан моноолеата, 10% простого моноэтилового эфира диэтиленгликоля, 0,1% сополимера Полиоксил 35 - гидрогенизированное касторовое масло и воды - до 100%.
Пример 5 описывает состав, состоящий из 3,5% толтразурила, 19,4% железа (в виде Глептоферрона), 0,3% сорбитан моноолеата, 0,1% сополимера Полиоксил 35 - гидрогенизированное касторовое масло и воды - до 100%.
Пример 7 описывает состав, состоящий из 3,5% толтразурила, 19,3% железа (в виде Глептоферрона), 0,3% пропиленгликоля монолаурата, 0,1% сополимера Полиоксил 35 - гидрогенизированное касторовое масло, 1% хлорида натрия и воды - до 100%.
Пример 8 описывает состав, состоящий из 3,5% толтразурила, 19,4% железа (в виде Глептоферрона), 0,3% сорбитан моноолеата, 0,1% сополимера Полиоксил 35 - гидрогенизированное касторовое масло и воды - до 100%.
Пример 9 описывает состав, состоящий из 4,2% толтразурила, 13,5% железа (в виде Глептоферрона), 0,1% докузата натрия, 0,1% силиконовой эмульсии, 1,5% хлорида натрия и воды - до 100%.
Пример 10 описывает состав, состоящий из 4,2% толтразурила, 13,5% железа (в виде Глептоферрона), 0,1% докузата натрия, 5% простого моноэтилового эфира диэтиленгликоля, 0,1% силиконовой эмульсии, 1% хлорида натрия и воды - до 100%.
Пример 11 описывает состав, состоящий из 4,2% толтразурила, 13,5% железа (в виде Глептоферрона), 0,6% фенола, 0,2% докузата натрия, 0,1% эмульсии симетикона USP 30%, 0,5% коллоидного диоксида кремния, 1% повидона, 0,5% хлорида натрия и воды - до 100%.
Пример 12 описывает состав, состоящий из 4,2% толтразурила, 13,5% железа (в виде Глептоферрона), 0,6% фенола, 0,2% докузата натрия, 0,1% эмульсии симетикона USP 30%, 0,5% коллоидного диоксида кремния, 1% повидона, 1% хлорида натрия и воды - до 100%.
Пример 13 описывает состав, состоящий из 4,2% толтразурила, 13,5% железа (в виде Глептоферрона), 0,6% фенола, 0,1% докузата натрия, 0,1% эмульсии симетикона USP 30%, 0,5% коллоидного диоксида кремния, 1% повидона, 1% хлорида натрия и воды - до 100%.
Пример 14 описывает состав, состоящий из 2,9% толтразурила, 18,8% железа (в виде Глептоферрона), 0,6% фенола, 0,1% докузата натрия, 0,1% эмульсии симетикона USP 30%, 0,5% коллоидного диоксида кремния, 1% повидона, 1% хлорида натрия и воды - до 100%.
Три явно упомянутые состава, приведенные на стр. 18 в WO 2014/086960 А1, состоят из 2,9% толтразурила, 18,8% железа (в виде Глептоферрона), 0,3% сорбитан моноолеата, 0,1% сополимера 15 Полиоксил 35 - гидрогенизированное касторовое масло, 1,5% хлорида натрия и воды, или 4,2% толтразурила, 13,5% железа (в виде Глептоферрона), 0,3% сорбитан моноолеата, 0,1% сополимера Полиоксил 35 - гидрогенизированное касторовое масло, 1,5% хлорида натрия и воды, или 4,2% толтразурила, 13,5% железа (в виде Глептоферрона), 1% хлорида натрия, 1% поливинилпирролидона, 0,6% фенола, 0,5% коллоидного диоксида кремния, 0,1% докузата натрия, 0,1% эмульсии симетикона и воды.
В WO 2014/086960 А1 в общем раскрывается, что любой из описанных составов подходит для лечения животных от кокцидиоза, но не раскрывается, что проводится одновременное лечение кокцидиоза и анемии, и в отношении тех специфических составов, упомянутых в Примерах 4, 5, 7, 8, 9 14 и на стр. 18, не раскрывается, что они могут быть особенно подходящими для цели этого одновременного лечения.
Исходя из вышеупомянутого уровня техники было решено несколько проблем, связанных с задачей обеспечения подходящих вариантов одновременного лечения кокцидиоза и анемии.
Более конкретно, проблема обеспечения синергизма между триазиноновым соединением и комплексным соединением железа была обнаружена и решена в ЕР 2164496 А1, а проблема пенообразования была обнаружена и решена в WO 2014/086960 А1 посредством добавления поверхностно-активных веществ с показателем ГЛБ ниже 8 к комбинации триазинона и комплексного соединения железа.
Исходя из этого, неожиданно было обнаружено, что полезные эффекты, обнаруженные в ЕР 2164496 А1, могут быть дополнительно улучшены путем выбора соответствующих поверхностно-активных веществ, которые способствуют синергизму между определенными триазиноновыми соединениями и определенными комплексными соединениями железа (III).
Соответственно, согласно первому аспекту настоящее изобретение относится к составу для применения для одновременного лечения кокцидиальных инфекций и железо дефицитных анемий у отличных от человека животных, где состав содержит толтразурил или диклазурил, многоядерное комплексное соединение железо (III)-полисахарид и по меньшей мере одно поверхностно-активное вещество, имеющее показатель ГЛБ, равный 10 или более.
Ни в одном из раскрытых ссылочных источников предшествующего уровня техники не раскрывается, что добавление по меньшей мере одного поверхностно-активного вещества, имеющего показатель ГЛБ, равный 10 или более, может благоприятно влиять на эффективность какого-либо из активных ингредиентов таких составов.
Вышеупомянутые лечения анемии и кокцидиоза предпочтительно объединить в одно лечение. Это снижает стресс у животных, улучшает их благополучие и снижает затраты на уход и затраты на персонал на коммерческих фермах, обеспечивая экономическое преимущество. Наконец, как впервые было доказано в ЕР 2164496 А1, такая комбинация приводит к улучшенному набору веса у животных, получавших лечение.
Еще одним преимуществом является то, что в соответствии с настоящим изобретением может быть еще более уменьшено воздействие активных веществ и их метаболитов на животных и окружающую среду, то есть путем снижения дозы без потери эффективности.
Согласно второму аспекту настоящее изобретение относится к составу для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, где состав содержит толтразурил или диклазурил, многоядерное комплексное соединение железо (III)-полисахарид и по меньшей мере одно поверхностно-активное вещество, имеющее показатель ГЛБ, равный 10 или более, за исключением составов, которые раскрыты в Примерах 4, 5, 7 и 8 в WO 2014/086960 А1.
Согласно указанному второму аспекту настоящего изобретения предпочтительными являются составы для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, где состав содержит толтразурил или диклазурил, многоядерное комплексное соединение железо (III)-полисахарид и по меньшей мере одно поверхностно-активное вещество, имеющее показатель ГЛБ, равный 10 или более, за исключением составов, содержащих сополимер Полиоксил 35 - гидрогенизированное касторовое масло в качестве поверхностно-активного вещества, когда применяется толтразурил.
Согласно третьему аспекту настоящее изобретение относится к составу для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, где состав содержит толтразурил или диклазурил, многоядерное комплексное соединение железо (III)-полисахарид и по меньшей мере одно поверхностно-активное вещество, имеющее показатель ГЛБ, равный 10 или более, за исключением составов, которые раскрыты в Примерах 9-14 в WO 2014/086960 А1.
Согласно указанному третьему аспекту настоящего изобретения предпочтительными являются составы для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, где состав содержит толтразурил или диклазурил, многоядерное комплексное соединение железо (III)-полисахарид и по меньшей мере одно поверхностно-активное вещество, имеющее показатель ГЛБ, равный 10 или более, за исключением составов, содержащих докузат натрия в качестве поверхностно-активного вещества, когда применяется толтразурил.
Согласно четвертому аспекту настоящее изобретение относится к составу для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, где состав содержит толтразурил или диклазурил, многоядерное комплексное соединение железо (III)-полисахарид и по меньшей мере одно поверхностно-активное вещество, имеющее показатель ГЛБ, равный 10 или более, за исключением составов, которые раскрыты в Примерах 4, 5, 7, 8, 9-14 в WO 2014/086960 А1, а также составов, указанных на стр. 18 в WO 2014/086960 А1.
Как указано выше, исключенные таким образом составы, раскрытые в WO 2014/086960 А1, необоснованным образом содержат поверхностно-активные вещества с показателем ГЛБ, равным 10 или более, хотя на самом деле, заявлено достижение подавления пенообразования посредством поверхностно-активных веществ, имеющих показатель ГЛБ ниже 8.
Согласно любому из вышеуказанных аспектов настоящего изобретения предпочтительными являются составы для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, где состав содержит толтразурил или диклазурил, многоядерное комплексное соединение железо (III)-полисахарид и по меньшей мере одно поверхностно-активное вещество, имеющее показатель ГЛБ, равный 10 или более, за исключением также состава, состоящего из 5% толтразурила, 22,8% железа в форме Fe(III)-декстран, 0,2% пропионата натрия, 0,2% бензоата натрия, 0,25% докузата натрия, 0,05% эмульсии симетикона USP 30%, 10,5% пропиленгликоля, 1,03% лимонной кислоты, 0,15% бентонита и воды - до 100%.
Однако в контексте настоящего изобретения было обнаружено, что благодаря добавлению указанного поверхностно-активного вещества с показателем ГЛБ, равным 10 или более, любая доза, в частности толтразурила (или диклазурила), может быть снижена благодаря двойному синергизму между толтразурилом (или диклазурилом) и многоядерным комплексным соединением железо (III)-полисахарид, а также между ними и поверхностно-активным веществом с показателем ГЛБ, равным 10 или более.
Неожиданно было обнаружено, что фармакокинетические параметры, такие как площадь под кривой (AUC) и Cmax, увеличивались, когда толтразурил (или диклазурил) вводили крысам вместе с поверхностно-активными веществами с показателем ГЛБ, равным 10 или более. Указанный эффект на AUC и Cmax также обнаруживается при совместном введении толтразурила (или диклазурила) с многоядерным комплексным соединением железо (III)-полисахарид, таким как железо-декстран или железо-декстран-глюкогептонат.
Очень неожиданно, что неизвестное преимущество добавления поверхностно-активного вещества с показателем ГЛБ, равным 10 или более, существенным образом добавляется к эффекту на AUC и Cmax, обнаруживаемому при комбинировании введения указанного поверхностно-активного вещества с совместным введением толтразурила или диклазурила и многоядерного комплексного соединения железо (III)-полисахарид у свиней.
Это является преимуществом, поскольку демонстрирует резко увеличенную биодоступность для этих комбинированных составов по сравнению с простым толтразурилом (или диклазурилом) или комбинированными составами толтразурила (или диклазурила) и многоядерного комплексного соединения железо (III)-полисахарид.
Как следствие, возможно снижение дозы по сравнению с имеющимися в продаже коммерчески доступными или раскрытыми толтразурилом (или диклазурилом) или комбинированными составами толтразурила (или диклазурила) и многоядерного комплексного соединения железо (III)-полисахарид.
Указанное преимущество не зависит от пути введения. Можно показать, что парентеральное, особенно инъекционное, и пероральное введение в соответствии с настоящим изобретением дает одно и то же преимущество.
В контексте настоящего изобретения показатель ГЛБ определяют либо согласно способу Девиса (Davies JT (1957), "A quantitative kinetic theory of emulsion type, I. Physical chemistry of the emulsifying agent", Gas/Liquid and Liquid/Liquid Interface, Proceedings of the International Congress of Surface Activity, pp.426 38), либо согласно способу Гриффина (Griffin WC (1954),"Calculation of HLB values of non-ionic surfactants", Journal of the Society of Cosmetic Chemists, pp. 249-56).
В обоих способах показатель гидрофильно-липофильного баланса коррелируют с химической природой молекулы на основе полуэмпирических уравнений, которые показывают корреляцию между количеством гидрофобных частей молекулы по сравнению с количеством гидрофильных частей указанной молекулы, которая рассматривается как поверхностно-активное вещество.
Оба способа приводят к похожим, но не идентичным показателям ГЛБ в отношении неионных поверхностно-активных веществ. Обычно для неионных поверхностно-активных веществ чаще указывают показатель ГЛБ по Гриффину.
Следовательно, в контексте настоящего изобретения, относящегося к добавлению поверхностно-активного вещества с показателем ГЛБ≥10, отклонения полученного показателя ГЛБ между формулами Девиса и Гриффина не являются существенными, поскольку они обычно не дают расхождений, превышающих отклонение более ±1 при применении к неионным поверхностно-активным веществам.
Другим классом поверхностно-активных веществ являются фосфолипиды. В рамках указанного класса отдельного рассмотрения требуют фосфатидилхолины, которые являются так называемыми цвиттер-ионными поверхностно-активными веществами. Соответствующий показатель ГЛБ существенно зависит от их фактического состава и степени чистоты. В качестве примера, неочищенный соевый лецитин имеет показатель ГЛБ, равный 3, а очищенный соевый фосфатидилхолин имеет показатель ГЛБ, равный приблизительно 7 (см. Gunstone FD, "Lipid Technologies and Applications" (1997) p. 62, Table 10).
Очевидно, что их соответствующие показатели ГЛБ получены скорее эмпирическим путем, чем рассчитаны по любой из указанных выше формул.
Соответственно, любой показатель ГЛБ, упомянутый в контексте настоящего изобретения, может быть получен либо по Девису, либо по Гриффину, либо определен иным образом, и значение, таким образом, должно пониматься как указанное значение ±1. В любом случае показатель ГЛБ, относящийся к настоящему изобретению, должен быть рабочим, не перекрываться с теми, которые указаны в WO 2014/086960 А1, быть указан только для расчета по Девису и быть релевантным для подавления чрезмерного пенообразования.
Согласно настоящему изобретению по меньшей мере одно поверхностно-активное вещество с показателем гидрофильно-липофильного баланса ≥10 («поверхностно-активное вещество с высоким показателем ГЛБ») предпочтительно имеет показатель ГЛБ от ≥10 до ≤18, более предпочтительно от ≥10 до ≤16,7.
Предпочтительные поверхностно-активные вещества с показателем ГЛБ≥10 представляют собой поверхностно-активные вещества, выбранные из перечня, состоящего из докузата натрия (ГЛБ 10), полисорбатов, сополимера Полиоксил 35 гидрогенизированное касторовое масло (ГЛБ 12-14), Плюроника F-68 (ГЛБ 29) и Витамина Е TPGS (ГЛБ 13,2).
Среди полисорбатов предпочтительными являются Полисорбат 20 (ГЛБ 16,7) и Полисорбат 80 (ГЛБ 15).
Более предпочтительно поверхностно-активные вещества с показателем ГЛБ≥10 представляют собой поверхностно-активные вещества, выбранные из перечня, состоящего из докузата натрия, Полисорбата 20 и Полисорбата 80.
Даже более предпочтительно поверхностно-активные вещества с показателем ГЛБ≥10 представляют собой поверхностно-активные вещества, выбранные из перечня, состоящего из Полисорбата 20 и Полисорбата 80.
Согласно другому предпочтительному варианту осуществления всех вышеуказанных аспектов настоящего изобретения в составе присутствует более чем одно поверхностно-активное вещество с показателем ГЛБ≥10.
В рамках указанного другого предпочтительного варианта осуществления по меньшей мере два поверхностно-активных вещества с показателем ГЛБ≥10 присутствуют в составе, причем среди этих по меньшей мере двух поверхностно-активных веществ двумя предпочтительно являются Полисорбат 20 (ГЛБ 16,7) и Полисорбат 80 (ГЛБ 15).
В контексте настоящего изобретения многоядерные комплексные соединения железо (III)-полисахарид понимают как означающие комплексы иона железа (3+) с гидроксид-ионами, (ОН-), группами воды (Н2О) и кислородом (О), которые присутствуют в олигомерной или полимерной форме и являются ассоциированными в их координационной сфере в форме комплексов с одним или несколькими из указанных олигомерных и полимерных углеводных соединений. По этой причине эти соединения также называют железа (III) гидроксид-полисахаридами или железа (III) оксигидрокси-полисахаридами, причем «полисахарид» означает соответствующие олигомерные или полимерные углеводные соединения или их производные.
Многоядерные комплексы железа (III) этого типа описаны, например, в (D.S. Kudasheva et al., "Structure of Carbohydrate-bound Polynuclear Oxyhydroxide Nanoparticles in Parenteral Formulation", J. Inorg. Biochem. 98 (2004) 1757-1769; I. Erni et al "Chemical Characterization of Iron(III) Hydroxide-Dextrin Complexes" Arzneim.-Forsch./Drug Res. 34 (II) (1984) 1555-1559; F. Funk et al., "Physical and Chemical Characterization of Therapeutic Iron Containing Materials", Hyperfine Interactions 136 (2001) 73-95; E. London "The Molecular Formula and Proposed Structure of the Iron-Dextran Complex, IMFERON", J. Pharm. Sci. 93 (2004) 1838-1846; A. John "Neue 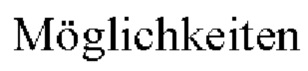 der Eisenversorgung neugeborener Ferkel unter Beachtung biochemischer Aspekte" [Novel possibilities of supplying iron to new born piglets, taking account of biochemical aspects], Trachtigkeit und Geburt beim Schwein [Pregnancy and birth in pigs]: 8th Bernburger Biotechnology Workshop, Bernburg (2002) 89-94).
der Eisenversorgung neugeborener Ferkel unter Beachtung biochemischer Aspekte" [Novel possibilities of supplying iron to new born piglets, taking account of biochemical aspects], Trachtigkeit und Geburt beim Schwein [Pregnancy and birth in pigs]: 8th Bernburger Biotechnology Workshop, Bernburg (2002) 89-94).
Поскольку состав этих соединений во многих случаях не описан количественно, а также может варьировать в пределах соединений в зависимости от типа получения, под этими многоядерными комплексными соединениями железо (III)-полисахарид следует понимать все комплексы описанных выше классов соединений, которые известны специалисту в данной области техники.
Примерами многоядерных комплексных соединений железо (III)-полисахарид, которые можно упомянуть, являются многоядерные комплексные соединения железо (III)-полисахарид, в которых многоядерный β-FeO(OH) ядерный комплекс содержит полимерные углеводные соединения, ассоциированные при свободных координационных сайтах, например, Глептоферрон, железо (III)-декстран, железа (III) гидрокси-полимальтоза (железо (III)-декстрин), нестехиометрические соединения β-FeO(OH) с сахаридами и олигосахаридами «железо(III)-сахароза» и «железо(III)-«сахар»».
Применяемые составы согласно настоящему изобретению могут представлять собой раствор, эмульсию или суспензию.
Растворы получают посредством растворения активного ингредиента или активных ингредиентов в подходящих растворителях или смесях растворителей. При необходимости добавляют дополнительные вспомогательные вещества, такие как солюбилизаторы, антиоксиданты, консерванты, загустители, адгезивы, вещества, регулирующие рН, УФ-стабилизаторы или красители.
В качестве растворителей можно упомянуть физиологические приемлемые растворители, такие как вода, спирты, такие как, например, одноатомные алканолы (например, этанол или н-бутанол), многоатомные спирты, такие как гликоли (например, этиленгликоль, пропиленгликоль, тетрагликоль/гликофурол), полиэтиленгликоли, полипропиленгликоли, глицерин, ароматически замещенные спирты, такие как бензиловый спирт, фенилэтанол, феноксиэтанол, сложные эфиры, такие как этилацетат, бутилацетат, бензилбензоат, этилолеат, простые эфиры, такие как алкиловые простые эфиры алкиленгликоля (например, монометиловый простой эфир дипропиленгликоля, монобутиловый простой эфир диэтиленгликоля), кетоны, такие как ацетон, метил-этил-кетон, ароматические и/или алифатические углеводороды, растительные или синтетические масла, глицеринформаль, солкеталь (2,2-диметил-4-гидроксиметил-1,3-диоксолан), N-метилрпирролидон, 2-пирролидон, N,N-диметилацетамид, гликофурол, диметилизосорбит, лаурогликоль, пропиленкарбонат, октилдодеканол, диметилформамид, а также смеси указанных растворителей.
Вода является предпочтительной в качестве растворителя и/или суспензионной среды.
В качестве солюбилизаторов можно упомянуть средства, которые способствуют растворению активного ингредиента в основном растворителе или которые препятствуют его выпадению в осадок. Примерами средств, которые препятствуют выпадению осадка, являются поливинилпирролидоны.
К антиоксидантам относятся сульфиты или метабисульфиты, такие как метабисульфит калия или метабисульфит натрия, дисульфит калия или дисульфит натрия, аскорбиновая кислота, изоаскорбиновая кислота, пальмитат аскорбиновой кислоты, сложные эфиры галловой кислоты, бутилгидрокситолуол, бутилгидроксианизол или токоферолы.
Синергетиками этих антиоксидантов могут быть аминокислоты (например, аланин, аргинин, метионин, цистеин), лимонная кислота, винная кислота, эдетовая кислота или их соли, производные фосфорной кислоты или полиспирты (полиэтиленгликоль).
Консервантами могут быть бензиловый спирт, бензалкония хлорид, трихлорбутанол, пара-гидроксибензоат, н-бутанол, хлоркрезол, крезол, фенол, бензойная кислота, лимонная кислота, винная кислота или сорбиновая кислота.
Загустителями могут быть неорганические загустители, такие как бетониты, коллоидный диоксид кремния, стеараты алюминия, органические загустители, такие как производные целлюлозы, например, гидроксипропилметилцеллюлоза 4000, поливиниловые спирты и их сополимеры, ксантан, акрилаты и метакрилаты, карбоксиметилцеллюлоза и ее соли.
Адгезивы представляют собой, например, производные целлюлозы, производные крахмала, полиакрилаты, природные полимеры, такие как альгинаты, желатин.
Адгезивы, которые также обладают свойствами загустителей, можно равным образом применять в качестве загустителей.
Вещества, регулирующие рН, представляют собой обычно используемые в фармацевтической области кислоты или основания. К основаниям относятся гидроксиды щелочных металлов или гидроксиды щелочноземельных металлов (например, NaOH, KOH), основные соли, такие как, например, хлорид аммония, основные аминокислоты, такие как, например, аргинин, холин, меглумин, этаноламины, или также буферы, такие как трис(гидроксиметил)аминометан, буферы на основе лимонной кислоты или фосфатные буферы. К кислотам относятся, например, соляная кислота, уксусная кислота, винная кислота, лимонная кислота, молочная кислота, янтарная кислота, адипиновая кислота, метансульфоновая кислота, октановая кислота, линоленовая кислота, глюконолактон, а также кислые аминокислоты, такие как, например, аспарагиновая кислота.
УФ-стабилизаторы представляют собой, например, вещества из класса бензофенонов или новантизоловую кислоту.
Красителями являются все допущенные к употреблению человеком или животными красители, которые можно растворять или суспендировать.
Суспензии получают, суспендируя активный ингредиент или активные ингредиенты в жидкости-носителе, при необходимости добавляя дополнительные вспомогательные вещества (в дополнение к указанным выше поверхностно-активным веществам), такие как смачивающие вещества, красители, вещества, способствующие всасыванию, загустители, диспергирующие средства, адгезивы, консерванты, антиоксиданты, УФ-стабилизаторы или пеногасители.
Составы, применяемые согласно настоящему изобретению, предпочтительно представляют собой составы «на основе воды».
Это означает, что, как правило, они содержат от ≥10 до 90 мас. %, предпочтительно от ≥20 до ≤80 мас. %, особенно предпочтительно от ≥30 до ≤50 мас. % воды.
Например, указанные выше составы могут содержать дополнительные смешивающиеся с водой растворители. Дополнительными смешивающимися с водой растворителями, которые можно указать в качестве примера, предпочтительно являются многоатомные алифатические спирты, такие как этиле нгликоль, диэтиленгликоль, триэтиленгликоль, пропиленгликоль и глицерин, причем среди них особенно предпочтительным является пропиленгликоль.
Такие дополнительные смешивающиеся с водой растворители обычно присутствуют при концентрациях от ≥1 до ≤45 мас. %, предпочтительно от ≥1 до ≤20 мас. %, особенно предпочтительно от ≥5 до ≤10 мас. %. Добавление таких многоатомных алифатических спиртов также имеет преимущество, состоящее в снижении температуры замерзания состава.
Составы, применяемые согласно настоящему изобретению, как указано выше, могут, кроме того, содержать консерванты, при необходимости, в сочетании с так называемыми синергистами. Консерванты обычно присутствуют при концентрациях от ≥0,01 до ≤5 мас. %, в частности от ≥0,05 до ≤1 мас. %.
Антиоксиданты, которые могут быть использованы при необходимости в указанных применяемых составах, представляют собой предпочтительно ВНА или ВНТ. Для обеспечения достаточного эффекта хранения консерванты можно использовать по отдельности или в комбинации с так называемыми синергистами. Синергисты, такие как лимонная кислота, винная кислота, аскорбиновая кислота или натриевая соль эдетовой кислоты, обычно присутствуют в концентрациях от ≥0,01 до ≤1 мас. %, в частности от ≥0,05 до ≤0,15 мас. %.
Составы, применяемые согласно настоящему изобретению, предпочтительно получают путем первоначально введения растворителя, предпочтительно воды, и предварительного растворения или диспергирования в нем соответствующих вспомогательных веществ и/или добавок, если они используются, как например, сорастворители, консерванты, антиоксиданты и добавки, регулирующие вязкость.
В предпочтительном способе вторая стадия предусматривает введение в этот исходный раствор толтразурила или диклазурила, необязательно в форме готового к применению концентрата дисперсии, с использованием мощного гомогенизатора и гомогенизации смеси до получения тонкодисперсной суспензии.
Затем в эту дисперсию вводят соединение железа, предпочтительно в форме порошка, в ходе чего смесь снова гомогенизируют. Наконец, на последней стадии устанавливают желаемое значение рН посредством добавления подходящих веществ, регулирующих рН. Отдельные или все вспомогательные вещества и/или добавки, если необходимо, также можно добавить после последней стадии гомогенизации, что может быть целесообразно, например, в случае некоторых загустителей, структура которых разрушается в процессе гомогенизации.
Как указано выше в отношении аспектов настоящего изобретения, составы согласно настоящему изобретению предназначены для применения в комбинированной борьбе с кокцидиями и железодефицитной анемией, в частности, у животных.
Указанное применение обеспечивает простое и одновременное введение противококцидиального толтразурила или диклазурила и железа.
Применение можно осуществлять в животноводстве и при разведении сельскохозяйственных животных, племенных животных, животных, содержащихся в зоопарках, лабораторных животных, подопытных животных, и домашних животных. Спектр действия толтразурила или диклазурил в принципе хорошо известен. Из кокцидий следует упомянуть отдельно:
Mastigophora (жгутиковые, Flagellata), как например, Trypanosomatidae, например, Trypanosoma brucei, Т. gambiense, Т. rhodesiense, Т. congolense, Т. cruzi, Т. evansi, Т. equinum, Т. lewisi, Т. percae, Т. simiae, Т. vivax, Leishmaniabrasiliensis, L. donovani, L. tropica, как например, Trichomonadidae, например, Giardia lamblia, G. canis.
Sarcomastigophora (Саркомастигофоры, Rhizopoda), как например, Entamoebidae, например, Entamoeba histolytica, Hartmanellidae, например, Acanthamoeba sp., Hartmanella sp.
Apicomplexa (споровики, Sporozoa), как например, Eimeridae, например, Eimeria ascervulina, E. adenoides, E. alabahmensis, E. anatis, E. anseris, E. arloingi, E. ashata, E. auburnensis, E. bovis, E. brunetti, E. canis, E. chinchillae, E. clupearum, E. columbae, E. contorta, E. crandalis, E. debliecki, E. dispersa, E. ellipsoidales, E. falciformis, E. faurei, E. flavescens, E. gallopavonis, E. hagani, E. intestinalis, E. iroquoina, E. irresidua, E. labbeana, E. leucarti, E. magna, E. maxima, E. media, E. meleagridis, E. meleagrimitis, E. mitis, E. necatrix, E. ninakohlyakimovae, E. ovis, E. parva, E. pavonis, E. perforans, E. phasani, E. piriformis, E. praecox, E. residua, E. scabra, E. spec., E. stiedai, E. suis, E. tenella, E. truncata, E. truttae, E. zuernii, Globidium spec., Isospora belli, I. canis, I. felis, I. ohioensis, I. rivolta, I. spec., I. suis, Neospora caninum, N. hugesi, Cystisospora spec., Cryptosporidium spec., как например, Toxoplasmadidae, например, Toxoplasma gondii, как например, Sarcocystidae, например, Sarcocystis bovicanis, S. bovihominis, S. neurona, S. ovicanis, S. ovifelis, S. spec., S. Suihominis, как например, Leucozoidae, например, Leucozytozoon simondi, как например, Plasmodiidae, например, Plasmodium berghei, P. falciparum, P. malariae, P. ovale, P. vivax, P. spec., как например, Piroplasmea, например, Babesia argentina, B. bovis, B. canis, B. spec., Theileria parva, Theileria spec., как например, Adeleina, например, Hepatozoon canis, H. spec.
Кроме того, Myxospora и Microspora, например, Glugea spec., Nosema spec.
Кроме того, Pneumocystis carinii, а также Ciliophora (Ciliata), как например, Balantidium coli, Ichthiophthirius spec., Trichodina spec., Epistylis spec.
Следует особо подчеркнуть те роды и виды простейших, которые вызывают у свиней инфекции с клиническими или субклиническими проявлениями, в частности: Eimeria debliecki, Е. suis, Е. scabra, Е. perminuta, Е. spinosa, Е. polita, Е. porci, Е. neodebliecki, Isospora suis, Cryptosporidium, Toxoplasma gondii, Sarcocystis miescheriana, S. suihominis, Babesia trautmanni, B. perroncitoi, Balantidium coli.
К сельскохозяйственным и племенным животным, для которых применение состава согласно настоящему изобретению является особенно предпочтительным, относятся млекопитающие, такие как, например, крупный рогатый скот, лошади, овцы, свиньи, козы, верблюды, азиатские буйволы, ослы, кролики, лани, северные олени, пушные звери, такие как, например, норки, шиншиллы, еноты, а также птицы, такие как, например, куры, гуси, индейки, утки, голуби, страусы и виды птиц для содержания дома и в зоопарке. Кроме того, к ним относятся промысловые и декоративные рыбы.
В этом контексте можно особенно выделить свиней, крупный рогатый скот, овец и собак всех видов, подвидов и пород.
Лабораторные и экспериментальные животные включают мышей, крыс, морских свинок, средних хомяков, собак и кошек. К домашним животным относятся собаки и кошки.
Применение у свиней является особенно предпочтительным.
Составы, применяемые согласно настоящему изобретению, могут содержать дополнительные активные ингредиенты или компоненты, по отдельности или в подходящих комбинациях, такие как, например, питательные вещества, которые включают, например, витамины, минеральные вещества и соединения фосфора, которые являются подходящими в качестве стимуляторов обмена веществ и иммуностимуляторов:
витамины, такие как, например, витамин Е, витамины группы В, такие как, например, витамин В12, витамин С, причем некоторые из вышеуказанных также могут действовать в качестве поверхностно-активных веществ;
минеральные вещества, предпочтительно, соли кальция или магния, в частности, например, глюконат кальция, глюкогептаноат кальция или сахарат кальция;
соединения фосфора, в частности фармакологически приемлемые органические производные фосфоновой кислоты, подходящие для применения в качестве стимуляторов обмена веществ и тонизирующих средств, причем из предпочтительных примеров можно упомянуть уже широко известные в течение длительного времени соединения толдимфос, в частности бутафосфан.
В результате плохой растворимости толтразурила или диклазурила они часто присутствуют в составах, применяемых согласно настоящему изобретению, в тонко измельченной форме.
В контексте настоящего изобретения диспергированный толтразурил или диклазурил предпочтительно имеет размер частиц (измеренный с помощью лазерной дифракции, Malvern Mastersizer® 2000) d(v, 90) <30 мкм, предпочтительно d(v, 90) <20 мкм, особенно предпочтительно d(v, 90) <10 мкм и особенно предпочтительно d (v, 90) 7 мкм или менее.
В контексте настоящего изобретения под d(v,90) понимают распределение частиц по размеру относительно объема, при котором 90% всех частиц имеют размер (диаметр), равный этому значению или меньше. Обычно эту величину обозначают как d(90), однако, чтобы подчеркнуть, что это распределение отнесено к объему, можно использовать более точное обозначение d(v,90). Соответственным образом следует понимать обозначения d(v,50), d(v,10) и т.д. Указанные в настоящем документе размеры частиц были определены методом лазерной дифракции на приборе Mastersizer 2000 (блок диспергирования Hydro 2000G) производства фирмы Malvern, с использованием способа оценки на основе дифракция Фраунгофера, поскольку коэффициенты преломления частиц действующего вещества неизвестны. При этом подходящее количество раствора образца предварительно диспергируют при перемешивании в 2-3 мл среды диспергирования (0,1% водный раствор диоктилнатрия сульфосукцината). Затем дисперсию вводят в блок диспергирования устройства, при перемешивании (300 об./мин.) и рециркулировании (900 об./мин.), где проводят измерение. Программное обеспечение выдает результат в виде размера частиц как d(0,5), d(0,9) и т.д.
Согласно предпочтительному варианту выполнения настоящего изобретения состав предназначен для применения при режиме дозирования от 1 до 60 мг толтразурила или диклазурила на кг массы тела (мг/кг) животного, подлежащего лечению, в день.
Согласно указанному предпочтительному варианту осуществления режим дозирования предпочтительно представляет собой от 10 до 40 мг толтразурила или диклазурила на кг массы тела (мг/кг) животного, более предпочтительно от 10 до 20 мг/кг в день, наиболее предпочтительно приблизительно 20 мг/кг в день.
Согласно наиболее предпочтительному варианту осуществления вышеуказанный режим дозирования применяют только один раз.
Согласно другому предпочтительному варианту осуществления настоящего изобретения состав предназначен для применения при режиме дозирования от 100 до 300 мг многоядерного комплексного соединения железо (III)-полисахарид.
Согласно указанному предпочтительному варианту осуществления режим дозирования предпочтительно составляет от 150 до 250 г многоядерного комплексного соединения железо (III)-полисахарид на кг массы тела (мг/кг) животного, более предпочтительно приблизительно 200 мг/кг в день.
Поскольку настоящее изобретение, в частности, относится к комбинированному применению вышеуказанных толтразурила или диклазурила и многоядерного комплексного соединения железо (III)-полисахарид, любые режимы дозирования, отдельно указанные непосредственно выше, предпочтительно комбинируются, причем особенно предпочтительным является режим дозирования приблизительно 20 мг/кг в день толтразурила или диклазурила и приблизительно 200 мг/кг в день многоядерного комплексного соединения железо (III)-полисахарид.
Согласно очень предпочтительному варианту осуществления состав предназначен для применения при режиме дозирования приблизительно 20 мг/кг в день толтразурила или диклазурила и приблизительно 200 мг/кг в день многоядерного комплексного соединения железо (III)-полисахарид, при этом применение осуществляют только в один день. Согласно указанному особенно предпочтительному варианту осуществления особенно предпочтительным является применение надень 2 или 3, предпочтительно надень 3 жизни животного, которым предпочтительно является поросенок.
Количество применяемого состава на введение зависит от того, насколько много толтразурила или диклазурила и многоядерного комплексного соединения железо (III)-полисахарид должно быть введено в каждом случае.
Одной из задач являются относительно небольшие объемы, которые можно легко применять и которые варьируются в зависимости от вида животных, для поросят на подсосе, например, стремятся к объемам применения от ≥0,3 до ≤2 мл, предпочтительно от ≥0,5 до ≤1 мл.
Особенно предпочтительные составы согласно настоящему изобретению позволяют парентерально обрабатывать поросят таким образом, чтобы могло быть достигнуто достаточное обеспечение поросят железом в первые четыре недели жизни при однократном введении от ≥0,7 мл до ≤1,3 мл, предпочтительно от ≥0,7 до ≤1,0 мл состава, даже на третий день после рождения, где уровень гемоглобина не менее ≥8 г/100 мл крови, предпочтительно более ≥9 г/100 мл крови, можно считать индикатором достаточного обеспечения. Кроме того, часть толтразурила или диклазурила предназначена для успешной борьбы с кокцидиями.
Согласно другому варианту осуществления применяемый состав содержит от ≥0,1% (мас/об) до ≤30% (мас/об) толтразурила или диклазурила. Это соответствует от ≥1 до ≤300 мг/мл. Предпочтительными являются содержания от ≥1,5 до ≤25% (мас/об), что соответствует от ≥15 до ≤250 мг/мл, особенно предпочтительно от ≥1,8 до ≤15% (мас/об), что соответствует от ≥18 до ≤150 мг/мл, в частности от ≥1,8 до ≤7% (мас/об), что соответствует от ≥18,5 до ≤70 мг толтразурила или диклазурила в 1 мл.
Согласно другому варианту осуществления применяемый состав содержит от ≥10% (мас/об) до ≤30% (мас/об) активного железа.
Вышеуказанные значения соответствуют от 100 до 300 мг активного железа в 1 мл. Предпочтительными являются значения от ≥11,4% (мас/об) до ≤25% (мас/об), что соответствует от ≥114 мг до ≤250 мг активного железа в 1 мл, особенно предпочтительно от ≥20% (мас/об) до ≤25% (мас/об), что соответствует от ≥200 мг до ≤250 мг активного железа в 1 мл состава.
Согласно другому варианту осуществления применяемый состав содержит от ≥0,01% (мас/об) до ≤10% (мас/об) по меньшей мере одного поверхностно-активного вещества с показателем ГЛБ ≥10.
Согласно другому варианту осуществления многоядерное комплексное соединение железо (III)-полисахарид представляет собой железо(III)-декстран-глюкогептонат или железо (III)-декстран, предпочтительно железо (III)-декстран-глюкогептонат.
Согласно особенно предпочтительному варианту осуществления настоящего изобретения состав для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных состоит из толтразурила, железа (III) в форме железо (III)-декстран-глюкогептонат, фенола, по меньшей мере одного поверхностно-активного вещества, выбранного из перечня, состоящего из полисорбатов и докузата натрия, эмульсии симетикона, хлорида натрия, воды и необязательно коллоидного диоксида кремния, а также необязательно поливинилпирролидона.
Среди указанных предпочтительных вариантов осуществления один особенно предпочтительный состав для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных состоит из от 3 до 5 г/100 мл толтразурила, от 10 до 20 г/100 мл железа (III) в форме железо (III)-декстран-глюкогептонат, от 0,3 до 0,8 г/100 мл фенола, либо от 0,05 до 0,2 г/100 мл докузата натрия, либо от 0,15 до 0,3 г/100 мл полисорбатов, где указанные полисорбаты представляют собой смесь от 0,1 до 0,2 г/100 мл Полисорбата 20 и от 0,05 до 0,1 г/100 мл Полисорбата 80, от 0,05 до 0,1 г/100 мл эмульсии симетикона, от 0,8 до 1,1 г/100 мл хлорида натрия, необязательно приблизительно 0,5 г/100 мл коллоидного диоксида кремния, необязательно приблизительно 1 г/100 мл поливинилпирролидона, и воды.
Даже более предпочтительным является состав для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, состоящий из приблизительно 5 г/100 мл толтразурила, от 15 до 20 г/100 мл железа (III) в форме железо (III)-декстран-глюкогептонат, приблизительно 0,5 г/100 мл фенола, от 0,1 до 0,2 г/100 мл Полисорбата 20 и от 0,05 до 0,1 г/100 мл Полисорбата 80, приблизительно 0,05 г/100 мл эмульсии симетикона, приблизительно 0,9 г/100 мл хлорида натрия и воды, а также состав для применения для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, состоящий из приблизительно 3 г/100 мл толтразурила, от 10 до 15 г/100 мл железа (III) в форме железо (III)-декстран-глюкогептонат, от 0,6 до 0,7 г/100 мл фенола, от 0,05 до 0,2 г/100 мл докузата натрия, приблизительно 0,1 г/100 мл эмульсии симетикона, приблизительно 1 г/100 мл хлорида натрия, приблизительно 0,5 г/100 мл коллоидного диоксида кремния, приблизительно 1 г/100 мл поливинилпирролидона и воды.
В рамках упомянутых выше особенно предпочтительных вариантов осуществления отличное от человека животное предпочтительно представляет собой поросенка в возрасте от новорожденного до 96 часов после рождения, даже более предпочтительно поросенка в возрасте от 24 часов до 72 часов или от 24 часов до 96 часов после рождения, а кокцидиоз вызван Cystoisospora suis.
Согласно другому варианту осуществления применяемый состав содержит молярное соотношение Са2+ и Na+ от ≥0 до ≤3, более предпочтительно от ≥0 до ≤1.
Согласно другому варианту осуществления применяемый состав имеет общее содержание CaCl2 и NaCl от ≥0,1% (мас/об) до ≤5% (мас/об). Предпочтительное общее содержание составляет от ≥0,5% (мас/об) до ≤4% (мас/об), более предпочтительно от ≥0,9% (мас/об) до ≤3% (мас/об).
Неожиданно было обнаружено, что присутствие NaCl и CaCl2 в количествах, указанных в двух предшествующих вариантах осуществления, увеличивает стабильность состава с течением времени.
Согласно другому варианту осуществления состав имеет содержание свободного железа ≤3500 частей на миллион, предпочтительно ≤2000 частей на миллион и более предпочтительно ≤1000 частей на миллион.
Количественное определение растворенных ионов железа может быть достигнуто, например, посредством диализа образца с последующим определением диализированного свободного железа с помощью атомно-абсорбционной спектроскопии (ААС) или любого другого подходящего способа, такого как полярография и фотометрия.
Согласно другому варианту осуществления состав, после хранения при температуре от ≥20°С до ≤40°С в течение 6 месяцев, имеет содержание растворенных свободных ионов железа ≤3500 частей на миллион, предпочтительно ≤2000 частей на миллион и более предпочтительно ≤1000 частей на миллион.
Более предпочтительно состав имеет эти содержания после хранения в течение 12 месяцев, даже более предпочтительно после хранения в течение 24 месяцев и наиболее предпочтительно после хранения в течение 36 месяцев. Например, состав, после хранения при температуре от ≥20°С до ≤40°С в течение 36 месяцев, может иметь содержание свободных ионов железа ≤3500 частей на миллион.
Измеренное содержание ионов железа в основном состоит из ионов железа из двух источников. Очевидно, что любые ионы железа, которые уже растворены в растворителе состава, являются частью свободного железа согласно настоящему изобретению.
Вторым источником свободного железа является любое железо, которое присутствует в виде свободного железа в форме небольших комплексных фрагментов, известных в литературе как лабильное железо. Другими словами, такое свободное железо более не связано стабильно в полисахар ид ном комплексе ни по своей природе, ни из-за того, что комплексное соединение полисахарида частично разложилось или иным образом нарушилось.
Эти комплексные фрагменты трансформируют в ионы Fe2+и/или Fe3+с помощью подходящих способов получения образцов и измеряют, как описано выше, вместе с ионами Fe2+ и Fe3+, которые изначально присутствуют в составах.
Следовательно, в объеме настоящего изобретения следует понимать, что содержание ионов железа, определенное с помощью AAS, полярографии или фотометрии, относится к содержанию ионов Fe2+ и/или Fe3+, свободно растворенных в составе, в дополнение к ионам, трансформированным в свободно растворенные ионы при получении образца, при этом ионы Fe2+ не являются непосредственно измеримыми, поскольку они в любом случае трансформируются в Fe3+ в ходе получения образца или другими активными средствами, что приводит к измеряемому свободному железу в форме свободно растворенных ионов Fe3+.
Термин «свободное» железо в контексте настоящего изобретения и измеряемое вышеупомянутыми способами, таким образом, включает все соединения железа, которые могут вызывать токсичность после введения за счет перегрузки железо-транспортной емкости транспортных белков, транспортирующих железо, упомянутых ранее.
Следовательно, любое количество свободного железа, измеренное одним из описанных выше способов, всегда идентично или превышает фактическое количество «свободного» железа в соответствии с функциональным определением, приведенным непосредственно выше, поскольку все способы измерения измеряют общее количество свободно растворенного железа и его нефункциональных комплексов, хотя только часть его может быть действительно вредной для субъекта, получающего его.
Вышеописанное «свободное» железо необходимо отделять от «активного железа». В контексте настоящего изобретения «активное железо» представляет собой количество железа, стабильно присутствующего в многоядерных комплексных соединениях железо (III)-полисахарид. Исходя из этого и в контексте настоящего изобретения активное железо не может представлять собой Fe2+, но должно представлять собой Fe3+.
Кроме того, если в контексте настоящего изобретения массовые проценты или соотношения раскрыты по отношению к указанному активному железу, такие количества всегда следует считать указанными без соответствующих количеств/масс агентов комплексообразования (т.е. полисахаридного комплекса)..
Поэтому в контексте настоящего изобретения любую ссылку на долю многоядерного комплексного соединения железо (III)-полисахарид, являющегося частью любого из применяемых составов, раскрытых в настоящем документе, следует понимать как количество фактического активного железа (III) в указанном составе, которое впоследствии превращается в многоядерное комплексное соединение железо (III)-полисахарид путем координации с полисахаридным комплексом. Таким образом, фактическое количество многоядерного комплексного соединения железо (III)-полисахарид в любом применяемом и раскрытом составе значительно превышает фактическое «активное железо».
Настоящее изобретение далее описано со ссылкой на следующие примеры, без ограничения ими.
Примеры
Получение составов, применяемых в Примерах 14
Составы толтразурила, применяемые в следующих примерах 1 4, получали путем взвешивания необходимого количества толтразурила в химическом стакане и растворения его приблизительно в половине количества основного растворителя.
Затем, если применимо, добавляли указанное количество сорастворителя этанола и поверхностно-активных веществ. Состав перемешивали до получения прозрачного раствора. Состав переносили в мерную колбу, доводили до температуры 20°С и заполняли основным растворителем до калибровочной отметки (необходимое количество до желаемого объема). Составы стерильно фильтровали во флаконы для инъекции и закрывали резиновыми пробками и гофрированными крышками.
Перечень применяемых поверхностно-активных веществ/диспергирующих средств.

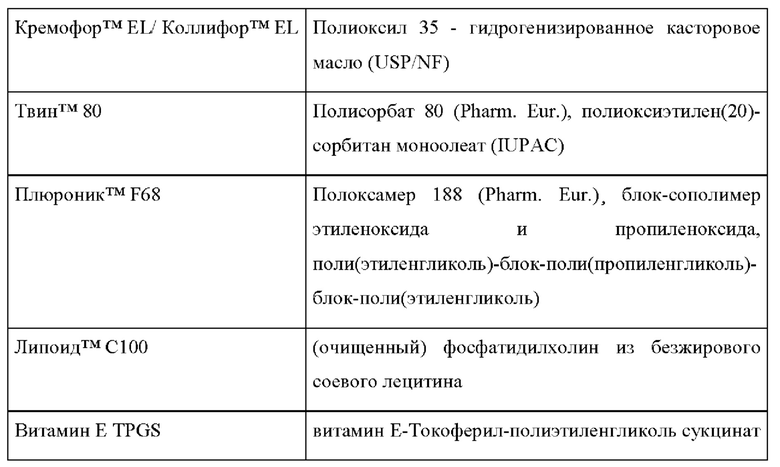
Введение составов, применяемых в Примерах 1-4, и оценка
Самкам крыс линии Вистар посредством подкожной инъекции вводили аликвоты составов по 1 мл/кг. Образцы крови собирали через разные интервалы времени, и образцы плазмы анализировали на концентрацию толтразурила в плазме. На основании этих данных определяли значения AUC и Cmax стандартными методами, известными клиницистам.
Пример 1
Составы толтразурила в растворителе диметилсульфоксид (DMSO) получали в соответствии с Таблицей 1, где композиции составов приведены в мас. % на объем (% мас/об). Содержание DMSO означает достаточное количество для доведения до 100. В Таблице 2 показаны фармакокинетические данные AUC и Cmax и изменение в % по сравнению с контрольным составом "ref", который не содержит поверхностно-активное вещество. [Необходимо отметить: "ч" = часы].

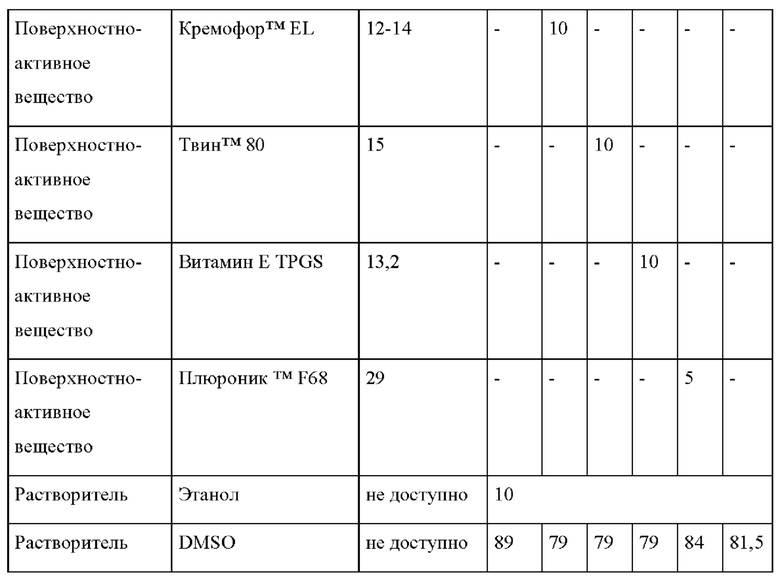
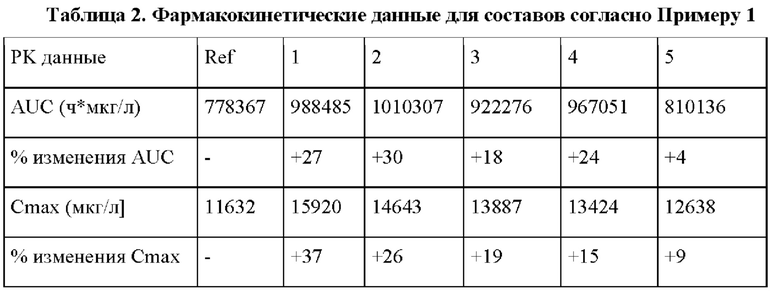
Приведенные выше данные ясно показывают положительный эффект добавления поверхностно-активных веществ с ГЛБ ≥10, в то время как эффект диспергирующего средства Коллидон™ 17PF, которое не является амфифильным соединением и, следовательно, по своей сути не имеет рассчитываемого показателя ГЛБ, является значительно меньшим.
Пример 2
Составы толтразурила в растворителе глицеринформаль (4-гидроксиметил-1,3-диоксолан) получали в соответствии с Таблицей 3, где композиции составов приведены в мас. % на объем (% мас/об). Содержание глицеринформаля означает достаточное количество для доведения до 100. В Таблице 4 приведены фармакокинетические данные AUC и Cmax и изменение в % по сравнению с контрольным составом "ref, который не содержит поверхностно-активное вещество. [Необходимо отметить: "ч" = часы].
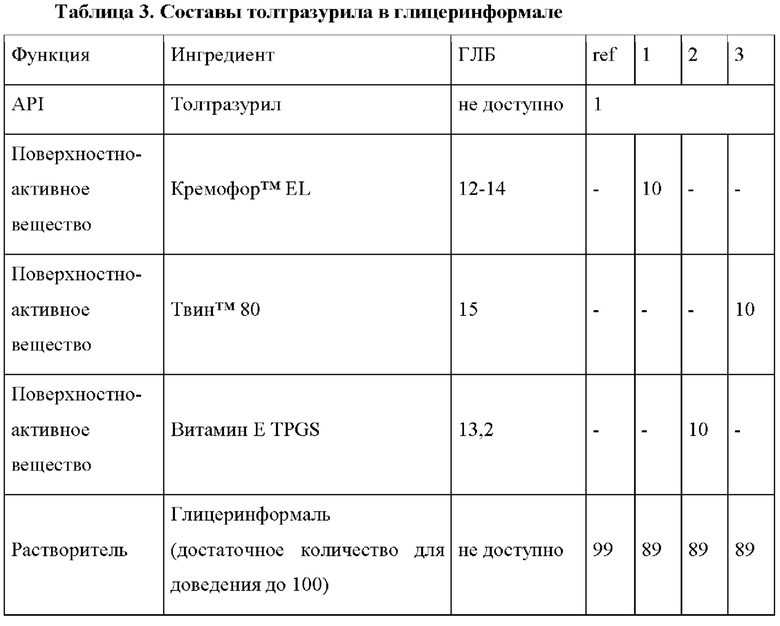

Приведенные выше данные ясно показывают положительный эффект добавления поверхностно-активных веществ с ГЛБ ≥10, который менее выражен в растворителе глицеринформаль, но все же является значительным.
Пример 3 (Сравнительный пример)
Составы толтразурила в растворителе глицеринформаль (4-гидроксиметил-1,3-диоксолан) и 10% этанола получали в соответствии с Таблицей 5, где композиции составов приведены в мас. % на объем (% мас/об). Содержание глицеринформаля и 10% этанола означает достаточное количество для доведения до 100. В Таблице 6 показаны фармакокинетические данные AUC и Cmax и изменение в % по сравнению с контрольным составом "ref", который не содержит поверхностно-активное вещество. [Необходимо отметить: "ч" = часы].
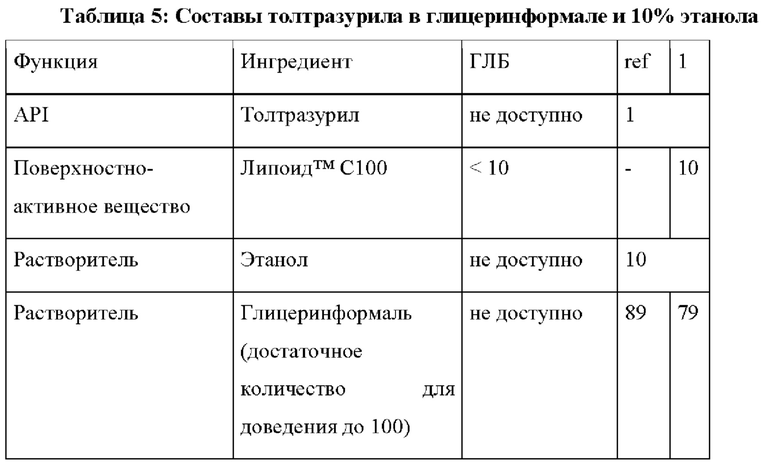

Приведенные выше данные показывают, что добавление поверхностно-активного вещества Липоид С100, имеющего ГЛБ ≤10, отрицательно влияет на фармакокинетические параметры.
Пример 4
Составы толтразурила в растворителе 2-пирролидон и 20% этанола получали в соответствии с Таблицей 7, где композиции составов приведены в мас. % на объем (% мас/об). Содержание 2-пирролидона и 20% этанола означает достаточное количество для доведения до 100. В Таблице 8 приведены фармакокинетические данные AUC и Cmax и изменение в % по сравнению с контрольным составом "ref", который не содержит поверхностно-активное вещество. [Необходимо отметить: "ч" = часы].
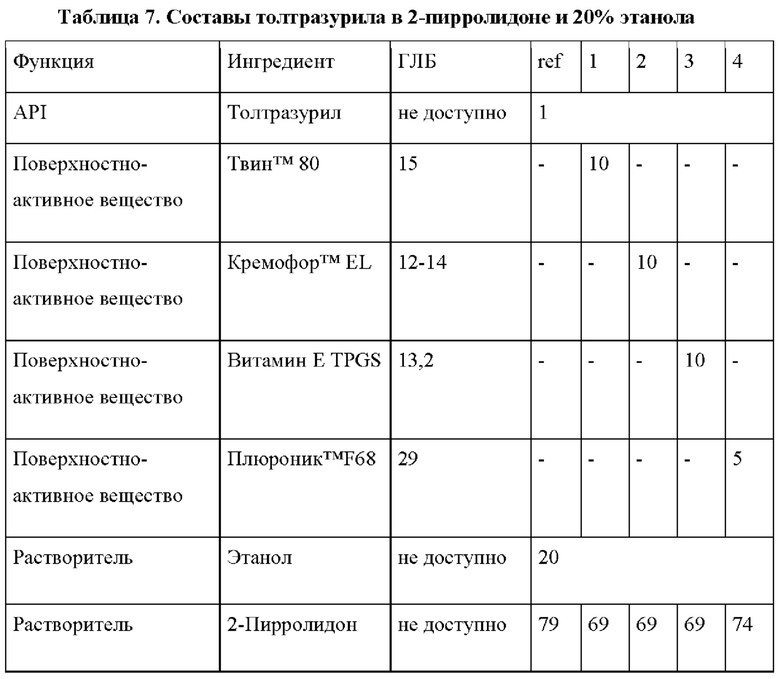

Приведенные выше данные ясно показывают положительный эффект добавления поверхностно-активных веществ с ГЛБ ≥10 также в 2-пирролидоне и 20% этанола в качестве растворителя.
Пример 5
Примеры 1-4 показали отдельный положительный эффект добавления поверхностно-активного вещества с ГЛБ ≥10. Чтобы продемонстрировать комбинированный эффект указанных поверхностно-активных веществ с добавлением многоядерного комплекса железо (III)-полисахарид, составы, представленные в Таблице 9, получали аналогично составам, раскрытым в ЕР 2164496 А1.
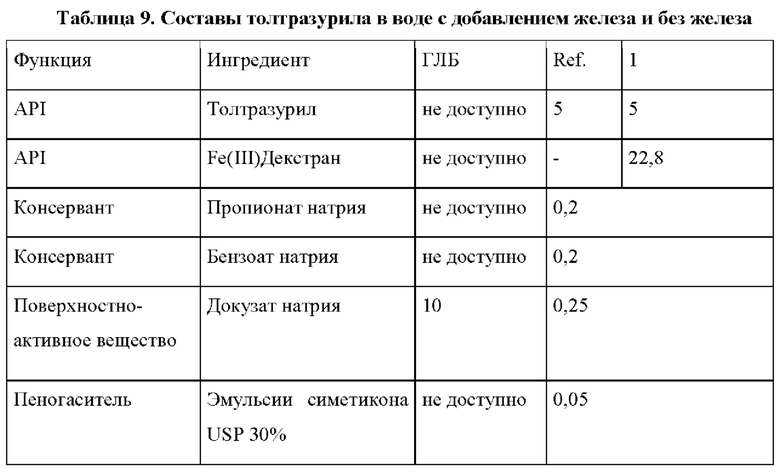
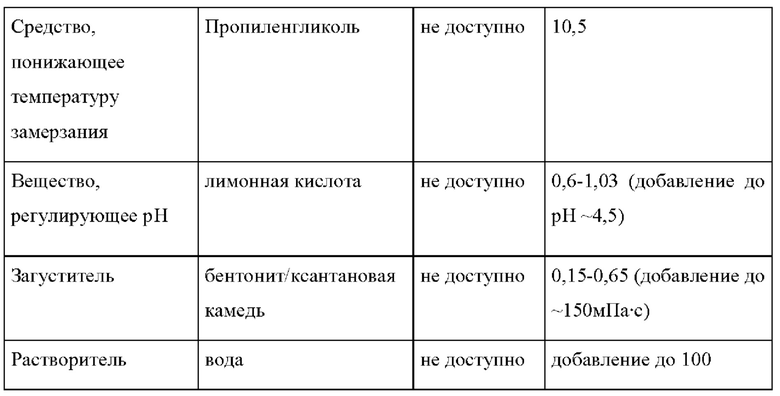
В общем 21 поросенка, рожденных от 2 свиноматок, случайным образом распределяли в 2 группы исследования по 10 и 11 поросенка в каждой. Оба состава вводили 3-х дневным поросятам соответствующих групп в виде одного перорального болюса.
Частые заборы крови (n=22 образца на поросенка) проводили после обработки по заранее установленному графику в течение всего периода времени, равного 84 дня, включая образец перед обработкой.
Концентрации активного вещества толтразурил в плазме анализировали с помощью хроматографии с турбулентным потоком/тандемной масс-спектрометрии. Предел количественного определения составлял 10 мкг/л.
На основании полученных образцов вычисляли РК данные, приведенные в Таблице 10.

Приведенные выше данные ясно показывают положительный комбинированный эффект добавления поверхностно-активного вещества с ГЛБ ≥10 с многоядерным комплексным соединением железо (III)-полисахарид.
В то время как примеры 1-4 показали положительный эффект поверхностно-активного вещества с ГЛБ ≥10, данные, приведенные в Таблице 10, показывают еще большее улучшение релевантных фармакокинетических параметров.
Пример 6
Примеры 1-4 показали отдельный положительный эффект добавления поверхностно-активного вещества с ГЛБ ≥10. Пример 5 показал положительный комбинированный эффект указанных поверхностно-активных веществ с добавлением многоядерного комплекса железо (III)-полисахарид при пероральном введении.
Для того, чтобы доказать, что общий комбинированный эффект не зависит от конкретного пути введения, составы, приведенные в таблице 11, получали для введения посредством инъекции. Состав «ref1» такой же, как указанный выше в Примере 5 состав «ref», что означает пероральный состав, содержащий только толтразурил. Состав «ref2» идентичен составу согласно обозначению 1 в этом примере, но без добавления активного железа.
Составы получали аналогично Примеру 5.
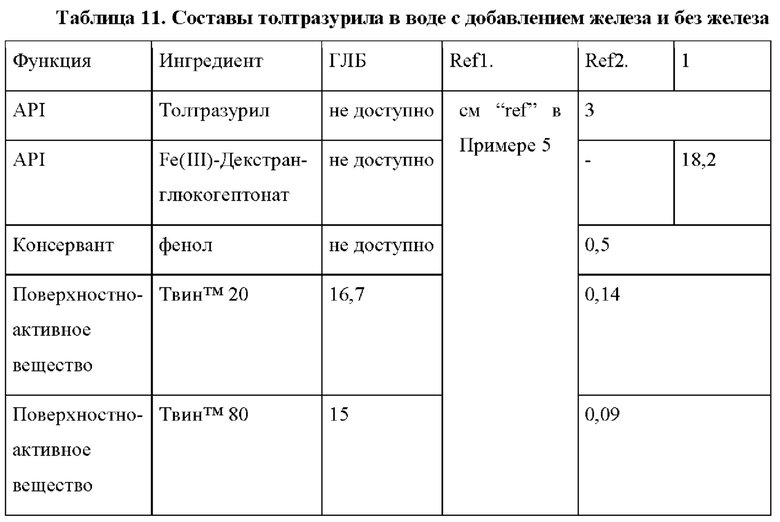

Получали 3 параллельные смоделированные группы исследования по 6 поросят в каждой. На 3-й день жизни животных обрабатывали соответствующими составами. Поросята группы, получавшей состав ref1, получали (точно так же, как в Примере 5) один пероральный болюс, в то время как поросята из двух других групп получили однократную инъекцию двух составов на 3-й день жизни.
Частый забор крови проводили после каждой обработки через 0, 4, 8, 24, 32, 48, 72, 7, 14, 21 и 28 дней (n=11/животное). Концентрации активного вещества толтразурила в плазме анализировали с помощью хроматографии с турбулентным потоком/тандемной масс-спектрометрии. Предел количественного определения составлял 25 мкг/л для каждого аналита.
На основании полученных образцов вычисляли РК данные, приведенные в Таблице 12.

Приведенные выше данные ясно показывают положительный комбинированный эффект добавления поверхностно-активного вещества с ГЛБ ≥10 с многоядерным комплексным соединением железо (III)-полисахарид независимо от пути введения, при этом поверхностно-активные вещества с даже более высоким показателем ГЛБ по сравнению с Примером 5, как оказалось, дополнительно увеличивают положительный эффект на достигаемые фармакокинетические свойства.
Обобщая приведенные выше Примеры 1-6, можно установить, что поверхностно-активные вещества с показателем ГЛБ ≥10 существенно увеличивают уже измененные фармакокинетические свойства комбинации толтразурила и многоядерного комплексного соединения железо (III)-полисахарид, при этом такой эффект не зависит ни от того, представляет ли собой состав раствор или дисперсию активных ингредиентов, ни от конкретного пути введения.
Настоящее изобретение относится к составу для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, где состав содержит толтразурил или диклазурил, многоядерное комплексное соединение железо (III)-полисахарид и по меньшей мере два поверхностно-активных вещества, имеющих показатель ГЛБ, равный 10 или более. Настоящее изобретение обеспечивает синергетический эффект между триазинонами, многоядерным полисахаридным комплексным соединением железа (III) и двумя поверхностно-активными веществами со значением ГЛБ 10 или более. 6 з.п. ф-лы, 12 табл., 6 пр.
1. Состав для одновременного лечения кокцидиальных инфекций и железодефицитных анемий у отличных от человека животных, где состав содержит толтразурил или диклазурил, многоядерное комплексное соединение железо (III)-полисахарид и по меньшей мере два поверхностно-активных вещества, имеющих показатель ГЛБ, равный 10 или более.
2. Состав по п. 1, где по меньшей мере два поверхностно-активных вещества, имеющих показатель ГЛБ, равный 10 или более, выбраны из перечня, состоящего из докузата натрия, полисорбатов, сополимера Полиоксил 35 - гидрогенизированное касторовое масло, Плюроника F-68 и Витамина E TPGS.
3. Состав по п. 2, где по меньшей мере два поверхностно-активных вещества, имеющих показатель ГЛБ, равный 10 или более, представляют собой Полисорбат 20 и Полисорбат 80.
4. Состав по любому из предшествующих пунктов, где применяемый состав представляет собой суспензию.
5. Состав по любому из предшествующих пунктов, где состав предназначен для применения посредством перорального введения.
6. Состав по любому из пунктов 1-4, где состав предназначен для применения посредством парентерального введения.
7. Состав по п. 6, где состав предназначен для применения посредством инъекционного введения.
| WO 2014086960 A1, 12.06.2014 | |||
| УСТАНОВКА КОМПЛЕКСНОЙ БИОЛОГИЧЕСКОЙ УТИЛИЗАЦИИ СЕЛЬХОЗОТХОДОВ | 1999 |
|
RU2164496C2 |
| WO 2016131853 A1, 25.08.2016 | |||
| CN 108066767 A, 25.05.2018 | |||
| СОСТАВЫ, СОДЕРЖАЩИЕ ТРИАЗИНОНЫ И ЖЕЛЕЗО | 2008 |
|
RU2506081C9 |
| US 20060240049 A1, 26.10.2006 | |||
| CN 102973502 A, 20.03.2013. | |||
Авторы
Даты
2024-10-16—Публикация
2019-05-29—Подача