Изобретение относится к области медицины, а именно к локальным гемостатическим средствам, применяемым для прекращения кровотечений, включая обширные венозные и артериальные, и может использоваться для предоставления медицинской помощи в экстренных и неотложных случаях при ранениях и травмах на предгоспитальном этапе и в стационарных условиях при ранениях и травмах, входить в состав аптечек и укладок различного назначения, а также применяться в ходе выполнения хирургических операций в медицинских учреждениях.
Известен способ изготовления гемостатического медицинского изделия, в котором медицинское изделие изготовляют непосредственно в процессе электроформования, образуя требуемую последовательность слоев изделия, например, в форме многослойной повязки, без использования дополнительных физико-механических способов соединения слоев, а также клеящих составов с возможностью формирования односторонней или двухсторонней многослойной повязки, состоящей, по меньшей мере, из подложки, выполненной из одного или нескольких слоев и содержащей, по меньшей мере, технологический и/или контактный (на основе полиамидов) слои с возможностью размещения гелеобразующего слоя и активного слоя из нетканого материала на основе нановолокон хитозана (см. патент на полезную модель РФ №135921, кл. A61L 15/22, опубл. 27.12.2013 г.).
При использовании данного гемостатического медицинского изделия после наложения его непосредственно на источник кровотечения необходимо осуществить ручную компрессию в течение 2-3 мин.
Однако данный способ изготовления гемостатического медицинского изделия, не смотря на кажущуюся простоту, требует тщательный подбор материалов, который позволил бы обеспечить надежное соединение между собой несколько слоев с образованием многослойной конструкции конечного изделия с использованием процесса электроформования. В результате конечное изделие при его применении имеет относительно низкую эффективность применения, что приводит к необходимости длительного сдавливания области раны после применения местных кровоостанавливающих средств. Кроме того, оно имеет относительно высокую частоту рецидивов кровотечений и нестабильность тромба, который образуется в месте повреждения сосудов при механическом движении конечностей.
Наиболее близким к изобретению по технической сущности и достигаемому результату является способ изготовления гемостатического медицинского изделия, заключающийся в том, что соединяют подложку из нетканого материала посредством клея с порошкообразной смесью из хитозана и полимера акриловой кислоты (см. международную заявку WO 2012/123728, кл. A61F 13/00, опубл. 20.09.2012).
Однако данное гемостатическое изделие не в полной мере использует возможности по использованию порошкообразных кровеостанавливающих средств в составе гемостатических изделий, что сужает возможности их использования.
Технической проблемой, на решение которой направлено настоящее изобретение, является преодоление выше выявленных недостатков известных гемостатических медицинский изделий.
Технический результат заключается в том, что достигается возможность повысить гемостатическую активность конечного изделия за счет создания в процессе его изготовления трехмерной структуры впитывающей поверхности с контролируемой внутренней структурой из смеси порошков хитозана и редкосшитого полимера акриловой кислоты при одновременном усилении бактерицидного эффекта с возможностью увеличения компрессионного воздействия на источник кровотечения при размещении изделия на ране.
Указанная техническая проблема решается, а технический результат достигается за счет того, что способ изготовления гемостатического медицинского изделия заключается в том, что соединяют подложку из нетканого материала посредством клея с порошкообразной смесью из хитозана и полимера акриловой кислоты, на подложку из нетканого материала толщиной от 0,5 до 2,0 мм в виде полотна из волокон целлюлозы и двухкомпонентного штапельного волокна из полиэтилентерефталата и полиэтилена, наносят слой клея БФ-6 равномерной толщины, на который наносят слой равномерной толщины порошкообразной смеси хитозана и редкосшитого полимера акриловой кислоты, где полотно состоит из 65% волокон целлюлозы и 35% двухкомпонентного штапельного волокна из полиэтилентерефталата и полиэтилена, а в качестве хитозана использован хитозан с молекулярной массой от 60 кДа до 600 кДа и степенью деацетилирования от 70% до 99%, и причем частицы порошка смеси хитозана и редкосшитого полимера акриловой кислоты по меньшей мере частично погружают в слой клея с образованием на поверхности слоя клея БФ-6 сплошной трехмерной поверхности частиц порошкообразной смеси, после чего полученную трехслойную структуру изделия высушивают в течение не менее 30 мин. в сушильном шкафу при температуре 25°С.
Предпочтительно размер частиц порошка смеси хитозана и редкосшитого полимера акриловой кислоты составляет от 0,1 мм до 0,75 мм, толщина слоя клея БФ-6 составляет от 0,1 мм до 1,5 мм, а толщина слоя гемостатического материала составляет от 0,5 мм до 2,5 мм, а количество хитозана в составе порошкообразной смеси составляет не более 1 масс. %.
В ходе проведенного исследования было установлено, что недостатком известных способов изготовления гемостатических медицинских изделий, в которых используются гемостатические материалы в виде порошка или гранул является возможность их удаления с подложки с кровью, вытекающей из раны (особенно при сильном кровотечении) во время использования, что особенно заметно по сравнению с гранулами с низкой удельной плотностью.
Особая сложность заключается в том, что кровоостанавливающие гранулы и порошок часто трудно удалить из раны из-за их плотного прилипания к поверхности и краям раны, что может привести к отрыву сгустка крови и возобновлению кровотечения. Находясь в ране, кровоостанавливающие гранулы и порошок могут изменять местное кровообращение тканей раневой полости (раневого канала), что проявляется изменением цвета и появлением припухлости после удаления кровоостанавливающего средства.
Описанная выше последовательность действий в сочетании с использованными материалами позволяют создать гемостатическое медицинское изделие, которое обеспечивает высокие показатели адсорбции местного гемостатического средства и обеспечивает более высокую гемостатическую активность за счет эффекта гемоконцентрации, связанной с впитыванием жидкой части плазмы, причем использование в вышеуказанной смеси редкосшитого полимера акриловой кислоты, как активного агента, позволяет получать материал с контролируемой внутренней структурой, что впоследствии повышает гемостатический эффект конечного изделия, а приведенное выявленное оптимальное количество активного агента позволяет добиться стабильной гемостатической активности. В ходе исследования различных материалов было подобрано сочетание материалов и их параметров, которое при описанной выше последовательности действий обеспечивает достижение заявленного технического результата. В первую очередь важно, что в качестве клея использован именно медицинский клей БФ-6. Однако необходимо добиться достижения одновременно нескольких параметров, а именно прочности соединения между собой используемых материалов в единую многослойную структуру, при этом изделие должно сохранить эластичность, чтобы плотно прилегать к ране и при этом должна быть обеспечена возможность формирования внешней трехмерной поверхности слоя из порошка смеси хитозана и редкосшитого полимера акриловой кислоты. В первую очередь важно создать на поверхности подложки ровный слой клея БФ-6, причем установлено, что требуемая прочность соединения этого клея обеспечивается именно с полотном из нетканого материала в виде полотна из смеси целлюлозных и синтетических волокон, которое в свою очередь обеспечивает требуемую эластичность конечного изделия, а после высыхания клея образуется эластичная пленка клея, которая повторяет форму подложки. Кроме того, затем необходимо сформировать на слое клея равномерной толщины слой прошкообразной смеси хитозана и редкосшитого полимера акриловой кислоты, причем частицы порошка важно по меньшей мере частично погрузить в слой клея, что с одной стороны позволяет надежно закрепить их в клее и с другой стороны создать трехмерную структуру наружной поверхности с высокой наружной площадью поверхности, что и обеспечивает в сочетании со свойствами использованных веществ (порошкообразные хитозан, содержание которого целесообразно иметь меньше 1 мас %, и редкосшитый полимер акриловой кислоты) высокие гемостатические свойства при сохранении требуемой эластичности конечного изделия будь то полотно, бинт, повязка или какое-либо другое изделие.
В ходе исследования были выявлены вышеуказанные наиболее предпочтительные величины толщины нетканого материала в сочетании с вышеуказанными толщинами слоя клея БФ-6 и слоя порошка гемостатического материала, которые показали наилучшие показатели прочности соединения между собой вышеуказанных слоев, которые исключали выпадение частиц порошка из слоя клея БФ-6, причем наличие смеси хитозана и редкосшитого полимера акриловой кислоты позволило создать трехмерную структуру с наиболее высокой внешней поверхностью, обращенной к ране, что в сочетании с плотным прижатием многослойной структуры к поверхности раны позволило создать высокую впитывающую поверхность и при этом прочную многослойную структуру, которая исключает механические повреждения в процессе использования описанного гемостатического медицинского изделия, а клеящий слой из клея БФ-6, кроме прочного соединения между собой слоев многослойной структуры гемостатического изделия обеспечивает бактерицидную защиту раны, на которую это изделие накладывается. Таким образом, вышеописанный способ изготовления гемостатического медицинского изделия позволил обеспечить высокие механические свойства готового изделия (прочность и плотность) и требуемое компрессионное воздействие на источник кровотечения при размещении средства в ране.
В ходе проведенных экспериментов были изучены основные параметры, которые характеризуют гемостатическую активность у полученных образцов, in vitro.
Была проведена оценка сорбционной емкости по воде, сорбционной емкости по крови, а также замерялось время коагуляции крови при добавлении на образец гемостатического средства стандартного размера.
В качестве образца сравнения использовали коммерчески доступное местное гемостатическое средство на основе хитозана: «Повязку Celox Z-сложенную гемостатическую» - образец сравнения (нетканый материал, на поверхность которого нанесен хитозан методом термоскрепления)
Для оценки эффективности образцов в условиях in vitro применяли следующие методики:
1) Проверка сорбционной емкости по воде
Был подготовлен образец размером 5*5 см (площадь 25 см2), вырезанный из гемостатического средства, затем образец взвешивают (масса сухого образца - W1), после чего помещают его в сухую чашку Петри. Для работы используют пинцет медицинский. К образцу добавляют 20 мл дистиллированной воды, предварительно нагретой до температуры 37°С, и оставляют на 30 мин в термостате при 37°С. Через 30 мин образец извлекают и взвешивают (масса образца с жидкостью - W2). Сорбционная емкость образца рассчитывается по формуле:
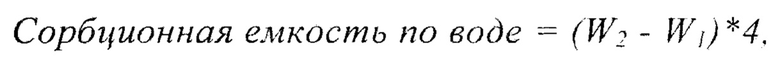
и выражается в массе жидкости в граммах, поглощенной образцом с S=100 см2.
Анализ проводили для пяти образцов идентичного состава, для каждого рассчитывали медиану, 1-й и 3-й квартили. Удовлетворительным считали значение показателя не менее 12 г/100 см2. Полученные значения для образцов, разработанных в соответствии с предлагаемым изобретением, сравнивали с образцом сравнения («Celox Z-сложенная гемостатическая повязка»). Значимыми считали различия при р<0,05.
2) Проверка сорбционной емкости по крови
Впитывающую способность определяли согласно методике [Ting-Ting Li, Ching-Wen Lou, An-Pang Chen, Mong-Chuan Lee, Tsing-Fen Ho, Yueh-Sheng Chen, and Jia-Horng Linl Highly/Absorbent Antibacterial Hemostatic Dressing for Healing Severe Hemorrhagic Wounds// Materials (Basel). 2016 Sep; 9(9): 793].
Был подготовлен образец размером 5*5 см (площадь 25 см2), вырезанный из гемостатического средства, затем образец взвешивают (масса сухого образца - W1), после чего помещают его в сухую чашку Петри. В работе использует пинцет медицинский. К образцу добавляют 20 мл цельной донорской крови, содержащей антикоагулянт натрия цитрат в соотношении 1:9, и оставляют на 30 мин в термостате при 37°С. Через 30 мин образец извлекают и взвешивают (масса образца с жидкостью - W2). Сорбционная емкость образца рассчитывается по формуле:
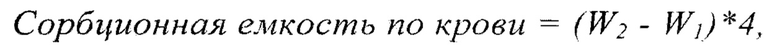
Впитывающая способность выражается в массе жидкости в граммах, поглощенной образцом с S=100 см2.
Анализ проведен для пяти образцов идентичного состава, для каждого рассчитывали медиану, 1-й и 3-й квартили. Удовлетворительным считали значение показателя не менее 12 г/100 см2. Полученные значения для образцов, разработанных в соответствии с предлагаемым изобретением, сравнивали с образцом сравнения («Celox Z-сложенная гемостатическая повязка»»). Значимыми считали различия при р<0,05.
3) Определение времени коагуляции
Для определения времени коагуляции используют модифицированную методику [Липатов В.А., Лазаренко С.В., Сотников К.А., Северинов Д.А., Ершов М.П. К вопросу о методологии сравнительного изучения степени гемостатической активности аппликационных кровоостанавливающих средств//Новости хирургии. 2018].
Стандартные образцы перевязочного гемостатического средства размерами 1 см*1 см укладывались на дно кюветы. Далее к исследуемому образцу, находящегося в термостате при 37°С, добавляли 1 мл цельной донорской крови (без ингибиторов свертывания) и 100 мкл 0,2М раствора кальция хлорида, затем перемешивали и включали секундомер. Пробирки наклонялись на 50-60 градусов каждые 30 с, фиксировалось время образования сгустка.
Анализ проводили для шести образцов идентичного состава, для каждого рассчитывали медиану, 1-й и 3-й квартили. Удовлетворительным считали значение показателя не более 15 мин. Полученные значения для образцов, разработанных в соответствии с предлагаемым изобретением, сравнивали с образцом сравнения 1 («Celox»). Значимыми считали различия при р<0,05.
Дополнительно для всех образцов оценивали прирост температуры при увлажнении, который во всех случаях не превышал 3,5°С, и потерю массы при высушивании, которая не превышала 10%.
К числу предпочтительных относили образцы с наименьшим временем коагуляции, далее выявляли образцы с наибольшими значениями сорбционной емкости по воде и крови.
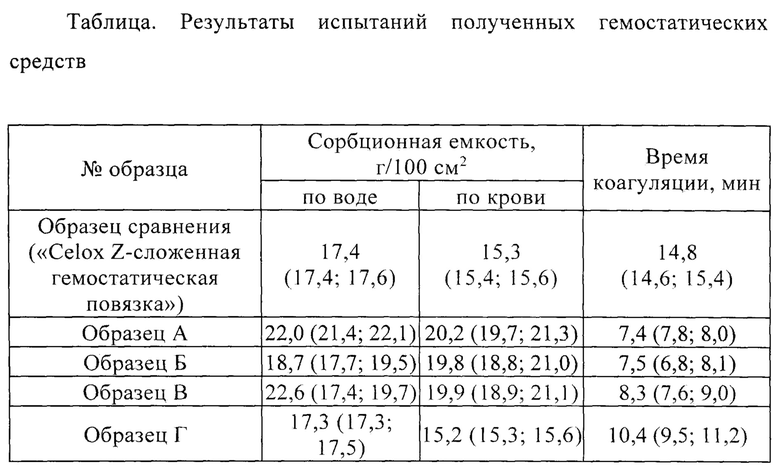
На основе полученных результатов были сделаны следующие выводы:
наилучшие показатели эффективности in vitro были получены для образцов А и Б. Для указанных образцов значение времени коагуляции были статистически достоверно меньше, чем для образца сравнения, сорбционная емкость по крови была сопоставимо больше с образцами сравнения, а сорбционная емкость по воде была выше, чем для образца сравнения.
Результаты оценки эффективности для образцов В и Г были удовлетворительными, что подтверждает возможность их применения для производства МГС.
На основании полученных результатов можно заключить, что оптимальная эффективность гемостатического средства достигается с следующих случаях: (1) нетканый материал, применяемый для изготовления гемостатического средства, должен иметь толщину от 0,5 до 2,0 мм, (2) содержание целлюлозы в исходном нетканом материале должно быть не менее 50%, (3) для изготовления гемостатического средства должен применяться хитозан с молекулярной массой от 60 кДа до 600 кДа и степенью деацетилирования от 70% до 99%.
В результате представляется возможность получения при изготовлении готового кровеостанавливающего изделия в форме рулонов, что в дальнейшем позволяет формировать из рулонов гемостатические изделия в виде бинтов, повязок или каких-либо других изделий, что идеально подходит для промышленного производства изделий на основе нетканого материала, с действующим составом из смеси хитозана и редкосшитого полимера акриловой кислоты.
| название | год | авторы | номер документа |
|---|---|---|---|
| Гемостатическое медицинское изделие | 2023 |
|
RU2829819C1 |
| Гемостатическое средство на основе хитозана | 2023 |
|
RU2807862C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСТАТИЧЕСКОГО СРЕДСТВА НА ОСНОВЕ ХИТОЗАНА | 2023 |
|
RU2806364C1 |
| ГЕМОСТАТИЧЕСКОЕ СРЕДСТВО НА ОСНОВЕ ХИТОЗАНОВОГО АЭРОГЕЛЯ | 2020 |
|
RU2743425C1 |
| Гемостатический материал, гемостатическое средство и перевязочный материал на его основе | 2016 |
|
RU2635465C1 |
| РАСТВОР ДЛЯ ПОЛУЧЕНИЯ МАТЕРИАЛА НА ОСНОВЕ ХИТОЗАНА, СПОСОБ ПОЛУЧЕНИЯ ГЕМОСТАТИЧЕСКОГО МАТЕРИАЛА ИЗ ЭТОГО РАСТВОРА (ВАРИАНТЫ) И МЕДИЦИНСКОЕ ИЗДЕЛИЕ С ИСПОЛЬЗОВАНИЕМ ВОЛОКОН НА ОСНОВЕ ХИТОЗАНА | 2011 |
|
RU2487701C2 |
| Многослойное комбинированное гемостатическое средство местного действия | 2023 |
|
RU2826069C1 |
| ГЕМОСТАТИЧЕСКИЙ ПЛАСТЫРЬ | 2009 |
|
RU2417076C2 |
| Местное гемостатическое антибактериальное средство | 2021 |
|
RU2776015C1 |
| ГЕМОСТАТИЧЕСКИЙ МАТЕРИАЛ | 2019 |
|
RU2830588C2 |
Настоящее изобретение относится к способу изготовления гемостатического медицинского изделия, заключающемуся в том, что соединяют подложку из нетканого материала посредством клея с порошкообразной смесью из хитозана и полимера акриловой кислоты, отличающемуся тем, что на подложку из нетканого материала толщиной от 0,5 до 2,0 мм в виде полотна из волокон целлюлозы и двухкомпонентного штапельного волокна из полиэтилентерефталата и полиэтилена наносят слой клея БФ-6 равномерной толщины, на который наносят слой равномерной толщины порошкообразной смеси хитозана и редкосшитого полимера акриловой кислоты, где полотно состоит из 65% волокон целлюлозы и 35% двухкомпонентного штапельного волокна из полиэтилентерефталата и полиэтилена, а в качестве хитозана использован хитозан с молекулярной массой от 60 кДа до 600 кДа и степенью деацетилирования от 70% до 99%, и причем частицы порошка смеси хитозана и редкосшитого полимера акриловой кислоты по меньшей мере частично погружают в слой клея с образованием на поверхности слоя клея БФ-6 сплошной трехмерной поверхности частиц порошкообразной смеси, после чего полученную трехслойную структуру изделия высушивают в течение не менее 30 мин в сушильном шкафу при температуре 25°С. Настоящее изобретение обеспечивает возможность повышения гемостатической активности конечного изделия за счет создания в процессе его изготовления трехмерной структуры впитывающей поверхности с контролируемой внутренней структурой из смеси порошков хитозана и редкосшитого полимера акриловой кислоты при одновременном усилении бактерицидного эффекта с возможностью увеличения компрессионного воздействия на источник кровотечения при размещении изделия на ране. 1 з.п. ф-лы, 1 табл.
1. Способ изготовления гемостатического медицинского изделия, заключающийся в том, что соединяют подложку из нетканого материала посредством клея с порошкообразной смесью из хитозана и полимера акриловой кислоты, отличающийся тем, что на подложку из нетканого материала толщиной от 0,5 до 2,0 мм в виде полотна из волокон целлюлозы и двухкомпонентного штапельного волокна из полиэтилентерефталата и полиэтилена наносят слой клея БФ-6 равномерной толщины, на который наносят слой равномерной толщины порошкообразной смеси хитозана и редкосшитого полимера акриловой кислоты, где полотно состоит из 65% волокон целлюлозы и 35% двухкомпонентного штапельного волокна из полиэтилентерефталата и полиэтилена, а в качестве хитозана использован хитозан с молекулярной массой от 60 кДа до 600 кДа и степенью деацетилирования от 70% до 99%, и причем частицы порошка смеси хитозана и редкосшитого полимера акриловой кислоты по меньшей мере частично погружают в слой клея с образованием на поверхности слоя клея БФ-6 сплошной трехмерной поверхности частиц порошкообразной смеси, после чего полученную трехслойную структуру изделия высушивают в течение не менее 30 мин в сушильном шкафу при температуре 25°С.
2. Способ изготовления гемостатического медицинского изделия по п. 1, отличающийся тем, что размер частиц порошка смеси хитозана и редкосшитого полимера акриловой кислоты составляет от 0,1 мм до 0,75 мм, толщина слоя клея БФ-6 составляет от 0,1 мм до 1,5 мм, а толщина слоя гемостатического материала составляет от 0,5 мм до 2,5 мм, а количество хитозана в составе порошкообразной смеси составляет не более 1 масс. %.
| US 2014105950 A1, 17.04.2014 | |||
| Гемостатическое средство на основе хитозана | 2023 |
|
RU2807862C1 |
| ГЕМОСТАТИЧЕСКОЕ СРЕДСТВО НА ОСНОВЕ ХИТОЗАНОВОГО АЭРОГЕЛЯ | 2020 |
|
RU2743425C1 |
Авторы
Даты
2024-11-06—Публикация
2023-12-04—Подача