Изобретение относится к медицине, конкретно к фармакологии, и касается средств, ослабляющих постинфарктное ремоделирование миокарда.
Ремоделирование миокарда в постинфарктном периоде является одной из причин формирования хронической сердечной недостаточности [1, 2]. На процесс ремоделирования левого желудочка (ЛЖ) после инфаркта миокарда (ИМ) влияет большое количество биологических реакций: локальная ишемия и смерть клеток; оксидативный стресс и воспалительные реакции в поврежденном миокарде; кардиодепрессивные реакции, обусловленные продукцией кислородных радикалов и воспалительных цитокинов; изменения в экстрацеллюлярном матриксе, следующие за активацией матриксных металл опротеаз; структурные изменения в миокарде в ответ на увеличивающееся напряжение; синтез коллагена и миокардиальный фиброз [3]. После инфаркта миокарда развивается патологический тип ремоделирования, обусловленный дилатацией полости левого желудочка, потерей значительного объема сократительного миокарда, что приводит к сердечной недостаточности. Ремоделирование левого желудочка после инфаркта миокарда с подъемом сегмента ST также может быть вызвано воспалительной реакцией, опосредованной различными клетками и цитокинами, что в конечном итоге приводит к деградации внеклеточного матрикса миокарда и смещению мышечных пучков в области инфаркта [4, 5]. В острой фазе расширение желудочков является результатом процесса растяжения миокарда, в то время как позднее расширение полости является результатом процесса эксцентричной гипертрофии [6, 7, 8]. Аневризматическая форма постинфарктного ремоделирования характеризуется наличием в зонах постинфарктных рубцов единичных или множественных аневризматических образований [9].
Известны средства, ослабляющие постинфарктное ремоделирование миокарда: бета-адреноблокаторы [10, 11, 12, 13], ингибиторы ангиотензинпревращающего фермента [11, 13], антагонисты кальция [11, 14], диуретики [11, 15, 16, 17], цитопротекторы [18, 19, 20]. Однако препараты, рекомендованные для предотвращения постинфарктного ремоделирования левого желудочка, либо имеют ряд противопоказаний, либо низкую доказательную базу [13], вследствие чего остается актуальным поиск перспективных препаратов, влияющих на несколько звеньев патогенеза заболевания.
Задачей изобретения является расширение арсенала средств, ослабляющих постинфарктное ремоделирование миокарда.
Поставленная задача достигается использованием n-тирозола (n-оксифенил-β-этанол, 4-(2-гидроксиэтил)фенол) в качестве средства, ослабляющего постинфарктое ремоделирование миокарда.
n-Тирозол представляет собой агликон салидрозида, действующего начала экстракта родиолы розовой [21]. Известно, что n-тирозол обладает широким спектром фармакологической активности: стресспротективной, адаптогенной, антигипоксической [21], противовоспалительной [22, 23], нейропротективной [24] и рядом других эффектов [25, 26, 27, 28, 29]. У n-тирозола также выявлено выраженное противоишемические действие. В условиях многократной транзиторной ишемии миокарда у крыс n-тирозол оказывал отчетливый противоишемический эффект, уменьшая подъем сегмента ST на ЭКГ в период ишемии, способствовал более полному восстановлению сегмента ST при реперфузии, снижал риск развития желудочковых фибрилляций и продолжительность эпизодов тахиаритмий (желудочковой тахикардии и фибрилляций) в периодах реперфузий [30]. На модели ИМ у крыс n-тирозол проявлял антиоксидантный эффект, уменьшал зону инфаркта [26], повышал экспрессию нуклеарного SIRT1, увеличивал уровень фосфорилирования Akt и модулировал РОХО3а-зависимые процессы повышения устойчивости к стрессу и процессы репарации ДНК [31].
Способность n-тирозола ослаблять постишемическое ремоделирование миокарда ранее не описана.
Принципиально новым в предлагаемом изобретении является то, что в качестве средства, ослабляющего постинфарктное ремоделирование миокарда, используется п-тирозол.
Способность n-тирозола ослаблять постишемическое ремоделирование миокарда явным образом не вытекает для специалиста из уровня техники.
n-Тирозол может использоваться для лечения постинфарктного ремоделирования миокарда.
Таким образом, данное техническое решение соответствует критериям изобретения: "новизна", "изобретательский уровень", "промышленная применимость".
Новые свойства n-тирозола были найдены экспериментальным путем.
Эксперименты выполнены на 40 крысах-самцах Вистар массой 300-350 г, полученных из Отдела экспериментальных биологических моделей НИИФиРМ им. Е.Д. Гольдберга. Содержание животных осуществлялось в соответствии с правилами, принятыми Европейской конвенцией по защите позвоночных животных (Страсбург, 1986) и Приказом Министерства здравоохранения Российской Федерации от 1 апреля 2016 г. №199н г. Москва «Об утверждении Правил надлежащей лабораторной практики».
Для проведения эксперимента животных разделяли на 3 группы: ложнооперированная (ЛО) группа (n=7) с введением растворителя, контрольная группа (n=17) с введением растворителя, опытная группа (n=16) с введением n-тирозола в дозе 20 мг/кг. n-Тирозол вводили внутрибрюшинно в объеме 2 мл, в качестве растворителя использовали физиологический раствор натрия хлорида. Первое введение n-тирозола проводили в период ишемии миокарда за 20 мин до начала реперфузии. Последующие введения проводили через 4 ч после начала реперфузии, а также в течение последующих 3 суток один раз в сутки. В исследовании использовали n-тирозол, синтезированный в ФГБУН Институт проблем химико-энергетических технологий СО РАН (чистота 99,7%).
ИМ моделировали у крыс методом окклюзии левой коронарной артерии в течение 1 ч с последующей реперфузией [32] без нарушения топографии сердца. Для анестезии использовали внутривенную инфузию пропофола (10 мг/кг/ч), температуру животных поддерживали в диапазоне 37±0.5°С с использованием Homeothermic Blanket Control Unit (Harvard Apparatus, США). Искусственную вентиляцию легких осуществляли через интубационную трубку по открытой схеме аппаратом Rodent Ventilator 7025 (UGO BASILE, Италия). Для верификации ИМ регистрировали ЭКГ в трех стандартных отведениях на компьютерном электрокардиографе Поли-Спектр-8/Л (Нейрософт, Россия). У ЛО животных проводили аналогичное оперативное вмешательство, но без окклюзии коронарной артерии.
Через 2 месяца после ИМ у выживших крыс определяли показатели сократительной функции сердца и основные гемодинамические показатели для оценки насосной функции сердца на аппаратном комплексе для электрофизиологических исследований MP 150 Biopac (Biopac System, Inc., США). Для анестезии при оценке параметров сердечной деятельности использовали внутривенное введение тиопентала натрия в дозе 30 мг/кг/ч. Частоту сердечных сокращений (ЧСС) определяли по ЭКГ, ударный объем (УО) определяли методом импедансометрии и вычисляли минутный объем кровообращения (МОК). Показатели сократительной функции сердца регистрировали датчиком TDS 175 В с помощью OpSens (Канада). Датчик вводили в полость ЛЖ через правую общую сонную артерию. Измеряли давление в восходящей части аорты (Даорт). По кривой давления в полости ЛЖ определяли систолическое давление в ЛЖ (СДЛЖ, мм рт. ст.), минимальное давление в ЛЖ (ДminЛЖ, мм рт. ст.), конечное диастолическое давление в ЛЖ (КДДЛЖ, мм рт. ст.), максимальную скорость нарастания (+dP/dt max, мм рт. ст./мин) и снижения (-dP/dt max, мм рт. ст./мин) давления в ЛЖ, индекс сократимости (ИС, с-1).
Эвтаназию крыс производили передозировкой диэтилового эфира.
После эвтаназии извлекали сердце и проводили морфометрическую оценку ремоделирования левого желудочка и развития соединительной ткани в очаге ИМ. Для морфометрических исследований ЛЖ нарезали на серию поперечных срезов толщиной 500 мкм на замораживающем микротоме МЗ-2 (Россия). Полученные срезы помещали на предметное стекло и сканировали на HP Scanjet 3770 (Hewlett-Packard, Китай) с использованием программного обеспечения «Директор НР» v. 43.1.6.000 при разрешении 600 dpi и сохраняли в формате *.tiff. Полученные изображения обрабатывали с использованием программы «Adobe Photoshop 6.0». На срезах подсчитывали площади миокарда, постинфарктного очага и полости левого желудочка, а также общую площадь среза в пикселях. Площадь миокарда и полости левого желудочка выражали в % от общей площади срезов, площадь постинфарктного очага - в % от площади ткани миокарда. Для выявления зон зрелой соединительной ткани срезы сердца на стеклах фиксировали и обезвоживали 95% этиловым спиртом, окрашивали пикрофуксином по Ван-Гизону в течение 2-5 мин при 25°С [33]. Окрашенные срезы накрывали предметным стеклом и сканировали окрашенную сторону срезов. На срезах подсчитывали площадь миокарда и площадь зон соединительной ткани, а также общую площадь среза в пикселях. Площадь зоны зрелой соединительной ткани выражали в % от площади миокарда.
Для статистической обработки данных использовали пакет программного обеспечения «Statistica 6.0». Рассчитывали среднее значение, стандартную ошибку. Достоверность различий (р<0,05) между сериями определяли с помощью критерия Краскела-Уоллеса, U-теста Манна-Уитни, точного критерия Фишера.
Результаты исследований представлены в примерах 1-3. Пример 1.
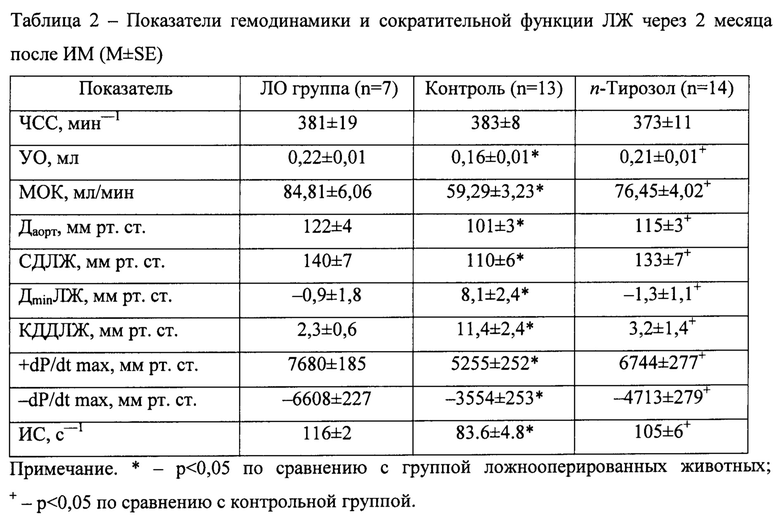
В группе ЛО животных в течение 2 месяцев эксперимента гибели животных не отмечено (табл. 1). У животных этой группы через 2 месяца после ложного оперативного вмешательства значения гемодинамических параметров и показателей сократительной функции миокарда (табл. 2) соответствовали нормальным значениям показателей для крыс соответствующей массы тела [34].

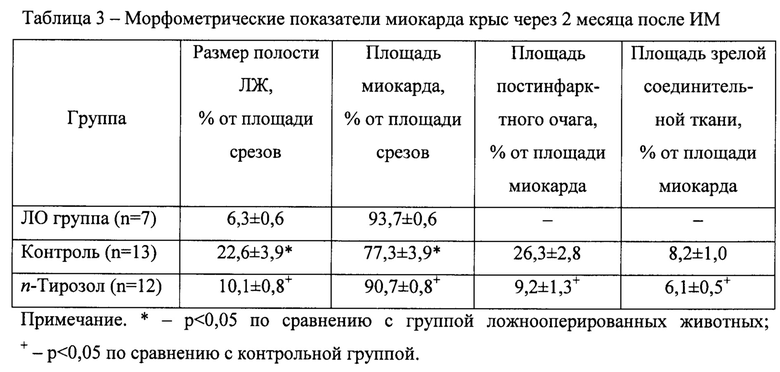
Морфометрическое исследование сердца ЛО крыс через 2 месяца после оперативного вмешательства показало, что размер полости ЛЖ составлял в среднем 6,3±0,6% от площади срезов (табл. 3).
Пример 2.
В контрольной группе погибло 4 крысы из 17 (23,5%) (табл. 1).
У контрольных животных через 2 месяца после ИМ отмечено достоверное снижение гемодинамических параметров без изменения ЧСС. УО и МОК были ниже показателя ЛО на 27,3% и 30,1% соответственно. Также у контрольных животных выявлено выраженное нарушение сократительной функции миокарда. Отмечено статистически значимое снижение показателей систолической функции сердца: СДЛЖ на 21,4%), +dP/dt max на 31,6%, ИС на 27,9% по сравнению с ЛО крысами. Формировалась резко выраженная диастолическая дисфункция миокарда. Происходило статистически значимое уменьшение -dP/dt max на 46,2%, повышение КДДЛЖ в 5 раз по сравнению с ЛО животными, ДminЛЖ увеличилось на 9 мм рт. ст. Даорт в контрольной группе крыс было ниже показателя ЛО животных на 17,2% (табл. 2).
В группе контрольных крыс через 2 месяца после ИМ отмечено расширение полости левого желудочка по сравнению с группой ЛО животных в 3,6 раза (табл. 3). Окрашивание соединительной ткани на срезах ЛЖ по Ван-Гизону показало наличие в зоне постинфарктного рубца сплошных полей зрелой соединительной ткани, занимающих у контрольных животных в среднем 8,2±1,0% от общей площади миокарда (табл. 3). У 3 животных этой группы произошло формирование аневризмы стенки ЛЖ со значительным расширением полости ЛЖ в 5,9-7,6 раза.
Пример 3.
В группе с введением n-тирозола за 2 месяца погибло 2 крысы из 16 (12,5%). Показатель смертности животных в группе с введением n-тирозола значимо не отличался от показателя контрольной группы (табл. 1).
В группе крыс с введением n-тирозола через 2 месяца после ИМ выявлено достоверное увеличение УО на 31,2% и МОК на 28,9% относительно контрольной группы при отсутствии значимых изменений ЧСС. Кроме того, у крыс с введением n-тирозола через 2 месяца после моделирования ИМ отмечено статистически значимое улучшение сократительной функции миокарда по сравнению с контрольной группой крыс. СДЛЖ было выше на 20,9%, Даорт - на 13,9% +dP/dt max - на 28,3%, ИС - на 25,6%. Улучшилась диастолическая функция миокарда. Значение -dP/dt max превосходило уровень контрольной группы на 32,6%, ДminЛЖ было на уровне ложнооперированных животных. В сравнении с ЛО группой КДДЛЖ было ниже в 3,6 раза (табл. 2).
В группе животных с введением n-тирозола через 2 месяца после моделирования ИМ размеры полости ЛЖ по сравнению с контрольной группой были меньше в среднем в 2,2 раза и значимо не отличались от показателя ЛО животных. Площадь постинфарктного очага в группе с введением n-тирозола была на 65% меньше, чем у контрольных крыс (табл. 3). У животных с введением n-тирозола соединительная ткань занимала площадь на 26% меньше по сравнению с контрольными животными (табл. 3).
Таким образом, введение n-тирозола в остром периоде ИМ уменьшало ремоделирование ЛЖ в отдаленном периоде ИМ, замедляло формирование систолической и диастолической дисфункции миокарда и улучшало насосную функции сердца с сохранением показателей гемодинамики на существенно более высоком уровне. В группе с введением n-тирозола не выявлено животных с формированием аневризмы передней стенки ЛЖ. Проведенное исследование демонстрирует способность n-тирозола существенно уменьшать степень повреждения миокарда и его последующего ремоделирования в отдаленном периоде при курсовом введении препарата в ишемическом и раннем реперфузионном периоде.
Источники литературы, принятые во внимание:
1. Yu С.М., Lin Н., Yang Н., Kong S.L., Zhang Q., Lee S.W. Progression of systolic abnormalities in patients with «isolated» diastolic heart failure and diastolic dysfunction // Circulation. - 2002. - Vol. 105. - P. 1195-1201.
2. Galli A., Lombardi F. Postinfarct Left Ventricular Remodelling: A Prevailing Cause of Heart Failure // Cardiol. Res. Pract. - 2016. - Vol. 2016. - Article ID 2579832. - 12 p.
3. Перуцкий Д.Н., Макеева Т.И., Константинов С.Л. Основные концепции постинфарктного ремоделирования миокарда левого желудочка // Белгородского государственного университета. Серия: Медицина. Фармация. - 2011. - Т. 14, №10 (105). - С. 51-59.
4. Van der Bijl P., Abou R., Gersh B.J., Holmes D.R., Marsan N.A., Delgado V., Bax J.J. Left Ventricular Post-Infarct Remodeling Implications for Systolic Function Improvement and Outcomes in the Modern Era // JACC Heart Fail. -2020. - Vol. 8, №2. - P. 131-140.
5. Sutton M.G., Sharpe N. Left ventricular remodeling after myocardial infarction: pathophysiology and therapy // Circulation. - 2000. - Vol. 101, Iss. 25. - P. 2981-2988.
6. Арипов M.A., Бережинский И.В., Иващенко A.A. Ишемическое ремоделирование левого желудочка: методологические аспекты, вопросы диагностики и лечения / под ред. Л. А. Бокерия и др. - М.: Медицина, 2002. - 234 с.
7. Батушкин В.В„ Комаревич Н.А., Дорохина А.Н. Основные компоненты постинфарктного ремоделирования левого желудочка и эхокардиографическая оценка прогноза // Кардиология: от науки к практике. - 2014. - №2. - С. 5-20.
8. Калюжин В.В., Тепляков А.Т., Соловцов М.А., Калюжина Е.В., Беспалова И.Д., Терентьева Н.Н. Ремоделирование левого желудочка: один или несколько сценариев? // Бюллетень сибирской медицины. - 2016. - Т. 15, №4. - С. 120-139.
9. Розенберг В.Д., Непомнящих Л.М. Патологическая анатомия ремоделирования постинфарктного сердца - М.: РАМН, 2002. - 103 с.
10. Мазур Н.А., Черепко В.Е. Влияние каптоприла, амлодипина и пропранолола на ремоделирование левого желудочка у больных, перенесших инфаркт миокарда // Рус. мед. журн. - 1998. - №6. - С. 1055-1058.
11. Мареев В.Ю., Фомин И.В., Агеев Ф.Т., Беграмбекова Ю.Л., Васюк Ю.А., Гарганеева А.А., Гендлин Г.Е., Глезер М.Г., Готье С.В., Довженко Т.В., Кобалава Ж.Д., Козиолова Н.А., Коротеев А.В., Мареев Ю.В., Овчинников А.Г., Перепеч Н.Б., Тарловская Е.И., Чесникова А.И., Шевченко А.О., Арутюнов Г.П., Беленков Ю.Н., Галявич А.С., Гиляревский С.Р., Драпкина О.М., Дупляков Д.В., Лопатин Ю.М., Ситникова М.Ю., Скибицкий В.В., Шляхто Е.В. Клинические рекомендации. ОССН - РКО - РНМОТ. Сердечная недостаточность: хроническая (ХСН) и острая декомпенсированная (ОДСН). Диагностика, профилактика и лечение // Кардиология. - 2018. - Т. 58, S 6. - С. 8-158.
12. Карпов Ю.А. Место бета-адреноблокаторов в новых рекомендациях Европейского общества кардиологов по артериальной гипертонии, стабильной ишемической болезни сердца и сердечной недостаточности // Эффективная фармакотерапия. Эндокринология. - 2013. - Т. 35, №4. - С. 16-21.
13. Никифоров B.C., Свистов А.С. Современная фармакотерапия хронической сердечной недостаточности // ФАРМиндекс. Практик. Кардиология. - 2003. - Вып. 4. - С. 3-19.
14. Мазур Н.А., Черепко В.Е. Влияние каптоприла, амлодипина и пропранолола на ремоделирование левого желудочка у больных, перенесших инфаркт миокарда // Рус. мед. журн. - 1998. - №6. - С. 1055-1058.
15. Ларина В.Н. Выбор эффективного диуретика для терапии хронической сердечной недостаточности на амбулаторном этапе: доводы в пользу торасемида // Consilium Medicum. - 2018. - №10. - С. 29-35.
16. Kasama S., Toyama Т., Hatori Т., Sumino H., Kumakura H., Takayama Y., Ichikawa S., Suzuki Т., Kurabayashi M. Effects of torasemide on cardiac sympathetic nerve activity and left ventricular remodellingin patients with congestive heart failure // Heart. - 2006. - Vol. 92, №10. - P. 1434-1440.
17. TORAFIC Investigators Group.Effects of prolonged-release torasemide versus furosemide on myocardial fibrosis in hypertensive patients with chronic heart failure: a randomized, blinded-end point, active-controlled study // Clin. Ther. - 2011. - Vol. 33, №9. - P. 12074-13. e3.
18. Hamm C.W., Bassand J.P., Agewall S., Bax J., Boersma E., Bueno H., Caso P., Dudek D., Gielen S., Huber K., Ohman M., Petrie M.C., Sonntag F., Uva M.S., Storey R.F., Wijns W., Zahger D. ESC Committee for Practice Guidelines. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: The Task Force for the management of acute coronary syndromes (ACS) in patients presenting without persistent ST-segment elevation of the European Society of Cardiology (ESC) // Eur. Heart J. - 2011. - Vol. 32, №23. - P. 2999-3054.
19. Морозова Т.Е. Метаболические лекарственные средства в кардиологической практике // Лечащий врач. - 2008. - №6. - С. 48-51.
20. Martins G.F., de Siqueira Filho A.G., de Figueiredo Santos J.B., Cavalcanti Assuncao C.R., Bottino F., de Carvalho K.G.,  Trimetazidine on ischemic injury and reperfusion in coronary artery bypass grafting // Arq. Bras. Cardiol. - 2011. - Vol. 97, №3. - P. 209-216.
Trimetazidine on ischemic injury and reperfusion in coronary artery bypass grafting // Arq. Bras. Cardiol. - 2011. - Vol. 97, №3. - P. 209-216.
21. Саратиков A.C., Краснов E.A. Родиола розовая (золотой корень) - Томск, 2004. - 288 с.
22. Kim Y.Y., Lee S., Kim M.J., Kang B.C., Dhakal H., Choi Y.A., Park P.H., Choi H., Shin T.Y., Choi H.G., Kwon Т.K., Khang D., Kim S.H. Tyrosol attenuates lipopolysaccharide-induced acute lung injury by inhibiting the inflammatory response and maintaining the alveolar capillary barrier // Food Chem. Toxicol. - 2017. - Vol. 109, Pt. 1. - P. 526-533.
23. Wang W.C., Xia Y.M., Yang В., Su X.N., Chen J.K., Li W., Jiang T. Protective effects of tyrosol against LPS-induced acute lung injury via inhibiting NF-кВ and AP-1 activation and activating the HO-1/Nrf2 pathways // Biol. Pharm. Bull. - 2017. - Vol. 40, №5. - P. 583-593.
24. Bu Y., Pvho S., Kim J., Kim MY., Lee D.H., Kim S.Y., Choi H., Kim H. Neuroprotective effect of tyrosol on transient focal cerebral ischemia in rats // Neurosci. Lett. - 2007. - Vol. 414, №3. - P. 218-221.
25. Плотников М.Б., Чернышева Г.А., Смольякова В.И., Маслов М.Ю., Черкашина И.В., Крысин А.П., Сорокина И.В., Толстикова Т.Г. Влияние n-тирозола на вязкость крови и агрегацию тромбоцитов // Бюл. экспер. биол. мед. - 2007. - Т. 143, №1. - С. 67-69.
26. Смольякова В.И., Чернышева Г.А., Плотников М.Б., Алиев О.И., Краснов Е.А. Антиоксидантные и кардиопротекторные эффекты n-тирозола при ишемии миокарда с реперфузией у крыс // Кардиология. - 2010. - Т. 50, №11. - С. 47-49.
27. Чернышева Г.А., Плотников М.Б., Смольякова В.И., Голубева И.В., Алиев О.И., Толстикова Т.Г., Крысин А.П., Сорокина И.В. Антиаритмическая активность n-тирозола в условиях острой ишемии и реперфузии миокарда // Бюл. экспер. биол. мед. - 2007. - Т. 143, №6. - С. 631-633.
28. Obied H.K., Prenzler P.D., Omar S.H., Ismael R., Servili M., Esposto S., Taticchi A., Selvaggini R., Urbani S. Pharmacology of olive biophenols // Advances in Molecular Toxicology / Ed. J. C. Fishbein. Oxford. - 2012. - Vol.6. - P. 195-242.
29. Plotnikov M.B., Plotnikova T.M. Tyrosol as a neuroprotector: strong effects of a "weak" antioxidant // Curr. Neuropharmacol. - 2021. - Vol.19, №4. - P. 434^48.
30. Плотников М.Б., Чернышева Г.А., Смольякова В.И., Плотникова Т.М., Сысолятин СВ., Крюков Ю.А. Противоишемическая активность л-тирозола в условиях многократной транзиторной ишемии миокарда у крыс // Бюл. экспер. биол. мед. - 2018. -Т. 165, №5. - С.566-570.
31. Samuel S.M., Thirunavukkarasu М., Penumathsa S.V., Paul D., Maulik N. Akt/FOXO3a/SIRT1-mediated cardioprotection by n-tyrosol against ischemic stress in rat in vivo model of myocardial infarction: switching gears toward survival and longevity // J. Agric. Food Chem. - 2008. - Vol.56, №20. - P. 9692-9628.
32. Коган A.X. Хирургический метод моделирования коронароокклюзионного инфаркта и аневризмы сердца у крыс // Патол. физиол. и эксперим. терапия. - 1979. - №3. -С.79-81.
33. Пирс Э. Гистохимия. - М.: Изд-во иностранной литературы, 1956. - 488 с.
34. Шаманаев А.Ю., Алиев О.И., Анищенко A.M., Сидехменова А.В., Плотников М.Б Показатели сердечной деятельности у крыс линии SHR до и после установления стабильно высокого артериального давления // Международный журнал прикладных и фундаментальных исследований. - 2016. - №4 (часть 6) - С.1115-1118.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, ослабляющее постинфарктное ремоделирование миокарда | 2020 |
|
RU2740895C1 |
| Трансляционная модель хронической сердечной недостаточности: способ и критерии оценки формирования | 2018 |
|
RU2744681C1 |
| СРЕДСТВО, УВЕЛИЧИВАЮЩЕЕ УСТОЙЧИВОСТЬ СЕРДЦА К ИШЕМИЧЕСКИМ И ПОСЛЕДУЮЩИМ РЕПЕРФУЗИОННЫМ ПОВРЕЖДЕНИЯМ | 2012 |
|
RU2488404C1 |
| ПРОТИВОИШЕМИЧЕСКОЕ СРЕДСТВО | 2008 |
|
RU2384327C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОСТИНФАРКТНОГО РЕМОДЕЛИРОВАНИЯ МИОКАРДА ЛЕВОГО ЖЕЛУДОЧКА У БОЛЬНЫХ ИНФАРКТОМ МИОКАРДА | 2011 |
|
RU2464936C1 |
| Способ оценки вероятности развития неблагоприятного ремоделирования левого желудочка сердца у больных острым инфарктом миокарда с подъемом сегмента ST | 2021 |
|
RU2770285C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЭНДОТЕЛИЙПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2563622C1 |
| СПОСОБ ЭКСПЕРИМЕНТАЛЬНОЙ ТЕРАПИИ ИНФАРКТА МИОКАРДА | 2005 |
|
RU2288738C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ НЕБЛАГОПРИЯТНЫХ СЕРДЕЧНО-СОСУДИСТЫХ СОБЫТИЙ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА С ИШЕМИЧЕСКОЙ И/ИЛИ ПОСТИНФАРКТНОЙ ДИСФУНКЦИЕЙ МИОКАРДА НА ФОНЕ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2014 |
|
RU2568577C1 |
| Средство, обладающее кардиопротекторной активностью | 2019 |
|
RU2791641C2 |
Изобретение относится к медицине, конкретно к фармакологии, и касается средств, ослабляющих постинфарктное ремоделирование миокарда. Раскрывается применение n-тирозола (n-оксифенил-β-этанол, 4-(2-гидроксиэтил)фенол) в качестве средства, ослабляющего постинфарктое ремоделирование миокарда. Использование изобретения позволяет эффективно уменьшать постинфарктое ремоделирование миокарда. 3 табл., 3 пр.
Применение n-тирозола (n-оксифенил-β-этанол, 4-(2-гидроксиэтил)фенол) в качестве средства, ослабляющего постинфарктое ремоделирование миокарда.
| Средство, ослабляющее постинфарктное ремоделирование миокарда | 2020 |
|
RU2740895C1 |
| ПРОТИВОИШЕМИЧЕСКОЕ СРЕДСТВО | 2008 |
|
RU2384327C1 |
| US 20120122777 A1, 17.05.2012 | |||
| Мазур Н.А., Черепко В.Е | |||
| Влияние каптоприла, амлодипина и пропранолола на ремоделирование левого желудочка у больных, перенесших инфаркт миокарда | |||
| Русский медицинский журнал, 1998, N6, с | |||
| ВСПОМОГАТЕЛЬНАЯ МАШИНА ДЛЯ РЕГУЛИРОВАНИЯ СКОРОСТИ ТРЕХФАЗНОГО АСИНХРОННОГО ДВИГАТЕЛЯ | 1924 |
|
SU1055A1 |
Авторы
Даты
2024-11-14—Публикация
2022-03-04—Подача