Область техники
Настоящее изобретение относится к новым соединениям, фармацевтическим композициям, содержащим их, и их применению в терапии, в частности в профилактике или лечении нарушений слуха, включая потерю слуха и шум в ушах, а также шизофрении, злоупотребления психоактивными веществами, боли и синдрома ломкой Х-хромосомы.
Предшествующий уровень техники
Семейство потенциалзависимых калиевых каналов Kv3 включает четыре представителя семейства: Kv3.1, Kv3.2, Ку3.3 и Kv3.4. Каналы Kv3 активируются путем деполяризации плазматической мембраны до напряжений более положительных чем -20 мВ; кроме того, эти каналы быстро деактивируются при реполяризации мембраны. Эти биофизические свойства обеспечивают открытие каналов в направлении пика деполяризующей фазы потенциала действия нейронов для инициирования реполяризации. Быстрое прекращение потенциала действия, опосредованного каналами Kv3, позволяет нейрону быстрее восстанавливаться, чтобы достичь подпороговых мембранных потенциалов, от которых могут быть вызваны дальнейшие потенциалы действия. В результате присутствие каналов Kv3 в определенных нейронах вносит вклад в их способность возбуждаться при высоких частотах (Rudy et al., 2001). Подтипы Kv3.1-3 преобладают в ЦНС, тогда как каналы Kv3.4 также обнаруживаются в скелетных мышцах и симпатических нейронах (Weiser et al., 1994). Подтипы Kv3.1-3 каналов дифференцированно экспрессируются подклассами интернейронов в кортикальных областях мозга и гиппокампе (например, Chow et al., 1999; Martina et al., 1998; McDonald et al., 2006; Chang et al., 2007), в таламусе (например, Kasten et al., 2007), мозжечке (например, Sacco et al., 2006; Puente et al., 2010) и ядрах слухового ствола мозга (Li et al., 2001).
Было показано, что тетраэтиламмоний (TEA) ингибирует эти каналы при низких миллимолярных концентрациях (Rudy et al., 2001), а токсины угнетающего кровь вещества (BDS) из морской анемоны Anemonia sulcala (Diochot et al., 1998) избирательно ингибируют каналы Kv3 с высокой аффинностью (Yeung et al., 2005).
Каналы Kv3 являются важными детерминантами функции мозжечка, области мозга, важной для контроля двигательной функции (Joho et al., 2009). Характеристика мышей, у которых был(и) удален(ы) один или несколько подтипов Kv3, показывает, что отсутствие Kv3.1 приводит к повышенной двигательной активности, измененной электроэнцефалографической активности и фрагментированному паттерну сна (Joho et al., 1999). Удаление Kv3.2 приводит к снижению порога судорожной готовности и изменению кортикальной электроэнцефалографической активности (Lau et al., 2000). Удаление Kv3.3 ассоциировано с легкой атаксией и двигательным дефицитом (McMahon et al., 2004). Двойная делеция Kv3.1 и Kv3.3 приводит к тяжелому фенотипу, характеризующемуся спонтанными припадками, атаксией и повышенной чувствительностью к воздействию этанола (Espinosa et al., 2001; Espinosa et al., 2008). Спонтанная мутация в гене Kv3.1 (KCNC1) вызывает прогрессирующую миоклоническую эпилепсию (Muona et al., 2014). Мутации гена Kv3.3 (KCNC3) у людей ассоцированы с формами спиноцеребеллярной атаксии (SCA13) (Figueroa et al., 2010).
Биполярное расстройство, шизофрения, тревога и эпилепсия являются тяжелыми расстройствами центральной нервной системы, которые ассоциированы со снижением функции тормозных интернейронов и передачи сигналов гамма-аминомасляной кислоты (ГАМК) (Reynolds et al., 2004; Benes et al., 2008; Brambilla et al., 2003; Aroniadou-Anderjaska et al., 2007; Ben-Ari, 2006). Парвальбумин-позитивные корзинчатые клетки, экспрессирующие каналы Kv3 в коре головного мозга и гиппокампе, играют ключевую роль в генерации ингибирования обратной связи в локальных цепях (Markram et al., 2004). Учитывая относительное преобладание возбуждающего синаптического входа над тормозящим входом в глутаматергические пирамидные нейроны в этих цепях, быстрое возбуждение интернейронов, снабжающих тормозящий вход, необходимо для обеспечения сбалансированного торможения. Кроме того, точный расчет времени тормозящего входа необходим для поддержания сетевой синхронизации, например, при генерации колебаний потенциала поля с частотой гамма, которые ассоциированы с когнитивной функцией (Fisahn et al., 2005; Engel et al., 2001). Примечательно, что снижение гамма-колебаний наблюдалось у пациентов с шизофренией (Spencer et al., 2004), и данные свидетельствуют о снижении экспрессии Kv3.1, но не Kv3.2, в дорсолатеральной префронтальной коре пациентов с шизофренией, которые не принимали антипсихотические препараты по меньшей мере за 2 месяца до смерти (Yanagi et al., 2014). Соответственно, можно ожидать, что положительные модуляторы каналов Kv3 будут усиливать возбуждающие способности определенных групп быстровозбуждающихся нейронов в головном мозге. Эти эффекты могут быть полезны при расстройствах, ассоциированных с аномальной активностью этих нейрональных групп. Кроме того, было показано, что каналы Kv3.2 экспрессируются нейронами суперхиазматического ядра (SCN), являющегося основным водителем ритма, контролирующим циркадные ритмы в ЦНС (Schulz et al., 2009).
Потенциалзависимые ионные каналы семейства Kv3 экспрессируются в высоких уровнях в ядрах слухового ствола мозга (Li et al., 2001), где они обеспечивают быстрое возбуждение нейронов, передающих слуховую информацию из улитки уха в высшие области мозга. Предполагается, что фосфорилирование каналов Kv3.1 и Kv3.3 в нейронах слухового ствола мозга способствует быстрой физиологической адаптации к уровню звука, что может играть защитную роль при воздействии шума (Desai et al., 2008; Song et al., 2005). Потеря способности к экспрессии канала Kv3.1 в центральных слуховых нейронах наблюдается у мышей с нарушением слуха (von Helm et al., 2004); кроме того, снижение экспрессии канала Kv3.1 может быть ассоциировано с потерей слуха у пожилых мышей (Jung et al., 2005), а потеря функции канала Kv3 может также сопровождаться потерей слуха, вызванной шумовой травмой (Pilali et al., 2012). Кроме того, патологическая пластичность слуховых сетей ствола мозга, вероятно, вносит свой вклад в симптомы, которые испытывают многие люди, страдающие потерей слуха различных типов. Недавние исследования показали, что регуляция функции и экспрессии канала Kv3.1 играет важную роль в контроле возбудимости слуховых нейронов (Kaczmarek et al., 2005; Anderson et al., 2018; Glait et al., 2018; Olsen et al., 2018; Chambers et al., 2017), подтверждая что этот механизм может объяснить некоторые пластические изменения, которые приводят к появлению шума в ушах. Шум в ушах может сопровождать вызванную шумом потерю слуха в результате адаптивных изменений в центральных слуховых путях от ствола мозга к слуховой коре (Roberts et al., 2010). Каналы Kv3.1 и/или Kv3.2 экспрессируются во многих из этих цепей и вносят свой вклад в функцию ГАМКергических тормозных интернейронов, которые могут контролировать функцию этих цепей.
Известно, что модуляторы Kv3.1 и/или Kv3.2 полезны в лечении боли (WO 2017/098254). В самом широком смысле боль можно разделить на острую и хроническую боль. Острую боль определяют как боль, которая купируется самостоятельно и обычно требует лечения в течение не более нескольких недель, например, послеоперационная или острая скелетно-мышечная боль, такая как при переломах (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, 2014). Хроническую боль можно определить как боль, сохраняющуюся более 1 месяца после разрешения исходной травмы, или боль, сохраняющуюся более трех месяцев. Часто нет явной причины хронической боли, и множество других проблем со здоровьем, таких как усталость, депрессия, бессонница, изменения настроения и снижение подвижности, часто сопровождают хроническую боль.
Хроническую боль можно подразделить на следующие группы: невропатическая боль, хроническая скелетно-мышечная боль и смешанная хроническая боль. Невропатическая боль обычно сопровождает повреждение тканей и возникает или вызывается повреждением нервной системы (периферической нервной системы и/или центральной нервной системы), например, ампутацией, ударом, диабетом или рассеянным склерозом. Хроническая скелетно-мышечная боль может быть симптомом таких заболеваний, как остеоартрит и хроническая боль в пояснице, и может возникать после повреждения мышечной ткани, а также травмы в области, например, переломов, растяжений и вывихов. Смешанная хроническая боль охватывает все другие типы долговременной боли и включает не являющиеся невропатическими болевые состояния, такие как раковая боль и фибромиалгия, а также головные боли и тендинит.
Хроническая боль представляет собой весьма разнородное состояние, которое остается одним из самых неприятных и трудно поддающихся лечению по клиническим показаниям (McCarberg et al., 2008; Woolf, 2010; Finnerup et al., 2015). Несмотря на годы исследований и разработки лекарств, был достигнут лишь незначительный прогресс в идентификации средств лечения, которые могут сравниться с опиоидами по эффективности без значительных побочных эффектов и риска зависимости. Потенциалзависимые ионные каналы представляют важные мишени для лечения конкретных болевых симптомов, в частности состояний невропатической боли. Кроме того, генетические мутации в определенных ионных каналах связаны с некоторыми хроническими болевыми расстройствами (Bennett et al., 2014). Примеры потенциалзависимых ионных каналов, которые исследуются в качестве фармацевтических мишеней, включают: натриевые каналы (в частности, NaV1.7) - Sun et al., 2014; Dib-Hajj et al., 2013; кальциевые каналы N-muna - Zamponi et al., 2015; калиевые каналы Kv7 - Devulder, 2010; Wickenden et al., 2009; и SLACK - Lu et al., 2015.
Гипотеза, лежащая в основе этих подходов, заключается в том, что состояния хронической боли ассоциированы с повышенной возбудимостью и/или аберрантным возбуждением периферических сенсорных нейронов, в частности нейронов, участвующих в передаче болезненных сенсорных стимулов, таких как С-волокна ганглиев задних корешков и специфических цепей внутри спинного мозга (Baranauskas et al., 1998; Cervero, 2009; Woolf et al., 2011; Baron et al., 2013). Животные модели невропатической и воспалительной хронической боли являются основным подтверждением этой гипотезы, хотя доказательства причинно-следственной связи все еще отсутствуют (Cervero, 2009).
Лекарственные средства, направленные на гипервозбудимость, такие как блокаторы натриевых каналов (например, CNV1014802, ламотриджин, карбамазепин и местные анестетики), положительные модуляторы Kv7 (например, флупертин и ретигабин) и модуляторы кальциевых каналов N-типа (например, габапентин, который взаимодействует с субъединицей α2δ кальциевого канала N-типа, и зиконитид, полученный из токсина конусообразной улитки), проявляют эффективность в моделях воспалительной и/или невропатической боли. Однако, среди этих лекарственных средств имеются противоречивые доказательства клинической эффективности, например, балансирующая эффективность и увеличенная тяжесть побочных эффектов на центральную нервную систему. Несоответствие между эффективностью в животных моделях и эффективностью у людей, вероятно, связано с рядом факторов, но, в частности, главными причинами проблемы могут быть достижимая концентрация препарата у людей (из-за плохой переносимости) и неоднородность болевых состояний человека. Для показаний боли также необходимо идентифицировать мишени, посредством которых может быть достигнуто облегчение боли с уменьшением толерантности или тахифилаксии и снижением предрасположенности к злоупотреблениям и/или риска зависимости.
Таким образом, улучшение фармакологического лечения боли сосредоточено на механизмах, которые могут обеспечить хорошую эффективность с уменьшенной тяжестью побочных эффектов, сниженной толерантностью или тахифилаксией, а также сниженными предрасположенностью к злоупотреблению и/или риском зависимости.
В последнее время каналы Kv3.4 стали мишенью, представляющей интерес для лечения хронической боли. Каналы Kv3.4 экспрессируются на нейронах ганглиев задних корешков (Ritter et al., 2012; Chien et al., 2007), где они преимущественно экспрессируются на сенсорных С-волокнах (Chien et al., 2007). Каналы Kv3 также экспрессируются определенными подмножествами нейронов спинного мозга. В частности, субъединицы Kv3.1b (Deuchars et al., 2001; Brooke et al., 2002), Kv3.3 (Brooke et al., 2006) и Kv3.4 (Brooke et al., 2004) были идентифицированы в спинном мозге грызунов, хотя и не всегда связаны с цепями, участвующими в обработке сенсорной информации. Вполне вероятно, что каналы Kv3 формируют возбуждающие свойства нейронов спинного мозга, включая двигательные нейроны.
Кроме того, недавние исследования показали, что каналы Kv3.4, экспрессирующиеся в ноцицепторах ганглиев дорсальных корешков (DRG), оказывают значительное влияние на глутаматергическую синаптическую передачу (Muqeem et al., 2018). Данные на животных моделях подтверждают регуляцию поверхностной экспрессии канала Kv3.4 по типу отрицательной обратной связи в нейронах DRG после повреждения спинного мозга, связанного с гиперчувствительностью к болевым стимулам (Ritter et al., 2015; Zemel et al., 2017; Zemel et al., 2018). Сходным образом, было замечено, что имеется регуляция экспрессии Kv3.4 по типу отрицательной обратной связи в DRG грызунов после перевязки спинного мозга (Chien et al., 2007). Это последнее исследование также показало, что интратекальное введение крысам антисмыслового олигонуклеотида для подавления экспрессии Kv3.4 приводило к гиперчувствительности к механическим стимулам. Было показано, что на инактивацию каналов Kv3.4 может влиять зависимое от протеинкиназы С фосфорилирование каналов, и что этот физиологический механизм может позволить нейронам DRG изменять свои характеристики возбуждения в ответ на болезненные стимулы (Ritter et al., 2012). Эти исследования подтверждают причинно-следственную связь между возникновением механической аллодинии и снижением экспрессии или функции канала Kv3.4. Ни в одном из этих исследований не проводилась оценка экспрессии Kv3.1, Kv3.2 или Kv3.3 в нейронах SC или DRG, и экспрессия этих двух подтипов не была явно продемонстрирована на нейронах DRG (хотя, как упоминалось выше, они распространены в определенных областях спинного мозга). Описанные выше исследования in vivo дают обоснование для модуляции Kv3.4 в качестве нового подхода к лечению определенных состояний невропатической боли.
Деменция с тельцами Леви (DLB) и болезнь Паркинсона (PD) являются тяжелыми нейродегенеративными расстройствами, которые ассоциированы с накоплением белка альфа-синуклеина в тельцах Леви, что приводит к потере связи и гибели нейрональных клеток. Симптомы DLB включают прогрессирующий когнитивный дефицит, в частности, трудности с планированием и вниманием. Зрительные галлюцинации также являются обычным явлением, возникая примерно у 60% пациентов. PD ассоциирована на начальной стадии с двигательным дефицитом, главным образом из-за потери дофаминовых нейронов. Хотя в настоящее время нет исследований, напрямую связывающих каналы Kv3 с DLB или PD, расположение и роль каналов Kv3, в частности Kv3.1, в цепях корковых и базальных ганглиев свидетельствуют о том, что модуляторы этих каналов могут улучшить симптомы DLB или PD, либо сами по себе, либо в комбинации с современными средствами лечения, такими как ингибиторы ацетилхолинэстеразы для DLB или L-DOPA для PD.
В публикациях международных заявок WO 2011/069951, WO 2012/076877, WO 2012/168710, WO 2013/175215, WO 2013/083994, WO 2013/182850, WO 2017/103604, WO 2018/020263 и WO 2018/109484 раскрыты соединения, которые являются модуляторами Kv3.1 и Kv3.2. Кроме того, полезность таких соединений продемонстрирована в животных моделях судорог, гиперактивности, расстройств сна, психоза, нарушений слуха и биполярных расстройств.
В публикации международной заявки WO 2013/182851 раскрыта модуляция каналов Kv3.3 некоторыми соединениями.
В публикации международной заявки WO 2013/175211 раскрыто, что модуляция каналов Kv3.1, Kv3.2 и/или Kv3.3 оказалась полезной для предупреждения или ограничения установления постоянной потери слуха в результате воздействия сильного шума. Преимущества такого предупреждения можно наблюдать даже после прекращения введения модулятора Kv3.1, Kv3.2 и/или Kv3.3.
В публикации международной заявки WO2017/098254 раскрыто, что модуляция каналов Kv3.1, Kv3.2 и/или Kv3.3 оказалась полезной в профилактике или лечении боли, в частности невропатической или воспалительной боли.
Остается необходимость в идентификации альтернативных модуляторов Kv3.1, Kv3.2 и/или Kv3.3, в частности модуляторов Kv3.1 и/или Kv3.2. Такие модуляторы могут демонстрировать высокую эффективность in vivo, избирательность в отношении каналов, улучшенный профиль безопасности или желаемые фармакокинетические параметры, например высокую доступность для мозга, что снижает дозу, необходимую для терапевтического эффекта in vivo. Альтернативные модуляторы могут обеспечить преимущество благодаря наличию метаболитов, отличных от известных модуляторов. Соединения, которые имеют сбалансированные модулирующие свойства в отношении Kv3.1, Kv3.2 и/или Kv3.3, могут быть желательными, например, соединения, которые модулируют Kv3.1 и Kv3.2 в той же или подобной степени. Для определенных терапевтических показаний также необходимо идентифицировать соединения с различающимся модулирующим действием в отношении каналов Kv3.1, Kv3.2 и/или Kv3.3, например соединения, которые изменяют кинетику открытия каналов или инактивации каналов и которые могут вести себя in vivo как отрицательные модуляторы каналов.
Краткое изложение сущности изобретения
Согласно настоящему изобретению предложено соединение формулы (I):
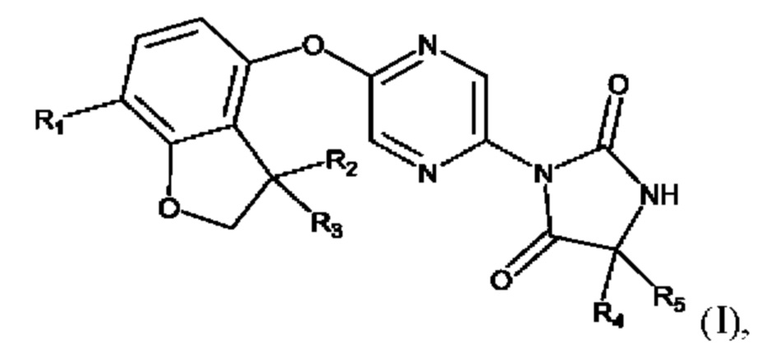
где:
R1 представляет собой Н или метил;
R2 и R3 оба представляют собой метил, или R2 и R3, вместе с атомом углерода, к которому они присоединены, образуют спироциклопропильное кольцо;
R4 представляет собой метил или этил;
R5 представляет собой Н или метил;
или R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют С3-С4 спирокарбоциклил.
Соединение формулы (I) может быть предложено в форме его соли и/или сольвата. Подходящим образом, соединение формулы (I) может быть предложено в форме его фармацевтически приемлемых соли и/или сольвата и/или его производного. В одном воплощении изобретения соединение формулы (I) предложено в форме фармацевтически приемлемой соли.
Соединения формулы (I) могут быть использованы в качестве лекарственных средств, в частности, для использования в профилактике или лечении нарушений слуха, включая потерю слуха и шум в ушах, а также шизофрении, злоупотребления психоактивными веществами, боли или синдрома ломкой Х-хромосомы.
Кроме того, предложен способ профилактики или лечения нарушений слуха, включая потерю слуха и шум в ушах, а также нарушений слуха, включающих потерю слуха и шум в ушах, а также шизофрении, злоупотребления психоактивными веществами, боли или синдрома ломкой Х-хромосомы.
Соединения формулы (I) могут быть использованы в изготовлении лекарственного средства для профилактики или лечения нарушений слуха, включая потерю слуха и шум в ушах, а также шизофрении, злоупотребления психоактивными веществами, боли или синдрома ломкой Х-хромосомы.
Также предложены фармацевтические композиции, содержащие соединение формулы (I) и фармацевтически приемлемый носитель или эксципиент.
Также предложены способы получения соединений формулы (I) и новые промежуточные соединения, используемые при получении соединений формулы (I).
Дополнительно предложены пролекарственные производные соединений формулы (I).
Подробное описание изобретения
Согласно настоящему изобретению предложены соединения формулы (I):

где:
R1 представляет собой Н или метил;
R2 и R3 оба представляют собой метил, или R2 и R3, вместе с атомом углерода, к которому они присоединены, образуют спироциклопропильное кольцо;
R4 представляет собой метил или этил;
R5 представляет собой Н или метил;
или R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют С3-С4спирокарбоциклил;
или их фармацевтически приемлемые соль и/или сольват и/или их производное.
Изложенные ниже воплощения, касающиеся относительной стереохимии и природы групп, включая R1, R2, R3, R4, R5, рассматриваются как независимые, полностью комбинируемые друг с другом, где это уместно для данных обстоятельств (т.е. где химически целесообразно), с получением дополнительных воплощений изобретения. Такие воплощения в равной степени применимы к промежуточным соединениям, которые могут быть использованы в синтезе соединения формулы (I), например соединений формул (II), (IV), (VI), (VII) и (XVI).
Соединения формулы (I) возможно могут быть предложены в форме фармацевтически приемлемых соли и/или сольвата. В одном воплощении изобретения соединение формулы (I) предложено в форме фармацевтически приемлемой соли. Во втором воплощении изобретения соединение формулы (I) предложено в форме фармацевтически приемлемого сольвата. В третьем воплощении изобретения соединение формулы (I) не находится в форме соли или сольвата.
В одном воплощении R1 представляет собой Н. Во втором воплощении R1 представляет собой метил.
В одном воплощении R2 представляет собой метил и R3 представляет собой метил. В другом воплощении R2 и R3 представляют собой спироциклопропил с образованием следующей группировки:

В одном воплощении R4 представляет собой метил. Во втором воплощении R4 представляет собой этил.
В одном воплощении R5 представляет собой водород. Во втором воплощении R5 представляет собой метил.
В одном воплощении R4 и R5 являются одинаковыми (т.е. представляют собой метил).
В воплощениях, где R4 и R5 являются разными, они могут иметь следующую стереохимическую конфигурацию:
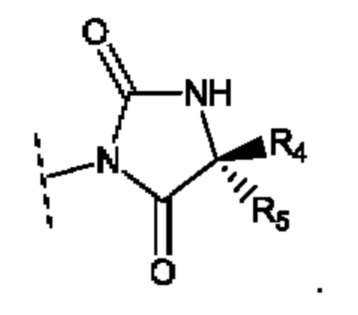
В данном воплощении, например, R4 представляет собой метил и R5 представляет собой Н, R4 представляет собой этил и R5 представляет собой Н, или R4 представляет собой этил и R5 представляет собой метил.
В воплощениях, где R4 и R5 являются разными, они могут альтернативно иметь следующую стереохимическую конфигурацию:

В данном воплощении, например, R4 представляет собой метил и R5 представляет собой Н, R4 представляет собой этил и R5 представляет собой Н, или R4 представляет собой этил и R5 представляет собой метил.
В одном воплощении R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют спироциклопропил.
В другом воплощении R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют спироциклобутил.
В одном воплощении соединение формулы (I) выбрано из группы, состоящей из:
5,5-диметил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
3-[5-[(3,3-диметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-5,5-диметил-имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-(5-спиро[2Н-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
5,5-диметил-3-(5-спиро[2Н-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
(5R)-3-[5-[(3,3-диметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-5-метил-имидазолидин-2,4-диона;
5,5-диметил-3-[5-[(3,3,7-триметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-[5-[(3,3,7-триметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-3-(5-спиро[2Н-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
(5R)-3-[5-[(3,3-диметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-имидазолидин-2,4-диона;
(5R)-5-этил-3-[5-[(3,3,7-триметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
7-[5-(7-метилспиро[2Н-бензофуран-3,1-циклопропан]-4-ил)оксипиразин-2-ил]-5,7-диазаспиро[3.4]октан-6,8-диона;
их фармацевтически приемлемых соли и/или сольвата и/или их производного.
В одном воплощении соединение формулы (I) представляет собой:
6-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-4,6-диазаспиро[2.4]гептан-5,7-дион;
его фармацевтически приемлемые соль и/или сольват и/или его производное.
В одном воплощении соединение формулы (I) представляет собой:
(5S)-5-этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-дион;
его фармацевтически приемлемые соль и/или сольват и/или его производное.
Когда соединение содержит С1-3алкильную группу, независимо от того, используется ли она сама по себе или составляет часть большей группы, данная алкильная группа может быть неразветвленной, разветвленной или циклической. Примеры С1-3алкила представляют собой метил, этил, н-пропил, изопропил и циклопропил. Ссылка на «пропил» включает н-пропил, изопропил и циклопропил.
Термин «галогено» или «галоген», как он использован здесь, относится к атому фтора, хлора, брома или йода. Конкретными примерами галогена являются фтор, хлор и бром, например, хлор или бром.
Термин «С3-4спирокарбоциклил», как он использован здесь, означает циклическую кольцевую систему, содержащую 3 или 4 атома углерода, а именно циклопропильную или циклобутильную группу, где циклическая кольцевая система присоединена к вторичному углероду через спироцентр, так что вторичный углерод является одним из этих 3-4 атомов углерода в циклическом кольце, как показано ниже:

Следует понимать, что для использования в медицине соли соединений формулы (I) должны быть фармацевтически приемлемыми. Подходящие фармацевтически приемлемые соли будут очевидны специалистам в данной области техники. Фармацевтически приемлемые соли включают соли, описанные Berge, Bighley и Monkhouse J.Pharm.Sci. (1977) 66, pp. 1-19. Такие фармацевтически приемлемые соли включают соли присоединения кислоты, образованные с неорганическими кислотами, такими как соляная, бромистоводородная, серная, азотная или фосфорная кислота, и органическими кислотами, такими как янтарная, малеиновая, уксусная, фумаровая, лимонная, винная, бензойная, пара-толуолсульфоновая, метансульфоновая или нафталинсульфоновая кислота. Соли, не являющиеся фармацевтически приемлемыми, могут быть использованы, например, при выделении соединений формулы (I), и они включены в объем данного изобретения.
Некоторые соединения формулы (I) могут образовывать соли присоединения кислоты с одним или несколькими эквивалентами кислоты. Настоящее изобретение включает в своем объеме все возможные стехиометрические и нестехиометрические формы.
Соединения формулы (I) могут быть получены в кристаллической или некристаллической форме и, в случае кристаллических форм, они могут быть возможно сольватированы, например как гидрат. Данное изобретение включает в своем объеме стехиометрические сольваты (например гидраты), а также соединения, содержащие вариабельные количества растворителя (например воды).
Следует понимать, что изобретение включает фармацевтически приемлемые производные соединений формулы (I) и что они включены в объем данного изобретения.
Используемый здесь термин «фармацевтически приемлемое производное» включает любой фармацевтически приемлемый сложный эфир или соль такого сложного эфира соединения формулы (I), которые при введении реципиенту способны обеспечить (прямо или косвенно) соединение формулы (I) или активный метаболит или их остаток.
Фармацевтически приемлемое пролекарство может быть образовано функционализацией вторичного азота гидантоина, например, группой «L», как показано ниже (где R4 и R5 являются такими, как описано выше):

В одном воплощении изобретения соединение формулы (I) функционализировано через вторичный азот гидантоина группой L, выбранной из:
а) РО(ОН)O-•М+, где М+ представляет собой фармацевтически приемлемый моновалентный противоион,
б) -РО(O-)2•2М+,
в) -РО(O-)2•D2+, где D2+ представляет собой фармацевтически приемлемый дивалентный противоион,
г) -CH(RX)-PO(OH)O-•M+, где RX представляет собой водород или С1-3алкил,
д) -CH(RX)-PO(O-)2•2М+,
е) -CH(RX)-PO(O-)2•D2+,
ж) -SO3-•M+,
з) -CH(RX)-SO3-•M+, и
и) -CO-CH2CH2-CO2•M+.
Следует понимать, что настоящее изобретение охватывает все изомеры формулы (I) и их фармацевтически приемлемые производные, включая все геометрические, таутомерные и оптические формы и их смеси (например рацемические смеси). Когда в соединениях формулы (I) присутствуют дополнительные хиральные центры, настоящее изобретение включает в своем объеме все возможные диастереоизомеры, включая их смеси. Различные изомерные формы могут быть разделены или отделены друг от друга обычными методами, или любой данный изомер может быть получен обычными методами синтеза или стереоспецифическим или асимметрическим синтезом.
Настоящее изобретение включает все изотопные формы предложенных здесь соединений по изобретению, независимо от того, находятся ли они в форме (1), где все атомы с данным атомным номером имеют массовое число (или совокупность массовых чисел), которое преобладает в природе (упоминается здесь как «природная изотопная форма»), или (2) где один или несколько атомов заменены атомами, имеющими тот же атомный номер, но массовое число, отличное от массового числа атомов, которое преобладает в природе (упоминается здесь «неприродный вариант изотопной формы»). Следует понимать, что атом может естественным образом существовать как совокупность массовых чисел. Термин «неприродный вариант изотопной формы» также включает воплощения, в которых доля атома с данным атомным номером, имеющего массовое число, реже встречающееся в природе (упоминается здесь как «нераспространенный изотоп»), была увеличена по сравнению с тем, что встречается в природе, например, до уровня более 20%, более 50%, более 75%, более 90%, более 95% или более 99% по числу атомов с этим атомным номером (последнее воплощение упоминается как «вариантная форма, обогащенная изотопами»). Термин «неприродный вариант изотопной формы» также включает воплощения, в которых доля нераспространенного изотопа снижена по сравнению с тем, который встречается в природе. Изотопные формы могут включать радиоактивные формы (т.е. в них включены радиоизотопы) и нерадиоактивные формы. Радиоактивные формы обычно представляют собой вариантные формы, обогащенные изотопами.
Таким образом, неприродный вариант изотопной формы соединения может содержать один или более искусственных или нераспространенных изотопов, таких как дейтерий (2Н или D), углерод-11 (11С), углерод-13 (13С), углерод-14 (14С), азот-13 (13N), азот-15 (15N), кислород-15 (15O), кислород-17 (17O), кислород-18 (18O), фосфор-32 (32Р), сера-35 (35S), хлор-36 (36Cl), хлор-37 (37Cl), фтор-18 (18F), йод-123 (123I), йод-125 (125I), в одном или более атомах или может содержать повышенную долю указанных изотопов по сравнению с долей, которая преобладает в природе в одном или более атомах.
Неприродные варианты изотопных форм, содержащие радиоизотопы, могут, например, быть использованы для исследований распределения лекарственного средства и/или субстрата в тканях. Радиоактивные изотопы тритий, то есть 3Н, и углерод-14, то есть 14С, особенно полезны для этой цели ввиду простоты их включения и готовых средств обнаружения. Неприродные варианты изотопных форм, которые включают дейтерий, то есть 2Н или D, могут давать определенные терапевтические преимущества, обусловленные большей метаболической стабильностью, например, увеличенный период полувыведения in vivo или уменьшенные требования к дозировке, и, следовательно, могут быть предпочтительными в некоторых обстоятельствах. Кроме того, могут быть получены неприродные варианты изотопных форм, которые включают изотопы, излучающие позитроны, такие как 11С, 18F, 15О и 13N, и могут быть полезны в исследованиях позитронно-эмиссионной топографии (PET) для изучения занятости рецепторов субстратом.
В одном воплощении соединения по изобретению предложены в природной изотопной форме.
В одном воплощении соединения по изобретению предложены в неприродном варианте изотопной формы. В конкретном воплощении неприродный вариант изотопной формы представляет собой форму, в которую включен дейтерий (т.е. 2Н или D), где водород указан в химической структуре в одном или более атомах соединения по настоящему изобретению. В одном воплощении атомы соединений по изобретению находятся в изотопной форме, которая не является радиоактивной. В одном воплощении один или более атомов соединений по изобретению находятся в изотопной форме, которая является радиоактивной. Подходящими радиоактивными изотопами являются стабильные изотопы. Подходящим образом, неприродный вариант изотопной формы представляет собой фармацевтически приемлемую форму.
В одном воплощении предложено соединение по изобретению, в котором один атом соединения существует в неприродном варианте изотопной формы. В другом воплощении предложено соединение по изобретению, в котором два или более атомов существуют в неприродном варианте изотопной формы.
Неприродные изотопные вариантные формы обычно могут быть получены общепринятыми способами, известными специалистам в данной области техники, или способами, описанными в данном документе, например, способами, аналогичными описанным в прилагаемых Примерах получения природных изотопных форм. Таким образом, неприродные изотопные вариантные формы могут быть получены с использованием подходящих изотопных вариантов (или меченых) реагентов вместо обычных реагентов, используемых в Примерах. Поскольку соединения формулы (I) предназначены для использования в фармацевтических композициях, легко понять, что каждое из них предпочтительно предложено в по существу чистой форме, например, с чистотой по меньшей мере 60%, более предпочтительно с чистотой по меньшей мере 75% и предпочтительно по меньшей мере 85%, особенно с чистотой по меньшей мере 98% (% указан в расчете на массу). Загрязненные примесями препараты соединений можно использовать для получения более чистых форм, используемых в фармацевтических композициях.
Поскольку соединения формулы (I) предназначены для использования в фармацевтических композициях, должно быть понятно, что каждое из них предпочтительно предложено в по существу чистой форме, например, с чистотой по меньшей мере 60%, более предпочтительно с чистотой по меньшей мере 75% и предпочтительно по меньшей мере 85%, особенно с чистотой по меньшей мере 98% (% указан в расчете на массу). Загрязненные примесями препараты соединений можно использовать для получения более чистых форм, используемых в фармацевтических композициях.
В общем, соединения формулы (I) могут быть получены в соответствии со способами органического синтеза, известными специалистам в данной области техники, а также иллюстративными способами, изложенными здесь ниже, способами, изложенными в Примерах, и их модификациями.
В патентных заявках WO 2011/069951, WO 2012/076877, WO 2012/168710, WO 2013/175215, WO 2013/083994, WO 2013/182850, WO 2017/103604, WO 2018/020263 и WO 2018/109484 представлены способы синтеза промежуточных соединений, которые могут быть использованы в получении соединений по настоящему изобретению.
Общие схемы синтеза
На следующих схемах подробно описаны пути синтеза соединений по изобретению и промежуточные соединения в синтезе таких соединений. На следующих схемах реактивные группы могут быть защищены защитными группами и подвергнуты снятию защиты в соответствии с установленными методиками, хорошо известными специалисту в данной области техники.
Соединения формулы (I), их соли и сольваты могут быть получены общими способами, описанными ниже. В нижеследующем описании группы R1, R2, R3, R4 и R5 имеют значения, определенные выше для соединений формулы (I), если не указано иное.
Схема 1а

стадия (1): Соединения формулы (I) могут быть получены посредством осуществления реакций перекрестного сочетания, катализируемого металлами. В этой реакции галогенпиразиновое производное формулы (II), где обычно X представляет собой Br, и гидантоин формулы (III) подвергают взаимодействию в присутствии металлического катализатора, такого как оксид меди(I), в подходящем растворителе, например в N,N-диметилацетамиде, при обычном нагревании или микроволновом нагревании.
Схема 1b

Соединения формулы (I), где R4 и R5 не представляют собой Н, могут быть получены путем нуклеофильного ароматического замещения. В этой реакции галогенпиразиновое производное формулы (IV), где обычно Y представляет собой Cl, и фенол формулы (V) подвергают взаимодействию в присутствии подходящего основания, такого как карбонат калия, в подходящем растворителе, например в N,N-диметилформамиде или в ацетонитриле, при обычном нагревании или микроволновом нагревании.
Схема 1с
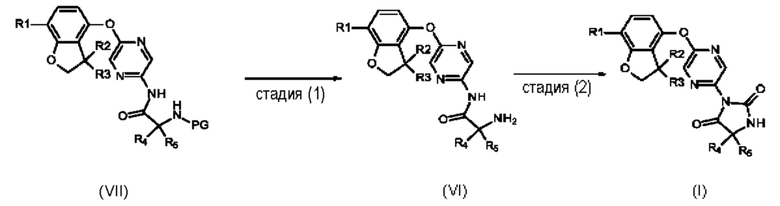
стадия (2): Соединения формулы (I) могут быть получены путем циклизации соединений формулы (VI) в подходящем растворителе, например дихлорметане, с карбонилирующим агентом, например трифосгеном, предпочтительно предварительно разбавленным в том же растворителе и добавляемым во второй раз при 0°С, в присутствии подходящего основания, например триэтиламина. Альтернативно, соединения формулы (I) могут быть получены путем циклизации соединений формулы (VI) с использованием карбонилирующего агента, такого как карбонилдиимидазол, в подходящем растворителе, таком как этилацетат, в присутствии основания, такого как триэтиламин или DIPEA.
стадия (1): Соединения формулы (VI) могут быть получены путем снятия защиты с соединений формулы (VII), где PG представляет собой защитную группу, причем подходящей защитной группой является ВОС, ВОС может быть удален в кислых условиях, например TFA в подходящем растворителе, например дихлорметане, при температуре от приблизительно 0°С до комнатной температуры.
Схема 1d
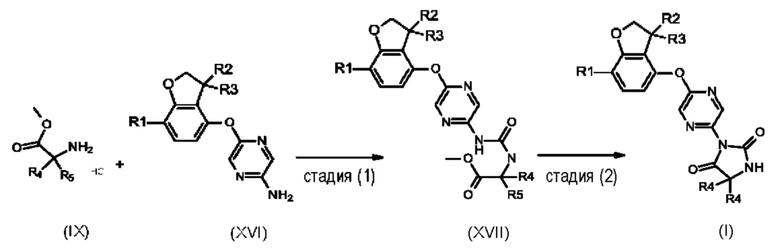
стадия (2): Соединения формулы (I) могут быть получены путем взаимодействия мочевины формулы (XVII) и подходящего основания, такого как метоксид натрия, в подходящем растворителе, таком как метанол, при температуре в диапазоне от 0°С до комнатной температуры.
стадия (1): Мочевины формулы (XVII) могут быть получены путем взаимодействия анилинов формулы (XVI) и сложных аминоэфиров (например в виде гидрохлоридной соли) формулы (IX) в подходящем растворителе, например дихлорметане или этилацетате, с карбонилирующим агентом, например трифосгеном, предпочтительно предварительно разбавленным в том же растворителе, в присутствии подходящего основания, например триэтиламина или диизопропилэтиламина, при температуре от 0°С до комнатной температуры.
Схема 2а
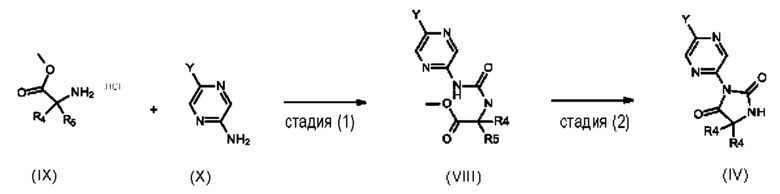
стадия (2): Соединения формулы (IV) могут быть получены путем взаимодействия мочевины формулы (VIII) и подходящего основания, такого как метоксид натрия, в подходящем растворителе, таком как метанол, при температуре в диапазоне от 0°С до комнатной температуры.
стадия (1): Мочевина формулы (VIII) может быть получена путем взаимодействия имеющегося в продаже производного галогенпиразина формулы (X), где обычно Y представляет собой Cl, и сложных аминоэфиров (например в виде гидрохлоридной соли) формулы (IX), в подходящем растворителе, например дихлорметане или этилацетате, с карбонилирующим агентом, например трифосгеном, предпочтительно предварительно разбавленным в том же растворителе, в присутствии подходящего основания, например триэтиламина или диизопропилэтиламина, при температуре в диапазоне от 0°С до комнатной температуры.
Схема 2б
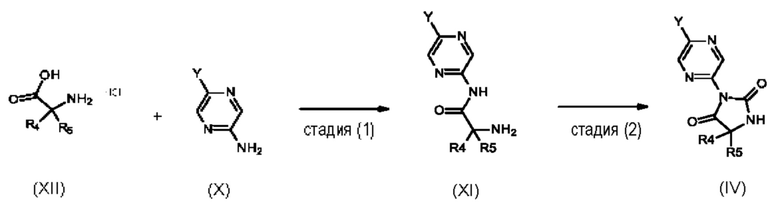
стадия (2): Соединения формулы (IV) могут быть получены путем циклизации соединений формулы (XI) в подходящем растворителе, например дихлорметане, с карбонилирующим агентом, например трифосгеном, предпочтительно предварительно разбавленным в том же растворителе и добавляемым во второй раз при 0°С, в присутствии подходящего основания, например триэтиламина.
стадия (1): Соединения формулы (XI) могут быть получены из анилинов формулы (X), где обычно Y представляет собой Cl, и аминокислот (в виде свободного основания или гидрохлоридной соли) формулы (XII) путем амидного сочетания в присутствии агента сочетания, например ТЗР, в подходящем растворителе, таком как этилацетат, ацетонитрил или их смесь.
Схема 3
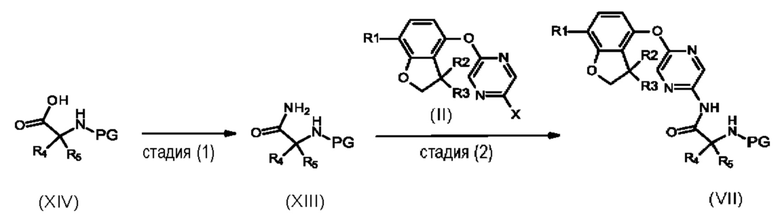
стадия (2): Соединения формулы (IV) могут быть получены посредством реакций перекрестного сочетания, катализируемого металлами. В этой реакции галогенпиразиновое производное формулы (II), где обычно X представляет собой Br, и амид формулы (XIII) подвергают взаимодействию в присутствии металлического катализатора, такого как трис(дибензилиденацетон)дипалладий(0), подходящего лиганда, такого как как дициклогексил-[2-(2,4,6-триизопропилфенил)фенил]фосфан (XPhos), и подходящего основания, такого как карбонат цезия, в подходящем растворителе, например в 1,4-диоксане, при обычном нагревании или микроволновом нагревании. Альтернативно, в этой реакции галогенпиразиновое производное формулы (II), где обычно X представляет собой Br, и амид формулы (XIII) подвергают взаимодействию в присутствии металлического катализатора, такого как йодид меди(I), подходящего лиганда, такого как N,N'-диметилэтан-1,2-диамин, и подходящего основания, такого как карбонат калия, в подходящем растворителе, например в 1-бутаноле, при обычном нагревании или микроволновом нагревании. Другой альтернативой получения соединений формулы (IV) является взаимодействие галогенпиразинового производного формулы (II), где обычно X представляет собой Br, и амида формулы (XIII), в присутствии металлического катализатора, такого как ацетат палладия(II), подходящего лиганда, такого как Xantphos, и подходящего основания, такого как карбонат цезия, в подходящем растворителе, например в 1,4-диоксане, при обычном нагревании или микроволновом нагревании.
стадия (1): Соединения формулы (XIII) могут быть получены из N-защищенных (например, посредством ВОС) аминокислот формулы (XIV) и амина, такого как гексаметилдисилазан, путем амидного сочетания в присутствии основания, например DIPEA, и агента сочетания, например HATU или TBTU, в растворителе, таком как N,N-диметилформамид.
Схема 4
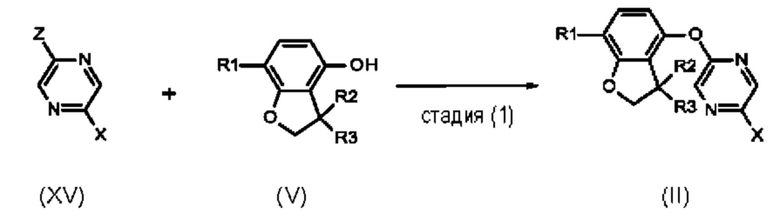
стадия (1): Соединения формулы (II), где обычно X представляет собой Br, могут быть получены путем нуклеофильного ароматического замещения. В этой реакции производное галогенпиразина формулы (XV), где обычно X и Z оба представляют собой Br, и фенол формулы (V) подвергают взаимодействию в присутствии основания, такого как карбонат калия, в подходящем растворителе, например в N,N-диметилформамиде, при обычном нагревании или микроволновом нагревании.
Схема 5
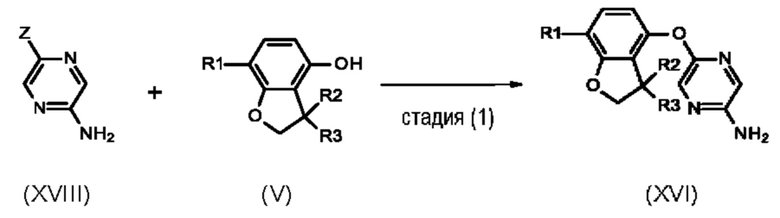
стадия (1): анилины формулы (XVI) могут быть получены посредством осуществления реакций перекрестного сочетания, катализируемых металлами. В этой реакции производное галогенпиразина формулы (XVIII), где обычно Z представляет собой Br, и фенол формулы (V) подвергают взаимодействию в присутствии металлического катализатора, такого как йодид меди(I), подходящей лигандоподобной пиколиновой кислоты в подходящем растворителе, например в N,N-диметилформамиде или N,N-диметилацетамиде, при обычном нагревании или микроволновом нагревании, возможно, может быть использовано подходящее основание, такое как карбонат калия или карбонат цезия.
Схема 6
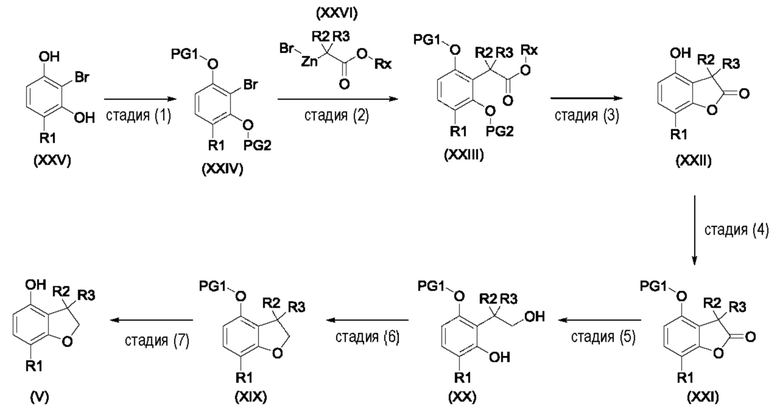
На Схеме 6, показанной выше, PG1 и PG2 представляют собой подходящие защитные группы. PG1 на стадиях (1)-(3) может отличаться от PG1 на стадиях (4)-(7). Подходящие защитные группы включают бензил, тетрагидропиранил или метилоксиметил. Подходящим образом, PG2 является такой же как PG1, например, обе представляют собой бензил.
Описание схемы, где PG1 и PG2 обе представляют собой бензил
стадия (7): Фенолы формулы (V) могут быть получены из бензилированных соединений формулы (XIX) путем снятия защиты, например, с использованием металлического катализатора, такого как палладий на углероде, и источника водорода, такого как атмосфера водорода или формиат аммония, в подходящем растворителе, таком как этанол или метанол, при температуре в диапазоне от комнатной температуры до температуры дефлегмации.
стадия (б): Бензилированные соединения формулы (ХГХ) могут быть получены из диолов формулы (XX) с использованием основания, такого как трет-бутоксид калия, и подходящего растворителя, такого как диметилкарбонат, при температуре в диапазоне от комнатной температуры до температуры дефлегмации.
стадия (5): Диолы формулы (XX) могут быть получены из лактонов формулы (XXI) с использованием восстановителя, такого как алюмогидрид лития, в подходящем растворителе, таком как THF, при температуре в диапазоне от 0°С до комнатной температуры.
стадия (4): Лактоны формулы (XXI) могут быть получены из фенолов формулы (XXII) с использованием бензилирующего агента, такого как бензилбромид, в присутствии основания, такого как карбонат калия, в подходящем растворителе, таком как ацетонитрил или THF или их смесь, при температуре в диапазоне от комнатной температуры до температуры дефлегмации.
стадия (3): Фенолы формулы (XXII) могут быть получены из дибензилированных сложных эфиров формулы (XXIII), где Rx представляет собой подходящую алкильную группу, такую как метил или этил, с использованием металлического катализатора, такого как палладий на углероде, и источника водорода, такого как атмосфера водорода или формиат аммония, в подходящем растворителе, таком как этанол или метанол, при температуре в диапазоне от комнатной температуры до температуры дефлегмации.
стадия (2): дибензилированные сложные эфиры формулы (XXIII), где Rx представляет собой подходящую алкильную группу, такую как метил или этил, могут быть получены из дибензилированных бромпроизводных формулы (XXIV) с использованием предварительно образованных цинкорганических производных формулы (XXVI), где Rx представляет собой подходящую алкильную группу, такую как метил или этил, в присутствии металлического каталитического комплекса, такого как бис(три-трет-бутилфосфин)палладий(0), в подходящем растворителе, таком как THF или DMF или их смесь, при температуре в диапазоне от комнатной температуры до температуры дефлегмации.
стадия (1): дибензилированные бромпроизводные формулы (XXIV) могут быть получены из имеющихся в продаже производных формулы (XXV) с использованием бензилирующего агента, такого как бензилбромид, в присутствии основания, такого как карбонат калия, в подходящем растворителе, таком как ацетонитрил, THF или ацетон или их смесь, при температуре в диапазоне от комнатной температуры до температуры дефлегмации.
Когда PG1 и/или PG2 представляют собой защитные группы, такие как тетрагидропиранил или метилоксиметил, применимы обычные условия введения/снятия защиты:
• Условия защиты фенолов тетрагидропиранилом включают взаимодействие фенола с дигидро-2Н-пираном в присутствии катализатора, такого как C:Py•p-MePhSO3H, в подходящем растворителе, таком как дихлорметан, при температуре в диапазоне от 0°С до температуры дефлегмации.
• Условия отщепления тетрагидропиранильной защитной группы от фенолов включают взаимодействие ТНР-защищенного фенола в присутствии кислоты, такой как серная кислота или p-MePhSO3H или HCl, в подходящем растворителе, таком как метанол или этанол, при температуре в диапазоне от 0°С до температуры дефлегмации.
• Условия защиты фенолов метилоксиметилом включают взаимодействие фенола с хлорметилметиловым эфиром в присутствии основания, такого как карбонат калия, в подходящем растворителе, таком как тетрагидрофуран или ацетонитрил, при температуре в диапазоне от 0°С до температуры дефлегмации.
• Условия отщепления метилоксиметиловой защитной группы от фенолов включают взаимодействие МОМ-защищенного фенола в присутствии кислоты, такой как серная кислота или p-MePhSO3H или HCl, в подходящем растворителе, таком как метанол или этанол, при температуре в диапазоне от 0°С до температуры дефлегмации.
Схема 7
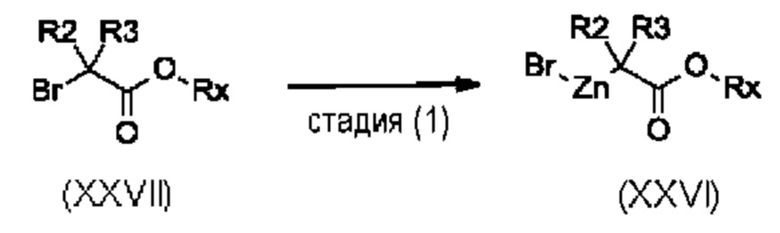
Стадия (1): Цинкорганические производные формулы (XXVI), где Rx представляет собой подходящую алкильную группу, такую как метил или этил, могут быть получены путем добавления имеющихся в продаже бромэфиров формулы (XXVII) к кипящей с обратным холодильником суспензии цинка(0) в присутствии 1,2-дибромэтана и хлортриметилсилана в подходящем растворителе, таком как THF.
Способы по изобретению
Согласно дополнительным аспектам настоящего изобретения предложены способы получения соединений формулы (I) и их производных, а также способы получения промежуточных соединений в синтезе соединений формулы (I).
Способы по изобретению описаны выше и включают любую индивидуальную стадию многостадийной схемы.
Промежуточные соединения
Настоящее изобретение также относится к новым промежуточным соединениям в синтезе соединений формулы (I). Такие новые промежуточные соединения включают соединения формул (II), (IV), (VI), (VII), (VIII), (XI), (XVI) и (XVII). Также представляют интерес промежуточные соединения формул (XIX)-(XXIV). Соли, такие как фармацевтически приемлемые соли, таких промежуточных соединений также предусмотрены настоящим изобретением.
Таким образом, промежуточные соединения по изобретению включают:
- соединения формулы (II):
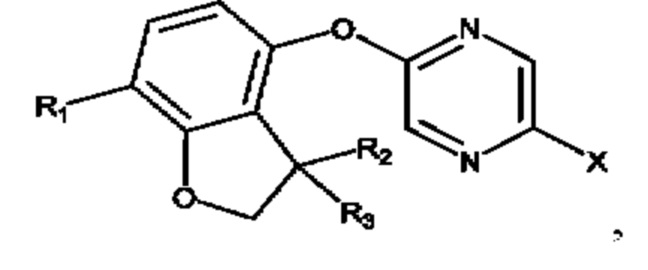
где R1, R2 и R3 являются такими, как определено выше, X представляет собой галоген, такой как Br;
- соединения формулы (IV):
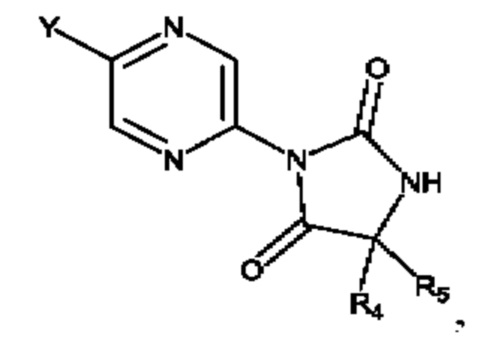
где R1, R2 и R3 являются такими, как определено выше, Y представляет собой галоген, такой как Cl;
- соединения формулы (VI):
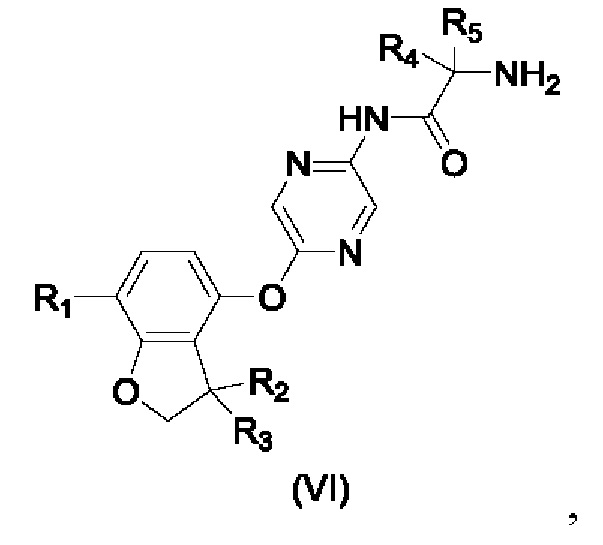
где R1, R2, R3, R4 и R5 являются такими, как определено выше;
- соединения формулы (VII):
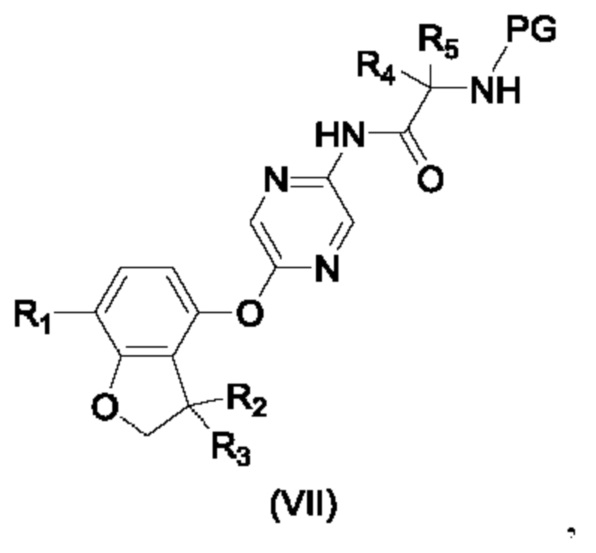
где R1, R2, R3, R4 и R5 являются такими, как определено выше, PG представляет собой подходящую защитную группу, такую как ВОС;
- соединения формулы (XVI):
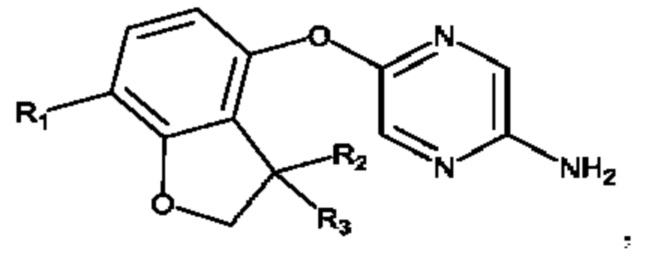
где R1, R2 и R3 являются такими, как определено выше.
Модуляция Kv3.1, Kv3.2 и/или Kv3.3
Соединения формулы (I) по настоящему изобретению представляют собой модуляторы Kv3.1. Соединения формулы (I) также могут быть модуляторами Kv3.2 и/или Kv3.3. Соединения по изобретению могут быть протестированы в анализах Биологического Примера 1 для определения их модулирующих свойств в отношении каналов Kv3.1 и/или Kv3.2 и/или Kv3.3.
«Модулятор», как используют здесь, относится к соединению, которое способно вызывать по меньшей мере 10%-ную потенциацию, и подходящим образом по меньшей мере 20%-ную потенциацию цельноклеточных токов, опосредованных человеческим Kv3.1 и/или человеческим Kv3.2 и/или человеческим Kv3.3 каналами, рекомбинантно экспрессированными в клетках млекопитающих.
Термин «Kv3.1, Kv3.2 и/или Kv3.3» должен означать то же, что и «Kv3.1 и/или Kv3.2 и/или Kv3.3», и может быть также обозначен как «Kv3.1/Kv3.2/Kv3.3».
В одном воплощении модулятор способен продуцировать по меньшей мере 10%-ную потенциацию и подходящим образом по меньшей мере 20%-ную потенциацию цельноклеточных токов, опосредованных человеческими каналами Kv3.1, рекомбинантно экспрессированными в клетках млекопитающих. Подходящим образом, рЕС50 модулятора находится в диапазоне 4-7 (например 5-6,5).
В одном воплощении модулятор способен продуцировать по меньшей мере 10%-ную потенциацию и подходящим образом по меньшей мере 20%-ную потенциацию цельноклеточных токов, опосредованных человеческими каналами Kv3.2, рекомбинантно экспрессированными в клетках млекопитающих. Подходящим образом, рЕС50 модулятора находится в диапазоне 4-7 (например 5-6,5).
В одном воплощении модулятор способен продуцировать по меньшей мере 10%-ную потенциацию и подходящим образом по меньшей мере 20%-ную потенциацию цельноклеточных токов, опосредованных человеческими каналами Kv3.3, рекомбинантно экспрессированными в клетках млекопитающих. Подходящим образом, рЕС50 модулятора находится в диапазоне 4-7 (например 5-6,5).
В другом воплощении модулятор способен продуцировать по меньшей мере 10%-ную потенциацию и подходящим образом по меньшей мере 20%-ную потенциацию цельноклеточных токов, опосредованных человеческими каналами Kv3.1 и Kv3.2, рекомбинантно экспрессированными в клетках млекопитающих.
В другом воплощении модулятор способен продуцировать по меньшей мере 10%-ную потенциацию и подходящим образом по меньшей мере 20%-ную потенциацию цельноклеточных токов, опосредованных человеческими каналами Kv3.1 и Kv3.3, рекомбинантно экспрессированными в клетках млекопитающих.
В другом воплощении модулятор способен продуцировать по меньшей мере 10%-ную потенциацию и подходящим образом по меньшей мере 20%-ную потенциацию цельноклеточных токов, опосредованных человеческими каналами Kv3.2 и Kv3.3, рекомбинантно экспрессированными в клетках млекопитающих.
В другом воплощении модулятор способен продуцировать по меньшей мере 10%-ную потенциацию и подходящим образом по меньшей мере 20%-ную потенциацию цельноклеточных токов, опосредованных человеческими каналами Kv3.1, Kv3.2 и Kv3.3, рекомбинантно экспрессированными в клетках млекопитающих.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или производные могут быть использованы для лечения или профилактики заболевания или расстройства, при котором требуется модулятор каналов Kv3.1 или Kv3.2 или Kv3.1 и Kv3.2. Как используют здесь, модулятор Kv3.1 или Kv3.2 или Kv3.1 и Kv3.2 представляет собой соединение, которое изменяет свойства этих каналов либо положительно, либо отрицательно. В конкретном аспекте данного изобретения соединение формулы (I) является положительным модулятором. Соединения по изобретению могут быть протестированы в анализе Биологического Примера 1 для определения их модулирующих свойств.
В одном воплощении данного изобретения соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или их производные являются селективными в отношении модуляции каналов Kv3.1 по сравнению с модуляцией каналов Kv3.2. Под селективным подразумевают, что соединения демонстрируют, например, по меньшей мере 2-кратную, 5-кратную или 10-кратную активность в отношении каналов Kv3.1 по сравнению с каналами Kv3.2. Активность соединения подходящим образом количественно определяют по его эффективности, на что указывает значение Ее50.
В другом воплощении изобретения соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или их производные являются селективными в отношении модуляции каналов Kv3.2 по сравнению с модуляцией каналов Kv3.1. Опять же, под селективным подразумевают, что соединения демонстрируют, например, по меньшей мере 2-кратную, 5-кратную или 10-кратную активность в отношении каналов Kv3.2 по сравнению с каналами Kv3.1.
В конкретном воплощении данного изобретения соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или их производные демонстрируют сопоставимую активность между модуляцией каналов Kv3.1 и Kv3.2, например, активность в отношении одного канала менее чем 2-кратную по сравнению с другим каналом, например, менее чем в 1,5 раза выше или менее чем в 1,2 раза выше.
При некоторых расстройствах может быть полезным использование модулятора Kv3.3 или Kv3.1, или Kv3.3 и Kv3.1, который демонстрирует определенный профиль селективности между этими двумя каналами. Например, соединение может быть селективным в отношении модуляции каналов Kv3.3 по сравнению с модуляцией каналов Kv3.1, демонстрируя, например, по меньшей мере 2-кратную, 5-кратную или 10-кратную активность в отношении каналов Kv3.3 по сравнению с каналами Kv3.1.
В другом воплощении данного изобретения соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или их производные являются селективными в отношении модуляции каналов Kv3.1 по сравнению с модуляцией каналов Kv3.3. Опять же, под селективным подразумевают, что соединения демонстрируют, например, по меньшей мере 2-кратную, 5-кратную или 10-кратную активность в отношении каналов Kv3.1 по сравнению с каналами Kv3.3.
В конкретном воплощении данного изобретения соединение может демонстрировать сопоставимую активность между модуляцией каналов Kv3.3 и Kv3.1, например, активность в отношении каждого канала менее чем 2-кратную по сравнению с другим каналом, например, менее чем в 1,5 раза выше или менее чем в 1,2 раза выше.
При определенных расстройствах может быть полезным использование модулятора Kv3.3 или Kv3.2, или Kv3.3 и Kv3.2, который демонстрирует определенный профиль селективности между этими двумя каналами. Соединение может быть селективным в отношении модуляции каналов Kv3.3 по сравнению с модуляцией каналов Kv3.2, демонстрируя, например, по меньшей мере 2-кратную, 5-кратную или 10-кратную активность в отношении каналов Kv3.3 по сравнению с каналами Kv3.2.
В другом воплощении изобретения соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или их производные являются селективными в отношении модуляции каналов Kv3.2 по сравнению с модуляцией каналов Kv3.3. Опять же, под селективным подразумевают, что соединения демонстрируют, например, по меньшей мере 2-кратную, 5-кратную или 10-кратную активность в отношении каналов Kv3.2 по сравнению с каналами Kv3.3.
В другом конкретном воплощении соединение может демонстрировать сопоставимую активность между модуляцией каналов Kv3.3 и Kv3.2, например, активность для каждого канала менее чем 2-кратную по сравнению с другим каналом, например, менее чем в 1,5 раза выше или менее чем в 1,2 раза выше.
В еще одном конкретном воплощении данного изобретения соединение может демонстрировать сопоставимую активность между модуляцией каналов Kv3.3, Kv3.2 и Kv3.1, например, активность для каждого канала менее чем 2-кратную по сравнению с другим каналом, например, менее чем в 1,5 раза выше или менее чем в 1,2 раза выше. Активность соединения подходящим образом количественно определяют по его эффективности, на что указывает значение ЕС50.
Терапевтические способы
В данном изобретении также предложено соединение формулы (I) или его фармацевтически приемлемая соль и/или сольват (например, соль) и/или производное для использования в лечении или профилактике заболевания или расстройства, при котором требуется модулятор Kv3.1, Kv3.2 и/или Kv3.3, например, при заболеваниях и расстройствах, упомянутых здесь ниже.
В данном изобретении предложен способ лечения или предупреждения заболевания или расстройства, при котором требуется модулятор Kv3.1, Kv3.2 и/или Kv3.3, например, заболеваний и расстройств, упомянутых здесь ниже, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I) или его фармацевтически приемлемых соли и/или сольвата (например, соли) и/или его производного.
В данном изобретении также предложено применение соединения формулы (I) или его фармацевтических приемлемых соли и/или сольвата (например, соли) и/или производного в изготовлении лекарственного средства для лечения или профилактики заболевания или расстройства, при котором требуется модулятор Kv3.1, Kv3.2 и/или Kv3.3, например, заболеваний и расстройств, упомянутых здесь ниже.
В одном воплощении предложено соединение формулы (I) или его фармацевтически приемлемые соль и/или сольват и/или его производное для применения в качестве лекарственного средства.
Используемый здесь термин «лечение» или «лечить» включает контроль, смягчение, уменьшение или модуляцию болезненного состояния или его симптомов.
Термин «профилактика» используют здесь для обозначения предупреждения симптомов заболевания или расстройства у субъекта или предупреждения повторного появления симптомов заболевания или расстройства у страдающего болезнью субъекта и не ограничивается полным предупреждением болезни.
Подходящим образом субъект представляет собой человека.
Заболевания или расстройства, которые могут быть опосредованы модуляцией каналов Kv3.1 и/или Kv3.2, могут быть выбраны из приведенного ниже перечня. Цифры в скобках после перечисляемых ниже заболеваний относятся к классификационному коду в Руководстве по диагностике и статистике психических расстройств, 4-е издание (Diagnostic and Stalistical Manual of Mental Disorders (DSM-IV)), опубликованном Американской психиатрической ассоциацией, и/или в Международной классификации болезней, 10-е издание (МКБ-10).
В одном воплощении изобретения соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или производные могут быть использованы для лечения или профилактики заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона.
В одном воплощении данного изобретения соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или их производные могут быть использованы для лечения или профилактики заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, включая потерю слуха и шум в ушах, шизофрении, злоупотребления психоактивными веществами, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона.
В одном воплощении данного изобретения соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или их производные могут быть использованы для лечения или профилактики заболевания или расстройства, выбранного из группы, состоящей из синдрома ломкой Х-хромосомы, болезни Ретта и болезни Альцгеймера.
В данном изобретении предложен способ профилактики или лечения заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I) или его фармацевтически приемлемых соли и/или сольвата (например, соли) и/или его производного.
В данном изобретении также предложено применение соединения формулы (I) или его фармацевтически приемлемых соли и/или сольвата (например, соли) и/или его производного в изготовлении лекарственного средства для лечения или профилактики заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона.
В конкретном воплощении данного изобретения предложено соединение формулы (I) или его фармацевтически приемлемые соли и/или сольваты (например, соли) и/или его производные для использования в лечении или профилактике нарушений слуха. Нарушения слуха включают слуховую невропатию, расстройство слуховой обработки информации, потерю слуха, которая включает внезапную потерю слуха, вызванную шумом потерю слуха, вызванную приемом веществ потерю слуха и потерю слуха у взрослых возраста старше 60, старше 65, старше 70 или старше 75 лет (старческая тугоухость), и шум в ушах.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики болезни Меньера, нарушений равновесия и заболеваний внутреннего уха.
В конкретном воплощении данного изобретения предложено соединение формулы (I) или его фармацевтически приемлемые соли и/или сольваты (например, соли) и/или его производные для использования в лечении или профилактике шизофрении. Шизофрения включает подтипы: параноидальный тип (295.30), дезорганизованный тип (295.10), кататонический тип (295.20), недифференцированный тип (295.90) и остаточный тип (295.60); шизофреноформное расстройство (295.40); шизоаффективное расстройство (295.70), включая подтипы биполярный тип и депрессивный тип; бредовое расстройство (297.1), включая подтипы эротоманиакальный подтип, подтип с манией величия, ревнивый подтип, подтип преследования, соматический подтип, смешанный тип и неуточненный тип; кратковременное психотическое расстройство (298.8); общее психотическое расстройство (297.3); психотическое расстройство, вызванное общим заболеванием, включая подтипы с бредом и с галлюцинациями; вызванное приемом психоактивных веществ психотическое расстройство, включая подтипы с бредом (293.81) и с галлюцинациями (293.82); и психотическое расстройство неуточненное (298.9).
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики депрессии и расстройств настроения, включая большой депрессивный эпизод, маниакальный эпизод, смешанный эпизод и гипоманиакальный эпизод; депрессивных расстройств, включая большое депрессивное расстройство, дистимическое расстройство (300.4), депрессивное расстройство неуточненное (311); биполярных расстройств, включая биполярное расстройство I типа, биполярное расстройство II типа (рекуррентные большие депрессивные эпизоды с гипоманиакальными эпизодами) (296.89), циклотимическое расстройство (301.13) и биполярное расстройство неуточненное (296.80); других расстройств настроения, включая расстройство настроения, вызванное общим заболеванием (293.83), включающее подтипы с признаками депрессии, с эпизодом, подобным большой депрессии, с признаками мании и со смешанными признаками, вызванное приемом психоактивных веществ расстройство настроения (включая подтипы с признаками депрессии, с признаками мании и со смешанными признаками) и расстройство настроения неуточненное (296.90); сезонного аффективного расстройства.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики эпилепсии (включая, без ограничения, локализованные эпилепсии, генерализованные эпилепсии, эпилепсии с генерализованными и локальными припадками и т.п.), припадков, связанных с синдромом Леннокса-Гасто, припадков как осложнения заболевания или состояния (таких как припадки, ассоциированные с энцефалопатией, фенилкетонурией, ювенильной формой болезни Гоше, прогрессирующей миоклонической эпилепсией Лундборга, инсультом, травмой головы, стрессом, гормональными изменениями, употреблением лекарственных средств или синдромом их отмены, употреблением алкоголя или синдромом его отмены, лишением сна, лихорадкой, инфекцией и тому подбное), эссенциального тремора, синдрома беспокойных ног, парциальных и генерализованных припадков (включая тонические, клонические, тонико-клонические, атонические, миоклонические, малые эпилептические припадки), вторичных генерализованных припадков, височной эпилепсии, малых эпилептических форм эпилепсии (включая детские, ювенильные, миоклонические, фотосенситивные и паттерн-сенситивные), тяжелых эпилептических энцефалопатии (включая связанные с гипоксией и синдром Расмуссена), фебрильных судорог, эпилепсии парциальной непрерывной, прогрессирующей миоклонической эпилепсии (включая болезнь Унферрихта-Лундборга и болезнь Лафора), посттравматических припадков/эпилепсии, включая связанные с травмой головы, простых рефлекторных эпилепсии (включая фотосенситивные, соматосенсорные и проприоцептивные, аудиогенные и вестибулярные), метаболических расстройств, часто ассоциированных с эпилепсией, таких как пиридоксин-зависимая эпилепсия, синдром курчавых волос при болезни Менкеса, болезнь Краббе, эпилепсия вследствие злоупотребления алкоголем и наркотиками (например кокаином), пороков развития коры, ассоциированных с эпилепсией (например, синдром двойной коры головного мозга или субкортикальная лентовидная гетеротопия), хромосомных аномалий, ассоциированных с припадками или эпилепсией, таких как частичная моносомия (15Q)/синдром Ангельмана).
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики расстройств, связанных с приемом психоактивных веществ, включая расстройства, вызванные употреблением психоактивных веществ, такие как зависимость от психоактивных веществ, пристрастие к психоактивным веществам и злоупотребление психоактивными веществами; вызванные приемом психоактивных веществ расстройства, такие как интоксикация психоактивными веществами, синдром отмены психоактивных веществ, вызванный приемом психоактивных веществ делирий, вызванная приемом психоактивных веществ персистирующая деменция, вызванное приемом психоактивных веществ персистирующее амнестическое расстройство, вызванное приемом психоактивных веществ психотическое расстройство, вызванное приемом психоактивных веществ расстройство настроения, вызванное приемом психоактивных веществ тревожное расстройство, вызванная приемом психоактивных веществ сексуальная дисфункция, вызванное приемом психоактивных веществ расстройство сна и галлюциногенное персистирующее расстройство восприятия (вспышки прошлого); расстройства, связанные с приемом алкоголя, такие как алкогольная зависимость (303.90), злоупотребление алкоголем (305.00), алкогольная интоксикация (303.00), синдром отмены алкоголя (291.81), алкогольный интоксикационный делирий, делирий отмены алкоголя, вызванная алкоголем персистирующая деменция, вызванное алкоголем персистирующее амнестическое расстройство, вызванное алкоголем психотическое расстройство, вызванное алкоголем расстройство настроения, вызванное алкоголем тревожное расстройство, вызванная алкоголем сексуальная дисфункция, вызванное алкоголем расстройство сна и вызванное алкоголем родственное расстройство неуточненное (291.9); расстройства, связанные с приемом амфетамина (или амфетаминоподобных веществ), такие как зависимость от амфетамина (304.40), злоупотребление амфетамином (305.70), интоксикация амфетамином (292.89), синдром отмены амфетамина (292.0), амфетаминовый интоксикационный делирий, вызванное амфетамином психотическое расстройство, вызванное амфетамином расстройство настроения, вызванное амфетамином тревожное расстройство, вызванная амфетамином сексуальная дисфункция, вызванное амфетамином расстройство сна и вызванное амфетамином родственное расстройство неуточненное (292.9); расстройства, связанные с приемом кофеина, такие как интоксикация кофеином (305.90), вызванное кофеином тревожное расстройство, вызванное кофеином расстройство сна и вызванное кофеином родственное расстройство неуточненное (292.9); расстройства, связанные с приемом каннабиноидов, такие как зависимость от каннабиноидов (304.30), злоупотребление каннабиноидами (305.20), интоксикация каннабиноидами (292.89), интоксикация каннабиноидами с делирием, вызванное приемом каннабиноидов психотическое расстройство, вызванное приемом каннабиноидов тревожное расстройство и связанное с каннабиноидами расстройство неуточненное (292.9); расстройства, связанные с приемом кокаина, такие как зависимость от кокаина (304.20), злоупотребление кокаином (305.60), интоксикация кокаином (292.89), синдром отмены кокаина (292.0), кокаиновый интоксикационный делирий, вызванное кокаином психотическое расстройство, вызванное кокаином расстройство настроения, вызванное кокаином тревожное расстройство, вызванная кокаином сексуальная дисфункция, вызванное кокаином расстройство сна и вызванное кокаином родственное расстройство неуточненное (292.9); расстройства, связанные с галлюциногенами, такие как зависимость от галлюциногенов (304.50), злоупотребление галлюциногенами (305.30), интоксикация галлюциногенами (292.89), вызванное галлюциногенами персистирующее расстройство восприятия (вспышки прошлого) (292.89), вызванный галлюциногенами интоксикационный делирий, вызванное галлюциногенами психотическое расстройство, вызванное галлюциногенами расстройство настроения, вызванное галлюциногенами тревожное расстройство и вызванное галлюциногенами родственное расстройство неуточненное (292.9); расстройства, связанные с ингалянтами, такие как зависимость от ингалянтов (304.60), злоупотребление ингалянтами (305.90), интоксикация ингалянтами (292.89), вызванный ингалянтами интоксикационный делирий, вызванная ингалянтами персистирующая деменция, вызванное ингалянтами психотическое расстройство, вызванное ингалянтами расстройство настроения, вызванное ингалянтами тревожное расстройство и вызванное ингалянтами родственное расстройство неуточненное (292.9); расстройства, связанные с никотином, такие как никотиновая зависимость (305.1), синдром отмены никотина (292.0) и вызванное никотином родственное расстройство неуточненное (292.9); расстройства, связанные с приемом опиоидов, такие как опиоидная зависимость (304.00), злоупотребление опиоидами (305.50), опиоидная интоксикация (292.89), синдром отмены опиоидов (292.0), вызванный опиоидами интоксикационный делирий, вызванное опиоидами психотическое расстройство, вызванное опиоидами расстройство настроения, вызванная опиоидами сексуальная дисфункция, вызванное опиоидами расстройство сна и вызванное опиоидами родственное расстройство неуточненное (292.9); расстройства, связанные с фенциклидином (или фенциклидин-подобными веществами), такие как зависимость от фенциклидина (304.60), злоупотребление фенциклидином (305.90), интоксикация фенциклидином (292.89), вызванный фенциклидином интоксикационный делирий, вызванное фенциклидином психотическое расстройство, вызванное фенциклидином расстройство настроения, вызванное фенциклидином тревожное расстройство и вызванное фенциклидином родственное расстройство неуточненное (292.9); расстройства, связанные с седативными, снотворными или анксиолитическими средствами, такие как зависимость от седативных, снотворных или анксиолитических средств (304.10), злоупотребление седативными, снотворными или анксиолитическими средствами (305.40), интоксикация седативными, снотворными или анксиолитическими средствами (292.89), синдром отмены седативных, снотворных или анксиолитических средств (292.0), вызванный седативными, снотворными или анксиолитическими средствами интоксикационный делирий, вызванный седативными, снотворными или анксиолитическими средствами делирий при абстиненции, вызванная седативными, снотворными или анксиолитическими средствами персистирующая деменция, вызванное седативными, снотворными или анксиолитическими средствами персистирующее амнестическое расстройство, вызванное седативными, снотворными или анксиолитическими средствами психотическое расстройство, вызванное седативными, снотворными или анксиолитическими средствами расстройство настроения, вызванное седативными, снотворными или анксиолитическими средствами тревожное расстройство, вызванная седативными, снотворными или анксиолитическими средствами сексуальная дисфункция, вызванное седативными, снотворными или анксиолитическими средствами расстройство сна и вызванное седативными, снотворными или анксиолитическими средствами родственное расстройство неуточненное; расстройство, связанное с употреблением нескольких веществ, такое как зависимость от нескольких веществ (304.80); и другие (или неизвестные) расстройства, связанные с приемом веществ, такими как анаболические стероиды, нитратные летучие вещества и оксид азота.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики тревожных расстройств, включая паническую атаку; паническое расстройство, включая паническое расстройство без агорафобии (300.01) и паническое расстройство с агорафобией (300.21); агорафобию; агорафобию без панического расстройства в анамнезе (300.22), специфическую фобию (300.29, ранее называемая простой фобией, включая подтипы: фобия животных, фобия естественных явлений окружающего мира, фобия вида крови/инъекций/травм, фобия определенной ситуации и другие типы), социальную фобию (социальное тревожное расстройство, 300.23), обсессивно-компульсивное расстройство (300.3), посттравматическое стрессовое расстройство (309.81), острое стрессовое расстройство (308.3), генерализованное тревожное расстройство (300.02), тревожное расстройство, вызванное общим заболеванием (293.84), тревожное расстройство, вызванное приемом психоактивных веществ, тревожное расстройство, вызванное разлукой (309.21), нарушения адаптации с тревогой (309.24) и тревожное расстройство неуточненное (300.00).
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики расстройств сна, включая первичные расстройства сна, такие как диссомнии, такие как первичная бессонница (307.42), первичная гиперсомния (307.44), нарколепсия (347), расстройство сна, связанное с дыханием (780.59), расстройство сна, связанное с нарушением циркадных ритмов (307.45) и диссомния неуточненная (307.47); первичные расстройства сна, такие как парасомнии, такие как расстройство в виде ночных кошмаров (307.47), расстройство в виде страха во сне (307.46), лунатизм (307.46) и парасомния неуточненная (307.47); расстройства сна, связанные с другим психическим расстройством, такие как бессонница, связанная с другим психическим расстройством (307.42), и гиперсомния, связанная с другим психическим расстройством (307.44); расстройство сна, вызванное общим заболеванием, в частности, нарушения сна, ассоциированные с такими заболеваниями, как неврологические расстройства, невропатическая боль, синдром беспокойных ног, сердечные и легочные заболевания; и расстройство сна, вызванное приемом психоактивных веществ, включая подтипы: тип бессонницы, тип гиперсомнии, тип парасомнии и смешанный тип; апноэ во сне и расстройство суточных биоритмов из-за смены часовых поясов.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики гиперакузии и нарушений слухового восприятия, включая синдром ломкой Х-хромосомы и аутизм.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики расстройств контроля над импульсами, включая: интермиттирующие эксплозивное расстройство (312.34), клептоманию (312.32), патологическую склонность к азартным играм (312.31), пироманию (312.33), трихотилломанию (312.39), расстройство контроля над импульсами неуточненное (312.3), расстройства пищевого поведения, непреодолимое влечение к покупкам, компульсивное сексуальное поведение и патологическое накопительство.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики сексуальных дисфункций, включая расстройства полового влечения, такие как расстройство в виде гипоактивного полового влечения (302.71) и расстройство в виде сексуального отвращения (302.79); расстройства сексуального возбуждения, такие как расстройство женского сексуального возбуждения (302.72) и мужское эректильное расстройство (302.72); оргазмические расстройства, такие как женское оргазмическое расстройство (302.73), мужское оргазмическое расстройство (302.74) и преждевременная эякуляция (302.75); расстройство в виде боли при половом контакте, такое как диспареуния (302.76) и вагинизм (306.51); сексуальная дисфункция неуточненная (302.70); парафилии, такие как эксгибиционизм (302.4), фетишизм (302.81), фроттеризм (302.89), педофилия (302.2), сексуальный мазохизм (302.83), сексуальный садизм (302.84), трансвестический фетишизм (302.3), вуайеризм (302.82) и парафилия неуточненная (302.9); расстройства половой идентификации, такие как расстройство половой идентификации у детей (302.6) и расстройство половой идентификации у подростков и взрослых (302.85); и сексуальное расстройство неуточненное (302.9).
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики расстройств личности, включая подтипы: параноидальное расстройство личности (301.0), шизоидное расстройство личности (301.20), шизотипическое расстройство личности (301.22), антисоциальное расстройство личности (301.7), пограничное расстройство личности (301.83), истерическое расстройство личности (301.50), нарциссическое расстройство личности (301,81), расстройство типа избегающей личности (301.82), расстройство типа зависимой личности (301.6), обсессивно-компульсивное расстройство личности (301.4) и расстройство личности неуточненное (301.9).
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики синдрома дефицита внимания и гиперактивности, включая подтипы: синдром дефицита внимания и гиперактивности по комбинированному типу (314.01), синдром дефицита внимания и гиперактивности с преобладанием дефицита внимания (314.00), синдром дефицита внимания и гиперактивности по гиперактивно-импульсивному типу (314.01) и синдром дефицита внимания и гиперактивности неуточненный (314.9); гиперкинетическое расстройство; расстройства социального поведения, включая подтипы, такие как с началом в детском возрасте (321.81), с началом в подростковом возрасте (312.82) и без уточнения момента появления (312.89), вызывающее оппозиционное расстройство (313.81) и расстройство социального поведения неуточненное; и тики, такие как синдром де ла Туретта (307.23).
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики расстройств аутистического спектра, включая аутизм (299.00), синдром Аспергера (299.80), болезнь Ретта (299.80), дезинтегративное расстройство детского возраста (299.10) и расстройство развития неуточненное (299.80, включая атипичный аутизм).
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики расстройств пищевого поведения, таких как нервная анорексия (307.1), включая подтипы: ограничительный тип и тип с приступами переедания и искусственным выведением пищи; нервная булимия (307.51), включая подтипы: тип с искусственным выведением пищи и тип без искусственного выведения пищи; ожирение; компульсивное расстройство пищевого поведения; расстройство приступообразного переедания; и расстройство пищевого поведения неуточненное (307.50).
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для улучшения познавательной способности, включая лечение нарушения познавательной способности при других заболеваниях, таких как шизофрения, биполярное расстройство, депрессия, других психиатрических расстройств и психотических состояний, ассоциированных с нарушением познавательной способности, например, болезни Альцгеймера. Альтернативно, соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты могут быть использованы для профилактики нарушения познавательной способности, например которое может быть ассоциировано с заболеваниями, такими как шизофрения, биполярное расстройство, депрессия, другие психиатрические расстройства и психотические состояния, ассоциированные с нарушением познавательной способности, например, болезнь Альцгеймера.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики атаксии, включая атаксию, в частности, спиноцеребеллярную атаксию, в особенности атаксию, ассоциированную с мутациями R420H, R423H или F448L.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или их производные могут быть использованы для лечения или профилактики боли, включая ноцицептивную, невропатическую, воспалительную или смешанную боль.
Ноцицептивная боль представляет собой нормальную реакцию на вредное воздействие или повреждение тканей, таких как кожа, мышцы, внутренние органы, суставы, сухожилия или кости. Примеры ноцицептивной боли, которые составляют часть изобретения, включают соматическую боль: скелетно-мышечную (боль в суставах, миофасциальную боль) или кожную, которая часто хорошо локализована; или висцеральную боль: в полых органах или гладких мышцах.
Невропатическая боль представляет собой боль, инициированную или вызванную первичным поражением или заболеванием соматосенсорной нервной системы. Сенсорные аномалии варьируются от дефицита, воспринимаемого как парестезия (онемение), до гиперчувствительности (гипералгезия или аллодиния) и дизестезии (покалывание и другие ощущения). Примеры невропатической боли, которые составляют часть изобретения, включают, без ограничения, диабетическую невропатию, постгерпетическую невралгию, боль при повреждении спинного мозга, фантомную боль (после ампутации) и центральную боль после инсульта. Другие причины невропатической боли включают травмы, химиотерапию и воздействие тяжелых металлов.
Воспалительная боль возникает в результате активации и сенсибилизации ноцицептивного болевого пути множеством медиаторов, высвобождаемых в месте воспаления ткани. Медиаторами, которые играют ключевую роль в воспалительной боли, являются провоспалительные цитокины, такие как интерлейкин-1 (ИЛ-1) альфа, ИЛ-1-бета, ИЛ-6 и фактор некроза опухоли (ФНО) альфа, хемокины, реакционноспособные виды кислорода, вазоактивные амины, липиды, АТФ, кислоты и другие факторы, высвобождаемые инфильтрирующими лейкоцитами, эндотелиальными клетками сосудов или резидентными тучными клетками ткани. Примеры причин воспалительной боли, которые составляют часть изобретения, включают аппендицит, ревматоидный артрит, воспалительное заболевание кишечника и опоясывающий лишай.
Смешанная боль относится к болевым состояниям или расстройствам, которые нелегко классифицировать. В настоящее время понимание механизмов, лежащих в их основе, все еще слабо развито, хотя специфические методы лечения этих расстройств хорошо известны; они включают боль при раке, мигрень и другие первичные головные боли и широко распространенную боль типа фибромиалгии.
Подходящим образом, конкретные болевые показания, которые могут быть опосредованы модулятором каналов Kv3.1 и/или Kv3.2 и/или Kv3.3, представляют собой невропатическую боль и/или воспалительную боль.
Боль представляет собой субъективное состояние и в клинических условиях, как правило, измеряется самооценкой пациента. Поэтому может оказаться затруднительным измерить и количественно оценить болевой порог. Для хронической боли обычно используют субъективную 11-балльную шкалу оценок, где 0 означает отсутствие боли, а 10 означает наихудшую боль, которую только можно представить. Субъекты обычно записывают свою наихудшую боль за определенный период, обычно за сутки. Также регистрируют минимальный средний исходный балл и реакцию на лекарство измеряют относительно исходного уровня, например, может наблюдаться уменьшение боли по меньшей мере на 10%, 20%, 30%, 40% или 50% по сравнению с исходным баллом.
Поскольку индивидуальные реакции на лекарственные средства могут различаться, не у всех людей может наблюдаться уменьшение боли по сравнению с исходной оценкой. Следовательно, подходящим образом, снижение наблюдается по меньшей мере у 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или у всех исследуемых индивидов.
Таким образом, в одном воплощении изобретения уменьшение боли по меньшей мере на 10%, 20%, 30%, 40% или 50% от исходной оценки наблюдается при введении субъекту, нуждающемуся в этом, модулятора Kv3.1/Kv3.2/Kv3, такого как соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное.
Введение модулятора Kv3.1/Kv3.2/Kv3.3 может быть осуществлено до ожидаемого возникновения боли или после возникновения боли. В случаях, когда ожидается, что развитие заболевания или расстройства может привести к усилению боли, испытываемой субъектом, может быть введен модулятор Kv3.1/Kv3.2/Kv3.3, такой как соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное. В случаях, когда субъект уже испытывает боль, модулятор Kv3.1/Kv3.2/Kv3.3, такой как соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное, могут быть введены субъекту, нуждающемуся в этом.
Лечение нуждающегося в этом субъекта может продолжаться столько, сколько требуется, например, 1 сутки, 1 неделю, 2 недели, 3 недели, 1 месяц, 6 месяцев, 1 год, более 1 года, более 2 лет, даже более 5 лет или более 10 лет. Следовательно, в одном воплощении данного изобретения терапевтически эффективное количество модулятора Kv3.1/Kv3.2/Kv3.3, такого как соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное, вводят субъекту, нуждающемуся в этом, в течение от 1 суток до 1 месяца, от 1 недели до 3 месяцев, от 1 месяца до 6 месяцев, от 3 месяцев до 1 года или более 1 года.
Уменьшение боли у субъекта можно измерить путем оценки реакции на внешние раздражители, такие как механические или термические (например, холод) раздражители (например, описанные в Экспериментальном разделе). Снижение может рассматриваться либо как процентное изменение (рассчитанное путем измерения пороговых значений до и после введения дозы для пораженного болевого участка с незатронутым участком боли, например, как более подробно описано в разделе «Анализ данных» в Экспериментальном разделе), либо путем измерения порога отдергивания на пораженном участке боли. Предпочтительно используют расчет обратного процента.
Следовательно, в одном воплощении изобретения чувствительность к боли (такой как невропатическая боль или воспалительная боль) устраняется более чем на 20%, более чем на 30%, более чем на 40%, более чем на 50%, более чем на 60%, более чем на 70%, более чем на 80% или более чем на 90% при введении терапевтически эффективного количества модулятора Kv3.1/Kv3.2/Kv3.3, такого как соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное. Подходящим образом, чувствительность к боли устраняется более чем на 80% или более чем на 90%.
Субъекты, получающие модулятор Kv3.1/Kv3.2/Kv3.3, могут испытывать дополнительные преимущества, такие как одно или более из улучшенных функции, настроения, сна, качества жизни, сокращенного времени отдыха от работы.
В конкретном воплощении соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или производные могут быть использованы для лечения или профилактики невропатической боли.
В конкретном воплощении соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или производные могут быть использованы для лечения или профилактики воспалительной боли.
В конкретном воплощении соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты (например, соли) и/или производные могут быть использованы для лечения или профилактики смешанной боли.
В одном воплощении предложено соединение формулы (I) для использования в профилактике потери слуха, вызванной шумом.
В одном воплощении предложен способ профилактики острой потери слуха, вызванной шумом, включающий введение субъекту, нуждающемуся в этом, соединения формулы (I).
В одном воплощении предложено применение соединения формулы (I) в изготовлении лекарственного средства для профилактики острой потери слуха, вызванной шумом.
Острая потеря слуха, вызванная шумом, может быть спровоцирована такими событиями, как воздействие громкого шума или взрывной волны. В этих случаях, когда ожидается, что будущее событие может привести к острой потере слуха из-за шума, соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное могут быть введены до такого события, чтобы предотвратить или уменьшить острую потерю слуха, вызванную шумом. Введение соединения (I) или его фармацевтически приемлемых соли, сольвата и/или производного может предотвратить любую острую потерю слуха из-за шума или может уменьшить тяжесть острой потери слуха, вызванной шумом, или может смягчить другие симптомы, возникающие при острой потере слуха, вызванной шумом, такие как шум в ушах.
«Острая потеря слуха» характеризуется как потеря слуха, которая возникает быстро в течение периода в несколько часов или суток. Например, потеря слуха может наступить в течение минут, часов или суток (например, в течение периода вплоть до 1 суток, например, до 2 суток, 3 суток, 4 суток, 5 суток, 6 суток или 7 суток). Острая потеря слуха обычно вызвана воздействием громкого звука или взрывной волны. Потерю слуха, вызванную воздействием громкого звука или взрывной волны, называют здесь «потерей слуха, вызванной шумом». Таким образом, «острая потеря слуха, вызванная шумом» представляет собой потерю слуха, которая возникает быстро в течение нескольких часов или суток из-за воздействия громкого звука или взрывной волны.
Важные симптомы острой потери слуха включают:
1) сдвиг слухового порога, то есть увеличение минимального уровня звука чистого тона, который можно услышать без присутствия других звуков;
2) шум в ушах; и
3) ухудшение центральной слуховой обработки, например нарушение слуховой временной обработки и/или понимания речи.
«Громкий» шум или взрыв может составлять по меньшей мере 90 дБ, например по меньшей мере 100 дБ, по меньшей мере 110 дБ, по меньшей мере 120 дБ или по меньшей мере 130 дБ.
В одном воплощении введение соединения формулы (I) или его фармацевтически приемлемых соли, сольвата и/или производного начинают до события, которое, как ожидается, вызовет острую потерю слуха из-за шума. Например, введение соединения формулы (I) или его фармацевтически приемлемых соли, сольвата и/или производного может быть начато вплоть до 2 недель, например, до 1 недели, 6 суток, 5 суток, 4 суток, 3 суток, 2 суток, 24 часов, 12 часов, 6 часов, 5 часов, 4 часов, 3 часов, 2 часов, 1 часа, за 30 минут или за 15 минут до события, которое, как ожидается, вызовет острую потерю слуха из-за шума. Соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное можно вводить несколько раз до события, которое, как ожидается, вызовет острую потерю слуха из-за шума.
В одном воплощении соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное вводят заранее до потенциального воздействия шума или взрыва, который, как ожидается, вызовет острую потерю слуха из-за шума, для предотвращения или уменьшения развития постоянного шума в ушах; для предотвращения или уменьшения развития стойкого сдвига слуховых порогов; или для предотвращения или уменьшения развития постоянно ухудшенной центральной слуховой обработки, включая, например, временную слуховую обработку и/или понимание речи.
Следует понимать, что заблаговременное введение может быть проведено в обстоятельствах, когда предполагается, что субъект подвергается риску воздействия шума или взрывной волны, которая, как ожидается, вызовет острую потерю слуха из-за шума, и не ограничивается теми обстоятельствами, когда такое воздействие в конечном итоге имеет место.
В одном воплощении введение соединения формулы (I) или его фармацевтически приемлемых соли, сольвата и/или производного начинают во время события, которое, как ожидается, вызовет острую потерю слуха из-за шума. Соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное можно вводить несколько раз во время события, которое, как ожидается, вызовет острую потерю слуха из-за шума.
В одном воплощении соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное первоначально вводят во время шума или взрыва, который, как ожидается, вызовет острую потерю слуха из-за шума, для предотвращения или уменьшения развития постоянного шума в ушах; для предотвращения или уменьшения развития стойкого сдвига слухового порога; или для предотвращения или уменьшения развития постоянно ухудшенной центральной слуховой обработки, включая, например, временную слуховую обработку и/или понимание речи.
В одном воплощении введение соединения формулы (I) или его фармацевтически приемлемых соли, сольвата и/или производного начинают после события, которое, как ожидается, вызовет острую потерю слуха из-за шума.
Таким образом, в одном из воплощений соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное первоначально вводят после шума или взрыва, который, как ожидается, вызовет острую потерю слуха из-за шума, для предотвращения или уменьшения развития стойкого шума в ушах; для предотвращения или уменьшения развития стойкого сдвига слухового порога; или для предотвращения или уменьшения развития постоянно ухудшенной центральной слуховой обработки, включая, например, временную слуховую обработку и/или понимание речи.
Когда соединение формулы (I) вводят после события, которое, как ожидается, вызовет острую потерю слуха из-за шума, такое введение обычно проводят во время «острой фазы», то есть до того, как потеря слуха установилась.
В одном воплощении введение соединения формулы (I) или его фармацевтически приемлемых соли, сольвата и/или производного может быть начато вплоть до 2 месяцев после события, которое, как ожидается, вызовет острую потерю слуха из-за шума, например, вплоть до 1 месяца, 2 недель, 1 недели, 6 суток, 5 суток, 4 суток, 3 суток, 2 суток, 24 часов, 12 часов, 6 часов, 5 часов, 4 часов, 3 часов, 2 часов, 1 часа, до 30 минут или до 15 минут после события, которое может вызвать острую потерю слуха из-за шума. Соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное можно вводить несколько раз после события, которое, как ожидается, вызовет острую потерю слуха из-за шума.
Соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное можно вводить в течение периода вплоть до 7 суток (например, до 1 суток, до 2 суток, до 3 суток, до 4 суток, до 5 суток, до 6 суток или до 7 суток) в течение 1-2 недель (например, 7-8 суток, 7-9 суток, 7-10 суток, 7-11 суток, 7-12 суток, 7-13 суток или 7-14 суток), в течение 2-4 недель (например, 2-3 недель или 2-4 недель) или в течение 1-2 месяцев (например, 4-6 недель или 4-8 недель).
Соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное можно первоначально вводить за 1 сутки заранее, например, за 2 суток заранее, за 3 суток заранее, за 5 суток заранее, за 1 неделю заранее, за 2 недели заранее или за 1 месяц заранее до шума или взрыва, который, как ожидается, вызовет острую потерю слуха из-за шума, причем введение, которое начинают в любой момент до начала воздействия шума или взрыва, которые, как ожидается, вызовут острую потерю слуха из-за шума, обычно продолжают в течение вплоть до 2 месяцев после воздействия шума или взрыва, которые, как ожидается, вызовут острую потерю слуха из-за шума, например, в течение периода вплоть до 1 месяца после, до 3 недель после, до двух недель после, до 1 недели после, до 5 суток после, до 3 суток после, до 2 суток после или до 1 суток после.
В одном воплощении предложено соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное для использования в предотвращении или уменьшении развития постоянного сдвига слухового порога, где постоянный сдвиг слухового порога снижен на по меньшей мере 10 дБ, например по меньшей мере 15 дБ, по меньшей мере 20 дБ, по меньшей мере 30 дБ, по меньшей мере 40 дБ или полностью.
Фармацевтические композиции
Для использования в терапии соединения по изобретению обычно вводят в виде фармацевтической композиции. В данном изобретении также предложена фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемые соль и/или сольват (например, соль) и/или производное и фармацевтически приемлемый носитель или эксципиент.
В одном воплощении предложена фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемые соль и/или сольват (например, соль) и/или производное, для использования в лечении или предупреждении заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона.
В дополнительном воплощении предложен способ профилактики или лечения заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона, включающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтически приемлемые соль и/или сольват (например, соль) и/или производное.
В данном изобретении также предложено применение фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтически приемлемые соль и/или сольват (например, соль) и/или производное, в изготовлении лекарственного средства для лечения или профилактики заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или производные можно вводить любым удобным способом, например путем перорального, парентерального, трансбуккального, сублингвального, интраназального, ректального или трансдермального введения, и фармацевтические композиции соответственно адаптированы. Другие возможные пути введения включают интратимпанальный и интракохлеарный.
Соединения формулы (I) или их фармацевтически приемлемые соли и/или сольваты и/или производные, которые активны при пероральном введении, могут быть приготовлены в виде жидкостей или твердых веществ, например, в виде сиропов, суспензий, эмульсий, таблеток, капсул или пастилок.
Жидкий препарат обычно состоит из суспензии или раствора активного ингредиента (такого как соединение формулы (I) или его фармацевтически приемлемые соль и/или сольват (например, соль) и/или его производное) в подходящем(их) жидком(их) носителе(ях), например, водном растворителе, таком как вода, этанол или глицерин, или неводном растворителе, таком как полиэтиленгликоль или масло. Препарат может также содержать суспендирующий агент, консервант, корригент и/или краситель.
Композицию в форме таблетки можно приготовить с использованием любого(ых) подходящего(их) фармацевтического(их) носителя(ей), обычно используемого(ых) для приготовления твердых препаратов, таких как стеарат магния, крахмал, лактоза, сахароза и целлюлоза.
Композиция в форме капсулы может быть приготовлена с использованием обычных методик инкапсулирования, например, гранулы, содержащие активный ингредиент (такой как соединение формулы (I) или его фармацевтически приемлемые соль и/или сольват (например, соль) и/или его производное), могут быть получены с использованием стандартных носителей и затем помещены в твердую желатиновую капсулу; альтернативно, дисперсию или суспензию можно приготовить с использованием любого(ых) подходящего(их) фармацевтического(их) носителя(ей), таких как водные камеди, целлюлозы, силикаты или масла, и этой дисперсией или суспензией затем заполняют мягкую желатиновую капсулу.
Типичные парентеральные композиции состоят из раствора или суспензии активного ингредиента (такого как соединение формулы (I) или его фармацевтически приемлемые соль и/или сольват (например, соль) и/или производное) в стерильном водном носителе или парентерально приемлемом масле, например, полиэтиле нглико л е, поливинилпирролидоне, лецитине, арахисовом масле или кунжутном масле. Альтернативно, раствор можно лиофилизировать и затем восстановить подходящим растворителем непосредственно перед введением.
Композиции для интраназального введения могут быть удобно приготовлены в виде аэрозолей, капель, гелей и порошков. Аэрозольные препараты обычно содержат раствор или высокодисперсную суспензию активного ингредиента в фармацевтически приемлемом водном или неводном растворителе и обычно представлены в одноразовых или многодозовых количествах в стерильной форме в герметичном контейнере, который может быть в форме картриджа или сменного блока для использования с распылительным устройством. Альтернативно, герметичный контейнер может представлять собой одноразовое дозирующее устройство, такое как однодозовый назальный ингалятор или дозатор аэрозолей, снабженный дозирующим клапаном. Если лекарственная форма включает дозатор аэрозоля, она будет содержать пропеллент, который может представлять собой сжатый газ, например воздух, или органический пропеллент, такой как фторхлоруглеводород или гидрофторуглерод. Аэрозольные лекарственные формы также могут иметь форму помповых распылителей.
Композиции, подходящие для трансбуккального или сублингвального введения, включают таблетки, лепешки и пастилки, в которых активный ингредиент приготовлен вместе с носителем, таким как сахар и аравийская камедь, трагакант или желатин и глицерин.
Композиции для ректального введения обычно имеют форму суппозиториев, содержащих традиционную основу для суппозиториев, такую как масло какао.
Композиции, подходящие для трансдермального введения, включают мази, гели и пластыри. В одном воплощении композиция находится в стандартной лекарственной форме, такой как таблетка, капсула или ампула.
Композиция может содержать от 0,1% до 100% по массе, например от 10 до 60% по массе, активного материала, в зависимости от способа введения. Композиция может содержать от 0% до 99% по массе, например от 40% до 90% по массе, носителя, в зависимости от способа введения. Композиция может содержать от 0,05 мг до 1000 мг, например от 1,0 мг до 500 мг, активного материала, в зависимости от способа введения. Композиция может содержать от 50 мг до 1000 мг, например от 100 мг до 400 мг носителя, в зависимости от способа введения. Доза соединения, используемого в лечении вышеупомянутых расстройств, будет варьировать обычным образом в зависимости от тяжести расстройств, веса пациента и других подобных факторов. Однако, в качестве общего руководства, подходящие стандартные дозы могут составлять от 0,05 мг до 1000 мг, более предпочтительно от 1,0 мг до 500 мг, и такие стандартные дозы можно вводить более одного раза в сутки, например, два или три раза в сутки. Такая терапия может продолжаться несколько недель или месяцев.
Доза, вводимая субъекту, обычно является безопасной и эффективной дозой, то есть представляет приемлемый баланс между желаемыми преимуществами и нежелательными побочными эффектами.
В дополнительном аспекте данного изобретения предложена комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемые соль, сольват и/или производное (например, комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемое производное) вместе с дополнительным фармацевтически приемлемым активным ингредиентом или ингредиентами.
В данном изобретении предложено соединение формулы (I) для использования в комбинации с дополнительным фармацевтически приемлемым активным ингредиентом или ингредиентами.
Когда соединения используют в комбинации с другими терапевтическими агентами, соединения можно вводить либо последовательно, либо одновременно любым удобным путем. Альтернативно, соединения можно вводить по отдельности.
Комбинации, упомянутые выше, могут быть удобным образом представлены для использования в форме фармацевтического препарата, и, таким образом, фармацевтические препараты, содержащие комбинацию, как определено выше, вместе с фармацевтически приемлемым носителем или эксципиентом, составляют дополнительный аспект изобретения. Индивидуальные компоненты таких комбинаций можно вводить либо последовательно, либо одновременно в отдельных или комбинированных фармацевтических препаратах. Индивидуальные компоненты комбинаций также можно вводить по отдельности одним и тем же путем или разными путями.
Когда соединение формулы (I) или его фармацевтически приемлемое производное используют в комбинации со вторым терапевтическим агентом, активным против того же самого болезненного состояния, доза каждого соединения может отличаться от дозы, когда соединение используется отдельно. Соответствующие дозы легко оценят специалисты в данной области.
Экспериментальный раздел
Данное изобретение проиллюстрировано описанными ниже соединениями. В следующих примерах описан лабораторный синтез конкретных соединений по изобретению, и они не предназначены для ограничения объема изобретения каким-либо образом в отношении соединений или способов. Следует понимать, что, хотя используются определенные реагенты, растворители, температуры и периоды времени, существует много возможных эквивалентных альтернатив, которые могут быть использованы с получением аналогичных результатов. Подразумевается, что данное изобретение включает такие эквиваленты.
Аналитическое оборудование
Исходные материалы, реагенты и растворители были получены от коммерческих поставщиков, и их использовали без дополнительной очистки, если не указано иное. Если не указано иное, все соединения с хиральными центрами являются рацемическими. В тех случаях, когда реакции описаны как проводимые таким же образом, как указанные выше реакции, описанные более подробно, общие используемые реакционные условия были по существу такими же. Используемые условия обработки были стандартными в данной области техники, но могли быть адаптированы для разных реакций. Исходный материал не обязательно был получен из упомянутой партии. Синтезированные соединения могут иметь различную степень чистоты, например, в диапазоне от 85% до 99%. Для этого в некоторых случаях скорректированы расчеты количества молей и выхода.
ВЭЖХ/масс-спектры (ВЭЖХ-МС) записывали на масс-спектрометре Agilent 1100 Series LC/MSD, соединенном с прибором HPLC Agilent 1100 Series, работающем в режиме положительной ионизации электрораспылением и в условиях кислотного градиента.
Контроль качества (3-минутный метод): ЖХ/МС-ЭР+ в кислых условиях проводили на колонке Zorbax SB С18 (1,8 мкм, 3×50 мм). Подвижная фаза: А: (H2O+0,05%) TFA по объему) / В: (CH3CN+0,05% TFA по объему). Градиент: t=0 мин 0% (В), от 0 до 95% (В) за 2,5 мин, 95% (В) за 0,2 мин, от 95 до 100% (В) за 0,2 мин, 100% (В) в течение 0,4 мин, от 100% до 0% (В) за 0,1 мин. Время окончания 4 мин. Т колонки равна 60°С. Скорость потока: 1,5 мл/мин. Диапазон масс ЭР+: (100-1000 а.е.м., F=60). Длины волн УФ-детектирования: DAD 1А=220,8, DAD 1B=254,8. Использование этой методологии обозначено «QC_3_MIN» в аналитических характеристиках описанных соединений.
Хиральный контроль: ЖХ/МС-ЭР+ в кислых условиях проводили на CHIRALCEL® OD-H (250×4,6 мм, 5 мкм). Подвижная фаза: А: (H2O+0,05% TFA по объему) / В: (CH3CN+0,05% TFA по объему). Градиент: t=0-6 мин 35% (В), t=6-40 мин от 35% до 50% (В), t=40-45 мин от 50% до 70% (В), t=45-50 мин от 70% до 35% (В), t=50-55 мин 35% (В). Время окончания 60 мин. Т колонки равна 40°С. Скорость потока: 1,0 мл/мин. Длины волн УФ-детектирования: DAD 1А=220,8, DAD 1B=254,8.
Спектры протонного магнитного резонанса (ЯМР) записывали либо на приборах Varian при 300, 400, 500 или 600 МГц, либо на приборах Bruker при 400 МГц. Химические сдвиги выражены в м.д. (δ) при использовании линии остаточного растворителя в качестве внутреннего стандарта. Картины расщепления обозначены как s (синглет), br.s (уширенный синглет), d (дублет), t (триплет), q (квартет), dd (дублет дублетов), dt (дублет триплетов) и m (мультиплет). Спектры ЯМР регистрировали при температурах в диапазоне от 25 до 60°С.
Данные экспериментов спектроскопии ядерного эффекта Оверхаузера (2D ЯМР NOESY) собирали при времени смешивания 500 мс с использованием спектральной ширины 3355 Гц как для f1, так и для f2. Всего было собрано 256 приращений, обработанных до 1К с использованием линейного прогнозирования, по 8 сканирований в каждом. Данные обрабатывали со сдвигом синусоидального колокола в обоих измерениях и с 1b=0,3 Гц по f1. В ряде препаратов очистку проводили с использованием автоматической флэш-хроматографии Biotage (SP1 и SP4) или систем Flash Master Personal.
Флэш-хроматографии выполняли на силикагеле 230-400 меш (предоставлен Merck AG Darmstadt, Германия) или на силикагеле 300-400 меш (предоставлен Sinopharm Chemical Reagent Co., Ltd.), предварительно упакованных картриджах Varian Mega Be-Si., предварительно упакованных картриджах с диоксидом кремния Biotage (например, картридже Biotage SNAP).
Сокращения
Примеры соединений
Промежуточное соединение 1
2-Бром-5-(7-метилспиро[2Н-бензофуран-3,1'-никлопропан]-4-ил)окси-пиразин
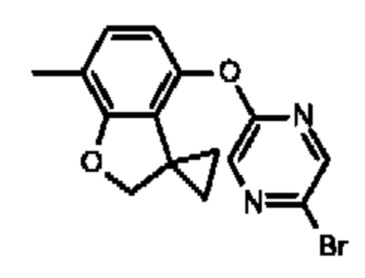
Смесь 7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ола (Промежуточное соединение 156 в WO 2012076877, 1,11 г, 6,30 ммоль), 2,5-дибромпиразина (1,5 г, 6,30 ммоль) и карбоната калия (1,31 г, 9,46 ммоль) в N,N-диметилформамиде (14 мл) перемешивали при 120°С в течение 3 часов. После охлаждения реакционную смесь разбавляли МТВЕ (100 мл) и промывали рассолом (50 мл). Фазы разделяли и водный слой промывали МТВЕ (100 мл) и EtOAc (100 мл). Все органические фазы собирали, сушили над Na2SO4, фильтровали и упаривали. Остаток очищали флэш-хроматографией (Biotage System) на силикагеле, используя SNAP 100g в качестве колонки и циклогексан:этилацетат от 100:0 до 90:10 в качестве элюента, с получением 2-бром-5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)окси-пиразина (1,8 г) в виде белого твердого вещества.
ЖХ/МС: QC_3_MIN: Rt 2,705 мин; m/z 333 & 335 [М+Н]+.
Следующие соединения получали с использованием вышеупомянутой методологии с заменой 7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ола на соответствующий фенол. Конечные продукты очищали флэш-хроматографией (картридж с диоксидом кремния; никлогексан/EtOAc или другая подходящая система растворителей).
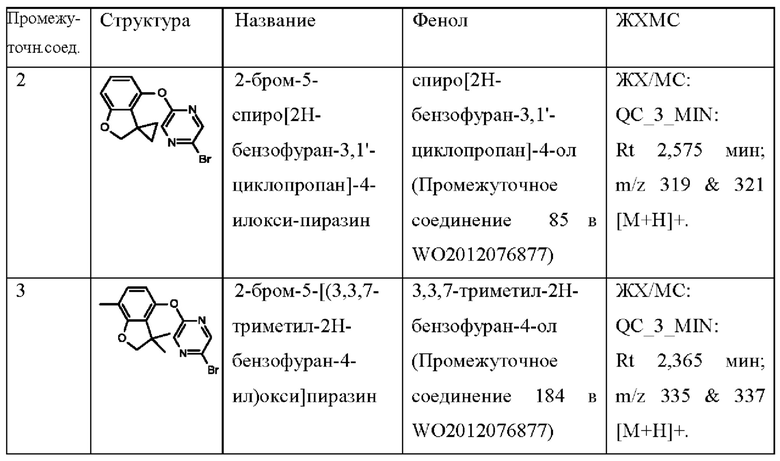

Промежуточное соединение 5, путь 1
3-(5-Хлорпиразин-2-ил)-5,5-диметил-имидазолидин-2,4-дион
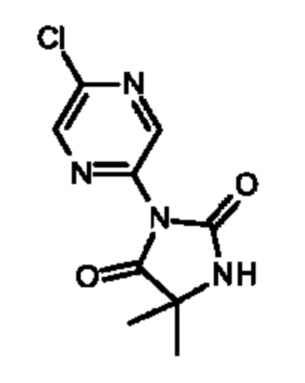
К раствору бис(трихлорметил)карбоната (950 мг, 3,20 ммоль) в этилацетате (30 мл) при 0°С добавляли по каплям раствор 5-хлорпиразин-2-амина (0,75 г, 5,79 ммоль)/N,N-диизопропилэтиламина (6,05 мл, 34,74 ммоль) в этилацетате (12 мл) и реакционную смесь перемешивали в течение 15 минут при той же температуре. Поддерживая реакционную смесь при 0°С, подсоединяли вакуум (5 минут) для удаления избытка фосгена. Добавляли раствор 4-(диметиламино)пиридина (710 мг, 5,81 ммоль) в этилацетате (8 мл)/дихлорметане (2 мл) и реакционную смесь перемешивали в течение 5 минут при той же температуре. Затем добавляли гидрохлорид метил-2-амино-2-метилпропаноата (1,4 г, 9,1 ммоль) при 0°С и реакционную смесь перемешивали в течение 30 минут при той же температуре. Реакционную смесь гасили раствором 0,2 н. HCl (100 мл) и две фазы разделяли. Органический слой промывали рассолом (100 мл), сушили над Na2SO4, фильтровали и упаривали с получением промежуточной мочевины.
Полученную мочевину растворяли в дихлорметане (20 мл) и добавляли метоксид натрия (315 мг, 5,83 ммоль) при 0°С. Реакционную смесь перемешивали 15 минут при той же температуре; реакционную смесь гасили насыщенным раствором NH4Cl, обеспечивая достижение рН 3-4. Смесь экстрагировали этилацетатом (50 мл); фазы разделяли и органический слой промывали рассолом (50 мл), сушили над Na2SO4, фильтровали и упаривали. Остаток очищали флэш-хроматографией с обращенной фазой (система Biotage) на фазе С-18, используя SNAP 30g в качестве колонки и смесь вода:ацетонитрил от 95:5 до 40:60 в качестве элюента. Соответствующие фракции объединяли и упаривали досуха с получением 3-(5-хлорпиразин-2-ил)-5,5-диметил-имидазолидин-2,4-диона (220 мг) в виде бледно-коричневого твердого вещества.
ЖХ/МС: QC_3_MIN: Rt 1,649 мин; m/z 241 & 243 [М+Н]+.
Следующие соединения получали с использованием вышеупомянутой методологии с заменой гидрохлорида сложного метилового эфира 2,2-диметилглицина на соответствующий гидрохлорид сложного аминоэфира. Конечные продукты очищали флэш-хроматографией (картридж с диоксидом кремния; циклогексан/EtOAc или другая подходящая система растворителей) или растирали в соответствующем растворителе или кристаллизовали из подходящего растворителя.

Промежуточное соединение 5, путь 2
3-(5-Хлорпиразин-2-ил)-5,5-диметил-имидазолидин-2,4-дион
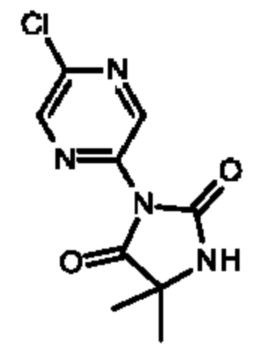
К раствору 5-хлорпиразин-2-амина (500 мг, 3,86 ммоль) и гидрохлорида 2-амино-2-метилпропановой кислоты (646 мг, 4,63 ммоль) в ацетонитриле (10 мл) добавляли медленно при комнатной температуре раствор пропилфосфонового ангидрида не менее 50 масс. % в этилацетате (3,68 г, 5,78 ммоль). Реакционную смесь перемешивали при 80°С в течение 6 часов. Реакционную смесь разбавляли этилацетатом (10 мл) и добавляли 1 н. водный раствор NaOH, при этом рН оставляли достигать значения приблизительно 8. Две фазы разделяли и органическую фазу промывали рассолом (10 мл), сушили над Na2SO4, концентрировали в вакууме и неочищенный продукт очищали флэш-хроматографией на силикагеле (BIOTAGE SYSTEM), используя SNAP 25g в качестве колонки и DCM:MEOH от 99/1 до 90/10 в качестве элюента, с получением 2-амино-N-(5-хлорпиразин-2-ил)-2-метилпропанамида (190 мг) в виде желтого твердого вещества.
ЖХ/МС: QC_3_MIN: Rt 1,181 мин; m/z 215 & 217 [М+Н]+.
К раствору 2-амино-М-(5-хлорпиразин-2-ил)-2-метилпропанамида (190 мг, 0,88 ммоль) и триэтиламина (268 мг, 2,6555 ммоль) в дихлорметане (5 мл) при 0°С медленно добавляли раствор бис(трихлорметил)карбоната (105,07 мг, 0,3541 ммоль) в дихлорметане (4 мл) и реакционную смесь перемешивали в течение 30 минут при той же температуре. Реакционную смесь разбавляли DCM (10 мл), промывали водным раствором 0,2 н. HCl (10 мл) и рассолом (10 мл). Органические фазы концентрировали под вакуумом и неочищенный продукт очищали флэш-хроматографией на силикагеле (система Biotage), используя SNAP 25g в качестве колонки и Chexane/EtOAc от 80/20 до 0/100 в качестве элюента, с получением 3-(5-хлорпиразин-2-ил)-5,5-диметил-имидазолидин-2,4-диона (130 мг) в виде белого твердого вещества.
ЖХ/МС: QC_3_MIN: Rt 1,598 мин; m/z 241 & 243 [М+Н]+.
Промежуточное соединение 7
трет-Бутил-N-[(1R)-1-карбамоилпропил]карбамат
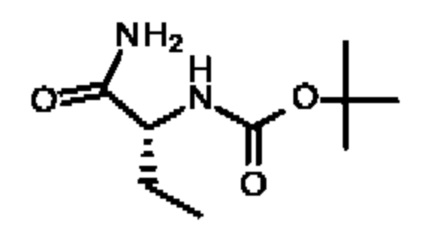
Смесь тетрафторбората [диметиламино-(3-оксидотриазоло[4,5-b]пиридин-3-ий-1-ил)метилен]-диметил-аммония (1,1084 г, 3,4415 ммоль), N,N-диизопропилэтиламина (0,7939 г, 6,1431 ммоль) и (2R)-2-(трет-бутоксикарбониламино)бутановой кислоты (0,5000 г, 2,4601 ммоль) в безводном N,N-диметилформамиде (8 мл) перемешивали при комнатной температуре в течение 10 минут. Добавляли гексаметилдисилазан (0,5960 г, 3,6928 ммоль) и смесь перемешивали в течение 18 часов.
Реакционную смесь разделяли в МТВЕ (30 мл) и рассоле (20 мл). Органический слой сушили с использованием сульфата натрия, фильтровали и растворитель удаляли. Полученное масло растирали в МТВЕ (3 мл), полученный осадок промывали МТВЕ и сушили в вакууме с получением трет-бутил-N-[(1R)-1-карбамоилпропил]карбамата (0,3000 г, 1,4833 ммоль, 60,294%) в виде белого твердого вещества.
ЖХ/МС: QC_3_MIN: m/z 147 [M-tBu+H]+.
Следующие соединения получали с использованием вышеупомянутой методологии с заменой (2R)-2-(трет-бутоксикарбониламино)бутановой кислоты на соответствующую защищенную аминокислоту.
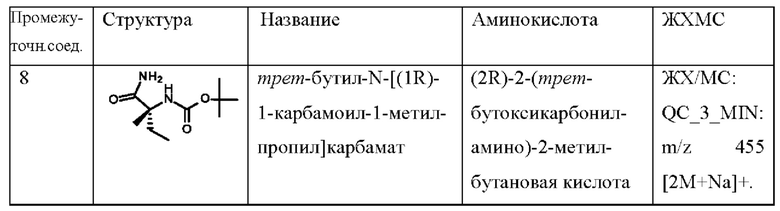
Промежуточное соединение 9 (путь 1)
трет-Бутил-N-[(1R)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]пропил]карбамат
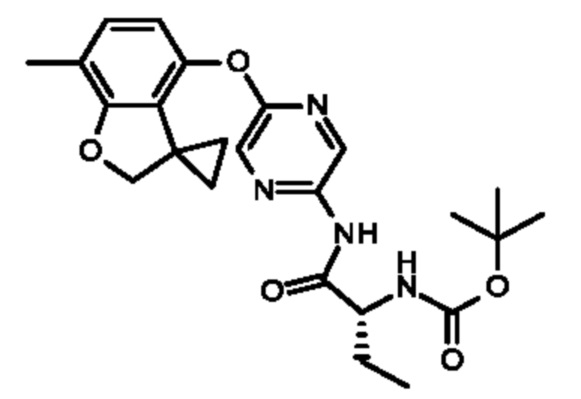
Смесь 2-бром-5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)окси-пиразина (Промежуточное соединение 1, 50 мг, 0,15 ммоль), трет-бутил-N-[(1R)-1-карбамоилпропил]карбамата (Промежуточное соединение 7, 46 мг, 0,23 ммоль), трис(дибензилиденацетон)дипалладия(0) (10,3 мг, 0,011 ммоль), дициклогексил-[2-(2,4,6-триизопропил)фенил]фосфана (XPhos) (5,4 мг, 0,011 ммоль) и карбоната цезия (73 мг, 0,22 ммоль) в 1,4-диоксане (2 мл) перемешивали в атмосфере азота при 80°С в течение 3 часов.
Реакционную смесь распределяли между этилацетатом и рассолом. Органический слой отделяли, сушили над сульфатом натрия, фильтровали и упаривали досуха. Остаток очищали флэш-хроматографией на силикагеле (система Biotage), используя колонку SNAP 10g и циклогексан и EtOAc от 100/0 до 0/100 в качестве элюента. Соответствующие фракции объединяли и упаривали досуха с получением трет-бутил-N-[(1R)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]карбамоил]пропил]карбамата (10 мг).
ЖХ/МС: QC_3_MIN: Rt 2,696 мин; m/z 455 [М+Н]+.
Промежуточное соединение 9 (путь 2)
трет-Бутил-N-[(1R)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]пропил]карбамат
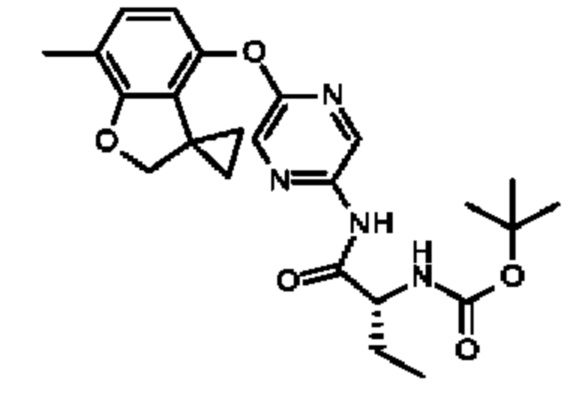
К смеси 2-бром-5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)окси-пиразина (Промежуточное соединение 1, 16 г, 48,0 ммоль), трет-бутил-N-[(1R)-1-карбамоилпропил]карбамата (Промежуточное соединение 7, 10 г, 49,4 ммоль), карбоната цезия (24,16 г, 74,17 ммоль) в 1,4-диоксане (150 мл) после продувки аргоном добавляли диацетоксипалладий (0,555 г, 2,47 ммоль) и (5-дифенилфосфанил-9,9-диметил-ксантен-4-ил)дифенилфосфан (2,15 г, 3,71 ммоль). Применяли трехкратный цикл вакуум-аргон и реакционную смесь перемешивали при 95°С в течение 1,5 часов. Реакционную смесь охлаждали с использованием внешней ледяной бани и затем фильтровали под вакуумом для удаления карбоната цезия. Фильтрат собирали, разбавляли EtOAc (150 мл) и промывали водным насыщенным раствором NH4Cl (100 мл), а затем водным насыщенным раствором NaCl (100 мл), сушили над сульфатом натрия, фильтровали и упаривали досуха.
Остаток очищали флэш-хроматографией на силикагеле (система Biotage), используя колонку 2х SNAP 100g (200 г диоксида кремния) и циклогексан/EtOAc от 0 до 40% в качестве элюента, с получением трет-бутил-N-[(1R)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]пропил]карбамата (16,8 г) в виде желтого твердого вещества.
Следующие соединения получали с использованием вышеуказанной методологии (путь 1 или путь 2) с заменой 2-бром-5-(7-метилспиро [2Н-бензофуран-3,1'-циклопропан]-4-ил)окси-пиразина (Промежуточное соединение 1) на соответствующий бромпиразин. Конечные продукты очищали флэш-хроматографией (картридж с диоксидом кремния; циклогексан/EtOAc или другая подходящая система растворителей).
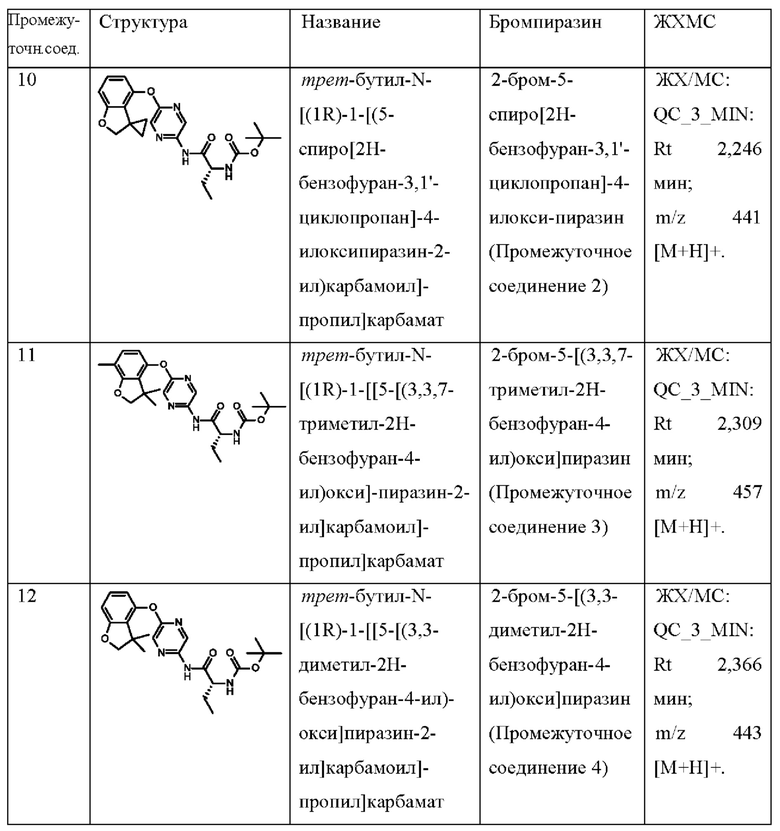
Промежуточное соединение 13
(2R)-2-Амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-пиклопропан]-4-ил)-оксипиразин-2-ил]бутанамид
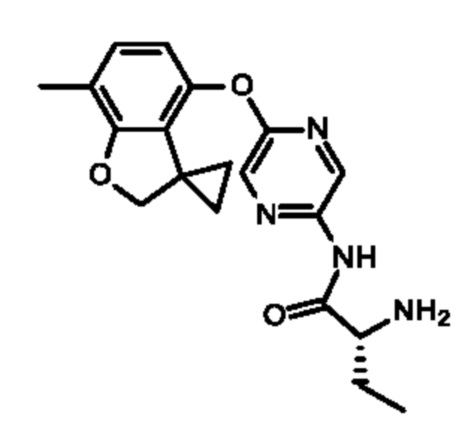
Смесь трет-бутил-N-[(1R)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]пропил]карбамата (Промежуточное соединение 9, 16 мг, 0,035 ммоль) и 2,2,2-трифторуксусной кислоты (0,50 мл, 6,53 ммоль) в дихлорметане (2 мл) перемешивали при комнатной температуре в течение 2 часов.
Реакционную смесь разбавляли дихлорметаном (20 мл) и добавляли насыщенный раствор NaHCO3 (водн.) до достижения значения рН 8. Фазы разделяли и органический слой промывали рассолом (20 мл), сушили над Na2SO4, фильтровали и упаривали с получением (2R)-2-амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]бутанамида (13 мг), который использовали на следующей стадии без дополнительной очистки.
ЖХ/МС: QC_3_MIN: Rt 2,009 мин; m/z 355 [М+Н]+.
Следующие соединения получали с использованием вышеуказанной методологии с заменой трет-бутил-N-[(1R)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]пропил]карбамата (Промежуточное соединение 9) на соответствующий Вос-амин.
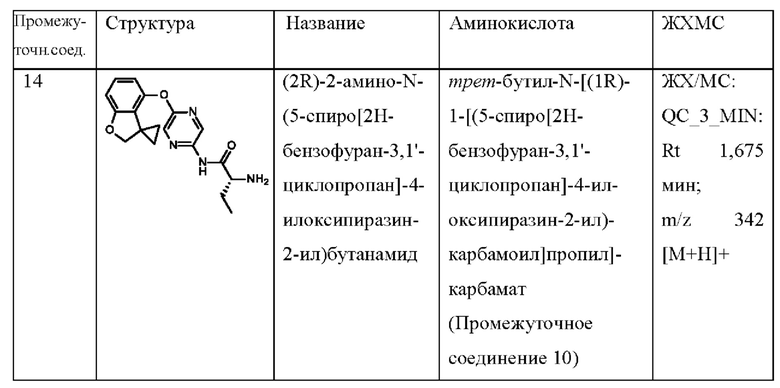
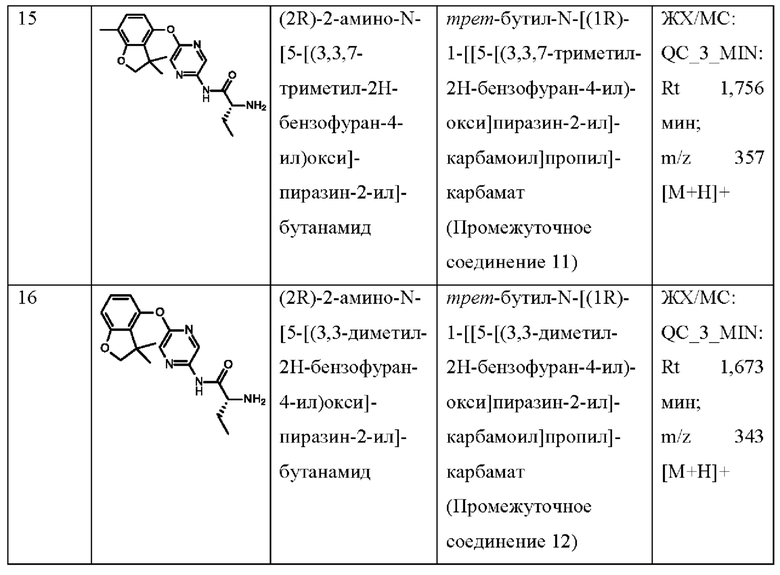
Промежуточное соединение 17
(5R)-5-Этил-5-метил-имидазолидин-2,4-дион
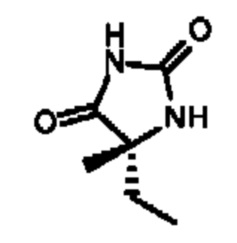
Смесь трет-бутил-N-[(1R)-1-карбамоил-1-метил-пропил]карбамата
(Промежуточное соединение 8, 100 мг, 0,4624 ммоль) и карбоната калия (191,71 мг, 1,3871 ммоль) в 1-бутаноле (5 мл) перемешивали в атмосфере азота при 95°С в течение ночи. После охлаждения карбонат калия отфильтровывали и реакционную смесь разбавляли этилацетатом (30 мл) и промывали водным 0,1 н. раствором HCl (30 мл), а затем рассолом (30 мл). Фазы разделяли и органический слой собирали, сушили над Na2SO4, фильтровали и упаривали с получением (5R)-5-этил-5-метил-имидазолидин-2,4-диона (60 мг, 0,4221 ммоль, 91,283%).
ЖХ/МС: QC_3_MIN: m/z 285 [2М+Н]+.
Промежуточное соединение 18
трет-Бутил-N-(1-карбамоилциклобутил)карбамат
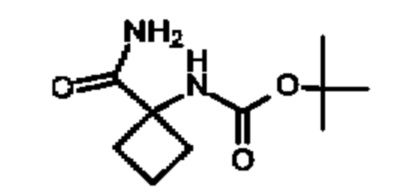
Промежуточное соединение 18 получали с использованием методологии, описанной для Промежуточного соединения 7, с заменой (2R)-2-(трет-бутоксикарбониламино)бутановой кислоты на 1-(трет-бутоксикарбониламино)-циклобутанкарбоновую кислоту.
ЖХ/МС: QC_3_MIN: m/z 159 [M-tBu+H]+.
Промежуточное соединение 19
трет-Бутил-N-[1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-никлопропан]-4-ил)-оксипиразин-2-ил]карбамоил]циклобутил]карбамат
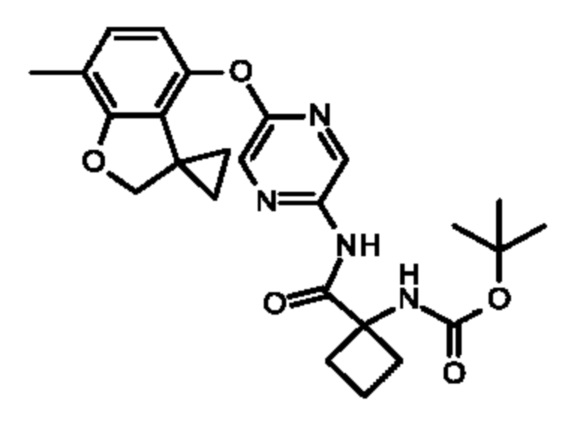
Смесь 2-бром-5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)окси-пиразина (Промежуточное соединение 1, 50 мг, 0,1501 ммоль), трет-бутил-N-(1-карбамоилциклобутил)карбамата (Промежуточное соединение 18, 64 мг, 0,2987 ммоль), карбоната калия (62 мг, 0,4486 ммоль), йодида меди(I) (2,9 мг, 0,0152 ммоль) и N,N'-диметилэтан-1,2-диамина (0,0065 мл, 0,0601 ммоль) в 1-бутаноле (1 мл) перемешивали в атмосфере азота при 95°С в течение 4 часов. После охлаждения реакционную смесь разбавляли этилацетатом (30 мл) и промывали водным 0,1М раствором HCl (30 мл), а затем рассолом (30 мл). Фазы разделяли, органический слой собирали, сушили над Na2SO4, фильтровали и упаривали. Остаток очищали флэш-хроматографией (Biotage System) на силикагеле, используя SNAP 10g в качестве колонки и циклогексан:этилацетат от 100:0 до 30:70 в качестве элюента, с получением трет-бутил-N-[1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]циклобутил]карбамата (18 мг).
ЖХ/МС: QC_3_ MIN: Rt 2,675 мин; m/z 467 [М+Н]+.
Промежуточное соединение 20
1-Амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]циклобутанкарбоксамид
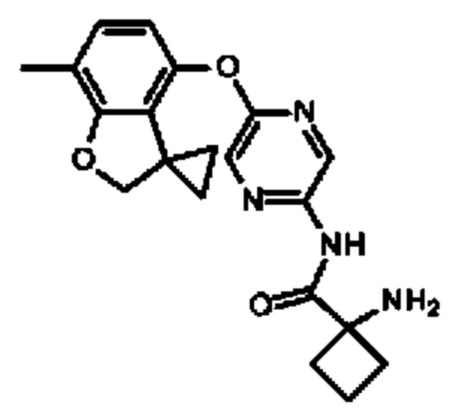
Промежуточное соединение 20 получали с использованием методологии, описанной для Промежуточного соединения 13, с заменой трет-бутил-N-[(1R)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]-пропил]карбамата (Промежуточное соединение 9) на трет-бутил-N-[1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]-циклобутил]карбамат (Промежуточное соединение 19).
ЖХ/МС: QC_3_MIN: Rt 1,979 мин; m/z 367 [М+Н]+.
Промежуточное соединение 21
трет-Бутил-N-(1-карбамоилциклопропил)карбамат
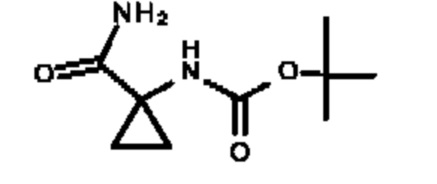
Промежуточное соединение 21 получали с использованием методологии, описанной для Промежуточного соединения 7, с заменой (2R)-2-(трет-бутил-карбониламино)бутановой кислоты на 1-(трет-бутоксикарбониламино)циклопропан-карбоновую кислоту.
Промежуточное соединение 22
трет-Бутил-N-[1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-никлопропан]-4-ил)-оксипиразин-2-ил]карбамоил]циклопропил]карбамат
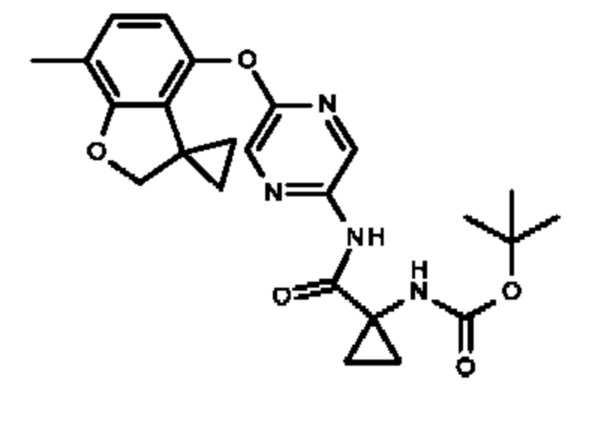
Смесь дициклогексил-[2-(2,4,6-триизопропилфенил)фенил]фосфана (12 мг, 0,0252 ммоль), трет-бутил-N-(1-карбамоилциклопропил)карбамата (Промежуточное соединение 21, 67 мг, 0,3346 ммоль), трис(дибензилиденацетон)дииалладия(0) (22 мг, 0,0240 ммоль), 2-бром-5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)окси-пиразина (Промежуточное соединение 1, 79,518 мг, 0,2387 ммоль) и карбоната цезия (116 мг, 0,3560 ммоль) в 1,4-диоксане (1 мл) перемешивали в атмосфере азота при 95°С в течение 2 часов. Добавляли дополнительно трет-бутил-N-(1-карбамоил-циклопропил)карбамат (Промежуточное соединение 21, 67 мг, 0,3346 ммоль) и трис(дибензилиденацетон)дипалладий(0) (22 мг, 0,0240 ммоль) и реакционную смесь перемешивали при 95°С в атмосфере азота в течение еще 2 часов с последующим дополнительным добавлением дициклогексил-[2-(2,4,6-триизопропилфенил)-фенил]фосфана (12 мг, 0,0252 ммоль), трис(дибензилиденацетон)дипалладия(0) (22 мг, 0,0240 ммоль) и карбоната цезия (58 мг) и смесь перемешивали в атмосфере азота еще 2 часа. Затем реакционную смесь гасили водой (10 мл), NH4Cl (10 мл) и экстрагировали этилацетатом (20 мл). Затем органический слой промывали рассолом (15 мл), сушили над Na2SO4, фильтровали, затем концентрировали в вакууме. Неочищенный продукт очищали флэш-хроматографией (Biotage System) на силикагеле с использованием SNAP 10g в качестве колонки и циклогексан:этилацетат от 90:10 до 70:30 в качестве элюента с получением трет-бутил-N-[1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]циклопропил]карбамата (55 мг) в виде желтого твердого вещества.
ЖХ/МС: QC_3_MIN: Rt 2,634 мин; m/z 453 [М+Н]+.
Промежуточное соединение 23
1-Амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]циклопропанкарбоксамид
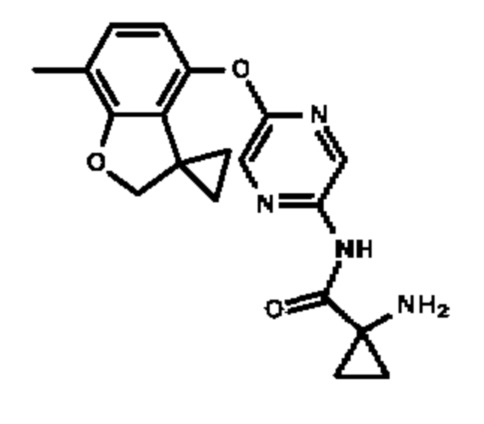
трет-Бутил-N-[1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]карбамоил]циклопропил]карбамат (Промежуточное соединение 22, 55 мг, 0,1215 ммоль) растворяли в дихлорметане (4 мл) и охлаждали до 0°С. По каплям добавляли 2,2,2-трифторуксусную кислоту (1154,7 мг, 10,026 ммоль) (0,8 мл) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Затем реакционную смесь охлаждали до 0°С и добавляли NaHCO3 до достижения рН 8. Затем эту смесь оставляли нагреваться до комнатной температуры и экстрагировали DCM (10 мл). Органический слой сушили над Na2SO4, фильтровали и концентрировали в вакууме с получением 1-амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]циклопропанкарбоксамида (40 мг) в виде желтого масла.
ЖХ/МС: QC_3_MIN: Rt 1,935 мин; m/z 353 [М+Н]+.
Промежуточное соединение 24
1,3-Дибензилокси-2-бром-бензол
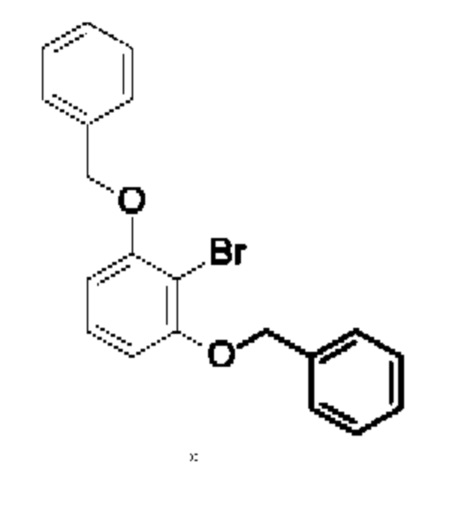
К раствору 2-бромбензол-1,3-диола (20 г, 105,8 ммоль) в ацетоне (200 мл) добавляли карбонат калия (43,87 г, 317,4 ммоль) с последующим добавлением бензилбромида (40,72 г, 238,1 ммоль) (28 мл) и реакционную смесь кипятили с обратным холодильником в течение 1,5 часов. После охлаждения реакционную смесь фильтровали под вакуумом и фильтрат концентрировали досуха. Остаток разбавляли этилацетатом (100 мл) и промывали водой (100 мл), а затем рассолом (100 мл). Фазы разделяли, органический слой сушили над Na2SO4, фильтровали и концентрировали. Остаток суспендировали в изопропаноле (8 объемов) и смесь нагревали при 80°С и перемешивали в течение 1 часа при этой температуре (до получения прозрачного раствора). Затем эту смесь оставляли нагреваться до комнатной температуры (в течение 1 часа) и полученную суспензию фильтровали. Твердое вещество промывали охлажденным на льду изопропанолом и затем сушили с получением указанного в заголовке соединения 1,3-дибензилокси-2-бром-бензола (34 г) в виде бледно-розового твердого вещества.
ЖХ/МС: QC_3_MIN: Rt 2,688 мин.
Промежуточное соединение 25
Бром-(1-метоксикарбонилциклопропил)цинк
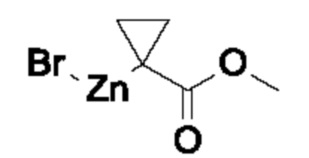
В двугорлую круглодонную колбу добавляли порошок активированного цинка (6,84 г, 104,6 ммоль) и этот порошок нагревали под вакуумом. Систему помещали в атмосферу аргона и добавляли безводный тетрагидрофуран (58 мл). Затем добавляли 1,2-дибромэтан (2,18 г, 11,62 ммоль) и эту смесь нагревали с обратным холодильником. Добавляли одной порцией хлортриметилсилан (505 мг, 4,65 ммоль) и смесь продолжали перемешивать при температуре дефлегмации. Раствор метил-1-бромциклопропилкарбоксилата (10,4 г, 58,1 ммоль) в безводном тетрагидрофуране (12 мл) медленно добавляли при той же температуре и реакционную смесь кипятили с обратным холодильником в течение 1,5 часов. Реакционную смесь охлаждали до комнатной температуры и оставляли стоять для оседания цинка с получением 70 мл 0,83М (теоретическое количество) раствора бром-(1-метоксикарбонилциклопропил)-цинка в THF, который использовали на следующей стадии без дополнительной обработки.
Промежуточное соединение 26
Метил-1-(2,6-дибензилоксифенил)циклопропанкарбоксилат
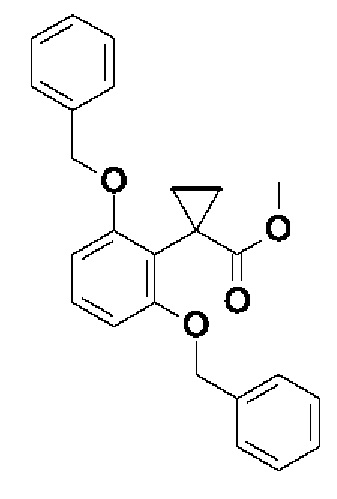
К раствору 1,3-дибензилокси-2-бром-бензола (Промежуточное соединение 24, 16 г, 43,33 ммоль) и бис(три-трет-бутилфосфин)палладия(0) (221 мг, 0,43 ммоль) в N,N-диметилформамиде (150 мл), предварительно нагретом до 70°С, добавляли 0,83М (теоретическое количество) раствор бром-(1-метоксикарбонилциклопропил)цинка в THF (Промежуточное соединение 25, 60 мл) (через катетер) и реакционную смесь перемешивали при той же температуре в течение 40 минут. После охлаждения реакционную смесь концентрировали под вакуумом до приблизительно 30 мл, остаток разбавляли этилацетатом (450 мл) и дважды промывали 1 н. водным раствором HCl (2×100 мл), а затем три раза охлажденным на льду рассолом (3×100 мл). Фазы разделяли и органический слой фильтровали под вакуумом на фильтре Гуча, собранном из фильтровальной бумаги и целлюлозы, и промывали этилацетатом. Фильтрат сушили над Na2SO4, фильтровали и упаривали с получением указанного в заголовке соединения метил-1-(2,6-дибензилоксифенил)циклопропанкарбоксилата (15,5 г), которое использовали на следующей стадии без дополнительной очистки.
ЖХ/МС: QC_3_MiN: Rt 2,606 мин; m/z 389 [М+Н]+.
Промежуточное соединение 27
4-Гидроксиспиро[бензофуран-3,1'-циклопропан]-2-он
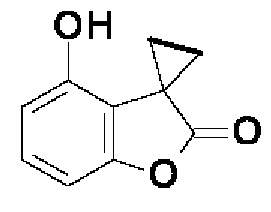
Реакцию проводили в трех разных циклах с использованием примерно 20 г исходного материала в каждом.
Общая методика: к смеси метил-1-(2,6-дибензилоксифенил)-циклопропанкарбоксилата (Промежуточное соединение 26, 20,4 г, 52,52 ммоль) и 5 масс. % палладия на углероде (1,02 г) в этаноле (200 мл) добавляли формиат аммония (16,56 г, 262,6 ммоль) и реакционную смесь перемешивали при 80°С в течение 1 часа. После охлаждения катализатор отфильтровывали через набивку целлюлозы и фильтрат концентрировали под вакуумом до приблизительно 20 мл.
Остатки, полученные от 3 циклов, объединяли и разбавляли этилацетатом (400 мл) и дважды промывали водой (2×300 мл). Две фазы разделяли и органическую фазу промывали рассолом (300 мл), сушили над Na2SO4 и концентрировали в вакууме с получением 4-гидроксиспиро[бензофуран-3,1'-циклопропан]-2-она (27,55 г) (содержащего приблизительно 10-15% нециклизованного промежуточного соединения метил-1-(2,6-дигидроксифенил)циклопропанкарбоксилата), который использовали на следующей стадии без дополнительной очистки.
ЖХ/МС: QC_3_MIN: Rt 1,707 мин.
Промежуточное соединение 28
4-Бензилоксиспиро[бензофуран-3,1'-циклопропан]-2-он
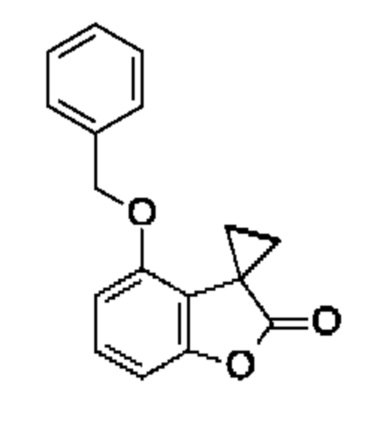
К раствору 4-гидроксиспиро[бензофуран-3,1'-циклопропан]-2-она
(Промежуточное соединение 27, 28,5 г, 161,8 ммоль) (содержащего приблизительно 10-15% нециклизованного промежуточного соединения метил-1-(2,6-дигидроксифенил)-циклопропанкарбоксилата) в ацетонитриле (200 мл)/тетрагидрофуране (50 мл) добавляли карбонат калия (33,54 г, 242,7 ммоль) и реакционную смесь перемешивали при 70°С в течение 1,5 часов. Затем реакционную смесь охлаждали до комнатной температуры и медленно добавляли бензилбромид (27,67 г, 161,8 ммоль). Реакционную смесь перемешивали при 60°С в течение 5 часов. После охлаждения реакционную смесь фильтровали под вакуумом и твердое вещество отбрасывали, фильтрат концентрировали до 50 мл, разбавляли этилацетатом (250 мл) и дважды промывали рассолом (2×100 мл). Фазы разделяли и органический слой сушили над Na2S04, фильтровали и упаривали с получением указанного в заголовке соединения 4-бензилоксиспиро[бензофуран-3,1'-циклопропан]-2-она (42,4 г), которое использовали на следующей стадии без дополнительной очистки.
ЖХ/МС: QC_3_MIN: Rt 2,389 мин; m/z 267 [М+Н]+.
Промежуточное соединение 29
3-Бензилокси-2-[1-(гидроксиметил)циклопропил]фенол
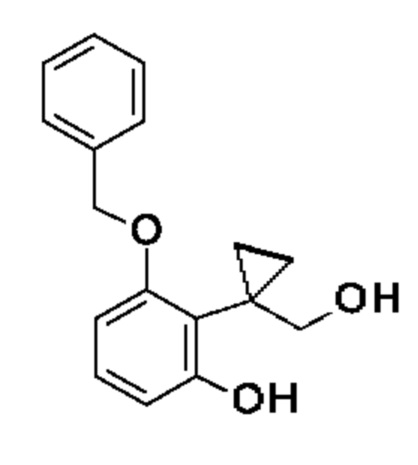
К раствору 4-бензилоксиспиро[бензофуран-3,1'-циклопропан]-2-она
(Промежуточное соединение 28, 42,4 г, 159,2 ммоль) в безводном тетрагидрофуране (300 мл) добавляли медленно при 0°С 1М раствор алюмогидрида лития в THF (79,6 мл, 79,6 ммоль) и реакционную смесь перемешивали при той же температуре в течение 30 минут. Реакционную смесь гасили льдом, водой (400 мл) и 1М водным раствором HCl (160 мл), а затем разбавляли этилацетатом (700 мл). Фазы разделяли и водный слой снова экстрагировали этилацетатом (500 мл). Объединенные органические фазы промывали рассолом (600 мл), сушили над Na2SO4, фильтровали и упаривали с получением указанного в заголовке соединения 3-бензилокси-2-[1-(гидроксиметил)циклопропил]фенола (43 г), которое использовали на следующей стадии без дополнительной очистки.
ЖХ/МС: QC_3_MIN: Rt 2,148 мин; m/z 271 [М+Н]+, m/z 293 [M+Na]+, m/z 253 [М-ОН]+.
Промежуточное соединение 30
4-Бензилоксиспиро[2Н-бензофуран-3,1'-циклопропан]
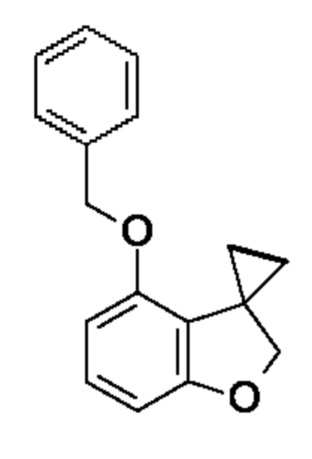
К раствору 3-бензилокси-2-[1-(гидроксиметил)циклопропил]фенола
(Промежуточное соединение 29, 43 г, 159,1 ммоль) в диметилкарбонате (430 мл) медленно добавляли трет-бутоксид калия (35,7 г, 318,1 ммоль) и реакционную смесь перемешивали при 85°С в течение 3,5 часов. Реакционную смесь охлаждали до комнатной температуры, концентрировали под вакуумом до 150 мл, разбавляли МТВЕ (400 мл) и промывали водой (400 мл). Фазы разделяли и водный слой снова экстрагировали МТВЕ (250 мл). Объединенные органические слои промывали рассолом (350 мл), сушили над Na2SO4, фильтровали и концентрировали с получением указанного в заголовке соединения 4-бензилоксиспиро[2Н-бензофуран-3,1'-циклопропана] (40 г), которое использовали на следующей стадии без дополнительной очистки.
ЖХ/МС: QC_3_MIN: Rt 2,457 мин; m/z 253 [М+Н]+.
Промежуточное соединение 31 (Промежуточное соединение 85 в WO 2012/076877)
1-спиро[2Н-бензофуран-3,1'-циклопропан]-4-ол
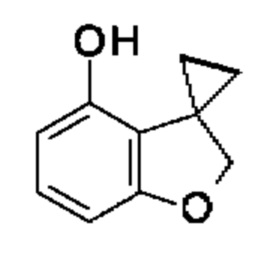
Реакцию проводили в два цикла с использованием 20 г исходного материала в каждом.
К смеси 4-бензилоксиспиро[2Н-бензофуран-3,1'-циклопропана] (Промежуточное соединение 30, 20 г, 79,27 ммоль) и формиата аммония (24,99 г, 396,34 ммоль) в этаноле (160 мл) добавляли 5 масс. % палладий на углероде (2,0 г) и реакционную смесь перемешивали при 80°С в течение 10 минут. После охлаждения катализатор отфильтровывали через набивку целлюлозы и фильтрат концентрировали под вакуумом до приблизительно 20 мл. Остатки, полученные от двух реакций, объединяли, смесь разбавляли этилацетатом (300 мл) и трижды промывали водой (3×200 мл), а затем рассолом (200 мл). Две фазы разделяли, органическую сушили над Na2SO4 и концентрировали под вакуумом. Остаток очищали флэш-хроматографией (Biotage System) на силикагеле, используя циклогексан:этилацетат от 99:1 до 85:15 в качестве элюента, с получением спиро[2Н-бензофуран-3,1'-циклопропан]-4-ола (17,75 г) в виде белого твердого вещества.
ЖХ/МС: QC_3_MIN: Rt 1,723 мин; m/z 163 [М+Н]+.
Промежуточное соединение 32
трет-Бутил-N-[(1S)-1-карбамоилпропил]карбамат
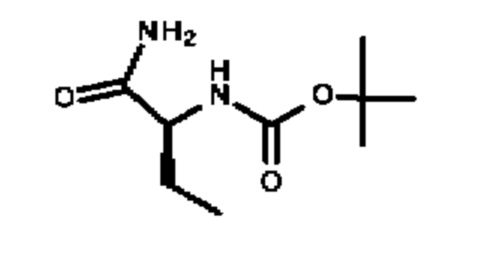
Указанное в заголовке соединение синтезировали по той же методологии, которую использовали для синтеза Промежуточного соединения 7, с заменой (2R)-2-(трет-бутоксикарбониламино)бутановой кислоты на (2S)-2-(трет-бутоксикарбониламино)бутановую кислоту.
ЖХ/МС: QC_3_MIN: m/z 147 [M-tBu+H]+, m/z 427 [2M+Na]+.
Промежуточное соединение 33
трет-Бутил-N-[(1S)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]пропил]карбамат
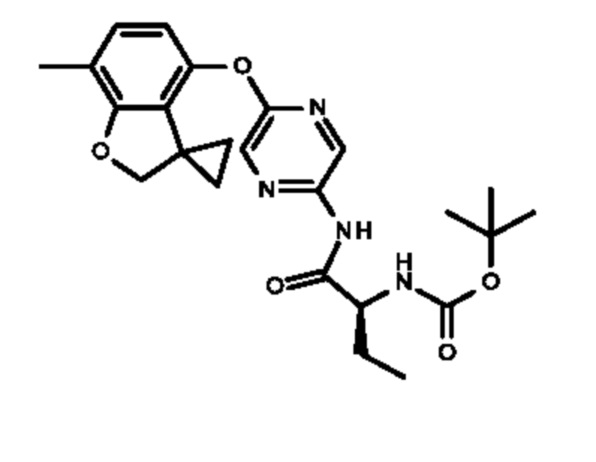
Указанное в заголовке соединение синтезировали в соответствии с методологией «пути 1», использованной для синтеза Промежуточного соединения 9, с заменой трет-бутил-N-[(1R)-1-карбамоилпропил]карбамата (Промежуточное соединение 7) на трет-бутил-N-[(1S)-1-карбамоилпропил]карбамат (Промежуточное соединение 32).
ЖХ/МС: QC_3_MIN: Rt 2,65 мин; m/z 455 [М+Н]+.
Промежуточное соединение 34
(2S)-2-Амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]бутанамид
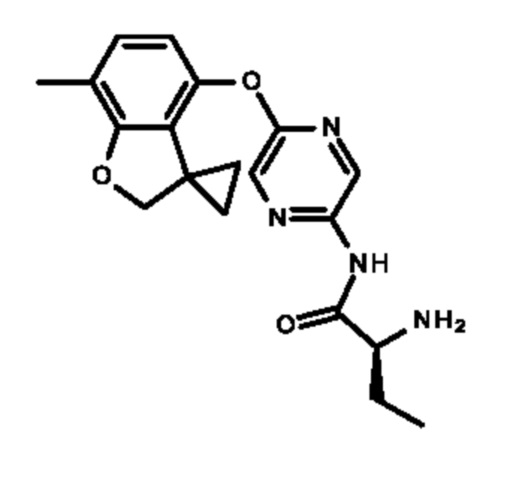
Указанное в заголовке соединение синтезировали по той же методике, что и для синтеза Промежуточного соединения 13, с заменой трет-бутил-N-[(1R)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]-пропил]карбамата (Промежуточное соединение 9) на трет-бутил-N-[(1S)-1-[[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]карбамоил]-пропил]карбамат (Промежуточное соединение 33).
ЖХ/МС: QC_3_MIN: Rt 1,98 мин; m/z 355 [М+Н]+.
Пример 1, путь 1
5,5-Диметил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-дион
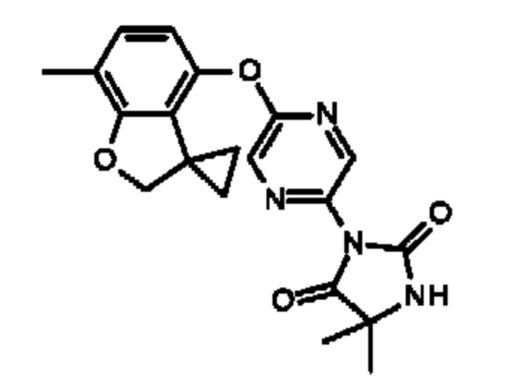
К раствору 2-бром-5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)окси-пиразина (Промежуточное соединение 1, 30 мг, 0,069 ммоль) в N,N-диметилацетамиде (1 мл) добавляли 5,5-диметилимидазолидин-2,4-дион (44,4 мг, 0,345 ммоль) и оксид меди(1) (5 мг, 0,035 ммоль). Колбу продували газообразным азотом и оставляли перемешиваться в течение ночи при 135°С. Реакционную смесь разбавляли EtOAc (10 мл) и сначала промывали водным насыщенным раствором хлорида аммония (20 мл), а затем рассолом (20 мл). Органический слой собирали, сушили над сульфатом натрия и упаривали досуха. Затем остаток очищали колоночной флэш-хроматографией, используя циклогексан:этилацетат от 80:20 до 40:60 в качестве элюента, с получением 5,5-диметил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона (17 мг) в виде белого твердого вещества.
1H-ЯМР (400 МГц; DMSO-d6): δ м.д. 8.72 (bs, 1H), 8.51 (d, 1H), 8.30 (d, 1H), 6.95 (dd, 1H), 6.53 (d, 1H), 4.46 (s, 2Н), 2.14 (s, 3Н), 1.42 (s, 6Н), 1.07-1.14 (m, 2Н),0.89-0.95 (m, 2Н).
Следующие соединения получали с использованием вышеуказанной методологии с заменой 2-бром-5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)окси-пиразина (Промежуточное соединение 1) на соответствующий бромпиразин и 5,5-диметилимидазолидин-2,4-диона на соответствующий гидантоин. Конечные продукты очищали флэш-хроматографией (картридж с диоксидом кремния; циклогексан/ЕЮАс или другая подходящая система растворителей) и/или обращенной хроматографией (картридж С-18; вода/ацетонитрил или другая подходящая система растворителей).
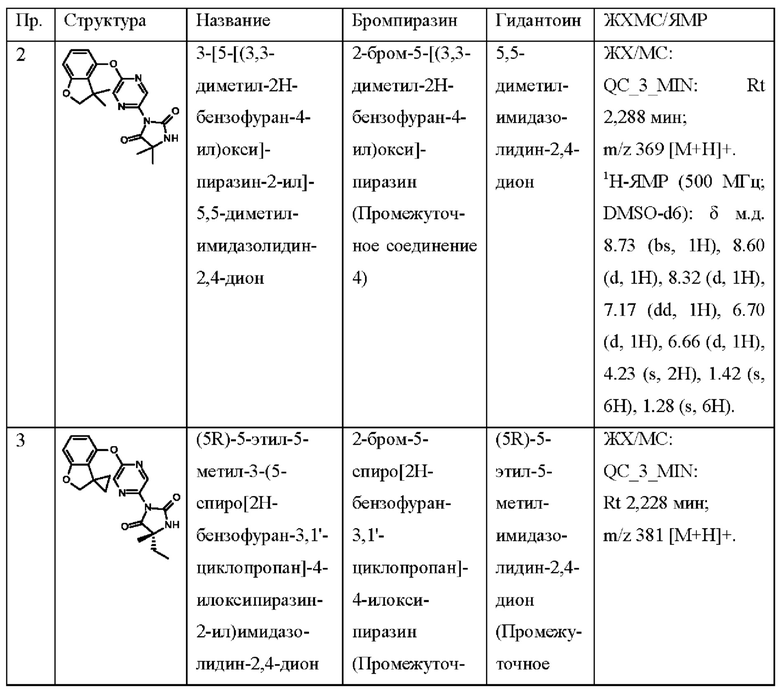

Пример 1, путь 2
5,5-Диметил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-дион
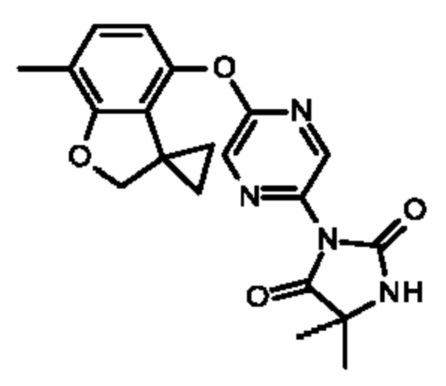
К раствору 3-(5-хлорпиразин-2-ил)-5,5-диметил-имидазолидин-2,4-диона (Промежуточное соединение 5, 20 мг, 0,083 ммоль) и 7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ола (Промежуточное соединение 156 в WO 2012076877, 22 мг, 0,125 ммоль) в ацетонитриле (1 мл) добавляли карбонат калия (17,2 мг, 0,12 ммоль). Реакционную смесь перемешивали в течение ночи при 60°С, а затем в течение 3 ч при 80°С. Реакционную смесь концентрировали под вакуумом и неочищенный продукт очищали флэш-хроматографией на силикагеле (BIOTAGE SYSTEM), используя SNAP 10g в качестве колонки и Chexane/EtOAc от 80/20 до 20/80 в качестве элюента. Фракция все еще была загрязненной примесями, и ее очищали обращенной хроматографией с использованием SNAP С-18 в качестве колонки и H2O/ACN от 95/5 до 5/95 в качестве элюента с получением 5,5-диметил-3-[5-(7-метилспиро)[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона (9,4 мг) в виде белого твердого вещества.
ЖХ/МС: QC_3_MIN: Rt 2,224 мин; m/z 381 [М+Н]+.
Следующие соединения получали с использованием вышеуказанной методологии с заменой 7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ола на соответствующий фенол и с использованием 3-(5-хлорпиразин-2-ил)-5,5-диметил-имидазолидин-2,4-диона (Промежуточное соединение 5) или с заменой его на соответствующее хлорпиразиновое промежуточное соединение. Конечные продукты очищали флэш-хроматографией (картридж с диоксидом кремния; никлогексан/EtOAc или другая подходящая система растворителей) и/или обращенной хроматографией (картридж С-18; вода/ацетонитрил или другая подходящая система растворителей).
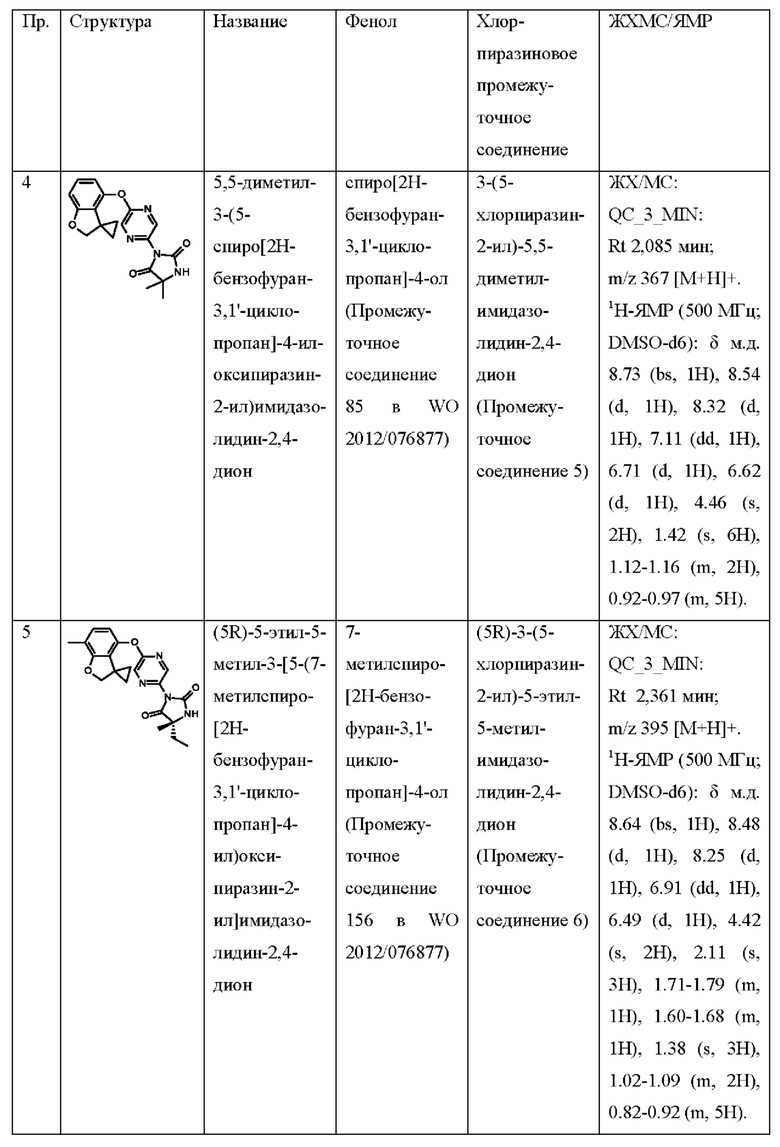
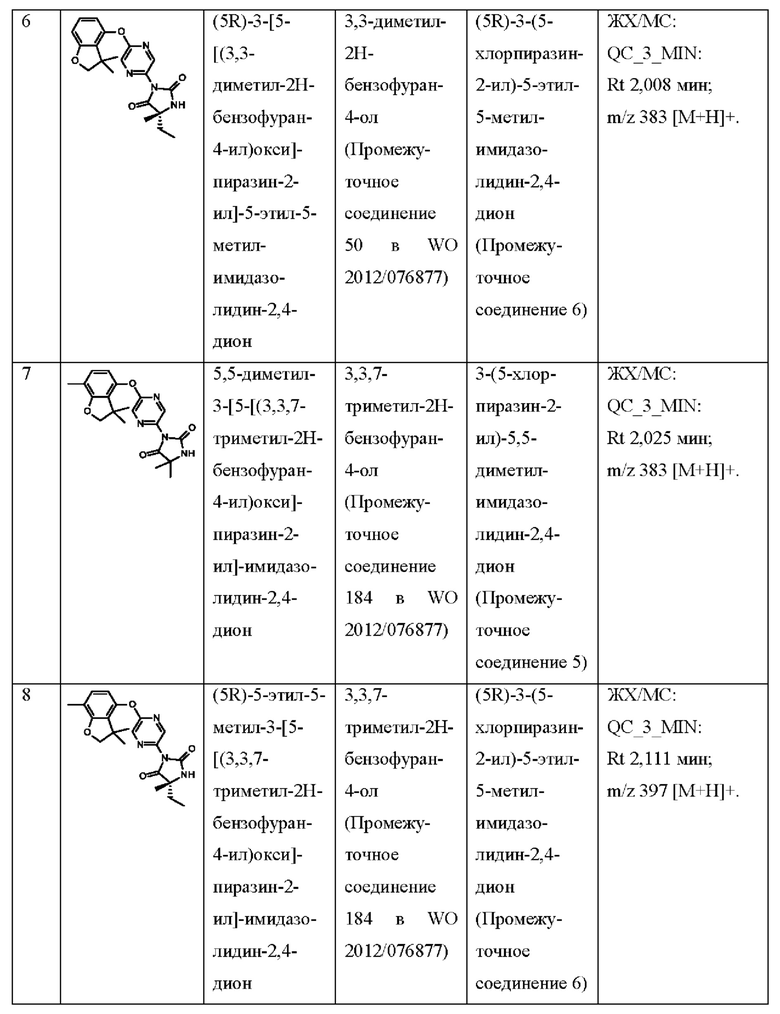
Пример 9 (путь 1)
(5R)-5-Этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-дион
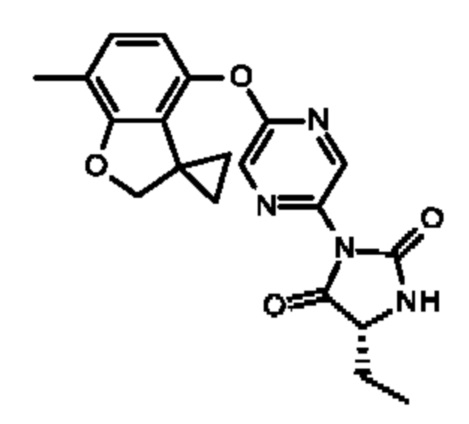
Смесь (2R)-2-амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]бутанамида (Промежуточное соединение 13, 13 мг, 0,037 ммоль) и N,N-диэтилэтанамина (11 мг, 0,11 ммоль) в дихлорметане (2 мл) охлаждали до 0°С. По каплям добавляли раствор бис(трихлорметил)карбоната (4,5 мг, 0,015 ммоль) в дихлорметане (0,5 мл) и реакционную смесь перемешивали в течение 1 часа при той же температуре. Добавляли дополнительное количество бис(трихлорметил)карбоната (1,5 мг) в дихлорметане (0,5 мл) и перемешивание продолжали в течение 30 минут. Смесь оставляли нагреваться до комнатной температуры. Реакционную смесь разбавляли дихлорметаном (20 мл) и органическую фазу промывали водным раствором 0,1 н. HCl (20 мл), а затем рассолом (20 мл). Фазы разделяли, органический слой сушили над Na2SO4, фильтровали и упаривали. Остаток очищали обращенно-фазовой хроматографией с использованием колонки SNAP С-18, элюируя смесью вода:ацетонитрил от 90:10 до 0:100. Соответствующие фракции объединяли и упаривали досуха с получением (5R)-5-этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона (7,5 мг) в виде белого твердого вещества.
ЖХ/МС: QC_3_MIN: Rt 2,305 мин; m/z 381 [М+Н]+. Энантиомерная чистота была подвтерждена как более 95% с использованием метода хирального контроля.
Пример 9 (путь 2)
(5R)-5-Этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-дион
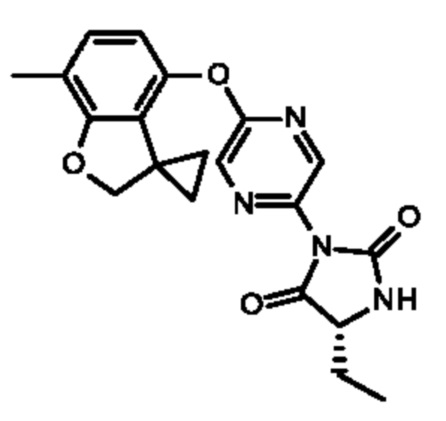
К раствору (2R)-2-амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]бутанамида (Промежуточное соединение 13, 21 г, 59,26 ммоль) в этилацетате (500 мл) добавляли 1-1'-карбонилдиимидазол (10,57 г, 65,18 ммоль) в 5 порциях по 2 г каждая и перемешивали при комнатной температуре в течение 4 часов. Реакционную смесь гасили льдом и добавляли водный 0,2 н. раствор HCl (250 мл). Две фазы разделяли и органический слой промывали водным 0,2 н. раствором HCl (250 мл) и рассолом (200 мл), затем сушили над сульфатом натрия, фильтровали и упаривали досуха. Неочищенный продукт разделяли на 4 аликвоты по приблизительно 4,2 г каждая, и каждую аликвоту очищали флэш-хроматографией на силикагеле, используя SNAP (100G) в качестве колонки и циклогексан/этилацетат от 80/20 до 20/80 в качестве элюента. Желаемые фракции из каждого опыта собирали и растворитель выпаривали до получения сухого остатка. Полученное светло-желтое твердое вещество суспендировали в растворе циклогексан/этилацетат (1/1, 3 объема) (90 мл) и перемешивали в течение 2 часов при 50°С. Затем смесь оставляли охлаждаться до комнатной температуры и фильтровали под вакуумом. Влажный осадок промывали охлажденным на льду циклогексаном (15 мл), твердое вещество собирали и сушили с получением указанного в заголовке соединения (5R)-5-этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1')-циклопропан]-4-ил)оксипиразин-2-ил]-имидазолидин-2,4-диона (13,6 г) в виде белого твердого вещества.
1H-ЯМР (500 МГц; DMSO-d6): δ м.д. 8.69 (bs, 1H), 8.52 (d, 1Н), 8.26 (d, 1H), 6.94 (d, 1Н), 6.53 (d, 1H), 4.46 (s, 2Н), 4.26-4.30 (m, 1H), 2.14 (s, 3Н), 1.77-1.86 (m, 1H), 1.65-1.76 (m, 1H), 1.07-1.12 (m, 2Н), 0.90-0.99 (m, 5Н).
Следующие соединения получали с использованием вышеуказанной методологии (либо путь 1, либо путь 2) с заменой (2R)-2-амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]бутанамида (Промежуточное соединение 13) на соответствующий бутанамид. Конечные продукты очищали флэш-хроматографией (картридж с диоксидом кремния; циклогексан/EtOAc или другая подходящая система растворителей) и/или обращенной хроматографией (картридж С-18; вода/ацетонитрил или другая подходящая система растворителей).
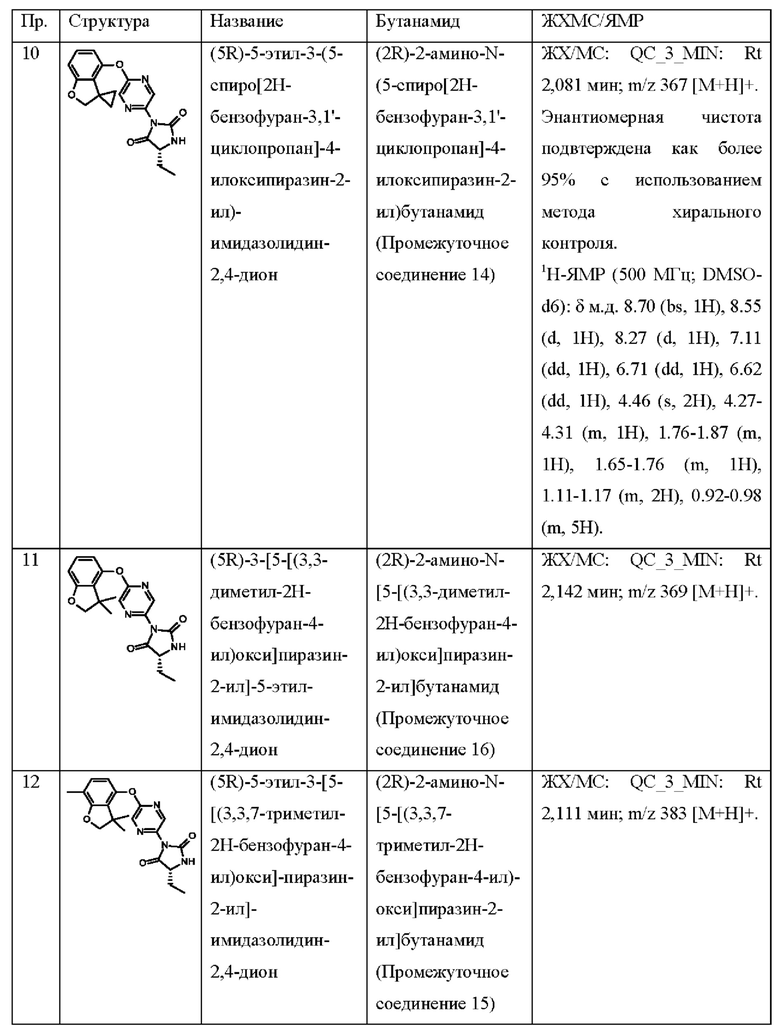
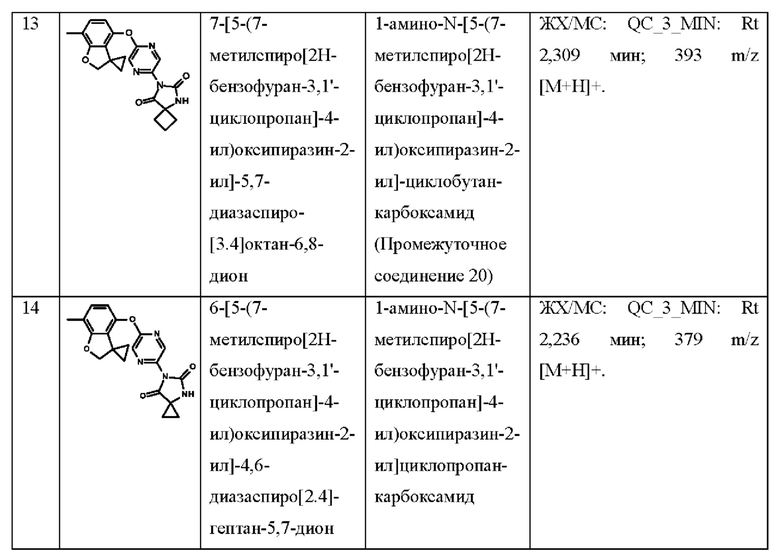
Пример 15
(5S)-5-Этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-дион
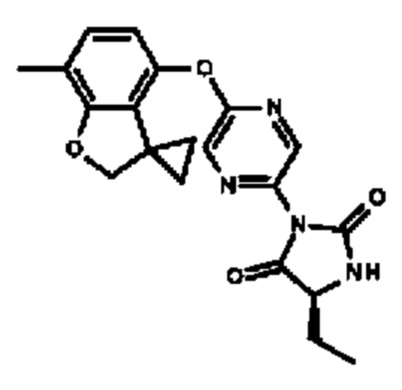
Указанное в заголовке соединение синтезировали в соответствии с методологией «пути 1», использованной для синтеза Промежуточного соединения 9, с заменой (2R)-2-амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]бутанамида (Промежуточное соединение 13) на (2S)-2-амино-N-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]бутанамид (Промежуточное соединение 34).
ЖХ/МС: QC_3_MIN: Rt 2,29 мин; m/z 381 [М+Н]+.
Биологические Примеры
Биологический Пример 1: Измерение модуляции каналов Kv3.1, Kv3.2 и Kv3.3
Способность соединений по изобретению модулировать подтипы потенциалзависимых калиевых каналов Kv3.3/Kv3.2/Kv3.1 может быть определена с использованием следующего анализа. Аналогичные методы могут быть использованы для исследования способности соединений по изобретению модулировать другие подтипы каналов.
Биология клетки
Для оценки эффектов соединений в отношении каналов Kv3.3 человека (hKv3.3) создавали стабильную клеточную линию, экспрессирующую каналы Kv3.3 человека, путем трансфекции клеток яичника китайского хомячка (CHO)-K1 вектором pBacMire_KCNC-3. Клетки культивировали в среде DMEM (Среда Игла, модифицированная по способу Дульбекко)/F12 (Gibco) с добавлением 10%-ной эмбриональной бычьей сыворотки (Gibco), 1X заменимых аминокислот (Invitrogen) и 400 мкг/мл генетицина (G418). Клетки выращивали и поддерживали при 37°С в увлажненной среде, содержащей 5% СО2 в воздухе.
Для оценки эффектов соединений в отношении каналов Kv3.2 человека (hKv3.2) создавали стабильную клеточную линию, экспрессирующую каналы Kv3.2 человека (hKv3.2), путем трансфекции клеток СНО-K1 вектором pCIH5-hKv3.2. Клетки культивировали в среде DMEM/F12 с добавлением 10%-ной эмбриональной бычьей сыворотки (Gibco), IX заменимых аминокислот (Invitrogen) и 500 мкг/мл гигромицина-В (Invitrogen). Клетки выращивали и поддерживали при 37°С в увлажненной среде, содержащей 5% СО2 в воздухе.
Для оценки эффектов соединений в отношении каналов Kv3.1 человека (hKv3.1):
Клеточную линию эмбриональной почки человека (HEK)-hKv3.1 генерировали путем трансфекции клеток HEK-293 экспрессионным вектором с человеческим Kv3.1 (NM_004976.4). Клетки культивировали в среде MEM с добавлением 10%-ного инактивированного нагреванием FBS, 2 мМ L-глутамина, 1%-ного пенициллина-стрептомицина и 0,6 мг/мл генетицина (G418). Клетки HEK-hKv3.1b амплифицировали в колбе Т175 см2 при 37°С с 5% СО2, используя среду MEM для амплификации, содержащую селективный антибиотик G418 (0,6 мг/мл). Клетки отделяли каждые 3-4 суток, используя забуференный фосфатом физиологический раствора Дульбекко (DPBS) для двукратной промывки колбы, затем TrypLE для удаления клеток, и повторно высевали при плотности 2-4×106 клеток/колбу.
Приготовление клеток для экспериментов IonWorks Quattro™
В день эксперимента клетки извлекали из инкубатора и культуральную среду удаляли. Клетки промывали 5 мл PBS Дульбекко (DPBS), не содержащего кальций и магний, и отделяли путем добавления 3 мл Versene (Invitrogen, Италия) с последующей кратковременной инкубацией при 37°С в течение 5 минут. Колбу встряхивали для разделения клеток и добавляли 10 мл DPBS, содержащего кальций и магний, с получением суспензии клеток. Затем эту суспензию клеток помещали в центрифужную пробирку на 15 мл и центрифугировали в течение 2 мин при 1200 об/мин. После центрифугирования супернатант удаляли и клеточный осадок повторно суспендировали в 4 мл DPBS, содержащего кальций и магний, используя пипетку на 5 мл для разрушения осадка. Затем объем клеточной суспензии корректировали для получения концентрации клеток для анализа примерно 3 миллиона клеток на мл.
Все растворы, добавляемые к клеткам, предварительно нагревали до 37°С.
Электрофизиология
Ionworks
Эксперименты проводили при к.т.с использованием электрофизиологической технологии на плоской матрице IonWorks Quattro™ (Molecular Devices Corp.) с помощью PatchPlate™ PPC. Протоколы стимуляции и сбор данных осуществляли с помощью микрокомпьютера (Dell Pentium 4). Межэлектродное сопротивление плоских электродов (Rp) определяли посредством подачи скачков разности потенциалов 10 мВ через каждую ячейку. Эти измерения выполняли перед добавлением клеток. После добавления клеток и создания изоляции проводили проверку изоляции посредством приложения скачка разности потенциалов от -80 мВ до -70 мВ в течение 160 мс. После этого добавляли раствор амфотерицина-В к стороне электрода внутри ячейки для получения доступа к внутреннему содержимому клетки. Клетки выдерживали при -70 мВ. Вычитание утечки проводили во всех экспериментах посредством применения 50 мс гиперполяризующих (10 мВ) опережающих импульсов, чтобы вызвать токи утечки, с последующим 20 мс периодом при потенциале покоя перед тестовыми импульсами.
Для hKv3.2 и hKv3.1 анализов, начиная от исходного потенциала -70 мВ, первый тестовый импульс при -15 мВ применяли в течение 100 мс, а после 100 мс при -70 мВ применяли второй импульс при +40 мВ в течение 50 мс. Затем клетки выдерживали в течение 100 мс при -100 мВ и применяли еще один импульс от -70 мВ до +40 мВ (длительность 50 мс), с последующей фиксацией напряжения при -40 мВ в течение 200 мс.
Для hKv3.3 анализов, начиная от исходного потенциала -70 мВ, первый тестовый импульс при 0 мВ применяли в течение 500 мс, а затем после 100 мс при -70 мВ применяли второй импульс до 40 мВ в течение 200 мс. Эти более длительные тестовые импульсы используют для изучения инактивации каналов hKv3.3. Протокол тестовых импульсов может быть осуществлен в отсутствие (до считывания) и в присутствии (после считывания) тестируемого соединения. Считывания до и после могут быть разделены добавлением соединения с последующей 3-минутной инкубацией.
Растворы и лекарственные средства
Внутриклеточный раствор содержал следующее (в мМ): K-глюконат 100, KCl 54, MgCl2 3,2, N-2-гидроксиэтилпиперазин-N-2-этансульфоновую кислоту (HEPES) 5, при значении рН, доведенном до 7,3 с помощью КОН. Раствор амфотерицина-В готовили в виде исходного раствора 50 мг/мл в DMSO и разбавляли до конечной рабочей концентрации 0,1 мг/мл во внутриклеточном растворе. Внешний раствор представлял собой забуференный фосфатом физиологический раствор Дульбекко (DPBS) и содержал следующее (в мМ): CaCl2 0,90, KCl 2,67, KH2PO4 1,47, MgCl⋅6H2O 0,493, NaCl 136,9, Na3PO4 8,06, с рН 7,4.
Соединения, используемые в изобретении (или референсные соединения, такие как N-циклогексил-N-[(7,8-диметил-2-оксо-1,2-дигидро-3-хинолинил)метил]-N'-фенил-мочевина) растворяли в диметилсульфоксиде (DMSO) при исходной концентрации 10 мМ. Эти растворы дополнительно разбавляли DMSO с использованием Biomek FX (Beckman Coulter) в планшете на 384 соединения. Каждое разведение (1 мкл) переносили в другой планшет для соединений и добавляли внешний раствор, содержащий 0,05% плюроновой кислоты (66 мкл). Добавляли 3,5 мкл из каждого планшета, содержащего соединение по изобретению, и инкубировали с клетками во время эксперимента Ion Works Quattro™ Конечное разведение для анализа составило 200, а конечные концентрации соединений находились в диапазоне от 50 мкМ до 50 нМ.
Анализ данных
Показания приборов анализировали и собирали, используя как сопротивление изоляции (более 20 МОм), так и максимальную амплитуду тока (более 500 пА при скачке разности потенциалов 40 мВ) в отсутствие соединения, чтобы исключить неподходящие клетки из дальнейшего анализа. Для анализов hKv3.2 и hKv3.1, парные сравнения значений вызванных токов перед добавлением лекарственного средства и после добавления лекарственного средства, измеренные для потенциала -15 мВ, использовали для определения эффекта положительной модуляции для каждого соединения. Опосредованные каналами Kv3 внешние токи определяли путем измерения средней амплитуды тока в течение заключительных 10 мс импульса напряжения -15 мВ минус средний базовый ток при -70 мВ в течение периода 10 мс сразу перед стадией -15 мВ. Эти токи каналов Kv3 после добавления тестируемого соединения затем сравнивали с токами, зарегистрированными до добавления соединения. Данные нормализовали по максимальному эффекту референсного соединения (50 мкМ N-циклогексил-N-[(7,8-диметил-2-оксо-1,2-дигидро-3-хинолинил)метил]-N'-фенил-мочевины) и по эффекту контрольного носителя (0,5% DMSO). Эти нормализованные данные анализировали с использованием программного обеспечения ActivityBase или Excel. Концентрацию соединения, требуемую для увеличения токов на 50% от максимального увеличения, вызываемого референсным соединением (ЕС50), определяли путем аппроксимации данных зависимости ответа от концентрации с использованием четырехпараметрической логистической функции в ActivityBase. Для анализов hKv3.3, парные сравнения вызванных токов в интервале до добавления лекарственного средства и после добавления лекарственного средства измеряли для шага 0 мВ, учитывая пиковый ток и затухание (инактивацию) тока в течение длительности тестового импульса 0 мВ (500 мс).
N-Циклогексил-N-[(7,8-диметил-2-оксо-1,2-дигидро-3-хинолинил)метил]-N'-фенилмочевину получили от ASINEX (регистрационный номер: 552311-06-5).
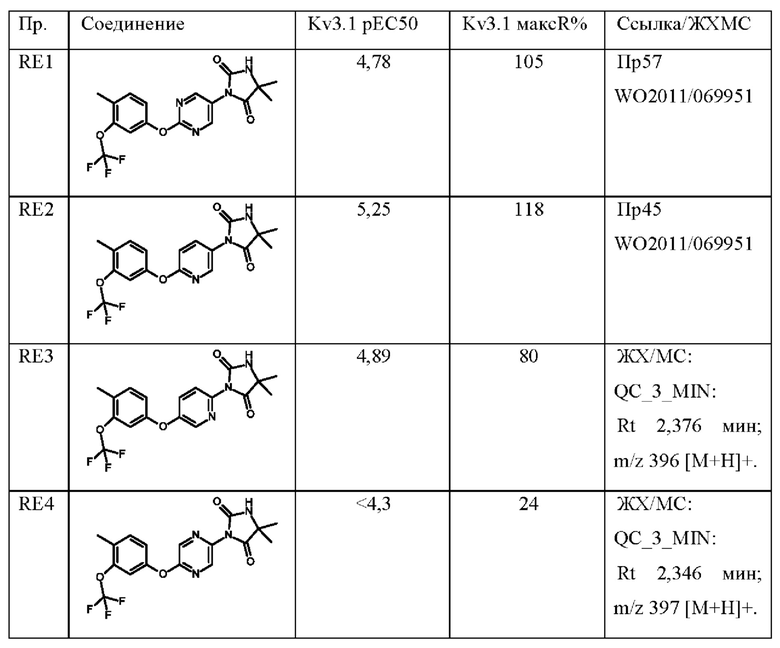
Как показано в тестировании RE1-RE4, включение пиразинового кольца может отрицательно влиять на значения рЕС50 и максR модуляторов Kv3.1.
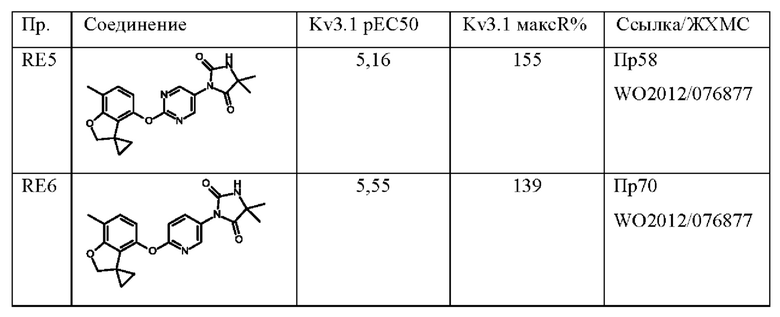
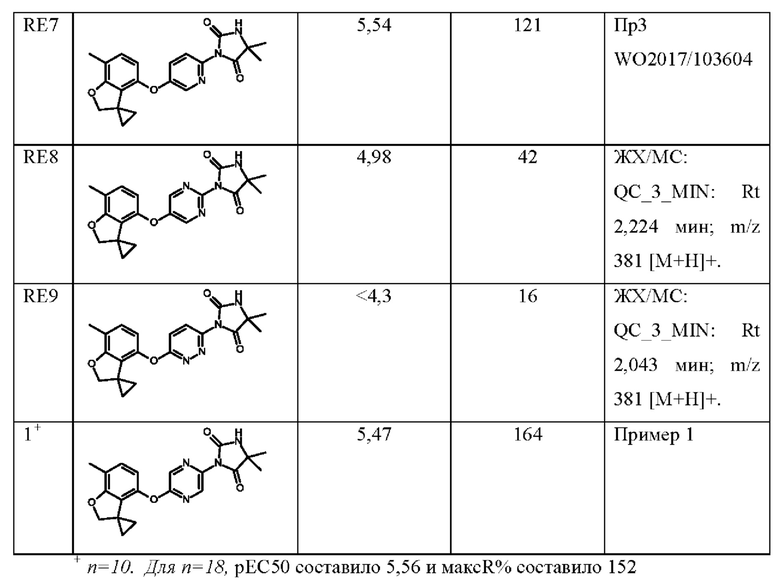
Как показано в тестировании RE5-RE9 по сравнению с Примером 1, включение пиразинового кольца в Примере 1 неожиданно приводит к высокому значению рЕС50 и высокому значению макcR в анализе Kv3.1.
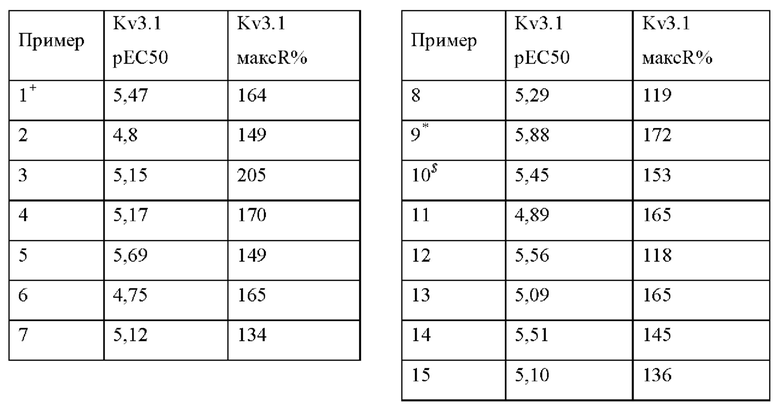

Все протестированные примеры соединений формулы (I) показаны выше и демонстрируют хорошие свойства в анализе Kv3.1, выраженные в рЕС50 и максR.
Вторичный анализ данных описанных hKv3.1, hKv3.2 и hKv3.3 анализов может быть использован для исследования эффектов соединений в отношении скорости нарастания тока от начала деполяризующих импульсов напряжения. Величина эффекта соединения может быть определена из постоянной времени (Tauact), полученной из нелинейной аппроксимации с использованием приведенного ниже уравнения нарастания токов Kv3.1, Kv3.2 и Kv3.3 после начала деполяризующего импульса напряжения -15 мВ.
Y=(Y0 - Yмакс) * ехр(-K*Х)+Yмакс,
где:
Y0 представляет собой значение тока в начале деполяризующего импульса напряжения;
Yмакс представляет собой значение тока при достижении плато;
K представляет собой константу скорости, и
Tauact представляет собой постоянную времени активации, которая является величиной, обратной K.
Аналогичным образом, можно исследовать эффект соединений в отношении времени затухания токов Kv3.1, Kv3.2 или Kv3.3 при закрытии каналов в конце деполяризующих импульсов напряжения -15 мВ. В этом последнем случае величина эффекта соединения в отношении закрытия канала может быть определена из постоянной времени (Taudeact) нелинейной аппроксимации затухания тока («следовой ток») сразу по окончании деполяризующего импульса напряжения.
Каналы Kv3.1, Kv3.2 и Kv3.3 должны активироваться и дезактивироваться очень быстро, чтобы дать возможность нейронам возбуждать потенциалы действия с высокой частотой (Rudy et at., 2001). Замедление активации будет, по-видимому, задерживать наступление реполяризации потенциала действия; замедление дезактивации может привести к гиперполяризующим токам, что снижает возбудимость нейрона и задерживает время до того, как нейрон сможет возбудить дополнительный потенциал действия. Вместе эти два замедляющих эффекта в отношении активации и дезактивации каналов скорее всего приведут к снижению, а не к облегчению способности нейронов возбуждаться при высоких частотах. Таким образом, соединения, которые обладают таким замедляющим эффектом в отношении каналов Kv3.1 и/или Kv3.2 и/или Kv3.3, будут эффективно вести себя как отрицательные модуляторы каналов, приводя к замедлению возбуждения нейронов. Этот последний эффект был продемонстрирован для некоторых соединений, раскрытых в WO 2011/069951, где заметное увеличение Tauact можно наблюдать из записей, снятых с «быстровозбуждающихся» интернейронов в коре головного мозга крысы с использованием электрофизиологических методов in vitro. Добавление соответствующих соединений снижает способность нейронов возбуждаться в ответ на серии деполяризующих импульсов при 300 Гц.
Следовательно, хотя некоторые соединения могут быть идентифицированы действующими как положительные модуляторы в анализе рекомбинантных клеток, те соединения, которые заметно увеличивают значение Tauact, могут снижать способность нейронов в нативных тканях возбуждаться при высокой частоте.
Биологический Пример 2: Определение связывания в крови и ткани мозга
Материалы и методы
Цельную кровь крысы, собранную на неделе эксперимента с использованием K3-EDTA в качестве антикоагулянта, разбавляли изотоническим фосфатным буфером 1:1 (об./об.). Цельный мозг крысы, хранящийся в замороженном виде при -20°С, размораживали и гомогенизировали в искусственной спинномозговой жидкости (CSF) 1:2 (масс./об.).
Соответствующее количество тестируемого соединения растворяли в DMSO с получением 5 миллимолярного раствора. Затем готовили дополнительные разведения для получения рабочего раствора 166,7 микромоль, используя 50% ацетонитрил в воде MilliQ. Этот рабочий раствор использовали для добавления в образец крови для получения конечной концентрации 0,5 мкмоль в цельной крови. Подобным образом, этот рабочий раствор использовали для добавления в образцы головного мозга, чтобы получить конечную концентрацию 5 микромоль в цельном мозге. Из этих препаратов крови и головного мозга сразу же извлекали контрольные образцы (n=3), которые использовали для расчета изначального восстановления тестируемых образцов.
150 мкл буфера, не содержащего соединений (изотонический фосфатный буфер для крови или буфер искусственной спинномозговой жидкости для мозга), распределяли в одну половину лунки, а 150 мкл подготовленного образца (кровь или мозг) загружали в другую половину лунки, где эти две половинки разделены полупроницаемой мембраной. После периода уравновешивания в течение 5 часов при 37°С, 50 мкл диализованного образца (кровь или мозг) добавляли к 50 мкл соответствующего буфера, не содержащего соединений, и наоборот для буфера, так что объем буфера для образца (кровь или мозг) остается прежним. Затем образцы экстрагировали путем осаждения белка с помощью 300 мкл ацетонитрила, содержащего ролипрам (контроль для режима положительной ионизации) или диклофенак (контроль для режима отрицательной ионизации) в качестве внутренних стандартов, и центрифугировали в течение 10 минут при 2800 об/мин. Супернатанты собирали (100 мкл), разбавляли 18% ACN в воде MilliQ (200 мкл) и затем вводили в систему ВЭЖХ-МС/МС или УЭЖХ-МС/МС для определения концентрации присутствующего тестируемого соединения.
Анализ
Связывание в крови и ткани мозга затем определяли по следующим формулам:
Afu=Буфер/Кровь или Afu=CSF/Мозг,
где Afu представляет собой кажущуюся несвязанную фракцию; Буфер представляет собой соотношение аналит/внутренний стандарт, определенное в буферном компартменте; Кровь представляет собой соотношение аналит/внутренний стандарт, определенное в компартменте крови; Мозг представляет собой соотношение аналит/внутренний стандарт, определенное в компартменте мозга.
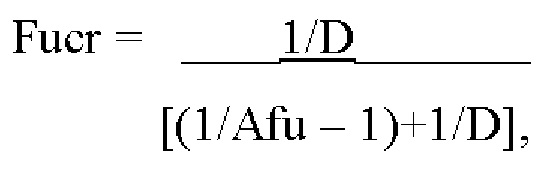
где: fucr представляет собой скорректированную несвязанную фракцию; D представляет собой коэффициент разведения образца (D=2 для крови и D=3 для мозга).
Затем:
% Связывания=(1-fucr) × 100
% Несвязанного=100 - % связанного
Определение соотношения Мозг/Кровь (Kbb)
Для соединений, свободно проникающих через гематоэнцефалический барьер (ВВВ), несвязанные концентрации в крови и головном мозге будут эквивалентны в условиях распределения в равновесном состоянии. Следовательно, значение Kbb может быть рассчитано как:
Fu(кровь)/Tu(мозг),
которое, как ожидается, будет эквивалентно соотношению концентраций в мозге и крови (Ct(мозг)/Ct(кровь)), если не задействованы переносчики эффлюксного насоса.
Биологический Пример 3: Определение фармакокинетических параметров in vivo
Материалы и методы
Взрослым самцам крыс (Charles River, Италия) перорально вводили тестируемое соединение в дозе 1 мг/кг (5 мл/кг, в 5% об./об. DMSO, 0,5% масс./об. НРМС в воде) и внутривенно в дозе 0,5 мг/кг (2 мл/кг в 5% об./об. DMSO (40% масс./об. PEG400 в физиологическом растворе). После перорального введения образцы крови собирали под глубокой анестезией изофлуораном из воротной вены и сердца каждой крысы (по 1 крысе на момент времени). После внутривенного введения у каждой крысы брали серийные образцы крови из латеральной хвостовой вены. Еще одна группа крыс (n=1 на каждое тестируемое соединение) получала однократное внутривенное введение ингибитора транспорта PgP элакридара (3 мг/кг) незадолго до перорального введения тестируемого соединения в дозе 1 мг/кг, как указано выше. Образцы крови и головного мозга собирали через 0,5 часа после введения дозы для этих животных. Во всех случаях образцы крови собирали в пробирки с EDTA калия.
Образцы крови и головного мозга могут быть проанализированы на концентрацию тестируемого соединения с использованием способа, основанного на осаждении белка ацетонитрилом с последующим анализом ВЭЖХ/МС-МС с помощью оптимизированного аналитического метода.
Анализ
Концентрации тестируемого соединения в крови (выраженные в нг/мл) и головном мозге (выраженные в нг/г) в различные моменты времени после перорального или внутривенного введения анализировали с использованием некомпартментной фармакокинетической модели с использованием WinNonLin Professional версии 4.1. Получали следующие параметры:
Внутривенное дозирование: максимальная концентрация с течением времени (Смаке), интегрированная концентрация с течением времени (AUC), клиренс (Clb), объем распределения (Vss) и период полувыведения (t1/2).
Пероральное дозирование: Смаке, время достижения максимальной концентрации (Тмакс), AUC, биодоступность (F%), абсорбированная фракция (Fa%), соотношение кровь-мозг (AUC ВВ) и кратное изменение AUC ВВ в присутствии элакридара.
Соединения по изобретению, как можно ожидать, демонстрируют хорошую доступность в ткани мозга.
Дополнительные животные модели
В патентных заявках WO 2011/069951, WO 2012/076877, WO 2012/168710, WO 2013/083994 WO 2013/175215 и WO 2013/182851 (все включены в качестве ссылки с целью иллюстрации потенциальной применимости соединений и предоставления животных моделей для тестирования соединений) продемонстрирована активность соединений, которые являются модуляторами Kv3.1 и Kv3.2, на животных моделях судорог, гиперактивности, расстройств сна, психоза, нарушений слуха и биполярных расстройств.
В патентной заявке WO 2013/175211 (включенной в качестве ссылки с целью иллюстрации потенциальной применимости соединений и предоставления животных моделей для тестирования соединений) продемонстрирована эффективность соединения, которое является модулятором Kv3.1 и Kv3.2, в модели острой потери слуха, вызванной шумом, у шиншиллы, а также оценена эффективность соединения в модели дефицита центральной слуховой обработки и в модели шума в ушах.
Glait et al 2018, Anderson et al 2018 и Chamber et al 2018 продемонстрировали эффективность модулятора Kv3.1 и Kv3.2 в моделях, связанных со слухом.
В патентной заявке WO 2017/098254 (включенной в качестве ссылки с целью иллюстрации потенциальной применимости соединений и предоставления животных моделей для тестирования соединений) продемонстрирована эффективность соединения, которое является модулятором Kv3.1 и Kv3.2, в моделях невропатической и воспалительной боли.
Во всем описании и следующей формуле изобретения, если по контексту не требуется иного, слово «содержать» и такие варианты, как «содержит» и «содержащий», следует понимать как подразумевающие включение указанного целого числа, стадии, группы целых чисел или группы стадий, но не исключение любого другого целого числа, стадии, группы целых чисел или группы стадий.
Заявка, частью которой является данное описание и формула изобретения, может быть использована в качестве основы для приоритета в отношении любой последующей заявки. Формула изобретения такой последующей заявки может быть направлена на любой признак или комбинацию признаков, описанных в данном документе. Они могут быть представлены как продукт, композиция, способ или пункт на применение и могут включать, в качестве примера и без ограничения, пункты, которые следуют ниже.
Пункты изобретения:
Пункт 1 - Соединение формулы (I):
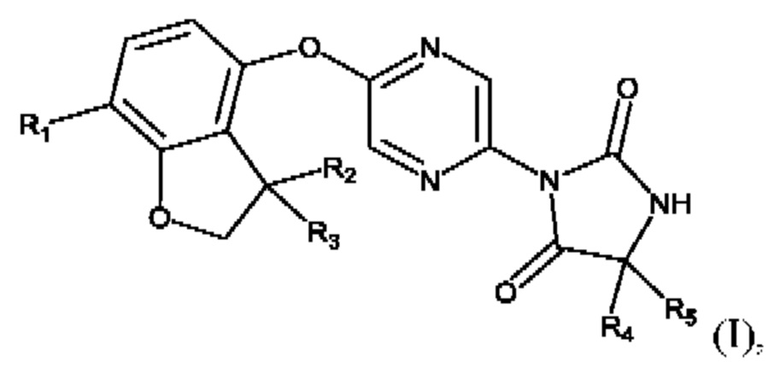
где:
R1 представляет собой Н или метил;
R2 и R3 оба представляют собой метил, или R2 и R3, вместе с атомом углерода, к которому они присоединены, образуют спироциклопропильное кольцо;
R4 представляет собой метил или этил;
R5 представляет собой Н или метил;
или R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют С3-С4 спирокарбоциклил;
или его соль и/или сольват и/или производное.
Пункт 2 - Соединение согласно пункту 1, где R1 представляет собой Н.
Пункт 3 - Соединение согласно пункту 1, где R1 представляет собой метил.
Пункт 4 - Соединение согласно любому из пунктов 1-3, где R2 и R3 представляют собой спироциклопропильное кольцо.
Пункт 5 - Соединение согласно любому из пунктов 1-3, где R2 представляет собой метил и R3 представляет собой метил.
Пункт 6 - Соединение согласно любому из пунктов 1-5, где R4 представляет собой метил.
Пункт 7 - Соединение согласно любому из пунктов 1-5, где R4 представляет собой этил.
Пункт 8 - Соединение согласно любому из пунктов 1-7, где R5 представляет собой Н.
Пункт 9 - Соединение согласно любому из пунктов 1-7, где R5 представляет собой метил.
Пункт 10 - Соединение согласно любому из пунктов 1-9, где, когда R4 и R5 являются разными, они имеют следующую стереохимическую конфигурацию:
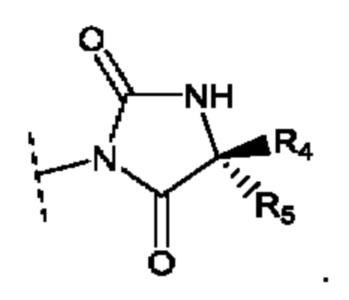
Пункт 11 - Соединение согласно любому из пунктов 1-9, где, когда R4 и R5 являются разными, они имеют следующую стереохимическую конфигурацию:
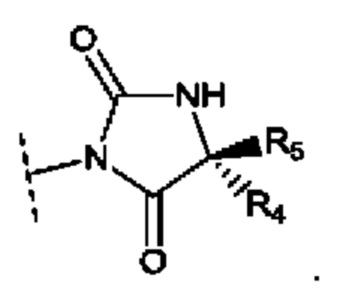
Пункт 12 - Соединение согласно любому из пунктов 1-5, где R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют спироциклопропил.
Пункт 13 - Соединение согласно любому из пунктов 1-5, где R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют спироциклобутил.
Пункт 14 - Соединение согласно пункту 1, выбранное из группы, состоящей из:
5,5-диметил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-диона;
3-[5-[(3,3-диметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-5,5-диметил-имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
5,5-диметил-3-(5-спиро[2Н-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
(5R)-3-[5-[(3,3-диметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-5-метил-имидазолидин-2,4-диона;
5,5-диметил-3-[5-[(3,3,7-триметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-имид азо лид ин-2,4-д ио на;
(5R)-5-этил-5-метил-3-[5-[(3,3,7-триметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-3-(5-спиро[2Н-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
(5R)-3-[5-[(3,3-диметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-имидазолидин-2,4-диона;
(5R)-5-этил-3-[5-[(3,3,7-триметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-имидазолидин-2,4-диона;
7-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-5,7-диазаспиро[3.4]октан-6,8-диона;
6-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-4,6-диазаспиро[2.4]гептан-5,7-диона;
(5S)-5-этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-диона;
или его соль и/или сольват и/или его производное.
Пункт 15 - Соединение согласно пункту 1, представляющее собой:
5,5-диметил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-дион.
Пункт 16 - Соединение согласно пункту 1, представляющее собой:
3-[5-[(3,3-диметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-5,5-диметил-имидазолидин-2,4-дион.
Пункт 17 - Соединение согласно пункту 1, представляющее собой:
(5R)-5-этил-5-метил-3-(5-спиро[2Н-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-дион.
Пункт 18 - Соединение согласно пункту 1, представляющее собой: 5,5-диметил-3-(5-спиро[2Н-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-дион.
Пункт 19 - Соединение согласно пункту 1, представляющее собой:
(5R)-5-этил-5-метил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-дион.
Пункт 20 - Соединение согласно пункту 1, представляющее собой:
(5R)-3-[5-[(3,3-диметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-5-метил-имидазолидин-2,4-дион.
Пункт 21 - Соединение согласно пункту 1, представляющее собой: 5,5-диметил-3-[5-[(3,3,7-триметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-имидазолидин-2,4-дион.
Пункт 22 - Соединение согласно пункту 1, представляющее собой:
(5R)-5-этил-5-метил-3-[5-[(3,3,7-триметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-дион.
Пункт 23 - Соединение согласно пункту 1, представляющее собой:
(5R)-5-этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-дион.
Пункт 24 - Соединение согласно пункту 1, представляющее собой:
(5R)-5-этил-3-(5-спиро[2Н-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-дион.
Пункт 25 - Соединение согласно пункту 1, представляющее собой:
(5R)-3-[5-[(3,3-диметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-имидазолидин-2,4-дион.
Пункт 26 - Соединение согласно пункту 1, представляющее собой:
(5R)-5-этил-3-[5-[(3,3,7-триметил-2Н-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-дион.
Пункт 27 - Соединение согласно пункту 1, представляющее собой:
7-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-5,7-диазаспиро[3.4]октан-6,8-дион.
Пункт 28 - Соединение согласно пункту 1, представляющее собой:
6-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-4,6-диазаспиро[2.4]гептан-5,7-дион.
Пункт 29 - Соединение согласно пункту 1, представляющее собой:
(5S)-5-этил-3-[5-(7-метилспиро[2Н-бензофуран-3,1'-циклопропан]-4-ил)-оксипиразин-2-ил]имидазолидин-2,4-дион.
Пункт 30 - Соединение формулы (I) согласно любому из пунктов 1-29 или его фармацевтически приемлемые соль и/или сольват.
Пункт 31 - Соединение согласно любому из пунктов 1-30 для использования в качестве лекарственного средства.
Пункт 32 - Соединение согласно пункту 31 для использования в профилактике или лечении заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона.
Пункт 33 - Соединение согласно пункту 31 для использования в профилактике или лечении шизофрении.
Пункт 34 - Соединение согласно пункту 31 для использования в профилактике или лечении нарушений слуха.
Пункт 35 - Соединение согласно пункту 31 для использования в профилактике или лечении боли.
Пункт 36 - Соединение согласно пункту 31 для использования в лечении синдрома ломкой Х-хромосомы.
Пункт 37 - Способ профилактики или лечения заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения согласно любому из пунктов 1-30.
Пункт 38 - Способ профилактики или лечения шизофрении, включающий введение субъекту, нуждающемуся в этом, соединения согласно любому из пунктов 1-30.
Пункт 39 - Способ профилактики или лечения нарушений слуха, включающий введение субъекту, нуждающемуся в этом, соединения согласно любому из пунктов 1-30.
Пункт 40 - Способ профилактики или лечения боли, включающий введение субъекту, нуждающемуся в этом, соединения согласно любому из пунктов 1-30.
Пункт 41 - Способ лечения синдрома ломкой Х-хромосомы, включающий введение субъекту, нуждающемуся в этом, соединения согласно любому из пунктов 1-30.
Пункт 42 - Применение соединения согласно любому из пунктов 1-30 в изготовлении лекарственного средства для профилактики или лечения заболевания или расстройства, выбранного из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, такой как невропатическая боль, воспалительная боль и смешанная боль, деменции с тельцами Леви и болезни Паркинсона.
Пункт 43 - Применение соединения согласно любому из пунктов 1-30 в изготовлении лекарственного средства для профилактики или лечения шизофрении.
Пункт 44 - Применение соединения согласно любому из пунктов 1-30 в изготовлении лекарственного средства для профилактики или лечения нарушений слуха.
Пункт 45 - Применение соединения согласно любому из пунктов 1-30 в изготовлении лекарственного средства для профилактики или лечения боли.
Пункт 46 - Применение соединения согласно любому из пунктов 1-30 в изготовлении лекарственного средства для лечения синдрома ломкой Х-хромосомы.
Пункт 47 - Фармацевтическая композиция, содержащая соединение согласно любому из пунктов 1-30 и фармацевтически приемлемый носитель или эксципиент.
Пункт 48 - Соединение согласно любому из пунктов 1-30 для использования в комбинации с дополнительным фармацевтически приемлемым активным ингредиентом.
Пункт 49 - Соединение формулы (II) или (XVI):
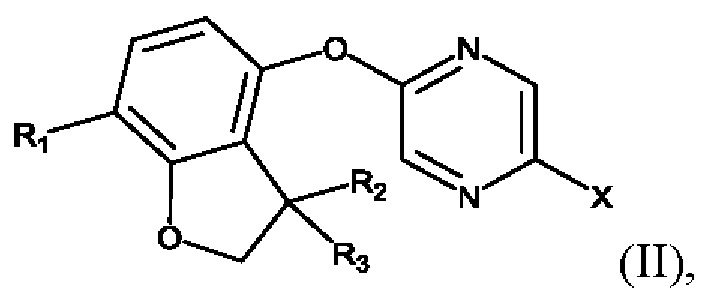
где R1, R2 и R3 являются такими, как определено в пункте 1, X представляет собой галоген, такой как Br.
Пункт 50 - Соединение формулы (XVI):
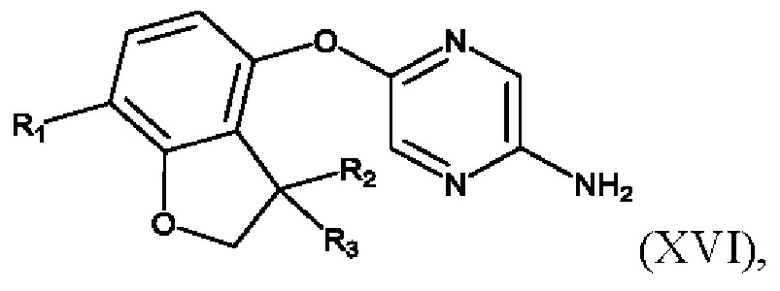
где R1, R2 и R3 являются такими, как определено в пункте 1.
Пункт 51 - Соединение формулы (IV):
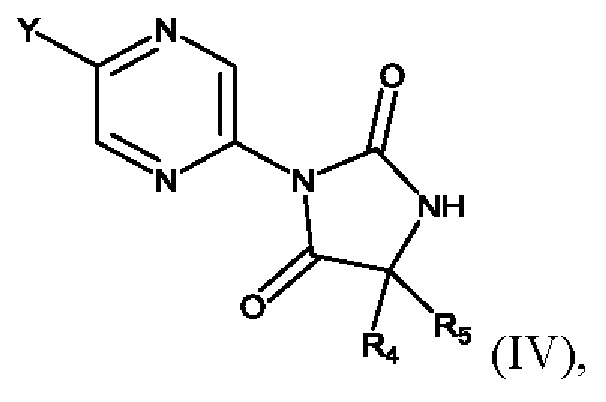
где R4 и R5 являются такими, как определено в пункте 1, Y представляет собой галоген, такой как Cl.
Пункт 52 - Производное соединения формулы (I) или его соль и/или сольват согласно любому из пунктов 1-30, функционализированное через вторичный атом азота гидантоина или через вторичный атом азота триазолона группой L, выбранной из групп, состоящих из:
а) РО(ОН)O-⋅М+, где М+ представляет собой фармацевтически приемлемый моновалентный противоион,
б) -РО(O-)2⋅2М+,
в) -РО(O-)2⋅D2+, где D2+ представляет собой фармацевтически приемлемый дивалентный противоион,
г) -CH(RX)-PO(OH)O-⋅M+, где RX представляет собой водород или С1-3алкил,
д) -CH(RX)-PO(O-)2⋅2М+,
е) -CH(RX)-PO(O-)2⋅D2+,
ж) -SO3-⋅M+,
з) -CH(RX)-SO3-⋅M+, и
и) -CO-CH2CH2-CO2⋅M+.
Пункт 53 - Соединение согласно любому из пунктов 1-36, которое находится в природной изотопной форме.
Ссылки
Все публикации, включая, без ограничения, патенты и заявки на патенты, процитированные в этом описании, включены в данное описание путем ссылки, как если бы каждая отдельная публикация была специально и индивидуально указана для включения в настоящий документ посредством ссылки, как если бы они были полностью изложены.
Anderson LA et al. Increased spontaneous firing rates in auditory midbrain following noise exposure are specifically abolished by a Kv3 channel modulator. Hear Res. 2018 Aug; 365:77-89
Aroniadou-Anderjaska V et al. Mechanisms regulating GABAergic inhibitory transmission in the basolateral amygdala: implications for epilepsy and anxiety disorders. Amino Acids 2007 Aug; 32:305-315.
Baranauskas G, Nistri A. Sensitization of pain pathways in the spinal cord: cellular mechanisms. Prog. Neurobiol. 1998 Feb; 54(3):349-65.
Baron R et al. Peripheral input and its importance for central sensitization. Ann. Neurol. 2013 Nov; 74(5):630-6.
Ben-Ari Y. Seizure Beget Seizure: The Quest for GABA as a Key Player. Crit. Rev. Neurobiol. 2006; 18(1-2):135-144.
Benes FM et al. Circuitry-based gene expression profiles in GABA cells of the trisynaptic pathway in schizophrenics versus bipolars. PNAS 2008 Dec; 105(52):20935-20940.
Bennett DL, Woods CG. Painful and painless channelopathies. Lancet Neurol. 2014 Jun; 13(6):587-99.
Berge S et al. Pharmaceutical Salts. J. Pharm. Sci. 1977; 66; 1-19.
Brambilla P et al. GABAergic dysfunction in mood disorders. Mol. Psych. 2003 Apr; 8:721-737.
Brooke RE et al. Spinal cord interneurones labelled transneuronally from the adrenal gland by a GFP-herpes virus construct contain the potassium channel subunit Kv3. 1b. Auton. Neurosci. 2002 Jun; 98(1-2):45-50.
Brooke RE et al. Association of potassium channel Kv3.4 subunits with pre- and postsynaptic structures in brainstem and spinal cord. Neuroscience 2004; 126(4): 1001-10.
Brooke RE et al. Immunohistochemical localisation of the voltage gated potassium ion channel subunit Kv3.3 in the rat medulla oblongata and thoracic spinal cord. Brain Res. 2006 Jan; 1070(1):101-15.
Cervero F. Spinal cord hyperexcitability and its role in pain and hyperalgesia. Exp. Brain Res. 2009 Jun; 196(1):129-37.
Chambers AR et al. Pharmacological modulation of Kv3.1 mitigates auditory midbrain temporal processing deficits following auditory nerve damage. Sci Rep. 2017 Dec 13; 7(1):17496.
Chang SY et al. Distribution of Kv3.3 Potassium Channel Subunits in Distinct Neuronal Populations of Mouse Brain. J. Comp. Neuro. 2007 Feb; 502:953-972.
Chien LY et al. Reduced expression of A-type potassium channels in primary sensory neurons induces mechanical hypersensitivity. J. Neurosci. 2007 Sep; 27(37):9855-65.
Chow A et al. K+ Channel Expression Distinguishes Subpopulations of Parvalbumin-and Somatostatin-Containing Neocortical Intemeurons. J. Neurosci. 1999 Nov; 19(21):9332-9345.
Desai R et al. Protein Kinase С Modulates Inactivation of Kv3.3 Channels. J. Biol. Chem. 2008; 283; 22283-22294.
Deuchars SA et al. Properties of interneurones in the intermediolateral cell column of the rat spinal cord: role of the potassium channel subunit Kv3.1. Neuroscience 2001; 106(2):433-46.
Devulder J. Flupirtine in pain management: pharmacological properties and clinical use. CNSDrugs 2010 Oct; 24(10):867-81.
Dib-Hajj SD et al. The Na(V)1.7 sodium channel: from molecule to man. Nat. Rev. Neurosci. 2013 Jan; 14(1):49-62.
Diochot S et al. Sea Anemone Peptides with a Specific Blocking Activity against the Fast Inactivating Potassium Channel Kv3.4. J. Biol. Chem. 1998 Mar; 273(12); 6744-6749.
Engel AK et al. Dynamic Predictions: Oscillations and Synchrony in Top-Down Processing. Nat. Rev. Neurosci. 2001 Oct; 2(10):704-716.
Espinosa F et al. Alcohol Hypersensitivity, Increased Locomotion, and Spontaneous Myoclonus in Mice Lacking the Potassium Channels Kv3.1 and Kv3.3. J. Neurosci. 2001 Sep; 21(17):6657-6665.
Espinosa F et al. Ablation of Kv3.1 and Kv3.3 Potassium Channels Disrupts Thalamocortical Oscillations In Vitro and In Vivo. J. Neurosci. 2008 May; 28(21):5570-5581.
Figueroa K et al. KCNC3: phenotype, mutations, channel biophysics - a study of 260 familial ataxia patients. Human Mutation. 2010; 31; 191-196.
Finnerup NB et al. Pharmacotherapy for neuropathic pain in adults: a systematic review and meta-analysis. Lancet Neurol. 2015 Feb; 14(2): 162-73.
Fisahn A. Kainate receptors and rhythmic activity in neuronal networks: hippocampal gamma oscillations as a tool. J. Physiol. 2005 Oct; 561(1):65-72.
Glait L et al. Effects of AUT00063, a Kv3.1 channel modulator, on noise-induced hyperactivity in the dorsal cochlear nucleus. Hear Res. 2018 Apr; 361:36-44
Greene TW, Wuts, PG. Greene's Protective Groups in Organic Synthesis, 2006, 4th Edition, John Wiley & Sons, Inc., Hoboken, NJ, USA.
Joho RH et al. Increased γ- and Decreased δ-Oscillations in a Mouse Deficient for a Potassium Channel Expressed in Fast-Spiking hiterneurons. J. Neurophysiol. 1999 Jun; 82:1855-1864.
Joho RH, Hurlock EC. The Role of Kv3-type Potassium Channels in Cerebellar Physiology and Behavior. Cerebellum 2009 Feb; 8:323-333.
Jung D et al. Age-related changes in the distribution of Kv1.1 and Kv3.1 in rat cochlear nuclei. Neurol. Res. 2005; 27; 436-440.
Kasten MR et al. Differential regulation of action potential firing in adult murine thalamocortical neurons by Kv3.2, Kv1, and SK potassium and N-type calcium channels. J. Physiol. 2007; 584(2):565-582.
Kaczmarek L et al. Regulation of the timing of MNTB neurons by short-term and long-term modulation of potassium channels. Hearing Res. 2005; 206; 133-145.
Lau D et al. Impaired Fast-Spiking, Suppressed Cortical Inhibition, and Increased Susceptibility to Seizures in Mice Lacking Kv3.2 K+ Channel Proteins. J. Neurosci. 2000 Dec; 20(24):9071-9085.
Li W et al. Localization of Two High-Threshol Potassium Channel Subunits in the Rat Central Auditory System. J. Comp. Neuro. 2001 May; 437:196-218.
Lu R et al. Slack channels expressed in sensory neurons control neuropathic pain in mice. J. Neurosci. 2015 Jan; 35(3):1125-35.
Markram H et al. hiterneurons of the neocortical inhibitory system. Nat. Rev. Neurosci. 2004 Oct; 5:793-807.
Martina M et al. Functional and Molecular Differences between Voltage-Gated K+ Channels of Fast-Spiking Interneurons and Pyramidal Neurons of Rat Hippocampus. J. Neurosci. 1998 Oct; 18(20):8111-8125.
McCarberg BH et al. The impact of pain on quality of life and the unmet needs of pain management: results from pain sufferers and physicians participating in an Internet survey. Am. J. Ther. 2008 Jul-Aug; 15(4):312-20.
McDonald AJ, Mascagni F. Differential expression of Kv3.1b and Kv3.2 potassium channel subunits in interneurons of the basolateral amygdala. Neuroscience 2006; 138:537-547.
McMahon A et al. Allele-dependent changes of olivocerebellar circuit properties in the absence of the voltage-gated potassium channels Kv3.1 and Kv3.3. Eur. J. Neurosci. 2004 Mar; 19:3317-3327.
Mitchell 1 et al. Aryl Pyrazoles as Potent Inhibitors of Arginine Methyltransferases: Identification of the First PRMT6 Tool Compound. ACS Med. Chem. Lett. 2015; 6(6); 655-659.
Muona M, et al. A recurrent de novo mutation in KCNC1 causes progressive myoclonus epilepsy. Nat Genet. 2015 Jan; 47(1):39-46.
Muqeem T et al. Regulation of Nociceptive Glutamatergic Signaling by Presynaptic Kv3.4 Channels in the Rat Spinal Dorsal Ham J Neurosci. 2018 Apr 11; 38(15):3729-3740.
Olsen T et al. Kv3 K+ currents contribute to spike-timing in dorsal cochlear nucleus principal cells. Neuropharmacology 2018 May 1; 133:319-333
Pilati N et al.. Acoustic over-exposure triggers burst firing in dorsal cochlear nucleus fusiform cells. Hearing Research 2012; 283;98-106.
Puente N et al. Precise localization of the voltage-gated potassium channel subunits Kv3.1b and Kv3.3 revealed in the molecular layer of the rat cerebellar cortex by a pre-embedding immunogold method. Histochem. Cell. Biol. 2010 Sep; 134:403-409.
Reynolds GP et al. Calcium Binding Protein Markers of GABA Deficits in Schizophrenia - Post Mortem Studies and Animal Models. Neurotox. Res. 2004 Feb; 6(1):57-62.
Ritter DM et al. Modulation of Kv3.4 channel N-type inactivation by protein kinase С shapes the action potential in dorsal root ganglion neurons. J. Physiol. 2012 Jan; 590(Pt 1):145-61.
Ritter DM et al. Dysregulation of Kv3.4 channels in dorsal root ganglia following spinal cord injury. J. Neurosci. 2015 Jan; 35(3): 1260-73.
Roberts L et al. Ringing Ears: The Neuroscience of Tinnitus. J. Neurosci. 2010:30(45); 14972-14979.
Rudy B, McBain CJ. Kv3 channels: voltage-gated K+ channels designed for high-frequency repetitive firing. TRENDS in Neurosci. 2001 Sep; 24(9):517-526.
Sacco T et al. Properties and expression of Kv3 channels in cerebellar Purkinje cells. Mol. Cell. Neurosci. 2006 Jul; 33:170-179.
Schulz P, Steimer T. Neurobiology of Circadian Systems. CNS Drugs 2009; 23 (Suppl. 2):3-13.
Song P et al. Acoustic environment determines phosphorylation state of the Kv3.1 potassium channel in auditory neurons Nat. Neurosci. 2005 Oct; 8(10): 1335-1342.
Spencer KM et al. Neural synchrony indexes disordered perception and cognition in schizophrenia. PNAS 2004 Dec; 101(49):17288-17293.
Sun S et al. Inhibitors of voltage-gated sodium channel Nav1.7: patent applications since 2010. Pharm. Pat. Anal. 2014 Sep; 3(5):509-21.
U.S. Department of Health and Human Services, Food and Drug Administration. Draft Guidance for Industry Analgesic Indications: Developing Drug and Biological Products: http://www.fda.gov/downloads/dmgs/guidancecomplianceregulatoryinformation/guidances/ucm384691.pdf 2014 Feb.
von Helm С et al. Loss of Kv3.1 Tonotopicity and Alterations in cAMP Response Element-Binding Protein Signaling in Central Auditory Neurons of Hearing Impaired Mice. J. Neurosci. 2004; 24:1936-1940.
Weiser M et al. Differential Expression of Shaw-related K+ Channels in the Rat Central Nervous System. J. Neurosci. 1994 Mar; 14(3):949-972.
Wickenden AD, McNaughton-Smith G. Kv7 channels as targets for the treatment of pain. Curr. Pharm. Des. 2009; 15(15): 1773-98.
Woolf CJ. What is this thing called pain? J. Clin. Invest. 2010 Nov; 120(11):3742-4.
Woolf CJ. Central sensitization: implications for the diagnosis and treatment of pain. Pain 2011 Mar; 152 (3 Suppl): S2-15.
Yanagi M et al. Kv3.1-containing K(+) channels are reduced in untreated schizophrenia and normalized with antipsychotic drugs. Mol Psychiatry. 2014. 19(5):573-9.
Yeung SYM et al. Modulation of Kv3 Subfamily Potassium Currents by the Sea Anemone Toxin BDS: Significance for CNS and Biophysical Studies. J. Neurosci. 2005 Mar; 25(38):8735-8745.
Zamponi GW et al. The Physiology, Pathology, and Pharmacology of Voltage-Gated Calcium Channels and Their Future Therapeutic Potential Pharmacol Rev. 2015 Oct; 67(4):821-70.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ СПИРО[ИМИДАЗОЛИДИН-4,3'-ИНДОЛ]-2,2',5(1'Н)-ТРИОНЫ ДЛЯ ЛЕЧЕНИЯ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С ВАНИЛЛОИДНЫМ РЕЦЕПТОРОМ 1 | 2007 |
|
RU2421457C2 |
| НОВЫЕ ГИДАНТОИНОВЫЕ ПРОИЗВОДНЫЕ ДЛЯ ЛЕЧЕНИЯ ОБСТРУКТИВНЫХ ЗАБОЛЕВАНИЙ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2005 |
|
RU2386629C2 |
| Макрогетероциклические нуклеозидные производные и их аналоги, получение и применение | 2017 |
|
RU2731385C1 |
| ПРОИЗВОДНЫЕ ОКСАДИАЗОЛА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПОТЕНЦИРУЮЩИХ СРЕДСТВ МЕТАБОТРОПНЫХ ГЛУТАМАТНЫХ РЕЦЕПТОРОВ-842 | 2008 |
|
RU2470931C2 |
| СОЕДИНЕНИЕ ГРИЗЕОФУЛЬВИНА И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2774618C2 |
| 5-[(ПИПЕРАЗИН-1-ИЛ)-3-ОКСО-ПРОПИЛ]-ИМИДАЗОЛИДИН-2,4-ДИОНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ADAMTS ДЛЯ ЛЕЧЕНИЯ ОСТЕОАРТРИТА | 2015 |
|
RU2693459C2 |
| ИНГИБИТОРЫ МЕТАЛЛОПРОТЕИНАЗ, ИХ ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 2002 |
|
RU2288228C2 |
| ПРОИЗВОДНЫЕ ЭТИНИЛА КАК МОДУЛЯТОРЫ МЕТАБОТРОПНОГО РЕЦЕПТОРА ГЛУТАМАТА | 2016 |
|
RU2721776C2 |
| ПИРИДОПИРИМИДИНОНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРА N-МЕТИЛ-D-АСПАРТАТА | 2016 |
|
RU2717665C2 |
| ИНГИБИТОРЫ МЕТАЛЛОПРОТЕИНАЗ, ИХ ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 2002 |
|
RU2293730C2 |
Настоящее изобретение относится к новым соединениям, фармацевтическим композициям, содержащим их, и их применению в терапии, в частности в профилактике или лечении нарушений слуха, а также шизофрении, злоупотребления психоактивными веществами, боли и синдрома ломкой Х-хромосомы. Предложено соединение формулы (I) или его соль, где R1 представляет собой H или метил; R2 и R3 оба представляют собой метил, или R2 и R3, вместе с атомом углерода, к которому они присоединены, образуют спироциклопропильное кольцо; R4 представляет собой метил или этил; R5 представляет собой H или метил; или R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют C3-C4спирокарбоциклил. Изобретение также относится к применению указанного соединения, его промежуточным соединениям, а также фармацевтической композиции и способу лечения на его основе. Технический результат заключается в получении альтернативных соединений для лечения расстройств, при которых требуется модулятор Kv3.1, и/или Kv3.2, и/или Kv3.3. 8 н. и 35 з.п. ф-лы, 15 пр.

1. Соединение формулы (I):
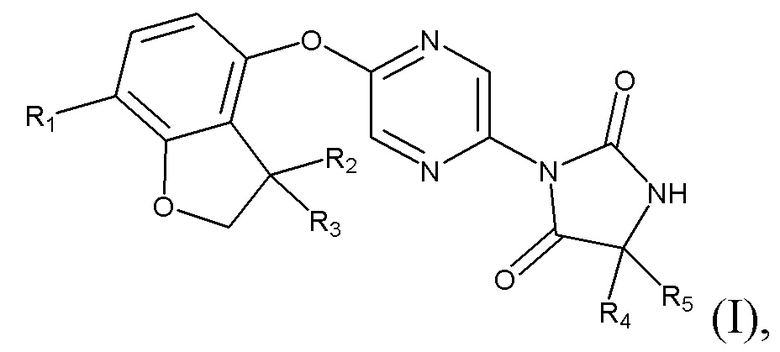
где:
R1 представляет собой H или метил;
R2 и R3 оба представляют собой метил, или R2 и R3, вместе с атомом углерода, к которому они присоединены, образуют спироциклопропильное кольцо;
R4 представляет собой метил или этил;
R5 представляет собой H или метил;
или R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют C3-C4спирокарбоциклил;
или его соль.
2. Соединение или его соль по п. 1, представляющие собой соединение формулы (I) или его фармацевтически приемлемую соль.
3. Соединение или его соль по п. 1, представляющие собой фармацевтически приемлемую соль соединения формулы (I).
4. Соединение или его соль по п. 1, представляющие собой соединение формулы (I).
5. Соединение или его соль по любому из пп. 1-4, где R1 представляет собой H.
6. Соединение или его соль по любому из пп. 1-4, где R1 представляет собой метил.
7. Соединение или его соль по любому из пп. 1-6, где R2 и R3 представляют собой спироциклопропил.
8. Соединение или его соль по любому из пп. 1-6, где R2 представляет собой метил и R3 представляет собой метил.
9. Соединение или его соль по любому из пп. 1-8, где R4 представляет собой метил.
10. Соединение или его соль по любому из пп. 1-8, где R4 представляет собой этил.
11. Соединение или его соль по любому из пп. 1-10, где R5 представляет собой H.
12. Соединение или его соль по любому из пп. 1-10, где R5 представляет собой метил.
13. Соединение или его соль по любому из пп. 1-8, где R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют спироциклопропил.
14. Соединение или его соль по любому из пп. 1-8, где R4 и R5, вместе с атомом углерода, к которому они присоединены, образуют спироциклобутил.
15. Соединение или его соль по любому из пп. 1-14, выбранные из группы, состоящей из:
5,5-диметил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
3-[5-[(3,3-диметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]-5,5-диметил-имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
5,5-диметил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
(5R)-3-[5-[(3,3-диметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-5-метил-имидазолидин-2,4-диона;
5,5-диметил-3-[5-[(3,3,7-триметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-[5-[(3,3,7-триметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
(5R)-3-[5-[(3,3-диметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-имидазолидин-2,4-диона;
(5R)-5-этил-3-[5-[(3,3,7-триметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
7-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-5,7-диазаспиро[3.4]октан-6,8-диона;
6-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-4,6-диазаспиро[2.4]гептан-5,7-диона;
(5S)-5-этил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона
или их фармацевтически приемлемой соли.
16. Соединение или его соль по любому из пп. 1-15, выбранные из группы, состоящей из:
5,5-диметил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
3-[5-[(3,3-диметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]-5,5-диметил-имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
5,5-диметил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
(5R)-3-[5-[(3,3-диметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-5-метил-имидазолидин-2,4-диона;
5,5-диметил-3-[5-[(3,3,7-триметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-5-метил-3-[5-[(3,3,7-триметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона;
(5R)-5-этил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-диона;
(5R)-3-[5-[(3,3-диметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-имидазолидин-2,4-диона;
(5R)-5-этил-3-[5-[(3,3,7-триметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-диона;
7-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-5,7-диазаспиро[3.4]октан-6,8-диона;
6-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-4,6-диазаспиро[2.4]гептан-5,7-диона;
(5S)-5-этил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-диона
или их фармацевтически приемлемой соли.
17. Соединение или его соль по п. 1, представляющие собой 5,5-диметил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-дион:
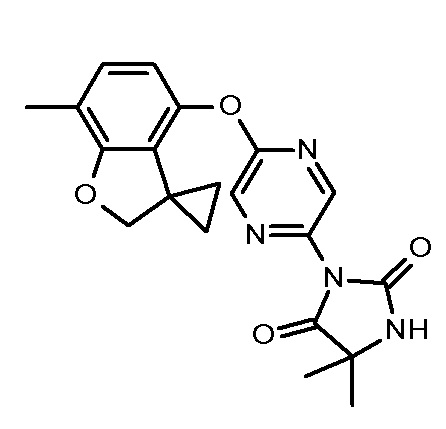
или его фармацевтически приемлемую соль.
18. Соединение или его соль по п. 17, представляющие собой соединение:
5,5-диметил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-дион:
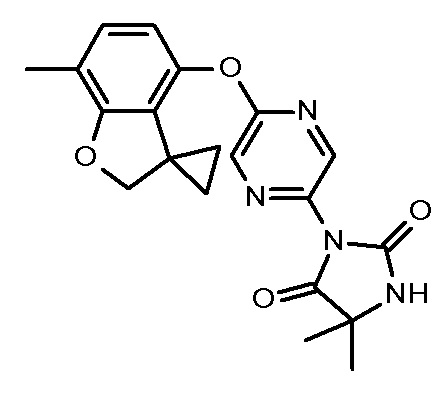
19. Соединение или его соль по п. 4, представляющее собой соединение:
3-[5-[(3,3-диметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]-5,5-диметил-имидазолидин-2,4-дион:
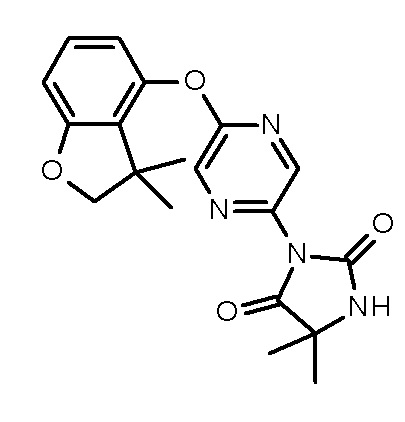
20. Соединение или его соль по п. 4, представляющее собой соединение:
(5R)-5-этил-5-метил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-дион:
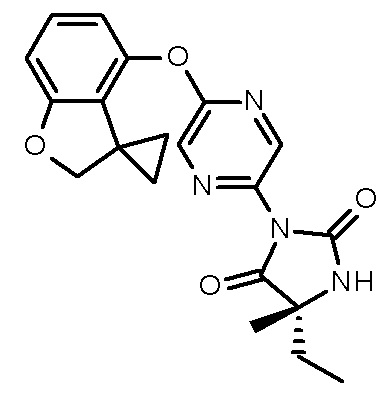
21. Соединение или его соль по п. 4, представляющее собой соединение:
5,5-диметил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-дион:
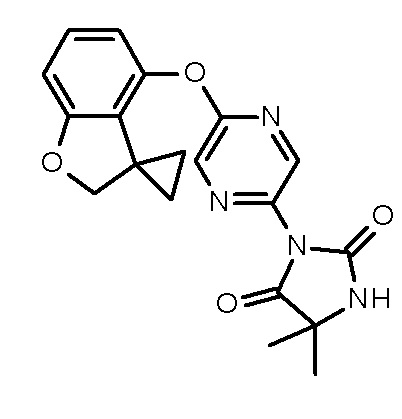
22. Соединение или его соль по п. 4, представляющее собой соединение:
(5R)-5-этил-5-метил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-дион:
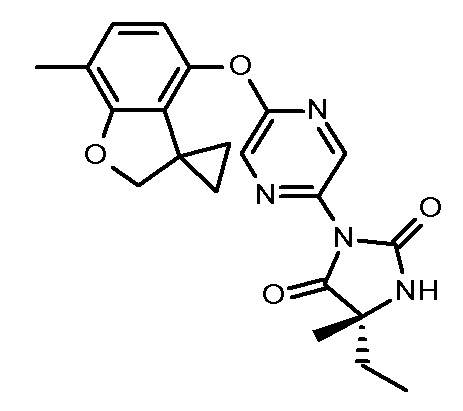
23. Соединение или его соль по п. 4, представляющее собой соединение:
(5R)-3-[5-[(3,3-диметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-5-метил-имидазолидин-2,4-дион:
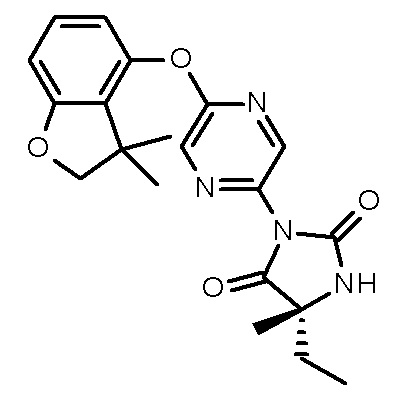
24. Соединение или его соль по п. 4, представляющее собой соединение:
5,5-диметил-3-[5-[(3,3,7-триметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-дион:
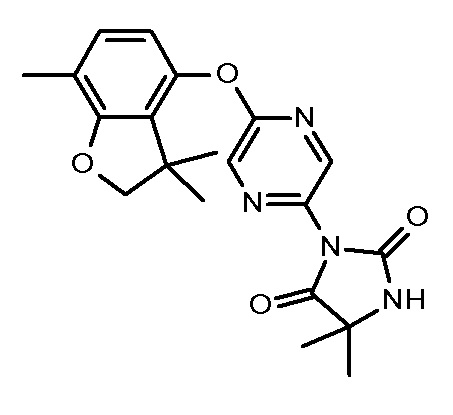
25. Соединение или его соль по п. 4, представляющее собой соединение:
(5R)-5-этил-5-метил-3-[5-[(3,3,7-триметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-дион:

26. Соединение или его соль по п. 1, представляющие собой (5R)-5-этил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-дион:
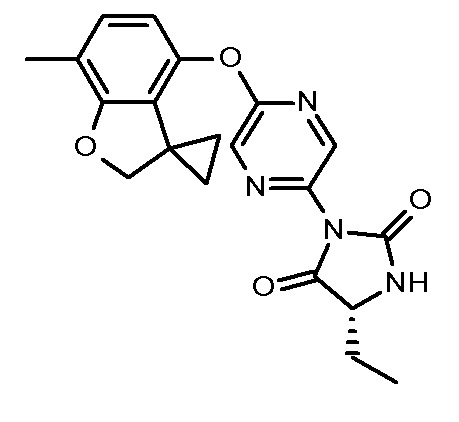
или его фармацевтически приемлемую соль.
27. Соединение или его соль по п. 26, представляющие собой соединение:
(5R)-5-этил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-дион:
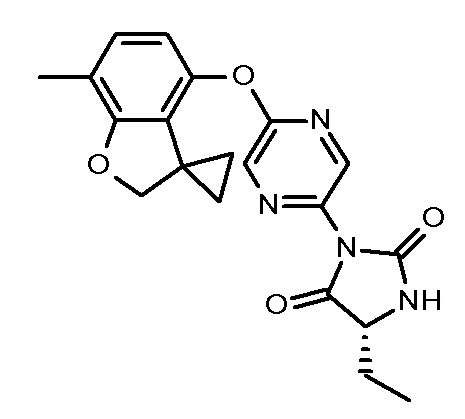
28. Соединение или его соль по п. 1, представляющие собой (5R)-5-этил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-дион:
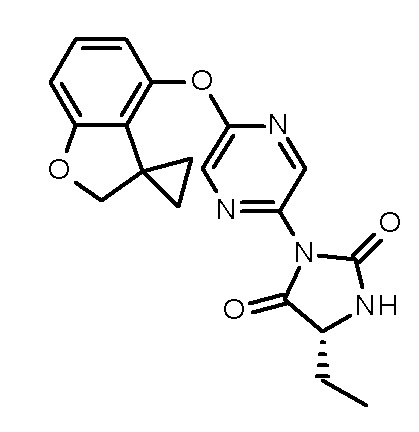
или его фармацевтически приемлемую соль.
29. Соединение или его соль по п. 28, представляющие собой соединение:
(5R)-5-этил-3-(5-спиро[2H-бензофуран-3,1'-циклопропан]-4-илоксипиразин-2-ил)имидазолидин-2,4-дион:
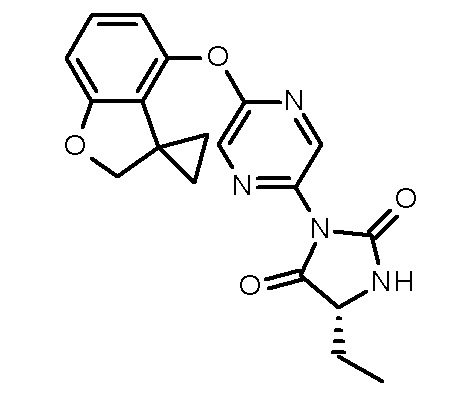
30. Соединение или его соль по п. 4, представляющее собой соединение:
(5R)-3-[5-[(3,3-диметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]-5-этил-имидазолидин-2,4-дион:
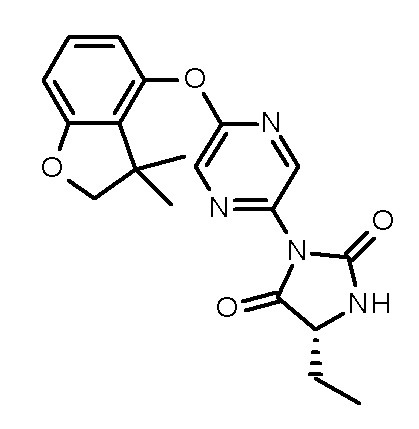
31. Соединение или его соль по п. 4, представляющее собой соединение:
(5R)-5-этил-3-[5-[(3,3,7-триметил-2H-бензофуран-4-ил)окси]пиразин-2-ил]имидазолидин-2,4-дион:
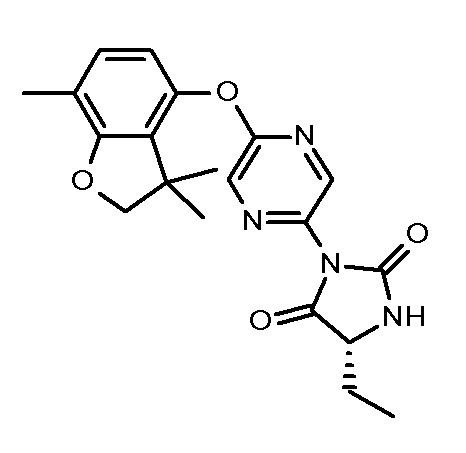
32. Соединение или его соль по п. 4, представляющее собой соединение:
7-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-5,7-диазаспиро[3.4]октан-6,8-дион:
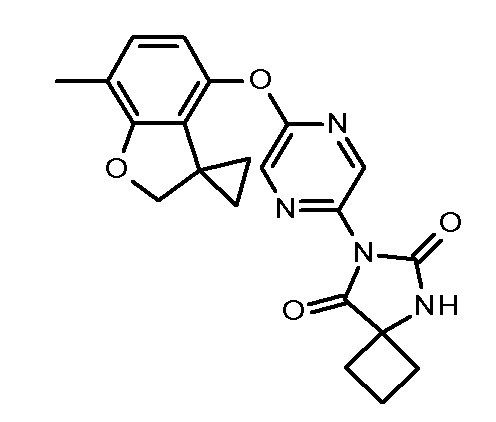
33. Соединение или его соль по п. 4, представляющее собой соединение:
6-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]-4,6-диазаспиро[2.4]гептан-5,7-дион:
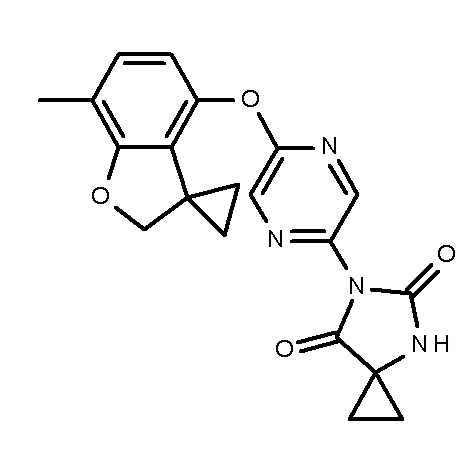
34. Соединение или его соль по п. 4, представляющее собой соединение:
(5S)-5-этил-3-[5-(7-метилспиро[2H-бензофуран-3,1'-циклопропан]-4-ил)оксипиразин-2-ил]имидазолидин-2,4-дион:
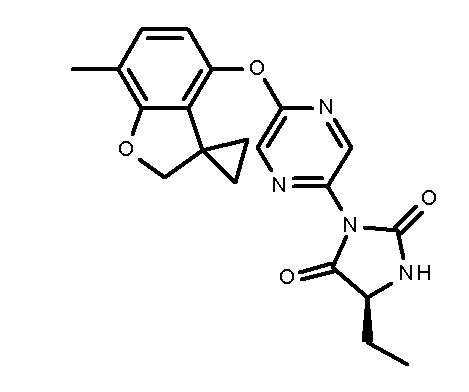
35. Применение соединения или его фармацевтически приемлемой соли по любому из пп. 2-34 в изготовлении лекарственного средства для профилактики или лечения заболевания или расстройства, при котором требуется модулятор Kv3.1, и/или Kv3.2, и/или Kv3.3, которое выбрано из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, деменции с тельцами Леви и болезни Паркинсона.
36. Применение соединения или его фармацевтически приемлемой соли по любому из пп. 2-34 в изготовлении лекарственного средства для профилактики или лечения заболевания или расстройства, при котором требуется модулятор Kv3.1, и/или Kv3.2, и/или Kv3.3, которое выбрано из группы, состоящей из шизофрении, нарушений слуха, боли и синдрома ломкой Х-хромосомы.
37. Способ профилактики или лечения заболевания или расстройства, при котором требуется модулятор Kv3.1, и/или Kv3.2, и/или Kv3.3, которое выбрано из группы, состоящей из нарушений слуха, шизофрении, депрессии и расстройств настроения, биполярного расстройства, злоупотребления психоактивными веществами, тревожных расстройств, расстройств сна, гиперакузии и нарушений слухового восприятия, болезни Меньера, нарушений равновесия и заболеваний внутреннего уха, расстройств контроля над импульсами, расстройств личности, синдрома дефицита внимания с гиперактивностью, расстройств аутистического спектра, расстройств пищевого поведения, нарушения познавательной способности, атаксии, боли, деменции с тельцами Леви и болезни Паркинсона, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп. 2-34.
38. Способ профилактики или лечения заболевания или расстройства, при котором требуется модулятор Kv3.1, и/или Kv3.2, и/или Kv3.3, которое выбрано из группы, состоящей из шизофрении, нарушений слуха, боли и синдрома ломкой Х-хромосомы, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп. 2-34.
39. Применение по п. 35 или 36 или способ по п. 37 или 38, где соединение вводят перорально.
40. Применение по п. 35 или 36 или способ по п. 37 или 38, где соединение вводят в количестве от 0,05 мг до 1000 мг на дозу; например, в количестве от 1,0 мг до 500 мг на дозу.
41. Фармацевтическая композиция, обладающая активностью модулятора Kv3.1, и/или Kv3.2, и/или Kv3.3 и содержащая от 0,05 мг до 1000 мг соединения или его фармацевтически приемлемой соли по любому из пп. 2-34 и фармацевтически приемлемый носитель или эксципиент.
42. Соединение формулы (II) или (XVI):
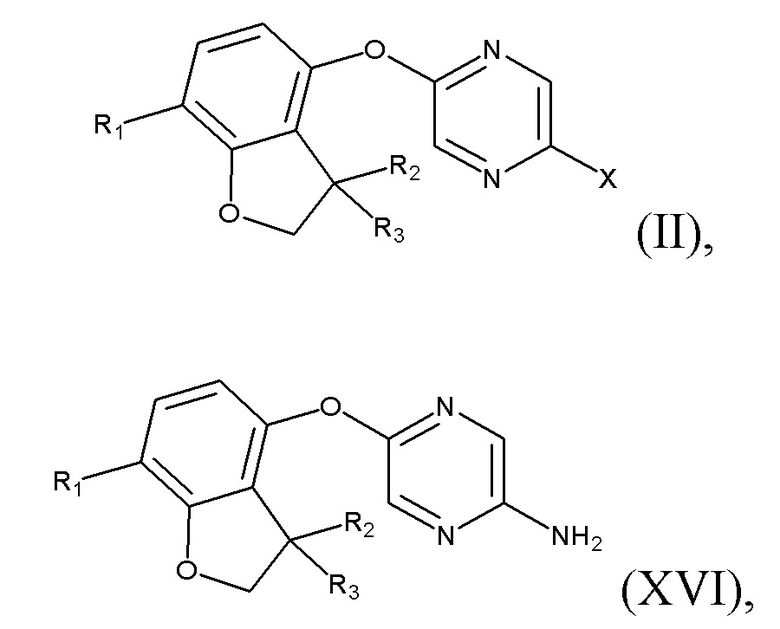
где R1, R2 и R3 являются такими, как определено в п. 1, X представляет собой галоген.
43. Соединение формулы (IV):
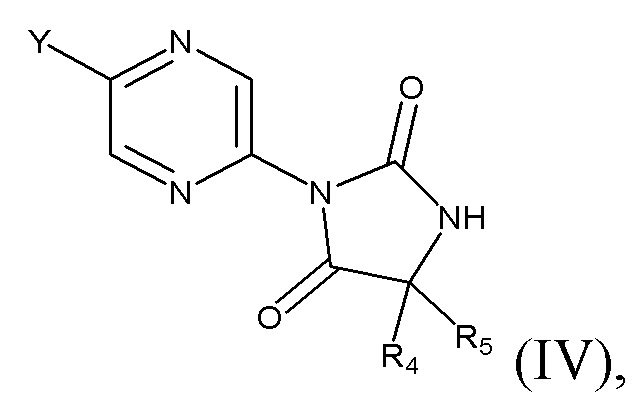
где R4 и R5 являются такими, как определено в п. 1, Y представляет собой галоген.
| WO 2012076877 A1, 14.06.2012 | |||
| WO 2013182851 A1, 12.12.2013 | |||
| WO 2017103604 A1, 22.06.2017 | |||
| WO 2018109484 A1, 21.06.2018 | |||
| Картофелемойка | 1932 |
|
SU27532A1 |
Авторы
Даты
2024-11-18—Публикация
2019-10-16—Подача