Изобретение относится к медицине, а именно к терапии критических состояний, и может быть использовано для оценки адекватности антикоагулянтной терапии.
Пациенты, требующие интенсивной терапии, зачастую нуждаются в длительной тромбопрофилактике нефракционированным гепарином (Giglia T.M., Massicotte M.P., Tweddell J.S. et al. Prevention and treatment of thrombosis in pediatric and congenital heart disease: a scientific statement from the American Heart Association. Circulation. 2013; 128 (24): 2622-2703. DOI: 10.1161/01.cir.0000436140.77832.7a). Антикоагулянтный эффект гепарина опосредован антитромбином, кофактором II гепарина и ингибитором пути тканевого фактора и преимущественно реализуется путем инактивации тромбина и фактора Ха. Однако на фоне активации воспалительных процессов, присущих критическим состояниям, изменений концентрации факторов свертывания (прежде всего, фактора VIII и фибриногена), применения многочисленных лекарственных препаратов и т. д. клинико-лабораторный эффект его использования нелинейно зависит от дозы препарата (Pesonen E., Passov A., Andersson S. et al. Glycocalyx degradation and inflammation in cardiac surgery. J. Cardiothorac. Vasc. Anesth. 2019; 33 (2): 341-5. DOI: 10.1053/j.jvca.2018.04.007; Passov A., Schramko A., Salminen U. et al. Endothelial glycocalyx during early reperfusion in patients undergoing cardiac surgery. Clinical Trial PLoS One. 2021; 16 (5): e0251747. DOI: 10.1371/journal.pone.0251747), что создает ощущение резистентности к нему. На этом фоне малое внимание уделяется кинетике гепарина и, соответственно, оценке его концентрации в плазме. Недостаточная доза гепарина, а также неэффективный лабораторный мониторинг концентрации препарата могут привести к развитию тромботических осложнений, частота развития которых в кардиохирургической практике остается достаточно высокой и составляет от 11 до 37% (Manlhiot C., Menjak I.B., Brandão L.R., Gruenwald C.E., Schwartz S.M., Sivarajan V.B. et al. Risk, clinical features, and outcomes of thrombosis associated with pediatric cardiac surgery. Circulation. 2011; 4; 124 (14): 1511-9. DOI: 10.1161/circulationaha.110.006304). Повышенная же концентрация вводимого гепарина в плазме может сопровождаться высокой частотой геморрагических событий, таким образом, точное определение концентрации гепарина в образцах крови пациента имеет большое практическое значение.
На сегодняшний день в клинической практике определение концентрации гепарина в плазме пациента возможно только косвенным способом. Ближайшим аналогом предлагаемого способа является способ определения активированного частичного тромбопластинового времени (АЧТВ). При терапевтических дозах гепарина отношение АЧТВ пациента к АЧТВ нормальной плазмы находится в пределах 1,5-2,5 (Byun J.H., Jang I.S., Kim J.W., Koh E.H. Establishing the heparin therapeutic range using aPTT and anti-Xa measurements for monitoring unfractionated heparin therapy. Blood Res. 2016; 51 (3): 171-4. DOI: 10.5045/br.2016.51.3.171).
Общими существенными признаками аналога и предлагаемого способа являются: использование венозной крови пациента, собранной в вакуумные пробирки с 3,2% цитратом натрия в соотношении 9:1, которую центрифугируют при 1600 g на протяжении 15 мин; использование 0,025 М раствора кальция хлорида для рекальцификации лишенной тромбоцитов плазмы; косвенная концентрации гепарина.
Отличительным существенным признаком предлагаемого способа от аналога является двойное центрифугирование, которое обеспечивает удаление из образца плазмы остатков клеточных элементов, тканевого дебриса, способных влиять на скорость образования фибринового сгустка. Тем самым уменьшается создаваемый ими «шум» при регистрации динамики образования фибринового сгустка, что способствует повышению точности исследования.
Использование в предлагаемом способе тканевого фактора, обеспечивающего активацию свертывания крови in vivo, вместо контактных активаторов (каолина, эллаговой кислоты), используемых в прототипе, позволяет оценивать суммарный эффект нефракционированного гепарина на свертывание крови в целом, а не на отдельные реакции каскада свертывания, что повышает чувствительность методики.
Представление результатов не в секундах, а единицах концентрации позволяет точно рассчитывать необходимую дозу нефракционированного гепарина.
Решаемой технической проблемой является повышение эффективности и безопасности гепаринотерапии за счет определения концентрации нефракционированного гепарина в плазме, основанное на параметрах пространственно-временной динамики образования фибринового сгустка.
Техническим результатом является повышение точности определения концентрации гепарина в плазме пациента за счет оценки как временных, так и пространственных характеристик образования сгустка.
В предлагаемом способе концентрацию гепарина в плазме человека определяли путем оценки изменений состояния системы гемостаза под влиянием гепарина на основании результатов анализа пространственно-временной динамики образования фибринового сгустка. Учитывали изменение начальной скорости роста фибринового сгустка в зависимости от концентрации гепарина, концентрацию гепарина рассчитывали по формуле.
Было проведено проспективное когортное исследование в условиях in vitro на образцах крови 13 здоровых доноров, для каждого из которых выполнено 7 тестов пространственно-временной динамики свертывания крови (исследован 91 образец). Данные образцы отличались содержанием в них нефракционированного гепарина, вносимого в образцы in vitro до пробоподготовки. Концентрация гепарина в образцах составляла: 0 Ед/мл; 0,04 Ед/мл; 0,08 Ед/мл; 0,12 Ед/мл; 0,17 Ед/мл; 0,20 Ед/мл; 0,25 Ед/мл.
По кривой зависимости размера сгустка от времени его образования определяли следующие параметры: время задержки роста сгустка (Tlag, мин), начальную скорость роста сгустка (Vi, мкм/мин), стационарную скорость роста сгустка (Vst, мкм/мин) и размер сгустка через 30 мин (CS, мкм). По интенсивности светорассеяния была определена плотность сгустка (D, усл. ед.).
При проведении одновариантного линейного регрессионного анализа концентрацию гепарина предсказывали Tlag (R2 = 0,121, р = 0,001, где R2 - коэффициент детерминации), Vi (R2 = 0,277, р < 0,0001), Vst (R2 = 0,246, р < 0,0001), CS (R2 = 0,197, р < 0,0001), D (R2 = 0,049, р = 0,04). В рамках многовариантной модели с пошаговым включением ковариат предсказательную ценность сохраняла только Vi (R2 = 0,277, р < 0,0001). Остальные коварианты не были включены в финальную модель, так как не повышали ее прогностическую ценность. Регрессионный анализ проводили при помощи пакета статистических программ SPSS 26.0.
Способ осуществляют следующим образом.
У пациентов, получающих нефракционированный гепарин, проводят взятие венозной крови в пробирку с 3,2% раствором цитрата натрия в соотношении 9:1. Кровь центрифугируют при 1600 g в течение 15 мин, забирают супернатант, который затем центрифугируют при 12000 g в течение 5 мин для получения лишенной тромбоцитов плазмы. Для данного образца плазмы проводят анализ пространственно-временной динамики образования фибринового сгустка. Полученную в результате лабораторного исследования начальную скорость роста фибринового сгустка (Vi, мкм/мин) используют в дальнейшем расчете концентрации гепарина в плазме пациента с использованием формулы: Y = 0,2126 - 0,0542 × ln(Vi), где Y - концентрация нефракционированного гепарина в плазме (Ед/мл); Vi - начальная скорость роста фибринового сгустка (мкм/мин), определенная в тесте пространственно-временной динамики образования фибринового сгустка; 0,2126 и 0,0542 - коэффициенты, полученные при построении модели.
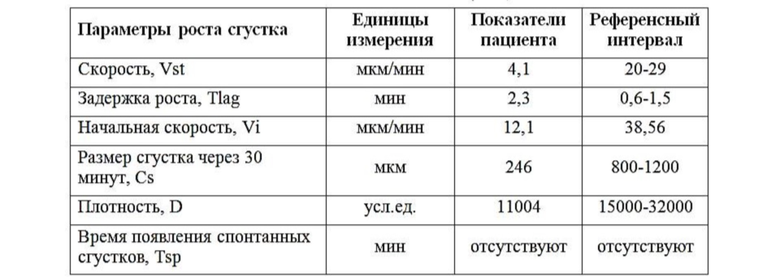
На фигуре 1 представлена зависимость концентрации гепарина (Ед/мл) от начальной скорости роста сгустка.
Концентрацию гепарина в плазме определяют по формуле:
Y = 0,2126 - 0,0542 × ln(Vi),
где Y - концентрация нефракционированного гепарина в плазме (Ед/мл); Vi - начальная скорость роста фибринового сгустка (мкм/мин), определенная в тесте пространственно-временной динамики образования фибринового сгустка; 0,2126 и 0,0542 - коэффициенты, полученные при построении модели.
Пример 1
Пациент Б. получал нефракционированный гепарин путем непрерывной внутривенной капельной инфузии со скоростью 25 Ед/кг/ч. При нормальной активности эндогенного антитромбина (76%) результаты клоттинговых тестов не отражали ожидаемой эффективности терапии (АЧТВ 34 с). Результаты пространственно-временной динамики роста фибринового сгустка при этом отражают гиперкоагуляционный профиль и высокую начальную скорость роста фибринового сгустка вблизи активатора - 60,5 мкм/мин. В результате предложенного нами способа после расчета по формуле Y = 0,2126 - 0,0542 × ln60 = 0,009 концентрация гепарина в плазме пациента составляла 0,009 Ед/мл, что фактически отражает отсутствие гепарина в плазме больного, несмотря на используемую дозу.
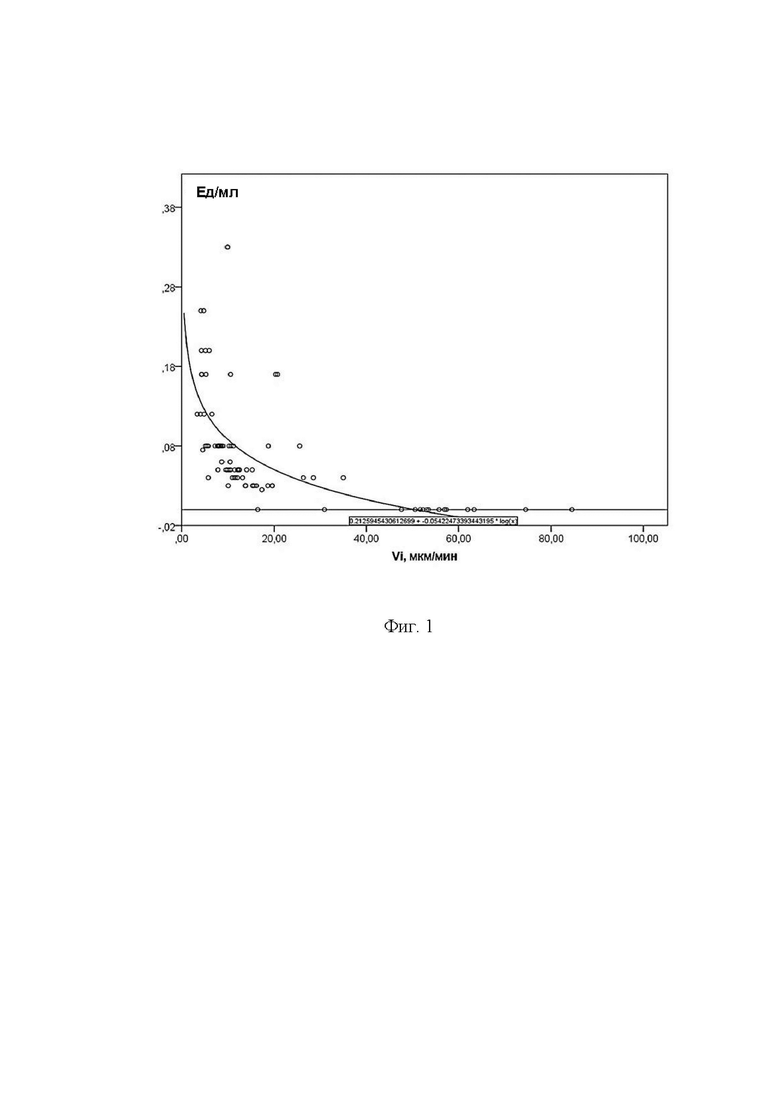
На фигуре 2 представлены результаты пространственно-временной динамики роста фибринового сгустка пациента Б., отражающие субтерапевтическую концентрацию нефракционированного гепарина (0,009 Ед/мл) на фоне его инфузии нефракционированного гепарина со скоростью 25 Ед/кг/ч и активности антитромбина 76%.
Коррекция дозы гепарина позволила добиться целевой гипокоагуляции. Показатели свертывающей системы крови представлены в таблице № 1.
Таблица 1
Пример 2
Пациент А. получал нефракционированный гепарин путем непрерывной внутривенной инфузии со скоростью 25 Ед/кг/ч. Активность антитромбина была равна 12%, результаты клоттинговых тестов не отражают ожидаемого лабораторного ответа (АЧТВ 35 с). Результаты пространственно-временной динамики свертывания крови отражают гипокоагуляционный профиль и низкую начальную скорость роста фибринового сгустка - 12,1 мкм/мин.
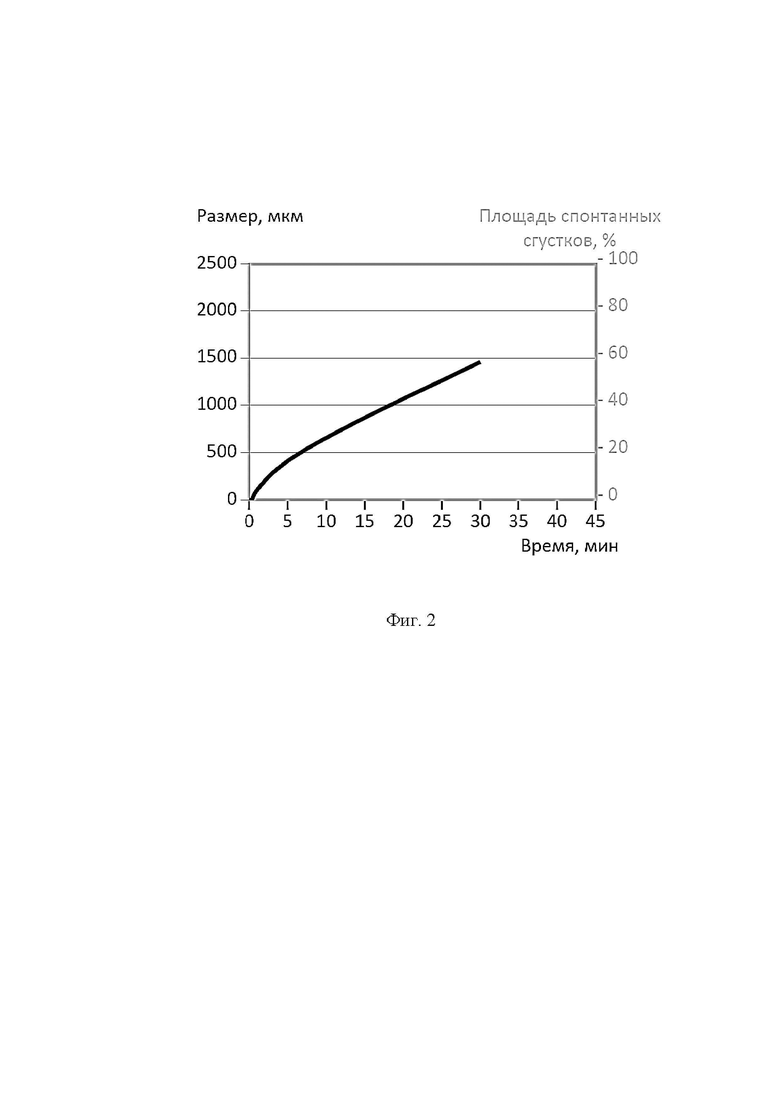
На фигуре 3 представлены результаты пространственно-временной динамики роста фибринового сгустка пациента А., отражающие терапевтическую концентрацию нефракционированного гепарина (0,08 Ед/мл) на фоне его инфузии со скоростью 25 Ед/кг/ч и активности антитромбина 12%.
На основании предлагаемого нами способа после расчета по формуле Y = 0,2126 - 0,0542 × ln12,1 = 0,08 концентрация гепарина в плазме пациента составляет 0,08 Ед/мл, что соответствует терапевтической концентрации. Показатели свертывающей системы крови показаны в таблице 2.
Таблица 2
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗА РИСКА РАЗВИТИЯ ВЕНОЗНЫХ ТРОМБОЭМБОЛИЧЕСКИХ ОСЛОЖНЕНИЙ ПРИ ТЯЖЕЛОЙ ОЖОГОВОЙ ТРАВМЕ | 2020 |
|
RU2737277C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДА ОЖОГОВОЙ БОЛЕЗНИ У ПАЦИЕНТОВ С ТЯЖЕЛОЙ ТЕРМИЧЕСКОЙ ТРАВМОЙ | 2020 |
|
RU2738303C1 |
| АНТИКОАГУЛЯНТНОЕ СРЕДСТВО НА ОСНОВЕ БИОЛОГИЧЕСКИ АКТИВНОГО КОМПЛЕКСА ИЗ КОРЫ КЕДРА СИБИРСКОГО | 2007 |
|
RU2366441C2 |
| АНТИКОАГУЛЯНТНОЕ СРЕДСТВО | 2009 |
|
RU2399377C1 |
| ВЫСОКОСЕЛЕКТИВНЫЙ ИНГИБИТОР КОНТАКТНОЙ АКТИВАЦИИ НА ОСНОВЕ ИНФЕСТИНА 4 | 2013 |
|
RU2556116C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕПАРИНА С НИЗКОЙ МОЛЕКУЛЯРНОЙ МАССОЙ И АНТИКОАГУЛЯНТНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2396282C1 |
| СРЕДСТВО С АНТИТРОМБОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2627435C1 |
| АНТИТРОМБОТИЧЕСКОЕ СРЕДСТВО ИЗ ЦЕЛЛЮЛОЗЫ ПИХТЫ СИБИРСКОЙ | 2014 |
|
RU2571555C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОМОЛЕКУЛЯРНОГО ГЕПАРИНА | 2007 |
|
RU2377993C2 |
| СПОСОБ ОЦЕНКИ УРОВНЯ АНТИКОАГУЛЯЦИИ НЕФРАКЦИОНИРОВАННЫМ ГЕПАРИНОМ ПРИ ПРОВЕДЕНИИ ГЕМОДИАЛИЗА У ПАЦИЕНТОВ С ОСТРЫМ ПОВРЕЖДЕНИЕМ ПОЧЕК | 2014 |
|
RU2571505C1 |
Изобретение относится к медицине, а именно к терапии, и может быть использовано для определения концентрации нефракционированного гепарина в плазме человека. Проводят забор у пациента венозной крови в пробирку с 3,2% раствором цитрата натрия в соотношении 9:1, центрифугирование образца крови при 1600 g в течение 15 мин с последующим забором супернатанта и его центрифугированием при 12000 g в течение 5 мин. Проводят анализ пространственно-временной динамики полученного фибринового сгустка. Расчет концентрации гепарина осуществляют по формуле: Y = 0,2126 – 0,0542 × ln(Vi), где Y – концентрация нефракционированного гепарина в плазме, Ед/мл; Vi – начальная скорость роста фибринового сгустка, мкм/мин, определенная в тесте пространственно-временной динамики образования фибринового сгустка, 0,2126 и 0,0542 – коэффициенты, полученные при построении модели. Способ обеспечивает возможность повышения точности определения концентрации гепарина в плазме пациента за счет оценки как временных, так и пространственных характеристик образования сгустка. 3 ил., 2 табл., 2 пр.
Способ определения концентрации нефракционированного гепарина в плазме человека, включающий забор у пациента венозной крови в пробирку с 3,2% раствором цитрата натрия в соотношении 9:1, центрифугирование образца крови при 1600 g в течение 15 мин с последующим забором супернатанта и его центрифугированием при 12000 g в течение 5 мин, проведение анализа пространственно-временной динамики полученного фибринового сгустка, расчет концентрации гепарина по формуле: Y = 0,2126 – 0,0542 × ln(Vi), где Y – концентрация нефракционированного гепарина в плазме, Ед/мл; Vi – начальная скорость роста фибринового сгустка, мкм/мин, определенная в тесте пространственно-временной динамики образования фибринового сгустка, 0,2126 и 0,0542 – коэффициенты, полученные при построении модели.
| HELIN T | |||
| et al | |||
| Laboratory assessment of unfractionated heparin (UFH) with activated clotting time (ACT) and anti-Xa activity during peripheral arterial angiographic procedure | |||
| Diagnostics (Basel) | |||
| Электромагнитный прерыватель | 1924 |
|
SU2023A1 |
| СПОСОБ ОЦЕНКИ УРОВНЯ АНТИКОАГУЛЯЦИИ НЕФРАКЦИОНИРОВАННЫМ ГЕПАРИНОМ ПРИ ПРОВЕДЕНИИ ГЕМОДИАЛИЗА У ПАЦИЕНТОВ С ОСТРЫМ ПОВРЕЖДЕНИЕМ ПОЧЕК | 2014 |
|
RU2571505C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ГЕПАРИНА | 2003 |
|
RU2249819C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ГЕПАРИНА В ВОДНОМ РАСТВОРЕ | 1999 |
|
RU2179314C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕПАРИНА | 1997 |
|
RU2123008C1 |
| WO 2015177293 A1, | |||
Авторы
Даты
2024-11-18—Публикация
2024-06-11—Подача