Область изобретения
Настоящее изобретение относится к новому способу синтезамоно- и бис-нитрозилированных пропандиолов, а также новым композициям и фармацевтическим составам, содержащим указанные соединения. Данное изобретение также относится к способам лечения патологического состояния, при котором введение оксида азота (NO) оказывает положительный эффект путем введения указанных соединений, композиций или составов.
Уровень техники
Содержание или обсуждение явно ранее опубликованного документа в этом описании не обязательно следует рассматривать как подтверждение того, что этот документ является частью современного уровня техники или общеизвестных знаний.
Легочную гипертензию (ЛГ) до недавнего времени определяли как повышение среднего давления в легочной артерии (mPAP) до уровня 25 мм рт. ст. или выше в покое, и ее можно разделить на более медленно развивающиеся хронические формы (ЛГ) и острую легочную гипертензию (ОЛГ). Это определение было недавно обновлено, и теперь оно означает повышение среднего давления в легочной артерии (mPAP) до уровня 20 мм рт. ст. или выше в покое в сочетании со значением Wood Units > 3. При ОЛГ, острое индуцированное сужение легочных сосудов быстро повышает mPAP; что может быть вызвано различными состояниями, такими как обширное оперативное вмешательство (например, операция на сердце), эмболия легких и сепсис. При ОЛГ не запускаются адаптационные механизмы правых отделов сердца, что увеличивает риск недостаточности правых отделов сердца, кроме того, пациенты обычно тяжело болеют из-за состояния, вызывающего ОЛГ, и, как правило, имеют критически низкое системное кровяное давление. У пациентов с более хроническими формами ЛГ, ОЛГ может накладываться на хроническую ЛГ, что приводит к пагубному высокому давлению, обуславливая недостаточность правых отделов сердца и смерть. Острая легочная гипертензия является огромной проблемой, вызывающей внезапную смерть и страдания миллионов людей во всем мире, и поскольку для диагностики обычно требуется катетеризация правых отделов сердца, а эффективные легочно-селективные методы лечения отсутствуют, полный масштаб этой проблемы не зарегистрирован и не известен.
В нормальных условиях правые отделы сердца получают деоксигенированную кровь из большого круга кровообращения и прокачивает кровь через легкие, где сердечный выброс малого круга кровообращения равен объему крови, циркулирующей по всем другим органам тела. Несмотря на высокую скорость кровотока в легких, кровяное давление в малом круге кровообращения составляет лишь одну пятую от давления в большом круге кровообращения. Низкое сопротивление в малом круге кровообращения объясняется большой площадью поперечного сечения легочных артерий и тем, что легочные сосуды намного короче системных сосудов. Левое сердце - это мощный насос (работающий против высокого давления), который обеспечивает приток крови в системном кровообращении, например, в печень, желудок, почки и само сердце, и при этом общеизвестно, что высокое кровяное давление в системном кровотоке может вызывать многие проблемы со здоровьем, включая сердечную недостаточность, инсульт и заболевание почек.
На комплексный контроль кровотока в большом и малом круге кровообращения влияют многие физиологические факторы. Кровеносные сосуды в большом круге кровообращения обычно находятся в состоянии вазоконструкции (мелкие мышцы в стенке сосуда сокращают сосуд), тогда как кровеносные сосуды в малом круге кровообращения находятся в состоянии постоянной вазодилатации (то есть расслабленные, расширенные сосуды), тем самым поддерживая очень низкое сопротивление кровотоку и, как следствие, очень низкое кровяное давление по сравнению с большим кругом кровообращения.
При различных угрожающих жизни заболеваниях и после больших операций патофизиологический ответ с интенсивной воспалительной реакцией изменяет физиологическое состояние системных и легочных кровеносных сосудов. Эти изменения обычно приводят к состоянию, при котором системные кровеносные сосуды внезапно расширяются и развивается критически низкое системное кровяное давление (системная гипотензия), что может уменьшить приток крови к жизненно важным органам, таким как головной мозг, сердце, печень и почки. Параллельно с этим, как ни парадоксально, внезапно сужаются легочные кровеносные сосуды, что приводит к острой легочной гипертензии и правожелудочковой недостаточности, что снижает сердечный выброс и еще больше усугубляет системную гипотензию. Эти критически больные и гемодинамически нестабильные пациенты обычно проходят лечение в отделениях интенсивной терапии, при этом сложная задача состоит в том, чтобы сбалансировать медикаментозную терапию с применением вазопрессоров и укрепляющих серде препаратов для восстановления системного кровяного давления и легочных сосудорасширяющих препаратов для ослабления острой угрожающей жизни легочной гипертензии.
Зачастую острая ЛГ недооценивается, и лечение часто откладывается (Rosenkranz, Stephan et al., European Heart Journal, 37(12), 942-954 (2016)). Причина того, что ОЛГ является настолько смертельной, заключается в том, что правые отделы сердца представляют собой слабый насос, обычно работающий против низкого давления, и могут проявить недостаточность (недостаточность правого желудочка), если среднее давление в малом круге кровообращения быстро достигает > 40 мм рт. ст. Острая ЛГ - это отдельное критическое патологическое состояние, и его не следует путать с хронической легочной гипертензией (Tiller, D et al., PLoS One, 8(3), e59225 (2013)). При хронических заболеваниях, когда давление в малом круге кровообращения с течением времени постепенно повышается, правые отделы сердца адаптируются и увеличиваются в размерах и силе, и тогда может поддерживаться гораздо более высокое давление оттока. Даже у здоровых людей, которые, например, проконтактировали с инфекцией, перенесли тромбоэмболию легочной артерии (сгусток крови в легком) или обширное оперативное вмешательство, может развиться ОЛГ с прогрессирующими осложнениями.
Острая легочная гипертензия является огромной проблемой, вызывающей мучительную и преждевременную смерть, а также страдания миллионов людей во всем мире, и поскольку надлежащая диагностика и лечение отсутствуют, масштаб проблемы в полной мере не зарегистрирован и не известен.
Варианты лечения пациентов, у которых развивается ОЛГ, сегодня сильно ограничены. Причина в том, что такие пациенты обычно имеют критически низкое системное кровяное давление. Попытки лечения с помощью внутривенных (в/в) сосудорасширяющих препаратов часто приводят к летальной системной гипотензии, поскольку доступные на сегодняшний день препараты проходят через легкие (обычно < 30 с) и «перетекают» в системный кровоток. Следовательно, оптимальный внутривенный препарат для лечения ОЛГ должен расширять только легочные сосуды и не оказывать никакого влияния на системный кровоток. На сегодняшний день на рынке нет внутривенных сосудорасширяющих препаратов, являющихся селективными для легких.
Чтобы преодолеть системные побочные эффекты сосудорасширяющих препаратов, вводимых внутривенно, было разработано введение путем ингаляции оксида азота или простациклина. К сожалению, этих препаратов, даже если они и оказываются эффективными в некоторых случаях, часто бывает недостаточно, потому что они часто инактивируются до того, как достигают целевых легочных сосудов. Еще один серьезный недостаток применяемых сегодня ингаляционных лекарственных средств состоит в том, что их введение путем ингаляции сложнее, чем внутривенная инфузия препарата. Сложность введения ингаляционного оксида азота настолько велика, что медицинскому персоналу требуется специальная подготовка, и поэтому многие клиники даже не имеют оборудования из-за связанной с этим дороговизны.
Оксид азота (NO) - важная молекула в нескольких биологических системах. Он постоянно вырабатывается в легких и может быть измерен на уровне ppb (частей на миллиард) в выдыхаемом газе. Открытие эндогенного NO в выдыхаемом воздухе и его применение в качестве диагностического маркера воспаления датируется началом 1990-х годов (см., например, WO 93/05709 и WO 95/02181). На сегодняшний день важность эндогенного NO широко признана, о чем свидетельствует коммерческая доступность клинического анализатора NO (NIOX®, первый специально разработанный анализатор NO для повседневного клинического применения у пациентов с астмой, производимый компанией AEROCRINE AB, Solna, Швеция.).
Начиная с этих ранних экспериментов, стало общеизвестным, что эндогенный оксид азота (NO) имеет решающее значение как медиатор вазодилятации в кровеносных сосудах. В частности, оксид азота играет важную роль в модуляции тонуса легочных сосудов для оптимизации соответствия вентиляции и перфузии у здоровых взрослых людей (то есть соответствия воздуха, который достигает альвеол, и кровь, которая поступает в альвеолы через капилляры, таким образом, что кислорода, поступающего путем вентиляции, достаточно для полного насыщения крови; см., например, публикацию Persson et al., Acta Physiol. Scand., 1990, 140, 449-57). Измерение NO в выдыхаемом воздухе представляет собой надежный способ отслеживагния изменений в продукции или поглощении эндогенного NO в легких (Gustafsson et al ., Biochem. Biophys. Res. Commun., 1991, 181, 852-7).
Поскольку нарушения вентиляции и перфузии и повышение кровяного давления в легочной артерии являются особенностями тромбоэмболии легочной артерии, вдыхаемый NO был протестирован в качестве потенциального способа лечения. Например, в US 5670177 описан способ лечения или профилактики ишемии, включающий введение пациенту внутрисосудистым путем газовой смеси, содержащей NO и диоксид углерода, и в которой NO присутствует в количестве, эффективном для лечения или профилактики ишемии. В US 6,103,769 описан аналогичный способ с той разницей, что применяют NO-насыщенный солевой раствор.
Кроме того, газовые смеси оксида азота/кислорода применяются в качестве «терапии отчания» в отделениях интенсивной терапии, чтобы способствовать расширению капилляров и легких для лечения первичной легочной гипертензии и постмекониевой аспирации у новорожденных, связанных с врожденными дефектами (см. публикацию Barrington et al., Cochrane Database Syst. Rev., 2001, 4, CD000399 and Chotigeat et al., J. Med. Assoc. Thai., 2007, 90, 266-71). Точно так же NO назначают в качестве «терапии спасения» пациентам с острой правожелудочковой недостаточностью, вторичной по отношению к тромбоэмболии легочной артерии (Summerfield et al., Respir. Care., 2011, 57, 444-8). Ингаляционный NO также одобрен в Европе и Японии для лечения острой легочной гипертензии у пациентов кардиохирургического профиля.
В качестве альтернативы предоставлению NO в виде газа или растворенного в растворе, другие авторы исследовали применение соединений, доставляющих NO. Например, в WO 94/16740 описано применение соединений, доставляющих NO, таких как S- нитрозотиолы, тионитриты, тионитраты, сиднонимины, фуроксаны, органические нитраты, нитропруссид, нитроглицерин, нитрозильные соединения железа и т.д., для лечения или профилактики алкогольного поражения печени.
В настоящее время нитраты применяются для лечения симптомов стенокардии (боли в за грудиной). Нитраты расслабляют кровеносные сосуды и увеличивают приток крови и кислорода к сердцу, снижая при этом его рабочую нагрузку. Примеры доступных в настоящее время нитратных препаратов включают:
a) Нитроглицерин (тринитрат глицерина) (1,2,3-пропантриолнитрат), который сегодня в основном принимают сублингвально для купирования острого приступа стенокардии. Однако сильные головные боли и головокружение из-за быстрого и общего сосудорасширяющего действия часто являются побочными эффектами. Также доступны концентраты для инфузий нитроглицерина, которые разводятся в изотонической глюкозе или физиологическом солевом растворе для внутривенной инфузии.
b) Изосорбид мононитрат (1,4:3,6-диангидро-D-глюцитол-5-нитрат), который принимают в качестве профилактического средства против стенокардии. Развитие толерантности - проблема при длительном приеме лечения. Частые побочные эффекты включают головную боль и головокружение, как при приеме нитроглицерина.
c) Изосорбида динитрат (1,4:3,6-диангидро-D-глюцитол-2,5-нитрат), который принимают как в острых ситуациях, так и профилактически при стенокардии и сердечной недостаточности.
d) Известно, что пентаэритритилнитраты, группа органических нитратов, обладают долгосрочным антиоксидантным и антиатерогенным действием за счет неустановленных в настоящее время механизмов. Пентаэритритилтетранитрат был исследован в контексте толерантности к нитратам, нежелательного механизма при терапии нитратами, и экспериментально протестирован при легочной гипертензии.
Ряд этих нитратных соединений, а также других нитратных и нитритных соединений были протестированы in vivo и было обнаружено, что они генерируют NO. Например, тринитрат глицерина, этилнитрит, изобутилнитрат, изобутилнитрит, изоамилнитрит и бутилнитрит были протестированы на модели кролика, и обнаружено, что они обеспечивают значительную корреляцию между образованием NO in vivo и влиянием на кровяное давление (Cederqvist et al., Biochem. Pharmacol., 1994, 47, 1047-53).
Соответственно, было высказано предположение, что определенные органические нитриты полезны для лечения мужской импотенции и эректильной дисфункции при местном или интракавернозном введении в половой член (см. US 5,646,181).
Относительно недавно была проведена переоценка роли пищевых нитратов и нитритов, особенно после того, как было обнаружена эндогенная продукция NO в системе аргинин-оксид азота и его роль в защите хозяина (Larsen et al. , N. Eng. J. . Med , 2006 , 355 , 2792-3). Следовательно, L-аргинин и его сложные эфиры, такие как этил-, метил- и бутил-L-аргинин, применялись для увеличения эндогенной продукции NO.
В WO 2006/031191 описаны композиции и способы применения для терапевтической доставки газообразного оксида азота. Такие композиции для доставки газообразного NO содержат соединение, способное образовывать обратимую связь или ассоциацию с NO, такое как спирты, углеводы и белки.
В WO 2007/106034 описаны способы получения органических нитритов из соединения, которое представляет собой одно-/многоатомный спирт или его альдегид- или кетонпроизводное. Указанные способы включают деаэрацию водного раствора указанного соединения с последующей продувкой газообразным оксидом азота (NO).
В публикации Nilsson, K. F. et al., Biochem Pharmacol., 82(3), 248-259 (2011) обсуждается образование и идентификацию новых биоактивных органических нитритов.
Несмотря на недавние достижения, существует ряд недостатков, ассоциированных с соединениями, композициями и способами получения, известными из уровня техники.
Например, среди доступных в настоящее время соединений и композиций многие ассоциированы с нежелательными свойствами или побочными эффектами, такими как проблемы токсичности, замедленное действие, необратимое действие или пролонгированное действие и т.д. Одной из конкретных проблем, часто встречающихся при введении NO-донорного соединения в форме инфузии, является продукция метгемоглобина (metHb).
Кроме того, известные органические нитриты и их терапевтическое применение часто связаны с проблемами, которые могут быть вызваны примесями и продуктами разложения, присутствующими в указанных композициях. Также трудно приготовить фармацевтические препараты, содержащие органические нитриты, поскольку стадии смешивания и применяемые носители могут вызвать дальнейшее разложение.
Кроме того, применение ингаляционного оксида азота и кислорода характеризуется значительными проблемами из-за образования диоксида азота, который необходимо постоянно контролировать во время введения.
Некоторые способы получения из предшествующего уровня техники обеспечивают только относительно низкую концентрацию органического нитрита в водном растворе, что означает, что свойства таких составов при хранении и транспортировке часто являются менее чем удовлетворительными.
Кроме того, способы получения их предшествующего уровня техники приводят к значительным количествам газообразного NO и неорганического нитрита, растворенного в растворе, в дополнение к желаемому органическому нитриту. Из-за очень реактивных свойств NO, необходимо осторожно обращаться с раствором и хранить его, чтобы избежать внезапного и спонтанного разложения. Также вероятно, что газ NO вступает в реакцию с пластиковыми материалами в контейнере для хранения.
Кроме того, присутствие неорганических нитритов увеличивает фракцию metHb в крови, что является ограничивающим дозу побочным эффектом.
Следовательно, существует значительная и срочная потребность в способе получения соединений, доставляющих NO, и содержащих их композиций, которые преодолевают один или большее количество недостатков, ассоциированных со способами получения и композициями из предшествующего уровня техники. Также существует потребность в способе, позволяющем применять соединения и композиции, полученные посредством таких процессов.
Описание изобретения
Авторы настоящего изобретения неожиданно обнаружили способ получения соединения, доставляющего NO, который преодолевает один или большее количество недостатков, ассоциированных со способами получения из предшествующего уровня техники.
Например, указанный способ по данному изобретению обеспечивает относительно высокую концентрацию соединений по изобретению в растворе, тем самым обеспечивая простоту обращения и минимизируя объемы хранения и транспортные расходы. Кроме того, способ по данному изобретению не приводит к растворению газообразного оксида азота или неорганического нитрита, тем самым сводя к минимуму риск внезапного и спонтанного разложения и снижая вероятность побочных эффектов, когда продукт, получаемый в результате осуществления указанного способа, применяется для лечения. Способ по данному изобретению также обеспечивает очень низкие уровни образования других примесей.
Кроме того, авторы данного изобретения обнаружили, что посредством таких способов можно доставлять химически стабильные, неводные композиции и составы, содержащие эти соединения, которые могут обеспечивать удобную транспортировку и хранение до терапевтического применения. Кроме того, авторы данного изобретения разработали удобные способы применения таких композиций и составов путем введения в комбинации с пригодным водным буфером.
Способы
В первом аспекте данного изобретения предлагается способ приготовления композиции, содержащей одно или большее количество соединений формулы I.
где:
R1, R2 и R3 каждый независимо представляет собой H или -NO;
n равно 0 или 1;
при этом, когда n равно 0, тогда R1 представляет собой H, а когда n равно 1, R2 представляет собой H; а также
при условии, что по меньшей мере один из R1, R2 и R3 представляет собой -NO,
указанный способ включает стадию:
(i) взаимодействия соответствующего соединения формулы I, но где R1, R2 и R3 представляют собой H, с источником нитрита, необязательно в присутствии пригодной кислоты,
при этом:
(а) когда источником нитрита является органический нитрит, стадию (i) выполняют в пригодном органическом растворителе; а также
(b) когда источником нитрита является неорганический нитрит, стадия (i) выполняется в двухфазной смеси растворителей, содержащей водную фазу и неводную фазу,
этот способ в дальнейшем может называться «способ по изобретению» или тому подобное.
Во избежание сомнений, продукт способа по данному изобретению (то есть соединение формулы I) может также (или вместо этого) называться моно- и бис-нитрозилированным 1,2-пропандиолом или 1,3-пропандиолом (или смесь таких соединений, то есть композиция, содержащая один или большее количество моно- или бис-нитрозилированных 1,2- или 1,3-пропандиолов).
Во избежание сомнений, соответствующее соединение формулы I, но где R1, R2 и R3 представляют собой H, может называться соответствующим 1,2-пропандиолом и/или 1,3-пропандиолом (то есть состав желаемого продукта). Другими словами, соответствующее соединение формулы I может быть соединением формулы (Ia), как определено ниже.
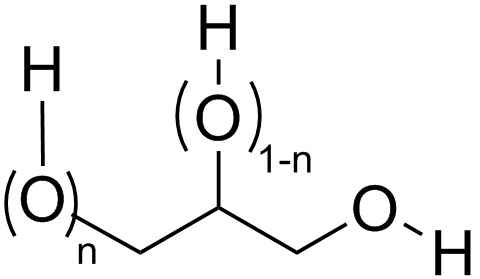 (Ia)
(Ia)
Во избежание сомнений, когда целое число (n или 1-n), относящееся к атомам кислорода, равно 0, атом кислорода отсутствует и заместитель R1 и R2 (и соответствующий H в соединении формулы (Ia )) связан с соответствующим углеродом.
Квалифицированному специалисту будет понятно, что ссылки в данном документе на способ изобретения (или, аналогично, на «способы изобретения» или тому подобное) будут включать ссылки на все варианты осуществления и их конкретные признаки.
Если не указано иное, все технические и научные термины, примененяемые в данном документе, имеют то же значение, которое обычно понимается специалистом в области техники, к которой относится это изобретение.
Все варианты осуществления данного изобретения и конкретные признаки, упомянутые в данном документе, могут быть взяты отдельно или в сочетании с любыми другими вариантами осуществления и/или конкретными признаками, упомянутыми в данном документе (следовательно, описывая более конкретные варианты осуществления и конкретные признаки, как описано в данном документе), в пределах объема изобретения.
В данном контекмте термин «содержит» будет иметь свое обычное значение в данной области техники, а именно будет означать, что компонент включает, но не ограничивается этим, соответствующие признаки (то есть включает, помимо прочего). По существу, термин «содержит» будет включать ссылки на компонент, состоящий по существу из соответствующего вещества (веществ).
В контексте настоящего описания, если не указано иное, термины «состоит по существу из» и «состоящий по существу из» будут относиться к соответствующему компоненту, состоящему из по меньшей мере 80% (например, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95%, например, по меньшей мере 99%) указанного вещества (веществ) в соответствии с соответствующей мерой (например, по весу). Термины «состоит по существу из» и «состоящий по существу из» могут быть заменены на «состоит из» и «состоящий из» соответственно.
Во избежание сомнений, термин «содержит» также будет включать ссылки на компонент, состоящий из соответствующего вещества (веществ).
Таким образом, квалифицированному специалисту будет понятно, что ссылки на получение композиции, содержащей одно или большее количество соединений формулы (I), будут относиться к приготовлению композиции, которая содержит в качестве составной части количество одного или большего количества соединений формулы (I). структура которого такая, как определено в формуле I, необязательно вместе с другими соединениями. Способ по данному изобретению также может быть отнесен к способу получения соединений формулы I (то есть к способу получения одного или большего количества соединений формулы I).
Квалифицированному специалисту будет понятно, что ссылки на способ, представляющий собой способ получения соединений формулы I, будут расцениваться как указывающие на то, что способ по данному изобретения может привести к получению одного или большего количества типов соединения, каждое из которых описано формулой I, как определено в данном документе (например, когда присутствует более одного такого соединения, в виде их смеси).
Таким образом, квалифицированному специалисту будет понятно, что соединения, образованные посредством способа по данному изобретению, могут принимать форму смеси каждого мононитрита и динитрита, при этом относительные количества каждого из них варьируются в зависимости от концентрации соединений формулы I.
В частности, согласно способу по данному изобретению можно приготовить композицию, в которой по меньшей мере 50 мас.%, 60 мас.%, 70 мас.% мли 80 мас.% (например, по меньшей мере 90 мас.% или по меньшей мере 99 мас.%, например, по меньшей мере 99,9 мас.%) соединений формулы I являются мононитрозилированными, так что каждый из R1, R2 и R3 независимо представляет собой H или -NO, при условии, что один из R1, R2 или R3 представляет собой - NO, а остальные группы представляют собой H.
В частности, согласно способу по данному изобретению можно приготовить композицию, которая содержит одно или большее количество соединений формулы I вместе с одним или большим количеством соответствующих соединений формулы I, но где R1, R2 и R3 представляют собой H (то есть 2-пропандиол и/или 1,3-пропандиол, например, непрореагировавший 1,2-пропандиол и/или 1,3-пропандиол, исходный материал) и, возможно, другие соединения.
В некоторых вариантах осуществления данного изобретения, способ по данному изобретению может представлять собой способ получения композиции, состоящей по существу из одного или большего количества соединений формулы I и одного или большего количества соответствующих соединений формулы I, но где R1, R2 и R3 представляют собой H (то есть 1,2-пропандиол и/или 1,3-пропандиол, например, в виде их смеси).
Квалифицированному специалисту будет понятно, что термин «реагирование» будет относиться к объединению соответствующих компонентов таким образом (например, в пригодном состоянии и среде), так что происходит химическая реакция. В частности, ссылка на реакцию исходного материала (то есть 1,2-пропандиола и/или 1,3-пропандиола) с источником нитрита будет относиться к химической реакции между исходным материалом и нитритом (то есть нитритом, обеспечиваемым источник нитрита).
Квалифицированному специалисту будет понятно, что ссылка на «источник нитрита» может вместо этого относиться просто к «нитриту», поскольку именно нитрит, полученный из источника нитрита, подвергается химической реакции. По существу, ссылки на источник нитрита следует понимать как относящиеся к соединению, которое обеспечивает для реакции нитритную составляющую (которая может присутствовать либо в ионной, либо в ковалентно связанной форме, в зависимости от присутствующего источника нитрита). Таким образом, источник нитрита может называться источником реакционноспособного (или реагирующего) нитрита (или нитритного фрагмента). Во избежание сомнений, источником нитрита может быть неорганический нитрит или органический нитрит.
Как указано в данном документе, когда источником нитрита является органический нитрит, стадия (i) выполняется в пригодном органическом растворителе.
Квалифицированному специалисту будет понятно, что в способе по данному изобретению можно применять различные органические нитриты, такие как алкилнитриты.
Конкретные алкилнитриты, которые можно упомянуть, включают этилнитрит, пропилнитриты, бутилнитриты и пентилнитриты. В конкретных вариантах осуществления данного изобретения, алкилнитрит представляет собой н-бутилнитрит, изобутилнитрит или трет-бутилнитрит, такой как трет-бутилнитрит.
Если источником нитрита является органический нитрит, квалифицированный специалист сможет выбрать пригодный растворитель. Например, пригодные растворители могут включать те, которые упоминаются в данном документе как пригодные органические компоненты двухфазной системы растворителей, и их смеси.
Во избежание сомнений, если не указано иное, ссылки на способ по данному изобретению, выполняемый с пригодным органическим растворителем, не указывают на то, что могут присутствовать другие неорганические растворители, такие как вода.
В конкретном варианте осуществления данного изобретения, когда способ по данному изобретению выполняется с пригодным органическим растворителем, указанный растворитель может по существу не содержать воды (что может называться «не содержащий воды» или «сухой»), что может указывать на то, что растворитель содержит менее чем около 1% (например, менее чем около 0,1%, например, менее чем около 0,01%) по весу воды.
Термин «около» определяется в данном документе как означающий, что определенное значение может отклоняться на ± 10%, например, на ± 5%, например, на ± 4%, ± 3%, ± 2% или ± 1%. Термин «около» может быть удален из описания, не выходя за рамки сущности изобретения.
Как указано в данном документе, когда источником нитрита является неорганический нитрит, стадия (i) выполняется в двухфазной смеси растворителей, содержащей водную фазу и неводную фазу.
Квалифицированному специалисту будет понятно, что термин «двухфазная смесь растворителей», применяемый в данном документе, будет относиться к системе, состоящей из двух растворителей или смесей растворителей, которые не смешиваются с образованием единой фазы растворителя, а вместо этого присутствуют в виде двух различных (то есть несмешанных) фаз.
Если такие смеси растворителей содержат воду и органический растворитель (или смесь органических растворителей), можно сказать, что такие системы растворителей включают «водную фазу» и «органическую фазу». Во избежание сомнений, термин двухфазный не означает, что вещества, образующие другие фазы, такие как вещества, образующие твердую фазу, могут присутствовать в дополнение к системе растворителей (то есть, другие фазы также могут присутствовать).
Конкретные источники неорганических нитритов, которые можно упомянуть, включают нитриты металлов, такие как нитриты щелочных металлов и нитриты щелочноземельных металлов. Ионные жидкости также могут быть пригодным источником неорганических нитритов.
Во избежание сомнений, термин «щелочной металл» имеет свое обычное значение в данной области техники, а именно относится к элементам и катионам группы 1 IUPAC, включая литий, натрий, калий, рубидий, цезий и франций.
Во избежание сомнений, термин щелочноземельный металл имеет свое обычное значение в данной области техники, а именно относится к элементам и катионам группы 2 IUPAC, включая бериллий, магний, кальций, стронций, барий и радий.
Более конкретные неорганические нитриты, которые можно упомянуть, включают нитриты щелочных металлов, такие как нитрит лития, нитрит натрия и нитрит калия. В конкретном варианте осуществления данного изобретения, источником нитрита является нитрит натрия.
В альтернативном варианте, нитрит металла может быть нитритом щелочноземельного металла, таким как нитрит лития, нитрит магния или нитрит кальция.
Во избежание сомнений, квалифицированному специалисту будет понятно, что неводная фаза в двухфазной системе растворителей может быть органическим растворителем, который, следовательно, может называться органической фазой.
Квалифицированный специалист сможет выбрать пригодный неводный (то есть органический) растворитель на основе свойств водных фаз. Например, если водная фаза имеет определенный уровень растворенных в ней веществ (например, ионных твердых веществ, таких как соли), можно выбрать широкий спектр органических растворителей, чтобы сформировать двухфазную систему растворителей.
В конкретных вариантах осуществления данного изобретения, неводная фаза состоит из органического растворителя, несмешивающегося с водой. В более конкретных вариантах осуществления данного изобретения, несмешивающийся с водой органический растворитель представляет собой апротонный органический растворитель.
Конкретные несмешивающиеся с водой органические растворители (то есть конкретные растворители, образующие неводную фазу), которые могут быть упомянуты, включают простые эфиры (например, трет-бутилметиловый эфир, циклопентилметиловый эфир, метилтетрагидрофуран, диэтиловый эфир, диизопропиловый эфир) и дихлорметан (DCM).
Более конкретные несмешивающиеся с водой органические растворители (то есть конкретные растворители, образующие неводную фазу), которые могут быть упомянуты, включают дихлорметан, диэтиловый эфир и трет-бутилметиловый эфир. В более конкретных вариантах осуществления данного изобретения, несмешивающийся с водой органический растворитель представляет собой трет-бутилметиловый эфир.
В определенных вариантах осуществления данного изобретения, которые можно упомянуть, смесь растворителей может содержать избыток соединений формулы I, но где R1, R2 и R3 представляют собой H (то есть 1,2-пропандиол и/или 1,3-пропандиол). Во избежание сомнений, в таких обстоятельствах 1,2-пропандиол и/или 1,3-пропандиол (то есть соединения формулы I, но где R1, R2 и R3 представляют собой H) могут присутствовать как в виде растворителя (например, компонент смеси растворителей), так и в виде реагента. Как таковой, в конкретных вариантах осуществления данного изобретения, указанный способ представляет собой способ получения соединений формулы I в виде раствора в соответствующих соединениях формулы I, но где R1, R2 и R3 представляют собой H, то есть 1,2-пропандиол и/или 1, 3-пропандиол (например, в форме смеси, содержащей 1,2-пропандиол и/или 1,3-пропандиол, исходя из конкретных условий). В некоторых вариантах осуществления данного изобретения, когда источником нитрита является органический нитрит, растворитель может состоять по существу из соединений формулы I, но где R1, R2 и R3 представляют собой H (то есть 1,2-пропандиол и/или 1,3- пропандиол). То есть соединения формулы I, но где R1, R2 и R3 представляют собой H, могут действовать как растворитель, так и реагент.
В альтернативном варианте осуществления данного изобретения, когда источником нитрита является неорганический нитрит, стадия (i) может быть выполнена в одном растворителе, при этом растворитель может состоять по существу из соединений формулы I, но где R1, R2 и R3 представляют собой H (то есть 1,2-пропандиол и/или 1,3-пропандиол). То есть соединения формулы I, но где R1, R2 и R3 представляют собой H, могут действовать как растворитель, так и реагент.
В альтернативных вариантах осуществления данного изобретения, способ по данному изобретению можно выполнять с избытком нитрита относительно исходного материала формулы I, но где R1, R2 и R3 представляют собой H (то есть 1,2-пропандиол и/или 1,3-пропандиол).
В данном контексте термин «избыток» будет иметь свое обычное значение в данной области техники, а именно означает, что компонент присутствует в количестве, превышающем стехиометрическое количество, для реакции, в которой он является реагентом.
Как указано в этом документе, способ по данному изобретению (в частности, реакция между компонентами) необязательно выполняют в присутствии пригодной кислоты.
Конкретные способы по данному изобретению, которые можно упомянуть, включают те, в которых стадию взаимодействия исходного материала (то есть 1,2-пропандиола и/или 1,3-пропандиола) с источником нитрита проводят в присутствии пригодной кислоты.
Конкретные кислоты, которые могут быть упомянуты в качестве пригодных кислот, включают кислоты Бренстеда (то есть протонодонорные кислоты), более конкретно, при этом такие кислоты могут называться сильными кислотами.
Во избежание сомнений, термин «сильная кислота» принимает свое обычное значение в данной области техники, относясь к кислотам Бренстеда, диссоциация которых практически полностью завершается в водном растворе при равновесии. В частности, ссылки на сильные кислоты могут относиться к кислотам Бренстеда с pKa (в воде) менее чем около 5 (например, менее чем около 4,8). Во избежание сомнений, для мультипротонных кислот, таких как серная кислота, термин сильная кислота относится к диссоциации первого протона.
Некоторые сильные кислоты, которые могут быть упомянуты, включают кислоты с pKa (в воде) менее чем около 1, например, менее чем около 0 (например, менее чем около -1 или -2). Например, сильные кислоты, которые могут быть упомянуты, включают кислоты с pKa (в воде) около -3. Квалифицированному специалисту в данной области техники буде понятно, что пригодные кислоты могут включать ненуклеофильные кислоты, как известно специалистам в данной области техники.
В качестве особенно пригодных кислот можно упомянуть серную кислоту, фосфорную кислоту, трифторуксусную кислоту и уксусную кислоту.
Более конкретные пригодные кислоты, которые можно упомянуть, включают минеральные кислоты (например, сильные минеральные кислоты), такие как серная кислота.
Квалифицированный специалист сможет выбрать пригодные количества реагентов для применения в способе по данному изобретения в рамках идеи данного изобретения. Например, соотношение (то есть молярное соотношение) соответствующего соединения формулы I, но где R1, R2 и R3 представляют собой H, к нитриту и кислоте (если они присутствуют) может составлять около 1: от около 1 до около 5: от около 0,5 до около 3,5, например, около 1: от около 1 до около 3: от около 0,5 до около 2 (например, около 1:4:2,7, или около 1:2:0,95, или около 1:2:1). Во избежание сомнений, если пригодная кислота отсутствует, могут применяться соотношения между соответствующим соединением формулы I, но где R1, R2 и R3 представляют собой H, и нитрит.
В конкретных вариантах осуществления данного изобретения, стадию (i) указанного способа проводят при температуре от около -30 °C до около 5 °C, например, от около -30 °C до около 0 °C, например, от около -30 °C до около -10 °C, предпочтительно от около -25 °C до около -15 °C.
В конкретных вариантах осуществления данного изобретения, стадию (i) указанного способа проводят в инертной атмосфере, такой как атмосфера азота или аргона, предпочтительно в атмосфере аргона. Кроме того, в конкретных вариантах осуществления данного изобретения, любые стадии указанного способа можно проводить в инертной атмосфере, такой как атмосфера азота или аргона, предпочтительно в атмосфере аргона.
Конкретные способы по данному изобретению, которые могут быть упомянуты, в частности, в которых применяется двухфазная система растворителей, включают те, в которых указанный способ дополнительно включает, после (например, непосредственно после) стадии (i), стадию:
(ii) удаления по существу всей водной фазы (то есть удаление по существу всей воды) из смеси растворителей.
Квалифицированному специалисту будет понятно, что водную фазу можно удалить из смеси растворителей любым пригодным для этого способом и с применением любого пригодного оборудования, известного в данной области техники (например, с помощью делительной воронки или аналогичного устройства).
В контексте настоящего описания, если не указано иное, термин «по существу весь» будет относиться по меньшей мере к 80% (например, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95%, например, по меньшей мере 99%) указанного вещества (веществ) в соответствии с соответствующей мерой (например, по весу).
Квалифицированному специалисту будет также понятно, что ссылки на «удаление по существу всей водной фазы из смеси растворителей» могут быть заменены ссылками на «удаление части или всей водной фазы из смеси растворителей» или просто «удаление водной фазы из смеси растворителей».
Во избежание сомнений, в контексте ее удаления, термин водная фаза будет относиться к (отдельной) фазе, образованной из воды и растворенных в ней компонентов.
Конкретные способы по данному изобретению, которые могут быть упомянуты, в частности, в которых применяется двухфазная система растворителей, включают те, в которых указанный способ дополнительно включает, после (например, непосредственно после) стадии (i), стадии (в приведенной последовательности):
(ii) удаления части или всей (например, по существу всей) водной фазы (то есть воды);
(iii) промывания оставшейся органической фазы одной или большим количеством дополнительных водных фаз;
(iv) необязательного повторения стадий (ii) и (iii) один или большее количество раз.
Дополнительные способы по данному изобретению, которые могут быть упомянуты, в частности, в которых применяется двухфазная система растворителей, включают те, в которых указанный способ дополнительно включает, после (например, непосредственно после) стадии (i), стадии (в приведенной последовательности):
(ii) удаления части или всей (например, по существу всей) водной фазы (то есть воды);
(iii) промывания оставшейся органической фазы одной или большим количеством дополнительных водных фаз;
(iv) необязательного повторения стадий (ii) и (iii) один или большее количество раз;
(v) необязательного уменьшения (то есть уменьшение количества/объема) органической фазы, например, путем удаления части или по существу всего несмешивающегося с водой органического растворителя (например, органического растворителя, отличного от 1,2-пропандиола и/или 1,3-пропандиола), и
(vi) необязательной сушки продукта,
при этом стадии (ii) - (vi) могут выполняться в любом порядке при условии, что стадии (ii) - (iv) выполняются перед стадиями (v) и (vi).
В конкретных вариантах осуществления данного изобретения, стадии (ii) - (iv) указанного способа можно выполнять при температуре от около -20 °C до около 5 °C, например, от около -10 °C до около 5 °C.
В конкретных вариантах осуществления данного изобретения, стадия (v) указанного способа может быть выполнена при температуре от около 0 °C до около 30 °C, например, от около 10 °C до около 30 °C, например, от около 15 °C до около 30 °С.
В конкретных вариантах осуществления данного изобретения, стадию (v) указанного способа проводят не более чем 6 часов, например, не более чем 5 часов, предпочтительно не более чем 4 часов.
В конкретных вариантах осуществления данного изобретения, выполняют каждую из стадий (ii) - (vi), например, при этом эти стадии выполняют в указанном порядке.
Во избежание сомнений, квалифицированному специалисту будет понятно, что промывание оставшейся органической фазы одной или большим количеством дополнительных водных фаз будет относиться к стадиям, включающим: добавление дополнительной части водного растворителя (например, воды); смешивание с (отдельной) органической фазой (например, путем перемешивания и/или встряхивания вместе); и удаление по существу всей водной фазы и, возможно, повторение указанных стадий один или большее количество раз.
Квалифицированному специалисту будет понятно, что стадия (iii) может быть выполнена любым пригодным для этого способом и с применением любого пригодного оборудования, известного в данной области техники (например, с помощью делительной воронки).
Квалифицированному специалисту будет понятно, что стадия (v) может быть выполнена любым пригодным для этого способом и с применением любого пригодного оборудования, известного в данной области техники (например, выпариванием при пониженном давлении).
В контексте стадии (v), ссылки на удаление части органической фазы могут относиться, в частности, к удалению по существу всего несмешивающегося с водой органического растворителя, как определено в данном документе. Более конкретно, удаление несмешивающегося с водой органического растворителя может относиться к удалению по меньшей мере 99% (например, по меньшей мере 99,5%, 99,9% или, в частности, 99,99%) по массе несмешивающегося с водой органического растворителя.
Такое удаление несмешивающегося с водой органического растворителя может также относиться к удалению таким образом, чтобы продукт после такого удаления содержал менее чем 1% (например, менее чем 0,5%, 0,1%, например, менее чем 0,05%, менее чем 0,01%) по массе несмешивающегося с водой органического растворителя.
Во избежание сомнений, в контексте стадии (v), ссылки на удаление органической фазы, такой как несмешивающийся с водой органический растворитель, будут относиться к удалению любых таких растворителей, как определено в данном документе (например, удаление дихлорметана или трет-бутилметилового эфира). Если присутствуют другие органические растворители (например, те, которые не смешиваются с водой, например, избыток 1,2-пропандиола и/или 1,3-пропандиола, действующего как растворитель), часть таких растворителей также может быть удалена (например, вместе с несмешивающимся с водой органическим растворителем).
В контексте стадий (vi), ссылки на сушку продукта относятся к удалению воды из материала, оставшегося после предыдущих стадий. Такое удаление воды может относиться к удалению таким образом, чтобы продукт после такой сушки содержал менее 1% (например, менее чем 0,5% или менее чем 0,1%, например, менее чем 0,05% или менее чем 0,01%) по массе воды.
Квалифицированному специалисту будет понятно, что стадия (vi) может быть выполнена любым пригодным для этого способом и с применением любого пригодного оборудования, известного в данной области техники (например, путем приведения в контакт оставшейся органической фазы с пригодным осушающим агентом, таким как безводный сульфат натрия, безводный магний. сульфатные и/или молекулярные сита).
Конкретные способы по данному изобретению, которые могут быть упомянуты, включают те, в которых указанный способ дополнительно включает стадию (например, после стадии (i) и, если присутствуют, других стадий, как описано в данном документе) добавления дополнительного количества соответствующего соединения формулы I, но где R1, R2 и R3 представляют собой H (то есть 1,2-пропандиол и/или 1,3-пропандиол), так что комбинированная смесь одного или большего количества соединений формулы I и соответствующих соединений формулы I, но где R1, R2 и R3 представляют собой H (то есть 1,2-пропандиол и/или 1,3-пропандиол) составляет от около 0,01% до около 9% (например, от около 0,01% до около 5%, например, от около 3% до около 5% или от около 5% до около 7%) по массе одного или большего количества соединений по данному изобретению.
Как указано выше, все варианты осуществления данного изобретения и конкретные признаки, упомянутые в данном документе, могут быть взяты отдельно или в сочетании с любыми другими вариантами осуществления и/или конкретными признаками, упомянутыми в данном документе (следовательно, описывая более конкретные варианты осуществления и конкретные признаки, как описано в данном документе), в пределах объема изобретения.
Например: стадия (i) указанного способа, выполняемая при температуре от около -30 °C до около 5 °C, может быть объединена с особенностью стадий (ii) - (iv) указанного способа, и может выполняться при температуре от около -20 °C до около 5 °C; при этом особенностью стадии (v) указанного способа является то, что она проводится при температуре от около 0 °C до около 30 ° C; и/или то, что стадия (v) указанного способа проводится не более 6 часов.
Более конкретные способы, которые могут быть упомянуты, включают те, в которых указанные параметры соответствуют приведенным в данном документе примерам.
Конкретный продукт способа по данному изобретению представляет собой соединение формулы (II).
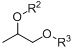 (II)
(II)
где R2 и R3 каждый независимо представляют собой H или -NO, при условии, что по меньшей мере один из R2 и R3 представляет собой -NO, при этом указанный способ включает стадию взаимодействия 1,2-пропандиола (то есть исходного материала) с источником нитрита в условиях, как описано в данном документе (включая все его варианты осуществления).
Существуют два энантиомера соединения формулы (II), которые представляют собой R- и S- формы, как показано ниже:
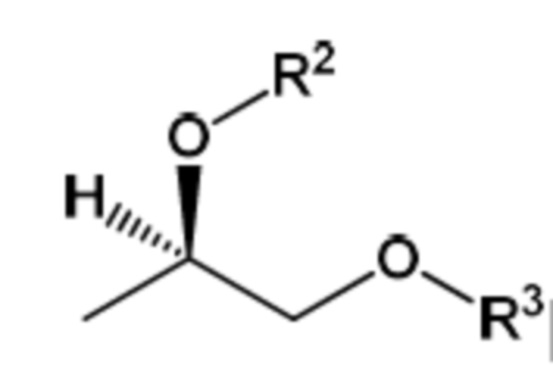 (II) R-форма
(II) R-форма
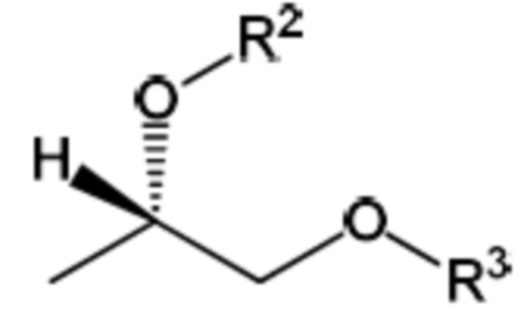 (II) S-форма
(II) S-форма
Еще одним конкретным продуктом способа по данному изобретению является соединение формулы (III), как показано ниже:
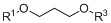 (III)
(III)
где R1 и R3 каждый независимо представляют собой H или -NO, при условии, что по меньшей мере один из R1 и R3 представляет собой -NO, при этом указанный способ включает стадию взаимодействия 1,3-пропандиола с источником нитрита.
Два конкретных процесса, описанных выше для получения соединений формулы (II) и (III), можно проводить вместе или независимо друг от друга.
Основываясь на имеющейся двухфазной природе реакционной смеси, необязательное добавление катализатора межфазного переноса (PTC) может способствовать образованию продукта. Обычными PTC являются, например, помимо прочего, ионы тетраалкиламмония, такие как Me4N+, Et4N+, Bu4N+, или Bu3(N+)CH2PHCl,, с противоионами, такими как = Cl-, Br-, HSO4-, или другие типы алкиламмониевых PTC, такие как Aliquat® 336, в субстехиометрических количествах < 1 эквивалента, например, но не исключительно, в диапазоне от около 0,05 до около 40 мол.%, например, от около 0,1 до около 30 мол.%, например, от около 0,1 до около 20 мол.%.
Еще одним конкретным продуктом способа по данному изобретению является соединение формулы (IV), как показано ниже.
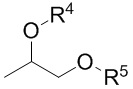 (IV)
(IV)
где R4 и R5 каждый независимо представляют собой H или -NO, при условии, что по меньшей мере один из R4 и R5 представляет собой -NO.
Таким образом, конкретный способ изобретения предназначен для приготовления композиции, содержащей одно или большее количество соединений формулы IV.
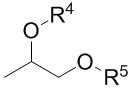 (IV)
(IV)
где R4 и R5 каждый независимо представляют собой H или -NO, при условии, что по меньшей мере один из R4 и R5 представляет собой -NO.
указанный способ включает стадию:
(i) взаимодействия 1,2-пропандиола с источником нитрита, необязательно в присутствии пригодной кислоты,
при этом:
(а) когда источником нитрита является органический нитрит, стадию (i) выполняют в пригодном органическом растворителе; а также
(b) когда источником нитрита является неорганический нитрит, стадию (i) выполняют в двухфазной смеси растворителей, содержащей водную фазу и неводную фазу.
Любой из этапов способа, описанных в данном документе, может быть объединен с конкретным способом, описанным выше в отношении формулы (IV), и при этом конкретные варианты осуществления изложены ниже.
В конкретном способе, неорганический нитрит представляет собой нитрит металла, необязательно, при этом нитрит металла представляет собой нитрит щелочного металла или нитрит щелочноземельного металла, предпочтительно нитрит щелочного металла.
В конкретном варианте осуществления данного изобретения, нитрит щелочного металла представляет собой нитрит натрия.
В другом конкретном варианте осуществления данного изобретения, органический нитрит представляет собой алкилнитрит, такой как трет-бутилнитрит.
В конкретном способе, пригодной кислотой является сильная кислота, такая как сильная минеральная кислота (например, серная кислота).
В конкретном варианте осуществления данного изобретения, неводная фаза включает несмешивающийся с водой органический растворитель, такой как несмешивающийся с водой апротонный органический растворитель.
В одном из вариантов осуществления данного изобретения, несмешивающийся с водой органический растворитель представляет собой дихлорметан.
В конкретном способе, смесь растворителей дополнительно содержит избыток 1,2-пропандиола.
В дополнительном конкретном способе, после стадии (i) указанный способ дополнительно включает стадию:
(ii) удаления по существу всей водной фазы из смеси растворителей.
В одном из вариантов осуществления данного изобретения, после стадии (i) указанный процесс дополнительно включает стадию (стадии):
(ii) удаления части или всей (например, по существу всей) водной фазы (то есть
воды);
(iii) промывания оставшейся органической фазы одной или большим количеством дополнительных водных фаз;
(iv) необязательно повторение стадий (ii) и (iii) один или большее количество раз;
(v) необязательного уменьшения (то есть уменьшение количества/объема) органической фазы,
а также
(vi) необязательной сушки продукта,
при этом стадии (ii) - (vi) могут выполняться в любом порядке при условии, что стадии (ii) - (iv) выполняются перед стадиями (v) и (vi).
В конкретном варианте осуществления данного изобретения, указанный способ дополнительно включает стадию добавления дополнительного количества 1,2-пропандиола, так что комбинированная смесь одного или большего количества соединений формулы I и 1,2-пропандиола содержит от около 0,01% до около 9 мас.% одного или большего количества соединений формулы IV.
Продукты и композиции
Во втором аспекте данного изобретения предлагается продукт, полученный с помощью (например, продукт, полученный или получаемый с помощью) способа по данному изобретению (то есть произведенный в соответствии с первым аспектом данного изобретения, включая все варианты осуществления и конкретные признаки), при этом полученные продукты в дальнейшем могут называться «соединениями по данному изобретению».
Соединения по данному изобретению могут содержать асимметричный атом углерода, как указано выше, и поэтому будут проявлять оптическую изомерию. Различные стереоизомеры могут быть выделены путем разделения рацемической или другой смеси соединений с помощью традиционных методов, например фракционной кристаллизации или ВЭЖХ. В альтернативном варианте, желаемые оптические изомеры могут быть получены в результате реакции соответствующих оптически активных исходных материалов в условиях, которые не вызывают рацемизацию (то есть метод «хирального пула»), путем реакции пригодного исходного материала с «хиральным вспомогательным веществом», которое впоследствии может быть удалено на подходящей стадии путем дериватизации (то есть разделения, включая динамическое разделение; например, с помощью гомохиральной кислоты с последующим разделением диастереомерных производных обычными способами, такими как хроматография), или путем реакции с пригодным хиральным реагентом или хиральным катализатором, в условиях, известных квалифицированному специалисту в данной области техники. Все стереоизомеры и их смеси включены в объем данного изобретения.
Способы по данному изобретению преимущественно позволяют получать по существу неводные композиции, содержащие одно или большее количество соединений по данному изобретению. В частности, способы по данному изобретению допускают относительно высокие концентрации одного или большего количества соединений по данному изобретению в композиции, тем самым обеспечивая простоту обращения и минимизируя объемы хранения и транспортные расходы.
Соответственно, в третьем аспекте данного изобретения предлагается по существу неводная композиция, содержащая:
(а) одно или большее количество соединений формулы I, как определено в данном описании; а также
(b) одно или большее количество соответствующих соединений формулы I, но где R1, R2 и R3 представляют собой H (например, 1,2-пропандиол и/или 1,3-пропандиол),
при этом эти композиции могут упоминаться в дальнейшем как «по существу неводные композиции по данному изобретению».
Квалифицированному специалисту будет понятно, что ссылки в данном документе на по существу неводные композиции изобретения будут включать ссылки на все варианты осуществления и их конкретные формы.
В данном контексте ссылки на «по существу неводный» будут относиться к компоненту, содержащему менее чем 1% (например, менее чем 0,5% или менее чем 0,1%, например, менее чем 0,05%, менее чем 0,01%) по массе воды.
Конкретные по существу неводные композиции изобретения, которые можно упомянуть, включают те, в которых композиция содержит от около 0,01% до около 9% (например, от около 0,01% до около 5%, например, от около 3% до около 5% или от около 5% до около 7%) по массе одного или большего количества соединений по данному изобретению (то есть соединений формулы I).
Конкретные по существу неводные композиции изобретения, которые можно упомянуть, включают те, в которых композиция содержит соединение формулы (II). Предпочтительно соединение формулы (II) представляет собой S-форму.
S-форма соединения формулы (II) является предпочтительной, поскольку она имеет более высокую скорость метаболизма по сравнению с R-формой. Кроме того, S-форма имеет другой путь метаболического расщепления, в результате чего метаболиты менее токсичны по сравнению с метаболитами R-формы.
Конкретные по существу неводные композиции изобретения, которые можно упомянуть, включают те, в которых композиция содержит соединение формулы (III).
Предпочтительно соединение формулы (II) представляет собой S-форму, хотя предполагается, что продукт представляет собой смесь как S-, так и R-формы формулы (II), при этом S-форма предпочтительно присутствует в энантиомерном избытке (ee).
В конкретных вариантах осуществления данного изобретения, когда продукт способа представляет собой соединение формулы (II), соединение формулы (II) может находиться в энантиомерном избытке S-формы указанного соединения. То есть больше чем 50 ее% продукта находится в S-форме, например, больше или равно 60 ее%, 70 ее%, 80 ее%, 90 ее%, 95 ее% или 98 ее% продукта находится в S-форме.
Чтобы достичь энантиомерного избытка S-формы соединения (II), в одном варианте осуществления данного изобретения исходный материал (то есть 1-2 пропандиол) может присутствовать в энантиомерном избытке S-формы. То есть больше чем или равно 50 ее% исходного материала (то есть 1-2 пропандиола) находится в S-форме, например, больше чем или равно 60 ее%, 70 ее%, 80 ее%, 90 ее%, 95 ее% или 98 ее% исходного материала находится в S-форме.
В варианте осуществления данного изобретения, когда продукт представляет собой мононитрозилированное соединение в соответствии с формулой (II), более 50 мас.% продукта нитрозилировано в положении 2 (то есть R2 представляет собой -NO), например, от около 55 мас. % до около 80 мас.% нитрозилировано в положении 2, например, между от около 55 мас.% до 75 мас.%.
Конкретные по существу неводные композиции по данному изобретения, которые можно упомянуть, включают те, в которых указанная композиция состоит по существу из одного или большего количества соединений формулы I и соответствующих соединений формулы I, но где R1, R2 и R3 представляют собой H (то есть 1, 2-пропандиол и/или 1,3-пропандиол).
В частности, когда исходным материалом является 1,2-пропандиол, то по существу неводные композиции по данному изобретению могут содержать (или, в частности, состоять в основном из или, более конкретно, состоять из) одно или большее количество соединений формулы II и 1,2-пропандиол.
Равным образом, когда исходный материал представляет собой 1,3-пропандиол, тогда по существу неводные композиции по данному изобретению могут содержать (или, в частности, состоять в основном из или, более конкретно, состоять из) одно или большее количество соединений формулы III и 1,3-пропандиол.
Под термином «в основном состоит из» следует понимать, что присутствует по меньшей мере 90 мас.% определенного признака, например, по меньшей мере 95 мас.%, 96 мас.%, 97 мас.%, 98 мас.% или 99 мас.% определенного признака.
Кроме того, конкретные по существу неводные композиции по данному изобретению, которые можно упомянуть, включают те, в которых указанная композиция содержит (или, в частности, состоит в основном из или, более конкретно, состоит из) одно или большее количество соединений формулы (II) и (III). наряду с 1,2-пропандиолом и 1,3-пропандиолом.
Конкретные по существу неводные композиции по данному изобретению, которые можно упомянуть, включают те, в которых указанная композиция по существу не содержит растворенного оксида азота.
Под термином «по существу не содержит» следует понимать, что неводные композиции по данному изобретению содержат менее чем 5 мас.%, 4 мас.%, 3 мас.%, 2 мас.% или 1 мас.% растворенного оксида азота, например, менее чем 0,5 мас.% или 0,1 мас.%.
Кроме того, конкретные по существу неводные композиции изобретения могут содержать:
а) одно или большее количество соединений формулы IV
 (IV)
(IV)
где R4 и R5 каждый независимо представляют собой H или -NO, при условии, что по меньшей мере один из R4 и R5 представляет собой -NO; а также
(b) 1,2-пропандиол.
Соединения по данному изобретению и по существу неводные композиции по данному изобретению являются пригодными в качестве фармацевтических препаратов. Такие соединения можно вводить сами по себе или можно вводить с помощью известных фармацевтических композиций/составов.
Соответственно, в четвертом аспекте предлагается фармацевтический состав, содержащий по существу неводную композицию по данному изобретению и, необязательно, один или большее количество фармацевтически приемлемых вспомогательных веществ, которые в дальнейшем могут упоминаться как «фармацевтические составы по данному изобретению».
Квалифицированному специалисту будет понятно, что ссылки в данном документе на фармацевтические составы по данному изобретению будут включать ссылки на все варианты осуществления и их конкретные формы.
В данном контексте термин «фармацевтически приемлемые вспомогательные вещества» включает ссылки на носители, адъюванты, разбавители, вещества, регулирующие рН, и буферные агенты, агенты, регулирующие тоничность, стабилизаторы, смачивающие агенты и тому подобное. В частности, такие вспомогательные вещества могут включать адъюванты, разбавители или носители.
Конкретные фармацевтические составы по данному изобретению, которые можно упомянуть, включают те, в которых фармацевтический состав содержит по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
Конкретные фармацевтические составы по данному изобретению, которые можно упомянуть, включают те, в которых один или большее количество фармацевтически приемлемых вспомогательных веществ являются по существу неводными.
Во избежание сомнений, ссылки в данном документе на соединения по данному изобретению, предназначенные для конкретных применений (и, аналогично, на применения и способы применения, относящиеся к соединениям по данному изобретению), также могут относиться к композициям и фармацевтическим составам, содержащим соединения по данному изобретению, как описано в данном документе.
Неожиданно было обнаружено, что соединения по данному изобретению можно вводить пациену (то есть субъекту) в сочетании с пригодным водным буфером. В частности, неожиданно было обнаружено, что соединения по данному изобретению являются пригодно стабильными (например, не подвергаются значительному расщеплению в течение по меньшей мере 15 минут) в водных буферах, более конкретно, в которых водный буфер является ненуклеофильным и слабоосновным.
Согласно пятому аспекту данного изобретения предлагается набор составных элементов, содержащий:
(А) фармацевтический состав согласно данному изобретению (то есть согласно четвертому аспекту данного изобретения, включая все варианты его осуществления и конкретные признаки); а также
(В) пригодный водный буфер,
при этом компоненты (А) и (В) представлены в форме, пригодной для введения друг с другом,
и такие наборы составных элементов в дальнейшем именуются «наборами составных элементов по данному изобретению».
Конкретные варианты осуществления данного изобретения, которые следует упомянуть, включают те, в которых буфер является ненуклеофильным и слабоосновным.
Более конкретные варианты осуществления данного изобретения, которые можно упомянуть, включают те, в которых буфер имеет pH от около 7,1 до около 10 (например, около 8 или около 9,2), такой как карбонатный (например, NaHCO3 , который может иметь рН около 7,4 или около 8,0) буфер или физиологический фосфатный буфер (необязательно с pH 8), или их смесь. В качестве буфера также можно применять физиологический солевой раствор.
В частности, буфер может быть буфером, который применяется в Примере 5, как описано ниже, например, карбонатным буфером с pH 9,2 или фосфатным буфером с pH 8,0 (например, 0,154 молярным буфером) или буфером NaHCO3 с pH 8,0.
Согласно шестому аспекту данного изобретения предлагается комбинированный продукт, полученный путем смешивания:
(А) фармацевтического состава по данному изобретению (то есть согласно четвертому аспекту данного изобретения, включая все варианты его осуществления и конкретные признаки); и
(В) пригодного водного буфера, как определено в пятом аспекте данного изобретения (включая все варианты его осуществления и конкретные признаки),
и такой комбинированный продукт в дальнейшем именуется «комбинированным продуктом по данному изобретению».
Согласно седьмому аспекту данного изобретения предлагается способ получения комбинированного продукта по данному изобретению (то есть согласно шестому аспекту данного изобретения, включая все его варианты осуществления и конкретные признаки), включающий стадию смешивания:
(А) фармацевтического состава по данному изобретению (то есть согласно четвертому аспекту данного изобретения, включая все варианты его осуществления и конкретные признаки); и
(В) пригодного водного буфера, как определено в пятом аспекте данного изобретения (включая все варианты его осуществления и конкретные признаки),
Конкретные наборы составных элементов и комбинированные продукты по данному изобретению, которые можно упомянуть, включают те, в которых соотношение фармацевтического состава по данному изобретению и пригодного водного буфера составляет от около 1:2 до 1:99 или от около 3:7 до 1:99 (например, от 1:3 до 1:99) по объему.
В альтернативном варианте, наборы составных элементов по данному изобретению, которые могут быть упомянуты, включают те, в которых указанный набор содержит инструкции по смешиванию компонентов (например, перед введением, например, с применением описанных в данном документе методик), так что соотношение фармацевтического состава по данному изобретению и пригодного водного буфера составляет от около 3:7 до 1:99 (например, от около 1:3 до 1:99) по объему.
Клиническое применение
Как обсуждалось выше, соединения по данному изобретению, неводные композиции по данному изобретению, фармацевтические составы по данному изобретению и, следовательно, наборы составных элементов и комбинированные продукты, содержащие их, являются пригодными для лечения патологических состояний, при которых введение NO имеет полезный эффект.
Согласно восьмому аспекту данному изобретения предлагается неводная композиция, как определено выше (то есть согласно третьему аспекту данного изобретения, включая все варианты его осуществления и конкретные признаки), фармацевтический состав, как определено выше (то есть согласно четвертому аспекту данного изобретения, включая все варианты его осуществления и конкретные признаки), набор составных элементов, как определено выше (то есть согласно пятому аспекту данного изобретения, включая все варианты его осуществления и конкретные признаки), или комбинированный продукт, как определено выше (то есть согласно шестому аспекту данного изобретения, включая все варианты его осуществления и конкретные признаки) для применения при лечении патологического состояния, при котором введение NO имеет полезный эффект.
В альтернативном восьмом аспекте данного изобретения предлагается способ лечения патологического состояния, при котором введение NO имеет положительный эффект, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества фармацевтического состава по данному изобретению или комбинированного продукта по данному изобретению.
В дополнительном альтернативном восьмом аспекте данного изобретения предлагается способ лечения патологического состояния, при котором введение NO имеет положительный эффект, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества следующих компонентов:
(А) фармацевтического состава по данному изобретению (то есть согласно четвертому аспекту данного изобретения, включая все варианты его осуществления и конкретные признаки); и
(В) пригодного водного буфера, как определено в пятом аспекте данного изобретения (включая все варианты его осуществления и конкретные признаки),
Конкретные способы, которые можно упомянуть, включают те, в которых смешивание компонентов (А) и (В) выполняется непосредственно перед введением пациенту, например, путем их совместного введения.
Авторы настоящего изобретения обнаружили, что введение соединений по данному изобретению может привести к повреждению клеток крови посредством гемолиза из- за осмотического стресса, но эти эффекты можно контролировать или избежать их путем введения соединения по данному изобретению в пригодном водном буфере.
Более конкретные способы, которые могут быть упомянуты, включают те, в которых смешивание выполняется в процессе смешанного потока, например, в момент введения пациенту. Еще более конкретные способы, которые можно упомянуть, включают те, в которых процесс смешанного потока представляет собой внутривенную инфузию с применением Y-образного соединителя.
Квалифицированному специалисту будет понятно, что ссылки на лечение конкретного патологического состояния (или, аналогично,для лечения этих патологических состояний)) имеют свои обычные значения, принятые в области медицины. В частности, указанные термины могут относиться к достижению снижения тяжести одного или большего количества клинических симптомов и/или признаков, ассоциированных с этим патологическим состоянием. Например, в случае тромбоэмболии легочной артерии этот термин может относиться к достижению уменьшения тяжести боли в груди, одышки и/или легочной гипертензии за счет расширения сосудов.
В данном контексте ссылки на пациентов будут относиться к живому субъекту, получающему лечение, включая пациентов-млекопитающих (например, людей). В частности, термин «пациент» может относиться к субъекту-человеку. Термин «пациент» может также относиться к животным (например, млекопитающим), таким как домашние животные (например, кошки и, в частности, собаки), домашний скот и лошади.
В данном контексте термин эффективное количество будет относиться к количеству соединния, которое оказывает терапевтический эффект на пролеченного пациента. Эффект может быть объективным (то есть измеряемым с помощью какого-либо теста или маркера) или субъективным (то есть субъект сам определяет и указывает на эффект и/или его ощущения).
Как указано в данном документе, фармацевтические составы по данному изобретению могут быть полезны при лечении патологического состояния, при котором введение NO имеет положительный эффект.
Конкретные состояния, которые можно упомянуть, включают состояния, выбранные из группы, состоящей из: острого сужения легочных сосудов различного генеза; легочной гипертензии различного генеза, в том числе первичной гипертензии и вторичной гипертензии; патологических состояний разного генеза, требующих расширения сосудов; системной гипертензии различного генеза; регионарного сужения сосудов разного генеза; местного сужения сосудов разного генеза; острой сердечной недостаточности (с сохраненной или несохраненной фракцией выброса (HFpEF)); коронарного заболевания сердца; инфаркта миокарда; ишемической болезни сердца; стенокардии; нестабильной стенокардии; аритмии сердца; острой легочной гипертензии у кардиохирургических пациентов; ацидоза; воспаления дыхательных путей; муковисцидоза; ХОЗЛ; синдрома дискинезии ресничек; воспаления легких; легочного фиброза; респираторного дистресс-синдрома взрослых; острого отека легких; острой горной болезни; астмы; бронхита; гипоксии разного генеза; инсульта; сужения сосудов головного мозга; воспаления желудочно-кишечного тракта; нарушения функции желудочно-кишечного тракта; желудочно-кишечных осложнении; ВЗК; болезни Крона; язвенного колита; болезни печени; заболевания поджелудочной железы; воспаления мочевого пузыря уретрального тракта; воспаления кожных покровов; диабетических язв; диабетической невропатии; псориаза; воспаления разного генеза; заживления раны; защиты органов в условиях ишемии-реперфузии; трансплантации органов; трансплантации тканей; трансплантации клеток; острой болезни почек; релаксации матки; релаксации шейки матки; заболеваний глаз, таких как глаукома, а также состояний, при которых требуется релаксация гладких мышц.
Более конкретные состояния, которые могут быть упомянуты, включают легочную гипертензию различного генеза, включая первичную гипертензию и вторичную гипертензию, острую сердечную недостаточность (с сохраненной или несохраненной фракцией выброса (HFpEF)). Например. Патологическое состояние может представлять собой легочную гипертензию после хирургического вмешательства.
Легочная гипертензия определяется как повышение среднего давления в легочной артерии (mPAP) до уровня 20 мм рт. ст. или выше в покое в сочетании со значением Wood Units > 3.
Квалифицированный специалист сможет определить, каким способом можно вводить фармацевтические составы вместе с пригодными буферами, как описано в данном документе, с целью лечения. В частности, описанные в данном документе комбинации фармацевтических составов и буферов можно вводить внутривенно или внутриартериально.
Квалифицированный специалист сможет определить подходящую дозу активных ингредиентов для применения в лечении на основе характеристик применяемой композиции (например, комбинация фармацевтического состава и пригодного буфера, как описано в данном документе), патологического состояния, которое подлежит лечению, а также состояния здоровья (например, течение болезни) пациента. Например, при внутривенном или внутриартериальном введении взрослому человеку подходящая доза может составлять от около 0,5 до около 3000 нмоль/кг/мин, например, от около 1 до около 3000 нмоль/кг/мин, например, от около 5 до около 3000 нмоль/кг/мин соединения (соединений) формулы I. Такие дозы можно вводить путем инфузии (непрерывной или импульсной), такой как инфузия в течение длительного периода времени (например, от 1 до 2 часов или даже до одной недели), или можно вводить в виде разовой (болюсной) дозы (такой как единичная доза или разовая доза на одно лечебное вмешательство, например, разовая доза, если требуется, или разовая доза каждые 24 часа во время лечения).
Квалифицированному специалисту будет понятно, что температура, при которой составы по данному изобретению (то есть фармацевтические композиции, содержащие соединения формулы I) составляются и/или вводятся при лечении (то есть вводятся субъекту), может соответствовать температуре окружающей среды, в которой происходит введение (то есть комнатная температура) или может контролироваться. Например, такие составы можно составлять и/или вводить при комнатной температуре или при пониженной температуре (то есть температура ниже комнатной), например, от около 0 до около 25 °C.
В конкретных вариантах осуществления данного изобретения, соединения формулы (II) имеют особое значение для применения у людей, а соединения формулы (III) имеют особое значение для применения в ветеринарии.
Не желая быть связанными теорией, следует отметить, что при введении пациенту соединения формулы I гидролизуются с высвобождением оксида азота, что обеспечивает желаемый терапевтический эффект. Отмечается, что описанные в данном документе способы неожиданно позволили получить пригодную концентрированную и стабильную композицию, содержащую требуемые активные ингредиенты. Кроме того, считается, что неожиданно был обнаружен определенный тип буфера, позволяющий безопасно вводить такие композиции без значительного разложения активного ингредиента (ов).
Краткое описание графических материалов
Фигура 1: демонстрирует результаты анализа стабильности композиций по данному изобретению в различных буферных растворах, как описано в Примере 5 данного документа.
Фигура 2: демонстрирует результаты исследования in vivo, сравнивающего эффекты лечения композиций по данному изобретению с ингаляционным оксидом азота, как описано в Примере 6 данного документа. Изменение среднего давления в легочной артерии (MPAP, панель a) и легочного сосудистого сопротивления (PVR, панель c), а также среднего артериального давления (MAP, панель b), системного сосудистого сопротивления (SVR, панель d) и концентрации метгемоглобина в анестезированных и механически вентилируемых свиней, получивших внутривенную инфузию PDNO (15, 30, 45 и 60 нмоль кг-1 мин-1 в потоке носителя бикарбоната натрия [50 мг мл-1 ; при скорости инфузии, в 10 раз превышающей скорость инфузии PDNO] n = 6) или ингаляцию NO (5, 10, 20 и 40 ppm; n = 7) во время внутривенной инфузии легочного вазоконстриктора U46619 (60-150 нг кг-1 мин-1 ). Дозу ингаляционного NO переводили в нмоль кг-1 мин-1 . Ось x отложена в логарифмической шкале. Данные представлены в виде медианы и межквартильного диапазона. * указывает на статистически значимый эффект указанной дозы только от U46619 в каждом препарате.φ указывает на статистическую разницу между PDNO в дозе 45 нмоль кг-1 мин-1 и ингаляционным NO при 5 ppm, то есть сравнимым количеством доставки NO.
На Фигуре 3 продемонстрированы результаты применения 1,2-PDNO-R, 1,2-PDNO-S и 1,3-PDNO для снижения среднего системного артериального давления и среднего давления в легочной артерии, с экспериментальной процедурой, описанной в Примере 13.
Примеры
Данное изобретение иллюстрируется следующими примерами, которые не предназначены для ограничения общего объема изобретения.
Список сокращений
водн водный
конц концентрация
ГХ газовая хроматография
ЯМР ядерный магнитный резонанс
эквив. эквивалент(ы)
отн. об. относительный объем (объемы)
Общие процедуры
Исходные материалы и химические реагенты, указанные для описанных ниже препаратов, коммерчески доступны у ряда поставщиков, таких как Sigma Aldrich.
Все эксперименты ЯМР проводили при 298 К на приборе Bruker 500 МГц AVI, оборудованном головкой зонда QNP с Z-градиентами, с применением программного обеспечения Bruker Topspin 2.1. Сигналы относятся к остаточному CHCl3 при 7,27 ppm, если не указано иное.
Анализы стабильности
Анализы образцов на стабильность проводили с помощью ГХ/FID в следующих условиях. 1,4-Диоксан применяли в качестве внутреннего стандарта (IS; приблизительно 0,50 мг/мл в CH3CN).
Колонка для ГХ: Rxi-5Sil MS, 20 м × 0,18 мм, 0,72 мкм
Газ-носитель: гелий
Вход: 200 °C, отношение деления потока 30:1
Постоянный поток: 1,0 мл/мин
Температурный профиль печи: 40 °C (3 мин.), 10 °C/мин., 250 °C (3 мин.)
FID: температура 300 °C; поток H2 30 мл/мин, поток воздуха 400 мл/мин, поток вспомогательного газа (N2) 25 мл/мин
Исследования in vivo
Перед проведением эксперимента было получено этическое одобрение от регионального комитета по этике животных Линчепинга (Линчепинг, Швеция; номер одобрения 953). Недавно были описаны анестезиологическое сопровождение, хирургическое вмешательство и методы измерения (Dogan et al. 2018, Sadeghi et al. 2018).
Вкратце, 8 самцов и самок свиней (помесь шведской деревенской породы, Хэмпшир и Йоркшир; возраст 3-4 месяца; средняя масса тела 27 кг, диапазон 21-34 кг) получили премедикацию азапероном на ферме и были доставлены в лабораторию. В лаборатории проводили анестезию смесью тилетамина, золазепама и азаперона (внутримышечная инъекция). При необходимости вводили пропофол через периферический венозный катетер в ушную вену. Болюсные дозы атропина и цефуроксима вводили внутривенно. Животных интубировали эндотрахеально и подвергали механической вентиляции (5 см H2O при положительном давлении в конце выдоха, минутная вентиляция была доведена до нормовентиляции). Общую анестезию поддерживали пропофолом и фентанилом посредством непрерывных внутривенных инфузий, при необходимости вводили дополнительные болюсные дозы. Растворы ацетата Рингера и глюкозы непрерывно вводили внутривенно, чтобы восполнить потерю жидкости. После хирургического вмешательства внутривенно болюсно вводили гепарин. После экспериментов животных умерщвляли под общей анестезией посредством инъекции пропофола с последующей быстрой внутривенной инъекцией хлорида калия (40 ммоль), и подтверждали асистолию.
Животным вводили артериальный катетер в правую сонную артерию для измерения системного артериального кровяного давления и частоты сердечных сокращений, а также для отбора проб артериальной крови. В правую наружную яремную вену помещали интродьюсер для введения легочно-артериального катетера. Этот катетер применяли для непрерывного измерения артериального кровяного давления в легочной артерии, полунепрерывного сердечного выброса и интермиттирующего давления заклинивания в легочной артерии. Центральный венозный катетер вставляли в левую наружную яремную вену для введения лекарственного препарата и жидкости. Все введения жидкости и лекарственного препарата осуществляли с помощью моторизованных шприцев или капельных насосов. Катетеризовали мочевой пузырь. Показатели дыхательных газов, давления и объемов измеряли на интубационной трубке. Респираторные и гемодинамические параметры измеряли с помощью Datex AS/3 (Хельсинки, Финляндия), а данные собирали с помощью компьютеризированной системы (MP150/Acknowledge 3.9.1, системы BIOPAC, Goleta, штат Калифорния, США). Показатели газов крови и концентрацию метгемоглобина измеряли с помощью прибора для определения газов крови (GEM 4000, Instrumental Laboratory, Lexington, штат Массачусетс, США). Легочное и системное сосудистое сопротивление рассчитывали по стандартной формуле. После хирургической операции следовал 1-часовой период без какого-либо вмешательства.
Из-за ненормального распределения данные представляли в виде медианы и межквартильного диапазона. Доза ppm вдыхаемого NO преобразовывали в дозу в нмоль кг-1 мин-1 с помощью закона идеального газа и минутной вентиляции и при условии полного поглощения NO легкими. Данные о лекарственном препарате анализировали с помощью критерия Фридмана с критерием знаковых рангов Уилкоксона для апостериорных множественных сравнений. U-критерии Манна-Уитни применяли для сравнения лекарственных препаратов в максимальной дозе и в дозе схожей доставки NO (45 нмоль кг-1 мин-1 PDNO и 5 ppm ингаляционного NO). Критическое P значение 0,05 применяли и корректировали с помощью пошаговой процедуры Бенджамини-Хохберга при множественных сравнениях.
Пример 1 - Приготовление 1-(нитрозоокси)пропан-2-ола, 2- (нитрозоокси)пропан-1-ола и 1,2-бис(нитрозоокси)пропана с нитритом натрия
1,2-пропандиол (15 мл, 205 ммоль), воду (100 мл), дихлорметан (200 мл) и нитрит натрия (57 г, 826 ммоль) добавляли в трехгорлую круглодонную колбу на 500 мл. Смесь охлаждали до 0 °C на ледяной бане. Концентрированную серную кислоту (30 мл, 546 ммоль) и воду (30 мл) добавляли в капельную воронку и охлаждали до 5 °C в холодильнике. Воронку приспособляли к круглодонной колбе, и добавляли кислоту к нитритной смеси в течение двух часов. Смесь перемешивали с помощью магнита в течение 20 минут, а затем выливали в делительную воронку вместе с дополнительным количеством дихлорметана (100 мл) и воды (100 мл). Органическую фазу отделяли и сушили сульфатом натрия и восстанавливали на роторном испарителе с получением смеси 1,2-пропандиола (3 мас.%), 1-(нитрозоокси)пропан-2-ола (23 мас.%). 2-(нитрозоокси)пропан-1-ола (13 мас.%) и 1,2-бис(нитрозоокси)пропана (57 мас.%).
Пример 2 - Приготовление 1-(нитрозоокси)пропан-2-ола, 2- (нитрозоокси)пропан-1-ола и 1,2-бис(нитрозоокси)пропана с нитритом натрия.
1,2-пропандиол (20 мл, 273,4 ммоль), воду (60 мл), дихлорметан (120 мл) и нитрит натрия (37,72 г, 546,7 ммоль) добавляли в реактор 0,5, снабженный мешалкой, продували азотом и выдерживали в ходе следующей реакции в атмосфере азота. Смесь охлаждали до температуры ниже 5 °C путем охлаждения кожуха до 0 °C. В капельную воронку добавляли концентрированную серную кислоту (26,3 г, 260,1 ммоль) и воду. Воронку присоединяли к реактору и кислоту добавляли к нитритной смеси в течение 33 минут. Смесь перемешивали в течение 54 минут и затем выливали в колбу, содержащую насыщенный водный раствор бикарбоната натрия (100 мл). Смесь переносили в делительную воронку и промывали органическую фазу. Водную фазу отбрасывали, а органическую фазу промывали дополнительным водным насыщенным раствором бикарбоната натрия (100 мл). Органическую фазу сушили сульфатом магния и затем переносили в круглодонную колбу на 1 л вместе с 1,2-пропандиолом (120 мл, 1640 ммоль). Раствор упаривали на роторном испарителе при пониженном давлении до удаления дихлорметана. Удаление дихлорметана контролировали с помощью ЯМР. Получали прозрачный раствор (134 г), содержащий 1,2-пропандиол (82,8 мас.%), 1-(нитрозоокси)пропан-2-ол (10,4 мас.%), 2-нитрозоокси)-пропан-1-ол (6 мас.%) и 1,2-бис(нитрозоокси)пропан (0,8 мас.%).
1H-ЯМР, δ ppm: 5.61 (br s 1H), 4.75-5.58 (m, 2H), 4.11 (br s, 1H), 3.90-3.87 (m, 1H), 3.83-3.69 (m, 2H), 3.60 (dd, J = 3.0, 11.2 Hz, 1H), 3.38 (dd, J = 7.9, 11.2 Hz, 1H),1. 47 (d, J = 6.6 Hz, 3H), 1. 39 (d, J = 6.4 Hz, 3H), 1.26 (d, J = 6.4 Hz, 3H), 1.15 (d, J = 6.3 Hz, 3H), сигналы для CH и CH2 1,2-бис(нитрозоокси)пропана были ниже предела обнаружения.
Пример 3 - Приготовление 1-(нитрозоокси)пропан-2-ола, 2-(нитрозоокси)пропан-1-ола и 1,2-бис(нитрозоокси)пропана с трет-бутилнитритом.
Трет-бутилнитрит (2 мл, 15,1 ммоль) добавляли в круглодонную колбу с 1,2-пропандиолом (11 мл, 150,3 ммоль) и полученный раствор перемешивали при температуре окружающей среды. Затем 1 мл реакционного раствора смешивали с 7,5 мл 1,2-пропандиола.
Пример 4 - Стабильность неводных смесей 1-(нитрозоокси)пропан-2-ола, 2-(нитрозоокси)пропан-1-ола и 1,2-пропандиола.
Готовили три различных концентрации 1-(нитрозоокси)-пропан-2-ола и 2-(нитрозоокси)-пропан-1-ола в 1,2-пропандиоле, которые хранили как в холодильнике (5 °C), так и в морозильной камере (- 20 °С). Периодически отбирали аликвоты каждого раствора и анализировали с помощью ГХ для определения концентрации 1-(нитрозоокси)пропан-2-ола и 2-(нитрозоокси)-пропан-1-ола.
Результаты анализа ГХ приведены в таблице ниже (колонка: Rxi-5Sil MS, 20 м x 0,18 мм, толщина пленки 0,36; носитель: He; вход: 250 °C, отношение деления потока 100:1; постоянный поток: 1,0 мл/мин; температурный профиль печи: 40 °C (3 мин), 10 °C/мин, 80 °C (0 мин), 30 °C /мин, 250 °C (3 мин); FID: 300 °C, H2 поток 30 мл/мин, поток воздуха 400 мл/мин, поток вспомогательного газа (N2 ) 25 мл/мин; внутренний стандарт: 1,1,1,3,5,5,5-гептаметилтрисилоксан):
Концентрация (мас.%)
Концентрация (мас.%)
Примечание: какого-либо повышения давления не наблюдалось ни для одного из образцов.
Пример 5 - Стабильность водных буферных растворов 1-(нитрозоокси)пропан-2-ола и 2-(нитрозоокси)пропан-1-ола (PDNO), а также 1,2-пропандиола (PD)
100 мкл образца стабильности добавляли в пробирку для ГХ. Добавляли 400 мкл раствора PD/буфер (1:9) и 400 мкл CH3CN. Затем добавляли 500 мкл CH2Cl2 и смесь экстрагировали осторожным встряхиванием в течение 1 мин. 500 мкл органической фазы (нижняя фаза) переносили в другой сосуд для ГХ и добавляли 50 мкл IS. Экстракт анализировали с помощью ГХ/FID в соответствии с условиями, указанными выше.
Строили калибровочные кривые для 1-нитрита и 2-нитрита соответственно. Строили график отношения площадей пиков (нитрит/IS) к количеству нитрита. Для приготовления стандартов применяли исходные растворы PDNO/PD с высокой концентрацией. Концентрации нитритов рассчитывали в мас.%.
Полученные результаты приведены в таблице ниже и на Фиг. 1.
(pH 8)*
(pH 9,2)*
(pH 8,0)*
* На основе известных значений.
Пример 6 - Исследования in vivo
После сбора исходных данных, стабильную легочную гипертензию индуцировали непрерывной внутривенной инфузией тромбоксанового А2-миметика 9,11-дидезокси-9α, 11α-метаноэпокси PGF2α (U46619, Cayman Chemical, Мичиган, США; который поставлялся в метилацетате и разбавлялся в NaCl 0,9% до конечной концентрации 30 мкг мл-1; 60-150 нг кг-1 мин-1 до целевого среднего давления в легочной артерии 35-45 мм рт.ст.). После этого проводили либо непрерывную внутривенную инфузию PDNO в возрастающих дозах (15, 30, 45 и 60 нмоль кг-1 мин-1 ) в поток раствора-носителя бикарбоната натрия (50 мг мл-1; pH приблизительно 8; Fresenius Kabi, Упсала, Швеция; скорость инфузии, в 10 раз превышающая скорость инфузии PDNO) или ингаляцию NO (5, 10, 20 и 40 ppm; доставляется в инспираторную часть аппарата ИВЛ Servo 300 с помощью дозатора вдыхаемого NO [Siemens-Elema, Стокгольм, Швеция] из резервуара с азотом 1000 ppm) в нерандомизированном перекрестном дизайне с периодом вымывания 30 мин между введениями препаратов. Введение правильной дозы вдыхаемого NO проверяли с помощью анализатора NO. Каждую дозу вводили в течение 5-10 мин. Гемодинамические и респираторные данные извлекали, а образцы артериальной крови собирали в последнюю минуту введения каждой дозы.
Внутривенная инфузия U46619 индуцировала стабильную легочную гипертензию со средним давлением в легочной артерии 43 (37-48) мм рт.ст. и 43 (41-46) мм рт.ст. и сопротивлением легочных сосудов 8,3 (6,7-11,7) мм рт.ст. мин л -1 и 9,8 (7,7-12,5) мм рт. ст. мин л -1 перед ингаляцией NO и инфузией PDNO соответственно. Как ингаляционный NO, так и внутривенно вводимый PDNO значительно снижали давление в легочной артерии и сосудистое сопротивление, но PDNO снижал среднее давление в легочной артерии более эффективно (более крутой наклон), чем ингаляционный NO, а PDNO снижал легочное сосудистое сопротивление значительно больше по сравнению с ингаляционным NO в сопоставимой дозе (как продемонстрировано на Фиг. 2). Ни один препарат не оказал значительного влияния на среднее артериальное давление и системное сосудистое сопротивление, но системное сосудистое сопротивление было немного ниже в группе PDNO по сравнению с группой, получавшей ингаляционный NO в сопоставимой дозе (Фиг. 2). Оба препарата значительно снижали соотношение легочного и системного сосудистого сопротивления, и при самых высоких дозах это соотношение было немного ниже в группе ингаляционного NO по сравнению с группой PDNO (данные не показаны). Сердечный выброс несколько снижался при введении U46619, но ни один лекарственный препарат не изменял сердечный выброс значительно (данные не показаны). Ни один препарат значительно не влиял на концентрацию метгемоглобина, но наблюдалась тенденция к ее повышению в группе ингаляционного NO, и было сделано предположение, что концентрация метгемоглобина ассоциировалась с дозой доставленного NO (Фиг. 2). Артериальное парциальное давление кислорода несколько снижалось при введении U46619, и оба препарата увеличивали эту переменную до нормального значения (данные не показаны).
Пример 7 - Приготовление без растворителя 1-(нитрозоокси)пропан-2-ола, 2-(нитрозоокси)пропан-1-ола и 1,2-бис(нитрозоокси)пропана с нитритом натрия
Воду (30 мл) и нитрит натрия (19,01 г, 272,8 ммоль) добавляли в трехгорлую круглодонную колбу на 100 мл, продували азотом и охлаждали до 1 °C на водяной бане, охлаждаемой внешним охладителем. Добавляли 1,2-пропандиол (10 мл, 136,7 ммоль). Концентрированную серную кислоту (7 мл, 127,4 ммоль) и воду (20 мл) предварительно охлаждали до комнатной температуры и добавляли по каплям в течение одного часа через капельную воронку. Во время добавления, слой воды образовывал густую суспензию и образовывался второй слой зеленого цвета. Перед завершением добавления кислоты (оставшееся 5 мл) колбу снимали с охлаждающей бани, а зеленый слой декантировали в делительную воронку и промывали 2-кратным насыщенным водным раствором NaHCO3. Зеленый слой преобрател желтый цвет, и после разделения его сушили над Na2SO4 и фильтровали через шприцевой фильтр (Acrodisc® 13 мм, 0,45 мкМ SUPOR®) с получением 1,1 г смеси 1-(нитрозоокси)-пропан-2-ола / 2-(нитрозоокси)пропан-1-ола / 1,2-бис (нитрозоокси)пропана в соотношении примерно 0,25 / 0,1 / 1. Исходный 1,2-пропандиол не обнаруживался в пределах чувствительности ЯМР.
1H-ЯМР, δ ppm: 5.81-5.76 (m, br, 1.0 H), 5.63 (br, 0.1 H), 4.93 (br, 2.08 H), 4.73-4.65 (br, m, 0.47 H), 4.14 (br, 0.19 H), 3.84-3.77 (br, m, 0.22 H), 1.49 - 1.48 (br, m, 3.21 H), 1.43 (br, 0.51 H), 1.28 (br, 0.72 H).
Пример 8 - Приготовление (2S)-1-(нитрозоокси)пропан-2-ола, (2S)-2-(нитрозоокси)пропан-2-ола и (2S)-1,2-бис(нитрозоокси)пропана
(S)-1,2-пропандиол (5 мл, 66,97 ммоль), воду (15 мл), дихлорметан (30 мл) и нитрит натрия (9,34 г, 134 ммоль) добавляли в трехгорлую круглодонную колбу на 100 мл, продували азотом и охлаждали до 1 °C на водяной бане, охлаждаемой внешним охладителем. Концентрированную серную кислоту (3,5 мл, 63,69 ммоль) и воду (10 мл) предварительно охлаждали до комнатной температуры и добавляли по каплям с помощью шприцевого насоса в течение 1 часа. После добавления смесь перемешивали еще 60 минут. После разделения двух слоев, слой DCM разбавляли дополнительным количеством DCM (15 мл) и промывали нас. водн. NaHCO3 (15 мл), затем солевым раствором (15 мл), и сушили над Na2SO4, фильтровали через фильтр из пористого стекла и упаривали в вакууме. Остаток снова растворяли в 30 мл DCM, промывали 1,4 мас.% водн. раствор бикарбоната, затем сушили над Na2SO4, фильтровали через фильтр из пористого стекла и упаривали в вакууме, получая 1 г смеси продуктов. Смесь состояла из (2S)-1,2-пропандиола (3%), (2S)-1-(нитрозоокси) пропан-2-ола (23%), (2S)-2-(нитрозоокси)пропан-1-ола (14%) и (2S) -1,2-бис(нитрозоокси)пропана (60%) на основе ЯМР.
1H-ЯМР, δ ppm: 5.83-5.74 (m, 1.0 H), 5.66-5.57 (br, 0.22 H), 4.99-4.85 (br, 1.98 H), 4.76-4.59 (br, 0.77 H), 4.17-4.07 (br, 0.38 H), 3.86-3.73 (br, 0.40 H), 1.8-1.6 (br, 0.97 H), 1.48 (d, J= 6.7 Hz, 3.12 H), 1.40 (d, J=6.6Hz, 0.63 H), 1.28 (d, J=6.5 Hz, 1.15 H).
Пример 9 - Приготовление (2R)-1-(нитрозоокси)пропан-2-ола, (2R)-2-(нитрозоокси)пропан-2-ола и (2R)-1,2-бис (нитрозоокси)пропана.
(R)-1,2-пропандиол (5 мл, 66,97 ммоль), воду (15 мл), дихлорметан (30 мл) и нитрит натрия (9,34 г, 134 ммоль) добавляли в трехгорлую круглодонную колбу на 100 мл, продували азотом и охлаждали до 1 °C на водяной бане, охлаждаемой внешним охладителем. Концентрированную серную кислоту (3,5 мл, 63,69 ммоль) и воду (10 мл) предварительно охлаждали до комнатной температуры и добавляли по каплям с помощью шприцевого насоса в течение 1 часа. После добавления смесь перемешивали еще 55 минут. После разделения двух слоев, слой DCM разбавляли дополнительным количеством DCM (10 мл) и промывали насыщенным водным NaHCO3 (20 мл), затем сушили над Na2SO4, фильтровали через фильтр из пористого стекла и упаривали в вакууме . Смесь состояла из (2R)-1,2-пропандиола (17%), (2R)-1-(нитрозоокси)пропан-2-ола (16%), (2R)-2-(нитрозоокси)пропан-1-ола (7%) и (2R)-1,2-бис(нитрозоокси)пропана (59%) на основании ЯМР.
1H-ЯМР, δ ppm: 5.83-5.74 (m, 1.0 H), 5.66-5.57 (br, 0.12 H), 4.99-4.85 (br, 2.10 H), 4.76-4.59 (br, 0.53 H), 4.17-4.07 (br, 0.24 H), 3.86-3.73 (br, 0.28 H), 2.4-2.1 (br, 0.38 H), 1.48 (d, J= 6.8 Hz, 3.20 H), 1.40 (br, 0.56 H), 1.28 (br(d), 0.88 H).
Пример 10 - Приготовление 1-(нитрозоокси)пропан-3-ола и 1,3-бис(нитрозоокси)пропана.
1,3-пропандиол (2,5 г, 32,86 ммоль), воду (7 мл), дихлорметан (15 мл) и нитрит натрия (4,53 г, 65,7 ммоль) добавляли в круглодонную колбу на 100 мл, продували азотом и охлаждали до 0 °C в течение 15 мин на водяной бане, охлаждаемой внешним охладителем. Концентрированную серную кислоту (1,7 мл, 31,2 ммоль) и воду (5 мл) предварительно охлаждали до комнатной температуры и добавляли по каплям в течение 5 минут. После добавления смесь перемешивали еще 60 минут при 0 °C. Затем два слоя разделяли, и органическую фазу разбавляли дополнительным количеством DCM (10 мл), промывали насыщенным водным NaHCO3 (2 × 25 мл), сушили над MgSO4, фильтровали через фильтр из пористого стекла. Наконец, к органической фазе добавляли 1,3-пропандиол (16,4 г, 216 ммоль) с последующим удалением DCM в вакууме. По данным ЯМР смесь (18,1 г) содержала 1,3-пропандиол (86,9 мас.%), 1-(нитрозоокси) пропан-3-ол (11,8 мас.%) и 1,3-бис(нитрозоокси)пропан (1,3 мас.%).
1H-ЯМР, δ 4.76-4.88 (m, 2H), 3.83 (t, J = 5.7 Hz, 2H), 3.73 (t, J = 6.1 Hz, 2H), 2.79 (s, 1H), 2.18 (quintet, J = 6.3 Hz, 2H), 1.99 (quintet, J = 6.2 Hz, 2H), 1.80 (quintet, J = 5.7 Hz, 2H).
Пример 11 - Способ приготоления в увеличенном масштабе 1-(нитрозоокси)пропан-2-ола, 2- (нитрозоокси)пропан-1-ола и 1,2-бис(нитрозоокси)пропана с нитритом натрия
11.1 Применяемые химические вещества
Исходные материалы закупали у ряда поставщиков из таблицы ниже. Если не указано иное, химические вещества применяли том виде, в котором они были получены, без дополнительной очистки.
11.2 Общая процедура синтеза PDNO с применением DCM в качестве растворителя (исходный процесс)
Колба с круглым дном была снабжена мешалкой и капельной воронкой. Добавляли воду (3,0 экв.) и в колбу загружали нитрит натрия (2,0 экв.). Раствор охлаждали до (0 °C) и также добавляли PD (1,0 экв.) и DCM (6 отн. об.). При дальнейшем охлаждении, готовили раствор серной кислоты (1,0 экв. H2SO4, 2,0 отн. об. воды). Далее к реакционной смеси по каплям добавляли раствор серной кислоты, поддерживая температуру реакционной смеси от 0 °C до 5 °C. После завершения добавления кислоты раствор дополнительно перемешивали в течение 1 часа для завершения реакции.
Затем реакцию гасили насыщенным раствором NaHCO3 (6,0 отн. об.). Фазы разделяли, и органический слой дополнительно промывали раствором NaHCO3 (6,0 отн. об.). Органическую фазу сушили над MgSO4, фильтровали, разбавляли PD и концентрировали при пониженном давлении с помощью роторного выпаривателя (температура водяной бани 40 °C).
Продукт получали в виде слегка желтоватой жидкости.
11.3 Общий синтез PDNO с применением TBME в качестве растворителя
Колба с круглым дном была снабжена мешалкой и капельной воронкой. В течение нескольких минут продували аргон. Разбавленный раствор серной кислоты (1,0 экв. H2SO4, 2.0 отн. об. воды) готовили в усовершенствованной и предварительно охлажденной (-30 °C) среде. В колбу добавляли воду (3,0 отн. об.). В воду добавляли нитрит натрия (2,0 экв.). Добавляли TBME (7,5 отн. об.). Добавляли пропандиол (1,0 экв.) и реакционную смесь охлаждали (-20 °C), постоянно продувая аргоном. Реакционную смесь хорошо перемешивали, добавляя по каплям предварительно охлажденную серную кислоту. Температуру реакции контролировали в течение всего добавления кислоты. После добавления реакционную смесь дополнительно перемешивали (30-60 мин) при низкой температуре (-20 °C). После этого реакционной смеси давали нагреться (-5 °C). Реакцию останавливали путем гашения насыщенным раствором NaHCO3 (6,0 отн. об.). Фазы разделяли. Органический слой дополнительно промывали насыщенным раствором NaHCO3 до достижения значения pH 7-8. Затем органическую фазу сушили над MgSO4. Неочищенный раствор PDNO разбавляли PD (3 отн. об.) и дополнительно концентрировали при пониженном давлении и температуре окружающей среды (25 °C).
Неочищенный раствор PDNO дополнительно очищали с помощью аппарата для выпаривания с вертикальными трубками.
PDNO получали в виде слегка желтоватой жидкости.
11.4 Детальное описание синтеза PDNO с применением TBME в качестве растворителя
Этот способ был разработан для продуцирования ок. 7,5 л 7% раствора PDNO за один цикл синтеза (один «прогон»). Синтез проводили несколько раз, чтобы получить желаемый размер партии. ГХ-анализ проводили каждый раз для определения чистоты. Прогоны, которые находятся в пределах спецификаций для родственных органических соединений, могут быть смешаны вместе для получения одной партии. Затем очищали всю партию неочищенного PDNO. После очистки сильный раствор PDNO дополнительно разбавляли PD для получения желаемой концентрации (обычно 7% раствор PDNO).
Пригодный реактор с двойными стенками (60 л) был оборудован специальной «чашечной мешалкой», капельной воронкой и насадкой для аргона. Реактор продували в течение 5-10 минут постоянным потоком аргона. В реактор добавляли воду (3,0 л). Через реактор добавляли нитрит натрия (2,0 экв., 1886 г). Реакционную смесь дополнительно перемешивали до растворения всей соли. Добавляли 1,2-пропандиол (1,0 эквив., 1040 г, 1 л), а затем трет- бутилметиловый эфир (7,5 отн. об., 7,5 л). Затем реакционную смесь охлаждали непрерывным перемешиванием и потоком аргона при внутренней температуре реакции -20 °C. Тем временем серную кислоту (1,0 экв., 1340 г, 728 мл) разбавляли водой (2,0 л) и охлаждали до -30 °C. После достижения внутренней температуры реакции -20 °C к реакционной смеси по каплям добавляли разбавленную кислоту при интенсивном перемешивании.
Скорость перемешивания менялась в ходе добавления кислоты. Начиная от примерно 350 об/мин до более медленной скорости перемешивания к концу реакции (примерно 180 об/мин). Такое изменение скорости перемешивания связано с двухфазной реакционной системой и медленным осаждением сульфата натрия при дальнейшем протекании реакции (из-за добавления все большего и большего количества серной кислоты).
В течение всего периода добавления серной кислоты контролировали температуру реакции. В идеале температура должна быть в диапазоне (-20 ± 3) °С. Кроме того, реакционную смесь перемешивали 30-60 мин при (-20 ± 3) °C.
Реакционной смеси давали нагреться от -5 °C до 0 °C. Реакцию останавливали добавлением насыщенного раствора NaHCO3 (6,0 отн. об., 6,0 л) с последующим добавлением воды (10 л). Фазы разделяли, и органический слой переносили в отдельный двухстенный реактор и охлаждали при температуре от 0 °C до -5 °C. Органический слой промывали несколько раз (примерно 2-3 раза) насыщенным раствором NaHCO3 (4,0 отн. об., 4,0 л). Значение pH водной фазы контролировали после каждого этапа промывки. Значение pH составляло около 7-8. Водные фазы отбрасывали. Органический слой сушили над MgSO4 и фильтровали через фильтровальную бумагу Whatman.
Неочищенный PDNO (раствор в TBME) разбавляли добавлением дополнительного PD (3,0 отн. об., 3,0 л). Этот неочищенный PDNO переносили в роторный испаритель и концентрировали при пониженном давлении. Температуру водяной бани во время выпаривания поддерживали на максимальном уровне 25 °C. Выпаривание основного количества TBME удалялось в интервале времени от 1,5 до 2,0 часов.
Затем выпаривание органических растворителей можно было продолжить при температуре водяной бани при (0 ± 2) °C в течение нескольких часов с применением высоковакуумного насоса (во время разработки, в этих условиях контролировали чистоту PDNO, и в течение 6 часов чистота продукта не ухудшалась).
11.5 Дополнительная очистка неочищенного раствора PDNO
Окончательную очистку раствора PDNO проводили выпариванием в аппарате с вертикальными трубками. Раствор PDNO перегоняли в высоком вакууме с непрерывным разжиженным паром PDNO при 0 °C. Резервуар для хранения «неочищенного» раствора PDNO охлаждали до 0 °C. Весь процесс перегонки проводили при 0 °C. Резервуар для хранения «очищенного» PDNO также охлаждали при температуре от -10 °C до 0 °C. После каждого цикла выпаривания всей партии PDNO, остаточный органический растворитель (TBME) можно было проверить с помощью ГХ. Это выпаривание продолжали до тех пор, пока не был достигнут желаемый предел остаточных растворителей. В случае PDNO предел для остаточного растворителя составляет 1000 ppm.
11.6 Приготовление конечного разведения
После очистки, PDNO дополнительно разбавляли для достижения желаемой концентрации. Первый этап - фильтрация раствора PDNO в чистый стеклянный флакон через фильтр Whatman. Кроме того, количественный состав раствора PDNO определяли с помощью q-ЯМР. Количество PD для разбавления можно было рассчитать. PD сначала фильтровали через фильтр Whatman. Конечное разбавление можно было проводить при температуре окружающей среды. Рассчитанное количество PD добавляли в раствор PDNO (или наоборот). Полученную смесь встряхивали несколько минут до получения гомогенного раствора. Конечный раствор PDNO разливали во флаконы с продуктом.
PDNO (7,5 кг; 7% раствор) получали в виде слегка желтоватой жидкости.
Пример 12 - Гемодинамические эффекты внутривенного PDNO: влияние различных растворов-носителей на анестезированных свиней
Изучали влияние различных растворов-носителей на гемодинамические эффекты органических мононитритов 1,2-пропандиола (PDNO), внутривенно вводимых анестезированным свиньям.
Перед проведением эксперимента было получено этическое одобрение от регионального комитета по этике животных Линчепинга (Линчепинг, Швеция; номер одобрения 953). Исследование проводили в соответствии с Директивой 2010/63/ЕС о защите животных, используемых в научных целях. В исследование были включены две здоровые домашние трехмесячные свиньи (помесь шведской деревенской породы Хэмпшир и Йоркшир; масса тела 26 и 27 кг).
На ферме животным предварительно ввели азаперон и доставили в лабораторию. В лаборатории анестезию индуцировали смесью тилетамина, золазепама и азаперона (внутримышечная инъекция). При необходимости вводили пропофол через периферический венозный катетер в ушную вену. Внутривенно вводили болюсные дозы атропина и цефуроксима. Животных эндотрахеально интубировали и подвергали механической вентиляции (5 см H2O при положительном давлении в конце выдоха, минутная вентиляция доводили до нормовентиляции). Общую анестезию поддерживали пропофолом и фентанилом посредством непрерывных внутривенных инфузий, при необходимости вводили дополнительные болюсные дозы. С целью восполнения потери жидкости непрерывно внутривенно вводили растворы ацетата Рингера и глюкозы. После хирургического вмешательства внутривенно болюсно вводили гепарин. После экспериментов животных умерщвляли под общей анестезией инъекцией пропофола с последующей быстрой внутривенной инъекцией хлорида калия (40 ммоль), и подтверждали асистолию.
Животным вводили артериальный катетер в правую сонную артерию для измерения системного артериального кровяного давления и частоты сердечных сокращений. В правую наружную яремную вену помещали интродьюсер для введения легочно-артериального катетера. Этот катетер использовался для непрерывного измерения артериального кровяного давления в легочной артерии и полунепрерывного сердечного выброса. Центральный венозный катетер вставляли в левую наружную яремную вену для введения лекарственных препаратов и жидкости. Все введения жидкостей и лекарственных препаратов осуществляли с помощью моторизованных шприцев или капельных насосов. Катетеризовали мочевой пузырь. Гемодинамические переменные измеряли с помощью Datex AS/3 (Хельсинки, Финляндия), а данные собирали с помощью компьютеризированной системы (MP150/Acknowledge 3.9.1, системы BIOPAC, Goleta, штат Калифорния, США). После хирургической операции проходил по меньшей мере 1 час без какого-либо вмешательства.
Внутривенные инфузии PDNO (Исследовательские институты Швеции, Södertälje, Швеция) вводили при 30 нмоль кг-1 мин-1 в течение 15 минут в потоке носителя при скорости инфузии, в 9 раз превышающей скорость инфузии PDNO, бикарбоната натрия (14 мг/мл; pH 7,4 или 8,0), физиологического фосфатного буфера при pH 8 или физиологического солевого раствора. Для изготовления растворов-носителей применяли стандартные химические вещества. Гемодинамический эффект измеряли в конце каждой инфузии.
Результаты представлены в таблице ниже. Исходные значения перед каждой внутривенной комбинацией PDNO и раствора-носителя были нормальными для здоровых анестезированных свиней. Внутривенное введение PDNO в растворе-носителе бикарбонатного буфера при pH 8 снижало среднее системное артериальное давление (MAP) и среднее давление в легочной артерии (MPAP) на -11 ± 1,2 мм рт.ст. и -2,4 ± 0,8 мм рт.ст., соответственно, тогда как внутривенное введение PDNO в растворе-носителе физиологического солевого раствора снижало MAP и MPAP на -6,9 ± 2,5 мм рт. ст. и -2,4 ± 0,1 мм рт. ст. Внутривенное введение PDNO в комбинации с бикарбонатным буфером при pH 7,4 и физиологическим фосфатным буфером при pH 8 оказывало такое же влияние на MAP и MPAP, что и физиологический солевой раствор. Инфузии лишь незначительно влияли на частоту сердечных сокращений и полунепрерывный сердечный выброс.
Гемодинамические переменные у анестезированных и искусственно вентилируемых свиней, подвергшихся повторным внутривенным инфузиям PDNO при 30 нмоль кг-1 мин-1 в сочетании с различными растворами-носителями (n = 2 на раствор-носитель).
(мм рт. ст.)
(мм рт. ст.)
(ударов мин-1)
(L мин-1)
Данные представлены в виде средних значений и стандартных отклонений.
Среднее системное артериальное давление (MAP), среднее давление в легочной артерии (MPAP), частота сердечных сокращений (ЧСС), полунепрерывный сердечный выброс (CCO).
Внутривенное введение PDNO в сочетании с раствором-носителем бикарбонатного буфера при pH 8 вызывало более сильные гемодинамические эффекты по сравнению с растворами-носителями физиологического солевого раствора, физиологического фосфатного буфера и бикарбонатного буфера при pH 7,4.
Пример 13 - Фармакологическое исследование 1,2-PDNO-R, 1,2-PDNO-S и 1,3-PDNO у анестезированных свиней
Перед проведением эксперимента было получено этическое одобрение от регионального комитета по этике животных Линчепинга (Линчепинг, Швеция; номер одобрения 953). Вкратце, 2 самца и самки свиней (помесь шведской деревенской породы, Хэмпшир и Йоркшир; возраст 3-4 месяца; 24-26 кг) получили премедикацию азапероном на ферме и были доставлены в лабораторию. В лаборатории проводили анестезию смесью тилетамина, золазепама и азаперона (внутримышечная инъекция). При необходимости вводили пропофол через периферический венозный катетер в ушную вену. Внутривенно вводили болюсные дозы атропина и цефуроксима. Животных эндотрахеально интубировали и подвергали механической вентиляции (5 см H2O при положительном давлении в конце выдоха, минутная вентиляция доводили до нормовентиляции). Общую анестезию поддерживали пропофолом и фентанилом посредством непрерывных внутривенных инфузий, при необходимости вводили дополнительные болюсные дозы. С целью восполнения потери жидкости непрерывно внутривенно вводили растворы ацетата Рингера и глюкозы. После хирургического вмешательства внутривенно болюсно вводили гепарин. После экспериментов животных умерщвляли под общей анестезией посредством инъекции пропофола с последующей быстрой внутривенной инъекцией хлорида калия (40 ммоль), и подтверждали асистолию.
Животным вводили артериальный катетер в правую сонную артерию для измерения системного артериального кровяного давления и частоты сердечных сокращений. В правую наружную яремную вену помещали интродьюсер для введения легочно-артериального катетера. Этот катетер применяли для непрерывного измерения артериального кровяного давления в легочной артерии, полунепрерывного сердечного выброса и интермиттирующего давления заклинивания в легочной артерии. Центральный венозный катетер вставляли в левую наружную яремную вену для введения лекарственных препаратов и жидкости. Все введения жидкости и лекарственного препарата осуществляли с помощью моторизованных шприцев или капельных насосов. Катетеризовали мочевой пузырь. Показатели дыхательных газов, давления и объемов измеряли на интубационной трубке. Респираторные и гемодинамические параметры измеряли с помощью Datex AS/3 (Хельсинки, Финляндия), а данные собирали с помощью компьютеризированной системы (MP100 или MP150/Acknowledge 3.9.1, системы BIOPAC, Goleta, штат Калифорния, США). После хирургической операции следовал 1-часовой период без какого-либо вмешательства.
После сбора исходных данных, 10-15-минутную внутривенную инфузию 1,2-PDNO-R (43 нмоль кг-1 мин-1 ), 1,2-PDNO-S (43 нмоль кг-1 мин-1 ) и 1,3-PDNO (30 нмоль кг-1 мин-1 ) вводили в поток-носитель раствора бикарбоната натрия (14 мг мл-1 ; pH приблизительно 8; со скоростью инфузии, в 9 раз превышающей скорость инфузии PDNO). Гемодинамические и респираторные данные собирали в конце каждой дозы.
1,2-PDNO-R, 1,2-PDNO-S и 1,3-PDNO снижали среднее системное артериальное давление и среднее давление в легочной артерии, что продемонстрировано на Фиг. 3. Вывод заключается в том, что 1,2-PDNO-R, 1,2-PDNO-S и 1,3-PDNO вызывают системную и легочную вазодилатацию, таким образом, обладая сосудорасширяющими характеристиками.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ХИНАЗОЛИНОНА, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ВАНИЛОИДНЫХ АНТАГОНИСТОВ | 2005 |
|
RU2449995C2 |
| ПРОИЗВОДНЫЕ 3,4-БИС(ФУРАЗАН-3-ИЛ)ФУРОКСАНА, ГЕНЕРИРУЮЩИЕ ОКСИД АЗОТА, АКТИВИРУЮЩИЕ РАСТВОРИМУЮ ФОРМУ ГУАНИЛАТЦИКЛАЗЫ, ИНГИБИРУЮЩИЕ АГРЕГАЦИЮ ТРОМБОЦИТОВ И ОБЛАДАЮЩИЕ СПАЗМОЛИТИЧЕСКИМ, СОСУДОРАСШИРЯЮЩИМ, ГИПОТЕНЗИВНЫМ ДЕЙСТВИЕМ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2002 |
|
RU2240321C2 |
| КОМПЛЕКСЫ ВКЛЮЧЕНИЯ ПРОИЗВОДНЫХ 1,2,5-ОКСАДИАЗОЛ-2-ОКСИДА С ПОЛИЦИКЛИЧЕСКИМИ ПРОИЗВОДНЫМИ ГЛЮКОПИРАНОЗЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2186782C1 |
| ПРОИЗВОДНЫЕ ХИНАЗОЛИНОНА, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ВАНИЛОИДНЫХ АНТАГОНИСТОВ | 2005 |
|
RU2396261C2 |
| ПРОИЗВОДНЫЕ 1,2,5-ОКСАДИАЗОЛО-[3,4-D]-ПИРИДАЗИН-5,6-ДИОКСИДА В КАЧЕСТВЕ АКТИВАТОРОВ РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ И СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 1997 |
|
RU2165256C2 |
| ИНГИБИТОРЫ СИНТАЗЫ ОКСИДА АЗОТА НА ОСНОВЕ МЕРКАПТО- И СЕЛЕНОПРОИЗВОДНЫХ | 1996 |
|
RU2191575C2 |
| АНАЛОГИ ХРОМЕНОНА В КАЧЕСТВЕ МОДУЛЯТОРОВ СИРТУИНА | 2009 |
|
RU2527269C2 |
| НАФТАЛИНОВЫЕ ПРОИЗВОДНЫЕ | 2001 |
|
RU2354646C2 |
| КОНЪЮГАТЫ И ПРОИЗВОДНЫЕ ПРОСТАГЛАНДИНА ДЛЯ ЛЕЧЕНИЯ ГЛАУКОМЫ И ВНУТРИГЛАЗНОЙ ГИПЕРТЕНЗИИ | 2015 |
|
RU2712221C2 |
| ХИНАЗОЛИНОН, ХИНОЛОН И РОДСТВЕННЫЕ АНАЛОГИ В КАЧЕСТВЕ МОДУЛЯТОРОВ СИРТУИНА | 2009 |
|
RU2519779C2 |
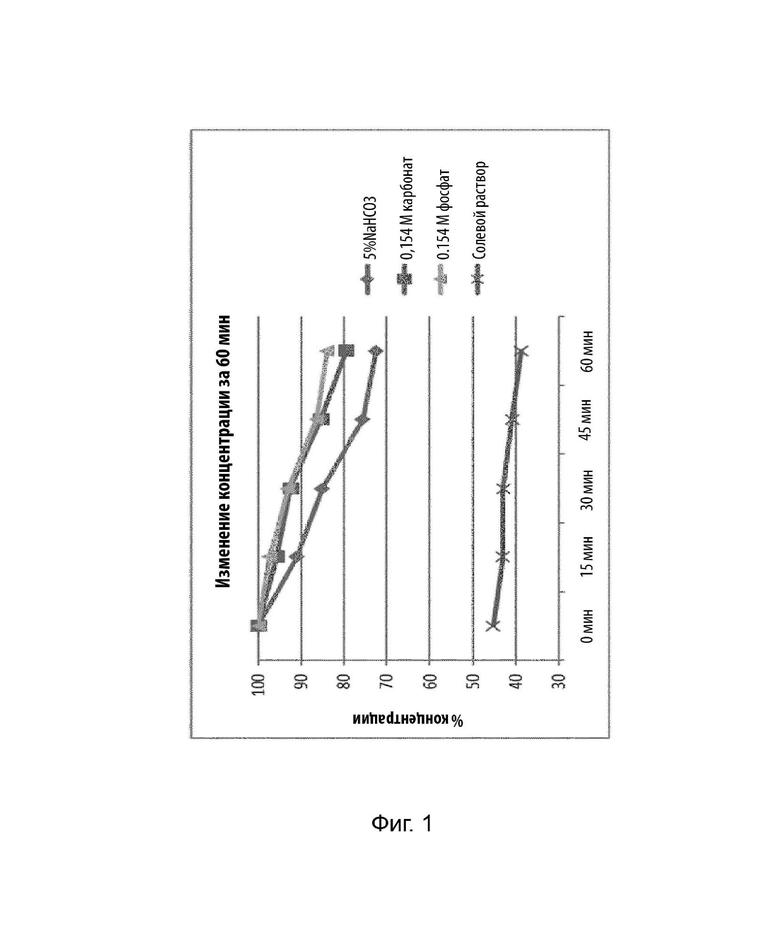
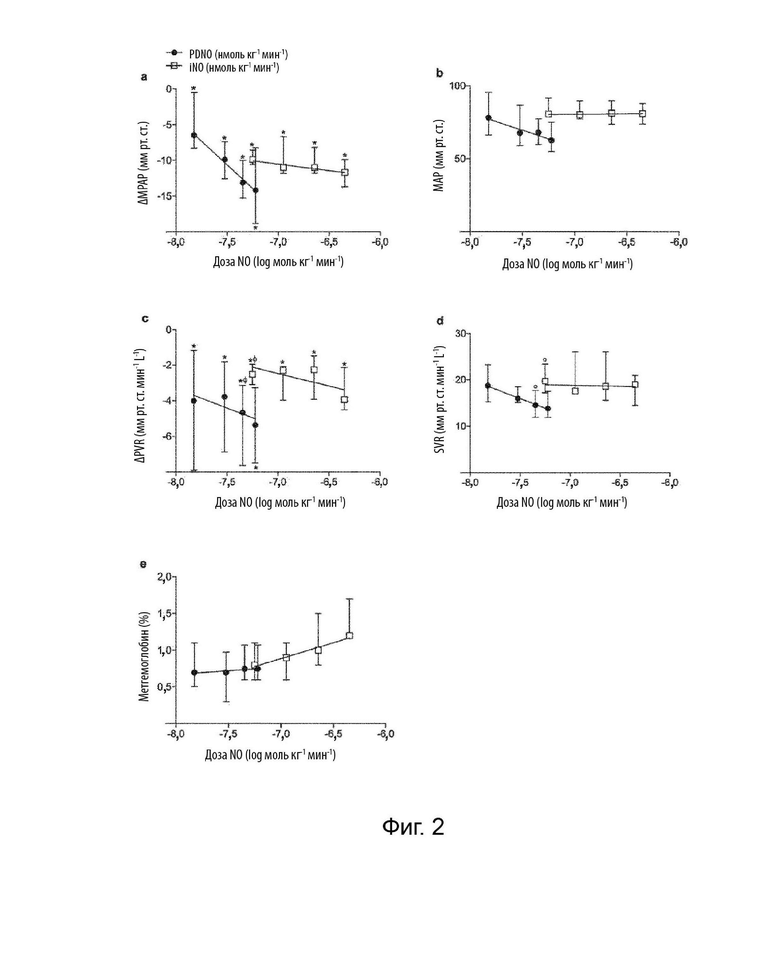
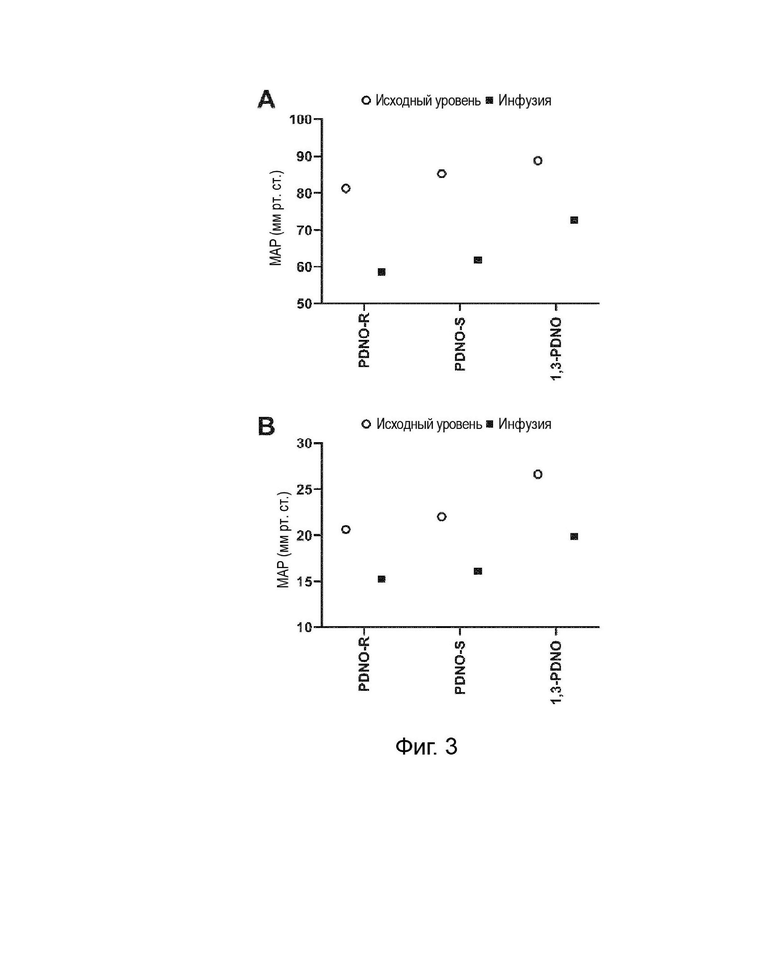
Настоящее изобретение относится к способу приготовления композиции, содержащей одно или большее количество соединений Формулы I 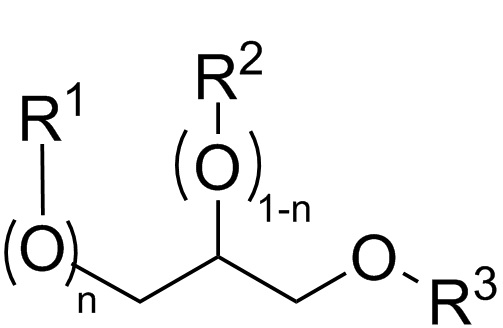 (I), где R1, R2 и R3 каждый независимо представляют собой H или -NO, где n равно 0 или 1; где, когда n равно 0, R1 представляет собой H; а также где, когда n равно 1, R2 представляет собой H при условии, что по меньшей мере один из R1, R2 и R3 представляет собой -NO. Данный способ включает стадию взаимодействия соответствующего соединения формулы I, где R1, R2 и R3 представляют собой H с источником нитрита, необязательно в присутствии пригодной кислоты. Когда источником нитрита является органический нитрит, стадию (i) выполняют в пригодном органическом растворителе; а когда источником нитрита является неорганический нитрит, стадию (i) выполняют в двухфазной смеси растворителей, содержащей водную фазу и неводную фазу. При этом способ дополнительно включает стадию добавления дополнительного количества соединения Формулы I, где R1, R2 и R3 представляют собой H, и композиции одного или большего количества соединений Формулы I и соединения Формулы I, где R1, R2 и R3 представляют собой H, содержит от 0,01% до 9 % мас. одного или большего количества соединений Формулы I. Также изобретение относится к композиции для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, к фармацевтической композиции, комбинированному продукту, фармацевтическому составу и набору элементов, содержащим данную композицию, к способу получения комбинированного продукта, к применениями заявленных продуктов, а также к способу лечения патологического состояния, при котором введение NO характеризуется положительным эффектом. Технический результат – разработка способа, обеспечивающего относительно высокую концентрацию соединений в растворе, минимизацию риска внезапного и спонтанного разложения и снижение вероятности побочных эффектов, когда продукт, получаемый в результате осуществления указанного способа, применяется для лечения. 12 н. и 26 з.п. ф-лы, 3 ил., 1 табл., 13 пр.
(I), где R1, R2 и R3 каждый независимо представляют собой H или -NO, где n равно 0 или 1; где, когда n равно 0, R1 представляет собой H; а также где, когда n равно 1, R2 представляет собой H при условии, что по меньшей мере один из R1, R2 и R3 представляет собой -NO. Данный способ включает стадию взаимодействия соответствующего соединения формулы I, где R1, R2 и R3 представляют собой H с источником нитрита, необязательно в присутствии пригодной кислоты. Когда источником нитрита является органический нитрит, стадию (i) выполняют в пригодном органическом растворителе; а когда источником нитрита является неорганический нитрит, стадию (i) выполняют в двухфазной смеси растворителей, содержащей водную фазу и неводную фазу. При этом способ дополнительно включает стадию добавления дополнительного количества соединения Формулы I, где R1, R2 и R3 представляют собой H, и композиции одного или большего количества соединений Формулы I и соединения Формулы I, где R1, R2 и R3 представляют собой H, содержит от 0,01% до 9 % мас. одного или большего количества соединений Формулы I. Также изобретение относится к композиции для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, к фармацевтической композиции, комбинированному продукту, фармацевтическому составу и набору элементов, содержащим данную композицию, к способу получения комбинированного продукта, к применениями заявленных продуктов, а также к способу лечения патологического состояния, при котором введение NO характеризуется положительным эффектом. Технический результат – разработка способа, обеспечивающего относительно высокую концентрацию соединений в растворе, минимизацию риска внезапного и спонтанного разложения и снижение вероятности побочных эффектов, когда продукт, получаемый в результате осуществления указанного способа, применяется для лечения. 12 н. и 26 з.п. ф-лы, 3 ил., 1 табл., 13 пр.
1. Способ приготовления композиции, содержащей одно или большее количество соединений Формулы I
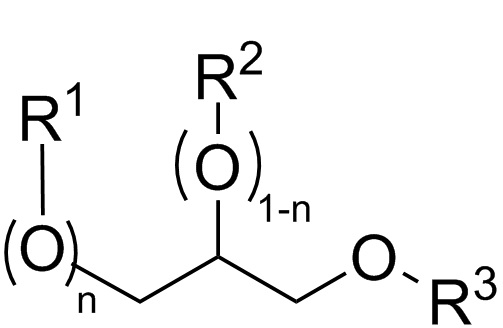 (I),
(I),
где R1, R2 и R3 каждый независимо представляют собой H или -NO,
где n равно 0 или 1;
где, когда n равно 0, R1 представляет собой H; а также
где, когда n равно 1, R2 представляет собой H
при условии, что по меньшей мере один из R1, R2 и R3 представляет собой -NO, при этом
указанный способ включает следующие стадии:
(i) взаимодействие соответствующего соединения формулы I, где R1, R2 и R3 представляют собой H с источником нитрита, необязательно в присутствии пригодной кислоты,
при этом:
(а) когда источником нитрита является органический нитрит, стадию (i) выполняют в пригодном органическом растворителе; а также
(b) когда источником нитрита является неорганический нитрит, стадию (i) выполняют в двухфазной смеси растворителей, содержащей водную фазу и неводную фазу, и
причем указанный способ дополнительно включает стадию добавления дополнительного количества соединения Формулы I, где R1, R2 и R3 представляют собой H, и композиции одного или большего количества соединений Формулы I и соединения Формулы I, где R1, R2 и R3 представляют собой H, содержит от 0,01% до 9 % мас. одного или большего количества соединений Формулы I.
2. Способ по п. 1, отличающийся тем, что указанный неорганический нитрит представляет собой нитрит металла.
3. Способ по п. 2, отличающийся тем, что указанный нитрит металла представляет собой нитрит щелочного металла или нитрит щелочноземельного металла.
4. Способ по п. 3, отличающийся тем, что указанный нитрит металла представляет собой нитрит щелочного металла.
5. Способ по п. 4, отличающийся тем, что указанный нитрит щелочного металла представляет собой нитрит натрия.
6. Способ по п. 1, отличающийся тем, что указанный органический нитрит представляет собой алкилнитрит.
7. Способ по п. 6, отличающийся тем, что указанный алкилнитрит представляет собой трет-бутилнитрит.
8. Способ по любому из пп. 1-7, отличающийся тем, что пригодной кислотой является сильная кислота, например сильная минеральная кислота.
9. Способ по п. 8, отличающийся тем, что указанная сильная минеральная кислота представляет собой серную кислоту.
10. Способ по любому из пп. 1-9, отличающийся тем, что неводная фаза содержит несмешивающийся с водой органический растворитель, такой как несмешивающийся с водой апротонный органический растворитель.
11. Способ по п. 10, отличающийся тем, что несмешивающийся с водой органический растворитель представляет собой дихлорметан или трет-бутилметиловый эфир.
12. Способ по любому из пп. 1-11, отличающийся тем, что смесь растворителей дополнительно содержит избыток соединения формулы I, но где R1, R2 и R3 представляют собой H.
13. Способ по любому из пп. 1-12, отличающийся тем, что после стадии (i) указанный способ дополнительно включает стадию:
(ii) удаления всей водной фазы из смеси растворителей.
14. Способ по любому из пп. 1-12, отличающийся тем, что после стадии (i) указанный способ дополнительно включает стадии:
(ii) удаления части или всей водной фазы;
(iii) промывания оставшейся органической фазы одной или большим количеством дополнительных водных фаз;
(iv) необязательно повторения стадий (ii) и (iii) один или большее количество раз;
(v) необязательно уменьшения количества/объема органической фазы, а также
(vi) необязательно сушки продукта,
при этом стадии (ii) - (vi) могут выполняться в любом порядке при условии, что стадии (ii) - (iv) выполняются перед стадиями (v) и (vi).
15. Способ по любому из пп. 1-14, для получения продукта для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом.
16. Композиция для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, содержащая:
(a) одно или большее количество соединений Формулы I
 (I),
(I),
где R1, R2 и R3 каждый независимо представляют собой H или -NO,
где n равно 0 или 1; а также
где, когда n равно 0, R1 представляет собой H; а также
где, когда n равно 1, R2 представляет собой H
при условии, что по меньшей мере один из R1, R2 и R3 представляет собой -NO; а также
(b) соединение Формулы I, где R1, R2 и R3 представляют собой Н,
причем компоненты (а) и (b) указанной композиции содержаться в совокупном количестве, составляющем по меньшей мере 80% по весу; и
причем указанная композиция содержит 0,01% до 9% мас. одного или большего количества соединений Формулы I.
17. Композиция по п. 16, отличающаяся тем, что не содержит растворенного оксида азота.
18. Композиция по п. 16 или 17, отличающаяся тем, что состоит из одного или большего количества соединений формулы I и соединения формулы I, где R1, R2 и R3 представляют собой H.
19. Фармацевтический состав для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, содержащий композицию по любому из пп. 16-18, и необязательно один или большее количество фармацевтически приемлемых вспомогательных веществ, причем одно или большее количество фармацевтически приемлемых вспомогательных веществ являются неводными.
20. Набор элементов для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, содержащий:
(A) фармацевтический состав по п.19; а также
(B) пригодный водный буфер,
при этом компоненты (А) и (В) представлены в форме, пригодной для введения друг с другом.
21. Комбинированный продукт, образованный путем смешивания следующих компонентов:
(A) фармацевтический состав по п. 19; а также
(B) пригодный водный буфер.
22. Набор элементов по п. 20 или комбинированный продукт по п. 21, отличающийся тем, что соотношение фармацевтического состава и водного буфера составляет от 3:7 до 1:99 по объему.
23. Набор элементов по пп. 20 или 22 или комбинированный продукт, как он заявлен по пп. 21 или 22, отличающийся тем, что указанный буфер является ненуклеофильным и слабоосновным.
24. Набор элементов по любому из пп. 20, 22 и 23 или комбинированный продукт по п. 21 или как он заявлен по пп. 22-23, отличающийся тем, что указанный буфер поддерживает pH от 7,1 до 10.
25. Набор элементов по любому из пп. 20 и 22-24, или комбинированный продукт по п. 21 или по пп. 22-24, отличающийся тем, что указанный буфер представляет собой карбонатный буфер, или фосфатный буфер, или их смесь.
26. Способ приготовления комбинированного продукта по любому из пп. 21 и 23-25, включающий стадию смешивания следующих компонентов:
(А) фармацевтический состав по любому из пп. 23-25; а также
(В) пригодный водный буфер как он заявлен по любому из пп. 23-25.
27. Применение композиция по любому из пп. 16-18 для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом.
28. Применение фармацевтического состава по п. 19 для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом.
29. Применение набора элементов как он заявлен по любому из пп. 20 и 22-25 для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом.
30. Применение комбинированного продукта как он заявлен по любому из пп. 21-25 для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом.
31. Способ лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества фармацевтического состава по п. 19 или комбинированного продукта по п. 21 или как он заявлен по любому из пп. 23-25.
32. Способ лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества следующих компонентов:
(А) фармацевтический состав по п. 19; а также
(В) пригодный водный буфер, как определено в любом из пп. 22-25,
при этом указанные компоненты (А) и (В) смешивают перед введением.
33. Применение по любому из пп. 27-30 для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, отличающееся тем, что указанное состояние выбирают из группы, состоящей из:
острого сужения легочных сосудов различного генеза; легочной гипертензии различного генеза, в том числе первичной гипертензии и вторичной гипертензии; патологических состояний разного генеза, требующих расширения сосудов; системной гипертензии различного генеза; регионарного сужения сосудов разного генеза; местного сужения сосудов разного генеза; острой сердечной недостаточности (с сохраненной или несохраненной фракцией выброса (HFpEF)); коронарного заболевания сердца; инфаркта миокарда; ишемической болезни сердца; стенокардии; нестабильной стенокардии; аритмии сердца; острой легочной гипертензии у кардиохирургических пациентов; ацидоза; воспаления дыхательных путей; муковисцидоза; ХОЗЛ; синдрома дискинезии ресничек; воспаления легких; легочного фиброза; респираторного дистресс-синдрома взрослых; острого отека легких; острой горной болезни; астмы; бронхита; гипоксии разного генеза; инсульта; сужения сосудов головного мозга; воспаления желудочно-кишечного тракта; нарушения функции желудочно-кишечного тракта; желудочно-кишечных осложнении; ВЗК; болезни Крона; язвенного колита; болезни печени; заболевания поджелудочной железы; воспаления мочевого пузыря уретрального тракта; воспаления кожных покровов; диабетических язв; диабетической невропатии; псориаза; воспаления разного генеза; заживления раны; защиты органов в условиях ишемии-реперфузии; трансплантации органов; трансплантации тканей; трансплантации клеток; острой болезни почек; релаксации матки; релаксации шейки матки; а также состояний, при которых требуется релаксация гладких мышц.
34. Способ по п. 31 или 32 для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, отличающееся тем, что указанное состояние выбирают из группы, состоящей из:
острого сужения легочных сосудов различного генеза; легочной гипертензии различного генеза, в том числе первичной гипертензии и вторичной гипертензии; патологических состояний разного генеза, требующих расширения сосудов; системной гипертензии различного генеза; регионарного сужения сосудов разного генеза; местного сужения сосудов разного генеза; острой сердечной недостаточности (с сохраненной или несохраненной фракцией выброса (HFpEF)); коронарного заболевания сердца; инфаркта миокарда; ишемической болезни сердца; стенокардии; нестабильной стенокардии; аритмии сердца; острой легочной гипертензии у кардиохирургических пациентов; ацидоза; воспаления дыхательных путей; муковисцидоза; ХОЗЛ; синдрома дискинезии ресничек; воспаления легких; легочного фиброза; респираторного дистресс-синдрома взрослых; острого отека легких; острой горной болезни; астмы; бронхита; гипоксии разного генеза; инсульта; сужения сосудов головного мозга; воспаления желудочно-кишечного тракта; нарушения функции желудочно-кишечного тракта; желудочно-кишечных осложнении; ВЗК; болезни Крона; язвенного колита; болезни печени; заболевания поджелудочной железы; воспаления мочевого пузыря уретрального тракта; воспаления кожных покровов; диабетических язв; диабетической невропатии; псориаза; воспаления разного генеза; заживления раны; защиты органов в условиях ишемии-реперфузии; трансплантации органов; трансплантации тканей; трансплантации клеток; острой болезни почек; релаксации матки; релаксации шейки матки; а также состояний, при которых требуется релаксация гладких мышц.
35. Способ по пп. 32 и 34, отличающийся тем, что смешивание компонентов (А) и (В) осуществляют непосредственно перед введением пациенту, например, путем их совместного введения.
36. Способ по любому из пп. 32, 34 или 35, отличающийся тем, что смешивание осуществляют с помощью процесса смешанного потока.
37. Способ по п. 36, отличающийся тем, что процесс смешанного потока происходит в момент введения компонентов пациенту.
38. Применение по п. 33, отличающееся тем, что для лечения патологического состояния, при котором введение NO характеризуется положительным эффектом, отличающееся тем, что указанное патологическое состояние выбирают из группы, состоящей из легочной гипертензии различного генеза, включая первичную гипертензию и вторичную гипертензию; и острой сердечной недостаточности (с сохраненной или несохраненной фракцией выброса (HFpEF)).
| Nilsson, K | |||
| F., et al | |||
| Formation of new bioactive organic nitrites and their identification with gas chromatography-mass spectrometry and liquid chromatography coupled to nitrite reduction | |||
| Biochemical Pharmacology, 2011, 82(3), 248-259 | |||
| WO 2007106034 A1, 20.09.2007 | |||
| WO 9401103 A1, 20.01.1994 | |||
| Nilsson, K | |||
| F., et al | |||
| The novel nitric oxide donor |
Авторы
Даты
2024-11-22—Публикация
2019-11-27—Подача