Изобретение относится к медицине и фармацевтической промышленности, конкретно к составам питательных сред для временного хранения зубов, потерянных в результате травмы, либо удаленных по хирургическим показаниям, содержащих клетки периодонтальной связки зубов, в частности фибробласты.
Распространенность травмы зубов у детей составляет 9,75%, что является вторым по частоте встречаемости заболеванием зубов после кариеса и его осложнений (69,02%) [5]. Таким образом, в среднем каждый 10-й ребенок сталкивается с клинически значимой травмой зубов.
Полный вывих зуба составляет от 0,5 до 3,0% всех травматических повреждений зубов. При вывихе зуб теряет связь с альвеолярной частью челюсти, что приводит к повреждению тканей периодонтальной связки, включая клетки периодонта, кровеносные сосуды и нервные волокна.
Реплантация представляет собой эффективный метод лечения травм зубов, таких как полный вывих, экстракция, перелом коронки; перелом корня. Однако, прогноз приживаемости реплантированных зубов зависит от таких факторов, как временной интервал между потерей связи зуба с костной тканью и реплантацией, вид хранения зуба - сухое хранение или питательная среда, жизнеспособность тканей пародонта и пульпы, а также тип, вид и сроки фиксации зуба (шинирование). Важнейшим фактором, влияющим на послеоперационный прогноз приживаемости зубов, вывихнутых в результате травмы или удаленных по хирургическим показаниям после их реплантации, является использование правильно подобранных питательных сред [1].
Оптимальными и клинически рекомендованными составами для хранения вывихнутых/удаленных зубов являются сбалансированный солевой раствор Хенкса (HBSS) и пастеризованное молоко. Кроме того, имеются сведения об использовании для консервации клеток периодонта таких сред, как соевое молоко, экстракт алоэ вера, прополис, кокосовая вода и яичный белок. Среда HBSS считается лучшим составом во многих исследованиях благодаря сбалансированному рН и осмолярности, которые могут поддерживать жизнеспособность, клоногенность и митогенную способность клеток периодонтальной связки [2, 3].
Известен ряд технических решений, направленных на получение питательных сред для хранения клеток периодонта в условиях in vitro.
Так, известна питательная среда для консервации и транспортировки клеток для дальнейшего цитологического и иммуноцитохимического исследования, защищенная патентом РФ №2710226, G01N 33/48, A01N 1/02, A61K 11/00, опубл. 25.12.2019. Питательная среда, согласно данному изобретению, содержит стерильный 10%-ный раствор альбумина человека, дополнительно включает раствор средне молекулярной фракции частично гидролизованного декстрана в изотоническом растворе натрия хлорида и раствор азида натрия при следующем соотношении компонентов, мас. %:
стерильный 10%-ный раствор альбумина человека - 33,0-33,3;
раствор средне молекулярной фракции частично гидролизованного декстрана -33,0-33,3;
натрий хлорид - 33,32-33,94;
раствор азида натрия - 0,06-0,08.
Вышеописанная питательная среда позволяет повысить длительность хранения образца клеточного материала до 233,5 часов.
Питательная среда описанного состава не лишена недостатков, к основным из которых относятся наличие в ее составе высокотоксичного азида натрия, а также ее применение для консервации, в основном, опухолевых клеток, предназначенных для последующих цитологических и иммуноцитохимических исследований.
Также известна жидкость для консервации зубов человека in vitro и способ ее приготовления (патент CN 111955454 А, A01N 1/02, опубл. 20.11.2020). Жидкость для консервации зубов человека in vitro состоит из следующих компонентов: сывороточный альбумин человека, астаксантин, альфа-линоленовая кислота, цитрат натрия, цефепима гидрохлорид для инъекций, амфотерицин В, супернатант концентрированного раствора и раствор хлорида натрия для инъекций с массовой концентрацией 0,9%. Консервирующая жидкость сбалансирована по питательным компонентам, не оказывает токсического и побочного воздействия на клетки, поддерживает жизнеспособность клеток пульпы зуба in vitro на высоком уровне при температуре 2-8°С (до 7 суток), эффективно предотвращает попадание экзогенных микроорганизмов в клетки. К недостаткам описанной жидкости можно отнести необходимость хранения зубов в ней при низкой температуре 2-8°С. При повышении температуры хранения клеток периодонта в среде описанного состава их выживаемость снижается.
Наиболее близкой к заявляемому изобретению, выбранной в качестве ближайшего аналога, является новая жидкость для консервации витальных зубов in vitro и способ ее приготовления, защищенная патентом CN 109526940 A, A01N 1/02, опубл. 29.03.2019. Жидкость для сохранения зубов готовят следующим образом: добавляют 200 ед./мл пенициллина, 100 ед./мл стрептомицина, 200 мг/мл дексаметазона и 272 мг/мл L-глутамина в раствор HBSS, регулируют значение рН до 7,2-7,4, а затем фильтруют и стерилизуют. Экспериментально показано, что клетки периодонтальной связки сохраняют высокую жизнеспособность и способность к размножению после консервации зуба в консервирующей жидкости, предусмотренной изобретением, в течение 24 часов. В качестве основного недостатка жидкости согласно изобретению CN 109526940 A можно считать недостаточную выживаемость клеток периодонта при консервации более 24 часов.
Техническая проблема, решаемая предлагаемым изобретением, - создание питательной среды, обеспечивающей высокую жизнеспособность периодонта зуба, содержащего фибробласты, при температуре окружающей среды в течение 72 часов.
Технический результат от использования изобретения заключается в повышении жизнеспособности фибробластов зубной связки, при температуре окружающей среды и достижении длительных сроков их хранения и транспортировки.
Указанный технический результат достигается тем, что питательная среда для временного хранения зубов, вывихнутых в результате травмы или удаленных по хирургическим показаниям, периодонт которых содержит фибробласты, включает сбалансированный солевой раствор Хенкса (HBSS) и дополнительные компоненты при следующих концентрациях:
L-глутамин - 250,0 мг/л
L-аргинин гидрохлорид - 150,0 мг/л
экстракт зеленого чая - 0,8 об. %
парааминобензойная кислота - 0,52 мг/л
докозагексаеновая кислота - 0,75 мг/л
ванкомицин - 50 ед./мл
амфотерицин В - 50 ед./мл.
Значение рН питательной среды указанного состава находится на уровне 7,2-7,4. Заявляемый состав питательной среды является оптимальным с точки зрения получения наилучших результатов по выживаемости тканей, содержащих фибробласты.
Изобретение иллюстрируется фиг. 1, на которой приведены результаты оценки жизнеспособности клеток удаленного зуба после инкубации в питательной среде заявленного состава (а) и в контрольной (б) среде.
Для приготовления питательной среды указанного состава для хранения зубов, периодонт которых содержит фибробласты, все компоненты смешивают в указанных пропорциях. Температура хранения питательной среды - (4±2)°С. Хранение и транспортировка зубов, периодонт которых содержит фибробласты, в питательной среде заявленного состава могут производиться в течение 72 часов при температуре окружающей среды.
Питательная среда, согласно заявленному изобретению, может быть использована для временного хранения и транспортировки витальных либо авитальных зубов, предназначенных для реплантации, с целью сохранения жизнеспособности тканей периодонта зуба. В указанной питательной среде могут временно
храниться/консервироваться зубы, вывихнутые в результате травмы или удаленные в стоматологических медицинских учреждениях в ходе хирургического вмешательства.
Применение питательной среды заявленного состава предусматривает следующую последовательность операций. Для хранения и транспортировки зубов применяют культуральные пробирки с герметичной завинчивающейся крышкой. В культуральную пробирку помещается необходимый объем питательной среды для консервации, туда же погружается вывихнутый/удаленный зуб, после чего крышка завинчивается, и пробирка транспортируется при температуре окружающей среды в течение 72 часов.
Примеры использования питательной среды заявленного состава.
Пример 1
Питательная среда для хранения зубов, корень которых содержит фибробласты, готовится путем смешивания в дистиллированной воде компонентов в следующих концентрациях, мг/л:
натрия хлорид - 8000,0
калия хлорид - 400,0
калия дигидрофосфат - 60,0
натрия гидроортофосфат - 48,0
магния хлорид - 47,0
магния сульфат 7-водный - 100,0
кальция хлорид 2-водный - 185,45
D-глюкоза- 1000,0
L-глутамин - 250,0
L-аргинин гидрохлорид - 150,0
парааминобензойная кислота - 0,52
докозагексаеновая кислота - 0,75
экстракт зеленого чая - 0,8 об. %
ванкомицин - 50 ед./мл
амфотерицин В - 50 ед./мл.
Отличием питательной среды заявленного состава от известного сбалансированного солевого раствора Хенкса (HBSS) является включение в ее состав источников азота (L-глутамин, L-аргинин гидрохлорид), полиненасыщенной незаменимой жирной кислоты (докозагексаеновой), аминокислоты, участвующей в процессах синтеза пуриновых и пиримидиновых оснований (парааминобензойной кислоты), компонента антиоксидантного действия (экстракт зеленого чая), а также компонентов антибактериального (ванкомицин) и противогрибкового (амфотерицин В) действия.
Пример 2
Для подтверждения способности питательной среды заявленного состава обеспечивать высокую жизнеспособность вывихнутых/удаленных зубов проведен эксперимент.В культуральную пробирку помещался необходимый объем питательной среды, приготовленной по примеру 1, затем в эту пробирку погружался удаленный зуб, после чего крышка завинчивалась, и пробирка выдерживалась при температуре окружающей среды в течение 72 часов. Аналогичным образом осуществлялось инкубирование удаленного зуба в коммерческом растворе DentoSafe (производитель Hager Werken, Дуйсбург, Германия).
В определенные периоды хранения (24, 36, 48, 60 часов) и по окончании консервации (72 часа) для обоих образцов (тестового и контрольного) устанавливалась выживаемость клеток удаленного зуба в соответствии с протоколом, описанным в работе RajendranH др. [4]. Каждый образец промывался буферным раствором PBS, после чего вносился в пробирку объемом 15 мл, содержащую раствор коллагеназы тип 4 и трипсина на 10 минут. Образец инкубировался при температуре 37°С в атмосфере СО2 (5%) в течение 7 минут. На заключительных 2-3 минутах инкубации для стимуляции отделения клеток образец ресуспендировали. После инкубирования 1 мл суспензии с отделенными клетками в растворе коллагеназы тип 4 и трипсина был помещен в пробирку объемом 2 мл. К данному объему добавлялось 10 мкл фетальной бычьей сыворотки (FBS). Затем растворы центрифугировались при 90 g в течение 4 минут. По окончании центрифугирования супернатант удалялся и осадок растворялся в 400 мкл буфера PBS. Клеточная масса окрашивалась с использованием 0,4%-ного раствора трипанового синего в пропорции 1:1 (100 мкл исследуемого раствора и 100 мкл трипанового синего). После этого осуществлялось микроскопирование образцов с использованием инвертированного светового микроскопа Leica DM 3000 (Leica Camera AG, Германия) с 40-кратным увеличением, а также подсчет клеточной жизнеспособности с использованием автоматического счетчика клеток Countess II FL Automated Cell Counter (Thermo Fisher Scientific, США).
Результаты оценки жизнеспособности клеток удаленного зуба после инкубации в питательной среде заявленного состава, в сравнении с контрольным раствором, в течение 24, 36,48, 60 и 72 часов приведены на фигуре 1.
Как следует из фиг. 1, питательная среда заявленного состава обеспечивает высокую выживаемость (не ниже 92%) клеток периодонта удаленного зуба вплоть до 48 часов, после чего отмечается снижение выживаемости клеток. Результаты эксперимента сопоставимы с данными, полученными для контрольного раствора DentoSafe. Важно отметить, что хранение вывихнутых/удаленных зубов в питательной среде более 72 часов нецелесообразно, так как за этот период времени в лунке зуба альвеолярного отростка челюсти происходят изменения, которые приводят к резкому ухудшению прогноза приживаемости реплантированных зубов.
Приведенные примеры могут служить иллюстрацией преимуществ заявленного состава питательной среды для временного хранения вывихнутых или удаленных зубов, поверхность корней которых содержит фибробласты, а именно:
- высокая жизнеспособность клеток удаленных зубов (не ниже 92%) при хранении в среде заявленного состава в течение 48 часов (не ниже 85% в течение 72 часов):
- возможность хранения и транспортировки зубов в описанной питательной среде при температуре окружающей среды.
Литература:
1. Clinical and practical implications of storage media used for tooth avulsion / V.I. Khinda, G. Kaur, G. S Brar, et al. // International Journal of Clinical Pediatric Dentistry. - 2017. - Vol. 10(2). - P. 158-165.
2. Effect of temperature and storage media on human periodontal ligament fibroblast viability / B.D.M. Souza, 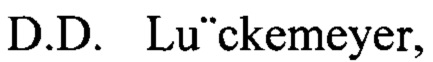 W.T. Felippe, et al. // Dental Traumatology. - 2010. - Vol. 26. - P. 271-275.
W.T. Felippe, et al. // Dental Traumatology. - 2010. - Vol. 26. - P. 271-275.
3. Evaluation of conditioned medium from placenta-derived mesenchymal stem cells as a storage medium for avulsed teeth: An in vitro study / L.-L. Ji, G. Song, L.-M. Jiang, et al. // Dental Traumatology. - 2021. - Vol. 37. - P. 73-80.
4. Rajendran, P. Evaluation, using extracted human teeth, of Ricetral as a storage medium for avulsions - an in vitro study / P. Rajendran, N.O. Varghese, J.M. Varughese, E. Muragaian // Dental Traumatology. - 2011. - Vol. 27. - P. 217-220.
5. Структура травматических повреждений временных зубов у детей г. Екатеринбурга И.М. Макеева, М.В. Сарапульцева //Пермский медицинский журнал 2011 том XXVIII №6 стр. 19-24.
| название | год | авторы | номер документа |
|---|---|---|---|
| Гидрогель для регенерации пульпы зуба и периодонта | 2019 |
|
RU2700933C1 |
| Способ индукции спонтанной дифференцировки клеток периодонтальной связки и надкостницы в одонтогенном и остеогенном направлениях путем использования децеллюляризированного матрикса зуба и периодонтальной связки человека | 2022 |
|
RU2813729C1 |
| СПОСОБ КОРРЕКЦИИ СТРУКТУРНО-ФУНКЦИОНАЛЬНЫХ ИЗМЕНЕНИЙ СОЕДИНИТЕЛЬНОЙ ТКАНИ | 2005 |
|
RU2277423C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДГЕЗИВНОЙ КУЛЬТУРЫ НЕЙТРАЛЬНЫХ СТВОЛОВЫХ/ПРОГЕНИТОРНЫХ КЛЕТОК ОБОНЯТЕЛЬНОЙ ВЫСТИЛКИ НОСА МЛЕКОПИТАЮЩИХ ДЛЯ ЛЕЧЕНИЯ ТРАВМ СПИННОГО МОЗГА | 2020 |
|
RU2749156C1 |
| Способ имплантации искусственного зуба | 2017 |
|
RU2649452C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГОМОГЕННОЙ ПОПУЛЯЦИИ СТВОЛОВЫХ КЛЕТОК И ЕЕ ПРИМЕНЕНИЕ | 2007 |
|
RU2433172C2 |
| Способ получения ноотропной композиции на основе полипептидных комплексов, выделенных из нейронов и глиальных клеток, полученных методом направленной дифференцировки индуцированных плюрипотентных стволовых клеток человека | 2018 |
|
RU2690498C1 |
| СПОСОБ, ПРОБИРКА И УСТРОЙСТВО ДЛЯ ПРИГОТОВЛЕНИЯ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2011 |
|
RU2667964C1 |
| СПОСОБ, ПРОБИРКА И УСТРОЙСТВО ДЛЯ ПРИГОТОВЛЕНИЯ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2011 |
|
RU2614722C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ОБКЛАДОЧНЫХ КЛЕТОК ОБОНЯТЕЛЬНОЙ ВЫСТИЛКИ МЛЕКОПИТАЮЩИХ ДЛЯ ЛЕЧЕНИЯ ТРАВМ СПИННОГО МОЗГА | 2017 |
|
RU2676142C2 |
Изобретение относится к области биотехнологии, в частности к составу питательной среды для временного хранения зубов, вывихнутых в результате травмы или удаленных по хирургическим показаниям. Указанный состав содержит L-глутамин в концентрации 250,0 мг/л, L-аргинин гидрохлорид в концентрации 150,0 мг/л, 0,8 об. % экстракта зеленого чая, парааминобензойную кислоту в концентрации 0,52 мг/л, докозагексаеновую кислоту в концентрации 0,75 мг/л, ванкомицин в концентрации 50 ед./мл, а также амфотерицин В в концентрации 50 ед./мл. Настоящее изобретение обеспечивает повышение жизнеспособности фибробластов зубной связки при температуре окружающей среды и достижение длительных сроков их хранения и транспортировки. 1 ил., 2 пр.
Состав питательной среды для временного хранения зубов, вывихнутых в результате травмы или удаленных по хирургическим показаниям, включающий сбалансированный солевой раствор Хенкса (HBSS), отличающийся тем, что включает дополнительные компоненты при следующих концентрациях:
- L-глутамин - 250,0 мг/л;
- L-аргинин гидрохлорид - 150,0 мг/л;
- экстракт зеленого чая - 0,8 об. %;
- парааминобензойная кислота - 0,52 мг/л;
- докозагексаеновая кислота - 0,75 мг/л;
- ванкомицин - 50 ед./мл;
- амфотерицин В - 50 ед./мл.
| CN 111955454 A, 20.11.2020 | |||
| US 11224217 B2, 18.01.2022 | |||
| JI YOUNG HWANG et al., The Use of Green Tea Extract as a Storage Medium for the Avulsed Tooth, Journal of endodontics, 2011, 37(7), pp | |||
| Способ гидрогенизации жиров, масел, жирных кислот из них и других непредельных органических соединений | 1913 |
|
SU962A1 |
| ЛИТВИНОВ С | |||
| Д | |||
| и др., Применение материала "ЛитАр" на альгинатной основе для консервации лунки зуба, Вестник медицинского института "Реавиз": | |||
Авторы
Даты
2024-12-09—Публикация
2024-03-25—Подача