Группа изобретений относится к медицине, к разделу травматологии и ортопедии, и может быть использована для создания персонифицированного бедренного компонента эндопротеза тазобедренного сустава (далее: «бедренный компонент»), используемого для оперативного лечения в объеме ревизионного эндопротезирования тазобедренного сустава, в частности для выполнения одноэтапного или для второго этапа двухэтапного ревизионного эндопротезирования тазобедренного сустава при лечении пациентов с индивидуальными антропометрическими особенностями, с имеющимся выраженным дефицитом костной массы бедренной кости.
В настоящее время эндопротезирование тазобедренного сустава является одной из самых успешных операций, активно применяемой при различных патологиях тазобедренного сустава [1]. По мере освоения хирургических технологий и увеличения количества выполняемых вмешательств по имплантации тазобедренных эндопротезов все чаще возникают вопросы лечения осложнений, которые неизбежно сопровождают любое хирургическое вмешательство в целом [2]. Развитие таких серьезных осложнений, как глубокая перипротезная инфекция, асептическое расшатывание компонентов эндопротеза, перипротезный перелом, износ пары трения и последующий остеолиз, требует последующего хирургического лечения в объеме ревизионного эндопротезирования тазобедренного сустава.
Успех ревизионных операций и отдаленных результатов после проведенного лечения зависят не только от квалификации операционной бригады и оснащения качественным специальным хирургическим инструментарием, но также от выбора самого импланта. Он должен максимально соответствовать требованиям, представленным в ходе предоперационного планирования, которые могут быть различными в зависимости от показаний к оперативному вмешательству, антропометрических особенностей, возраста, соматического состояния самого пациента, качества костной ткани, ее возможного остеогенного потенциала, наличия дефектов, и от планируемой дальнейшей тактики лечения.
На сегодняшний день существует довольно широкий выбор имплантов и, в частности, бедренных компонентов эндопротеза тазобедренного сустава различных размеров и форм, изготовленных из разнообразных материалов, с различным покрытием, предназначенным для цементного или бесцементного способов фиксации. Если в большинстве случаев первичного эндопротезирования выбор подходящих для данного пациента компонентов эндопротеза не представляется серьезной проблемой, то в случае необходимости ревизионного эндопротезирования (как одноэтапного, так и второго этапа двухэтапного) врач может столкнуться с отсутствием на рынке медицинских изделий бедренного компонента эндопротеза, который полностью соответствовал бы требованиям, установленным в ходе предоперационного планирования, и возместил бы бедренную составляющую эндопротеза.
Каждый вид бедренного компонента эндопротеза массового производства тазобедренного сустава имеет свои показания и противопоказания для имплантации, которые зависят от формы бедренной кости, величины шеечно-диафизарного угла, размера и формы канала бедренной кости, состояния костной ткани, а также объема деструкции и дефицита костной ткани бедренной кости. В ряде случаев невозможно подобрать «универсальный» бедренный компонент той или иной формы таким образом, чтобы он соответствовал всем требованиям, представленным в ходе предоперационного планирования, для данного клинического случая.
Стоит учитывать, что в периоде между первым и вторым этапами ревизионного эндопротезирования, а также после первичного эндопротезирования костная ткань в процессе активизации пациента может подвергаться неизбежным процессам ремоделирования, таким как образование участков остеопороза, остеолиза, расшатывание и миграция компонентов, которые могут рассматриваться как следствие реактивных изменений и резорбции костной ткани в ответ на возникшую переменную нагрузку, а также неадекватность функциональных напряжений, испытываемых костью в зоне контакта с протезом [3]. Также нередки случаи периимплантных переломов - 2,28 % среди всех причин ревизионных вмешательств на тазобедренном суставе на 2019 год [4].
По другим данным перипротезные переломы – одно из наиболее частых осложнений эндопротезирования. По частоте они уступают только позднему расшатыванию компонентов сустава, составляя от 0,7 до 11% после первичных операций и 4-25% после ревизий [5].
Подавляющее большинство перипротезных переломов бедра происходит у пациентов с имплантом бесцементной фиксации. И, учитывая тенденцию к росту числа операций эндопротезирования протезами с бесцементным способом фиксации, следует ожидать статистически значимый рост абсолютного числа случаев перипротезных переломов [6].
Все перечисленные факторы могут приводить к появлению дефицита и качественным дефектам костной ткани на различных участках предполагаемой имплатации бедренного компонента ревизионного эндопротеза, при этом некоторые участки костной ткани могут оставаться интактными.
Для выхода из сложившейся ситуации, травматологам-ортопедам приходится делать выбор в пользу имплантов бóльших размеров для обеспечения стабильной фиксации компонента, что заставляет применять более агрессивные хирургические техники, расширенный хирургический доступ, менее щадящее отношение к мягким тканям и самой кости, а также использование дополнительных фиксаторов (пластин, тросов, винтов) в случае остеотомии или интраоперационных переломов. Также большие костные дефекты, плохое качество костной ткани и ее сниженный остеогенный потенциал заставляет врачей отдавать предпочтение цементному способу фиксации, лишаясь всех преимуществ бесцементного способа, который мог бы быть использован на участках с сохранной костной тканью.
Сутью тотального бесцементного эндопротезирования является прецизионная импакция бедренного компонента эндопротеза, фиксация поверхности эндопротеза к перипротезной костной ткани без промежуточных третьих сред (адгезивов), за счет плотного контакта с окружающими костными трабекулами. Преимущества бесцементной фиксации: меньший риск возникновения осложнений, прогнозируемая более стабильная фиксация за счет остеоинтеграции, возможность регенерации костной ткани в периимплантной зоне. Недостатки: больший риск развития синдрома стресс-шилдинг, высокий риск возникновения интраоперационных переломов. Суть тотального цементного эндопротезирования заключается в использовании адгезива (далее: «костного цемента»), с помощью которого эндопротез плотно фиксируется в бедренной кости. Критерии выбора: пациенты с выраженным остеопорозом, с неудовлетворительным предполагаемым остеогенным потенциалом и качеством кости, пациенты пожилого возраста и т.п. Преимущества: меньший стресс-шилдинг, меньший риск интраоперационных переломов. Недостатки: сложности при дальнейшем ревизионном вмешательстве, которые связаны с удалением цемента из канала бедренной кости, нагревание цемента приводит к термическому периферическому остеолизу, отсутствие возможности репарации костной ткани в зоне фиксации эндопротеза [6].
Таким образом, в ряде случаев ревизионного эндопротезирования, при больших костных дефектах, снижении качества костной ткани на отдельных участках и сохранности костной ткани на других участках, а также при наличии антропометрических и анатомических особенностей пациента, стандартный бедренный компонент эндопротеза не всегда подходит, и возникает потребность в применении персонифицированного для данного пациента компонента эндопротеза с возможностью выбора его размеров и формы, а также с учетом протяженности участков поверхности компонента эндопротеза, предназначенных для цементного и бесцементного способа фиксации.
При подборе бедренного компонента эндопротеза важно учитывать такие параметры как шеечно-диафизарный угол и офсет (горизонтальное расстояние между вершиной конуса бедренного компонента и продольной осью тела ножки), величина которого зависит от шеечно-диафизарного угла и длины шейки бедренного компонента эндопротеза. Эти параметры бедренного компонента эндопротеза также должны соответствовать анатомическим особенностям тазобедренного сустава пациента. Выбор бедренного компонента эндопротеза с различным способом фиксации на его протяжении, а также размеры импланта и его форма, величина шеечно-диафизарного угла и офсета должен осуществляться на основании данных предоперационного планирования. Это создает необходимость применения аддитивных технологий и персонализированный подход к выбору бедренного компонента. В связи с этим становится очевидна актуальность применения 3D печати бедренного компонента, который бы идеально подошел для пациента, которому невозможно адекватно подобрать бедренный компонент исходя из стандартизированного пула имплантов представленного на рынке.
Технической проблемой, на решение которой направлена группа изобретений, является необходимость создания монолитного индивидуального бедренного компонента эндопротеза тазобедренного сустава, обеспечивающего возможность персонифицированного подбора его размеров, формы, величины шеечно-диафизарного угла и офсета, а также протяженности участков поверхности корпуса и ножки, предназначенных для разных способов фиксации: с помощью костного цемента в зонах с дефектами костной массы или неудовлетворительным качеством костной ткани и ее низким остеогенным потенциалом, и с бесцементным способом фиксации на участках сохранной костной ткани. Данная комбинация позволит добиться персонифицированого использования преимуществ разных типов фиксации на различных участках предполагаемой имплантации, с учетом качества костной ткани, предпочтительных для выбора каждого способа фиксации (цементного и бесцементного), а также уменьшить степень хирургической травматичности вследствие возможности подбора бедренного компонента с идеально подходящим размером и формой для данного пациента, а не ограниченного выбора имплантов, предлагаемых современной медицинской промышленностью массового производства. Спланированный, разработанный и изготовленный 3D компонент будет полностью соответствовать предъявляемым требованиям к установке и фиксации персонифицированного бедренного компонента при операции ревизионного эндопротезирования тазобедренного сустава. Таким образом индивидуально изготовленный бедренный 3D компонент эндопротеза позволит добиться улучшения качества жизни и конечного функционального результата пациентов с выраженными костными дефектами и локальными дефектами качества костной ткани бедренной кости. Также можно с уверенностью сказать, что данная методика изготовления бедренного компонента эндопротеза будет востребована как при особо сложном первичном, так и в сложных случаях одноэтапного и 2-го этапа ревизионного эндопротезирования после удаления спейсера и позволит компенсировать недостатки техники только цементного или бесцементного эндопротезирования, добившись стабильной гибридной фиксации на всем протяжении установленного бедренного компонента.
На сегодняшний день существует множество стандартизированных моделей бедренных компонентов эндопротеза, используемых для ревизионного эндопротезирования тазобедренного сустава. Самыми часто используемыми являются ревизионные бедренные компоненты, а также онкологические импланты. Они имеют шероховатую поверхность с покрытием, предназначенным для остеоинтеграции. Их преимуществами являются большая размерная линейка с возможностью выбора длины ножки и дистальный тип фиксации. Однако длина бедренного компонента все равно остается фиксированной. К примеру, у компонента Wagner Revision размерная линейка представлена 190, 225, 265, 305 мм. А если хирургам требуется длина, к примеру 210 мм, приходится рассверливать бедренную кость под компонент больших размеров, то есть под 225 мм.
Прямая форма ножки, отсутствие анатомических персонифицированных изгибов не может повторять естественную геометрию бедренной кости, которая имеет изгибы в нескольких плоскостях, а в некоторых случаях имеет угловую деформацию вследствие посттравматических и постинфекционных изменений. В этом случае имплантация длинной прямой ножки создает риск интраоперационного перелома и/или выхода дистальной части ножки за кортикальный слой. Также диафиз бедренной кости может быть подвергнут дегенеративным изменениям и иметь дефект, что делает его непригодным для бесцементной фиксации.
Максимально приближенным прототипом является модульный бедренный компонент эндопротеза, которые на данный момент применяются при ревизионном эндопротезировании тазобедренного сустава в случае невозможности адекватной стабильной фиксации в костномозговом канале бедренной кости стандартного бедренного компонента. Данный бедренный компонент содержит шеечную часть на верхнем конце, предназначенную для посадки шарнирной головки, поверхность которой выполнена для безадгезивной фиксации в проксимальном эпиметафизе и диафизе, а ее размер в длину выбран для обеспечения его простирания в диафиз кости, и дистальный модуль, примыкающий к шеечной части, который представляет собой съемную часть бедренного компонента, размер длины которого подобран таким, что его вершина простирается в дистальный эпиметафиз кости.
Также использование модульных систем при эндопротезировании тазобедренного сустава позволяет оптимально восстановить анатомические параметры конечностей (оффсет, длину, антеверсию) и обеспечить хорошую и долгосрочную их функцию. Однако создание дополнительного узла может вести к новым, иногда специфическим, неприятностям, возникающим в том числе и в ходе неизбежных ревизионных операций [8].
Недостатками данного прототипа является фиксация его дистального модуля в дистальном метаэпифизе бедренной кости и как следствие необходимость хирургического воздействия на интактную часть кости (дистальный метаэпифиз). Стоит подчеркнуть, что участок соединения двух модулей наиболее подвержен фреттинг-коррозии и усталостным переломам металлоконструкции, так как конструкция не является монолитной и участок крепления менее толерантен к нагрузкам на излом [8,10].
В ходе одного из исследований проведен анализ осложнений операций (31 случай) в период с 2010-го по 2020 год, когда по разным причинам проводилась операция ревизии эндопротезов тазобедренного сустава с модульными бедренными компонентами, 5 случаев составили переломы шейки эндопротеза (16 % от всех осложнений, 1,6 % от всех установленных протезов) именно в месте соединения двух частей модульного бедренного компонента [8].
Некоторые авторы в проведенных исследованиях отмечают меньший процент случаев развития стресс-шилдинг синдрома в так называемой High Contact Group, то есть в группе, где имплант надежно фиксирован в кости на значительном своем протяжении, и, напротив, высокий риск развития стресс-шилдинг синдрома и, как следствие расшатывание, компонента с дистальным типом фиксации [9].
Сущность предлагаемой группы изобретений пояснена следующими графическими материалами:
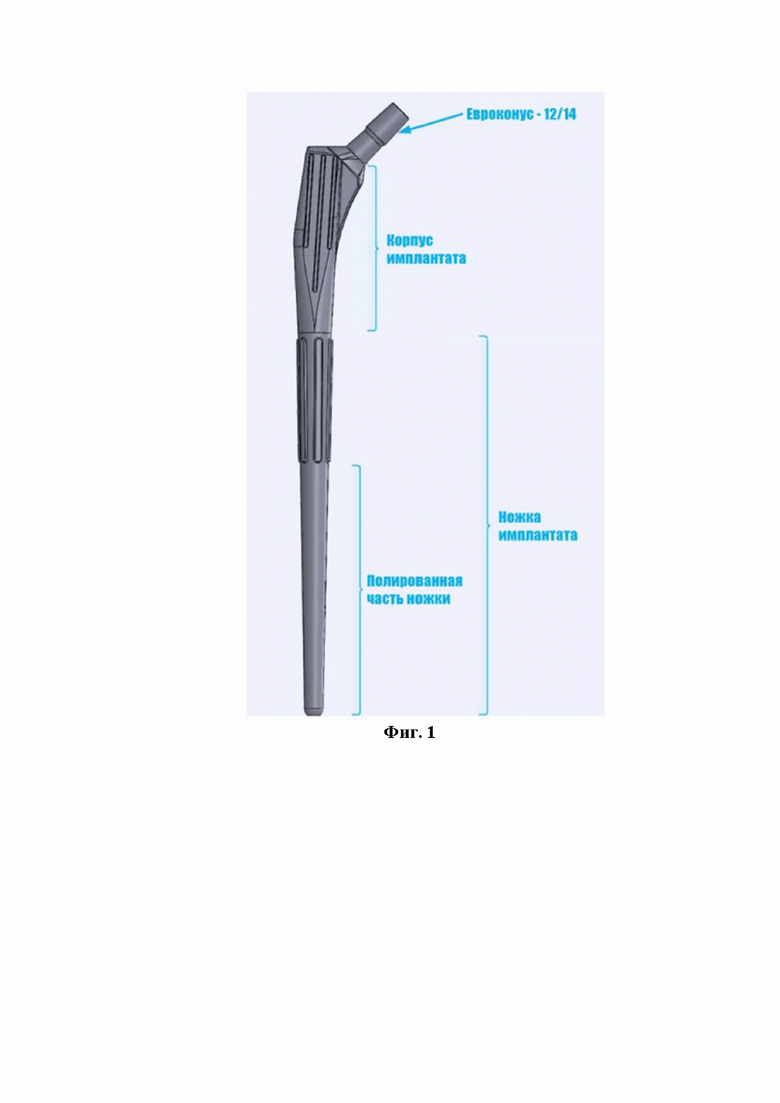
Фиг. 1 – Вид индивидуально изготовленного бедренного компонента эндопротеза, где представлены:
- евроконус,
- корпус,
- ножка эндопротеза,
- пример участка с полированной поверхностью для цементного способа фиксации,
- пример участка с ребристо-пористой поверхностью для бесцементного способа фиксации.
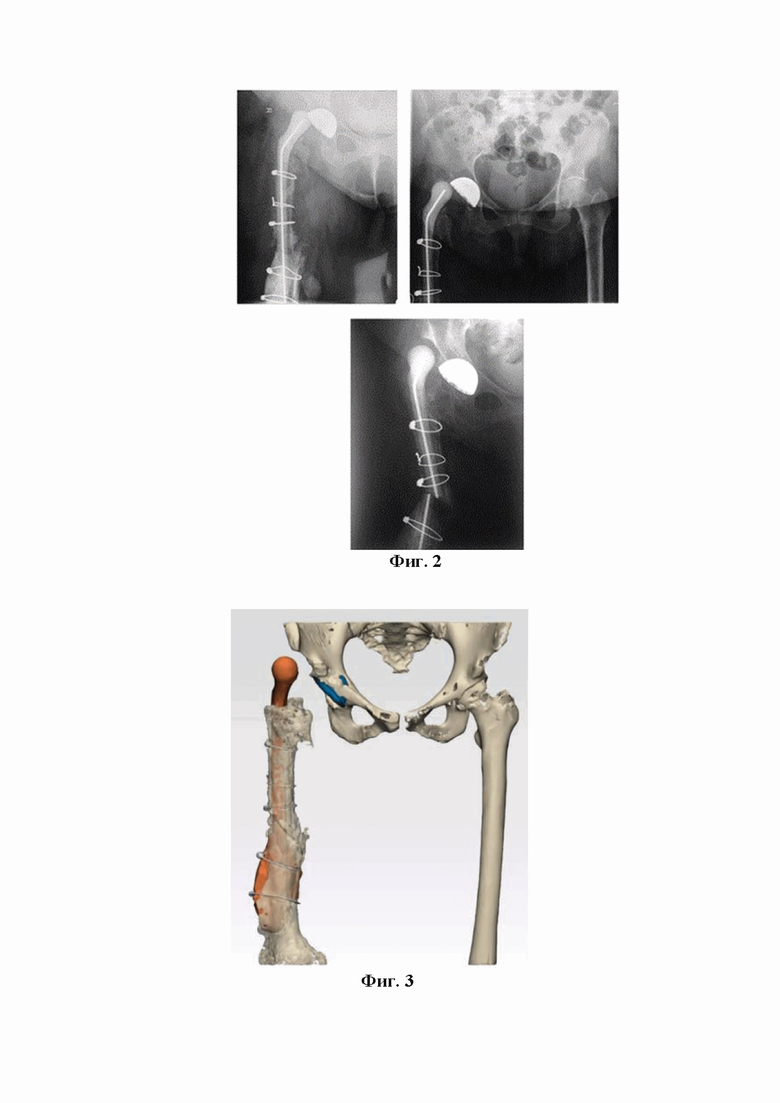
Фиг. 2 - Рентгенологическая картина вывиха и перелома ножки бедренного компонента спейсера правого тазобедренного сустава.
Предоперационные рентгенограммы правой бедренной кости с захватом тазобедренного сустава:
- На первом рисунке: рентгенограмма тазобедренного сустава в прямой проекции, на которой визуализируется вывих головки спейсера.
- На втором рисунке: прямая проекция тазобедренного сустава и средней трети бедренной кости: отмечается дефект костной массы большого вертела бедренной кости, дефект латеральной стенки бедренной кости на уровне нижней трети, замещенный костным цементом, а также явления остеопороза бедренной кости (отмечаются на всех 3 рисунках).
- На третьем рисунке отмечается перелом ножки спейсера.
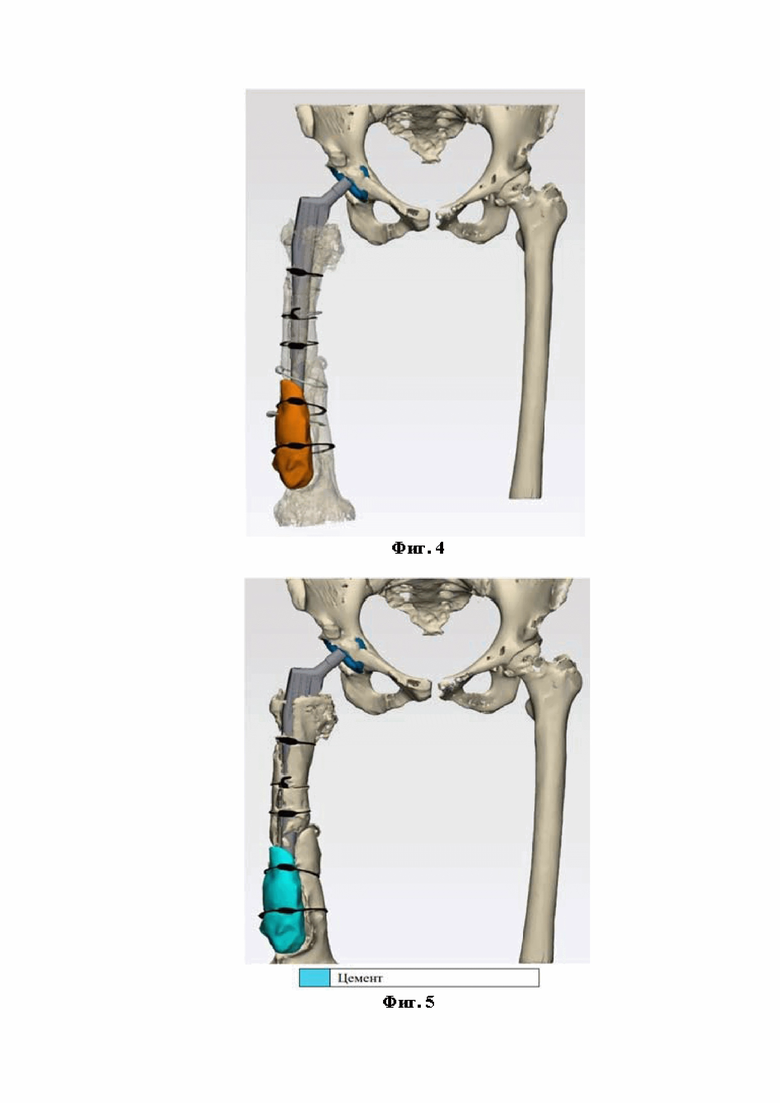
Фиг. 3 – Компьютерная модель тазобедренного сустава до операции (с антибактериальным спейсером).
Фиг. 4 – Компьютерная модель позиционирования импланта после операции.
Фиг. 5 – Компьютерная модель позиционирования импланта тазобедренного сустава, на которой более точно представлено изображение способ фиксации компонентов.
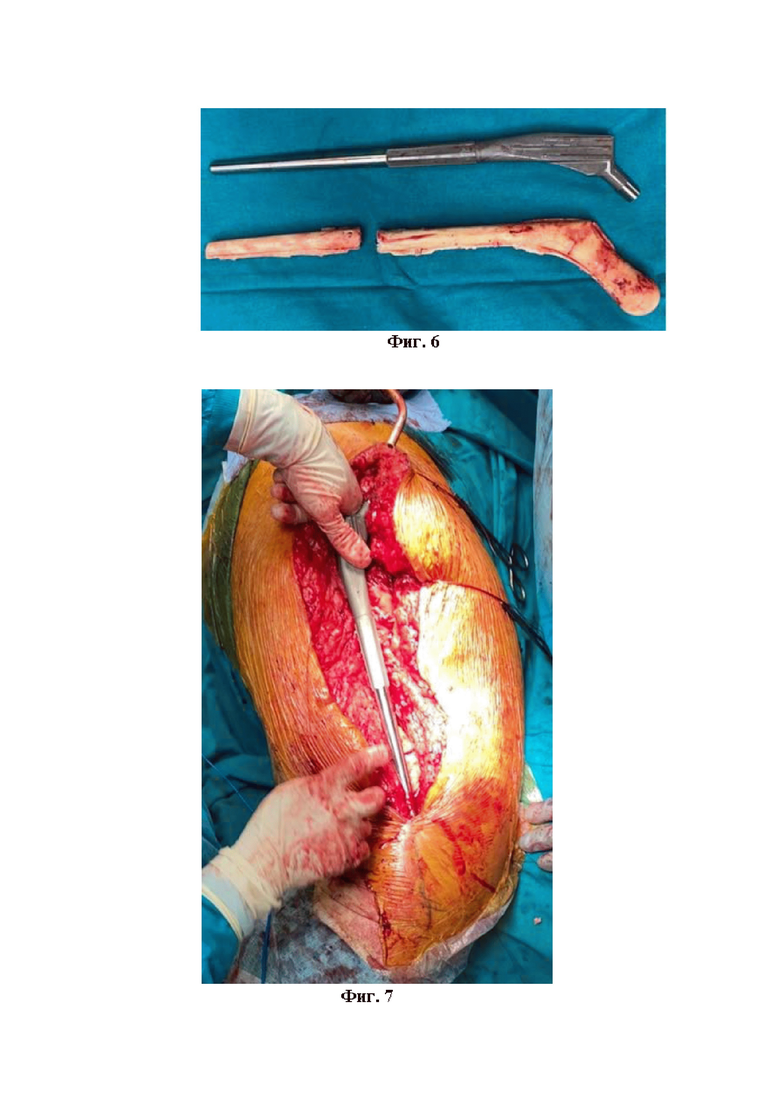
Фиг. 6 - Внешний вид индивидуально изготовленного бедренного компонента эндопротеза и спейсера.
Фиг. 7 – Интраоперационная примерка бедренного компонента.
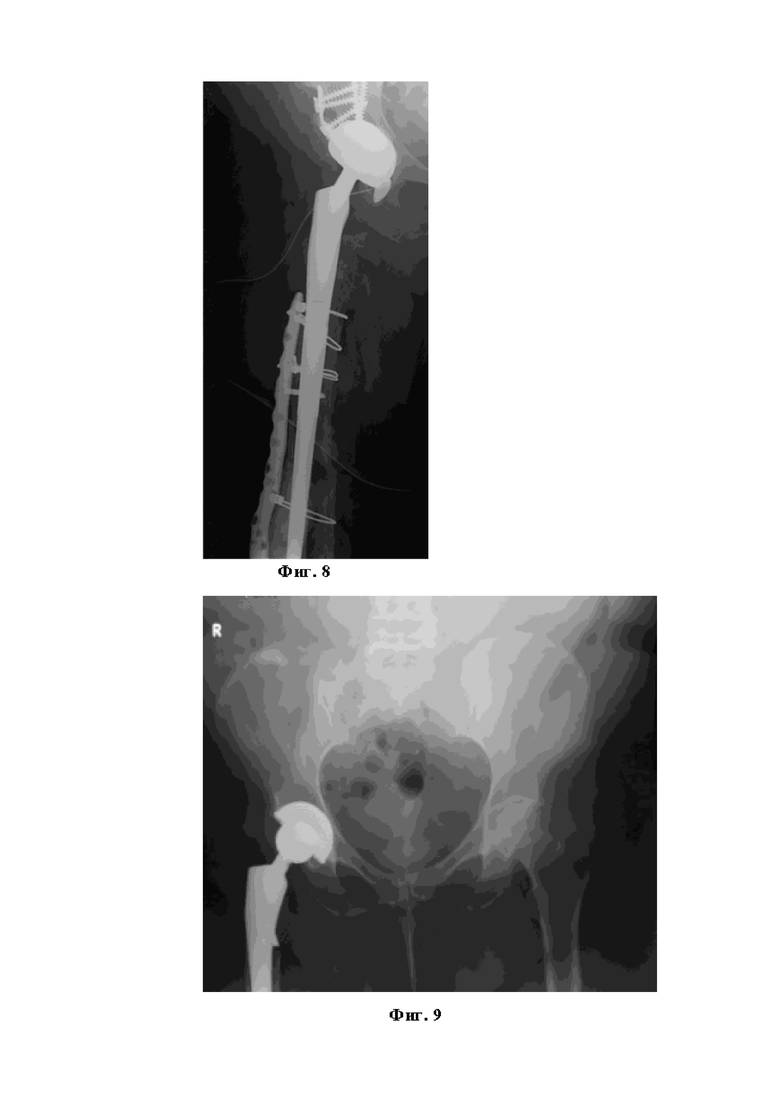
Фиг. 8 – Общая рентгенологическая картина установленного ревизионного эндопротеза тазобедренного сустава. Перелом бедренной кости фиксирован серкляжами и пластиной.
Фиг. 9 – Рентгенологическая картина тотального эндопротезирования правого тазобедренного сустава. Правильное и стабильное положение компонентов эндопротеза.
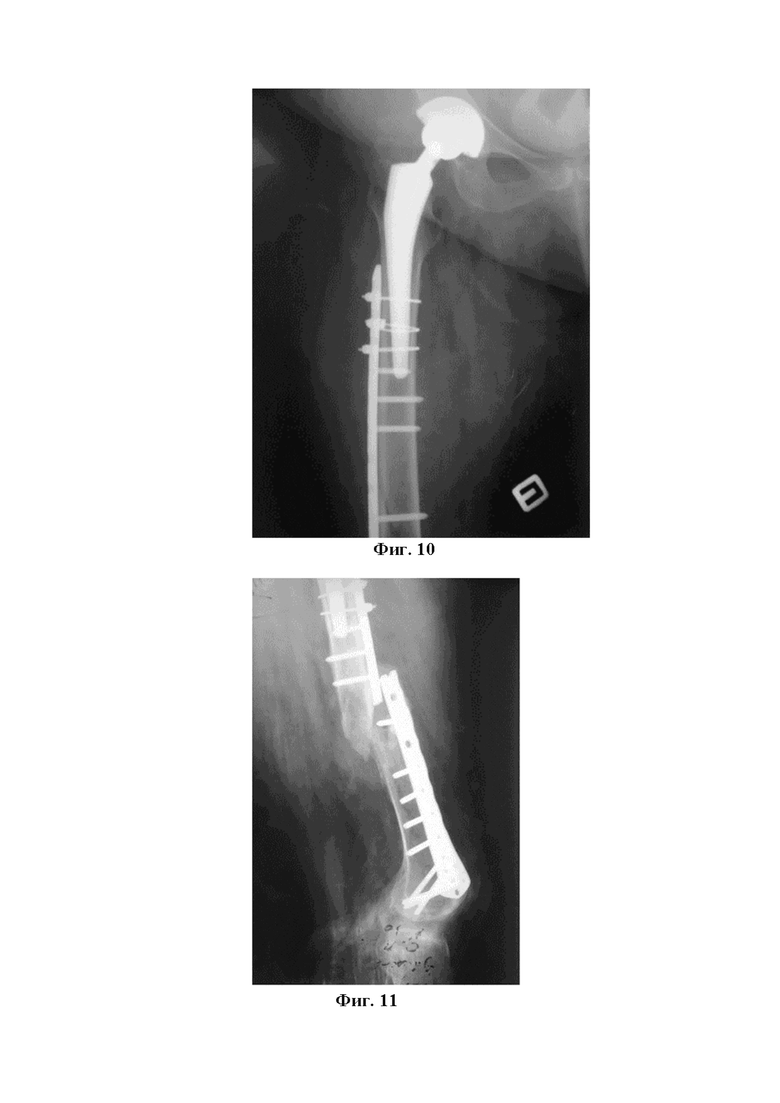
Фиг. 10 – Остеосинез перипротезного перелома пластиной. Фиксация стабильная.
Фиг. 11 – Рефрактура бедренной кости, перелом пластины.
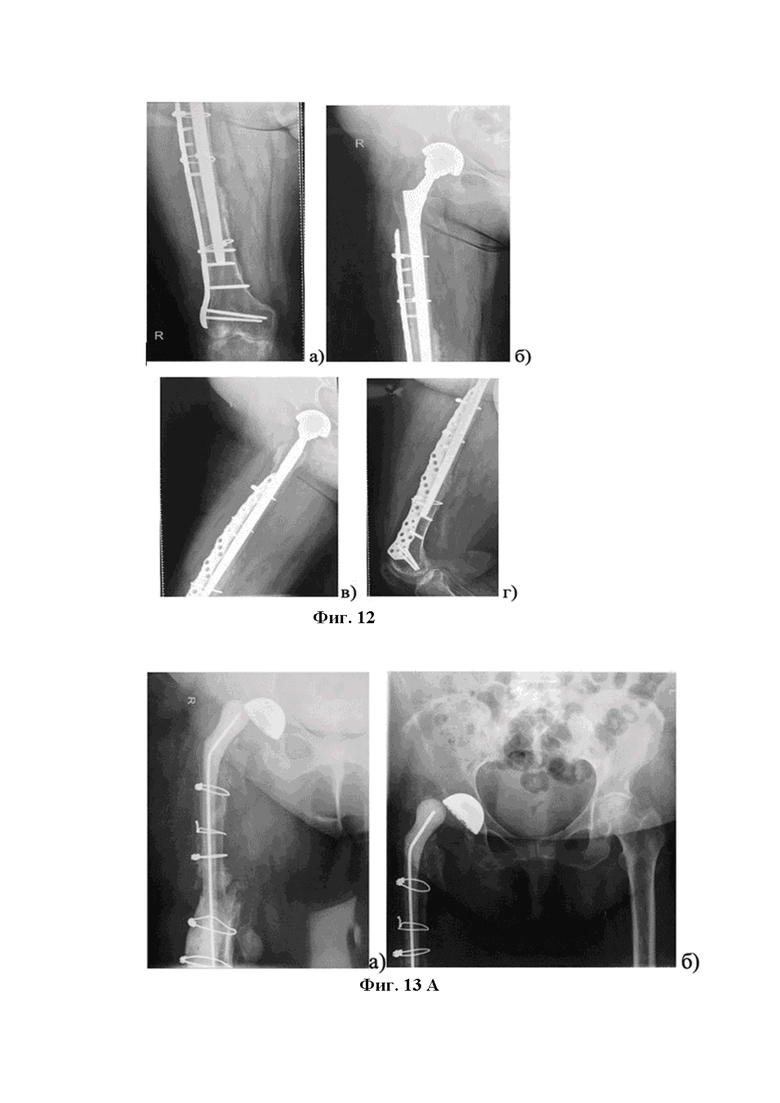
Фиг. 12 – Рентгенологическая картина после ревизионного эндопротезирования правого тазобедренного сустава: замена ножка и остеосинтез пластиной NBC.
Фиг. 13 А – На рентгенограммах а) и б) определяется вывих головки антимикробного спейсера.
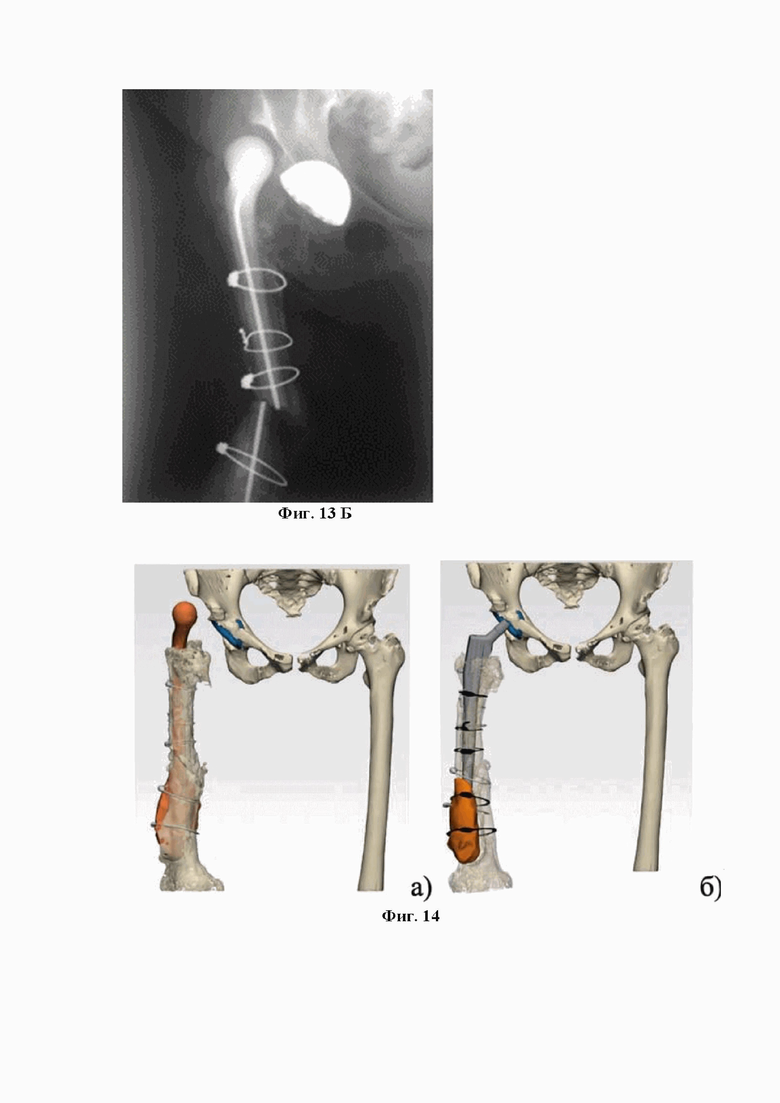
Фиг. 13 Б – На рентгенограмме определяется перелом ножки антимикробного спейсера, перелом бедренной кости.
Фиг. 14 – а) Компьютерная 3D модель таза и бедренной кости со всеми дефектами костной ткани;
б) Компьютерная 3D модель таза, бедренной кости и ревизионного эндопротеза после: предполагаемое позиционирование 3D бедренного компонента.
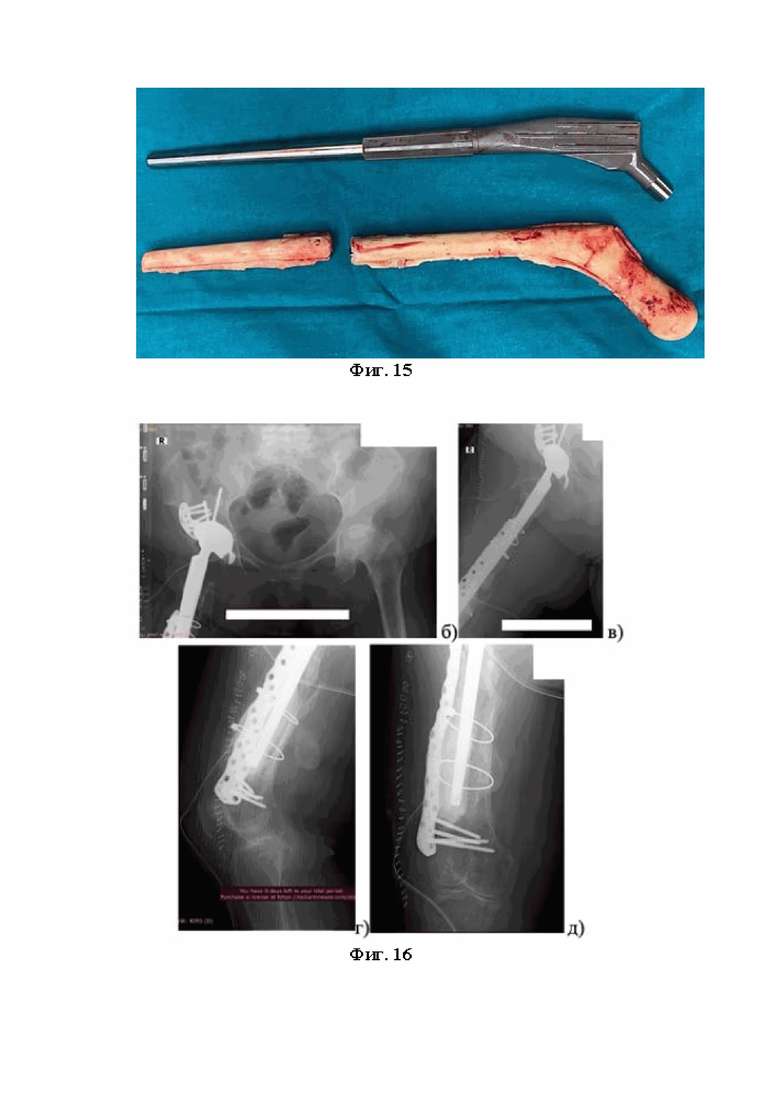
Фиг. 15 – Внешний вид удаленного антимикробного спейсера (определяется перелом его ножки) и индивидуального 3D бедренного компонента.
Фиг. 16 – Послеоперационные рентгенограммы: правильное и стабильное положение компонентов эндопротеза. Дефект дистальной части бедренной кости замещен костным цементом, перелом бедренной кости фиксирован тросами и пластиной.
Предлагаемая нами индивидуальная конструкция является монолитной и не имеет очевидных механически слабых мест на своем протяжении. При этом четко подобранная в ходу предоперационного планирования геометрическая форма точно повторяет изгиб канала бедренной кости пациента во всех плоскостях, что обеспечивают надежную фиксацию на всем своем протяжении и, как следствие, равномерное распределение нагрузки на компонент и на кость, что в дальнейшем предотвращает расшатывание компонента.
Персонифицированный 3D бедренный компонент эндопротеза представляет собой монолитную конструкцию и состоит из евроконуса, корпуса импланта с отверстием для установки импактора, размер и форма которого подходят для стандарного импактора, входящего в набор инструментов для эндопротезирования, а также ножки, имеющий подобранные в ходе предоперационного планирования геометрическую форму точно повторяющую изгиб канала бедренной кости пациента во всех плоскостях, размеры компонента, величину шеечно-диафизарного угла, офсета и антеверсии шейки, при этом корпус и ножка имеют на своем протяжении чередующиеся участки поверхностей полированного и ребристо-пористого покрытия, предназначенных для цементного и бесцементного способов фиксации (Фиг. 1).
И основное преимущество предложенной нами конструкции заключается в том, что она не предполагает использование для фиксации дистального интактного участка кости и позволяет избежать излишней хирургической агрессии по отношению к здоровой кости.
Техническим результатом, на достижение которого направлена группа заявленных изобретений, является создание бедренного компонента эндопротеза тазобедренного сустава, обеспечивающего возможность индивидуального подбора размеров компонента, выбора подходящей величины шеечно-диафизарного угла, офсета и антеверсии шейки, а также регулирования протяженности участков его поверхности, предназначенных для различных способов фиксации, способа его изготовления и установки. Изобретение обеспечивает возможность использования всех имеющихся преимуществ и избегания недостатков разных способов фиксации имплантата на участках костной ткани по ходу бедренной кости, подходящих для разных способов имплантации, а также возможность выбора формы и размера имплантата, что в совокупности обеспечит необходимую стабильность фиксации и замещение костных дефектов в тех участках, где это необходимо. Также возможность индивидуального подбора размеров, формы ножки эндопротеза, величины офсета позволит максимально точно восстановить биомеханику движений за счет восстановления правильного центра ротации, подбора величины плеча силы абдукторов и правильно сбалансировать нагрузку на ножку эндопротеза и бедренную кость пациента в местах контакта с компонентом эндопротеза.
Технический результат достигается за счет построения по данным лучевой диагностики 3D моделей костных дефектов костей проксимального отдела бедренной кости и создания индивидуально изготовленного бедренного компонента тазобедренного сустава с помощью технологий 3D печати из материала Rematitan СL, выполненного в виде конусовидной ножки, четырехгранного корпуса и циллиндрической шейки. Поверхность конусовидной ножки имеет полированную поверхность на протяжении, в соответствии с участком предполагаемой имплантации с цементным способом фиксации. Протяженность этого участка определяется в ходе предоперационного планирования, при котором используются технологии лучевой диагностики, в частности, компьютерная томография пораженной бедренной кости с возможностью 3D моделирования. Участок ножки с цементным способом фиксации соответствует участкам с выраженными дефектами костной ткани, а также зонам остеопороза и предполагаемого снижения остеогенного потенциала. Покрытые на протяжении остальной части ножки, а также корпуса представлены пористым материалом с возможным использованием покрытия, предназначенного для остеоинтеграции. Толщина, геометрическая форма, подходящая под индивидуальную геометрию костномозгового канала данного пациента, и длина компонента также может выбираться с учетом данных предоперационного планирования.
Таким образом предлагаемый способ изготовления бедренного компонента эндопротеза позволяет с максимальной точностью реализовать тщательно спланированную комбинацию участков цементной и бесцементной фиксации, а также персонифицировать размеры, форму имплантата, антеверсию шейки и офсет, что обеспечивает надежную гибридную фиксацию бедренного компонента эндопротеза, возможность восстановления правильной биомеханики движений и использование преимуществ обоих видов фиксации на различных участках костной ткани. Разработанная фиксация ножки комбинированным способом позволяет достичь регенерации костной ткани и остеоинтеграции на участках соприкосновения пористой части бедренного компонента по типу Press-fit с бедренной костью и на участках с остеопорозными изменениями или дефицитом костной массы заполнить зону прилегания ножки к этим участкам за счет использования костного цемента. Всех этих преимуществ невозможно добиться, используя стандартизированные бедренные компоненты.
Сущность группы изобретений пояснена примерами осуществления, которые не ограничивают объем правовой охраны.
Пример 1. Осуществление заявляемой группы изобретений, касающихся персонифицированного бедренного 3D компонента, его изготовления и установки, которые могут подвергаться различным изменениям и модификациям, понятным специалисту на основе прочтения данного описания.
Перед выполнением оперативного вмешательства проводят оценку рентгенограмм пораженного тазобедренного сустава пациента и бедренной кости (Фиг.2), проводят компьютерную томографию (КТ) таза и бедренной кости с толщиной среза не более 0,6 мм. На основании полученных данных строят 3D модель таза и бедренной кости со всеми дефектами (удаляя при этом артефакты и металлические объекты) (Фиг. 3). Для построения трехмерной модели используют, например, программное обеспечения PME Planner, позволяющее строить 3D-модели органов и костных структур различной степени сложности. На данном этапе также проводят предоперационное планирование параметров индивидуального 3D бедренного компонента эндопротеза, места его установки, его необходимых размеров и формы, протяженность участков полированного и пористого покрытия ножки и корпуса бедренного компонента (Фиг. 4-5).
После построения цифровой 3D модели таза и бедренной кости со всеми дефектами костной ткани, бедренный компонент печатают методом 3D-печати на основе металлического порошка, состоящего из титанового сплава Rematitan СL. Плавление порошка осуществляется оптоволоконным лазером мощностью от 200 Вт и происходит в герметичной камере, заполненной инертным газом. Таким образом получают модель бедренного компонента эндопротеза, размеры которого максимально точно соответствуют антропометрическим данным пациента, а его форма и протяженность участков ножки с различным покрытием максимально точно соответствует участкам утраченных костных структур в области дефекта и участкам сохранной костной ткани.
Полученный титановый компонент эндопротеза стерилизуют. После кожного разреза, осуществляют доступ к эндопротезу или спейсеру тазобедренного сустава. Хирургическая техника имплантации 3D ножки отличается от стандартной. Выполняют иссечение нежизнеспособных тканей, затем при необходимости производят расширенную остеотомию, вывих эндопротеза или спейсера и удаление компонентов. Удаленный антимикробный спейсер и изготовленный 3D бедренный компонент представлены на Фиг. 6. Далее проводится тщательная санация раны с помощью растворов антисептика. После чего согласно предоперационному планированию, происходит имплантация вертлужного компонента. Затем производят обработку костномозгового канала и его подготовку к имплантации бедренного компонента и имплантацию индивидуально изготовленного бедренного компонента эндопротеза (Фиг. 7) с фиксацией костным цементом с антибиотиком на полированных участках персонифицированного бедренного компонента эндопротеза, и фиксацией по типу Press fit на участках бедренного компонента с покрытием, предназначенным для остеоинтеграции. После полимеризации костного цемента и примерки, устанавливают выбранную из стандартного пула имплантов головку эндопротеза подходящего размера, вправляют бедренный компонент эндопротеза, повторно проверяют стабильность в суставе и амплитуду движений. Фиксация участка остеотомии (если она проводилась) тросами или пластиной. (Фиг. 8) Затем выполняют послойное ушивание раны с установкой активных дренажей.
Таким образом, в условиях, когда использование ни одного из стандартизированных бедренных компонентов не может гарантировать хороший функциональный результат, используют индивидуально созданный для каждого клинического случая бедренный компонент эндопротеза, который соответствует антропометрическим данным пациента, наличию дефектов костной ткани и участки поверхности которого соответствуют предпочтительному способу фиксации в соответствующих зонах костной ткани. Использование предлагаемого изобретения позволяет подобрать подходящие для каждого пациента индивидуальные форму, размеры и характеристики поверхности, которые обеспечивают максимальную стабильность импланта.
Пример 2. Клинический пример.
Пациентка К.С.П. 64 года, поступила в клинику с жалобами на боли в области правого тазобедренного сустава, нарушение опороспособности правой нижней конечности. Длительный анамнез болей в правом тазобедренном суставе. Диагностирован правосторонний коксартроз 3 степени. В 2010 г. выполнено тотальное эндопротезирование правого тазобедренного сустава. (Фиг.9)
Далее в 2012 г. был диагностирован перипротезный перелом, полученный вследствие травмы, был выполнен остеосинез пластиной (Фиг.10).
В 2013 г. произошла рефрактура правой бедренной кости и поломка пластины (Фиг.11).
В 2014 г. выполнено ревизионное эндопротезирование правого тазобедренного сустава: замена ножки и остеосинтез пластиной NBC (Фиг.12).
В 2016 г. развился отек правой нижней конечности, болевой синдром, повышение температуры тела до 38,5 гр. Пластина удалена, рана зажила вторичным натяжением. Болевой синдром через 3 месяца прогрессировал, больная обследована и диагностирована ППИ. В декабре 2019 г. выполнено удаление бедренного компонента и установка спейсера. На догоспитальном этапе выполнена пункция правого тазобедренного сустава: роста микрофлоры нет. На представленных рентгенограммах и данных КТ – Спейсер правого тазобедренного сустава. Вывих бедренного компонента установленного спейсера тазобедренного сустава (Фиг. 13 А) с переломом его ножки (Фиг.13 Б). Инфекционный агент не подтвержден клинически и лабораторно. Больная направлена на второй этап ревизионного эндопротезирования правого тазобедренного сустава: удаление спейсера с санацией послеоперационной раны и установкой ревизионного эндопротеза правого тазобедренного сустава с индивидуально изготовленным 3D бедренным компонентом, в связи с имеющимся дефицитом костной ткани. Кроме того, требуется фиксация перипротезного перелома.
Перед госпитализацией пациентки в стационар, на основании КТ-снимков была построена 3D модель таза и бедренной кости со всеми дефектами костной ткани, а также определены параметры и размеры бедренного компонента и протяженность участков поверхности его ножки с участками полированной и пористой поверхности (Фиг.14). По данным денситометрии у пациентки выявлен остеопороз, дефект латеральной стенки бедренной кости в нижней трети.
Пациентке было выполнена остеотомия бедренной кости, было произведено удаление компонентов спейсера правого тазобедренного сустава и костного цемента и, после тщательной санации раны, были имплантированы вертлужный компонент и индивидуально изготовленный с помощью 3D печати бедренный компонент эндопротеза (Фиг. 15), дистальная часть которого была фиксирована костным цементом, дефект латеральной стенки нижней трети бедренной кости при этом был замещен костным цементом, перипротезный перелом фиксирован пластиной (Фиг. 16). Размеры, форму, параметры и свойства поверхности бедренного компонента эндопротеза и место его имплантации прецизионно подобрали в ходе предоперационного планирования. После примерки выполняли вправление бедренного компонента эндопротеза, затем проводилась дополнительная фиксация бедренной кости пластиной и послойное ушивание раны.
В результате использования предлагаемого решения удалось добиться стабильной фиксации компонентов эндопротеза тазобедренного сустава. При этом использовано меньшее количество костного цемента. Он был использован на тех участках костной ткани, где это было необходимо, а применение бесцементного способа фиксации на тех участках костной ткани, где это было возможно. Пациентка наблюдается в динамике. Через 6 месяцев после операции пациентка ходит с дополнительной опорой на ходунки. При этом показатель по шкале Harris hip Score составлял 64 балла, по шкале WOMAC – 35 баллов, по шкале ВАШ – 0 баллов, что свидетельствовало о хороших функциональных результатах. Через 12 месяцев после операции пациентка ходит с дополнительной опорой на ходунки. При этом показатель по шкале Harris hip Score составлял 69 балла, по шкале WOMAC – 30 баллов, по шкале ВАШ – 0 баллов, что свидетельствовало о хороших функциональных результатах.
Перечень источников информации, используемых при составлении описания группы изобретений:
1. Parvizi J, Adeli B, Zmistowski B, Restrepo C, Greenwald AS. Management of Periprosthetic Joint Infection: The Current Knowledge // J Bone Joint Surg Am. - 2012 - №94 – pp. e104(1-9).
2. Волокитина Е.А., Зайцева О.П., Колотыгин Д.А., Вишняков А.А. Локальные интраоперационные и ранние послеоперационные осложнения эндопротезирования тазобедренного сустава // Гений ортопедии. – 2009. – № 3. – С. 71–77.; Волокитина Е.А., Чепелева М.В. Лазерная проточная цитометрия в лабораторном иммунологическом мониторинге эндопротезирования коленного и тазобедренного суставов // Гений ортопедии. – 2011. – № 3. – С. 131–135.; Кузьмин И.И. Методологические основы профилактики и лечения осложнений при эндопротезировании тазобедренного сустава: автореф. дис. докт. мед. наук: 14.01.17, 14.01.15. – М., 2010. – 41 с.; Прохоренко В.М., Павлов В.В. Инфекционные осложнения при эндопротезировании тазобедренного сустава. – Новосибирск: Наука, 2010. – 179 с.\; Слободской А.Б., Осинцев Е.Ю., Лежнев А.Г. Осложнения после эндопротезирования тазобедренного сустава // Вестн. травматол. и ортопед. им. Н.Н. Приорова. – 2011. – № 3. – С. 59–63.
3. ВЕСТНИК ТРАВМАТОЛОГИИ И ОРТОПЕДИИ ИМ. Н.Н. ПРИОРОВА: О возможности оптимизации стрессового ремоделирования кости при эндопротезировании коленного сустава. Резник Л.Б; Турушев М.А.
4. С.Г.Баламетов С.Г. В книге: VII Всероссийская (81-й Итоговая) студенческая научная конференция "Студенческая наука и медицина XXI века: традиции, инновации и приоритеты", посвященная 90-летию СНО СамГМУ. сборник материалов. Под редакцией Г.П. Котельникова и В.А. Куркина. 2013. С. 36b.
5. Перипротезные переломы бедра при тотальном эндопротезировании тазобедренного сустава (алгоритм профилактики): Н. А. Шестерня 1 , А. Ф. Лазарев2 , С. В. Иванников 1 , Т. А. Жарова 1 , Э. И. Солод 2 , А-М Абдул 1. 1 Первый МГМУ им. И.М.СЕЧЕНОВА МЗ Российской Федерации, Москва 2 Центральный научно-исследовательский институт травматологии и ортопедии им. Н.Н. Приорова Минздрава России, Москва
6. Lindberg-Larsen M, Jørgensen CC, Solgaard S, Kjersgaard AG, Kehlet H. Increased risk of intraoperative and early postoperative periprosthetic femoral fracture with uncemented stems. Acta orthopaedica. 2017;88(4):390–4.
7. СОВРЕМЕННЫЕ АСПЕКТЫ ПРОТЕЗИРОВАНИЯ ТАЗОБЕДРЕННОГО СУСТАВА: Белякова Юлия Дмитриевна Хорак Константин Иосифович. ФГБОУ ВО «Тверской государственный медицинский университет»
8. Опыт ревизионного эндопротезирования тазобедренных суставов с использованием модульных систем А. Г. Рыков, Б. В. Щебеньков , С. Ю. Кожевникова, В. Е. Воловик , В. Ю. Коршняк , Г. А. Пальшин
9. Sanki T, Endo H, Tetsunaga T, Furumatsu T, Yamada K, Ozaki T. Ten-year outcomes of total hip arthroplasty using fit-and-fill type cementless collared straight stem implants: relationship between the initial contact status and stress shielding. Acta medica Okayama. 2020;74(1):7–15
10. Бесцементные бедренные компоненты: история и современное состояние вопроса И.И. Шубняков, А. Риахи, М.И. Шубняков, А.О. Денисов, И.Э. Хужаназаров, Р.М. Тихилов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ индивидуального эндопротезирования тазобедренного сустава при типе костного дефекта бедренной кости Paproksy IV | 2022 |
|
RU2802391C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ПЕРИПРОТЕЗНОЙ ИНФЕКЦИЕЙ С ВОСПОЛНЕНИЕМ КАВИТАРНЫХ ДЕФЕКТОВ ВЕРТЛУЖНОЙ ВПАДИНЫ | 2023 |
|
RU2821558C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ДЕФЕКТОВ ДИСТАЛЬНОГО ОТДЕЛА БЕДРЕННОЙ КОСТИ ПРИ ВЫПОЛНЕНИИ ЭНДОПРОТЕЗИРОВАНИЯ КОЛЕННОГО СУСТАВА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2019 |
|
RU2724490C1 |
| Способ реверсивного эндопротезирования плечевого сустава у больных с посттравматическим дефицитом костной ткани проксимального отдела плечевой кости с использованием персонифицированного 3D аугмента проксимального отдела плечевой кости | 2023 |
|
RU2810943C1 |
| Способ удаления стабильных бесцементных бедренных компонентов эндопротеза тазобедренного сустава | 2021 |
|
RU2773382C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ СПЕЙСЕРА ТАЗОБЕДРЕННОГО СУСТАВА ПРИ НЕОПОРОСПОСОБНОЙ ВЕРТЛУЖНОЙ ВПАДИНЕ И ВЕРТЛУЖНЫЙ КОМПОНЕНТ СПЕЙСЕРА ТАЗОБЕДРЕННОГО СУСТАВА | 2020 |
|
RU2759655C1 |
| Способ аугментации неограниченного костного дефекта тазовой кости в области вертлужной впадины | 2019 |
|
RU2732960C1 |
| СПОСОБ РЕВИЗИОННОГО ЭНДОПРОТЕЗИРОВАНИЯ КОЛЕННОГО СУСТАВА ПРИ ДЕФЕКТЕ БЕДРЕННОЙ КОСТИ | 2017 |
|
RU2680221C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ДЕФЕКТОВ ПРОКСИМАЛЬНОГО ОТДЕЛА БОЛЬШЕБЕРЦОВОЙ КОСТИ ПРИ ВЫПОЛНЕНИИ ЭНДОПРОТЕЗИРОВАНИЯ КОЛЕННОГО СУСТАВА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2019 |
|
RU2730985C1 |
| Способ изготовления спейсера тазобедренного сустава при неопороспособной вертлужной впадине | 2017 |
|
RU2675551C1 |
Группа изобретений относится к медицине. Персонифицированный бедренный компонент эндопротеза для пациентов с выраженными костными дефектами и локальными дефектами качества костной ткани бедренной кости для выполнения одноэтапного или второго этапа двухэтапного ревизионного эндопротезирования тазобедренного сустава состоит из евроконуса, шейки, корпуса имплантата с отверстием для установки импактора и ножки. Персонифицированный бедренный компонент эндопротеза выполнен монолитным с использованием компьютерной томографии пораженной бедренной кости с возможностью 3D-моделирования и с помощью технологий 3D-печати из титанового сплава Rematitan СL. Ножка выполнена конусовидной. Корпус выполнен четырехгранным. Шейка выполнена цилиндрической. Конусовидная ножка выполнена с полированной поверхностью для цементной фиксации, расположенной на участке для зоны с выраженными дефектами костной ткани и зонами остеопороза, а остальная часть конусовидной ножки и корпус выполнены с пористой поверхностью для бесцементной фиксации. Способ изготовления персонифицированного бедренного компонента эндопротеза для пациентов с выраженными костными дефектами и локальными дефектами качества костной ткани бедренной кости для выполнения одноэтапного или второго этапа двухэтапного ревизионного эндопротезирования тазобедренного сустава состоит в следующем: оценивают рентгенограммы пораженного тазобедренного сустава пациента и бедренной кости, проводят компьютерную томографию таза и бедренной кости с толщиной среза 0,6 мм, строят 3D-модель таза и бедренной кости со всеми дефектами, удаляя при этом артефакты и металлические объекты. Проводят предоперационное планирование параметров индивидуального 3D бедренного компонента эндопротеза, места его установки, его размеров и формы, протяженности участков поверхностей полированных для цементной фиксации у конусовидной ножки и пористого покрытия для бесцементной фиксации, корпуса и остальной части ножки бедренного компонента в соответствии с участками утраченных костных структур в области дефекта и участками сохранной костной ткани. Печатают бедренный компонент методом 3D-печати на основе металлического порошка, состоящего из титанового сплава Rematitan СL. Плавление порошка осуществляют оптоволоконным лазером мощностью от 200 Вт в герметичной камере, заполненной инертным газом. Способ имплантации персонифицированного бедренного компонента эндопротеза для пациентов с выраженными костными дефектами и локальными дефектами качества костной ткани бедренной кости для выполнения одноэтапного или второго этапа двухэтапного ревизионного эндопротезирования тазобедренного сустава, изготовленного по способу п. 2, заключается в том, что после кожного разреза осуществляют доступ к эндопротезу или спейсеру тазобедренного сустава, выполняют иссечение нежизнеспособных тканей, вывих эндопротеза или спейсера, удаление эндопротеза или спейсера. Затем проводят санацию раны с помощью растворов антисептика. После чего согласно предоперационному планированию имплантируют вертлужный компонент. Затем проводят обработку костномозгового канала и его подготовку к имплантации бедренного компонента и имплантацию конусовидной ножки, выполненной с полированной поверхностью для цементной фиксации, расположенной на участке для зоны с выраженными дефектами костной ткани и зонами остеопороза, и фиксацию по типу Press fit остальной части конусовидной ножки и корпуса, выполненных с пористой поверхностью для бесцементной фиксации, предназначенных для остеоинтеграции. После полимеризации костного цемента и примерки устанавливают головку эндопротеза стандартного типа, вправляют бедренный компонент эндопротеза, проверяют стабильность в суставе и амплитуду движений. Изобретения обеспечивают создание бедренного компонента эндопротеза тазобедренного сустава, обеспечивающего возможность индивидуального подбора размеров компонента, выбора подходящей величины шеечно-диафизарного угла, офсета и антеверсии шейки, а также регулирования протяженности участков его поверхности, предназначенных для различных способов фиксации, способа его изготовления и установки. 3 н. и 2 з.п. ф-лы, 16 ил., 2 пр.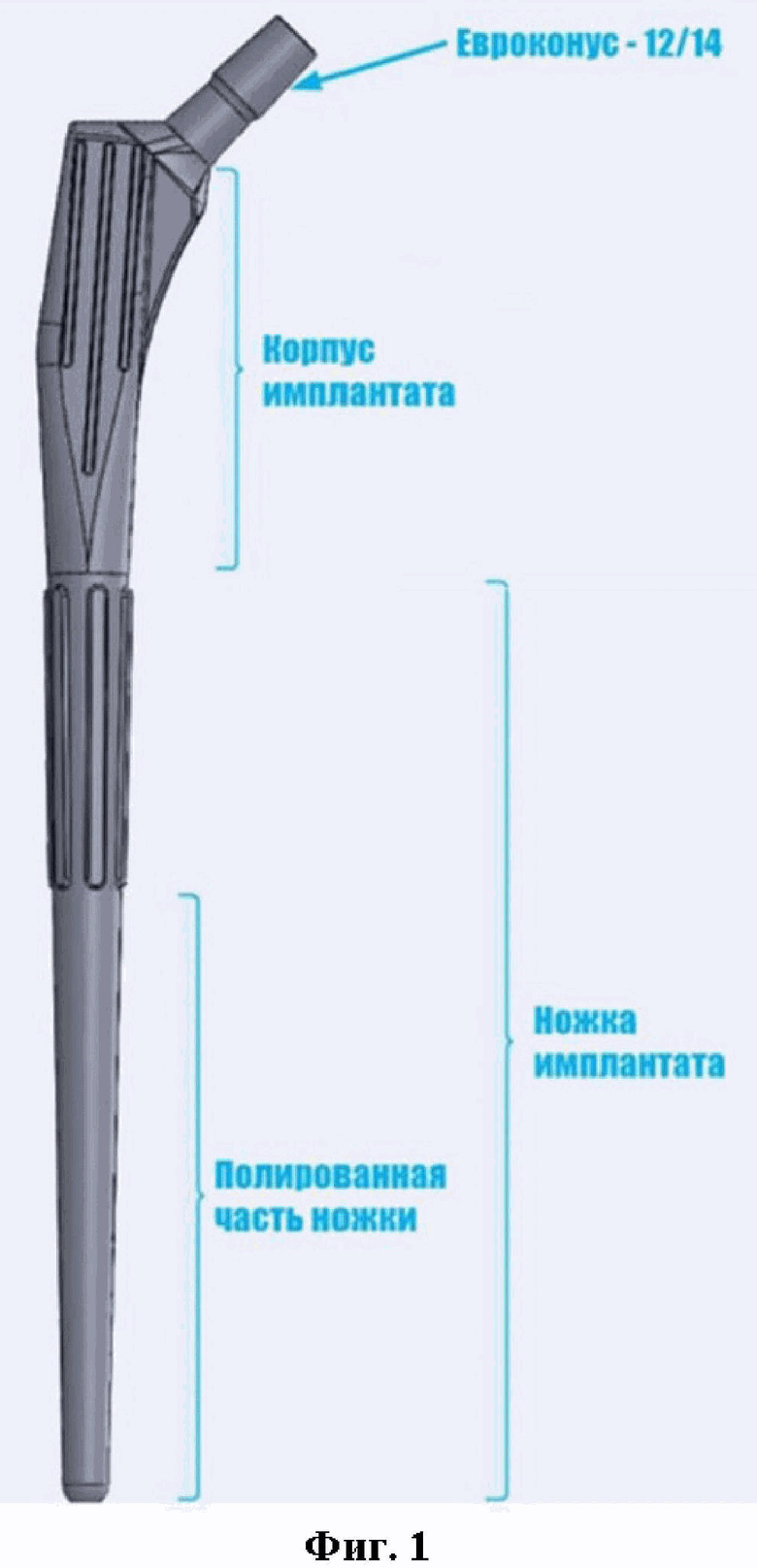
1. Персонифицированный бедренный компонент эндопротеза для пациентов с выраженными костными дефектами и локальными дефектами качества костной ткани бедренной кости для выполнения одноэтапного или второго этапа двухэтапного ревизионного эндопротезирования тазобедренного сустава, состоящий из евроконуса, шейки, корпуса имплантата с отверстием для установки импактора и ножки, отличающийся тем, что он выполнен монолитным с использованием компьютерной томографии пораженной бедренной кости с возможностью 3D-моделирования и с помощью технологий 3D-печати из титанового сплава Rematitan СL, ножка выполнена конусовидной, корпус четырехгранным, а шейка цилиндрической, конусовидная ножка выполнена с полированной поверхностью для цементной фиксации, расположенной на участке для зоны с выраженными дефектами костной ткани и зонами остеопороза, а остальная часть конусовидной ножки и корпус выполнены с пористой поверхностью для бесцементной фиксации.
2. Способ изготовления персонифицированного бедренного компонента эндопротеза для пациентов с выраженными костными дефектами и локальными дефектами качества костной ткани бедренной кости для выполнения одноэтапного или второго этапа двухэтапного ревизионного эндопротезирования тазобедренного сустава, состоящий в следующем: оценивают рентгенограммы пораженного тазобедренного сустава пациента и бедренной кости, проводят компьютерную томографию таза и бедренной кости с толщиной среза 0,6 мм, строят 3D-модель таза и бедренной кости со всеми дефектами, удаляя при этом артефакты и металлические объекты, проводят предоперационное планирование параметров индивидуального 3D бедренного компонента эндопротеза, места его установки, его размеров и формы, протяженности участков поверхностей полированных для цементной фиксации у конусовидной ножки и пористого покрытия для бесцементной фиксации, корпуса и остальной части ножки бедренного компонента в соответствии с участками утраченных костных структур в области дефекта и участками сохранной костной ткани, печатают бедренный компонент методом 3D-печати на основе металлического порошка, состоящего из титанового сплава Rematitan СL, плавление порошка осуществляют оптоволоконным лазером мощностью от 200 Вт в герметичной камере, заполненной инертным газом.
3. Способ имплантации персонифицированного бедренного компонента эндопротеза для пациентов с выраженными костными дефектами и локальными дефектами качества костной ткани бедренной кости для выполнения одноэтапного или второго этапа двухэтапного ревизионного эндопротезирования тазобедренного сустава, изготовленного по способу п. 2, заключающийся в том, что после кожного разреза осуществляют доступ к эндопротезу или спейсеру тазобедренного сустава, выполняют иссечение нежизнеспособных тканей, вывих эндопротеза или спейсера, удаление эндопротеза или спейсера, затем проводят санацию раны с помощью растворов антисептика, после чего согласно предоперационному планированию имплантируют вертлужный компонент, затем проводят обработку костномозгового канала и его подготовку к имплантации бедренного компонента и имплантацию конусовидной ножки, выполненной с полированной поверхностью для цементной фиксации, расположенной на участке для зоны с выраженными дефектами костной ткани и зонами остеопороза, и фиксацию по типу Press fit остальной части конусовидной ножки и корпуса, выполненных с пористой поверхностью для бесцементной фиксации, предназначенных для остеоинтеграции, после полимеризации костного цемента и примерки устанавливают головку эндопротеза стандартного типа, вправляют бедренный компонент эндопротеза, проверяют стабильность в суставе и амплитуду движений.
4. Способ по п. 3, отличающийся тем, что после иссечения нежизнеспособных тканей производят остеотомию бедренной кости.
5. Способ по п. 4, отличающийся тем, что после проверки стабильности в суставе и амплитуды движений фиксируют участки остеотомии тросами или пластиной.
| НОЖКА ДЛЯ РЕВИЗИОННОГО ЭНДОПРОТЕЗА СУСТАВА | 2017 |
|
RU2727582C1 |
| ЭНДОПРОТЕЗ ТАЗОБЕДРЕННОГО СУСТАВА | 2003 |
|
RU2251995C1 |
| Способ формирования индивидуального эндопротеза тазобедренного сустава | 2015 |
|
RU2621874C2 |
| RU 223920 U1, 06.03.2024 | |||
| ПРОТЕЗ ТАЗОБЕДРЕННОГО СУСТАВА СО СТЕРЖНЕМ ДЛЯ АНКЕРНОГО ЗАКРЕПЛЕНИЯ В КОСТНО-МОЗГОВОМ КАНАЛЕ БЕДРЕННОЙ КОСТИ | 2004 |
|
RU2304941C2 |
| БЕДРЕННЫЙ КОМПОНЕНТ ЭНДОПРОТЕЗА ТАЗОБЕДРЕННОГО СУСТАВА | 1999 |
|
RU2149603C1 |
| Электрический кабель | 1933 |
|
SU33593A1 |
| ВЗАИМОДЕЙСТВИЕ МЕЖДУ ТРАНСПОРТНЫМИ СРЕДСТВАМИ ДЛЯ УПОРЯДОЧИВАНИЯ ДОРОЖНОГО ДВИЖЕНИЯ | 2017 |
|
RU2674744C1 |
Авторы
Даты
2024-12-17—Публикация
2024-04-11—Подача