Область техники, к которой относится изобретение
Изобретение относится к медицине, а именно к нейрохирургии, анестезиологии и реаниматологии, и может быть использовано при интраоперационном ведении пациентов с субарахноидальным кровоизлиянием (САК) вследствие разрыва аневризмы с целью профилактики и лечения церебрального ангиоспазма, возникающего при манипуляции на церебральных артериях (арахноидальная диссекция, временное клипирование и т.п.).
Уровень техники
Интраоперационные манипуляции на церебральных артериях при операциях по поводу церебральных аневризм, наложении экстра-интра, интра-интракраниальных анастомозов могут вызывать манипуляционный спазм артерий. У ряда пациентов с уже имеющимися нарушениями церебральной перфузией (например, у больных с нетравматическим субарахноидальным кровоизлиянием, окклюзионнно-стенотическим поражением церебральных артерий) манипуляционный спазм может увеличивать частоту развития церебральной ишемии в послеоперационном периоде.
Из уровня техники известно использование различных вазодилятаторов интратекально для снижения выраженности манипуляционного спазма артерий. В частности, известен способ интраоперационного лечения и профилактики церебрального ангиоспазма, основанный на интрацистернальном введении папаверина гидрохлорида [Sabouri M. et al. The effect of irrigation of intracisternal papaverine on cerebral blood flow in subarachnoid hemorrhage //Advanced biomedical research. – 2013. – Т. 2]. Однако известный способ не позволяет избежать таких осложнений как системная гипотензия, аритмия, внутричерепные кровоизлияния, пародоксальная вазоконстрикция [Segawa H. et al. Efficacy of intracisternal papaverine on symptomatic vasospasm //No Shinkei geka. Neurological Surgery. – 1986. – Т. 14. – №. 7. – С. 847-854; Zhou X. et al. Prolonged intracisternal papaverine toxicity: index case description and proposed mechanism of action //World neurosurgery. – 2018. – Т. 109. – С. 251-257].
Из уровня техники известно использование монооксида азота для регуляции церебрального кровотока путем изменения тонуса церебральных артериол и капилляров, которые могут расширяться или сужаться в зависимости от изменений артериального давления [Fog M. The relationship between the blood pressure and the tonic regulation of the pial arteries. J Neurol Psychiatry 1: 187–197, 1938. doi:10.1136/jnnp.1.3.187. 21610927].
В частности, известен способ профилактики и лечения церебрального ангиоспазма вследствие разрыва аневризм церебральных артерий при субарахноидальном кровоизлиянии в раннем послеоперационном периоде в ОРИТ [Fung C, Z'Graggen WJ, Jakob SM, Gralla J, Haenggi M, Rothen HU, et al. Inhaled Nitric Oxide Treatment for Aneurysmal SAH Patients With Delayed Cerebral Ischemia. Front Neurol. 2022;13:817072. PMID: 35250821 https://doi.org/10.3389/fneur.2022.817072], основанный на использовании газообразной формы монооксида азота (NO), который вводят в воздушную смесь, подаваемую пациенту через дыхательный контур, в концентрации от 1 ppm до 40 ppm в течение 24 часов длительностью 5 дней. По завершении лечения подачу NO в дыхательный контур прекращают постепенно посредством снижения концентрации с 40 ppm до 1 ppm в течение 30 минут. Однако данный способ предназначен для использования в раннем послеоперационном периоде. Из уровня техники не известно использование монооксида азота при интраопреационном ведении пациентов с САК вследствие разрыва аневризмы. При интраоперационном применении монооксида азота необходимо учитывать множество факторов, от которых зависит результат профилактики и лечения церебрального ангиоспазма. Кроме того, ключевое значение для профилактики и лечения церебрального ангиоспазма в процессе проведения операций на церебральных артериях имеет и схема подачи монооксида азота.
Технической проблемой, решаемой заявленным изобретением, является разработка способа профилактики и лечения интраоперационного манипуляционного церебрального ангиоспазма в интраоперационном периоде.
Раскрытие сущности изобретения
Достигаемым техническим результатом является снижение интраоперационного риска возникновения манипуляционного спазма после клипирования артерии головного мозга, снижение частоты церебральной ишемии и инфарктов головного мозга у пациентов после операций на церебральных артериях в раннем послеоперационном периоде.
Технический результат достигается совокупностью последовательно выполняемых приемов:
- в течение интраоперационного периода подают в контур ИВЛ газо-воздушную смесь с контролем давления (концентрации) СО2 на выдохе, которое должно находиться в интервале от 30 до 35 мм рт. ст., сатурации – в интервале от 97 до 100%, соотношения объема газовоздушной смеси вдох/выдох в минуту - от 1/1,5 до 1/2,
- после наложения постоянной клипсы через дыхательный контур ИВЛ пациенту, в газо-воздушную смесь подают газообразную форму монооксида азота (NO), при этом концентрацию NO увеличивают ступенчато – сначала каждые 5 минут концентрацию увеличивают в 2 раза, начиная с 1 ppm до 64 ppm (1 ppm, 2 ppm, 4 ppm, 8 ppm, 16 ppm, 32 ppm, 64 ppm), затем каждую минуту концентрацию увеличивают на 5 ppm до достижения целевого значения;
- в процессе ступенчатого увеличения концентрации NO контролируют следующие параметры:
• дыхательный объем (ДО), который должен находиться в интервале «от 6 до 10 мл/кг», и соотношение объема газовоздушной смеси вдох/выдох в минуту – «от 1/1,5 до 1/2», измерение данных параметров производят с целью поддержания адекватного газообмена,
• концентрацию (давление) углекислого газа в выдыхаемой смеси, которая должна находиться в интервале «не более 35 мм рт.ст.», измерение данного параметра производят с целью предотвращения повышения внутричерепного давления (ВЧД) и падения церебрального перфузионного давления (ЦПД),
• концентрацию тромбоцитов в крови, которая должна находиться в интервале «не менее 50 тыс. в мкл»; концентрацию тромбоцитов в крови измеряют перед оперативным вмешательством,
• концентрацию метгемоглобина в яремной вене, которая должна находиться в интервале «не более 3%»; метгемоглобин в яремной вене измеряют путем взятия венозной крови из центрального венозного катетера (ЦВК), с целью недопущения снижения кислородной ёмкости крови,
• давление систолическое, которое должно находиться в интервале «от 100 до 150 мм.рт.ст.», диастолическое – «от 60 до 90 мм.рт.ст.», при этом допустимым является изменение давления не более чем на 15 % от исходного нормального давления пациента, измеренного до начала операции,
• сатурацию кислорода в луковице яремной вене, которая должна находиться в интервале «от 50 до 75%»,
• сердечный индекс, который должен находиться в интервале «более 2,5 л/мин/м2»,
• количество внесосудистой воды легких, при этом предельно допустимым значением является «менее 15 мл/кг»;
увеличение концентрации NO прекращают при получении по меньшей мере у одного из контролируемых параметров значения за пределами указанных интервалов допустимых значений, эту концентрацию NO считают целевой;
далее подачу NO осуществляют на достигнутом (целевом) значении концентрации до окончания операции (наложения швов) при контроле указанных параметров;
по окончании операции концентрацию NO уменьшают с целевого значения до 0 ppm в течение 30 минут.
В процессе подачи NO необходимо контролировать указанный выше комплекс параметров и уменьшать концентрацию NO в случае получения значений данных параметров, выходящих за границы указанных диапазонов.
В случае выхода за границы вышеуказанного комплекса параметров, следует уменьшать концентрацию монооксида азота по ступенчатой схеме, с целью снижения влияния на центральную гемодинамику, ВЧД, ЦПД, тромбоцитарное звено гемостаза.
Подачу в контур ИВЛ в течение интраоперационного периода газо-воздушной смеси осуществляют в объеме, обеспечивающем ДО от 6 до 10 мл газовоздушной смеси на 1 кг веса пациента из расчета идеальной массы тела.
В случае превышения давления (концентрации) СО2 более 35 мм рт. ст. увеличивают минутный объем дыхания (МОД) путем увеличения ЧДД до 20 вдохов в минуту; если при данных значениях ЧДД значение давления СО2 находится на уровне, превышающем 30 мм рт. ст., изменяют объем подаваемой в контур ИВЛ газо-воздушной смеси до значения соотношения вдох/выдох 1/4.
Контроль параметров ДО, соотношение объема газовоздушной смеси вдох/выдох в минуту, давление (концентрацию) углекислого газа в выдыхаемой смеси на выдохе осуществляют в непрерывном режиме.
Управляемое изменение концентрации монооксида азота, подаваемого в дыхательный контур пациента, подключенного к наркозно-дыхательному аппарату, осуществляется посредством интеграции в данный контур аппарата «Тианокс».
Схема подачи монооксида азота в дыхательный контур пациента, комплекс контролируемых параметров пациента, условия для начала ингаляционной терапии NO, были разработаны в результате обследования, интра- и послеоперационного ведения более 50 пациентов, поступивших в ОРИТ с САК вследствие разрыва аневризмы. При этом исследовались случаи возникновения манипуляционного спазма, частота церебральной ишемии и инфарктов головного мозга в раннем послеоперационном периоде. Всем пациентам в предоперационном периоде проводилась диагностика с использованием инструментальных и лабораторных методов, включая физикальный осмотр, КТ головного мозга (для оценки выраженности внутричерепного кровоизлияния с применением шкал Hijdra, Graeb, Fisher, исключения наличия зон ишемии головного мозга) КТ ангиографию церебральных артерий (для оценки анатомических особенностей патологии церебральных артерий, исключения наличия церебрального спазма до операции), выявление нарушения церебральной перфузии по данным КТ-перфузии головного мозга, оценку линейных скоростей кровотока по данным транскраниальной доплерографии (ТКДГ). В интраоперационном периоде проводились: контроль и анализ данных кислотно-щелочного состояния (КЩС) венозной и артериальной крови для оценки продолжительности и тяжести степени гипоксемии/гиперкапнии (кислородного статуса пациента), оценка показателей парциального давления кислорода и углекислого газа в артериальной крови (PaO2 и PaCO2), и в венозной крови (PvO2 и PvCO2); контактная допплерография артерий до и после манипуляций на церебральных артериях с измерением линейных скоростей кровотока, оценки допплерографического спектра церебрального кровотока.
На основании полученных данных был определен диагностически значимый комплекс параметров, необходимый и достаточный для контроля состояния пациента в процессе подачи в его дыхательный контур монооксида азота с целью предупреждения ангиоспазма. При этом было выявлено, что существенным в заявленном изобретении является начало подачи монооксида азота - сразу по завершении основного этапа манипуляций на церебральных артериях, а также предложенная схема подачи монооксида азота, а именно: использование целевого значения концентрации предпочтительно из интервала значений от 64 до 80 ppm, ступенчатое увеличение концентрации в 2 раза каждые 5 минут с момента подключения аппарата «Тианокс» - начиная с 1 ppm до достижения значения 64 ppm (1 ppm, 2 ppm, 4 ppm, 8 ppm, 16 ppm, 32 ppm, 64 ppm), затем увеличения концентрации на 5 ppm каждую минуту до достижения целевого значения из указанного интервала. При проведении исследований именно применение данной схемы продемонстрировало наилучшие результаты профилактики возникновения манипуляционного спазма после операции на церебральных артериях головного мозга, которые характеризовались также снижением частоты церебральной ишемии и инфарктов головного мозга у пациентов после операций на церебральных артериях.
Краткое описание чертежей
Изобретение поясняется иллюстративными материалами.
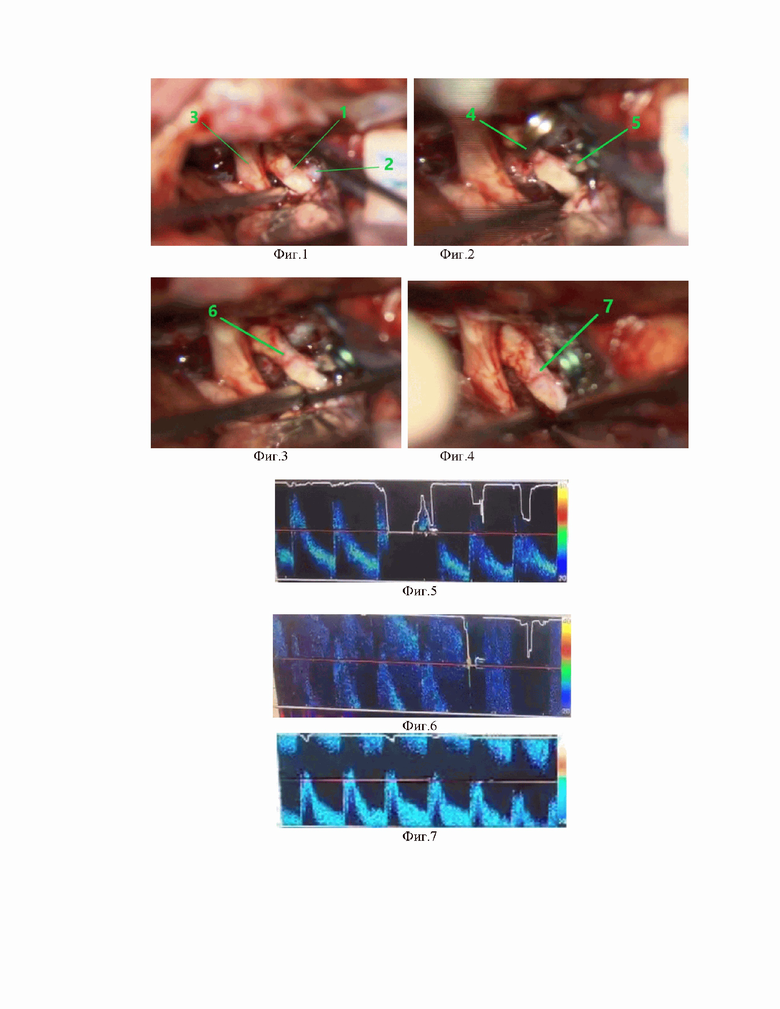
На фиг.1 – 4 представлены интраоперационные фотографии, а именно: на фиг.1 представлен этап выделения аневризмы; на фиг.2 - этап клипирования аневризмы на фоне временного клипирования правой внутренней сонной артерии (ВСА); на фиг.3 - этап после снятия временного клипса; на фиг.4 - через 15 мин после ингаляции NO. Позициями на фигурах обозначены: 1 – супраклиноидный сегмент правой ВСА, 2 – шейка аневризмы, 3 – правый зрительный нерв, 4 – временный клипс на ВСА, 5 – клипс на шейке аневризмы, 6 – сегментарный спазм в области наложения временного клипса, 7 – сегментарный спазм регрессировал.
На фиг.5 – 7 представлен спектр кровотока по правой ВСА, полученный при контактной допплерографии, а именно: на фиг. 5 – спектр кровотока до наложения временного клипса, на фиг.6 - непосредственно после снятия временного клипса, на фиг.7 - через 20 мин после ингаляции NO.
Осуществление изобретения
С целью профилактики интраоперационного манипуляционного спазма церебральных артерий при микрохирургическом клипировании артерии головного мозга осуществляют ингаляцию монооксидом азота NO с применением ИВЛ. Генерация оксида азота (NO) осуществляется путем импульсно-периодического разряда в разрядной камере из окружающего воздуха с помощью аппарата «Тианокс». Синтезируемая газовая смесь, содержащая NO, с объемной скоростью 0,45±0,2 л/мин подвергается процедуре очистки, после чего поступает в терапевтический контур пациента, где происходит его смешивание с основным дыхательным потоком, поступающим из внешнего источника (например, аппарата искусственной вентиляции легких, компрессора, концентратора кислорода) или встроенного блока подачи воздуха аппарата.
Перед подачей газа пациенту из дыхательного контура отбирают пробу газа для последующего анализа в блоке мониторинга. Для анализа состава поступающего газа в блоке мониторинга использованы электрохимические измерительные датчики NO и NO2.
Все данные о концентрации NO в дыхательной смеси, параметрах дыхательного потока и эффективности терапии фиксируются и документируются для последующего анализа и оценки. Подачу NO в дыхательный контур пациента начинают сразу после клипирования разорвавшейся аневризмы. Начальная концентрация NO, которая подаётся в контур с воздушной смесью, составляет 1 ppm. Далее концентрацию увеличивают ступенчато – каждые 5 минут в 2 раза до достижения целевого значения. Таким образом, концентрацию каждые 5 минут изменяют по следующей схеме: 1, 2, 4, 8, 16, 32, 64, далее каждую минуту на 5 ppm и т.д. Таким образом, в течение 35 минут, целевая концентрация NO в воздушной смеси достигает значения из интервала 64-80 ppm. Данную концентрацию поддерживают на протяжении всей операции. В течение первых 10 минут после наложения постоянной клипсы оценивают состоятельность интраоперационного гемостаза посредством визуального осмотра раны на наличие кровотечения из оперируемого сосуда на фоне вазорелаксации, и в случае выраженных нарушений гемостаза концентрацию NO уменьшают в аналогичной последовательности до достижения 0 -го значения. По окончании терапии подачу NO из аппарата Тианокс в дыхательный контур пациента останавливают по схеме постепенного снижения концентрации в течение 30 мин до 0 ppm.
В процессе интраоперационного применения оксида азота (NO) проводят:
А) Мониторинг концентрации NO: используется газоанализатор для непрерывного контроля концентрации оксида азота в выдыхаемом воздухе пациента.
Б) Регулирование концентрации NO: система автоматически регулирует подачу NO в дыхательный контур, чтобы поддерживать заданную концентрацию в определенном диапазоне.
В) Контроль дыхательного потока: операционный персонал контролирует дыхательный поток, чтобы обеспечить соответствие между подаваемым и забираемым объемом газа, с регулируемыми параметрами режима ИВЛ, МОД, ДО, PEEP, EtCO2, I:E в определенных диапазонах.
Г) Контроль гемодинамики, в том числе PiCCO, в определенных границах с целью поддержания адекватного ЦПД, СИ и показателя внесосудистой воды в легких.
Д) Контроль лабораторных показателей сатурации кислорода в луковице яремной вены, концентрацию метгемоглобина в крови, концентрацию тромбоцитов клиническом анализе крови.
Е) Оценку эффективности терапии: изменения концентрации NO в выдыхаемом воздухе используются для оценки эффективности терапии в реальном времени.
Ж) Документирование данных: все данные о концентрации NO, дыхательном потоке и эффективности терапии регистрируются для последующего анализа и документации.
После операции в ОРИТ пациенту осуществляют следующие манипуляции:
А) ТКДГ в течение 24 часов для оценки линейной скорости по магистральным церебральным артериям, исключения нарастания церебрального сосудистого спазма;
Б) КТ головного мозга и КТ-перфузию головного мозга/ в течение 24 после операции для оценки состояния вещества головного мозга, оценки церебральной перфузии и выявления новых зон ишемии.
Примеры реализации изобретения
Интраоперационную ингаляцию NO осуществляли у 18 пациентов с манипуляционным спазмом на церебральных артериях после операций по поводу клипирования церебральных аневризм. Манипуляционный спазм регистрировали визуально при сравнении с диаметром приводящей артерии до и после временного клипирования артерии, по данным контактной допплерографии (наблюдали увеличение линейной скорости кровотока (ЛСК) на 15-35% от исходных значений, появление признаков турбулентного спектра кровотока). После начала ингаляционной терапии NO наблюдали визуальное расширение церебральных артерий и нормализацию показателей контактной допплерографии у всех пациентов в течение 5-15 мин после начала терапии.
В послеоперационном периоде в течение первых 24 часов выполняли контрольную КТ головного мозга и церебральную КТ-перфузию. По данным исследований отсутствовали признаки инфаркта мозга или нарушения церебральной перфузии в бассейне кровоснабжения оперированных артерий у всех пациентов.
Клинический пример.
Пациентка Ю. с нетравматическим субарахноидально-вентрикулярным кровоизлиянием из аневризмы коммуникатного сегмента правой ВСА.
Диагноз: нетравматическое субарахноидально-вентрикулярное кровоизлияние. Разрыв аневризмы коммуникатного сегмента правой внутренней сонной артерии. Hunt-Hess 3+1. Fisher III+IV. Hijdra 26 б. Graeb 5 б. ШКГ 12 баллов (при поступлении). Гипертоническая болезнь 3 стадии, 3 степени, риск ССО 4.
По данным ТКДГ, КТ-ангиографии, КТ перфузии головного мозга признаков ангиоспазма и нарушения церебральной перфузии до операции не выявлено. Линейная скорость по средним мозговым артериям составляла 60 см/с слева, 70 см/с справа.
В первые 24 часа с момента кровоизлияния проведена нейрохирургическая операция: декомпресссивная трепанация черепа, клипирование аневризмы коммуникантного сегмента внутренней сонной артерии.
Интраоперационно возникла необходимость выполнения временного клипирования для выделения шейки аневризмы и предупреждения интраоперационного неуправляемого кровотечения. Ниже представлены этапы операции (см. фигуры), демонстрирующие сегментарный манипуляционный спазм после в области временного клипирования.
Терапию оксидом азота (NO) осуществляли через контур аппарата ИВЛ после клипирование аневризмы.
Ниже приведены этапы проведения терапии ингаляционным NO через контур аппарата ИВЛ, их можно использовать как руководство для данного пациента:
Подготовление аппарата ИВЛ и установка режима, в данном случае это был режим PC-SIMV с параметрами МОД – от 8,3 до 9,2, ДО - 500 мл, ЧДД – 17-18, PEEP – 6, FiO2 – 45, ASB – 16-19, I:E – ½, EtCO2 – 31 мм.рт.ст.
Аппарат для терапии ингаляционным оксидом азота (NO) был подготовлен. Сразу по окончании этапа клипирования аневризмы, начинали ингаляцию NO с низкой концентрации (1 ppm) и постепенно увеличивали каждые 5 минут, согласно установленным этапам начала процедуры. Когда достигнута целевая концентрация NO 80 ppm, она поддерживалась на протяжении оставшегося интраоперационного периода. Параметры ИВЛ на период подачи ингаляций: МОД – от 9,1 до 9,2, ДО – 500 мл, ЧДД - 18 PEEP – 6, FiO2 – 45, ASB – 18, I:E – ½, EtCO2 на выдохе составлял 30 мм.рт.ст. АД в течении основного этапа операции варьировалось не более чем на 10% от значений 140/90 мм.рт.ст., в то время как исходное значение составляло 146/85 мм.рт.ст.
По окончании операции, началось постепенное снижение концентрации NO каждые 5 минут, в соответствии с заданными этапами окончания процедуры. По окончании ингаляции аппарат Тианокс отсоединялся от аппарата искусственной вентиляции легких. Ингаляции NO проходили под строгим контролем уровня метгемоглобина в крови, не превышая 2% в течение всего периода терапии. Тромбоциты пациента 164 тыс. в мкл.
Интраоперационно кровоток по церебральным артериям оценивали при помощи контактной допплерографии. После временного клипирования наблюдали нарушение нормального спектра кровотока, с последующим восстановлением спектра после ингаляции NO. (см. фиг 5, фиг 6, фиг 7).
В послеоперационном периоде пациентка была переведена в отделение реанимации, где проводилась интенсивная терапия. В течение 6 часов больная была переведена на самостоятельное дыхание, восстановила уровень бодрствования до умеренного оглушения. По данным КТ перфузии через сутки после операции признаков нарушения церебральной перфузии не отмечали. По данным ТКДГ линейная скорость по средним мозговым артериям составила 85 см/с слева и 70 см/с справа
Таким образом, при использовании заявленного изобретения был отмечен регресс церебрального манипуляционного ангиоспазма в интраоперационном периоде, который является следствием применения технологии ингаляций NO через контур наркозно-дыхательного аппарата, который достигается путем реализации следующих эффектов: расслабление мышечной стенки артерии, снижение скорости притока крови по артерии. Данные эффекты обеспечивают снижение частоты развития инфаркта и уменьшение зоны ишемии головного мозга по данным КТ, улучшение перфузии по данным КТ-перфузии головного мозга.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ ЦЕРЕБРАЛЬНОГО СОСУДИСТОГО СПАЗМА ПРИ НЕТРАВМАТИЧЕСКИХ СУБАРАХНОИДАЛЬНЫХ КРОВОИЗЛИЯНИЯХ ВСЛЕДСТВИЕ РАЗРЫВА АНЕВРИЗМ СОСУДОВ ГОЛОВНОГО МОЗГА | 2016 |
|
RU2632622C1 |
| СПОСОБ ВЫПОЛНЕНИЯ ОБХОДНОГО ШУНТИРОВАНИЯ ГОЛОВНОГО МОЗГА С ИСПОЛЬЗОВАНИЕМ УСТЬЯ ВЕРХНЕЧЕЛЮСТНОЙ АРТЕРИИ (анастомоз по типу конец-в-конец) | 2021 |
|
RU2781443C1 |
| СПОСОБ ОЦЕНКИ РИСКА НЕБЛАГОПРИЯТНОГО ИСХОДА ЗАБОЛЕВАНИЯ У БОЛЬНЫХ С НЕТРАВМАТИЧЕСКИМ СУБАРАХНОИДАЛЬНЫМ КРОВОИЗЛИЯНИЕМ (НСАК) ВСЛЕДСТВИЕ РАЗРЫВА АРТЕРИАЛЬНЫХ АНЕВРИЗМ ГОЛОВНОГО МОЗГА | 2019 |
|
RU2723754C1 |
| СПОСОБ ВЫБОРА ТИПА ЭКСТРА-ИНТРАКРАНИАЛЬНОГО ШУНТА ПО ПРОПУСКНОЙ СПОСОБНОСТИ ПРИ ОСТРЫХ И ХРОНИЧЕСКИХ ЦЕРЕБРОВАСКУЛЯРНЫХ ПАТОЛОГИЯХ, ТРЕБУЮЩИХ РЕВАСКУЛЯРИЗИРУЮЩЕГО ВМЕШАТЕЛЬСТВА | 2021 |
|
RU2784442C1 |
| СПОСОБ ВЫПОЛНЕНИЯ СЕЛЕКТИВНОГО ЭИКМА В РЕГИОНЕ ГИПОПЕРФУЗИИ С ИСПОЛЬЗОВАНИЕМ НЕЙРОНАВИГАЦИИ | 2017 |
|
RU2648001C1 |
| СПОСОБ КОНТРОЛЯ ВНУТРИЧЕРЕПНОГО ДАВЛЕНИЯ ПРИ ПРОВЕДЕНИИ ГИПЕРБАРИЧЕСКОЙ ОКСИГЕНАЦИИ В УСЛОВИЯХ ИСКУССТВЕННОЙ ВЕНТИЛЯЦИИ ЛЕГКИХ У БОЛЬНЫХ С ВНУТРИЧЕРЕПНЫМИ КРОВОИЗЛИЯНИЯМИ, НАХОДЯЩИХСЯ В КРИТИЧЕСКОМ СОСТОЯНИИ | 2010 |
|
RU2447833C1 |
| Способ интраоперационного предупреждения локального ишемического повреждения головного мозга при микрохирургической операции по поводу церебральной артериальной аневризмы | 2016 |
|
RU2629019C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ АНЕВРИЗМЫ БРЮШНОЙ АОРТЫ | 2024 |
|
RU2834529C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ПОВТОРНОГО ЛУЧЕВОГО ЛЕЧЕНИЯ РЕЦИДИВИРУЮЩИХ ГЛИОМ ГОЛОВНОГО МОЗГА (варианты) | 2024 |
|
RU2830798C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ИНТРАОПЕРАЦИОННЫХ ИШЕМИЧЕСКИХ СОСУДИСТЫХ ОСЛОЖНЕНИЙ ПРИ ПРОВЕДЕНИИ КАРОТИДНОЙ ЭНДАРТЕРЭКТОМИИ | 2020 |
|
RU2723757C1 |
Изобретение относится к медицине, а именно к нейрохирургии, анестезиологии и реаниматологии, и может быть использовано для профилактики интраоперационного манипуляционного спазма церебральных артерий при микрохирургическом клипировании артерии головного мозга. По завершении наложения клипсы через дыхательный контур ИВЛ начинают подачу в газовоздушную смесь газообразной формы монооксида азота (NO), при этом концентрацию NO увеличивают ступенчато – каждые 5 мин в 2 раза, начиная с 1 до 64 ppm, затем каждую минуту концентрацию увеличивают на 5 ppm до достижения целевого значения в пределах 64-80 ppm. В процессе ступенчатого увеличения концентрации NO контролируют следующие параметры: дыхательный объем, соотношение объема газовоздушной смеси вдох/выдох в минуту, концентрацию углекислого газа в выдыхаемой смеси, концентрацию тромбоцитов в крови, концентрацию метгемоглобина в яремной вене, давление систолическое и диастолическое, сатурацию кислорода в луковице яремной вены, сердечный индекс, количество внесосудистой воды легких, при этом увеличение концентрации NO прекращают при получении значения по меньшей мере одного из контролируемых, а достигнутое значение концентрации NO принимают за целевое. Далее подачу NO осуществляют при целевом значении концентрации до окончания операции при контроле указанных параметров, по окончании операции концентрацию NO уменьшают с целевого значения до 0 ppm в течение 30 мин. Способ обеспечивает регресс церебрального манипуляционного ангиоспазма в интраоперационном периоде, снижение частоты развития инфаркта, уменьшение зоны ишемии головного мозга по данным КТ, улучшение перфузии по данным КТ-перфузии головного мозга за счет расслабления мышечной стенки артерии и снижения скорости притока крови по артерии. 2 з.п. ф-лы, 7 ил., 1 пр.
1. Способ профилактики интраоперационного манипуляционного спазма церебральных артерий при микрохирургическом клипировании артерии головного мозга, включающий подачу в контур ИВЛ пациента в течение интраоперационного периода газовоздушной смеси с контролем давления СО2 на выдохе, сатурации и соотношения объема газовоздушной смеси вдох/выдох; по завершении наложения клипсы через дыхательный контур ИВЛ начинают подачу в газовоздушную смесь газообразной формы монооксида азота (NO), при этом концентрацию NO увеличивают ступенчато – каждые 5 мин в 2 раза, начиная с 1 до 64 ppm, затем каждую минуту концентрацию увеличивают на 5 ppm до достижения целевого значения в пределах 64-80 ppm; в процессе ступенчатого увеличения концентрации NO контролируют следующие параметры: дыхательный объем (ДО), соотношение объема газовоздушной смеси вдох/выдох в минуту, концентрацию углекислого газа в выдыхаемой смеси, концентрацию тромбоцитов в крови, концентрацию метгемоглобина в яремной вене, давление систолическое и диастолическое, сатурацию кислорода в луковице яремной вены, сердечный индекс, количество внесосудистой воды легких, при этом увеличение концентрации NO прекращают при получении значения по меньшей мере одного из контролируемых параметров за пределами указанных интервалов:
дыхательный объем (ДО) от 6 до 10 мл/кг,
соотношение объема газовоздушной смеси вдох/выдох в минуту от 1/1,5 до 1/2,
концентрация углекислого газа в выдыхаемой смеси не более 35 мм рт. ст.,
концентрация тромбоцитов в крови не менее 50 тыс. в мкл,
концентрация метгемоглобина в яремной вене не более 3%,
давление систолическое от 100 до 150 мм рт. ст., диастолическое от 60 до 90 мм рт. ст., при этом не более 15 % от исходного давления пациента, измеренного до начала операции,
сатурация кислорода в луковице яремной вены от 50 до 75%,
сердечный индекс более 2,5 л/мин/м2,
количество внесосудистой воды легких менее 15 мл/кг;
достигнутое значение концентрации NO принимают за целевое, далее подачу NO осуществляют при целевом значении концентрации до окончания операции при контроле указанных параметров, по окончании операции концентрацию NO уменьшают с целевого значения до 0 ppm в течение 30 мин.
2. Способ по п.1, характеризующийся тем, что контроль параметров ДО, соотношение объема газовоздушной смеси вдох/выдох в минуту, концентрацию углекислого газа в выдыхаемой смеси на выдохе осуществляют в непрерывном режиме.
3. Способ по п.1, характеризующийся тем, что ступенчатое уменьшение концентрации NO осуществляют в последовательности, аналогичной при ее увеличении.
| СПОСОБ ПРОФИЛАКТИКИ ЦЕРЕБРАЛЬНОГО СОСУДИСТОГО СПАЗМА ПРИ НЕТРАВМАТИЧЕСКИХ СУБАРАХНОИДАЛЬНЫХ КРОВОИЗЛИЯНИЯХ ВСЛЕДСТВИЕ РАЗРЫВА АНЕВРИЗМ СОСУДОВ ГОЛОВНОГО МОЗГА | 2016 |
|
RU2632622C1 |
| Способ изготовления угольных электродов | 1929 |
|
SU17207A1 |
| КРЫЛОВ В.В | |||
| и др | |||
| Методы профилактики сосудистого спазма и отсроченной ишемии головного мозга у пациентов с массивным субарахноидальным кровоизлиянием вследствие разрыва аневризм сосудов головного мозга | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| МИРОНОВ А.В | |||
| и др | |||
| Селективная химическая ангиопластика в | |||
Авторы
Даты
2025-02-11—Публикация
2024-06-10—Подача