Область техники, к которой относится изобретение
Изобретение относится к области медицины, а именно нейрохирургии, и может быть использовано при проведении хирургического лечения пациентов с острым ишемическим инсультом и хронической церебральной недостаточностью.
Уровень техники
Известен способ хирургического лечения пациентов с окклюзией внутренней сонной артерии и хронической церебральной недостаточностью с использованием нейронавигации - способ наложения экстра-интракраниального микроанастомоза (ЭИКМА) из минидоступа с использованием 3D КТ планирования и нейронавигации (Coppens J.R., Cantando J.D., Abdulrauf S.I. // Minimally invasive superficial temporal artery to middle cerebral artery bypass through an enlarged bur hole: the use of computed tomography angiography neuronavigation in surgical planning. // J Neurosurg. - 2008. - Vol. Sep; 109 (3) - P. 553-558; Лукьянчиков B.A., Каландари A.A., Далибалдян B.A., Шестов Е.В., Нахабин О.Ю., Полунина Н.А., Токарев А.С., Сенько И.В., Григорьева Е.В., Хамидова Л.Т., Порошина И.В. Возможность выполнения экстра-интракраниального микроанастомоза с использованием системы безрамной нейронавигации. // Нейрохирургия. - 2014. - №2. - С.66-72). Согласно этому методу проводят предоперационное планирование с использованием данных КТ-ангиографии сосудов головного мозга, выполняют разметку артерии-реципиента, артерии-донора, с последующим сопоставлением результатов планирования с интраоперационными данными и созданием экстра-интракраниального микроанастомоза между теменной ветвью поверхностной височной артерии и М4 сегментом средней мозговой артерии (СМА) по типу конец-в-бок. Указанный способ позволяет с высокой точностью находить во время операции артерию-донор и артерию-реципиент, снижает риск периоперационных осложнений, уменьшает хирургическую травму, создает возможность выполнения мини-инвазивного вмешательства, позволяет выполнять операцию под местной анестезией.
Известны также способы выполнения ЭИКМА с использованием данных МР-ангиографии (Fischer G, Stadie A, Schwandt Е, et al // Minimally invasive superficial temporal artery to middle cerebral artery bypass through a minicranitomy: benefit of three-dimensional virtual reality planning using magnetic resonance angiography // Neurosurg Focus. - 2009. - Vol. 26 (5). - P. E20.), дигитальной церебральной ангиографии (Nakagawa I, Kurokawa S, Tanisaka M, Kimura R, Nakase H. // Virtual surgical planning for superficial temporal artery to middle cerebral artery bypass using three-dimensional digital subtraction angiography. // Acta Neurochir (Wien). - 2010. - Vol. Sep; 152 (9). - P. 1535-40) в качестве исходных данных для нейронавигационного планирования.
Основным недостатком этих методик является возможность навигации и разметки только ветвей поверхностной височной артерии и корковых ветвей средней мозговой артерии для выполнения классической операции ЭИКМА в проекции правой или левой латеральной щели. Методики не позволяют определить регион гипоперфузии головного мозга, артерию-донор и артерию-реципиент в проекции нарушенной перфузии и выполнить реваскуляризацию именно этого региона, что может уменьшить эффективность операции у определенной группы пациентов. Методики не предполагают использование отличных от ветвей поверхностной височной артерии артерий-доноров.
Раскрытие изобретения
Задачей изобретения является создание способа выполнения операции селективного ЭИКМА в проекции региона гипоперфузии головного мозга с использованием предоперационного планирования и навигации.
Техническим результатом, на достижение которого направлено заявленное изобретение, является возможность селективной (избирательной) реваскуляризации необходимого региона головного мозга с высокой точностью, с целью улучшения перфузии и функциональных исходов после перенесенного острого нарушения мозгового кровообращения у пациентов с окклюзией внутренней сонной артерии.
Поставленная задача решается тем, что способ хирургического лечения пациентов с окклюзией внутренней сонной артерии в остром периоде острого нарушения мозгового кровообращения (ОНМК) или после перенесенных нарушений мозгового кровообращения, включает выполнение операции ЭИКМА, при этом на дооперационном этапе выполняют КТ-ангиографию экстра-интракраниальных артерий и ОФЭКТ головного мозга (нативное исследование), на ОФЭКТ выявляют зону (или очага) гипоперфузии (соответствующую зоне ишемической пенумбры) с показателями кровотока на уровне менее 38 мл/мин/100 г, путем последовательного оконтуривания вышеописанной зоны на всех аксиальных срезах создают 3D-модель зоны гипоперфузии, после выявления очага пониженного кровоснабжения производят предоперационное планирование на навигационной станции, где совмещают в одном диалоговом окне (fusion) данные ОФЭКТ и КТ-ангиографии с построением 3D-модели, при этом на каждом срезе оконтуривают изображение интракраниальной артерии реципиента, находящейся в очаге пониженного кровоснабжения, имеющей диаметр 0,8-1,0 мм, и изображение до трех потенциальных артерий-доноров из бассейна наружной сонной артерии (толщиной до 1,0-1,5 мм и длиной не менее 6 см), находящихся в проекции артерии реципиента, далее на 3D модели из отмеченных артерий - доноров выбирают артерию, расположенную как можно ближе к очагу пониженного кровоснабжения и имеющую диаметр, равный или больше диаметра артерии реципиента, снабжающей очаг, и находящуюся на расстоянии от артерии-реципиента на расстоянии не более чем 1-3 см (т.е. имеющий дефицит длины не менее 1-3 см), затем (с целью уменьшения хирургической травмы) производят моделирование минимально достаточной краниотомии, для чего на 3D-модели выделяют область диаметром 2-4 см, центром которой является точка пересечения проекции артерии реципиента на выбранную артерию донора, после чего в условиях операционной с использованием безрамной нейронавигации проводят сопоставление кожных ориентиров с полученными на 3D-модели, выполняют разметку артерий и операционного доступа, выполняют трепанацию в проекции региона гипоперфузии и осуществляют наложение ЭИКМА между искомыми артериями.
Таким образом, в ходе предоперационного планирования производят совмещение данных КТ-ангиографии и однофотонной эмиссионной компьютерной томографии (ОФЭКТ) таким образом, что становится возможным визуализировать и использовать в ходе операции артерию-донор, артерию-реципиент в проекции зоны гипоперфузии головного мозга и выполнить реваскуляризацию именно этого региона.
Ранее навигацию использовали только для выполнения операции ЭИКМА в классической проекции трепанации в правой или левой височной области. Целью навигации являлось уточнение расположения артерии-донора и артерии реципиента, уменьшения операционной травмы, уменьшения размеров кожного разреза и трепанационного окна. В предложенных ранее способах расположение зоны гипоперфузии (очага инфаркта головного мозга и зоны пенумбры) не уточняли, ЭИКМА выполняли в необходимом полушарии, без конкретизации доли или очага пониженного кровоснабжения. Предлагаемое изобретение имеет все перечисленные преимущества выполнения операции только по данным ангиографических методик. Основной ценностью заявляемого способа является возможность (благодаря совмещению данных ангиографии и перфузии головного мозга) селективной, направленной реваскуляризации необходимого региона головного мозга, что существующие на сегодняшний день способы предоставить не могут. У пациентов с окклюзией внутренней сонной артерии (ВСА) ишемические инсульты, как правило, возникают на границе артериальных бассейнов, однако установить точно долю и регион головного мозга, в котором имеется недостаточность кровоснабжения, позволяют только перфузионные методики: ОФЭКТ, КТ-перфузия, MP-перфузия. Из уровня техники не известны способы, основанные на совмещении (fusion) методик перфузии и ангиографии на навигационной станции для решения поставленной задачи. Использование данных о регионе гипоперфузии позволит принципиально по новому рассматривать показания к реваскуляризирующей хирургии головного мозга, применять операции реваскуляризации направленно, улучшая кровоснабжение необходимого региона или очага ишемического поражения у пациентов с острым ишемическим инсультом или хронической церебральной недостаточностью. Использование заявляемого способа позволит отойти от классической методики наложения ЭИКМА и выбирать донор и реципиент, отличные от оригинальной методики: артерией-донором не обязательно может быть ветвь поверхностной височной артерии, артерией-реципиентом не обязательно может быть центральная ветвь средней мозговой артерии, а, например, как в нижеприведенном клиническом примере - затылочная артерия и ангулярная ветвь средней мозговой артерии.
Применение разработанного способа позволяет улучшить перфузию необходимого региона головного мозга, улучшить исходы лечения у пациентов с острым нарушением мозгового кровообращения на фоне окклюзированной внутренней сонной артерии, а также профилактировать повторные нарушения.
Краткое описание чертежей
Изобретение поясняется данными навигационного моделирования и интраоперационными фото.
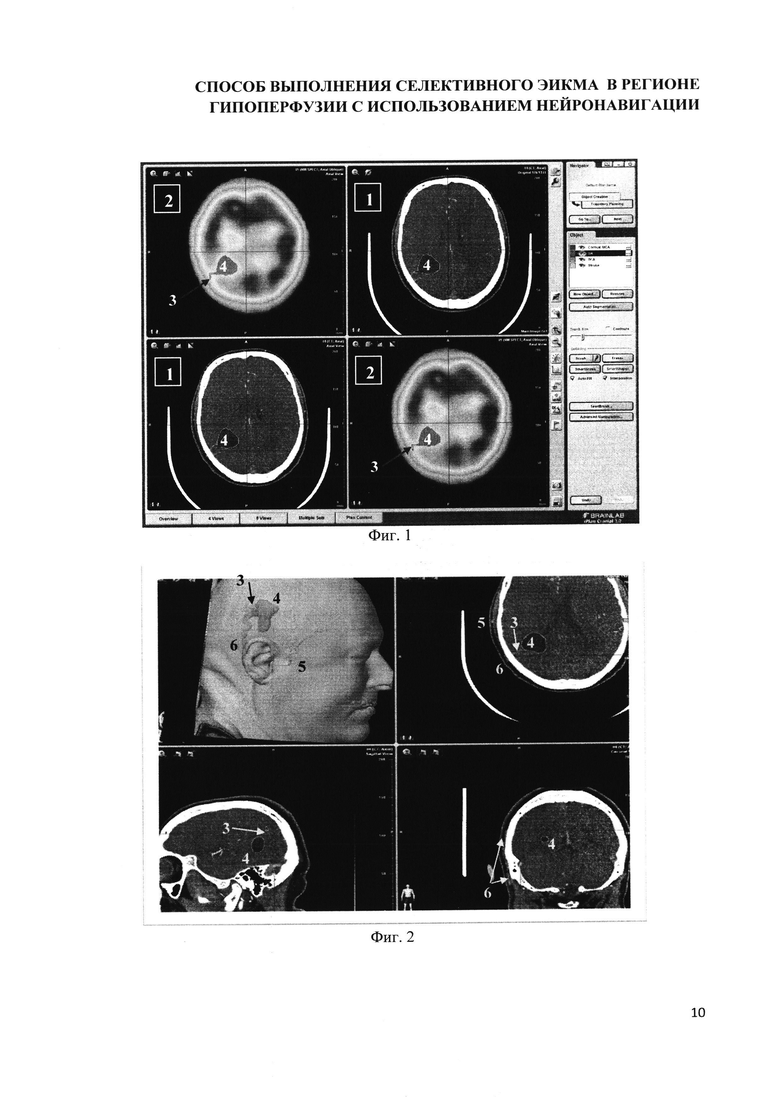
На фиг. 1 представлено предоперационное планирование на навигационной станции «Brain lab". Совмещены данные КТ-ангиографии (1) и ОФЭКТ (2), выделены артерия-реципиент (3) и регион гипоперфузии в правой теменно-височно-затылочной области (4);
на фиг. 2 представлено предоперационное планирование на навигационной станции «brain lab". Выполнено 3D моделирование возможных артерий-доноров: правая поверхностная височная артерия (5), правая затылочная артерия (6), артерии-реципиента: М4 сегмента правой СМА (3), которые сопоставлены с проекцией церебральной гипоперфузии (4);
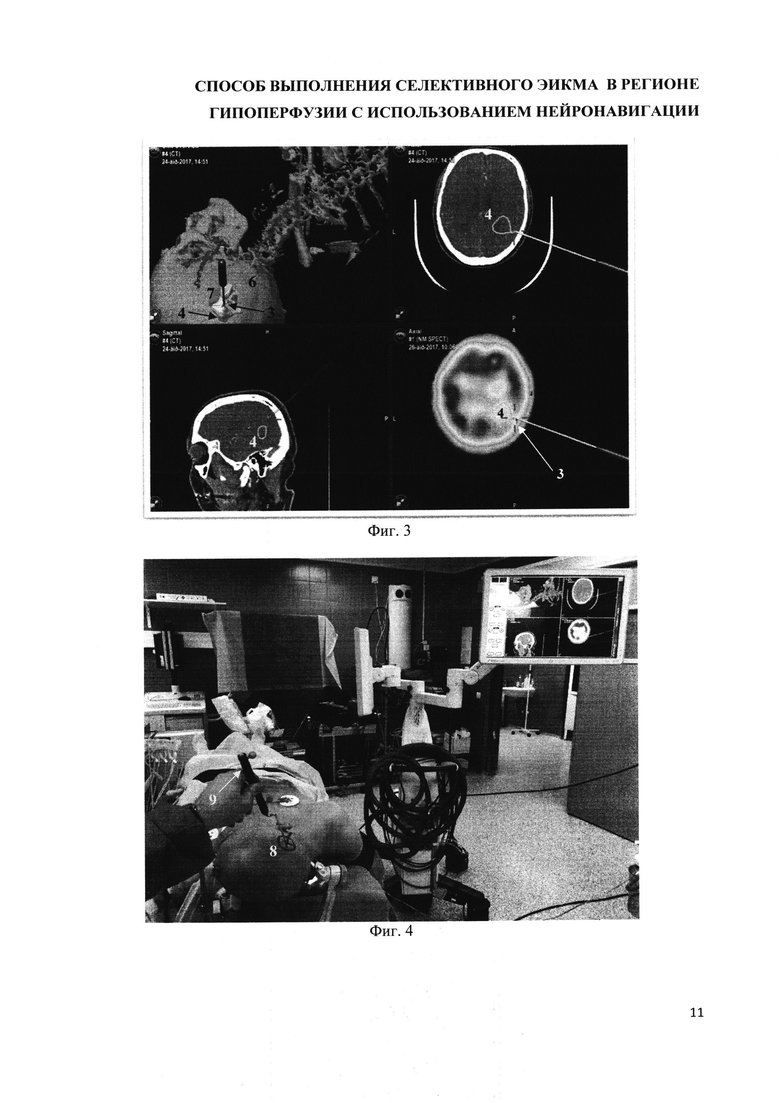
на фиг. 3 - интраоперационная нейронавигация с учетом кожных ориентиров пациента. Поиск артерии-донора, в качестве которой принято решение использовать затылочную артерию (6), артерии-реципиента (3), региона гипоперфузии (4), планирование трепанации (7);
на фиг. 4 - интраоперационное фото; разметка хирургического доступа (8) с использованием нейронавигационной указки (9);
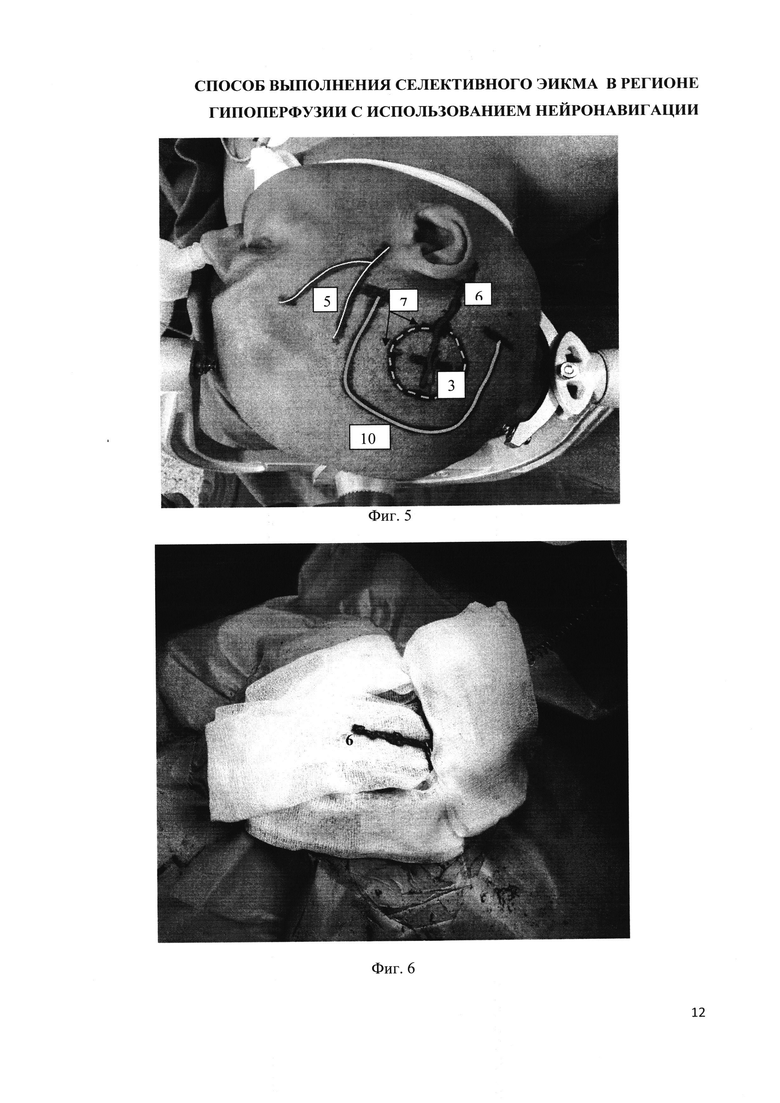
на фиг. 5 - интраоперационное фото: разметка кожного разреза (10), артерии-донора (затылочной артерии) (6), артерии-реципиента (М4 сегмента СМА) (3), трепанации (7), поверхностная височная артерия (5);
на фиг. 6 - интраоперационное фото. Выделение артерии-донора (6);
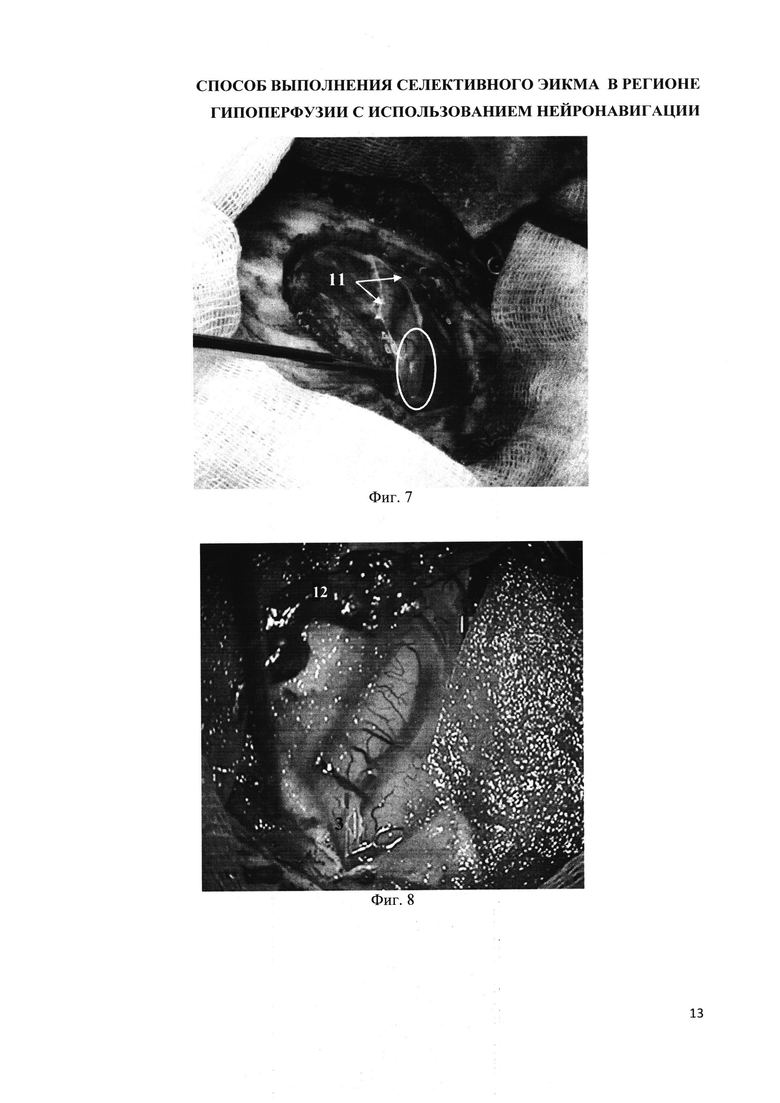
на фиг. 7 - интраоперационное фото. Разрез ТМО (11). Выделение артерии-реципиента (выделен белым кругом);
на фиг. 8 - интраоперационное фото. Подготовка к выполнению анастомоза. Артерия-донор помещена в проекцию костного окна (12), выполнена артериотомия артерии-реципиента (3);
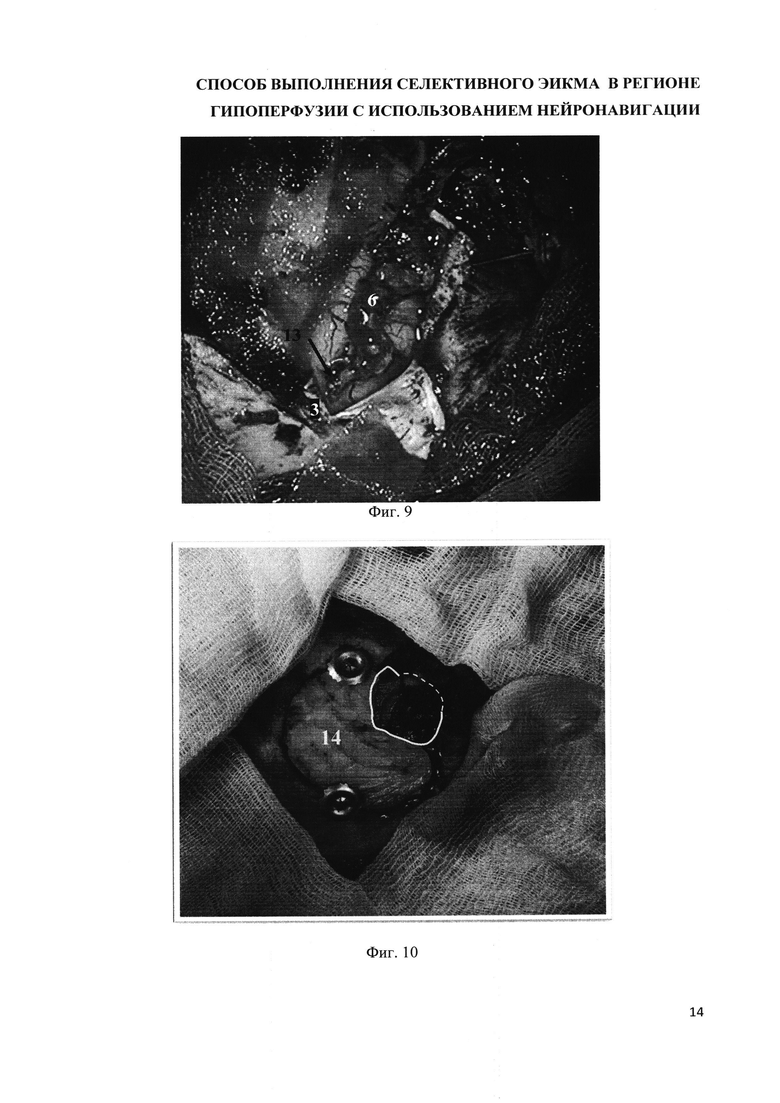
на фиг. 9 - интраоперационное фото. Выполнения анастомоза по типу конец-в-бок (13) между артерией-донором (6) и артерией-реципиентом (3);
на фиг. 10 - интраоперационное фото. Закрытие костного окна свободным костным лоскутом (14) с оставлением пространства для прохождения созданного обходного шунта (ЭИКМА) (обведено желтым кругом).
Осуществление изобретения
На дооперационном этапе выполняют КТ-ангиографию экстра-интракраниальных артерий и ОФЭКТ головного мозга. На ОФЭКТ выявляют зону гипоперфузии (соответствующую зоне ишемической пенумбры) с показателями кровотока на уровне менее 38 мл/мин/100 г, путем последовательного оконтуривания вышеописанной зоны на всех аксиальных срезах создают 3D-модель зоны гипоперфузии. После выявления очага пониженного кровоснабжения производят предоперационное планирование на навигационной станции, где совмещают в одном диалоговом окне данные ОФЭКТ и КТ-ангиографии с построением 3D-модели, при этом на каждом срезе оконтуривают изображение интракраниальной артерии - реципиента, находящейся в очаге пониженного кровоснабжения, имеющей диаметр 0,8-1,0 мм, и изображение до трех потенциальных артерий - доноров из бассейна наружной сонной артерии (толщиной до 1,0-1,5 мм и длиной не менее 6 см), находящихся в проекции артерии реципиента, далее на 3D-модели из отмеченных артерий-доноров выбирают артерию, расположенную как можно ближе к очагу пониженного кровоснабжения и имеющую диаметр, равный или больше диаметра артерии реципиента, снабжающей очаг, и находящуюся на расстоянии от артерии-реципиента на расстоянии не более чем 1-3 см (т.е. имеющий дефицит длины не менее 1-3 см), затем производят моделирование краниотомии, для чего на 3D-модели выделяют область диаметром 2-4 см, центром которой является точка пересечения проекции артерии-реципиента на выбранную артерию донора. Операцию выполняют в положении больного на спине с фиксацией головы пациента в скобе "Mayfield" с использованием безрамной нейронавигации проводят разметку артерии-донора и артерии-реципиента на коже согласно совмещенным на навигации КТ и ОФЭКТ данным и полученной 3D-модели. Осуществляют подковообразный разрез кожи и подкожной клетчатки в проекции запланированной трепанации до кости. Выделяют артерию-донор в мягко-тканной муфте на протяжении 6-8 см, на ее основание накладывают временный клипс. Скелетируют подлежащую кость. С использованием стерильной указки навигационной системы определяют границы запланированной трепанации в проекции региона гипоперфузии. Выполняют костно-пластическую трепанацию диаметром около 3 см. Твердую мозговую оболочку фиксируют по краю костного дефекта фиксирующими швами. С использованием нейронавигационной указки осуществляют разрез ТМО в проекции артерии-реципиента. Далее производят подготовку кончика артерии-донора, освобождение ее от мягкотканой муфты, усечение конца артерии под углом (создание «fish-mouth»). После подготовки артерии-донора производят вскрытие арахноидальной оболочки над артерией-реципиентом, подготовку артерии-реципиента, освобождение ее от мягкой мозговой оболочки на протяжении около 5-7 мм. Производят проверку проходимости артерии-донора путем пробного снятия временного клипса, промывание ее стерильным физиологическим раствором после повторной установки временного клипса. При условии проходимости артерии-донора на артерию-реципиент накладывают временные клипсы для выключения сегмента, на котором планируется наложение анастомоза. Далее артерию-донор вскрывают алмазным ножом на протяжении около 1-2 мм, ее просвет промывают стерильным физиологическим раствором. После подготовки артерии-донора и артерии-реципиента выполняют анастомоз по типу конец-в-бок. Далее снимают временные клипсы сначала с артерии-реципиента, попутно осуществляя гемостаз зоны анастомоза с использованием гемостатической ваты, снимают временную клипсу с артерии-донора, осуществляя повторный гемостаз. Производят интраоперационный контроль проходимости анастомоза с помощью флоуметра, допплерографии.
По данному способу операция ЭИКМА была выполнена трем пациентам.
Пример 1. Пациент Т., 58 лет, поступил в НИИ СП с клинической картиной острого ишемического инсульта в бассейне правой средней мозговой артерии на фоне тромбоза правой внутренней сонной артерии. Развитие заболевания более 8 часов от поступления. В клинической картине отмечена слабость в левой руке и ноге, тонус мышц снижен до 3-х баллов. В качестве предоперационного планирования пациенту выполнена КТ-ангиография и ОФЭКТ, произведено моделирование операционного доступа и артерий согласно полученным данным. Выделен регион церебральной гипоперфузии в правой теменно-височно-затылочной области, артерия-донор - правая затылочная артерия, артерия-реципиент - конечные ветви средней мозговой артерии в регионе гипоперфузии. В условиях операционной произведена разметка доступа и операция ЭИКМА по заявляемому способу. С помощью нейронавигации удалось с высокой точностью и минимальной хирургической травмой выделить артерию-донор (затылочную артерию), выполнить трепанацию в проекции региона гипоперфузии, визуализировать артерию-реципиент (М4 сегмент СМА) и создать анастомоз по типу конец-в-бок. Объемный кровоток по шунту составил 22 мл/мин. В послеоперационном периоде отмечена четкая положительная динамика в неврологическом статусе пациента, через 7 дней послеоперационного периода левосторонний гемипарез регрессировал. При контрольной КТ-ангиографии анастомоз проходим, по данным ОФЭКТ зарегистрировано значительное улучшение перфузии в правой теменно-височно-затылочной области (на 30-35%), в проекции работающего анастомоза и необходимого региона головного мозга. Пациент активизирован, ходит по коридору, выписан в удовлетворительном состоянии без неврологического дефицита.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ планирования мини-доступа для создания экстра-интракраниального микроанастомоза с использованием МСКТ-ангиографии головного мозга в 3D реконструкции. | 2016 |
|
RU2637826C1 |
| СПОСОБ ДИНАМИЧЕСКОГО ОПРЕДЕЛЕНИЯ ОБЪЁМА РЕВАСКУЛЯРИЗАЦИИ ГОЛОВНОГО МОЗГА С ИСПОЛЬЗОВАНИЕМ ИНТРАОПЕРАЦИОННОЙ МАГНИТНО-РЕЗОНАНСНОЙ ТОМОГРАФИИ | 2023 |
|
RU2811955C1 |
| СПОСОБ ВЫПОЛНЕНИЯ ОБХОДНОГО ШУНТИРОВАНИЯ ГОЛОВНОГО МОЗГА С ИСПОЛЬЗОВАНИЕМ УСТЬЯ ВЕРХНЕЧЕЛЮСТНОЙ АРТЕРИИ (анастомоз по типу конец-в-конец) | 2021 |
|
RU2781443C1 |
| СПОСОБ РЕВАСКУЛЯРИЗАЦИИ ГОЛОВНОГО МОЗГА ПРИ ОСТРОМ ИШЕМИЧЕСКОМ ИНСУЛЬТЕ | 2019 |
|
RU2707258C1 |
| СПОСОБ АУТОВЕНОЗНОГО ШУНТИРОВАНИЯ ПРИ ОККЛЮЗИРУЮЩИХ ПОРАЖЕНИЯХ АРТЕРИЙ ГОЛОВНОГО МОЗГА | 2014 |
|
RU2554210C1 |
| Способ выбора акцепторной артерии при хирургической реваскуляризации головного мозга у пациентов с хронической церебральной ишемией | 2019 |
|
RU2742191C1 |
| СПОСОБ ОТБОРА ПАЦИЕНТОВ ДЛЯ ОПЕРАЦИИ ЭКСТРА-ИНТРАКРАНИАЛЬНОГО МИКРОАНАСТОМОЗА ПРИ АТЕРОСКЛЕРОТИЧЕСКОЙ ОККЛЮЗИИ ВНУТРЕННЕЙ СОННОЙ АРТЕРИИ | 2018 |
|
RU2695275C1 |
| СПОСОБ ЛЕЧЕНИЯ ЦЕРЕБРАЛЬНОЙ ИШЕМИИ | 2008 |
|
RU2408300C2 |
| СПОСОБ ОЦЕНКИ ПЕРФУЗИИ ГОЛОВНОГО МОЗГА | 1995 |
|
RU2116800C1 |
| СПОСОБ ВЫБОРА ТИПА ЭКСТРА-ИНТРАКРАНИАЛЬНОГО ШУНТА ПО ПРОПУСКНОЙ СПОСОБНОСТИ ПРИ ОСТРЫХ И ХРОНИЧЕСКИХ ЦЕРЕБРОВАСКУЛЯРНЫХ ПАТОЛОГИЯХ, ТРЕБУЮЩИХ РЕВАСКУЛЯРИЗИРУЮЩЕГО ВМЕШАТЕЛЬСТВА | 2021 |
|
RU2784442C1 |
Изобретение относится к области медицины, а именно нейрохирургии, лучевой диагностике, и может быть использовано при выполнении селективного ЭИКМА в регионе гипоперфузии с использованием нейронавигации. На дооперационном этапе выполняют КТ-ангиографию экстра- и интракраниальных артерий и ОФЭКТ головного мозга. На ОФЭКТ головного мозга выявляют зону гипоперфузии с показателями кровотока на уровне менее 38 мл/мин/100 г. Путем последовательного оконтуривания вышеописанной зоны на всех аксиальных срезах создают 3D-модель зоны гипоперфузии. На навигационной станции совмещают в одном диалоговом окне данные ОФЭКТ и КТ-ангиографии. На каждом срезе оконтуривают изображение интракраниальной артерии-реципиента. Артерия-реципиент должна находиться в очаге пониженного кровоснабжения и иметь диаметр 0,8-1,0 мм. Также на изображении оконтуривают до трех потенциальных артерий-доноров из бассейна наружной сонной артерии толщиной до 1,0-1,5 мм и длиной не менее 6 см. Артерии-доноры должны находиться в проекции артерии-реципиента, для этого на 3D-модели из отмеченных артерий-доноров выбирают артерию, расположенную как можно ближе к очагу пониженного кровоснабжения, имеющую диаметр, равный или больше диаметра артерии-реципиента, и находящуюся на расстоянии от артерии-реципиента не более чем 1-3 см. Затем проводят моделирование краниотомии, для чего на 3D-модели выделяют область диаметром 2-4 см, центром которой является точка пересечения проекции артерии-реципиента на выбранную артерию-донора. В условиях операционной с использованием безрамной нейронавигации проводят сопоставление кожных ориентиров с полученными данными на 3D-модели и выполняют разметку артерий и операционного доступа. Осуществляют трепанацию в проекции региона гипоперфузии с последующим наложением ЭИКМА между искомыми артериями. Способ обеспечивает возможность селективной реваскуляризации необходимого региона головного мозга с высокой точностью с целью улучшения перфузии и функциональных исходов после перенесенного острого нарушения мозгового кровообращения у пациентов с окклюзией внутренней сонной артерии. 10 ил., 1 пр.
Способ хирургического лечения пациентов с окклюзией внутренней сонной артерии в остром периоде острого нарушения мозгового кровообращения (ОНМК) или после перенесенных нарушений мозгового кровообращения, включающий выполнение операции ЭИКМА, при этом на дооперационном этапе выполняют КТ-ангиографию экстра-интракраниальных артерий и ОФЭКТ головного мозга, на ОФЭКТ выявляют зону гипоперфузии с показателями кровотока на уровне менее 38 мл/мин/100 г, далее путем последовательного оконтуривания вышеописанной зоны на всех аксиальных срезах создают 3D-модель зоны гипоперфузии, после чего на навигационной станции совмещают в одном диалоговом окне данные ОФЭКТ и КТ-ангиографии, где на каждом срезе оконтуривают изображение интракраниальной артерии-реципиента, находящейся в очаге пониженного кровоснабжения, имеющей диаметр 0,8-1,0 мм, и изображение до трех потенциальных артерий-доноров из бассейна наружной сонной артерии толщиной до 1,0-1,5 мм и длиной не менее 6 см, находящихся в проекции артерии реципиента, далее на 3D-модели из отмеченных артерий-доноров выбирают артерию, расположенную как можно ближе к очагу пониженного кровоснабжения и имеющую диаметр, равный или больше диаметра артерии-реципиента, снабжающей очаг, и находящуюся на расстоянии от артерии реципиента на расстоянии не более чем 1-3 см, затем производят моделирование краниотомии, для чего на 3D-модели выделяют область диаметром 2-4 см, центром которой является точка пересечения проекции артерии-реципиента на выбранную артерию донора, после чего в условиях операционной с использованием безрамной нейронавигации проводят сопоставление кожных ориентиров с полученными на 3D-модели, выполняют разметку артерий и операционного доступа, выполняют трепанацию в проекции региона гипоперфузии и осуществляют наложение ЭИКМА между искомыми артериями.
| Лукьянчиков B.A | |||
| и др | |||
| Возможность выполнения экстра-интракраниального микроанастомоза с использованием системы безрамной нейронавигации | |||
| // Нейрохирургия | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Приспособление для соединения пучка кисти с трубкою или втулкою, служащей для прикрепления ручки | 1915 |
|
SU66A1 |
| Способ планирования мини-доступа для создания экстра-интракраниального микроанастомоза с использованием МСКТ-ангиографии головного мозга в 3D реконструкции. | 2016 |
|
RU2637826C1 |
| Противоугонное устройство | 1940 |
|
SU59645A1 |
| Крылов В.В | |||
| и др | |||
| Применение экстра-интракраниального микроанастомоза в лечении ишемии головного мозга у больных с нетравматическим субарахноидальным кровоизлиянием | |||
| // Журнал неврологии и психиатрии им | |||
| С.С | |||
| Корсакова | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Способ получения бензидиновых оснований | 1921 |
|
SU116A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Амелин М.Е | |||
| и др | |||
| Изменение мозговой перфузии при экстра-интракраниальном микроанастомозе при хронической окклюзии внутренней сонной артерии | |||
| // Лучевая диагностика и терапия | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Приспособление для получения кинематографических стерео снимков | 1919 |
|
SU67A1 |
| Burkhardt J.K | |||
| et al | |||
| Emergency Extracranial-Intracranial Bypass to Revascularize Salvageable Brain Tissue in Acute Ischemic Stroke Patients | |||
| // World Neurosurg | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Chou C.W | |||
| et al | |||
| Extracranial-intracranial (EC-IC) bypass of symptomatic middle cerebral artery (MCA) total occlusion for haemodynamic impairment patients | |||
| // Br J Neurosurg | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
Авторы
Даты
2018-03-21—Публикация
2017-06-26—Подача